Башкирский государственный университет.ppt
- Количество слайдов: 24
 Вода – самое уникальное вещество на нашей планете. Выполнила: студентка химического факультета гр. 1 В Шарипова Элина
Вода – самое уникальное вещество на нашей планете. Выполнила: студентка химического факультета гр. 1 В Шарипова Элина
 Введение • Наша Земля отличается от • других планет – она живая. Ведь на ней есть вода. Вода – самое уникальное вещество на нашей планете. Если резко сократить ее количество или изменить хотя бы одно из ее удивительных свойств жизнь на Земле исчезнет. Ведь вода – это то самое вещество, без которого не может существовать ничего живого. Вся наша жизнь и все живое основано на воде.
Введение • Наша Земля отличается от • других планет – она живая. Ведь на ней есть вода. Вода – самое уникальное вещество на нашей планете. Если резко сократить ее количество или изменить хотя бы одно из ее удивительных свойств жизнь на Земле исчезнет. Ведь вода – это то самое вещество, без которого не может существовать ничего живого. Вся наша жизнь и все живое основано на воде.
 Вода в природе • Вода является самым распространенным веществом на Земле. Почти ¾ поверхности нашей планеты занято океанами и морями. Однако 97% - это соленая вода морей и океанов, и лишь 3% пресная. Из них около трех четвертей недоступны живым организмам, так как эта пресная вода “законсервирована” в ледниках гор и полярных шапках (ледники Арктики и Антарктики). Это настоящий мировой резерв пресной питьевой воды.
Вода в природе • Вода является самым распространенным веществом на Земле. Почти ¾ поверхности нашей планеты занято океанами и морями. Однако 97% - это соленая вода морей и океанов, и лишь 3% пресная. Из них около трех четвертей недоступны живым организмам, так как эта пресная вода “законсервирована” в ледниках гор и полярных шапках (ледники Арктики и Антарктики). Это настоящий мировой резерв пресной питьевой воды.
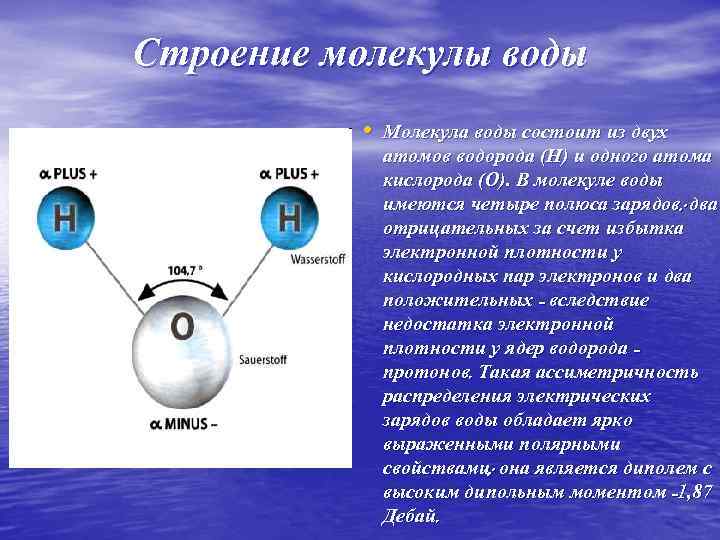 Строение молекулы воды • Молекула воды состоит из двух атомов водорода (Н) и одного атома кислорода (О). В молекуле воды имеются четыре полюса зарядов: два отрицательных за счет избытка электронной плотности у кислородных пар электронов и два положительных - вследствие недостатка электронной плотности у ядер водорода протонов. Такая ассиметричность распределения электрических зарядов воды обладает ярко выраженными полярными свойствами; она является диполем с высоким дипольным моментом -1, 87 Дебай.
Строение молекулы воды • Молекула воды состоит из двух атомов водорода (Н) и одного атома кислорода (О). В молекуле воды имеются четыре полюса зарядов: два отрицательных за счет избытка электронной плотности у кислородных пар электронов и два положительных - вследствие недостатка электронной плотности у ядер водорода протонов. Такая ассиметричность распределения электрических зарядов воды обладает ярко выраженными полярными свойствами; она является диполем с высоким дипольным моментом -1, 87 Дебай.
 Физические свойства • Бесцветное вещество без вкуса и запаха, плотность 1 г/см 3, • температура кипения 1000 С, температура плавления (замерзания)- 0 С. Вода – единственное вещество в природе, которое в земных условиях существует в трех агрегатных состояниях: жидком, газообразном и твёрдом.
Физические свойства • Бесцветное вещество без вкуса и запаха, плотность 1 г/см 3, • температура кипения 1000 С, температура плавления (замерзания)- 0 С. Вода – единственное вещество в природе, которое в земных условиях существует в трех агрегатных состояниях: жидком, газообразном и твёрдом.
 Температура плавления и кипения воды • Самое удивительное и благостное • для живой природы свойство воды это ее способность при "нормальных" условиях быть жидкостью. Объясняется это довольно просто большая часть молекул воды соединена водородными связями. Именно этими связями отличается вода от жидких гидридов H 2 S, H 2 Se и H 2 Te. Энергия водородных связей достаточно велика, и разорвать их можно лишь при значительно более высокой температуре.
Температура плавления и кипения воды • Самое удивительное и благостное • для живой природы свойство воды это ее способность при "нормальных" условиях быть жидкостью. Объясняется это довольно просто большая часть молекул воды соединена водородными связями. Именно этими связями отличается вода от жидких гидридов H 2 S, H 2 Se и H 2 Te. Энергия водородных связей достаточно велика, и разорвать их можно лишь при значительно более высокой температуре.
 Плотность воды и льда • Жизненно важной для всей биосферы является способность воды при замерзании уменьшать, а не увеличивать свою плотность. Если взять обычную воду и, постепенно охлаждая ее, следить за изменением плотности то можно заметить, что в начале будет происходить совершенно обычный и естественный процесс - вода становится при охлаждении все плотнее и плотнее, и никаких отклонений от нормы мы не увидим до тех пор, пока не охладим воду до 4 °C. Ниже этой температуры вопреки общим представлениям вода вдруг становится легче, а замерзая она делается еще легче и образует лед, который плавает по поверхности воды. Замерзая, вода расширяется на 9% по отношению к прежнему объему. Это расширение может оказаться роковым для водопровода в случае наступления неожиданных морозов. Вода, замерзая в трубах, разорвет их.
Плотность воды и льда • Жизненно важной для всей биосферы является способность воды при замерзании уменьшать, а не увеличивать свою плотность. Если взять обычную воду и, постепенно охлаждая ее, следить за изменением плотности то можно заметить, что в начале будет происходить совершенно обычный и естественный процесс - вода становится при охлаждении все плотнее и плотнее, и никаких отклонений от нормы мы не увидим до тех пор, пока не охладим воду до 4 °C. Ниже этой температуры вопреки общим представлениям вода вдруг становится легче, а замерзая она делается еще легче и образует лед, который плавает по поверхности воды. Замерзая, вода расширяется на 9% по отношению к прежнему объему. Это расширение может оказаться роковым для водопровода в случае наступления неожиданных морозов. Вода, замерзая в трубах, разорвет их.
 Капиллярность воды • Капиллярность играет важную роль во многих природных процессах, происходящих на Земле. Благодаря этому вода смачивает толщу почвы, лежащую значительно выше зеркала грунтовых вод и доставляет корням растений растворы питательных веществ. Капиллярностью обусловлено движение крови и тканевых жидкостей в живых организмах.
Капиллярность воды • Капиллярность играет важную роль во многих природных процессах, происходящих на Земле. Благодаря этому вода смачивает толщу почвы, лежащую значительно выше зеркала грунтовых вод и доставляет корням растений растворы питательных веществ. Капиллярностью обусловлено движение крови и тканевых жидкостей в живых организмах.
 Охлаждение. . . кипятком! • На многих металлургических производствах Донбасса в качестве охладителя используют не холодную воду, а кипяток. Охлаждение идет за счет использования теплоты парообразования – эффективность процесса повышается в несколько раз, к тому же отпадает надобность в сооружении громоздких градирен. Конечно, кипятокохладитель используют там, где нужно охладить объекты, нагретые выше 100°C. Также это используется в сельского хозяйства, садоводства. Когда поздней весной внезапные ночные заморозки угрожают цветущим плодовым деревьям, опытные садоводы находят выход, кажущийся совершенно неожиданным: они проводят дождевание сада. Пелена мельчайших водных брызг окутывает замерзающие деревья. Капельки воды покрывают лепестки цветов. Превращаясь в лед, вода надевает на цветы ледяную шубу, отдавая при этом им свое тепло (335 Дж от 1 г замерзающей воды).
Охлаждение. . . кипятком! • На многих металлургических производствах Донбасса в качестве охладителя используют не холодную воду, а кипяток. Охлаждение идет за счет использования теплоты парообразования – эффективность процесса повышается в несколько раз, к тому же отпадает надобность в сооружении громоздких градирен. Конечно, кипятокохладитель используют там, где нужно охладить объекты, нагретые выше 100°C. Также это используется в сельского хозяйства, садоводства. Когда поздней весной внезапные ночные заморозки угрожают цветущим плодовым деревьям, опытные садоводы находят выход, кажущийся совершенно неожиданным: они проводят дождевание сада. Пелена мельчайших водных брызг окутывает замерзающие деревья. Капельки воды покрывают лепестки цветов. Превращаясь в лед, вода надевает на цветы ледяную шубу, отдавая при этом им свое тепло (335 Дж от 1 г замерзающей воды).
 ”Память” воды • Структурные различия воды сохраняются в течение определенного времени, что позволило ученым говорить о загадочном механизме «памяти» этой удивительной жидкости. Не вызывает сомнение тот факт, что вода некоторое время «помнит» осуществленное на нее физическое воздействие, и эта «записанная» в воде информация оказывает влияние на живые организмы, в том числе на человека. Ведь в состав тела любого организма вода входит в весьма значительных количествах. И, как показали исследования, внутри организма вода находится в особом состоянии, еще более сходном с состоянием твердого тела, по сравнению с обычной водой. Бетховен, симфония № 6 Ты - дурак Спасибо
”Память” воды • Структурные различия воды сохраняются в течение определенного времени, что позволило ученым говорить о загадочном механизме «памяти» этой удивительной жидкости. Не вызывает сомнение тот факт, что вода некоторое время «помнит» осуществленное на нее физическое воздействие, и эта «записанная» в воде информация оказывает влияние на живые организмы, в том числе на человека. Ведь в состав тела любого организма вода входит в весьма значительных количествах. И, как показали исследования, внутри организма вода находится в особом состоянии, еще более сходном с состоянием твердого тела, по сравнению с обычной водой. Бетховен, симфония № 6 Ты - дурак Спасибо
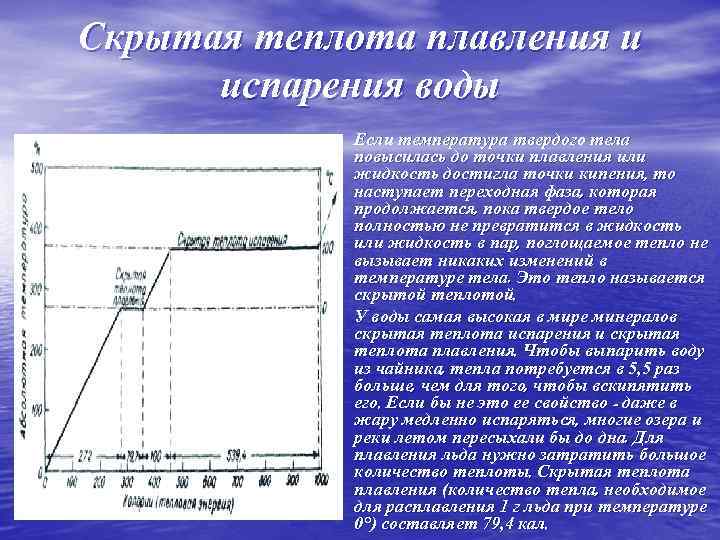 Скрытая теплота плавления и испарения воды • Если температура твердого тела • повысилась до точки плавления или жидкость достигла точки кипения, то наступает переходная фаза, которая продолжается, пока твердое тело полностью не превратится в жидкость или жидкость в пар, поглощаемое тепло не вызывает никаких изменений в температуре тела. Это тепло называется скрытой теплотой. У воды самая высокая в мире минералов скрытая теплота испарения и скрытая теплота плавления. Чтобы выпарить воду из чайника, тепла потребуется в 5, 5 раз больше, чем для того, чтобы вскипятить его. Если бы не это ее свойство - даже в жару медленно испаряться, многие озера и реки летом пересыхали бы до дна. Для плавления льда нужно затратить большое количество теплоты. Скрытая теплота плавления (количество тепла, необходимое для расплавления 1 г льда при температуре 0°) составляет 79, 4 кал.
Скрытая теплота плавления и испарения воды • Если температура твердого тела • повысилась до точки плавления или жидкость достигла точки кипения, то наступает переходная фаза, которая продолжается, пока твердое тело полностью не превратится в жидкость или жидкость в пар, поглощаемое тепло не вызывает никаких изменений в температуре тела. Это тепло называется скрытой теплотой. У воды самая высокая в мире минералов скрытая теплота испарения и скрытая теплота плавления. Чтобы выпарить воду из чайника, тепла потребуется в 5, 5 раз больше, чем для того, чтобы вскипятить его. Если бы не это ее свойство - даже в жару медленно испаряться, многие озера и реки летом пересыхали бы до дна. Для плавления льда нужно затратить большое количество теплоты. Скрытая теплота плавления (количество тепла, необходимое для расплавления 1 г льда при температуре 0°) составляет 79, 4 кал.
 Поверхностное натяжение воды • Мы видим его проявление всякий раз, когда • • наблюдаете, как вода медленно капает из водопроводного крана. Падающие капельки принимают почти шарообразную форму. Если бы не было внешних сил, они были бы строго шарообразны. Это является одним из проявлений необычной способности воды "стягиваться", "самоуплотняться”. Капля воды, капающая из крана, стягивается в крошечный шар, а шар из всех возможных геометрических тел обладает наименьшей поверхностью при данном объеме. Вследствие сцепления на поверхности воды образуется натяжение, и для того, чтобы разорвать поверхность воды, требуется физическая сила, причем довольно значительная. Ненарушенная водная поверхность может удерживать на себе предметы, которые значительно "тяжелее" воды, например стальную иголку или лезвие бритвы, или некоторых насекомых, которые скользят по воде, словно это не жидкость, а твердое тело. Из всех жидкостей, кроме ртути, у воды самое большое поверхностное натяжение.
Поверхностное натяжение воды • Мы видим его проявление всякий раз, когда • • наблюдаете, как вода медленно капает из водопроводного крана. Падающие капельки принимают почти шарообразную форму. Если бы не было внешних сил, они были бы строго шарообразны. Это является одним из проявлений необычной способности воды "стягиваться", "самоуплотняться”. Капля воды, капающая из крана, стягивается в крошечный шар, а шар из всех возможных геометрических тел обладает наименьшей поверхностью при данном объеме. Вследствие сцепления на поверхности воды образуется натяжение, и для того, чтобы разорвать поверхность воды, требуется физическая сила, причем довольно значительная. Ненарушенная водная поверхность может удерживать на себе предметы, которые значительно "тяжелее" воды, например стальную иголку или лезвие бритвы, или некоторых насекомых, которые скользят по воде, словно это не жидкость, а твердое тело. Из всех жидкостей, кроме ртути, у воды самое большое поверхностное натяжение.
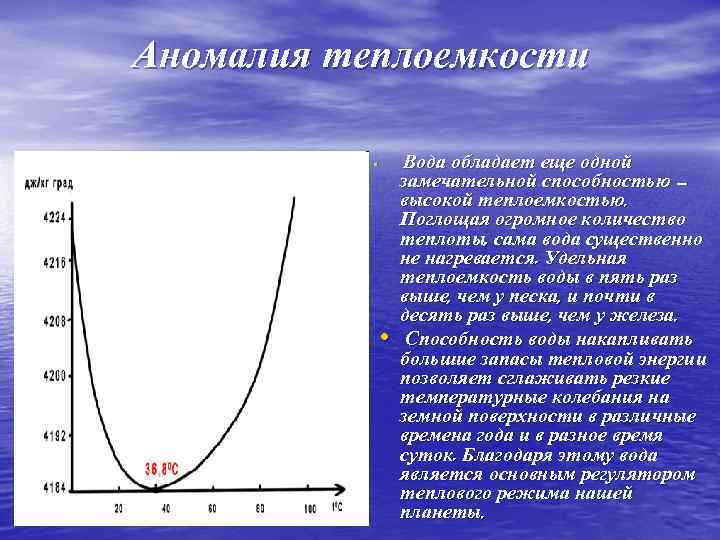 Аномалия теплоемкости • • Вода обладает еще одной замечательной способностью – высокой теплоемкостью. Поглощая огромное количество теплоты, сама вода существенно не нагревается. Удельная теплоемкость воды в пять раз выше, чем у песка, и почти в десять раз выше, чем у железа. Способность воды накапливать большие запасы тепловой энергии позволяет сглаживать резкие температурные колебания на земной поверхности в различные времена года и в разное время суток. Благодаря этому вода является основным регулятором теплового режима нашей планеты.
Аномалия теплоемкости • • Вода обладает еще одной замечательной способностью – высокой теплоемкостью. Поглощая огромное количество теплоты, сама вода существенно не нагревается. Удельная теплоемкость воды в пять раз выше, чем у песка, и почти в десять раз выше, чем у железа. Способность воды накапливать большие запасы тепловой энергии позволяет сглаживать резкие температурные колебания на земной поверхности в различные времена года и в разное время суток. Благодаря этому вода является основным регулятором теплового режима нашей планеты.
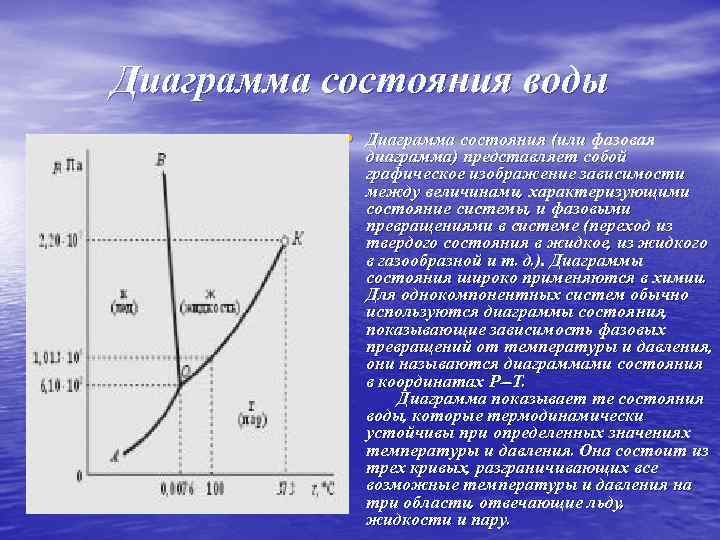 Диаграмма состояния воды • Диаграмма состояния (или фазовая диаграмма) представляет собой графическое изображение зависимости между величинами, характеризующими состояние системы, и фазовыми превращениями в системе (переход из твердого состояния в жидкое, из жидкого в газообразной и т. д. ). Диаграммы состояния широко применяются в химии. Для однокомпонентных систем обычно используются диаграммы состояния, показывающие зависимость фазовых превращений от температуры и давления, они называются диаграммами состояния в координатах Р—Т. Диаграмма показывает те состояния воды, которые термодинамически устойчивы при определенных значениях температуры и давления. Она состоит из трех кривых, разграничивающих все возможные температуры и давления на три области, отвечающие льду, жидкости и пару.
Диаграмма состояния воды • Диаграмма состояния (или фазовая диаграмма) представляет собой графическое изображение зависимости между величинами, характеризующими состояние системы, и фазовыми превращениями в системе (переход из твердого состояния в жидкое, из жидкого в газообразной и т. д. ). Диаграммы состояния широко применяются в химии. Для однокомпонентных систем обычно используются диаграммы состояния, показывающие зависимость фазовых превращений от температуры и давления, они называются диаграммами состояния в координатах Р—Т. Диаграмма показывает те состояния воды, которые термодинамически устойчивы при определенных значениях температуры и давления. Она состоит из трех кривых, разграничивающих все возможные температуры и давления на три области, отвечающие льду, жидкости и пару.
 • • Химические свойства воды Вода — весьма реакционноспособное вещество. Молекулы воды отличаются большой устойчивостью к нагреванию. Однако при температурах выше 1000 °С водяной пар начинает разлагаться на водород и кислород: • 2 H 2 O = 2 H 2 + O 2 Вода реагирует в присутствии катализатора: с амидами, эфирами карбоновых кислот CH 3 COOCH 3 + H 2 O = CH 3 COOH + CH 3 OH с ацетиленом и другими алкинами C 2 H 2 + H 2 O = СH 3 -CHO с алкенами СH 2=CH 2 + H 2 O = CH 3 -CH 2 OH
• • Химические свойства воды Вода — весьма реакционноспособное вещество. Молекулы воды отличаются большой устойчивостью к нагреванию. Однако при температурах выше 1000 °С водяной пар начинает разлагаться на водород и кислород: • 2 H 2 O = 2 H 2 + O 2 Вода реагирует в присутствии катализатора: с амидами, эфирами карбоновых кислот CH 3 COOCH 3 + H 2 O = CH 3 COOH + CH 3 OH с ацетиленом и другими алкинами C 2 H 2 + H 2 O = СH 3 -CHO с алкенами СH 2=CH 2 + H 2 O = CH 3 -CH 2 OH
 Химические свойства воды • Вода реагирует при комнатной температуре: • с активными металлами (натрий, кальций, барий и др. ) • 2 H 2 O + 2 Na =2 Na. OH + H 2 • с галогенами (фтором, хлором) и межгалоидными соединениями • H 2 O + Cl 2 = HCl + HCl. O • с солями, образованными слабой кислотой и слабым основанием, вызывая их полный гидролиз • (NH 4)2 S + H 2 O = 2 NH 4 OH + H 2 S • с ангидридами и галогенангидридами карбоновых и неорганических кислот • P 2 O 5 +3 Н 2 О = 2 H 3 PO 4 • с активными металлорганическими соединениями (диэтилцинк, реактивы Гриньяра, метилнатрий и т. д. ) • (C 2 H 5)2 Zn + H 2 O = Zn. O + 2 C 2 H 6
Химические свойства воды • Вода реагирует при комнатной температуре: • с активными металлами (натрий, кальций, барий и др. ) • 2 H 2 O + 2 Na =2 Na. OH + H 2 • с галогенами (фтором, хлором) и межгалоидными соединениями • H 2 O + Cl 2 = HCl + HCl. O • с солями, образованными слабой кислотой и слабым основанием, вызывая их полный гидролиз • (NH 4)2 S + H 2 O = 2 NH 4 OH + H 2 S • с ангидридами и галогенангидридами карбоновых и неорганических кислот • P 2 O 5 +3 Н 2 О = 2 H 3 PO 4 • с активными металлорганическими соединениями (диэтилцинк, реактивы Гриньяра, метилнатрий и т. д. ) • (C 2 H 5)2 Zn + H 2 O = Zn. O + 2 C 2 H 6
 Химические свойства воды • С карбидами, нитридами, фосфидами, силицидами, гидридами активных металлов (кальция, натрия, лития и др. ) • Ca. C 2 + 2 H 2 O = C 2 H 2 + Ca(OH)2 • со многими солями, образуя гидраты • Cu. SO 4 + 5 H 2 O = Cu. SO 4*5 H 2 O • с боранами, силанами • Si. H 4 + 2 Н 2 О = Si. O 2 + 4 Н 2 • с кетенами, недоокисью углерода • О=С=С=С=О + 2 Н 2 О = НООС—СН 2—СООН • с фторидами благородных газов • Au. F 3 + ЗН 20 = Au(OH)3 + 3 HF.
Химические свойства воды • С карбидами, нитридами, фосфидами, силицидами, гидридами активных металлов (кальция, натрия, лития и др. ) • Ca. C 2 + 2 H 2 O = C 2 H 2 + Ca(OH)2 • со многими солями, образуя гидраты • Cu. SO 4 + 5 H 2 O = Cu. SO 4*5 H 2 O • с боранами, силанами • Si. H 4 + 2 Н 2 О = Si. O 2 + 4 Н 2 • с кетенами, недоокисью углерода • О=С=С=С=О + 2 Н 2 О = НООС—СН 2—СООН • с фторидами благородных газов • Au. F 3 + ЗН 20 = Au(OH)3 + 3 HF.
 Химические свойства воды • Вода реагирует при нагревании: • с железом, магнием • 3 Fe + 4 H 2 O = 4 H 2 + Fe 3 O 4 • с углем, метаном • C + H 2 O = H 2 + CO • CH 4 + 2 H 2 O = 4 H 2 + CO 2 • с некоторыми алкилгалогенидами • Н 3 С-СН 2 -I + H 2 О ↔ Н 3 С-СН 2 -ОН + HI
Химические свойства воды • Вода реагирует при нагревании: • с железом, магнием • 3 Fe + 4 H 2 O = 4 H 2 + Fe 3 O 4 • с углем, метаном • C + H 2 O = H 2 + CO • CH 4 + 2 H 2 O = 4 H 2 + CO 2 • с некоторыми алкилгалогенидами • Н 3 С-СН 2 -I + H 2 О ↔ Н 3 С-СН 2 -ОН + HI
 Охрана гидросферы • Вода распространена на нешей планете • • • повсеместно. Однако мы все чаще слышим об экологических проблемах на Земле. Поэтому сегодня первостепенное значение приобретают вопросы охраны окружающей среды, в том числе водных источников от загрязнения. Огромный урон живым организмам в водоемах наносят промышленные сточные воды, содержащие ядовитые вещества. Способы очистки сточных вод зависят от характера содержащихся в них загрязнений. Бытовые сточные вод в основном содержат органические вещества. Поэтому они после обеззаражевания хлором или озоном подвергаются биологической очистке. Для очистки воды от неорганических солей применяются дистилляция, вымораживание и другие методы. Наиболее надежный способ защиты водоемов основан на создании экономически рациональных замкнутых систем, обеспечивающих многократное использование воды в производстве.
Охрана гидросферы • Вода распространена на нешей планете • • • повсеместно. Однако мы все чаще слышим об экологических проблемах на Земле. Поэтому сегодня первостепенное значение приобретают вопросы охраны окружающей среды, в том числе водных источников от загрязнения. Огромный урон живым организмам в водоемах наносят промышленные сточные воды, содержащие ядовитые вещества. Способы очистки сточных вод зависят от характера содержащихся в них загрязнений. Бытовые сточные вод в основном содержат органические вещества. Поэтому они после обеззаражевания хлором или озоном подвергаются биологической очистке. Для очистки воды от неорганических солей применяются дистилляция, вымораживание и другие методы. Наиболее надежный способ защиты водоемов основан на создании экономически рациональных замкнутых систем, обеспечивающих многократное использование воды в производстве.
 Питьевая вода • За свою жизнь человек выпивает около 75 тонн • • • воды. И, как утверждал Луи Пастер, при этом получает 80 процентов всех своих болезней. Ежегодно от заболеваний, передающихся с водой, в мире умирает 25 миллионов человек. Все эти пугающие данные говорят об одном: нельзя относиться безразлично к тому, что мы пьем. Нужно знать, что вода, пригодная для употребления, должна отвечать целому ряду требований. Во-первых, не содержать вредных примесей, микроорганизмов, солей тяжелых металлов, хлора и т. д. Во-вторых, быть легко усвояемой. В-третьих, иметь слабо-щелочную реакцию, как все основные жизненные среды (кровь, лимфа, слюна, межклеточная и спинномозговая жидкость). В-четвертых, иметь определенный минеральный состав и определенную жесткость (она зависит от содержания кальция, магния и др. ).
Питьевая вода • За свою жизнь человек выпивает около 75 тонн • • • воды. И, как утверждал Луи Пастер, при этом получает 80 процентов всех своих болезней. Ежегодно от заболеваний, передающихся с водой, в мире умирает 25 миллионов человек. Все эти пугающие данные говорят об одном: нельзя относиться безразлично к тому, что мы пьем. Нужно знать, что вода, пригодная для употребления, должна отвечать целому ряду требований. Во-первых, не содержать вредных примесей, микроорганизмов, солей тяжелых металлов, хлора и т. д. Во-вторых, быть легко усвояемой. В-третьих, иметь слабо-щелочную реакцию, как все основные жизненные среды (кровь, лимфа, слюна, межклеточная и спинномозговая жидкость). В-четвертых, иметь определенный минеральный состав и определенную жесткость (она зависит от содержания кальция, магния и др. ).
 Биологическое значение воды • Известно, что человеческий организм почти на 65% состоит из воды. Вода входит в состав тканей, без нее невозможно нормальное функционирование организма, осуществление процесса обмена, поддержание теплового баланса, удаление продуктов метаболизма и т. д. Потеря организмом большого количества воды опасна для жизни человека. Если количество воды, которое теряет человек, достигает 10% массы тела в сутки, наступает значительное снижение работоспособности, а если оно возрастает до 25%, то это обычно приводит к смерти. Однако даже при большой потере воды все нарушенные процессы в организме быстро восстанавливаются, если организм пополнится водой до нормы.
Биологическое значение воды • Известно, что человеческий организм почти на 65% состоит из воды. Вода входит в состав тканей, без нее невозможно нормальное функционирование организма, осуществление процесса обмена, поддержание теплового баланса, удаление продуктов метаболизма и т. д. Потеря организмом большого количества воды опасна для жизни человека. Если количество воды, которое теряет человек, достигает 10% массы тела в сутки, наступает значительное снижение работоспособности, а если оно возрастает до 25%, то это обычно приводит к смерти. Однако даже при большой потере воды все нарушенные процессы в организме быстро восстанавливаются, если организм пополнится водой до нормы.
 Применение • Земледелие • Питьё и приготовление пищи • Растворитель • Теплоноситель • Замедлитель • Пожаротушение • Спорт • Инструмент • Смазка
Применение • Земледелие • Питьё и приготовление пищи • Растворитель • Теплоноситель • Замедлитель • Пожаротушение • Спорт • Инструмент • Смазка
 Заключение • “Так что такое вода? ” – довольно сложный вопрос. Даже все то, что известно ученым не дает исчерпывающий ответ на него. Есть множество вопросов, которые остаются загадкой и на сегодняшний день. К примеру, причины многочисленных аномалий воды, ее структура, и еще многие свойства, о которых мы даже не подозреваем. Однозначно можно сказать лишь то, что вода - самое уникальное вещество на Земле.
Заключение • “Так что такое вода? ” – довольно сложный вопрос. Даже все то, что известно ученым не дает исчерпывающий ответ на него. Есть множество вопросов, которые остаются загадкой и на сегодняшний день. К примеру, причины многочисленных аномалий воды, ее структура, и еще многие свойства, о которых мы даже не подозреваем. Однозначно можно сказать лишь то, что вода - самое уникальное вещество на Земле.
 • Спасибо за внимание=)
• Спасибо за внимание=)


