Вода.ppt
- Количество слайдов: 36
 Вода. Розчини. Властивості розчинів неелектролітів 1. 2. 3. 4. 5. 6. Вода в природі. Фізичні властивості води. Будова молекули води. Хімічні властивості води. Діаграма стану води. Характеристика розчинів. Процес розчинення. Концентрація. Способи вираження концентрації. Властивості розчинів неелектролітів. 1
Вода. Розчини. Властивості розчинів неелектролітів 1. 2. 3. 4. 5. 6. Вода в природі. Фізичні властивості води. Будова молекули води. Хімічні властивості води. Діаграма стану води. Характеристика розчинів. Процес розчинення. Концентрація. Способи вираження концентрації. Властивості розчинів неелектролітів. 1
 Фізичні властивості води: n n n аномально високі температури плавлення і кипіння; надзвичайно висока теплоємність; значні теплоти плавлення і випаровування; n значний поверхневий натяг; n висока діелектрична проникність. 2
Фізичні властивості води: n n n аномально високі температури плавлення і кипіння; надзвичайно висока теплоємність; значні теплоти плавлення і випаровування; n значний поверхневий натяг; n висока діелектрична проникність. 2
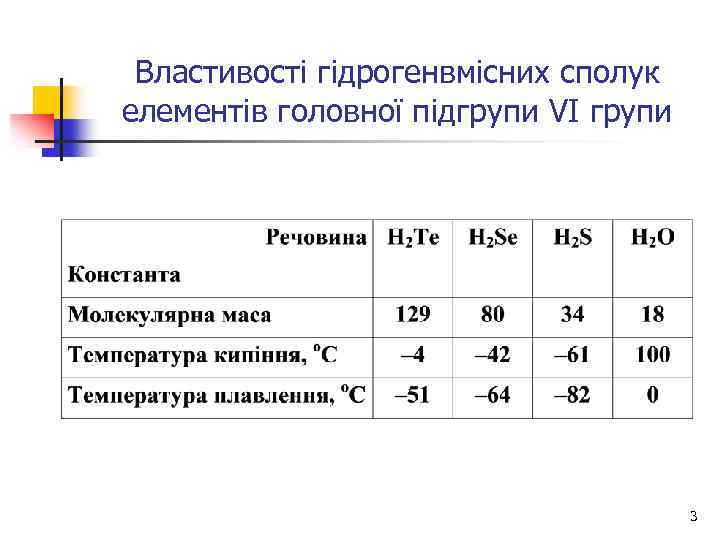 Властивості гідрогенвмісних сполук елементів головної підгрупи VI групи 3
Властивості гідрогенвмісних сполук елементів головної підгрупи VI групи 3
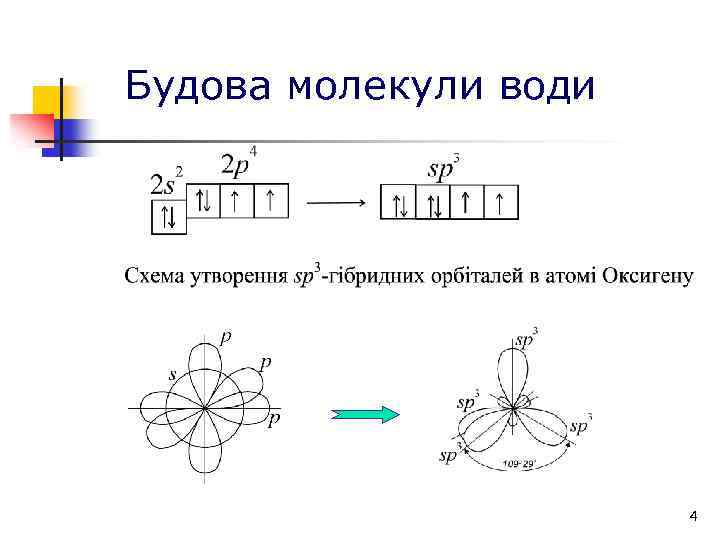 Будова молекули води 4
Будова молекули води 4
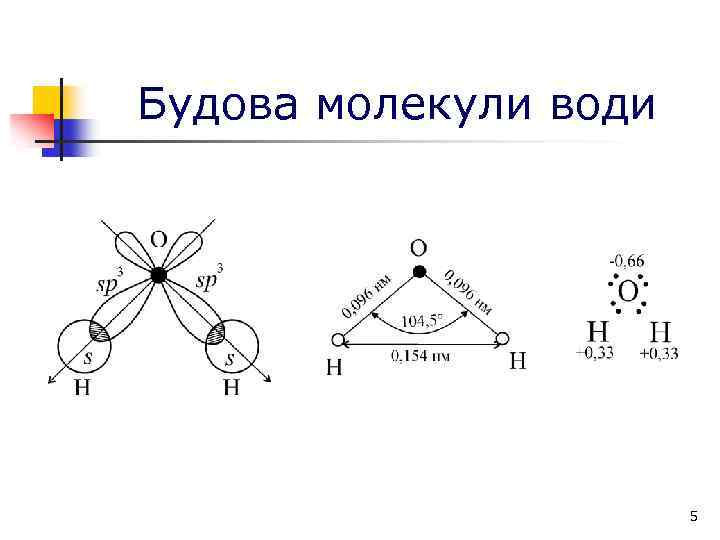 Будова молекули води 5
Будова молекули води 5
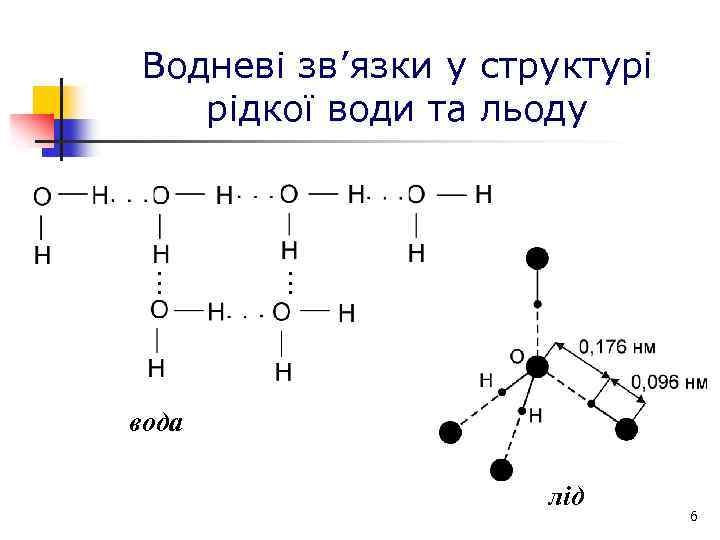 Водневі зв’язки у структурі рідкої води та льоду . . . вода лід 6
Водневі зв’язки у структурі рідкої води та льоду . . . вода лід 6
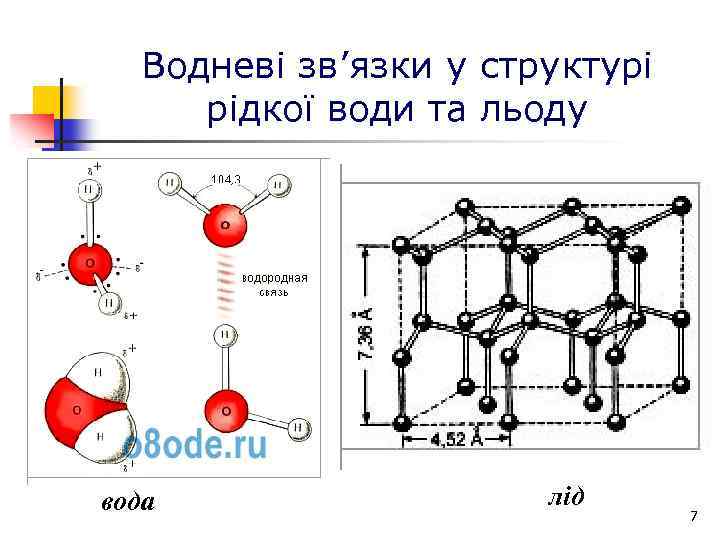 Водневі зв’язки у структурі рідкої води та льоду вода лід 7
Водневі зв’язки у структурі рідкої води та льоду вода лід 7
 Хімічні властивості води: 1) реагує з активними металами 2 K + 2 H 2 O = 2 KOH + H 2 2 Na + 2 H 2 O = 2 Na. OH + H 2 Mg + H 2 O(пара) = Mg. O + H 2 8
Хімічні властивості води: 1) реагує з активними металами 2 K + 2 H 2 O = 2 KOH + H 2 2 Na + 2 H 2 O = 2 Na. OH + H 2 Mg + H 2 O(пара) = Mg. O + H 2 8
 Хімічні властивості води: 2) сполучається з деякими основними і кислотними оксидами Na 2 O + H 2 O = 2 Na. OH; Сa. O +H 2 O = Ca(OH)2; SO 3 + H 2 O = H 2 SO 4; P 2 O 5 + 3 H 2 O = 2 H 3 PO 4. 9
Хімічні властивості води: 2) сполучається з деякими основними і кислотними оксидами Na 2 O + H 2 O = 2 Na. OH; Сa. O +H 2 O = Ca(OH)2; SO 3 + H 2 O = H 2 SO 4; P 2 O 5 + 3 H 2 O = 2 H 3 PO 4. 9
 Хімічні властивості води 3) реагує з активними неметалами (галогени) 2 F 2 + 2 H 2 O = 4 HF + O 2; Cl 2 + H 2 O = HCl + HCl. O; 4) каталізує деякі реакції 2 Al + 3 J 2 = 2 Al. J 3. 10
Хімічні властивості води 3) реагує з активними неметалами (галогени) 2 F 2 + 2 H 2 O = 4 HF + O 2; Cl 2 + H 2 O = HCl + HCl. O; 4) каталізує деякі реакції 2 Al + 3 J 2 = 2 Al. J 3. 10
 Хімічні властивості води 5) реагує iз залізом на повітрі, утворюючи іржу 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3; 6) бере участь в реакції гідролізу Al 2 S 3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 S ; Al 2(CO 3)3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 O + 3 CO 2. 11
Хімічні властивості води 5) реагує iз залізом на повітрі, утворюючи іржу 4 Fe + 3 O 2 + 6 H 2 O = 4 Fe(OH)3; 6) бере участь в реакції гідролізу Al 2 S 3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 S ; Al 2(CO 3)3 + 6 H 2 O = 2 Al(OH)3 + 3 H 2 O + 3 CO 2. 11
 Кристалогідрати Ø Cu. SO 4 5 H 2 O – мідний купорос; Ø Fe. SO 4 7 H 2 O – залізний купорос; Ø Na 2 CO 3 10 H 2 O – кальцинована сода; Ø Na 2 SO 4 10 H 2 O – глауберова сіль (мірабіліт); Ø Mg. SO 4 7 H 2 O – гірка сіль; Ø Сa. SO 4 2 H 2 O – гіпс. 12
Кристалогідрати Ø Cu. SO 4 5 H 2 O – мідний купорос; Ø Fe. SO 4 7 H 2 O – залізний купорос; Ø Na 2 CO 3 10 H 2 O – кальцинована сода; Ø Na 2 SO 4 10 H 2 O – глауберова сіль (мірабіліт); Ø Mg. SO 4 7 H 2 O – гірка сіль; Ø Сa. SO 4 2 H 2 O – гіпс. 12
 Кристалогідрати Мідний купорос Залізний купорос Cu. SO 4 5 H 2 O Fe. SO 4 7 H 2 O 13
Кристалогідрати Мідний купорос Залізний купорос Cu. SO 4 5 H 2 O Fe. SO 4 7 H 2 O 13
 Кристалогідрати Мірабіліт Гіпсова “троянда” Na 2 SO 4 10 H 2 O Сa. SO 4 2 H 2 O 14
Кристалогідрати Мірабіліт Гіпсова “троянда” Na 2 SO 4 10 H 2 O Сa. SO 4 2 H 2 O 14
 Діаграма стану води n n Діаграма стану – графічне зображення залежності між різними величинами, що характеризують стан системи. Система – тіло або група тіл, мислено відособлених від оточуючого середовища. Гомогенна система складається з однієї фази, гетерогенна – з кількох фаз. Фаза – однорідна частина системи, відділена від інших її частин поверхнею поділу, при переході через яку стрибкоподібно змінюються властивості. 15
Діаграма стану води n n Діаграма стану – графічне зображення залежності між різними величинами, що характеризують стан системи. Система – тіло або група тіл, мислено відособлених від оточуючого середовища. Гомогенна система складається з однієї фази, гетерогенна – з кількох фаз. Фаза – однорідна частина системи, відділена від інших її частин поверхнею поділу, при переході через яку стрибкоподібно змінюються властивості. 15
 Діаграма стану n n n Компоненти – індивідуальні хімічні речовини, які утворюють всі фази даної системи. Параметри – величини, що характеризують стан системи (тиск, температура, концентрація тощо). Ступені вільності – незалежні параметри рівноважної системи, які можуть набувати довільних значень в певному інтервалі, не викликаючи зміни числа фаз у цій системі. 16
Діаграма стану n n n Компоненти – індивідуальні хімічні речовини, які утворюють всі фази даної системи. Параметри – величини, що характеризують стан системи (тиск, температура, концентрація тощо). Ступені вільності – незалежні параметри рівноважної системи, які можуть набувати довільних значень в певному інтервалі, не викликаючи зміни числа фаз у цій системі. 16
 Правило фаз Гіббса n n n Правило фаз: в ізольованій рівноважній системі число фаз (Ф) плюс число ступенів вільності (С) дорівнює числу компонентів (К) плюс два: Ф + С = К + 2. Число ступенів вільності показує, скільки параметрів, які характеризують стан рівноважної системи, можна довільно змінювати, не змінюючи числа фаз у системі. Для однокомпонентної системи: С = 3 – Ф. 17
Правило фаз Гіббса n n n Правило фаз: в ізольованій рівноважній системі число фаз (Ф) плюс число ступенів вільності (С) дорівнює числу компонентів (К) плюс два: Ф + С = К + 2. Число ступенів вільності показує, скільки параметрів, які характеризують стан рівноважної системи, можна довільно змінювати, не змінюючи числа фаз у системі. Для однокомпонентної системи: С = 3 – Ф. 17
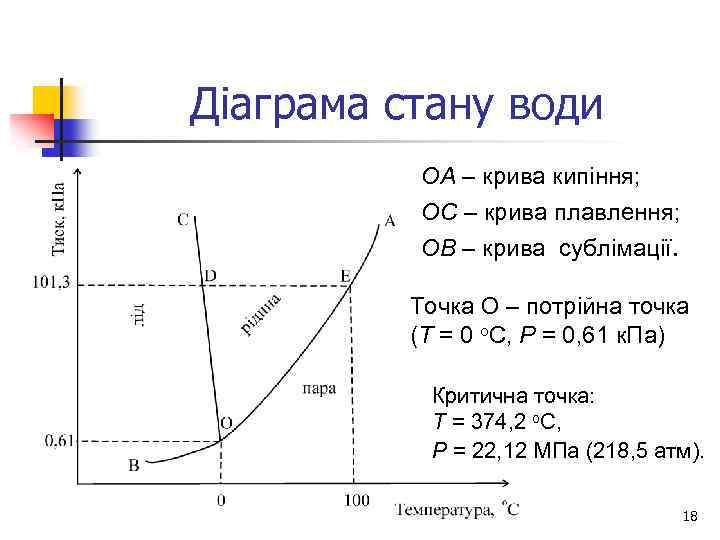 Діаграма стану води ОА – крива кипіння; ОС – крива плавлення; ОВ – крива сублімації. Точка О – потрійна точка (Т = 0 о. С, Р = 0, 61 к. Па) Критична точка: Т = 374, 2 о. С, Р = 22, 12 МПа (218, 5 атм). 18
Діаграма стану води ОА – крива кипіння; ОС – крива плавлення; ОВ – крива сублімації. Точка О – потрійна точка (Т = 0 о. С, Р = 0, 61 к. Па) Критична точка: Т = 374, 2 о. С, Р = 22, 12 МПа (218, 5 атм). 18
 Характеристика розчинів n n n Розчини – гомогенні, термодинамічно стійкі, рівноважні системи, що складаються з двох і більше компонентів та продуктів їх взаємодії. Розчини: рідкі, тверді і газоподібні. Розчинник – компонент, який кількісно переважає і зберігає свій агрегатний стан при утворенні розчину; інші компоненти – розчинені речовини. 19
Характеристика розчинів n n n Розчини – гомогенні, термодинамічно стійкі, рівноважні системи, що складаються з двох і більше компонентів та продуктів їх взаємодії. Розчини: рідкі, тверді і газоподібні. Розчинник – компонент, який кількісно переважає і зберігає свій агрегатний стан при утворенні розчину; інші компоненти – розчинені речовини. 19
 Процес розчинення n n Процес утворення розчину включає фізичну і хімічну взаємодію. Процеси при розчиненні: Ø Ø n руйнування структури речовини, що розчиняється; взаємодія розчинника з частинками розчиненої речовини (сольватація). Сольвати - асоціати, утворені при взаємодії молекул розчиненої речовини і розчинника, (якщо розчинником є вода – гідрати). 20
Процес розчинення n n Процес утворення розчину включає фізичну і хімічну взаємодію. Процеси при розчиненні: Ø Ø n руйнування структури речовини, що розчиняється; взаємодія розчинника з частинками розчиненої речовини (сольватація). Сольвати - асоціати, утворені при взаємодії молекул розчиненої речовини і розчинника, (якщо розчинником є вода – гідрати). 20
 Процес розчинення n n Ентальпія розчинення –кількість теплоти, яка виділяється або поглинається при розчиненні 1 моля речовини. Тепловий ефект розчинення ( Н 0) залежить від співвідношення енергії кристалічної ґратки речовини, яка розчиняється (Е), і енергії взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації, Н 1): Н 0 = –Е + Н 1. n Якщо Н 1 > Е, то Н 0 < 0 – процес екзотермічний; n Якщо Н 1 < E, то Н 0 > 0 – процес ендотермічний. 21
Процес розчинення n n Ентальпія розчинення –кількість теплоти, яка виділяється або поглинається при розчиненні 1 моля речовини. Тепловий ефект розчинення ( Н 0) залежить від співвідношення енергії кристалічної ґратки речовини, яка розчиняється (Е), і енергії взаємодії розчиненої речовини з молекулами розчинника (ентальпія сольватації, Н 1): Н 0 = –Е + Н 1. n Якщо Н 1 > Е, то Н 0 < 0 – процес екзотермічний; n Якщо Н 1 < E, то Н 0 > 0 – процес ендотермічний. 21
 Класифікація розчинів за кількістю розчиненої речовини n n n Розчин, що перебуває в рівновазі з надлишком речовини, яка розчиняється, - насичений. У ненасиченому розчині міститься менше розчиненої речовини, а в пересиченому – більше, ніж у насиченому. Розчинність речовин залежить від: Ø природи розчиненої речовини і розчинника, Ø агрегатного стану розчиненої речовини, Ø зовнішніх умов (температура, тиск). 22
Класифікація розчинів за кількістю розчиненої речовини n n n Розчин, що перебуває в рівновазі з надлишком речовини, яка розчиняється, - насичений. У ненасиченому розчині міститься менше розчиненої речовини, а в пересиченому – більше, ніж у насиченому. Розчинність речовин залежить від: Ø природи розчиненої речовини і розчинника, Ø агрегатного стану розчиненої речовини, Ø зовнішніх умов (температура, тиск). 22
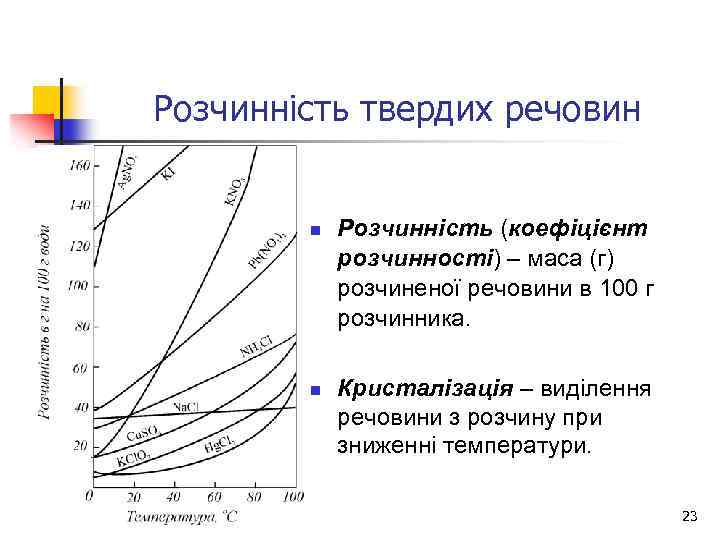 Розчинність твердих речовин n n Розчинність (коефіцієнт розчинності) – маса (г) розчиненої речовини в 100 г розчинника. Кристалізація – виділення речовини з розчину при зниженні температури. 23
Розчинність твердих речовин n n Розчинність (коефіцієнт розчинності) – маса (г) розчиненої речовини в 100 г розчинника. Кристалізація – виділення речовини з розчину при зниженні температури. 23
 Розчинність рідин n Розчинність рідин у воді: а) необмежено розчинні (спирт, гліцерин, Н 2 О 2 тощо); б) обмежено розчинні (діетиловий етер, анілін); в) майже нерозчинні (бензен, гас). n Критична температура розчинення - температура, при якій обмежена взаємна розчинність рідин переходить у необмежену. 24
Розчинність рідин n Розчинність рідин у воді: а) необмежено розчинні (спирт, гліцерин, Н 2 О 2 тощо); б) обмежено розчинні (діетиловий етер, анілін); в) майже нерозчинні (бензен, гас). n Критична температура розчинення - температура, при якій обмежена взаємна розчинність рідин переходить у необмежену. 24
 Закон розподілу Речовина, здатна розчинятися у двох розчинниках, які не змішуються між собою, розподіляється між ними так, що відношення її концентрацій у цих розчинниках за сталої температури залишається сталим, незалежно від загальної кількості розчиненої речовини: де С 1 і С 2 – концентрації розчиненої речовини відповідно у першому і другому розчиннику; K – коефіцієнт розподілу. 25
Закон розподілу Речовина, здатна розчинятися у двох розчинниках, які не змішуються між собою, розподіляється між ними так, що відношення її концентрацій у цих розчинниках за сталої температури залишається сталим, незалежно від загальної кількості розчиненої речовини: де С 1 і С 2 – концентрації розчиненої речовини відповідно у першому і другому розчиннику; K – коефіцієнт розподілу. 25
 Екстракція n n Екстракція – спосіб вилучення розчиненої речовини з розчину за допомогою іншого розчинника, який не змішується з першим. Екстракція, як спосіб розділення і концентрування речовин, широко використовується в лабораторній практиці і у хімічній промисловості. 26
Екстракція n n Екстракція – спосіб вилучення розчиненої речовини з розчину за допомогою іншого розчинника, який не змішується з першим. Екстракція, як спосіб розділення і концентрування речовин, широко використовується в лабораторній практиці і у хімічній промисловості. 26
 Розчинність газів n Розчинність газів у рідинах залежить від тиску, температури і від хімічної природи газу. Закон Генрі: маса газу, що розчиняється за сталої температури в певному об’ємі рідини, прямо пропорційна парціальному тиску газу: С = k. P при Т = const, С – масова концентрація газу в насиченому розчині; Р – парціальний тиск газу; k – константа Генрі. Наслідок: об’єм газу, який розчиняється за сталої температури у певному об’ємі рідини, не залежить від парціального тиску газу. 27
Розчинність газів n Розчинність газів у рідинах залежить від тиску, температури і від хімічної природи газу. Закон Генрі: маса газу, що розчиняється за сталої температури в певному об’ємі рідини, прямо пропорційна парціальному тиску газу: С = k. P при Т = const, С – масова концентрація газу в насиченому розчині; Р – парціальний тиск газу; k – константа Генрі. Наслідок: об’єм газу, який розчиняється за сталої температури у певному об’ємі рідини, не залежить від парціального тиску газу. 27
 Концентрація. Способи вираження концентрацій Концентрація – це вміст розчиненої речовини в певному об’ємі або масі розчину чи розчинника. n Способи вираження концентрацій: 1) масова частка (%) n 2) молярна концентрація (моль/л) 28
Концентрація. Способи вираження концентрацій Концентрація – це вміст розчиненої речовини в певному об’ємі або масі розчину чи розчинника. n Способи вираження концентрацій: 1) масова частка (%) n 2) молярна концентрація (моль/л) 28
 Способи вираження концентрацій 3) молярна концентрація еквівалента (моль/л) 4) моляльна концентрація (моль/1000 г розчинника) 5) мольна частка 6) титр (г/мл) 29
Способи вираження концентрацій 3) молярна концентрація еквівалента (моль/л) 4) моляльна концентрація (моль/1000 г розчинника) 5) мольна частка 6) титр (г/мл) 29
 Властивості розчинів неелектролітів n Колігативні властивості розчинів залежать лише від концентрації розчину і не залежать від природи розчиненої речовини: Ø явище осмосу, Ø зниження тиску пари над розчином, Ø зниження температури замерзання і підвищення температури кипіння розчинів стосовно до чистого розчинника. 30
Властивості розчинів неелектролітів n Колігативні властивості розчинів залежать лише від концентрації розчину і не залежать від природи розчиненої речовини: Ø явище осмосу, Ø зниження тиску пари над розчином, Ø зниження температури замерзання і підвищення температури кипіння розчинів стосовно до чистого розчинника. 30
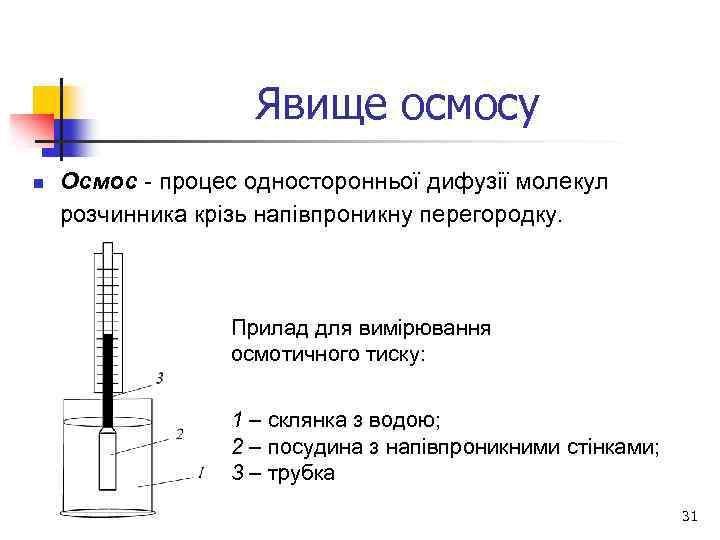 Явище осмосу n Осмос - процес односторонньої дифузії молекул розчинника крізь напівпроникну перегородку. Прилад для вимірювання осмотичного тиску: 1 – склянка з водою; 2 – посудина з напівпроникними стінками; 3 – трубка 31
Явище осмосу n Осмос - процес односторонньої дифузії молекул розчинника крізь напівпроникну перегородку. Прилад для вимірювання осмотичного тиску: 1 – склянка з водою; 2 – посудина з напівпроникними стінками; 3 – трубка 31
 Осмотичний тиск n Осмотичний тиск не залежить від природи компонентів розчину, а збільшується пропорційно до концентрації розчиненої речовини і абсолютної температури: росм = CМRT. Закон Вант-Гоффа: осмотичний тиск розчину дорівнює тиску, який би чинила розчинена речовина, якби вона за цієї ж температури була в газоподібному стані і займала об’єм, що дорівнює об’єму розчину. n Знаходження молярної маси розчиненої речовини за осмотичним тиском: n 32
Осмотичний тиск n Осмотичний тиск не залежить від природи компонентів розчину, а збільшується пропорційно до концентрації розчиненої речовини і абсолютної температури: росм = CМRT. Закон Вант-Гоффа: осмотичний тиск розчину дорівнює тиску, який би чинила розчинена речовина, якби вона за цієї ж температури була в газоподібному стані і займала об’єм, що дорівнює об’єму розчину. n Знаходження молярної маси розчиненої речовини за осмотичним тиском: n 32
 Зниження тиску пари над розчином n n n Тиск пари розчинника над розчином нелеткої речовини є завжди меншим, ніж тиск пари над чистим розчинником за однакової температури. р0–р = р – зниження тиску пари над розчином: р0 – тиск насиченої пари розчинника над чистим розчинником; р - тиск насиченої пари розчинника над розчином. Відносне зниження тиску пари над розчином: 33
Зниження тиску пари над розчином n n n Тиск пари розчинника над розчином нелеткої речовини є завжди меншим, ніж тиск пари над чистим розчинником за однакової температури. р0–р = р – зниження тиску пари над розчином: р0 – тиск насиченої пари розчинника над чистим розчинником; р - тиск насиченої пари розчинника над розчином. Відносне зниження тиску пари над розчином: 33
 Зниження тиску пари над розчином Перший закон Рауля: відносне зниження тиску насиченої пари розчинника над розчином прямо пропорційне мольній частці розчиненої речовини n де n 2 – мольна частка розчиненої речовини. n Визначення молярної маси розчиненої речовини (М 2): m 2 – маса розчиненої речовини, г; 1 – число молів розчинника. 34
Зниження тиску пари над розчином Перший закон Рауля: відносне зниження тиску насиченої пари розчинника над розчином прямо пропорційне мольній частці розчиненої речовини n де n 2 – мольна частка розчиненої речовини. n Визначення молярної маси розчиненої речовини (М 2): m 2 – маса розчиненої речовини, г; 1 – число молів розчинника. 34
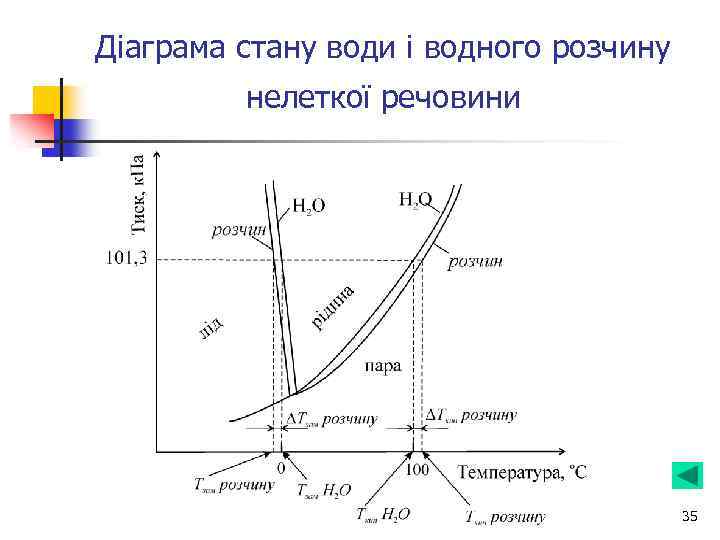 Діаграма стану води і водного розчину нелеткої речовини 35
Діаграма стану води і водного розчину нелеткої речовини 35
 Температура замерзання та кипіння розчину n Другий закон Рауля: підвищення температури кипіння і зниження температури замерзання розчину прямо пропорційне моляльній концентрації (Сm) розчиненої речовини: Ткип = ЕСm; Е – ебуліоскопічна стала; Тзам = KСm; K – кріоскопічна стала. n Визначення молярної маси розчиненої речовини: 36
Температура замерзання та кипіння розчину n Другий закон Рауля: підвищення температури кипіння і зниження температури замерзання розчину прямо пропорційне моляльній концентрації (Сm) розчиненої речовини: Ткип = ЕСm; Е – ебуліоскопічна стала; Тзам = KСm; K – кріоскопічна стала. n Визначення молярної маси розчиненої речовини: 36


