lecture_2008b.ppt
- Количество слайдов: 117
 Внутри- и межклеточная сигнализация
Внутри- и межклеточная сигнализация
 Основная цель сигнальных систем - адаптация 1) Сигнал - То, что служит толчком к началу какогонибудь действия 2) Сигнал - Условный знак для передачи на расстояние каких-нибудь сведений, сообщений 3) Сигнал - Предупреждение, сообщение о чем-нибудь нежелательном Сигнал - (от лат. signum - знак) - знак, физический процесс (или явление), несущий сообщение (информацию) о каком-либо событии, состоянии объекта наблюдения либо передающий команды управления, указания, оповещения и т. д. (напр. , световой сигнал светофора). Из разных толковых словарей СИГНАЛ лиганд гормон
Основная цель сигнальных систем - адаптация 1) Сигнал - То, что служит толчком к началу какогонибудь действия 2) Сигнал - Условный знак для передачи на расстояние каких-нибудь сведений, сообщений 3) Сигнал - Предупреждение, сообщение о чем-нибудь нежелательном Сигнал - (от лат. signum - знак) - знак, физический процесс (или явление), несущий сообщение (информацию) о каком-либо событии, состоянии объекта наблюдения либо передающий команды управления, указания, оповещения и т. д. (напр. , световой сигнал светофора). Из разных толковых словарей СИГНАЛ лиганд гормон
 Узнавание сигнала - первый шаг в адаптивной реакции Сигнал из внешней среды - может быть угрозой целостности организма, органа или единственной клетки в пределах того же организма или способствовать сохранению этой целостности. На уровне организма узнавание сигнала обеспечивается нервной системой и специальными органами чувств (зрение, слух, боль, запах, контакт). На уровне органов и клеток сигналами могут быть физикохимические факторы: концентрация О 2 , температура, осмолярность, р. Н, изменение поступления питательных веществ, появление вредных метаболитов и др. Адекватное узнавание изменений клеткой вызывает образование и высвобождение ею одного или нескольких собственных сигналов (лигандов) , которые должны генерировать необходимую адаптивную реакцию со стороны других клеток или организма в целом
Узнавание сигнала - первый шаг в адаптивной реакции Сигнал из внешней среды - может быть угрозой целостности организма, органа или единственной клетки в пределах того же организма или способствовать сохранению этой целостности. На уровне организма узнавание сигнала обеспечивается нервной системой и специальными органами чувств (зрение, слух, боль, запах, контакт). На уровне органов и клеток сигналами могут быть физикохимические факторы: концентрация О 2 , температура, осмолярность, р. Н, изменение поступления питательных веществ, появление вредных метаболитов и др. Адекватное узнавание изменений клеткой вызывает образование и высвобождение ею одного или нескольких собственных сигналов (лигандов) , которые должны генерировать необходимую адаптивную реакцию со стороны других клеток или организма в целом
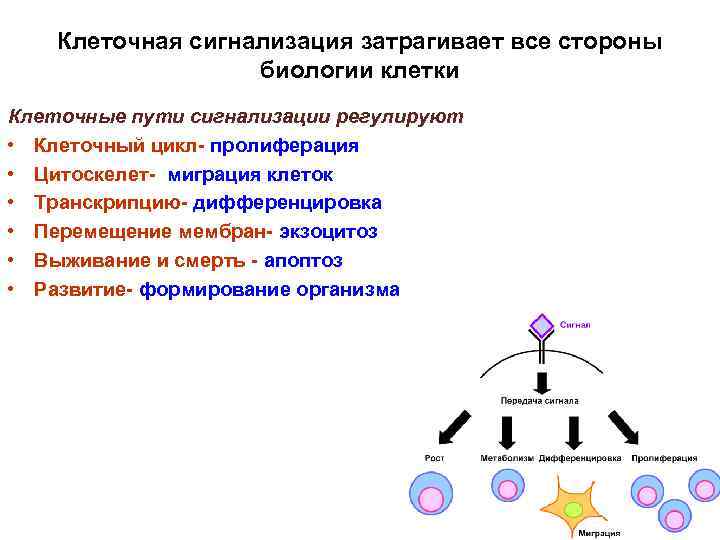 Клеточная сигнализация затрагивает все стороны биологии клетки Клеточные пути сигнализации регулируют • Клеточный цикл- пролиферация • Цитоскелет- миграция клеток • Транскрипцию- дифференцировка • Перемещение мембран- экзоцитоз • Выживание и смерть - апоптоз • Развитие- формирование организма
Клеточная сигнализация затрагивает все стороны биологии клетки Клеточные пути сигнализации регулируют • Клеточный цикл- пролиферация • Цитоскелет- миграция клеток • Транскрипцию- дифференцировка • Перемещение мембран- экзоцитоз • Выживание и смерть - апоптоз • Развитие- формирование организма
 Нарушения меж- и внутриклеточной сигнализации – основная причина болезней Диабет Опухоли Стероиды Виагра СПИД Холера Болезни сердца и сосудов Нейродегенеративные болезни (б-нь Альцгеймера……. Циррозы …и многое другое
Нарушения меж- и внутриклеточной сигнализации – основная причина болезней Диабет Опухоли Стероиды Виагра СПИД Холера Болезни сердца и сосудов Нейродегенеративные болезни (б-нь Альцгеймера……. Циррозы …и многое другое
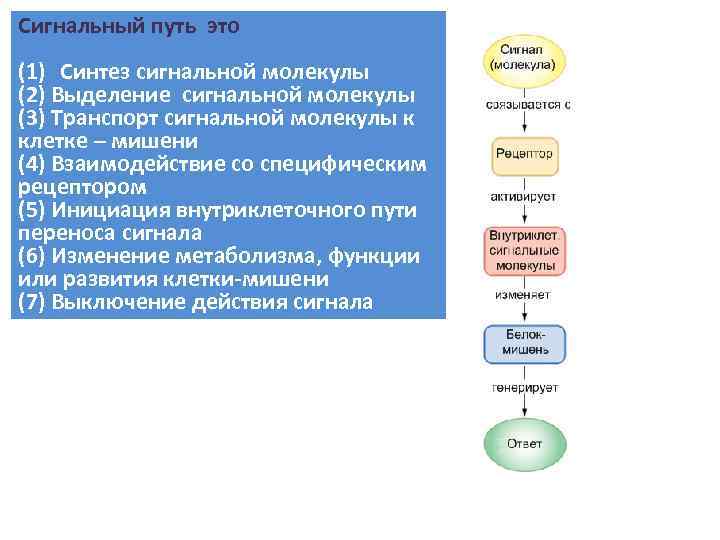 Сигнальный путь это (1) Cинтез сигнальной молекулы (2) Выделение сигнальной молекулы (3) Транспорт сигнальной молекулы к клетке – мишени (4) Взаимодействие со специфическим рецептором (5) Инициация внутриклеточного пути переноса сигнала (6) Изменение метаболизма, функции или развития клетки-мишени (7) Выключение действия сигнала
Сигнальный путь это (1) Cинтез сигнальной молекулы (2) Выделение сигнальной молекулы (3) Транспорт сигнальной молекулы к клетке – мишени (4) Взаимодействие со специфическим рецептором (5) Инициация внутриклеточного пути переноса сигнала (6) Изменение метаболизма, функции или развития клетки-мишени (7) Выключение действия сигнала
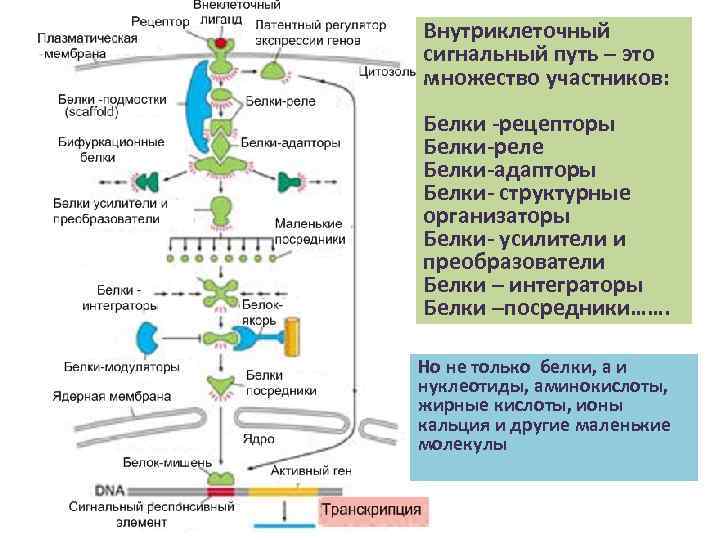 Внутриклеточный сигнальный путь – это множество участников: Белки -рецепторы Белки-реле Белки-адапторы Белки- структурные организаторы Белки- усилители и преобразователи Белки – интеграторы Белки –посредники……. Но не только белки, а и нуклеотиды, аминокислоты, жирные кислоты, ионы кальция и другие маленькие молекулы
Внутриклеточный сигнальный путь – это множество участников: Белки -рецепторы Белки-реле Белки-адапторы Белки- структурные организаторы Белки- усилители и преобразователи Белки – интеграторы Белки –посредники……. Но не только белки, а и нуклеотиды, аминокислоты, жирные кислоты, ионы кальция и другие маленькие молекулы
 Откуда пошли сигналы Лиганды-сигналы – это побочные продукты метаболических путей , означавших избыток или недостаток источников питания Рецепторы и регуляторные белки были отобраны в процессе эволюции. В пользу этого говорит высокий консерватизм у разных видов живого в строении и функциях многих сигнальных путей
Откуда пошли сигналы Лиганды-сигналы – это побочные продукты метаболических путей , означавших избыток или недостаток источников питания Рецепторы и регуляторные белки были отобраны в процессе эволюции. В пользу этого говорит высокий консерватизм у разных видов живого в строении и функциях многих сигнальных путей
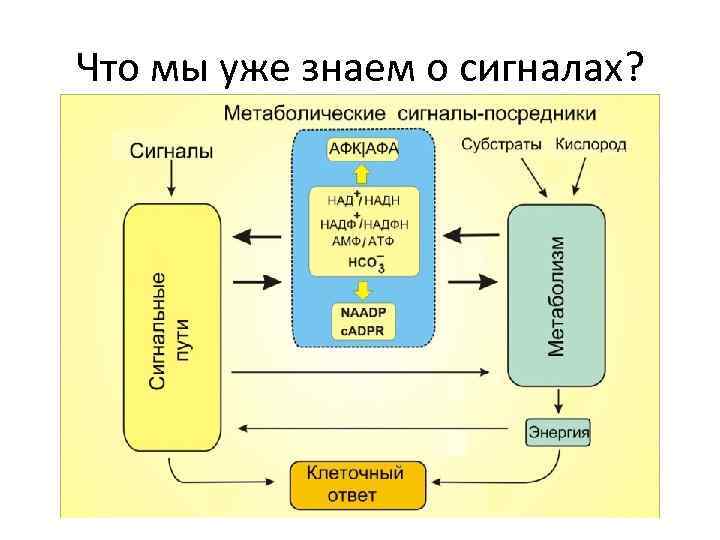 Что мы уже знаем о сигналах?
Что мы уже знаем о сигналах?
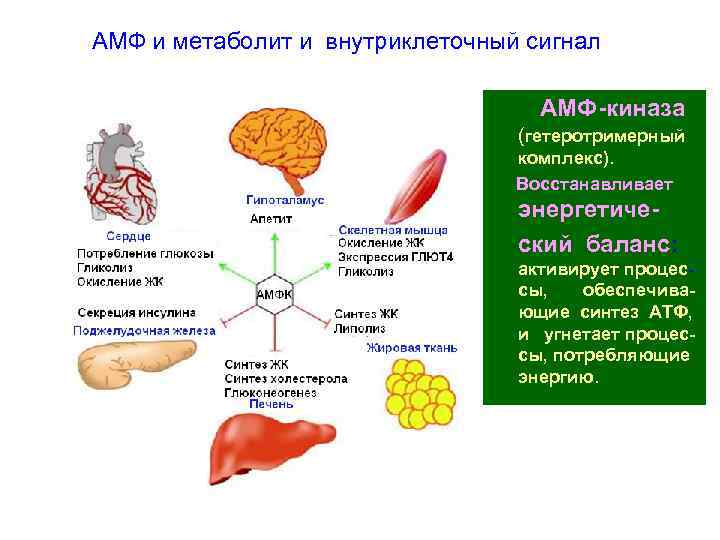 АМФ и метаболит и внутриклеточный сигнал АМФ-киназа (гетеротримерный комплекс). Восстанавливает энергетический баланс: активирует процессы, обеспечивающие синтез АТФ, и угнетает процессы, потребляющие энергию.
АМФ и метаболит и внутриклеточный сигнал АМФ-киназа (гетеротримерный комплекс). Восстанавливает энергетический баланс: активирует процессы, обеспечивающие синтез АТФ, и угнетает процессы, потребляющие энергию.
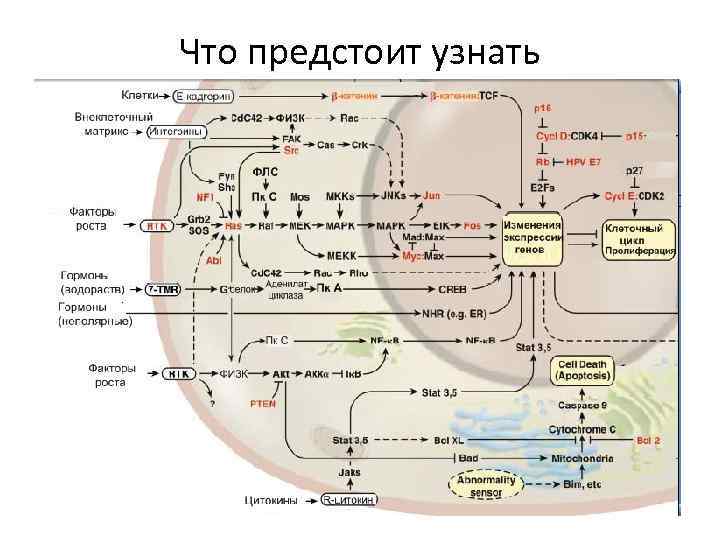 Что предстоит узнать
Что предстоит узнать
 Сигналы бывают разные Антигены Факторы роста Гликопротеины Гормоны поверхности клеток р. Н, осмотическое Свет, звук давление Компоненты Механическое внеклеточного матрикса воздействие Нейромедиаторы Одоранты Феромоны Вкусовые вещества Разделим молекулы-сигналы на липофильные и гидрофильные потому…. .
Сигналы бывают разные Антигены Факторы роста Гликопротеины Гормоны поверхности клеток р. Н, осмотическое Свет, звук давление Компоненты Механическое внеклеточного матрикса воздействие Нейромедиаторы Одоранты Феромоны Вкусовые вещества Разделим молекулы-сигналы на липофильные и гидрофильные потому…. .
 …что свойства сигналов определяют механизм их действия • Липофильные молекулы, взаимодействуют с внутриклеточными рецепторами(стероиды, ретиноиды, NO и др. ) • Гидрофильные молекулы, взаимодействуют с поверхностными рецепторами (нейромедиаторы, пептидные гормоны и факторы роста , цитокины) • Некоторые липофильные молекулы могут взаимодействовать с поверхностными рецепторами (простагландины и лейкотриены) • Факторы внешней среды, взаимодействуют с поверхностными рецепторами (свет, одоранты)
…что свойства сигналов определяют механизм их действия • Липофильные молекулы, взаимодействуют с внутриклеточными рецепторами(стероиды, ретиноиды, NO и др. ) • Гидрофильные молекулы, взаимодействуют с поверхностными рецепторами (нейромедиаторы, пептидные гормоны и факторы роста , цитокины) • Некоторые липофильные молекулы могут взаимодействовать с поверхностными рецепторами (простагландины и лейкотриены) • Факторы внешней среды, взаимодействуют с поверхностными рецепторами (свет, одоранты)
 …что свойства сигналов определяют механизм их действия • Большинство гидрофильных молекул - сигналов синтезируется и хранится в секреторных везикулах • Секреция их часто регулируется ионами [Ca ] 2+ • Гидрофобные сигналы высвобождаются по мере их образования • Время полужизни гидрофобного сигнала определяет продолжительность хронического эндокринного ответа или преходящего паракринного ответа.
…что свойства сигналов определяют механизм их действия • Большинство гидрофильных молекул - сигналов синтезируется и хранится в секреторных везикулах • Секреция их часто регулируется ионами [Ca ] 2+ • Гидрофобные сигналы высвобождаются по мере их образования • Время полужизни гидрофобного сигнала определяет продолжительность хронического эндокринного ответа или преходящего паракринного ответа.
 Быстрая и продолжительная сигнализация • Изменение активности фермента в клеткахмишенях => быстрый ответ Это обычный первичный эффект лигандов, которые связываются с поверхностными рецепторами • Изменение характера экспрессии генов => хронический ответ Это обычный первичный эффект лигандов, которые связываются с внутриклеточными рецепторами (исключение : NO) и более поздний эффект лигандов, которые связываются с поверхностными рецепторами
Быстрая и продолжительная сигнализация • Изменение активности фермента в клеткахмишенях => быстрый ответ Это обычный первичный эффект лигандов, которые связываются с поверхностными рецепторами • Изменение характера экспрессии генов => хронический ответ Это обычный первичный эффект лигандов, которые связываются с внутриклеточными рецепторами (исключение : NO) и более поздний эффект лигандов, которые связываются с поверхностными рецепторами
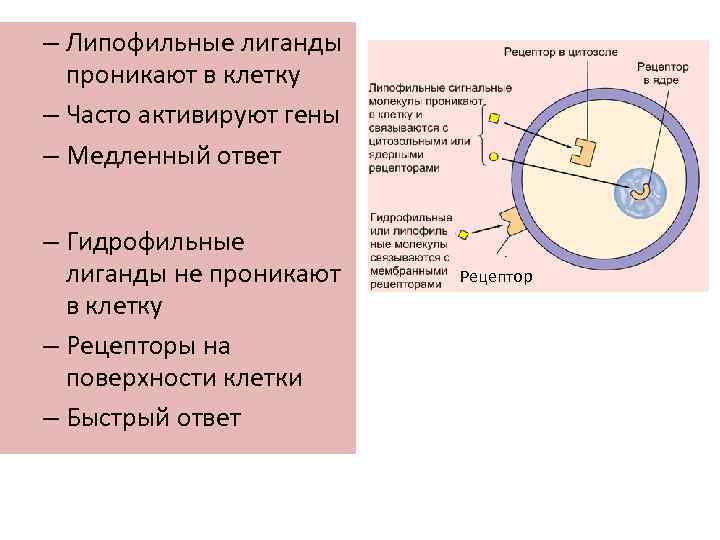 – Липофильные лиганды проникают в клетку – Часто активируют гены – Медленный ответ – Гидрофильные лиганды не проникают в клетку – Рецепторы на поверхности клетки – Быстрый ответ Рецептор
– Липофильные лиганды проникают в клетку – Часто активируют гены – Медленный ответ – Гидрофильные лиганды не проникают в клетку – Рецепторы на поверхности клетки – Быстрый ответ Рецептор
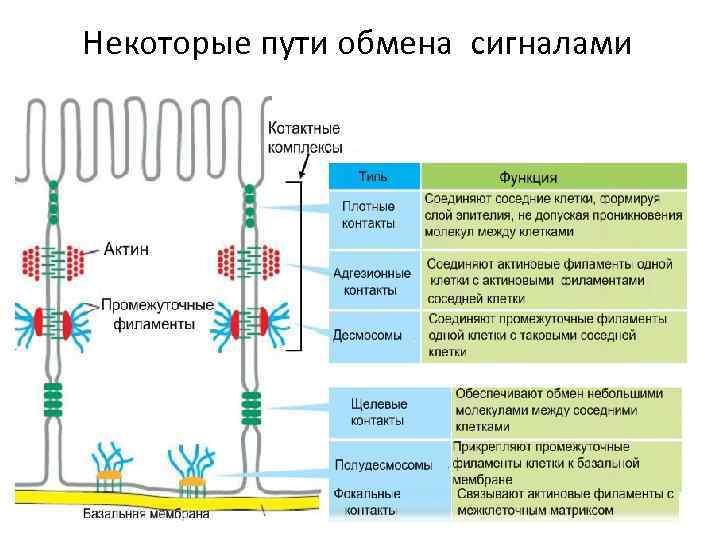 Некоторые пути обмена сигналами
Некоторые пути обмена сигналами
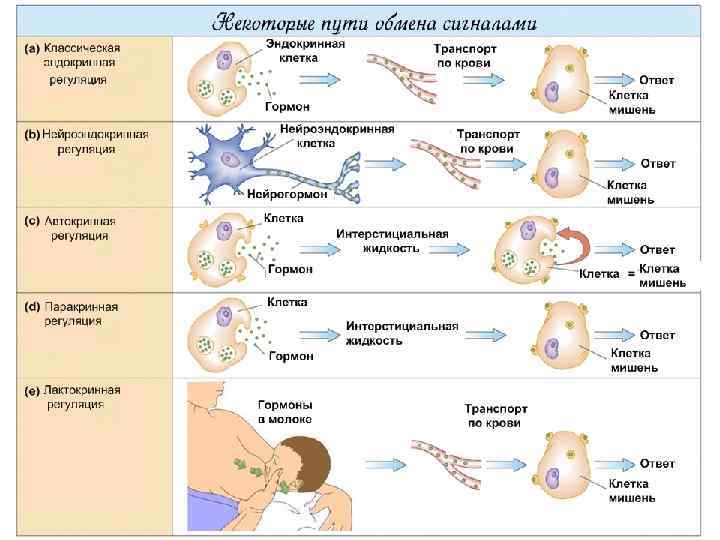
 Классификация молeкул-сигналов 1. Сигнальные молекулы, построенные из аминокислот • Сигналы - сложные белки (тиреотропин, гонадотропины) • Сигналы - простые белки (соматотропин, инсулин ) • Сигналы- пептиды ( глюкагон, кортикотропин , факторы роста, цитокины ) 2. Производные аминокислот (адреналин, серотонин, тироксин, мелатонин) 3. Стероиды (производные холестерола и других полиизопренов) (альдостерон, кортизол, ретиноевая кислота, витамин Д) 4. Эйкозаноиды ( производные 20 -углеродных, полиненасыщенных жирных кислот) (простагландин Е 1, тромбоксан А 2). Сигналы можно разделить по месту образования, растворимости в воде и неполярных растворителях и по другим критериям
Классификация молeкул-сигналов 1. Сигнальные молекулы, построенные из аминокислот • Сигналы - сложные белки (тиреотропин, гонадотропины) • Сигналы - простые белки (соматотропин, инсулин ) • Сигналы- пептиды ( глюкагон, кортикотропин , факторы роста, цитокины ) 2. Производные аминокислот (адреналин, серотонин, тироксин, мелатонин) 3. Стероиды (производные холестерола и других полиизопренов) (альдостерон, кортизол, ретиноевая кислота, витамин Д) 4. Эйкозаноиды ( производные 20 -углеродных, полиненасыщенных жирных кислот) (простагландин Е 1, тромбоксан А 2). Сигналы можно разделить по месту образования, растворимости в воде и неполярных растворителях и по другим критериям
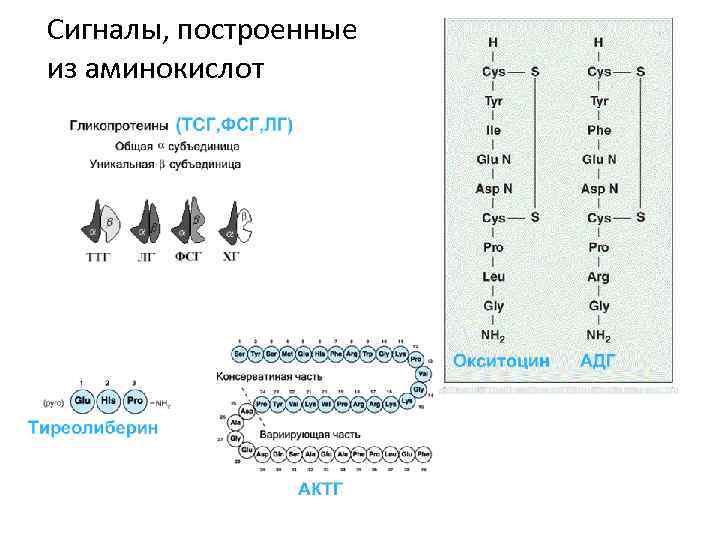 Сигналы, построенные из аминокислот
Сигналы, построенные из аминокислот
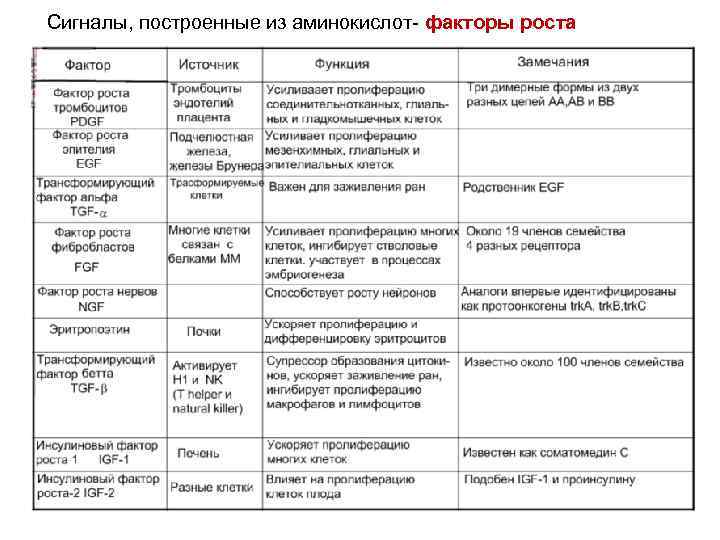 Сигналы, построенные из аминокислот- факторы роста
Сигналы, построенные из аминокислот- факторы роста
 Сигналы, построенные из аминокислот • Цитокины • Низкомолекулярные белки (30 к. Да) • Действуют аутокринно, паракринно и эндокринно. • Термин ЦИТОКИН общий для монокинов, интерлейкинов, лимфокинов, хемокинов. • Наиболее хорошо изучено их участие в иммунитете, воспалении
Сигналы, построенные из аминокислот • Цитокины • Низкомолекулярные белки (30 к. Да) • Действуют аутокринно, паракринно и эндокринно. • Термин ЦИТОКИН общий для монокинов, интерлейкинов, лимфокинов, хемокинов. • Наиболее хорошо изучено их участие в иммунитете, воспалении
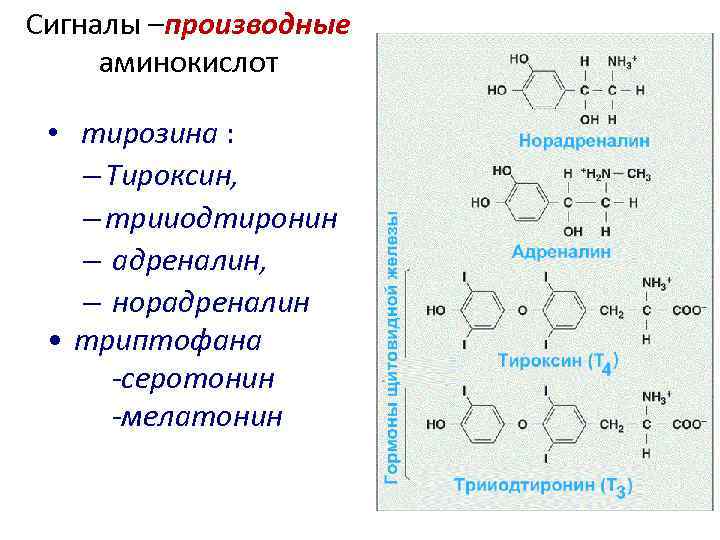 Сигналы –производные аминокислот • тирозина : – Тироксин, – трииодтиронин – адреналин, – норадреналин • триптофана -серотонин -мелатонин
Сигналы –производные аминокислот • тирозина : – Тироксин, – трииодтиронин – адреналин, – норадреналин • триптофана -серотонин -мелатонин
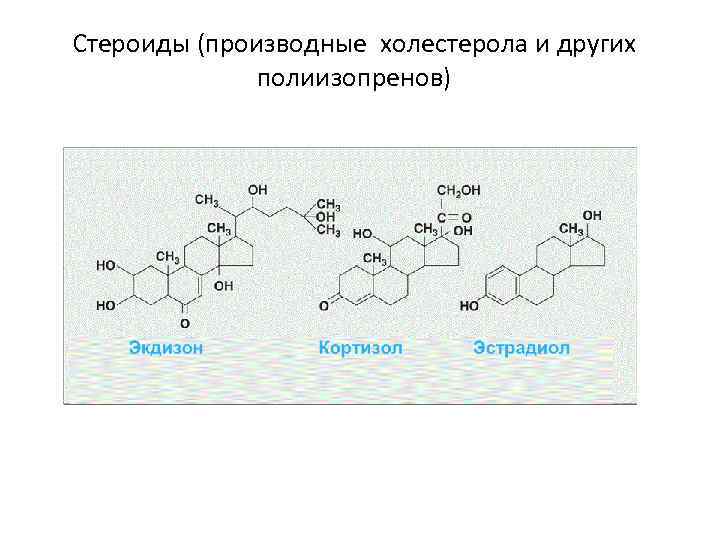 Стероиды (производные холестерола и других полиизопренов)
Стероиды (производные холестерола и других полиизопренов)
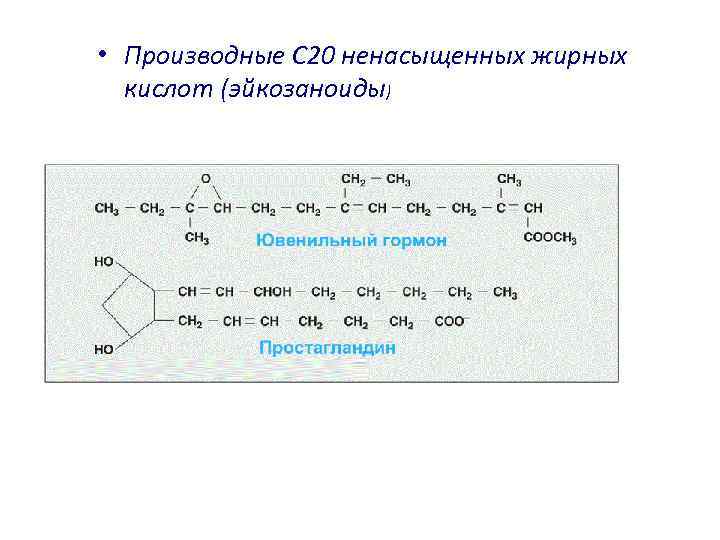 • Производные С 20 ненасыщенных жирных кислот (эйкозаноиды)
• Производные С 20 ненасыщенных жирных кислот (эйкозаноиды)
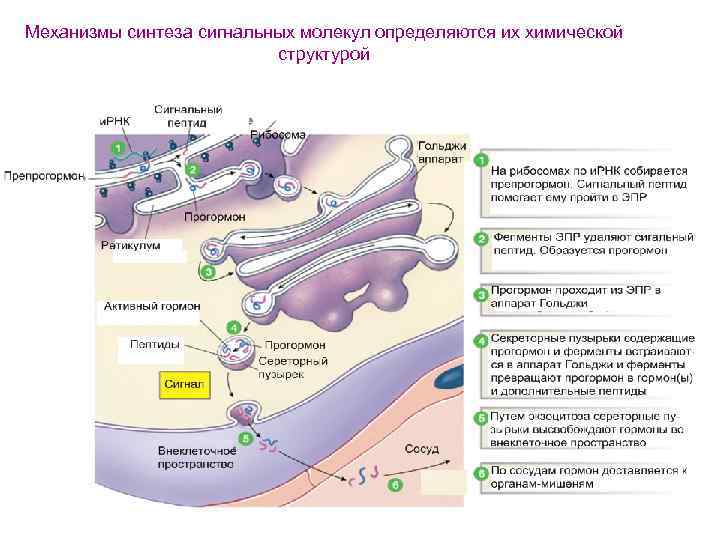 Механизмы синтеза сигнальных молекул определяются их химической структурой
Механизмы синтеза сигнальных молекул определяются их химической структурой
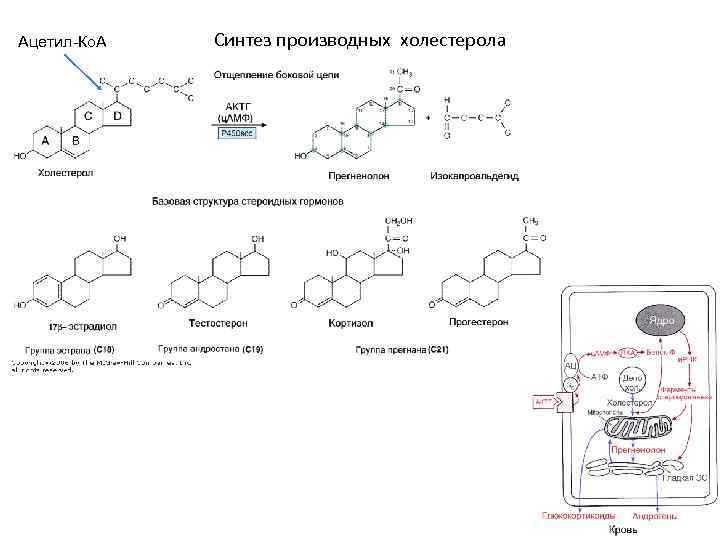 Ацетил-Ко. А Синтез производных холестерола
Ацетил-Ко. А Синтез производных холестерола
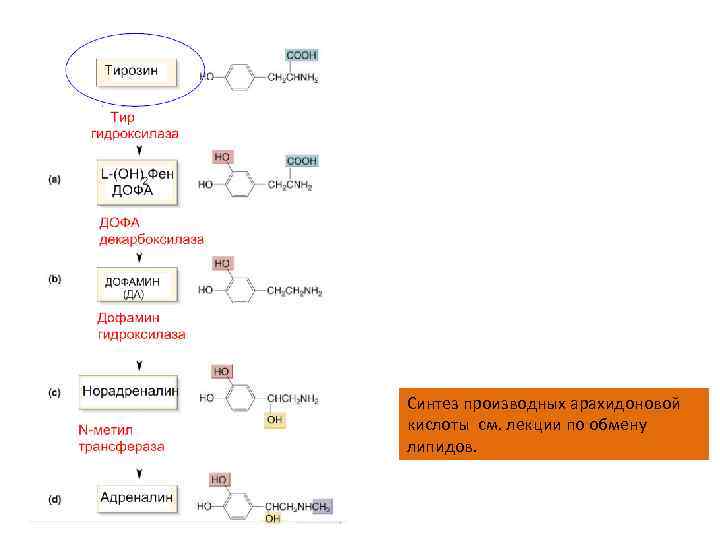 Синтез производных арахидоновой кислоты см. лекции по обмену липидов.
Синтез производных арахидоновой кислоты см. лекции по обмену липидов.
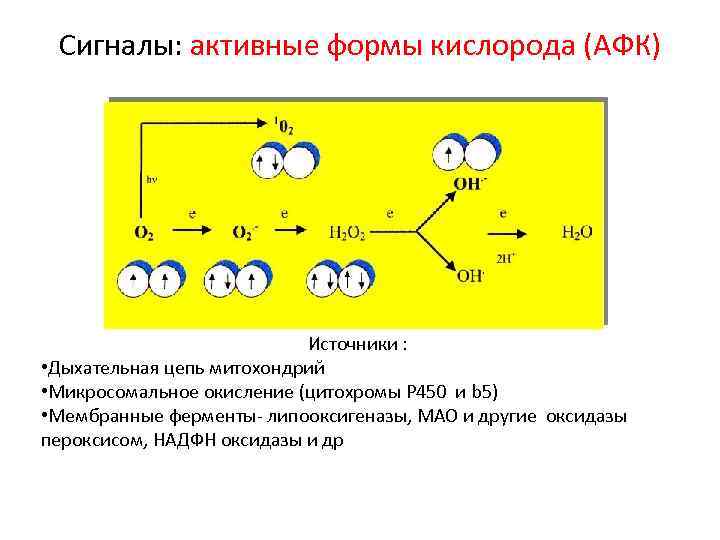 Сигналы: активные формы кислорода (АФК) Источники : • Дыхательная цепь митохондрий • Микросомальное окисление (цитохромы Р 450 и b 5) • Мембранные ферменты- липооксигеназы, МАО и другие оксидазы пероксисом, НАДФН оксидазы и др
Сигналы: активные формы кислорода (АФК) Источники : • Дыхательная цепь митохондрий • Микросомальное окисление (цитохромы Р 450 и b 5) • Мембранные ферменты- липооксигеназы, МАО и другие оксидазы пероксисом, НАДФН оксидазы и др
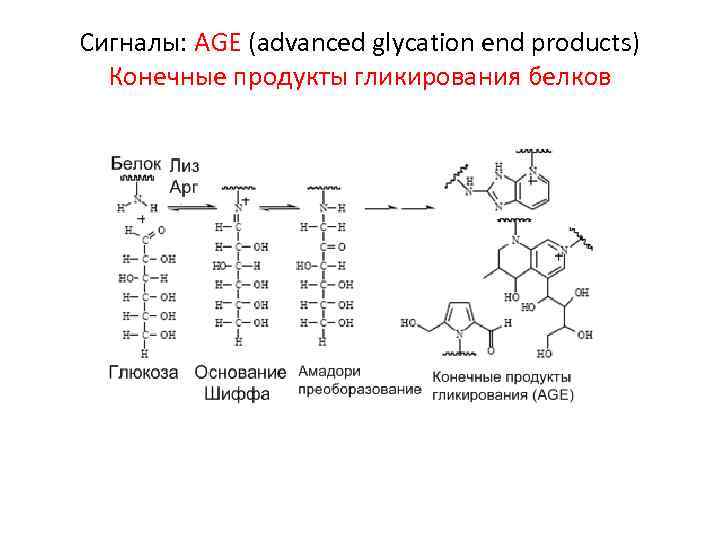 Сигналы: AGE (advanced glycation end products) Конечные продукты гликирования белков
Сигналы: AGE (advanced glycation end products) Конечные продукты гликирования белков
 Оксид азота (NO) образуется из аргинина Фермент синтаза оксида азота (NOS) содержит четыре кофермента –ФАД, ФМН, гем и тетрагидроптерин и катализирует обе стадии этой реакции NO – короткоживущий посредник (мессенжер), участвующий в регуляции артериального давления, свертывания крови и проведения нервных импульсов. NO связывается с гуанилатциклазой и активирует образование ц. ГМФ вторичного посредника сигнальных систем клеток.
Оксид азота (NO) образуется из аргинина Фермент синтаза оксида азота (NOS) содержит четыре кофермента –ФАД, ФМН, гем и тетрагидроптерин и катализирует обе стадии этой реакции NO – короткоживущий посредник (мессенжер), участвующий в регуляции артериального давления, свертывания крови и проведения нервных импульсов. NO связывается с гуанилатциклазой и активирует образование ц. ГМФ вторичного посредника сигнальных систем клеток.
 Свойства сигналов • Плейотропия – один и тот же сигнал действует на разные клетки, имеющие разные функции • Избыточность – разные сигналы оказывают одинаковый эффект • Синергичность – сигналы усиливают действие друга • Антагонизм – сигналы уменьшают действие друга • Каскадная индукция – значительное увеличение эффективности сигнала –одни сигналы индуцируют образование других
Свойства сигналов • Плейотропия – один и тот же сигнал действует на разные клетки, имеющие разные функции • Избыточность – разные сигналы оказывают одинаковый эффект • Синергичность – сигналы усиливают действие друга • Антагонизм – сигналы уменьшают действие друга • Каскадная индукция – значительное увеличение эффективности сигнала –одни сигналы индуцируют образование других
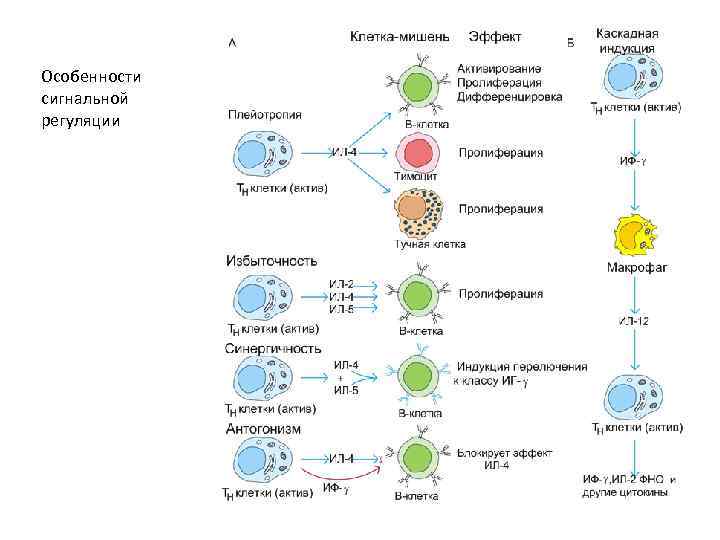 Особенности сигнальной регуляции
Особенности сигнальной регуляции
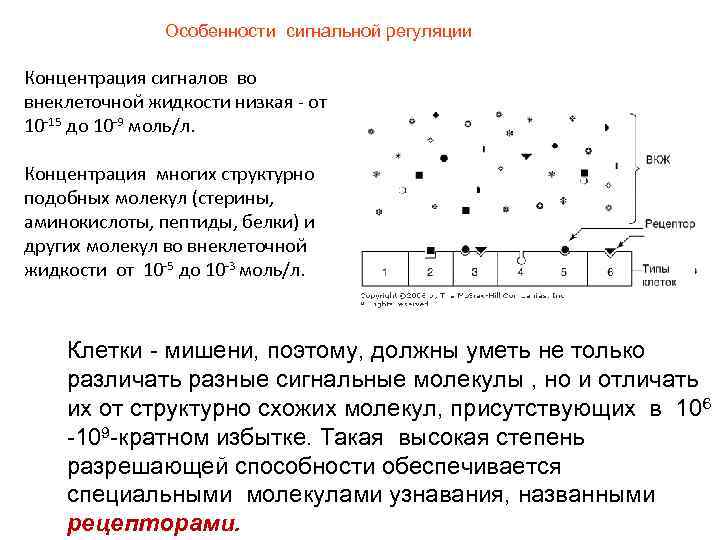 Особенности сигнальной регуляции Концентрация сигналов во внеклеточной жидкости низкая - от 10 -15 до 10 -9 моль/л. Концентрация многих структурно подобных молекул (стерины, аминокислоты, пептиды, белки) и других молекул во внеклеточной жидкости от 10 -5 до 10 -3 моль/л. Клетки - мишени, поэтому, должны уметь не только различать разные сигнальные молекулы , но и отличать их от структурно схожих молекул, присутствующих в 106 -109 -кратном избытке. Такая высокая степень разрешающей способности обеспечивается специальными молекулами узнавания, названными рецепторами.
Особенности сигнальной регуляции Концентрация сигналов во внеклеточной жидкости низкая - от 10 -15 до 10 -9 моль/л. Концентрация многих структурно подобных молекул (стерины, аминокислоты, пептиды, белки) и других молекул во внеклеточной жидкости от 10 -5 до 10 -3 моль/л. Клетки - мишени, поэтому, должны уметь не только различать разные сигнальные молекулы , но и отличать их от структурно схожих молекул, присутствующих в 106 -109 -кратном избытке. Такая высокая степень разрешающей способности обеспечивается специальными молекулами узнавания, названными рецепторами.
 Рецепторы можно разделить на две большие группы – рецепторы, встроенные в плазматическую мембрану (наиболее распространенная группа) и внутриклеточные рецепторы (цитозольные и ядерные) Рецепторы первой группы по способу организации их в мембране разделяют на : • 7 -ТМС -рецепторы • 1 -ТМС-рецепторы(наиболее разнообразная группа) • Рецепторы - ионные каналы
Рецепторы можно разделить на две большие группы – рецепторы, встроенные в плазматическую мембрану (наиболее распространенная группа) и внутриклеточные рецепторы (цитозольные и ядерные) Рецепторы первой группы по способу организации их в мембране разделяют на : • 7 -ТМС -рецепторы • 1 -ТМС-рецепторы(наиболее разнообразная группа) • Рецепторы - ионные каналы
 Молекулы – рецепторы ( R) • • 1. 7 -ТМС-рецепторы или R, ассоциированные с тримерными Gбелками 2. 1 -ТМС -рецепторы a) R, не обладающие каталитической активностью, но ассоциированные с цитозольными тирозинкиназами. b) R, обладающие каталитической активностью (тирозинкиназы, гуанилатциклазы, протеинфосфатазы, серин/треонин киназы, и др) c) R – молекулы клеточной адгезии d) R, ассоциированные с процессами протеолиза 3. R – лигандзависимые ионные каналы ( рецептор ацетилхолина, глутамата и др. ) 4. Цитозольные и ядерные R.
Молекулы – рецепторы ( R) • • 1. 7 -ТМС-рецепторы или R, ассоциированные с тримерными Gбелками 2. 1 -ТМС -рецепторы a) R, не обладающие каталитической активностью, но ассоциированные с цитозольными тирозинкиназами. b) R, обладающие каталитической активностью (тирозинкиназы, гуанилатциклазы, протеинфосфатазы, серин/треонин киназы, и др) c) R – молекулы клеточной адгезии d) R, ассоциированные с процессами протеолиза 3. R – лигандзависимые ионные каналы ( рецептор ацетилхолина, глутамата и др. ) 4. Цитозольные и ядерные R.
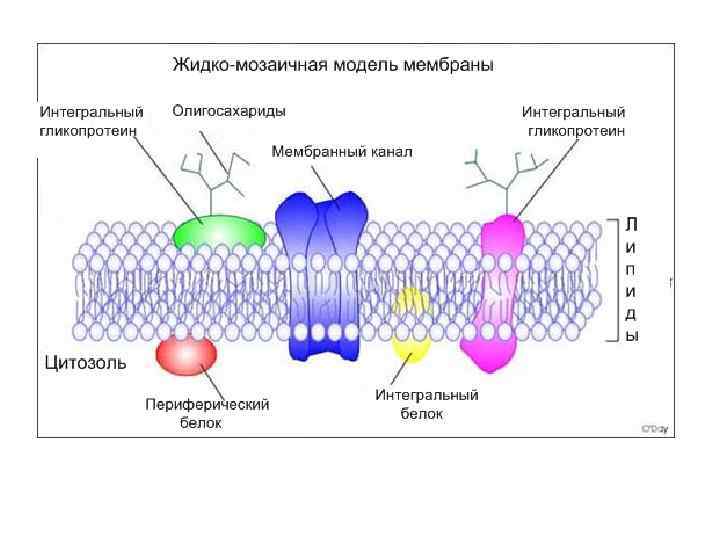
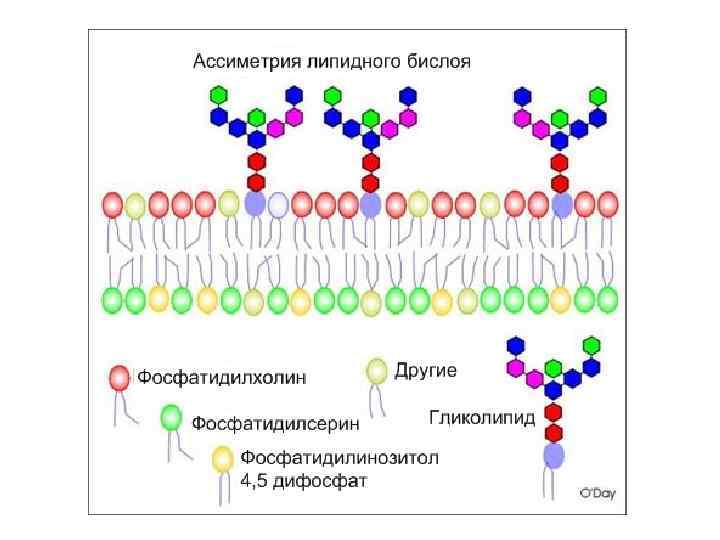
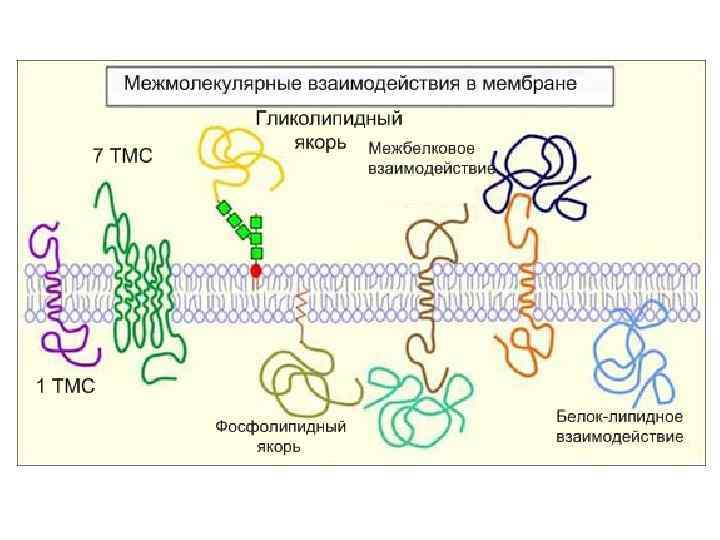
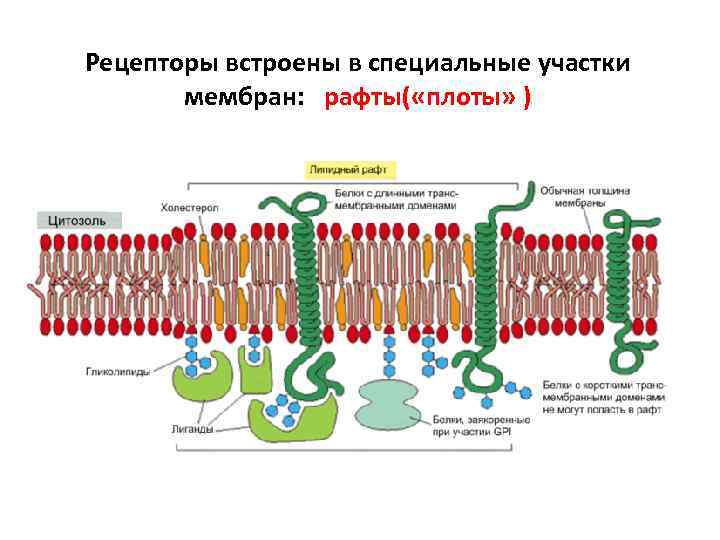 Рецепторы встроены в специальные участки мембран: рафты( «плоты» )
Рецепторы встроены в специальные участки мембран: рафты( «плоты» )
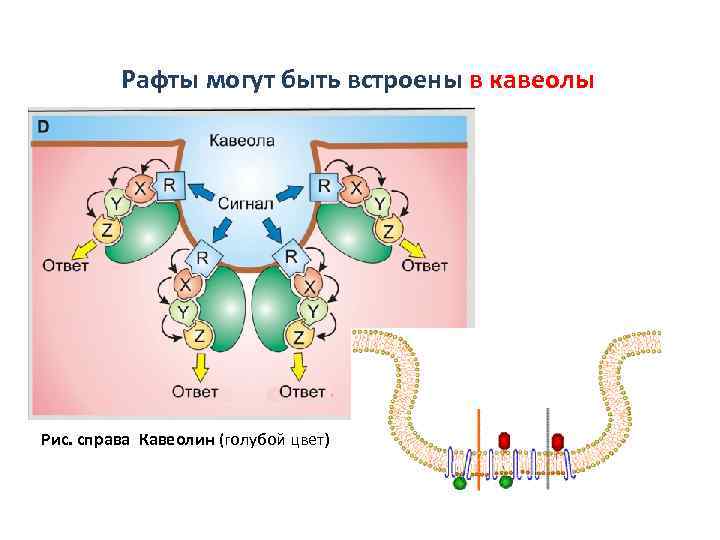 Рафты могут быть встроены в кавеолы Рис. справа Кавеолин (голубой цвет)
Рафты могут быть встроены в кавеолы Рис. справа Кавеолин (голубой цвет)
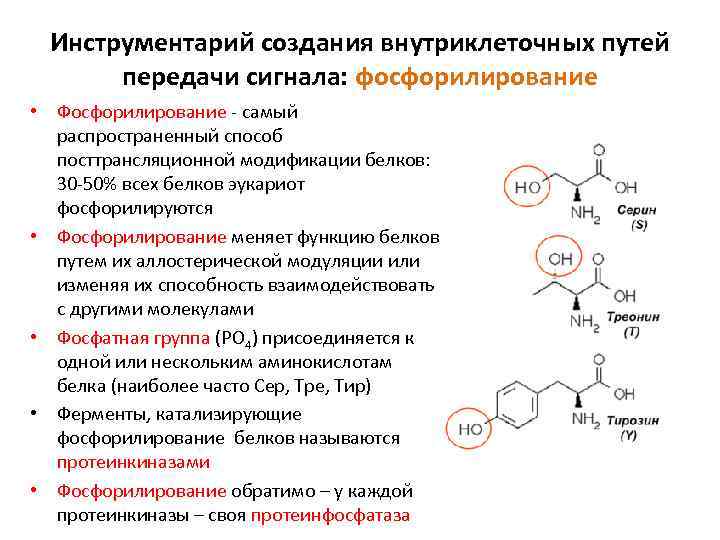 Инструментарий создания внутриклеточных путей передачи сигнала: фосфорилирование • Фосфорилирование - самый распространенный способ посттрансляционной модификации белков: 30 -50% всех белков эукариот фосфорилируются • Фосфорилирование меняет функцию белков путем их аллостерической модуляции или изменяя их способность взаимодействовать с другими молекулами • Фосфатная группа (PO 4) присоединяется к одной или нескольким аминокислотам белка (наиболее часто Сер, Тре, Тир) • Ферменты, катализирующие фосфорилирование белков называются протеинкиназами • Фосфорилирование обратимо – у каждой протеинкиназы – своя протеинфосфатаза
Инструментарий создания внутриклеточных путей передачи сигнала: фосфорилирование • Фосфорилирование - самый распространенный способ посттрансляционной модификации белков: 30 -50% всех белков эукариот фосфорилируются • Фосфорилирование меняет функцию белков путем их аллостерической модуляции или изменяя их способность взаимодействовать с другими молекулами • Фосфатная группа (PO 4) присоединяется к одной или нескольким аминокислотам белка (наиболее часто Сер, Тре, Тир) • Ферменты, катализирующие фосфорилирование белков называются протеинкиназами • Фосфорилирование обратимо – у каждой протеинкиназы – своя протеинфосфатаза
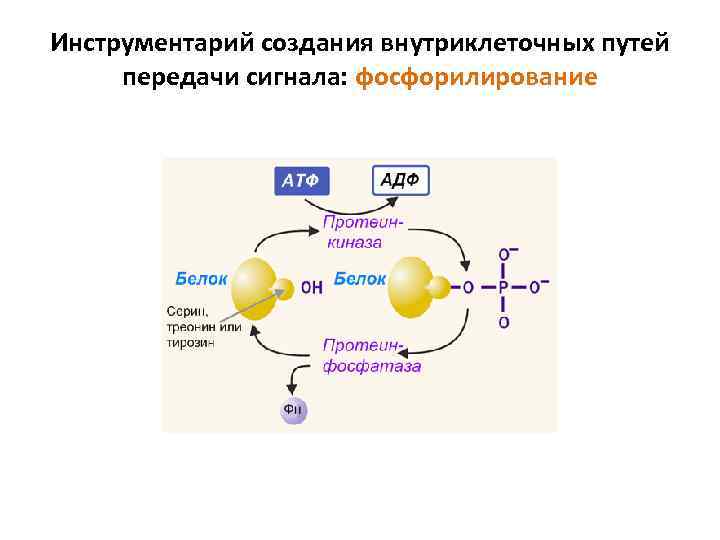 Инструментарий создания внутриклеточных путей передачи сигнала: фосфорилирование
Инструментарий создания внутриклеточных путей передачи сигнала: фосфорилирование
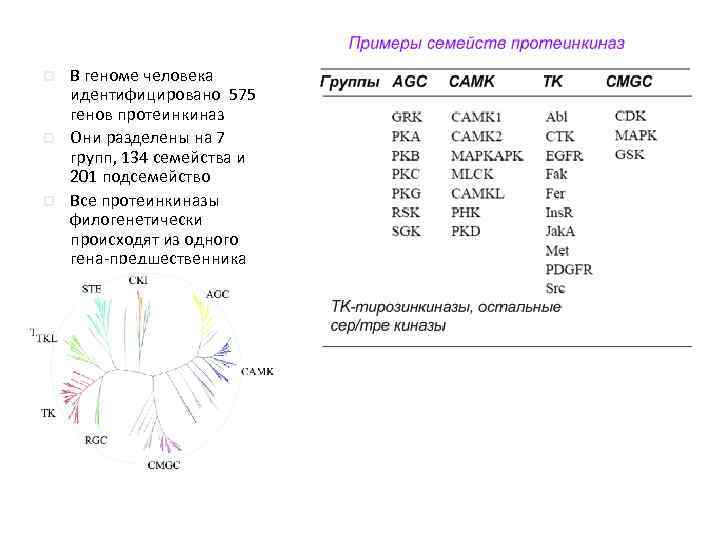 p p p В геноме человека идентифицировано 575 генов протеинкиназ Они разделены на 7 групп, 134 семейства и 201 подсемейство Все протеинкиназы филогенетически происходят из одного гена-предшественника
p p p В геноме человека идентифицировано 575 генов протеинкиназ Они разделены на 7 групп, 134 семейства и 201 подсемейство Все протеинкиназы филогенетически происходят из одного гена-предшественника
 Одна из задач внутриклеточного переноса сигнала – усиление сигнала У каждого рецептора - как минимум два домена: • Домен, обеспечивающий специфическое узнавание сигнала • Домен, обеспечивающий связь с системой усиления сигнала Механизмы усиления сигнала зависят от типа рецептора: • В системе усиления сигналов 7 -ТМС-рецепторами усиление достигается синтезом небольших молекул- вторичных посредников • В системе усиления сигналов 1 -ТМС-рецепторами усиление достигается при помощи специальных каскадов ферментов • В системе усиления сигналов рецепторами –ионными каналами усиление достигается увеличением концентрации ионов в цитозоле • Ядерные рецепторы после соединения с сигналами регулируют синтез белков –эффекторов
Одна из задач внутриклеточного переноса сигнала – усиление сигнала У каждого рецептора - как минимум два домена: • Домен, обеспечивающий специфическое узнавание сигнала • Домен, обеспечивающий связь с системой усиления сигнала Механизмы усиления сигнала зависят от типа рецептора: • В системе усиления сигналов 7 -ТМС-рецепторами усиление достигается синтезом небольших молекул- вторичных посредников • В системе усиления сигналов 1 -ТМС-рецепторами усиление достигается при помощи специальных каскадов ферментов • В системе усиления сигналов рецепторами –ионными каналами усиление достигается увеличением концентрации ионов в цитозоле • Ядерные рецепторы после соединения с сигналами регулируют синтез белков –эффекторов
 1. 7 -ТМС-рецепторы или рецепторы, ассоциированные с тримерными G-белками • Среди мембранных рецепторов это наиболее распространенная группа рецепторов. • У позвоночных это семейство состоит из 1000 – 2000 членов (>1% генома). • Это самая преуспевшая в течении эволюции группа рецепторов, способная участвовать в восприятии таких различных сигналов как фотоны, органические одоранты, нуклеотиды, пептиды, липиды и белки. • Они построены из общей центральной структуры, образованной 7 трансмембранными спиральными доменами.
1. 7 -ТМС-рецепторы или рецепторы, ассоциированные с тримерными G-белками • Среди мембранных рецепторов это наиболее распространенная группа рецепторов. • У позвоночных это семейство состоит из 1000 – 2000 членов (>1% генома). • Это самая преуспевшая в течении эволюции группа рецепторов, способная участвовать в восприятии таких различных сигналов как фотоны, органические одоранты, нуклеотиды, пептиды, липиды и белки. • Они построены из общей центральной структуры, образованной 7 трансмембранными спиральными доменами.
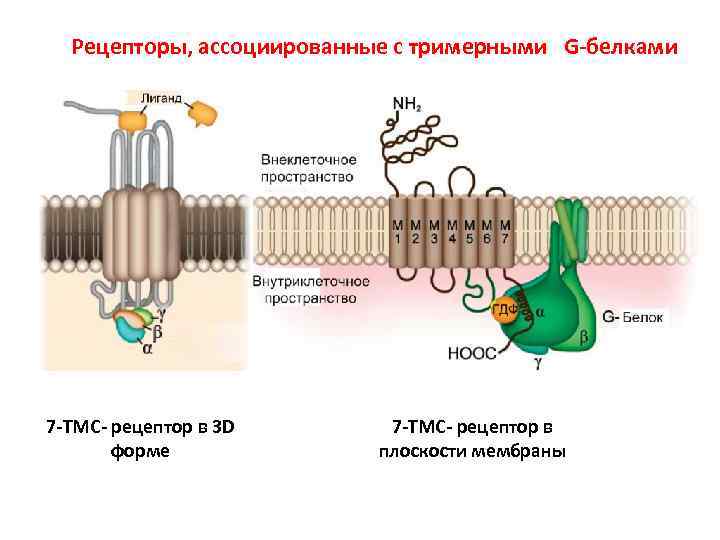 Рецепторы, ассоциированные с тримерными G-белками 7 -ТМС- рецептор в 3 D форме 7 -ТМС- рецептор в плоскости мембраны
Рецепторы, ассоциированные с тримерными G-белками 7 -ТМС- рецептор в 3 D форме 7 -ТМС- рецептор в плоскости мембраны
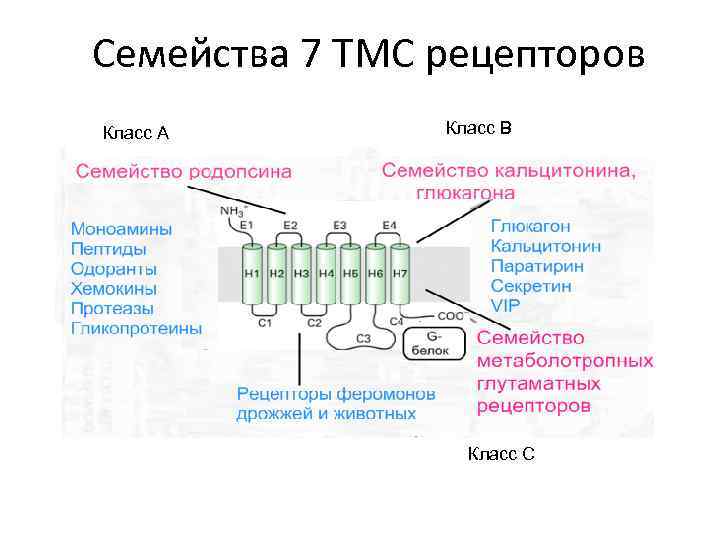 Семейства 7 ТМС рецепторов Класс А Класс B Класс C
Семейства 7 ТМС рецепторов Класс А Класс B Класс C
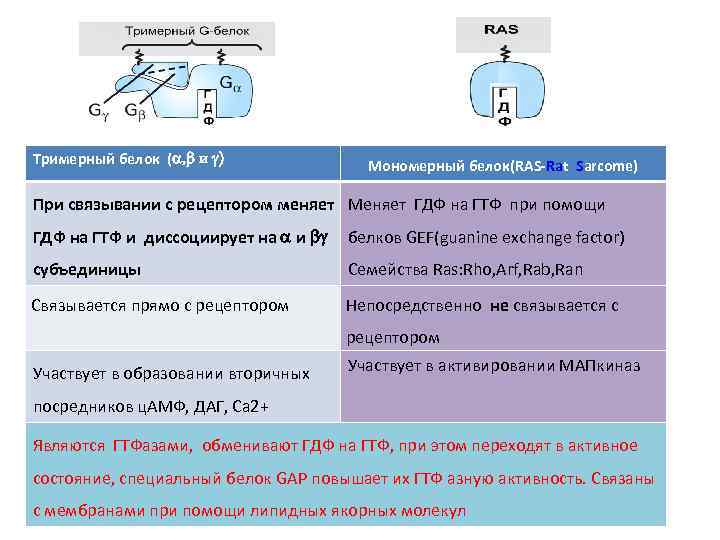 Тримерный белок (a, b и g) Мономерный белок(RAS-Rat Sarcome) При связывании с рецептором меняет Меняет ГДФ на ГТФ при помощи ГДФ на ГТФ и диссоциирует на a и bg белков GEF(guanine exchange factor) субъединицы Семейства Ras: Rho, Arf, Rab, Ran Связывается прямо с рецептором Непосредственно не связывается с рецептором Участвует в образовании вторичных Участвует в активировании МАПкиназ посредников ц. АМФ, ДАГ, Са 2+ Являются ГТФазами, обменивают ГДФ на ГТФ, при этом переходят в активное состояние, специальный белок GAP повышает их ГТФ азную активность. Связаны с мембранами при помощи липидных якорных молекул
Тримерный белок (a, b и g) Мономерный белок(RAS-Rat Sarcome) При связывании с рецептором меняет Меняет ГДФ на ГТФ при помощи ГДФ на ГТФ и диссоциирует на a и bg белков GEF(guanine exchange factor) субъединицы Семейства Ras: Rho, Arf, Rab, Ran Связывается прямо с рецептором Непосредственно не связывается с рецептором Участвует в образовании вторичных Участвует в активировании МАПкиназ посредников ц. АМФ, ДАГ, Са 2+ Являются ГТФазами, обменивают ГДФ на ГТФ, при этом переходят в активное состояние, специальный белок GAP повышает их ГТФ азную активность. Связаны с мембранами при помощи липидных якорных молекул
 Нобелевская премия по физиологии и медицине 1994 г Alfred G. Gilman Martin Rodbell за открытие "G-белков и их роли а переносе сигналов в клетке". Тримерные G-белки могут активировать (G(s)) или ингибировать (G(i)) белки эффекторы в системе переноса сигнала
Нобелевская премия по физиологии и медицине 1994 г Alfred G. Gilman Martin Rodbell за открытие "G-белков и их роли а переносе сигналов в клетке". Тримерные G-белки могут активировать (G(s)) или ингибировать (G(i)) белки эффекторы в системе переноса сигнала
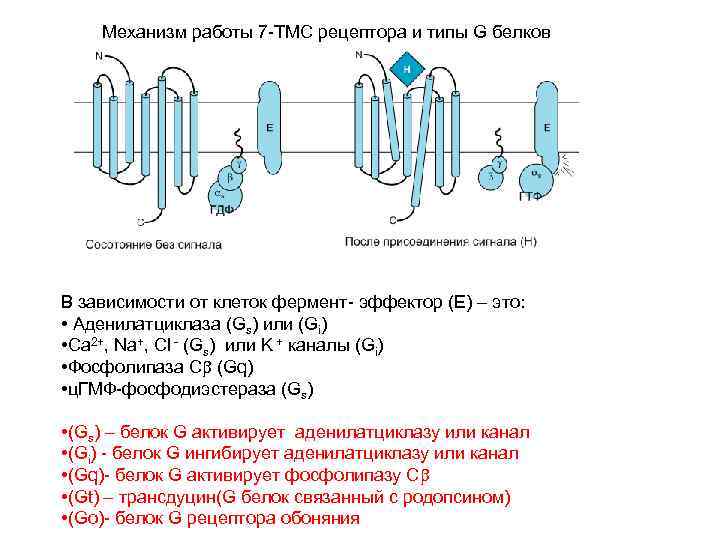 Механизм работы 7 -ТМС рецептора и типы G белков В зависимости от клеток фермент- эффектор (Е) – это: • Аденилатциклаза (Gs) или (Gi) • Ca 2+, Na+, Cl - (Gs) или K + каналы (Gi) • Фосфолипаза Сb (Gq) • ц. ГМФ-фосфодиэстераза (Gs) • (Gs) – белок G активирует аденилатциклазу или канал • (Gi) - белок G ингибирует аденилатциклазу или канал • (Gq)- белок G активирует фосфолипазу Сb • (Gt) – трансдуцин(G белок связанный с родопсином) • (Go)- белок G рецептора обоняния
Механизм работы 7 -ТМС рецептора и типы G белков В зависимости от клеток фермент- эффектор (Е) – это: • Аденилатциклаза (Gs) или (Gi) • Ca 2+, Na+, Cl - (Gs) или K + каналы (Gi) • Фосфолипаза Сb (Gq) • ц. ГМФ-фосфодиэстераза (Gs) • (Gs) – белок G активирует аденилатциклазу или канал • (Gi) - белок G ингибирует аденилатциклазу или канал • (Gq)- белок G активирует фосфолипазу Сb • (Gt) – трансдуцин(G белок связанный с родопсином) • (Go)- белок G рецептора обоняния
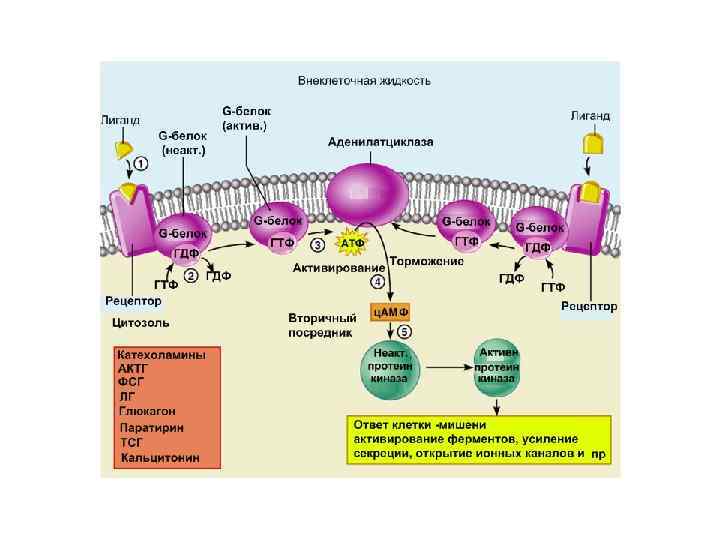
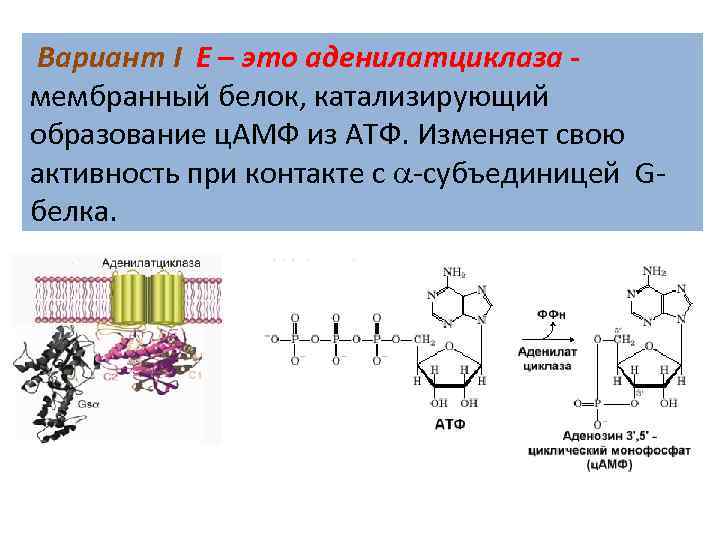 Вариант I Е – это аденилатциклаза мембранный белок, катализирующий образование ц. АМФ из АТФ. Изменяет свою активность при контакте с -субъединицей G- белка.
Вариант I Е – это аденилатциклаза мембранный белок, катализирующий образование ц. АМФ из АТФ. Изменяет свою активность при контакте с -субъединицей G- белка.
 Earl Wilbur Sutherland, Jr. (1915– 1974) В 1958 году Sutherland сделал открытие, за которое ему была присуждена в 1971 году Нобелевская премия по физиологии и медицине «за открытие, связанное с выяснением механизма действия гормонов. " В это время Sutherland изолировал ранее не известное соединение, названное циклический аденозинмонофосфат (ц. AMФ) и показал, что это соединение имеет непосредственное отношение к функциям многих гормонов.
Earl Wilbur Sutherland, Jr. (1915– 1974) В 1958 году Sutherland сделал открытие, за которое ему была присуждена в 1971 году Нобелевская премия по физиологии и медицине «за открытие, связанное с выяснением механизма действия гормонов. " В это время Sutherland изолировал ранее не известное соединение, названное циклический аденозинмонофосфат (ц. AMФ) и показал, что это соединение имеет непосредственное отношение к функциям многих гормонов.
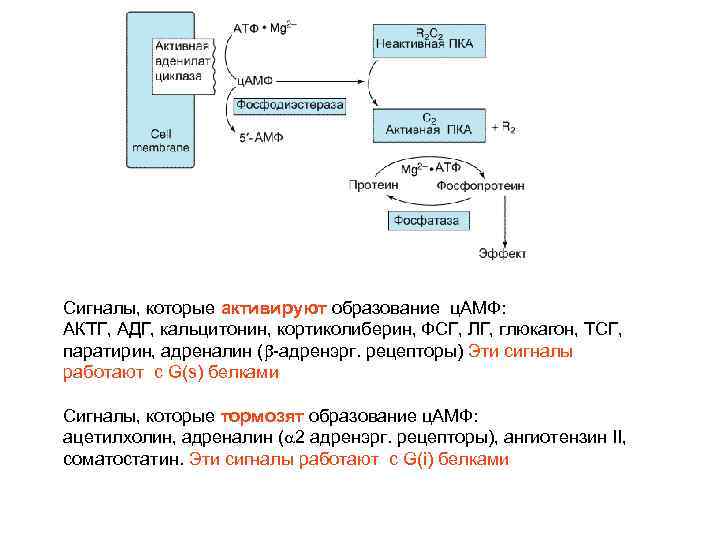 Сигналы, которые активируют образование ц. АМФ: АКТГ, АДГ, кальцитонин, кортиколиберин, ФСГ, ЛГ, глюкагон, ТСГ, паратирин, адреналин (b-адренэрг. рецепторы) Эти сигналы работают с G(s) белками Сигналы, которые тормозят образование ц. АМФ: ацетилхолин, адреналин ( 2 адренэрг. рецепторы), ангиотензин II, соматостатин. Эти сигналы работают с G(i) белками
Сигналы, которые активируют образование ц. АМФ: АКТГ, АДГ, кальцитонин, кортиколиберин, ФСГ, ЛГ, глюкагон, ТСГ, паратирин, адреналин (b-адренэрг. рецепторы) Эти сигналы работают с G(s) белками Сигналы, которые тормозят образование ц. АМФ: ацетилхолин, адреналин ( 2 адренэрг. рецепторы), ангиотензин II, соматостатин. Эти сигналы работают с G(i) белками
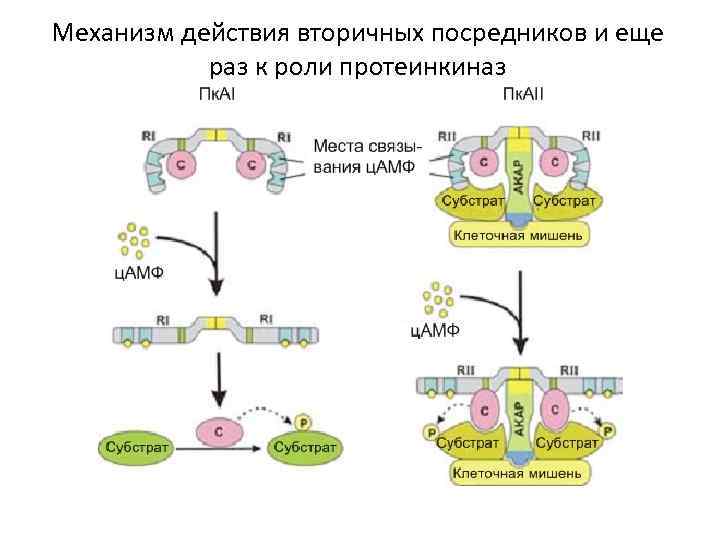 Механизм действия вторичных посредников и еще раз к роли протеинкиназ
Механизм действия вторичных посредников и еще раз к роли протеинкиназ
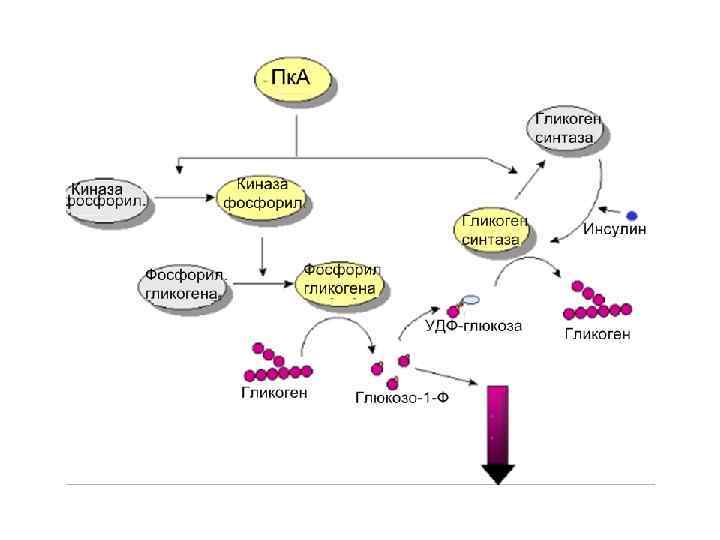
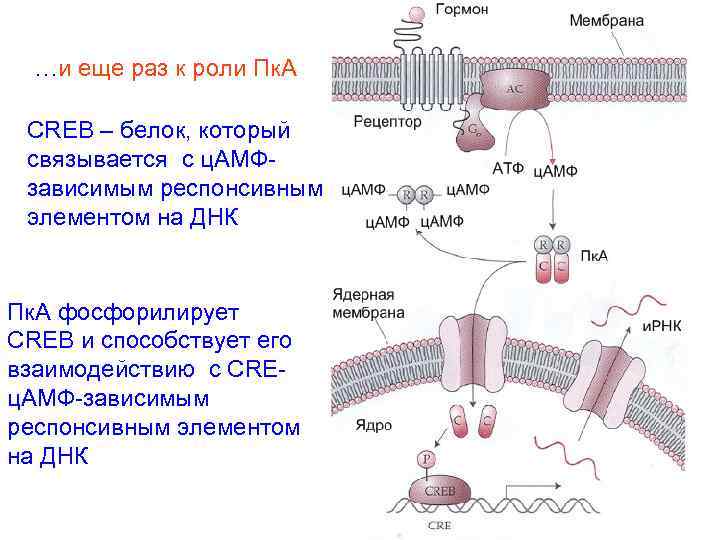 …и еще раз к роли Пк. А CREB – белок, который связывается с ц. АМФзависимым респонсивным элементом на ДНК Пк. А фосфорилирует CREB и способствует его взаимодействию с CREц. АМФ-зависимым респонсивным элементом на ДНК
…и еще раз к роли Пк. А CREB – белок, который связывается с ц. АМФзависимым респонсивным элементом на ДНК Пк. А фосфорилирует CREB и способствует его взаимодействию с CREц. АМФ-зависимым респонсивным элементом на ДНК
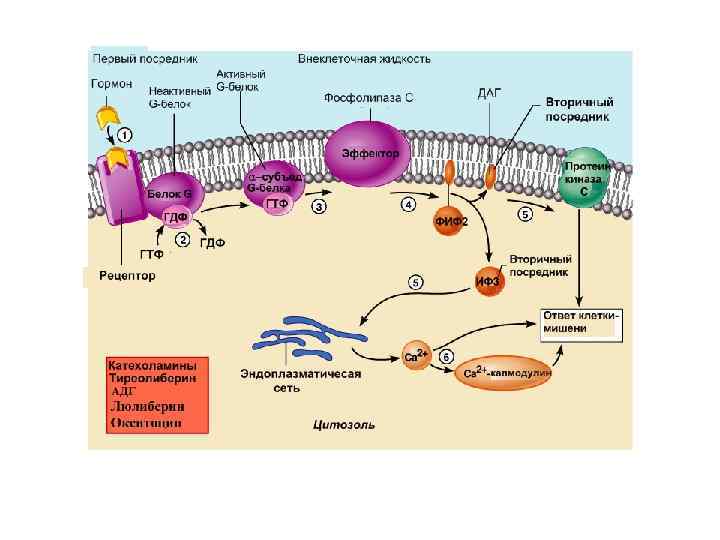
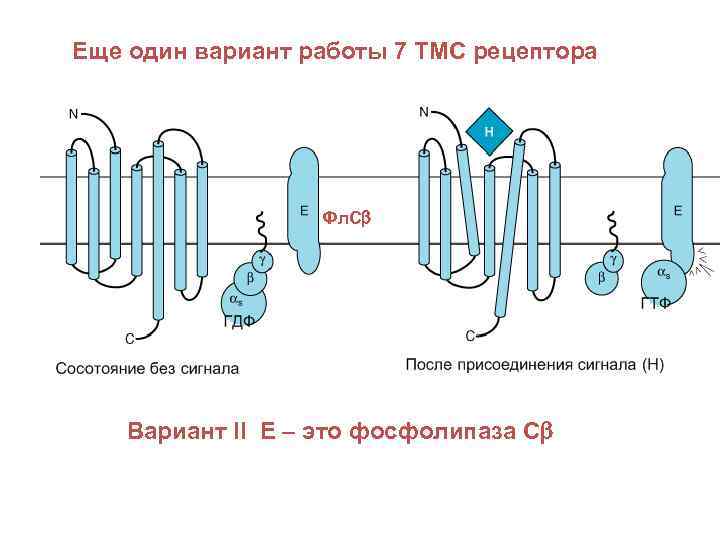 Еще один вариант работы 7 ТМС рецептора Фл. Сb Вариант II Е – это фосфолипаза Сb
Еще один вариант работы 7 ТМС рецептора Фл. Сb Вариант II Е – это фосфолипаза Сb
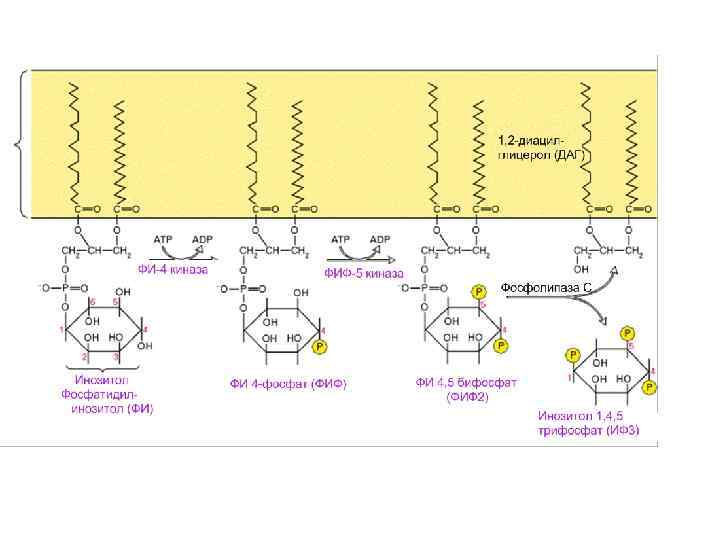
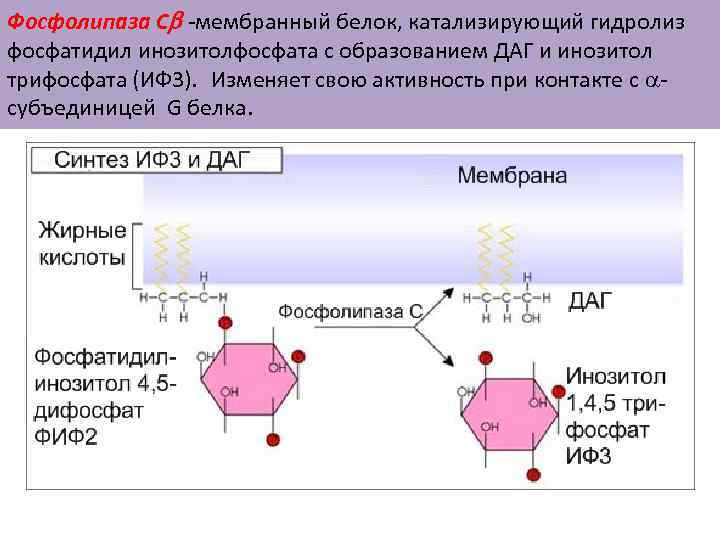 Фосфолипаза Сb -мембранный белок, катализирующий гидролиз фосфатидил инозитолфосфата с образованием ДАГ и инозитол трифосфата (ИФ 3). Изменяет свою активность при контакте с субъединицей G белка.
Фосфолипаза Сb -мембранный белок, катализирующий гидролиз фосфатидил инозитолфосфата с образованием ДАГ и инозитол трифосфата (ИФ 3). Изменяет свою активность при контакте с субъединицей G белка.
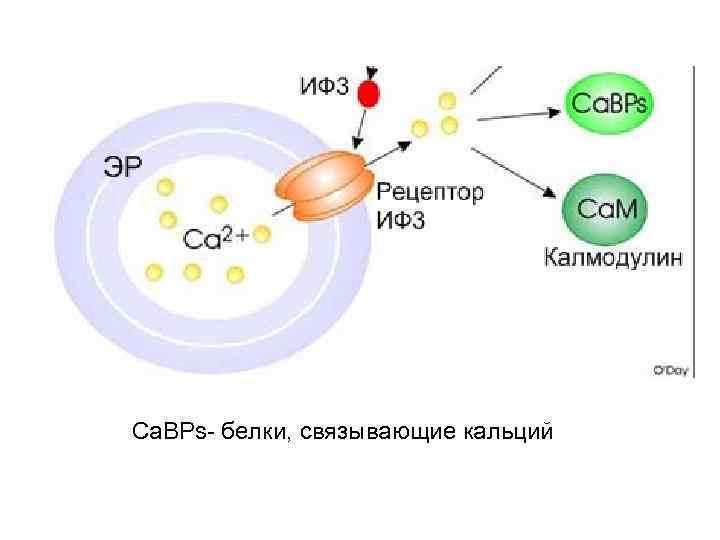 Ca. BPs- белки, связывающие кальций
Ca. BPs- белки, связывающие кальций
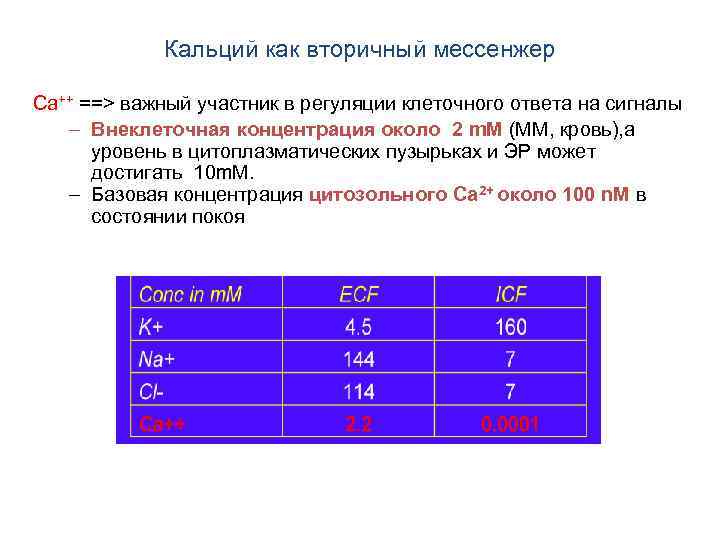 Кальций как вторичный мессенжер Ca++ ==> важный участник в регуляции клеточного ответа на сигналы – Внеклеточная концентрация около 2 m. M (МM, кровь), а уровень в цитоплазматических пузырьках и ЭР может достигать 10 m. M. – Базовая концентрация цитозольного Ca 2+ около 100 n. M в состоянии покоя
Кальций как вторичный мессенжер Ca++ ==> важный участник в регуляции клеточного ответа на сигналы – Внеклеточная концентрация около 2 m. M (МM, кровь), а уровень в цитоплазматических пузырьках и ЭР может достигать 10 m. M. – Базовая концентрация цитозольного Ca 2+ около 100 n. M в состоянии покоя
 Кальций как вторичный мессенжер Высокий градиент делает кальций очень быстрой и чувствительной сигнальной системой: незначительные изменения проницаемости мембран вызывают резкие изменения концентрации [Ca 2+]in. Низкий уровень [Ca 2+]in необходим для облегчения метаболизма ориентированного на фосфат (высокие концентрации кальция и фосфата несовместимы!!) Два класса Ca-связывающих белков: Связанные с мембраной (неограниченная емкость -->транспортные системы: Ca-каналы, кальциевые насосы) Не связанные с мембраной (ограниченная емкость --> не только связывают, но участвуют в переносе сигналов путем конформационных изменений, которые обеспечивают взаимодействие с белками мишенями: калмодулин, тропонин C. . . )
Кальций как вторичный мессенжер Высокий градиент делает кальций очень быстрой и чувствительной сигнальной системой: незначительные изменения проницаемости мембран вызывают резкие изменения концентрации [Ca 2+]in. Низкий уровень [Ca 2+]in необходим для облегчения метаболизма ориентированного на фосфат (высокие концентрации кальция и фосфата несовместимы!!) Два класса Ca-связывающих белков: Связанные с мембраной (неограниченная емкость -->транспортные системы: Ca-каналы, кальциевые насосы) Не связанные с мембраной (ограниченная емкость --> не только связывают, но участвуют в переносе сигналов путем конформационных изменений, которые обеспечивают взаимодействие с белками мишенями: калмодулин, тропонин C. . . )
![Кальций как вторичный мессенжер Источники Ca++: Внеклеточный компартмент [Ca 2+]out : (преимущественно для нервных, Кальций как вторичный мессенжер Источники Ca++: Внеклеточный компартмент [Ca 2+]out : (преимущественно для нервных,](https://present5.com/presentation/95890909_142130200/image-67.jpg) Кальций как вторичный мессенжер Источники Ca++: Внеклеточный компартмент [Ca 2+]out : (преимущественно для нервных, мышечных клеток и клеток сердечной мышцы) В мембране расположены три типа кальциевых каналов: 1. Потенциалзависимые кальциевые каналы: Потенциал действия деполяризует плазматическую мембрану, что ведет к открытию потенциалзависимых кальциевых каналов (каналы могут открываться увеличением внеклеточного K+). Каждый канал состоит из четырех гомологичных доменов, каждый содержит шесть трансмембранных -спиралей (одна из них выполняет функцию сенсора изменений потенциала).
Кальций как вторичный мессенжер Источники Ca++: Внеклеточный компартмент [Ca 2+]out : (преимущественно для нервных, мышечных клеток и клеток сердечной мышцы) В мембране расположены три типа кальциевых каналов: 1. Потенциалзависимые кальциевые каналы: Потенциал действия деполяризует плазматическую мембрану, что ведет к открытию потенциалзависимых кальциевых каналов (каналы могут открываться увеличением внеклеточного K+). Каждый канал состоит из четырех гомологичных доменов, каждый содержит шесть трансмембранных -спиралей (одна из них выполняет функцию сенсора изменений потенциала).
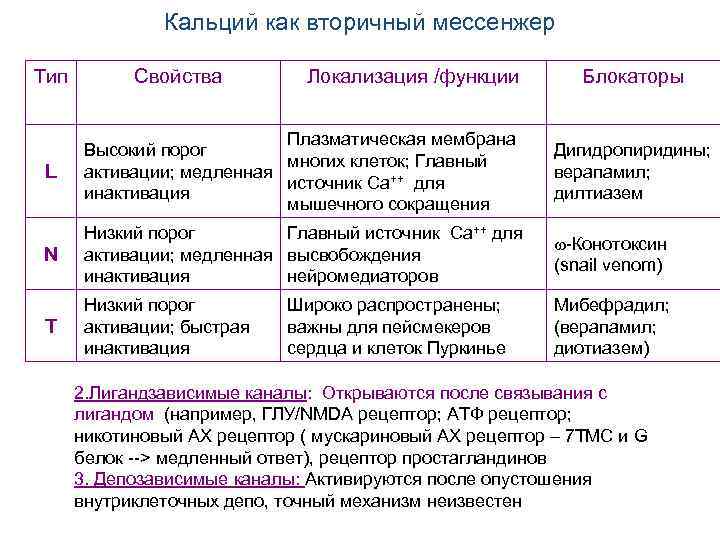 Кальций как вторичный мессенжер Тип Свойства Локализация /функции Блокаторы L Плазматическая мембрана Высокий порог многих клеток; Главный активации; медленная источник Ca++ для инактивация мышечного сокращения Дигидропиридины; верапамил; дилтиазем N Низкий порог Главный источник Ca++ для активации; медленная высвобождения инактивация нейромедиаторов w-Конотоксин (snail venom) T Низкий порог активации; быстрая инактивация Mибефрадил; (верапамил; диотиазем) Широко распространены; важны для пейсмекеров сердца и клеток Пуркинье 2. Лигандзависимые каналы: Открываются после связывания с лигандом (например, ГЛУ/NMDA рецептор; АТФ рецептор; никотиновый АХ рецептор ( мускариновый АХ рецептор – 7 ТМС и G белок --> медленный ответ), рецептор простагландинов 3. Депозависимые каналы: Активируются после опустошения внутриклеточных депо, точный механизм неизвестен
Кальций как вторичный мессенжер Тип Свойства Локализация /функции Блокаторы L Плазматическая мембрана Высокий порог многих клеток; Главный активации; медленная источник Ca++ для инактивация мышечного сокращения Дигидропиридины; верапамил; дилтиазем N Низкий порог Главный источник Ca++ для активации; медленная высвобождения инактивация нейромедиаторов w-Конотоксин (snail venom) T Низкий порог активации; быстрая инактивация Mибефрадил; (верапамил; диотиазем) Широко распространены; важны для пейсмекеров сердца и клеток Пуркинье 2. Лигандзависимые каналы: Открываются после связывания с лигандом (например, ГЛУ/NMDA рецептор; АТФ рецептор; никотиновый АХ рецептор ( мускариновый АХ рецептор – 7 ТМС и G белок --> медленный ответ), рецептор простагландинов 3. Депозависимые каналы: Активируются после опустошения внутриклеточных депо, точный механизм неизвестен
 Внутриклеточный компартмент: (преимущественно в мышечных клетках) Ca 2+ хранится в m. M концентрациях в эндо/саркоплазматической сети в связанной с кальсеквестрином форме. (Ранее ведущую роль в хранении Ca 2+ отводили митохондриям, но скорость обмена в них Са в 10 раз ниже чем в ЭР/СР ) Высвобождение Са++ из ЭР/СР регулируется двумя рецепторами в мембранах ЭР/СР: Рианодиновый рецептор (Ry. R): Назван по чувствительности к Рианодину: алкалоиду растений, необратимый ингибитор Важен в скелетной мышце: напрямую связан с дигидропиридиновым рецептором Т-трубочек (дигидропиридиновый рецептор относится к L-типу Ca 2+ каналов) Aктивность Ry. R в немышечных клетках без. T-трубочек регулируется ц AДФ рибозой Коффеин: обратимый активатор RYR ИФ 3 - рецептор (ИФ 3 R): Инозитол-1, 4, 5 -трифосфат образуется рецепторактивируемой фосфолипазой C --> дифундирует через цитозоль и связывает ИФ 3 R
Внутриклеточный компартмент: (преимущественно в мышечных клетках) Ca 2+ хранится в m. M концентрациях в эндо/саркоплазматической сети в связанной с кальсеквестрином форме. (Ранее ведущую роль в хранении Ca 2+ отводили митохондриям, но скорость обмена в них Са в 10 раз ниже чем в ЭР/СР ) Высвобождение Са++ из ЭР/СР регулируется двумя рецепторами в мембранах ЭР/СР: Рианодиновый рецептор (Ry. R): Назван по чувствительности к Рианодину: алкалоиду растений, необратимый ингибитор Важен в скелетной мышце: напрямую связан с дигидропиридиновым рецептором Т-трубочек (дигидропиридиновый рецептор относится к L-типу Ca 2+ каналов) Aктивность Ry. R в немышечных клетках без. T-трубочек регулируется ц AДФ рибозой Коффеин: обратимый активатор RYR ИФ 3 - рецептор (ИФ 3 R): Инозитол-1, 4, 5 -трифосфат образуется рецепторактивируемой фосфолипазой C --> дифундирует через цитозоль и связывает ИФ 3 R
 Удаление Ca++ из цитозоля : Ca++ - насосы: Активность этих насосов индуцируется увеличением Са++ в цитозоле. Na+/Ca 2+ обмен (в возбуждаемых клетках, напр. клетки сердца) три иона Na+ обмениваются на один ион Ca++ Алкалоиды наперстянки: ингибиторы Na+/ K+-ATФазы => внутри клеточный Na+ растет => Na+/Ca 2+ обмен менее эфективен=>Ca 2+ внутри клеток растет => усиление сокращений Ca 2+-ATФаза плазматической мембраны(ПMCA) два иона Ca++ переносятся при гидролизе одной молекулы ATФ; регулируется Ca. M, ПKA или ПKC СР/ЭР Ca++-ATФаза (СЭРCA): 80% (!) интегрального белка мембран СР – мишень thapsigargin ( => высвобождение Ca++ из внутриклеточных депо) Ca++ - буферы: Низкое сродство (!) но высокая емкость (50 -100 ионов Ca++-/ молекулу) Калсеквестрин (очень кислый, 37% аминокислот это асп и глу), калретикулин, парвальбумин
Удаление Ca++ из цитозоля : Ca++ - насосы: Активность этих насосов индуцируется увеличением Са++ в цитозоле. Na+/Ca 2+ обмен (в возбуждаемых клетках, напр. клетки сердца) три иона Na+ обмениваются на один ион Ca++ Алкалоиды наперстянки: ингибиторы Na+/ K+-ATФазы => внутри клеточный Na+ растет => Na+/Ca 2+ обмен менее эфективен=>Ca 2+ внутри клеток растет => усиление сокращений Ca 2+-ATФаза плазматической мембраны(ПMCA) два иона Ca++ переносятся при гидролизе одной молекулы ATФ; регулируется Ca. M, ПKA или ПKC СР/ЭР Ca++-ATФаза (СЭРCA): 80% (!) интегрального белка мембран СР – мишень thapsigargin ( => высвобождение Ca++ из внутриклеточных депо) Ca++ - буферы: Низкое сродство (!) но высокая емкость (50 -100 ионов Ca++-/ молекулу) Калсеквестрин (очень кислый, 37% аминокислот это асп и глу), калретикулин, парвальбумин
 Ca++ сенсоры: Аннексины: Семейство белков с общим свойством взаимодействовать с мембранами при соединении с Ca++. Низкое сродство к ионам Ca++ ограничивает их действие только при непосредственном приближении к мембране (высокая локальная концентрация Ca++. !); участвуют в регуляции Фл. A 2, реорганизации цитоскелета и перемещении везикул EF-hand - белки: Названы по форме, образуемой E и F -спиралями Ca++-связывающего домена; высокое сродство к кальцию
Ca++ сенсоры: Аннексины: Семейство белков с общим свойством взаимодействовать с мембранами при соединении с Ca++. Низкое сродство к ионам Ca++ ограничивает их действие только при непосредственном приближении к мембране (высокая локальная концентрация Ca++. !); участвуют в регуляции Фл. A 2, реорганизации цитоскелета и перемещении везикул EF-hand - белки: Названы по форме, образуемой E и F -спиралями Ca++-связывающего домена; высокое сродство к кальцию
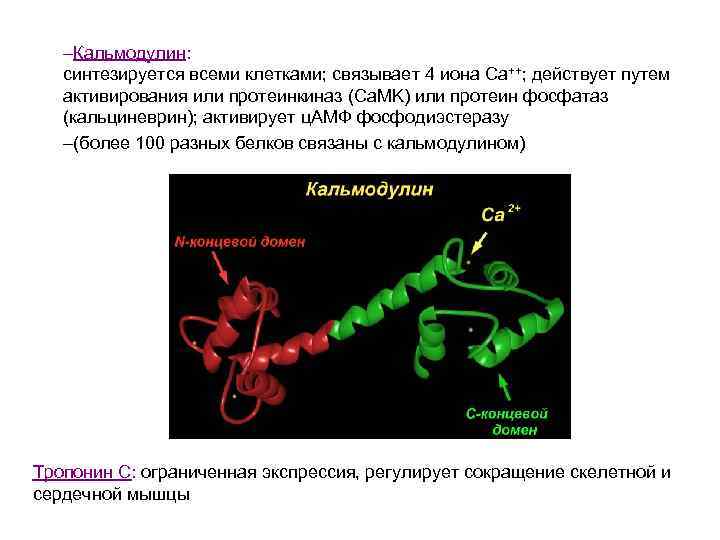 –Кальмодулин: синтезируется всеми клетками; связывает 4 иона Ca++; действует путем активирования или протеинкиназ (Ca. MK) или протеин фосфатаз (кальциневрин); активирует ц. AMФ фосфодиэстеразу –(более 100 разных белков связаны с кальмодулином) Тропонин C: ограниченная экспрессия, регулирует сокращение скелетной и сердечной мышцы
–Кальмодулин: синтезируется всеми клетками; связывает 4 иона Ca++; действует путем активирования или протеинкиназ (Ca. MK) или протеин фосфатаз (кальциневрин); активирует ц. AMФ фосфодиэстеразу –(более 100 разных белков связаны с кальмодулином) Тропонин C: ограниченная экспрессия, регулирует сокращение скелетной и сердечной мышцы
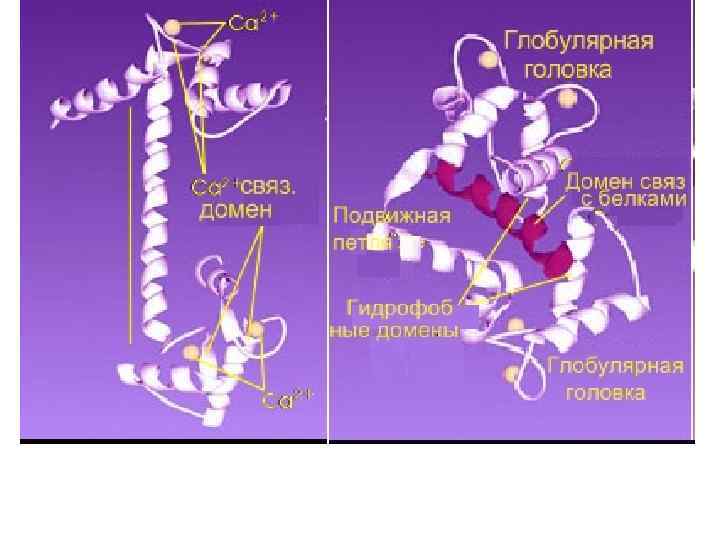
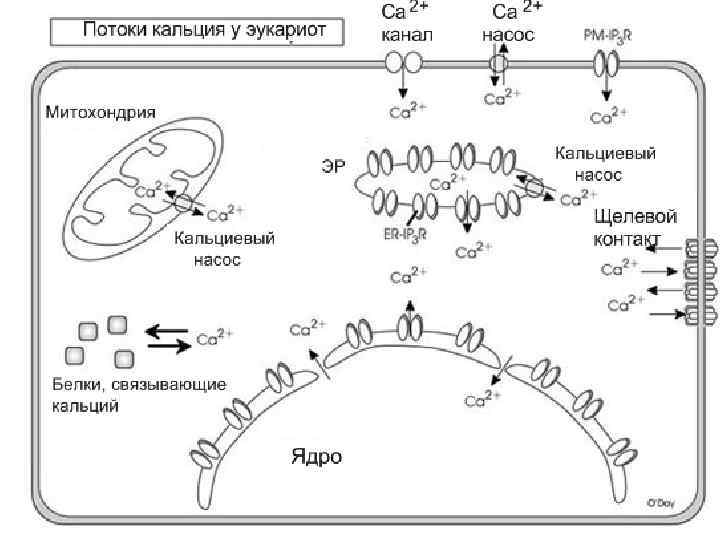
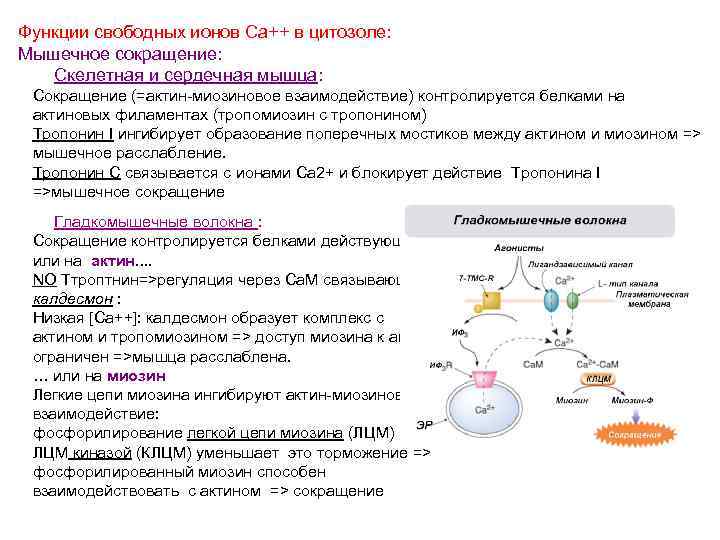 Функции свободных ионов Ca++ в цитозоле: Мышечное сокращение: Скелетная и сердечная мышца: Сокращение (=актин-миозиновое взаимодействие) контролируется белками на актиновых филаментах (тропомиозин с тропонином) Tропонин I ингибирует образование поперечных мостиков между актином и миозином => мышечное расслабление. Tропонин C связывается с ионами Ca 2+ и блокирует действие Tропонина I =>мышечное сокращение Гладкомышечные волокна : Сокращение контролируется белками действующими или на актин. . NO Tтроптнин=>регуляция через Ca. M связывающий калдесмон : Низкая [Ca++]: калдесмон образует комплекс с актином и тропомиозином => доступ миозина к актину ограничен =>мышца расслаблена. … или на миозин Легкие цепи миозина ингибируют актин-миозиновое взаимодействие: фосфорилирование легкой цепи миозина (ЛЦМ) ЛЦМ киназой (КЛЦМ) уменьшает это торможение => фосфорилированный миозин способен взаимодействовать с актином => сокращение
Функции свободных ионов Ca++ в цитозоле: Мышечное сокращение: Скелетная и сердечная мышца: Сокращение (=актин-миозиновое взаимодействие) контролируется белками на актиновых филаментах (тропомиозин с тропонином) Tропонин I ингибирует образование поперечных мостиков между актином и миозином => мышечное расслабление. Tропонин C связывается с ионами Ca 2+ и блокирует действие Tропонина I =>мышечное сокращение Гладкомышечные волокна : Сокращение контролируется белками действующими или на актин. . NO Tтроптнин=>регуляция через Ca. M связывающий калдесмон : Низкая [Ca++]: калдесмон образует комплекс с актином и тропомиозином => доступ миозина к актину ограничен =>мышца расслаблена. … или на миозин Легкие цепи миозина ингибируют актин-миозиновое взаимодействие: фосфорилирование легкой цепи миозина (ЛЦМ) ЛЦМ киназой (КЛЦМ) уменьшает это торможение => фосфорилированный миозин способен взаимодействовать с актином => сокращение
![Нейрональная секреция: Увеличение [Ca ++] индуцирует слияние синаптических пузырьков с плазматической мембраной => это Нейрональная секреция: Увеличение [Ca ++] индуцирует слияние синаптических пузырьков с плазматической мембраной => это](https://present5.com/presentation/95890909_142130200/image-76.jpg) Нейрональная секреция: Увеличение [Ca ++] индуцирует слияние синаптических пузырьков с плазматической мембраной => это вызывает экзоцитоз нейромедиаторов в синаптическую щель. Ферменты, активируемые калмодулином Аденилатциклаза Ca 2+-зависимая протеинкиназа Ca 2+-Mg 2+ AТФаза Ca 2+-фосфолипидзависимая протеинкиназа Фосфодиэстераза циклических нуклеотидов Некоторые белки цитоскелета Ионные каналы( L-тип Са 2+ канал) NO синтаза Киназа фосфорилазы Фосфопротеинфосфатаза 2 В Некоторые рецепторы ( NMDA-тип глутаматного рецептора)
Нейрональная секреция: Увеличение [Ca ++] индуцирует слияние синаптических пузырьков с плазматической мембраной => это вызывает экзоцитоз нейромедиаторов в синаптическую щель. Ферменты, активируемые калмодулином Аденилатциклаза Ca 2+-зависимая протеинкиназа Ca 2+-Mg 2+ AТФаза Ca 2+-фосфолипидзависимая протеинкиназа Фосфодиэстераза циклических нуклеотидов Некоторые белки цитоскелета Ионные каналы( L-тип Са 2+ канал) NO синтаза Киназа фосфорилазы Фосфопротеинфосфатаза 2 В Некоторые рецепторы ( NMDA-тип глутаматного рецептора)
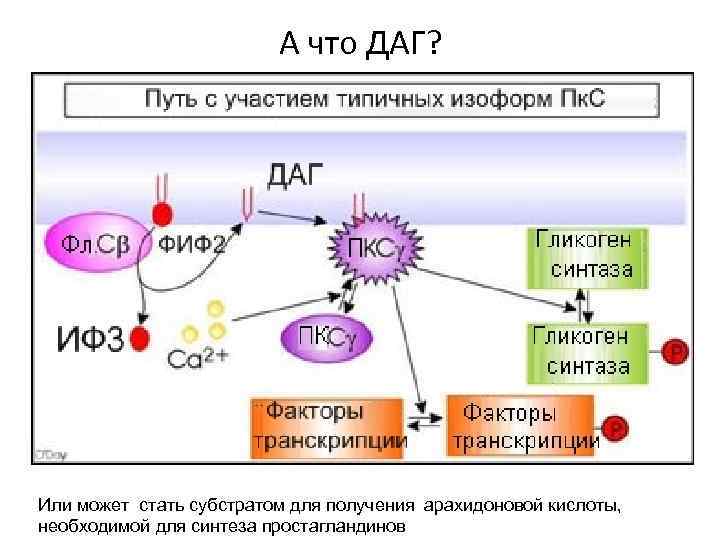 А что ДАГ? Или может стать субстратом для получения арахидоновой кислоты, необходимой для синтеза простагландинов
А что ДАГ? Или может стать субстратом для получения арахидоновой кислоты, необходимой для синтеза простагландинов
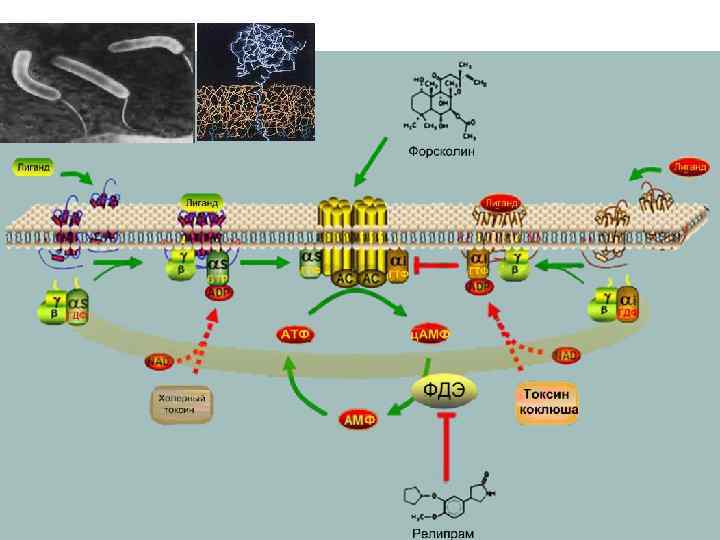
 Холерный токсин: катализирует AДФ-риболизирование Gs => гидролиз ГТФ тормозится => Gs остается активной. ц. AMФ регулирует секрецию жидкости в кишечник=> чрезмерно большие потери воды и электролитов => смерть! Коклюшный токсин: катализирует AДФ-риболизирование Gi , замена ГДФ на ГТФ тормозится => Gi застывает в неактивной форме => Аденилатциклаза не ингибируется !
Холерный токсин: катализирует AДФ-риболизирование Gs => гидролиз ГТФ тормозится => Gs остается активной. ц. AMФ регулирует секрецию жидкости в кишечник=> чрезмерно большие потери воды и электролитов => смерть! Коклюшный токсин: катализирует AДФ-риболизирование Gi , замена ГДФ на ГТФ тормозится => Gi застывает в неактивной форме => Аденилатциклаза не ингибируется !
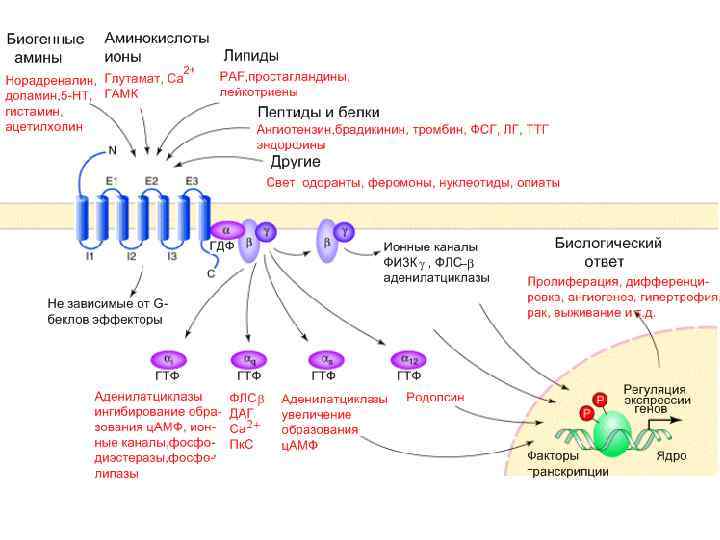
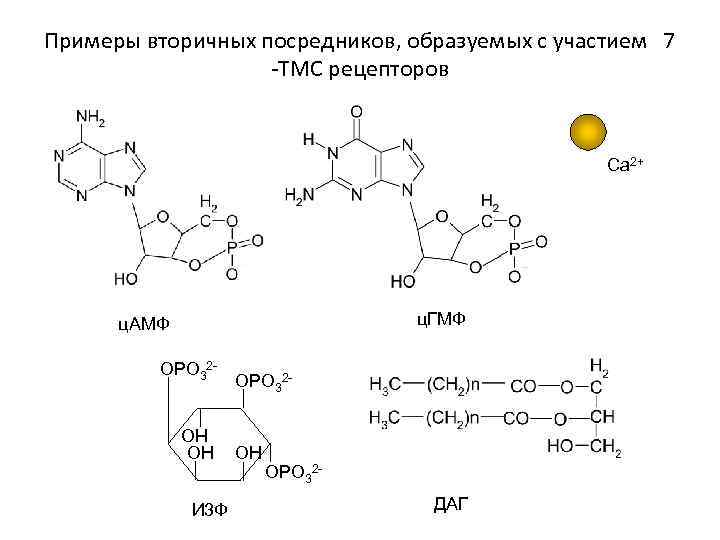 Примеры вторичных посредников, образуемых с участием 7 -ТМС рецепторов Ca 2+ ц. ГМФ ц. АМФ OPO 32 HO OH И 3 Ф OPO 32 - OH OPO 32 ДАГ
Примеры вторичных посредников, образуемых с участием 7 -ТМС рецепторов Ca 2+ ц. ГМФ ц. АМФ OPO 32 HO OH И 3 Ф OPO 32 - OH OPO 32 ДАГ
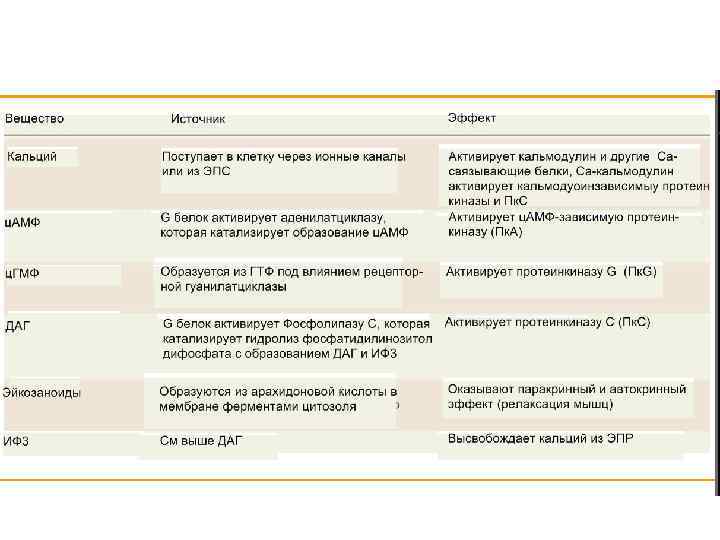
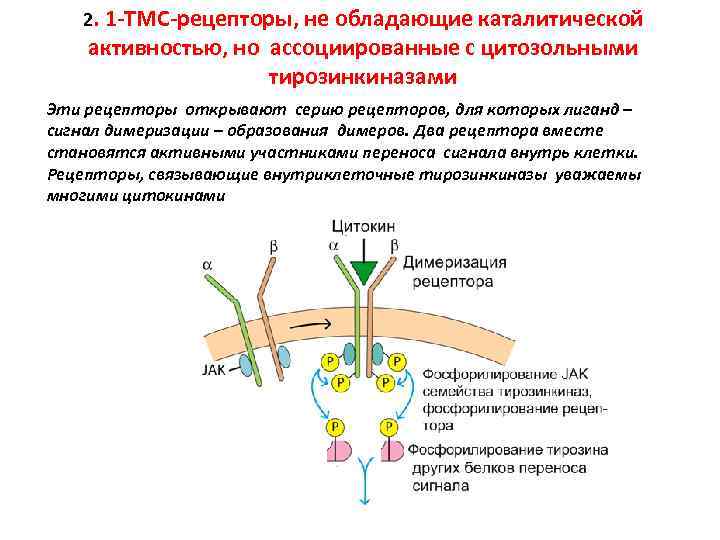 2. 1 -ТМС-рецепторы, не обладающие каталитической активностью, но ассоциированные с цитозольными тирозинкиназами Эти рецепторы открывают серию рецепторов, для которых лиганд – сигнал димеризации – образования димеров. Два рецептора вместе становятся активными участниками переноса сигнала внутрь клетки. Рецепторы, связывающие внутриклеточные тирозинкиназы уважаемы многими цитокинами
2. 1 -ТМС-рецепторы, не обладающие каталитической активностью, но ассоциированные с цитозольными тирозинкиназами Эти рецепторы открывают серию рецепторов, для которых лиганд – сигнал димеризации – образования димеров. Два рецептора вместе становятся активными участниками переноса сигнала внутрь клетки. Рецепторы, связывающие внутриклеточные тирозинкиназы уважаемы многими цитокинами
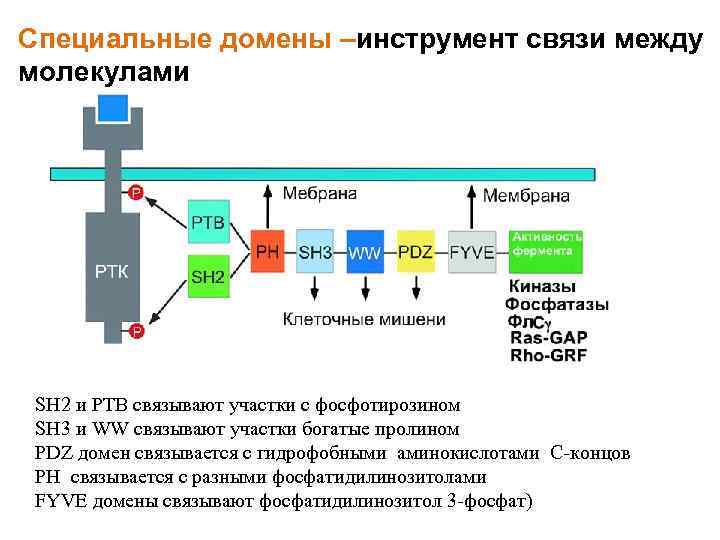 Специальные домены –инструмент связи между молекулами SH 2 и PTB связывают участки с фосфотирозином SH 3 и WW связывают участки богатые пролином PDZ домен связывается с гидрофобными аминокислотами C-концов PH связывается с разными фосфатидилинозитолами FYVE домены связывают фосфатидилинозитол 3 -фосфат)
Специальные домены –инструмент связи между молекулами SH 2 и PTB связывают участки с фосфотирозином SH 3 и WW связывают участки богатые пролином PDZ домен связывается с гидрофобными аминокислотами C-концов PH связывается с разными фосфатидилинозитолами FYVE домены связывают фосфатидилинозитол 3 -фосфат)
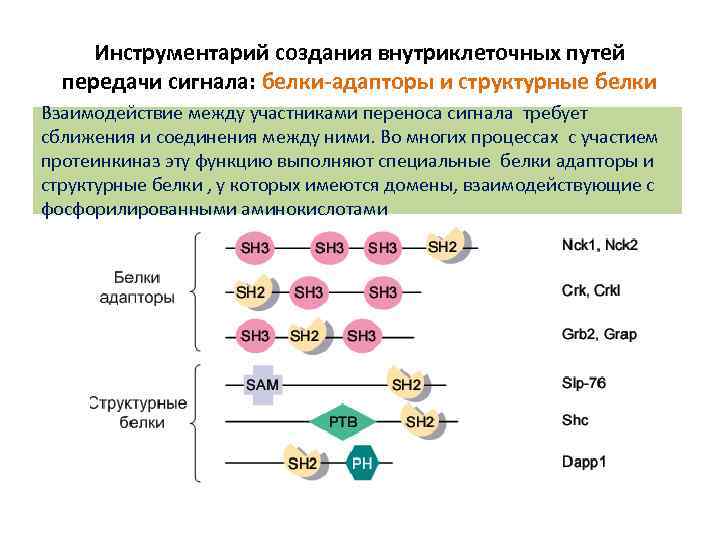 Инструментарий создания внутриклеточных путей передачи сигнала: белки-адапторы и структурные белки Взаимодействие между участниками переноса сигнала требует сближения и соединения между ними. Во многих процессах с участием протеинкиназ эту функцию выполняют специальные белки адапторы и структурные белки , у которых имеются домены, взаимодействующие с фосфорилированными аминокислотами
Инструментарий создания внутриклеточных путей передачи сигнала: белки-адапторы и структурные белки Взаимодействие между участниками переноса сигнала требует сближения и соединения между ними. Во многих процессах с участием протеинкиназ эту функцию выполняют специальные белки адапторы и структурные белки , у которых имеются домены, взаимодействующие с фосфорилированными аминокислотами
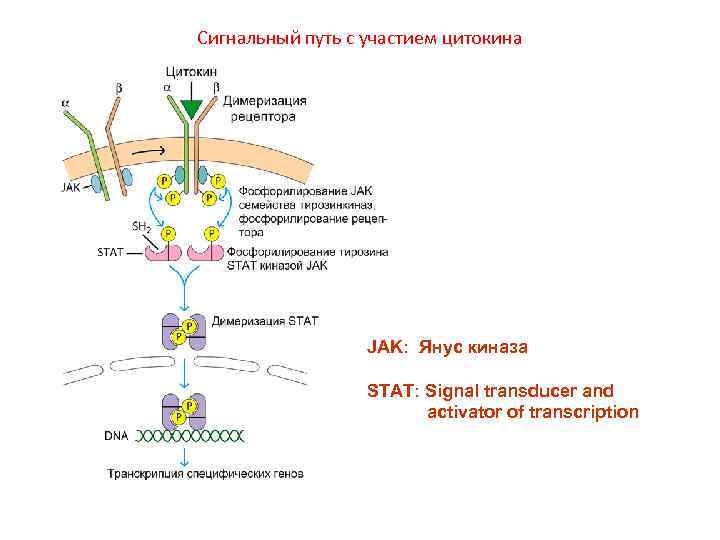 Сигнальный путь с участием цитокина JAK: Янус киназа STAT: Signal transducer and activator of transcription
Сигнальный путь с участием цитокина JAK: Янус киназа STAT: Signal transducer and activator of transcription
 3. Рецепторы, обладающие каталитической активностью 1. Тирозинкиназы: рецепторы, фосфорилирующие тирозины молекул переноса сигнала. 2. Тирозинфосфатазы: рецепторы, удаляющие фосфатные группы, связанные с тирозином. Лиганд их неизвестен. 3. Серин/треонин киназы: рецепторы, фосфорилирующие Сер или Тре молекул переноса сигнала. 4. Гуанилатциклазы : рецепторы, катализирующие образование ц. ГМФ 5. Рецепторы, асоциированные с гистидинкиназой: фофорилируют свой гистидин и затем быстро переносят фосфат на другие молекулы
3. Рецепторы, обладающие каталитической активностью 1. Тирозинкиназы: рецепторы, фосфорилирующие тирозины молекул переноса сигнала. 2. Тирозинфосфатазы: рецепторы, удаляющие фосфатные группы, связанные с тирозином. Лиганд их неизвестен. 3. Серин/треонин киназы: рецепторы, фосфорилирующие Сер или Тре молекул переноса сигнала. 4. Гуанилатциклазы : рецепторы, катализирующие образование ц. ГМФ 5. Рецепторы, асоциированные с гистидинкиназой: фофорилируют свой гистидин и затем быстро переносят фосфат на другие молекулы
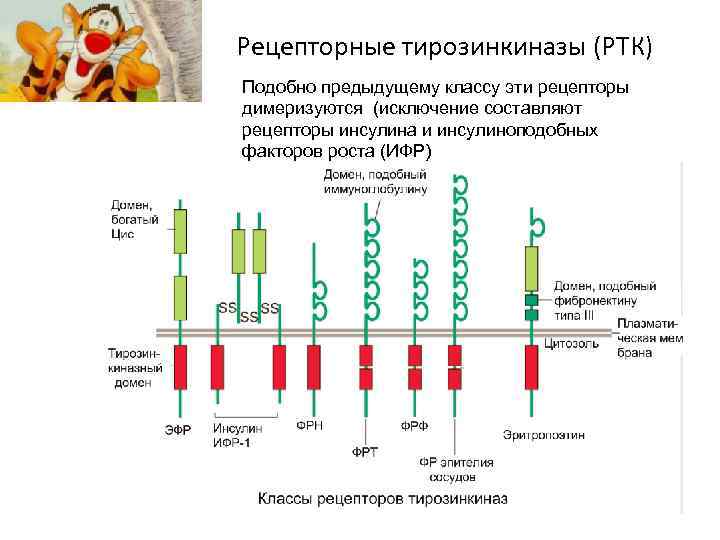 Рецепторные тирозинкиназы (РТК) Подобно предыдущему классу эти рецепторы димеризуются (исключение составляют рецепторы инсулина и инсулиноподобных факторов роста (ИФР)
Рецепторные тирозинкиназы (РТК) Подобно предыдущему классу эти рецепторы димеризуются (исключение составляют рецепторы инсулина и инсулиноподобных факторов роста (ИФР)
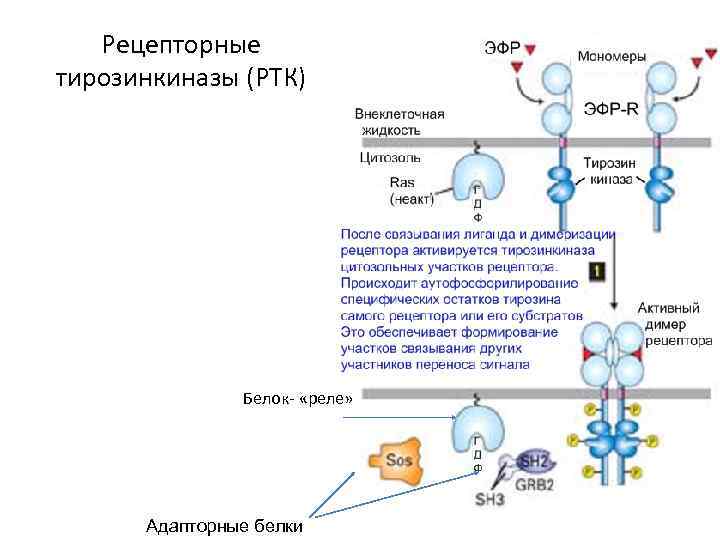 Рецепторные тирозинкиназы (РТК) Белок- «реле» Адапторные белки
Рецепторные тирозинкиназы (РТК) Белок- «реле» Адапторные белки
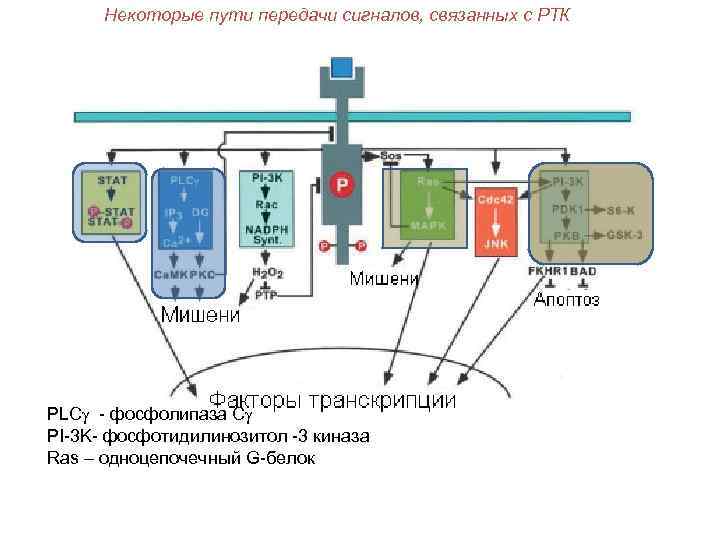 Некоторые пути передачи сигналов, связанных с РТК PLCg - фосфолипаза Сg PI-3 K- фосфотидилинозитол -3 киназа Ras – одноцепочечный G-белок
Некоторые пути передачи сигналов, связанных с РТК PLCg - фосфолипаза Сg PI-3 K- фосфотидилинозитол -3 киназа Ras – одноцепочечный G-белок
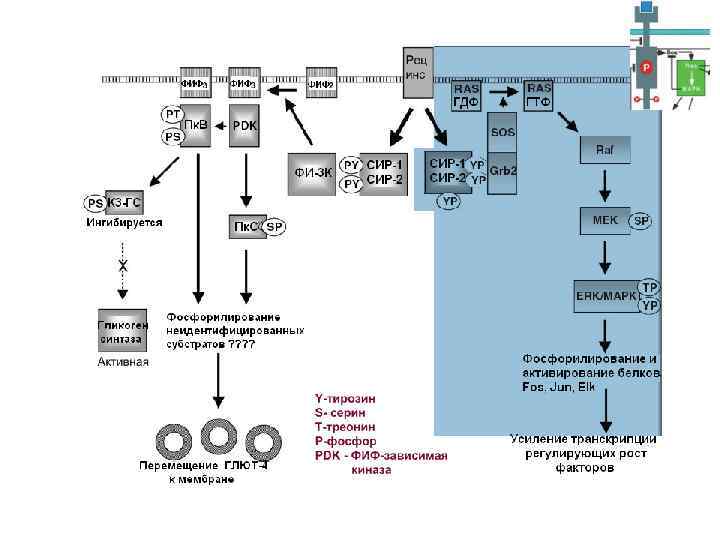
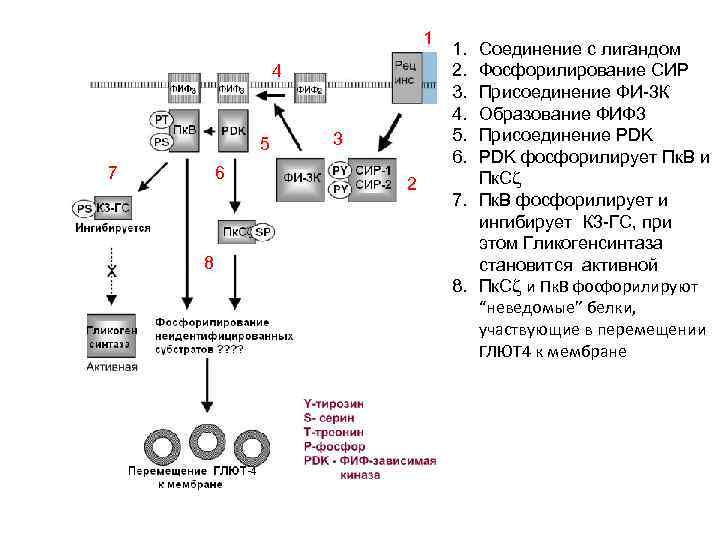 1 4 5 7 6 8 3 2 1. 2. 3. 4. 5. 6. Соединение с лигандом Фосфорилирование СИР Присоединение ФИ-3 К Образование ФИФ 3 Присоединение PDK фосфорилирует Пк. В и Пк. Сz 7. Пк. В фосфорилирует и ингибирует К 3 -ГС, при этом Гликогенсинтаза становится активной 8. Пк. Сz и Пк. В фосфорилируют “неведомые” белки, участвующие в перемещении ГЛЮТ 4 к мембране
1 4 5 7 6 8 3 2 1. 2. 3. 4. 5. 6. Соединение с лигандом Фосфорилирование СИР Присоединение ФИ-3 К Образование ФИФ 3 Присоединение PDK фосфорилирует Пк. В и Пк. Сz 7. Пк. В фосфорилирует и ингибирует К 3 -ГС, при этом Гликогенсинтаза становится активной 8. Пк. Сz и Пк. В фосфорилируют “неведомые” белки, участвующие в перемещении ГЛЮТ 4 к мембране
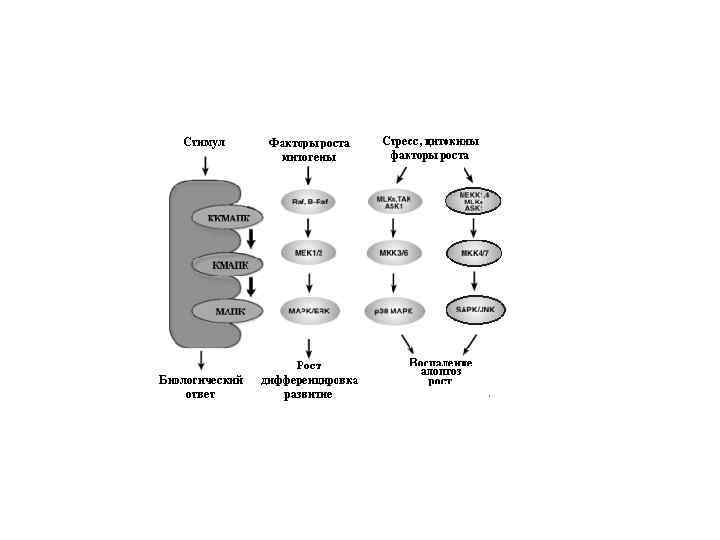
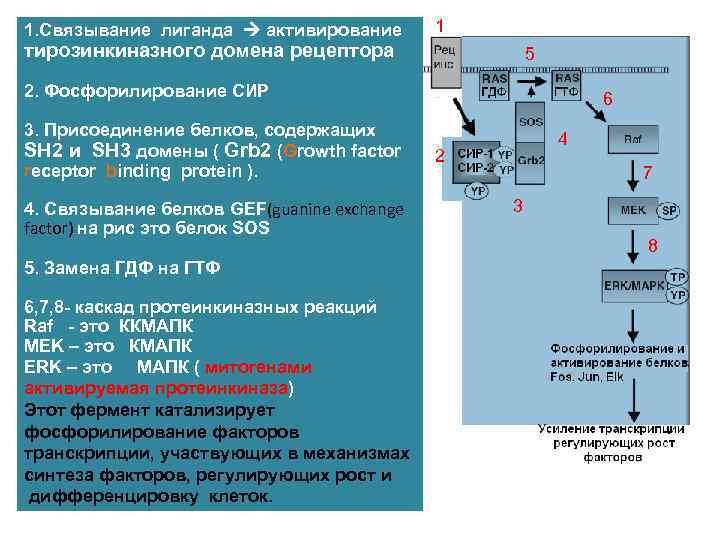 1. Связывание лиганда активирование 1 тирозинкиназного домена рецептора 5 2. Фосфорилирование СИР 3. Присоединение белков, содержащих SH 2 и SH 3 домены ( Grb 2 (Growth factor receptor binding protein ). 4. Связывание белков GEF(guanine exchange factor) на рис это белок SOS 5. Замена ГДФ на ГТФ 6, 7, 8 - каскад протеинкиназных реакций Raf - это ККМАПК MEK – это КМАПК ERK – это МАПК ( митогенами активируемая протеинкиназа) Этот фермент катализирует фосфорилирование факторов транскрипции, участвующих в механизмах синтеза факторов, регулирующих рост и дифференцировку клеток. 6 4 2 7 3 8
1. Связывание лиганда активирование 1 тирозинкиназного домена рецептора 5 2. Фосфорилирование СИР 3. Присоединение белков, содержащих SH 2 и SH 3 домены ( Grb 2 (Growth factor receptor binding protein ). 4. Связывание белков GEF(guanine exchange factor) на рис это белок SOS 5. Замена ГДФ на ГТФ 6, 7, 8 - каскад протеинкиназных реакций Raf - это ККМАПК MEK – это КМАПК ERK – это МАПК ( митогенами активируемая протеинкиназа) Этот фермент катализирует фосфорилирование факторов транскрипции, участвующих в механизмах синтеза факторов, регулирующих рост и дифференцировку клеток. 6 4 2 7 3 8
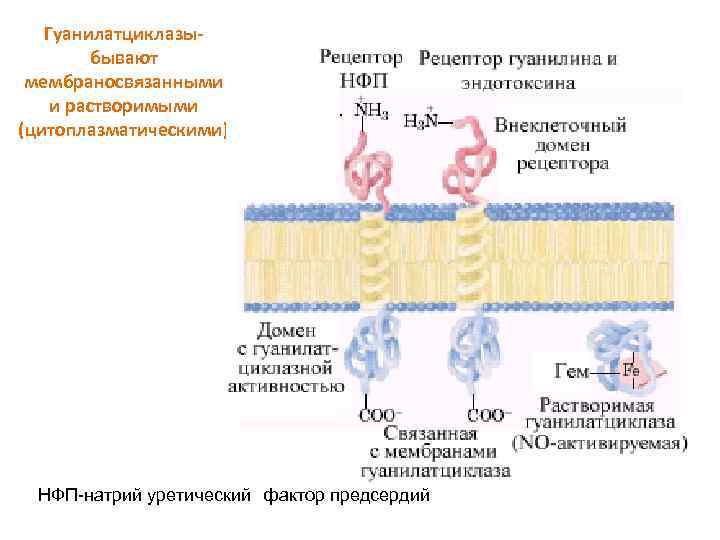 Гуанилатциклазыбывают мембраносвязанными и растворимыми (цитоплазматическими) НФП-натрий уретический фактор предсердий
Гуанилатциклазыбывают мембраносвязанными и растворимыми (цитоплазматическими) НФП-натрий уретический фактор предсердий
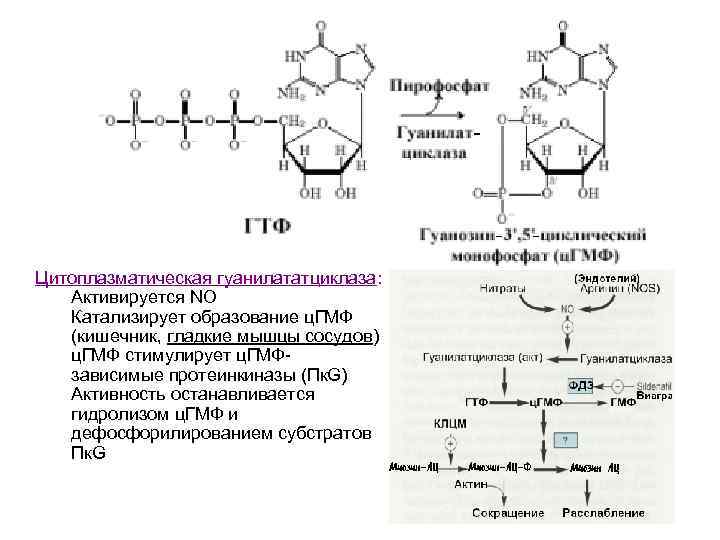 Цитоплазматическая гуанилататциклаза: Активируется NO Катализирует образование ц. ГМФ (кишечник, гладкие мышцы сосудов) ц. ГМФ стимулирует ц. ГМФзависимые протеинкиназы (Пк. G) Активность останавливается гидролизом ц. ГМФ и дефосфорилированием субстратов Пк. G
Цитоплазматическая гуанилататциклаза: Активируется NO Катализирует образование ц. ГМФ (кишечник, гладкие мышцы сосудов) ц. ГМФ стимулирует ц. ГМФзависимые протеинкиназы (Пк. G) Активность останавливается гидролизом ц. ГМФ и дефосфорилированием субстратов Пк. G
 4. Ядерные и цитозольные рецепторы В геноме червя C. elegans, ядерные рецепторы –наиболее популярная группа рецепторов. Это семейство включает больше 200 членов. В геноме человека пока идентифицировано около 50 ядерных рецепторов. Ядерные рецепторы – факторы транскрипции (TF) опосредуют изменение транскрипции в ответ на многие внеклеточные сигналы формируют короткий сигнальный путь липофильная сигнальная молекула→ TF→ ответ (изменение транскрипции) для классических стероидных гормонов: секреция железой → транспорт по крови→ клетка-мишень → диффузия в клетку → связывание с рецептором → активирование → ответ
4. Ядерные и цитозольные рецепторы В геноме червя C. elegans, ядерные рецепторы –наиболее популярная группа рецепторов. Это семейство включает больше 200 членов. В геноме человека пока идентифицировано около 50 ядерных рецепторов. Ядерные рецепторы – факторы транскрипции (TF) опосредуют изменение транскрипции в ответ на многие внеклеточные сигналы формируют короткий сигнальный путь липофильная сигнальная молекула→ TF→ ответ (изменение транскрипции) для классических стероидных гормонов: секреция железой → транспорт по крови→ клетка-мишень → диффузия в клетку → связывание с рецептором → активирование → ответ
 A/B: переменная по длине, конститутивная функция активатора AF-1 N-концевой домен вариирует по длине и последовательности обладает функцией активатора (AF-1) (активатор факторов транскрипции) C: консервативный домен, связывающий ДНК имеет два C 4 -цинковых пальца, которые могут опосредовать димеризацию рецептора и узнавание респонсивного элемента на ДНК D: петля вариирующая область, выполняющая роль сигнала ядерной локализации (NLS) E: домен, связывающий лиганд, лигандзависимая функция активатора AF-2 консервативный домен, обеспечивающий связывание лиганда, взаимодействие с hsp (белки теплового шока), димеризацию и NLS F: вариабельная C-концевая область без специфических функций Автономные активирующие функции
A/B: переменная по длине, конститутивная функция активатора AF-1 N-концевой домен вариирует по длине и последовательности обладает функцией активатора (AF-1) (активатор факторов транскрипции) C: консервативный домен, связывающий ДНК имеет два C 4 -цинковых пальца, которые могут опосредовать димеризацию рецептора и узнавание респонсивного элемента на ДНК D: петля вариирующая область, выполняющая роль сигнала ядерной локализации (NLS) E: домен, связывающий лиганд, лигандзависимая функция активатора AF-2 консервативный домен, обеспечивающий связывание лиганда, взаимодействие с hsp (белки теплового шока), димеризацию и NLS F: вариабельная C-концевая область без специфических функций Автономные активирующие функции
 Классификация ядерных и цитозольных рецепторов Классификация по типу лиганда и сродству к нему
Классификация ядерных и цитозольных рецепторов Классификация по типу лиганда и сродству к нему
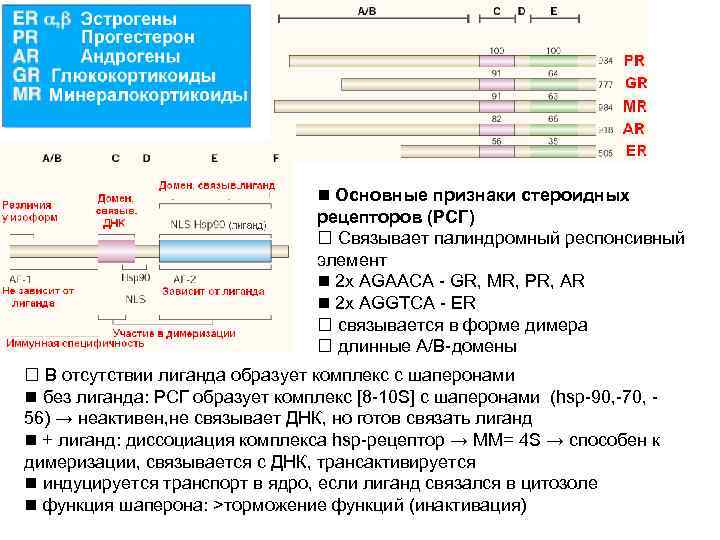 Основные признаки стероидных рецепторов (РСГ) Связывает палиндромный респонсивный элемент 2 x AGAACA - GR, MR, PR, AR 2 x AGGTCA - ER связывается в форме димера длинные A/B-домены В отсутствии лиганда образует комплекс с шаперонами без лиганда: РСГ образует комплекс [8 -10 S] с шаперонами (hsp-90, -70, 56) → неактивен, не связывает ДНК, но готов связать лиганд + лиганд: диссоциация комплекса hsp-рецептор → ММ= 4 S → способен к димеризации, связывается с ДНК, трансактивируется индуцируется транспорт в ядро, если лиганд связался в цитозоле функция шаперона: >торможение функций (инактивация)
Основные признаки стероидных рецепторов (РСГ) Связывает палиндромный респонсивный элемент 2 x AGAACA - GR, MR, PR, AR 2 x AGGTCA - ER связывается в форме димера длинные A/B-домены В отсутствии лиганда образует комплекс с шаперонами без лиганда: РСГ образует комплекс [8 -10 S] с шаперонами (hsp-90, -70, 56) → неактивен, не связывает ДНК, но готов связать лиганд + лиганд: диссоциация комплекса hsp-рецептор → ММ= 4 S → способен к димеризации, связывается с ДНК, трансактивируется индуцируется транспорт в ядро, если лиганд связался в цитозоле функция шаперона: >торможение функций (инактивация)
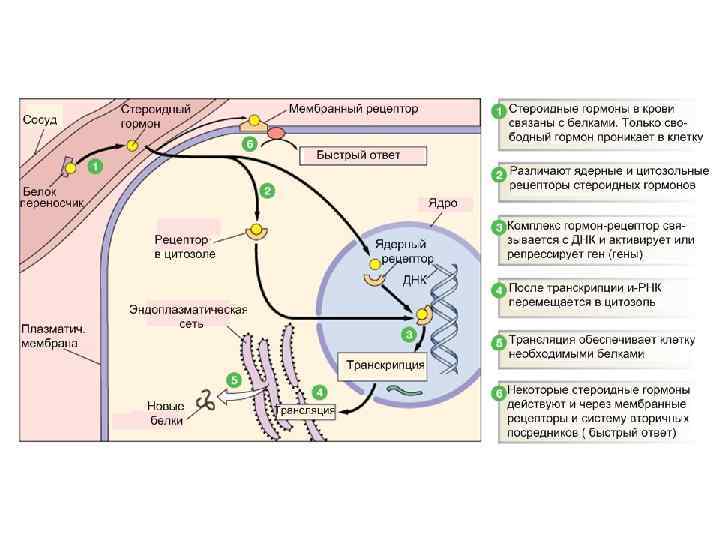
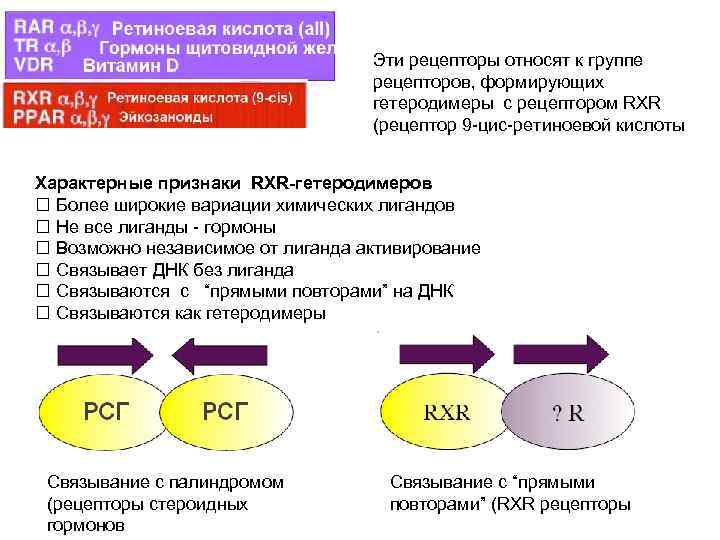 Эти рецепторы относят к группе рецепторов, формирующих гетеродимеры с рецептором RXR (рецептор 9 -цис-ретиноевой кислоты Характерные признаки RXR-гетеродимеров Более широкие вариации химических лигандов Не все лиганды - гормоны Возможно независимое от лиганда активирование Связывает ДНК без лиганда Связываются с “прямыми повторами” на ДНК Связываются как гетеродимеры Связывание с палиндромом (рецепторы стероидных гормонов Связывание с “прямыми повторами” (RXR рецепторы
Эти рецепторы относят к группе рецепторов, формирующих гетеродимеры с рецептором RXR (рецептор 9 -цис-ретиноевой кислоты Характерные признаки RXR-гетеродимеров Более широкие вариации химических лигандов Не все лиганды - гормоны Возможно независимое от лиганда активирование Связывает ДНК без лиганда Связываются с “прямыми повторами” на ДНК Связываются как гетеродимеры Связывание с палиндромом (рецепторы стероидных гормонов Связывание с “прямыми повторами” (RXR рецепторы
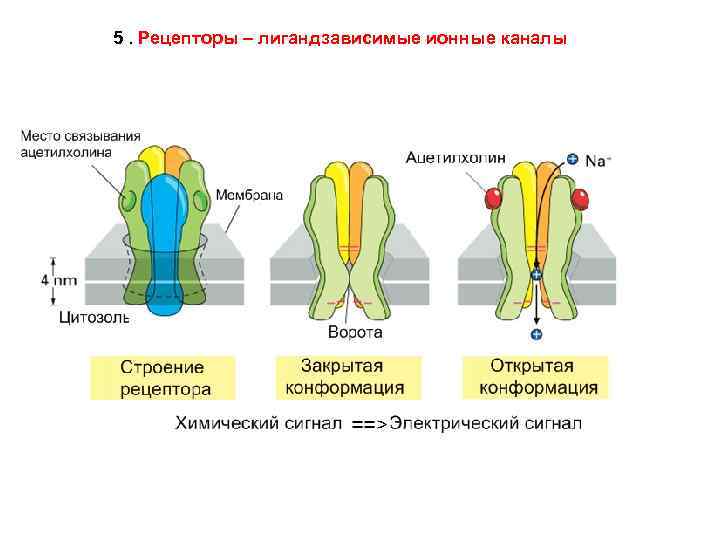 5. Рецепторы – лигандзависимые ионные каналы
5. Рецепторы – лигандзависимые ионные каналы
 7. Рецепторы – молекулы клеточной адгезии Обеспечивают прямое взаимодействие между клетками • • • I. Замыкающие (плотные) контакты II. Прикрепительные соединения 1. c актиновыми филаментами (адгезионные контакты) а) между клетками (например, адгезионные пояса) б) между клетками и матриксом (например, фокальные контакты) 2. С промежуточными филаментами а) между клетками (десмосомы) б) между клетками и матриксом (полудесмосомы) III. Коммуникационные соединения 1. Щелевые контакты 2. Химические синапсы
7. Рецепторы – молекулы клеточной адгезии Обеспечивают прямое взаимодействие между клетками • • • I. Замыкающие (плотные) контакты II. Прикрепительные соединения 1. c актиновыми филаментами (адгезионные контакты) а) между клетками (например, адгезионные пояса) б) между клетками и матриксом (например, фокальные контакты) 2. С промежуточными филаментами а) между клетками (десмосомы) б) между клетками и матриксом (полудесмосомы) III. Коммуникационные соединения 1. Щелевые контакты 2. Химические синапсы
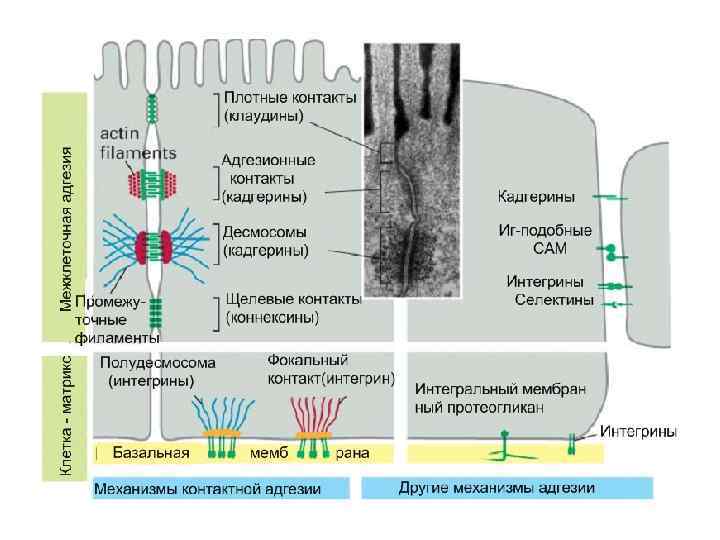
 Клетки связываются и общаются при помощи CAM. Клетка - клетка Молекулы межклеточной адгезии CAM (cell adhesion molecules) 1) Ca 2+ - зависимые CAM: кадгерины, селектины, интегрины 2)Ca 2+ - независимые CAM
Клетки связываются и общаются при помощи CAM. Клетка - клетка Молекулы межклеточной адгезии CAM (cell adhesion molecules) 1) Ca 2+ - зависимые CAM: кадгерины, селектины, интегрины 2)Ca 2+ - независимые CAM
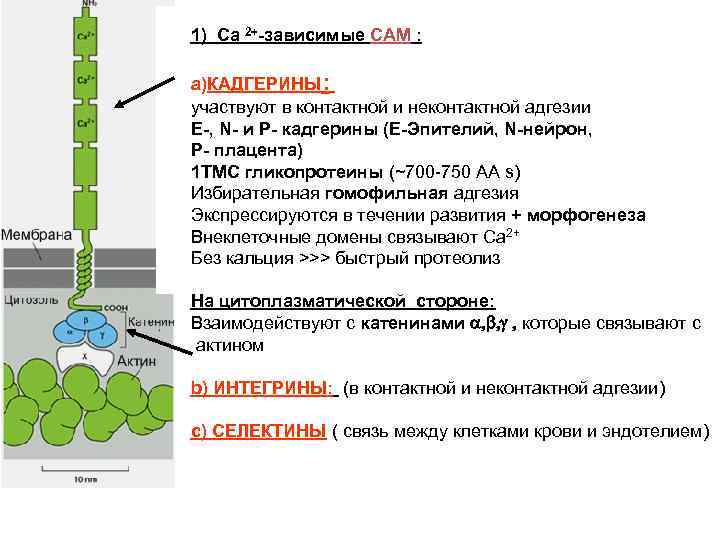 1) Cа 2+-зависимые СAM : a)КАДГЕРИНЫ: участвуют в контактной и неконтактной адгезии E-, N- и P- кадгерины (E-Эпителий, N-нейрон, P- плацента) 1 ТМС гликопротеины (~700 -750 AA s) Избирательная гомофильная адгезия Экспрессируются в течении развития + морфогенеза Внеклеточные домены связывают Ca 2+ Без кальция >>> быстрый протеолиз На цитоплазматической стороне: Взаимодействуют с катенинами a, b, g , которые связывают с актином b) ИНТЕГРИНЫ: (в контактной и неконтактной адгезии) c) СЕЛЕКТИНЫ ( связь между клетками крови и эндотелием)
1) Cа 2+-зависимые СAM : a)КАДГЕРИНЫ: участвуют в контактной и неконтактной адгезии E-, N- и P- кадгерины (E-Эпителий, N-нейрон, P- плацента) 1 ТМС гликопротеины (~700 -750 AA s) Избирательная гомофильная адгезия Экспрессируются в течении развития + морфогенеза Внеклеточные домены связывают Ca 2+ Без кальция >>> быстрый протеолиз На цитоплазматической стороне: Взаимодействуют с катенинами a, b, g , которые связывают с актином b) ИНТЕГРИНЫ: (в контактной и неконтактной адгезии) c) СЕЛЕКТИНЫ ( связь между клетками крови и эндотелием)
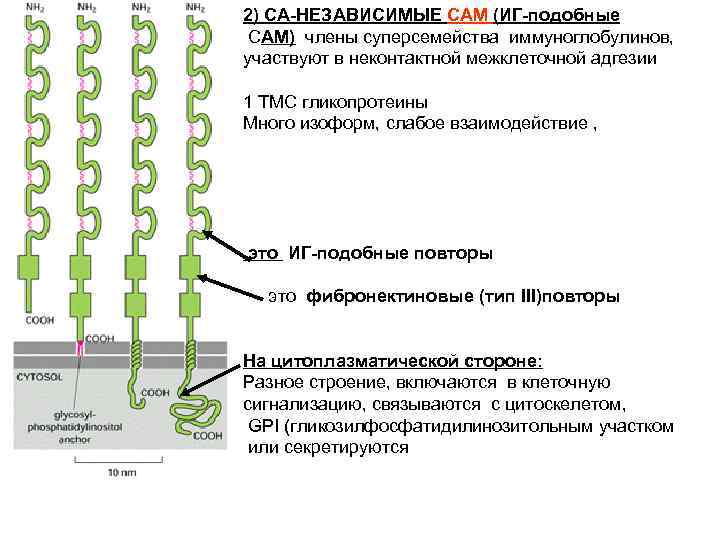 2) CA-НЕЗАВИСИМЫЕ CAM (ИГ-подобные CAM) члены суперсемейства иммуноглобулинов, участвуют в неконтактной межклеточной адгезии 1 ТМС гликопротеины Много изоформ, слабое взаимодействие , это ИГ-подобные повторы это фибронектиновые (тип III)повторы На цитоплазматической стороне: Разное строение, включаются в клеточную сигнализацию, связываются с цитоскелетом, GPI (гликозилфосфатидилинозитольным участком или секретируются
2) CA-НЕЗАВИСИМЫЕ CAM (ИГ-подобные CAM) члены суперсемейства иммуноглобулинов, участвуют в неконтактной межклеточной адгезии 1 ТМС гликопротеины Много изоформ, слабое взаимодействие , это ИГ-подобные повторы это фибронектиновые (тип III)повторы На цитоплазматической стороне: Разное строение, включаются в клеточную сигнализацию, связываются с цитоскелетом, GPI (гликозилфосфатидилинозитольным участком или секретируются
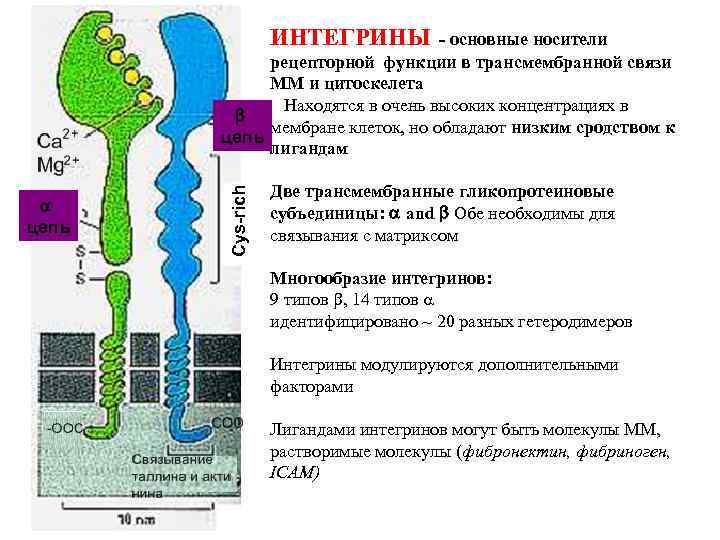 ИНТЕГРИНЫ a цепь Cys-rich - основные носители рецепторной функции в трансмембранной связи ММ и цитоскелета Находятся в очень высоких концентрациях в b мембране клеток, но обладают низким сродством к цепь лигандам Две трансмембранные гликопротеиновые субъединицы: a and b Обе необходимы для связывания с матриксом Многообразие интегринов: 9 типов b, 14 типов идентифицировано ~ 20 разных гетеродимеров Интегрины модулируются дополнительными факторами Лигандами интегринов могут быть молекулы ММ, растворимые молекулы (фибронектин, фибриноген, ICAM)
ИНТЕГРИНЫ a цепь Cys-rich - основные носители рецепторной функции в трансмембранной связи ММ и цитоскелета Находятся в очень высоких концентрациях в b мембране клеток, но обладают низким сродством к цепь лигандам Две трансмембранные гликопротеиновые субъединицы: a and b Обе необходимы для связывания с матриксом Многообразие интегринов: 9 типов b, 14 типов идентифицировано ~ 20 разных гетеродимеров Интегрины модулируются дополнительными факторами Лигандами интегринов могут быть молекулы ММ, растворимые молекулы (фибронектин, фибриноген, ICAM)
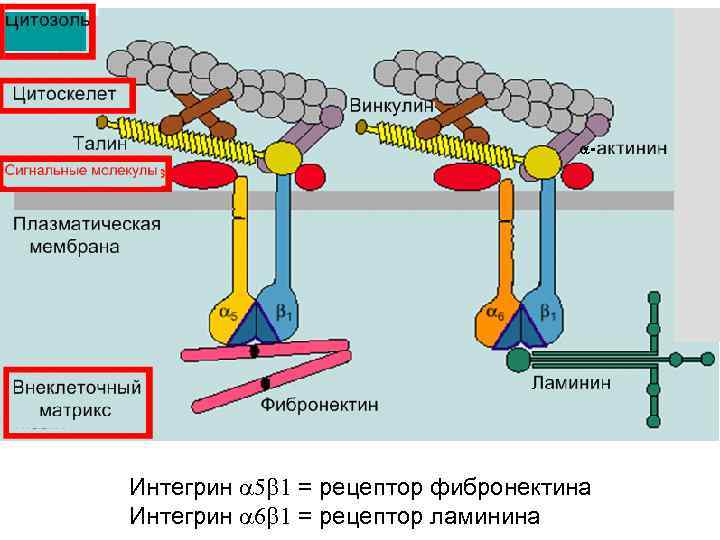 Интегрин 5 b 1 = рецептор фибронектина Интегрин 6 b 1 = рецептор ламинина
Интегрин 5 b 1 = рецептор фибронектина Интегрин 6 b 1 = рецептор ламинина
 Интегрины обеспечиают СИГНАЛИЗАЦИЮ ИЗ ВНЕКЛЕТОЧНОЙ СРЕДЫ: Внеклеточныый домен связывается с лигандом (ММ или CAM) Конформационные изменения цитозольного домена (хвост) Взаимодействие цитоскелета и сигнальных молекул. фосфорилирование, экспрессия генов и СИГНАЛИЗАЦИЮ ИЗ КЛЕТКИ: Молекулярный сигнал Конформационные изменения цитозольного домена Конформационные изменения внеклеточного лигандсвязывающего участка Изменение сродства к лиганду
Интегрины обеспечиают СИГНАЛИЗАЦИЮ ИЗ ВНЕКЛЕТОЧНОЙ СРЕДЫ: Внеклеточныый домен связывается с лигандом (ММ или CAM) Конформационные изменения цитозольного домена (хвост) Взаимодействие цитоскелета и сигнальных молекул. фосфорилирование, экспрессия генов и СИГНАЛИЗАЦИЮ ИЗ КЛЕТКИ: Молекулярный сигнал Конформационные изменения цитозольного домена Конформационные изменения внеклеточного лигандсвязывающего участка Изменение сродства к лиганду
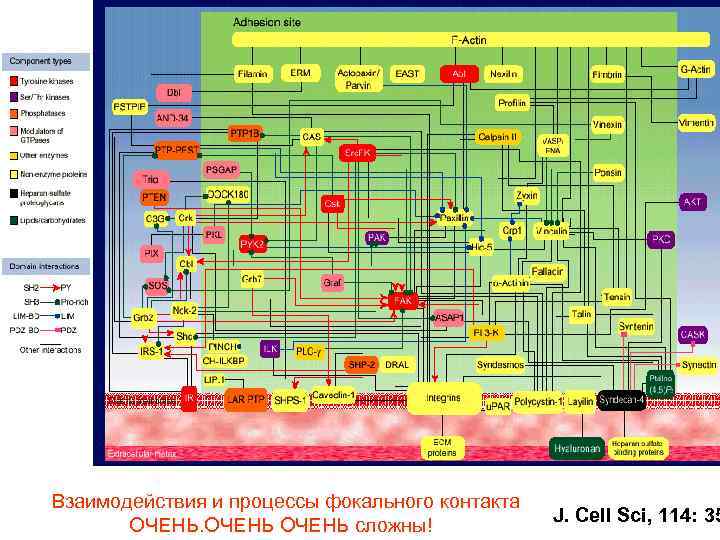 Взаимодействия и процессы фокального контакта ОЧЕНЬ сложны! J. Cell Sci, 114: 35
Взаимодействия и процессы фокального контакта ОЧЕНЬ сложны! J. Cell Sci, 114: 35
 Механизмы выключения переноса сигналов • Секвестрация рецепторов • Модификация рецепторов (фосфорилирование) • Инактивация белков участвующих в переносе (фосфатазы) • Белки- «реле» • Изменение концентрации вторичных посредников • Образование белков ингибиторов • Взаимодействие между различными сигнальными путями Большая часть участников регулируются по принципу обратной связи
Механизмы выключения переноса сигналов • Секвестрация рецепторов • Модификация рецепторов (фосфорилирование) • Инактивация белков участвующих в переносе (фосфатазы) • Белки- «реле» • Изменение концентрации вторичных посредников • Образование белков ингибиторов • Взаимодействие между различными сигнальными путями Большая часть участников регулируются по принципу обратной связи
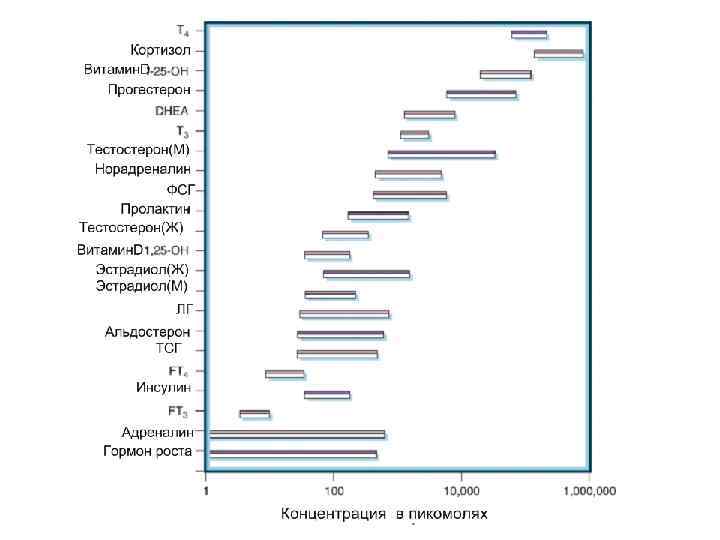
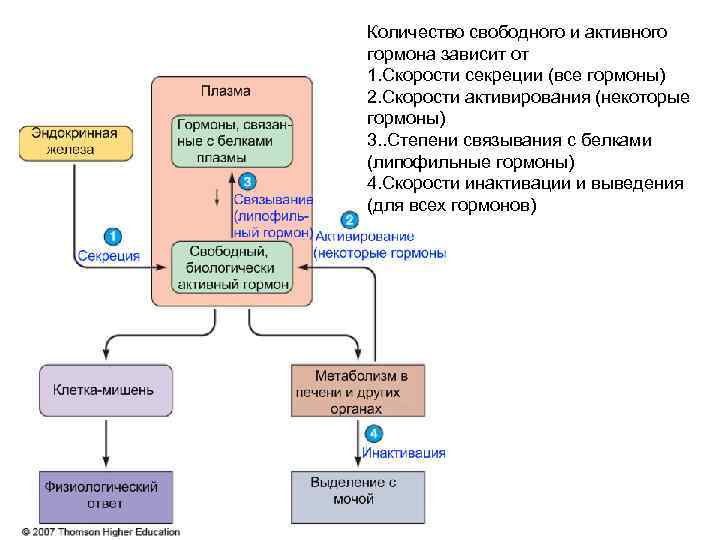 Количество свободного и активного гормона зависит от 1. Скорости секреции (все гормоны) 2. Скорости активирования (некоторые гормоны) 3. . Степени связывания с белками (липофильные гормоны) 4. Скорости инактивации и выведения (для всех гормонов)
Количество свободного и активного гормона зависит от 1. Скорости секреции (все гормоны) 2. Скорости активирования (некоторые гормоны) 3. . Степени связывания с белками (липофильные гормоны) 4. Скорости инактивации и выведения (для всех гормонов)
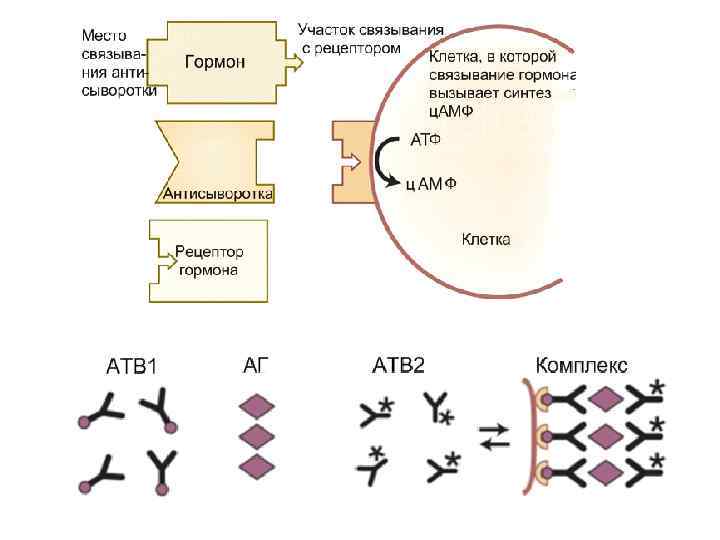
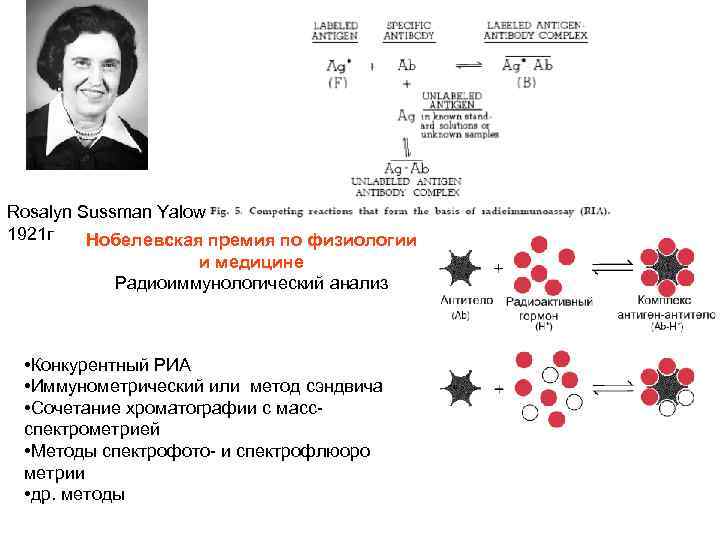 Rosalyn Sussman Yalow 1921 г Нобелевская премия по физиологии и медицине Радиоиммунологический анализ • Конкурентный РИА • Иммунометрический или метод сэндвича • Сочетание хроматографии с массспектрометрией • Методы спектрофото- и спектрофлюоро метрии • др. методы
Rosalyn Sussman Yalow 1921 г Нобелевская премия по физиологии и медицине Радиоиммунологический анализ • Конкурентный РИА • Иммунометрический или метод сэндвича • Сочетание хроматографии с массспектрометрией • Методы спектрофото- и спектрофлюоро метрии • др. методы