Внутренняя энергия газа.pptx
- Количество слайдов: 27
 Внутренняя энергия газа Основы термодинамики
Внутренняя энергия газа Основы термодинамики
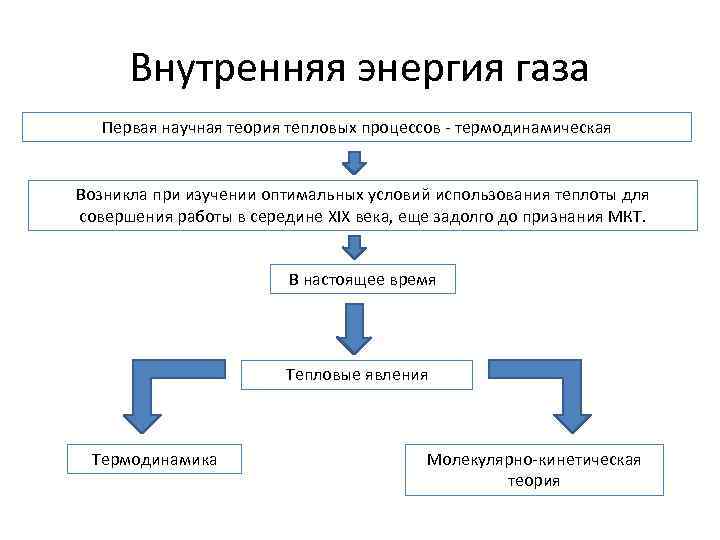 Внутренняя энергия газа Первая научная теория тепловых процессов - термодинамическая Возникла при изучении оптимальных условий использования теплоты для совершения работы в середине XIX века, еще задолго до признания МКТ. В настоящее время Тепловые явления Термодинамика Молекулярно-кинетическая теория
Внутренняя энергия газа Первая научная теория тепловых процессов - термодинамическая Возникла при изучении оптимальных условий использования теплоты для совершения работы в середине XIX века, еще задолго до признания МКТ. В настоящее время Тепловые явления Термодинамика Молекулярно-кинетическая теория
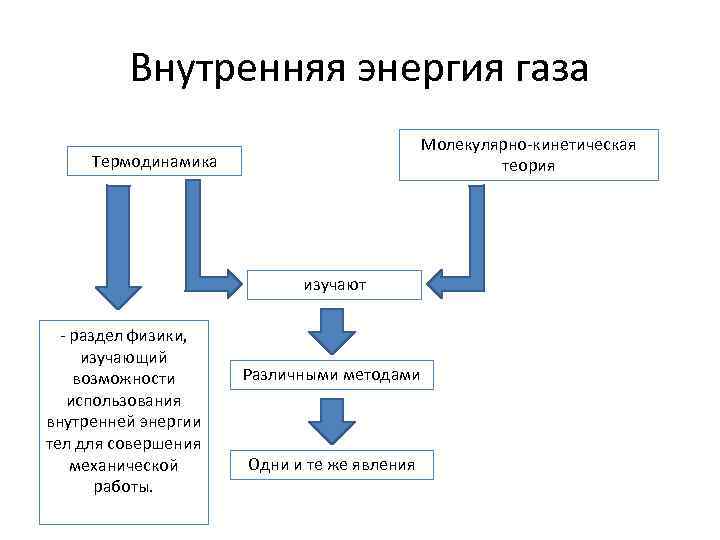 Внутренняя энергия газа Молекулярно-кинетическая теория Термодинамика изучают - раздел физики, изучающий возможности использования внутренней энергии тел для совершения механической работы. Различными методами Одни и те же явления
Внутренняя энергия газа Молекулярно-кинетическая теория Термодинамика изучают - раздел физики, изучающий возможности использования внутренней энергии тел для совершения механической работы. Различными методами Одни и те же явления
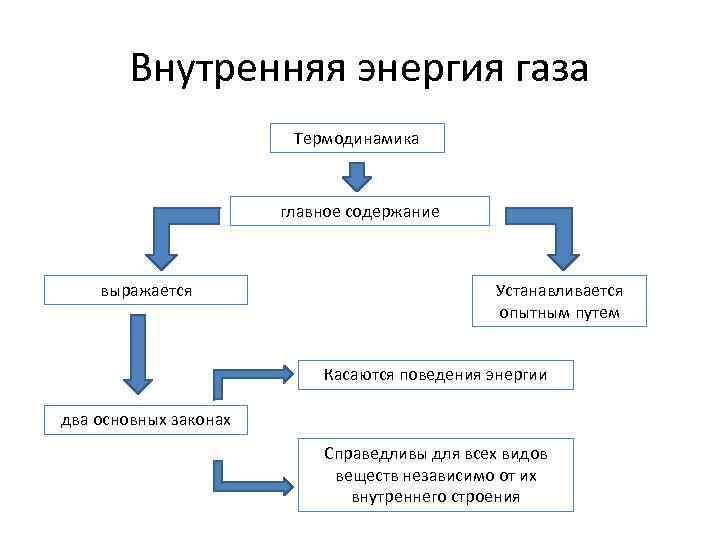 Внутренняя энергия газа Термодинамика главное содержание выражается Устанавливается опытным путем Касаются поведения энергии два основных законах Справедливы для всех видов веществ независимо от их внутреннего строения
Внутренняя энергия газа Термодинамика главное содержание выражается Устанавливается опытным путем Касаются поведения энергии два основных законах Справедливы для всех видов веществ независимо от их внутреннего строения
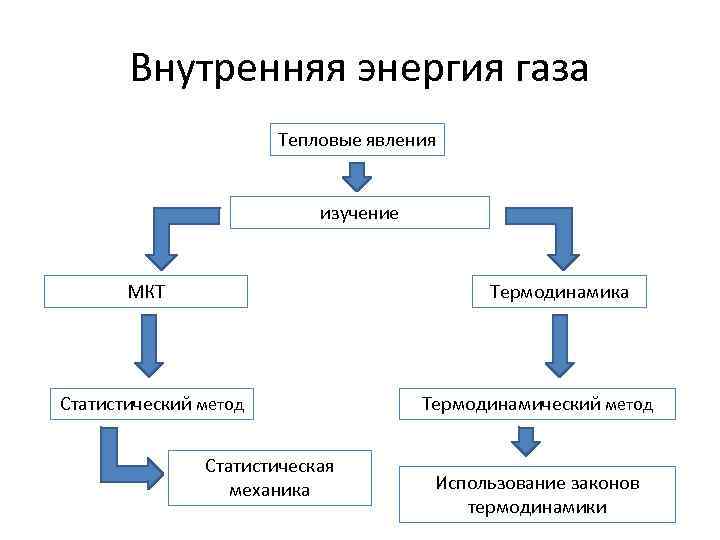 Внутренняя энергия газа Тепловые явления изучение МКТ Термодинамика Статистический метод Статистическая механика Термодинамический метод Использование законов термодинамики
Внутренняя энергия газа Тепловые явления изучение МКТ Термодинамика Статистический метод Статистическая механика Термодинамический метод Использование законов термодинамики
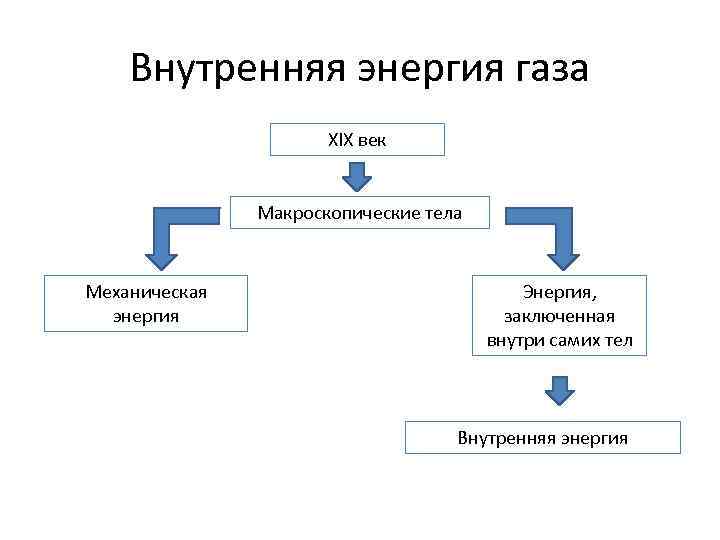 Внутренняя энергия газа XIX век Макроскопические тела Механическая энергия Энергия, заключенная внутри самих тел Внутренняя энергия
Внутренняя энергия газа XIX век Макроскопические тела Механическая энергия Энергия, заключенная внутри самих тел Внутренняя энергия
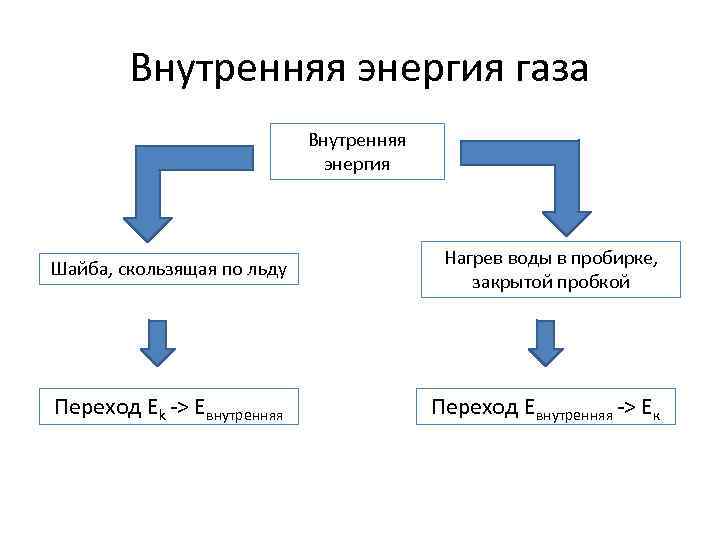 Внутренняя энергия газа Внутренняя энергия Шайба, скользящая по льду Нагрев воды в пробирке, закрытой пробкой Переход Ek -> Eвнутренняя Переход Eвнутренняя -> Eк
Внутренняя энергия газа Внутренняя энергия Шайба, скользящая по льду Нагрев воды в пробирке, закрытой пробкой Переход Ek -> Eвнутренняя Переход Eвнутренняя -> Eк
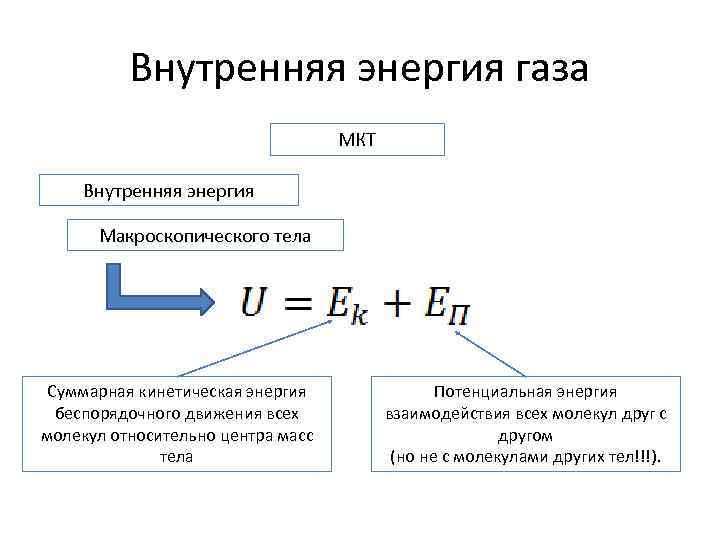 Внутренняя энергия газа МКТ Внутренняя энергия Макроскопического тела Суммарная кинетическая энергия беспорядочного движения всех молекул относительно центра масс тела Потенциальная энергия взаимодействия всех молекул друг с другом (но не с молекулами других тел!!!).
Внутренняя энергия газа МКТ Внутренняя энергия Макроскопического тела Суммарная кинетическая энергия беспорядочного движения всех молекул относительно центра масс тела Потенциальная энергия взаимодействия всех молекул друг с другом (но не с молекулами других тел!!!).
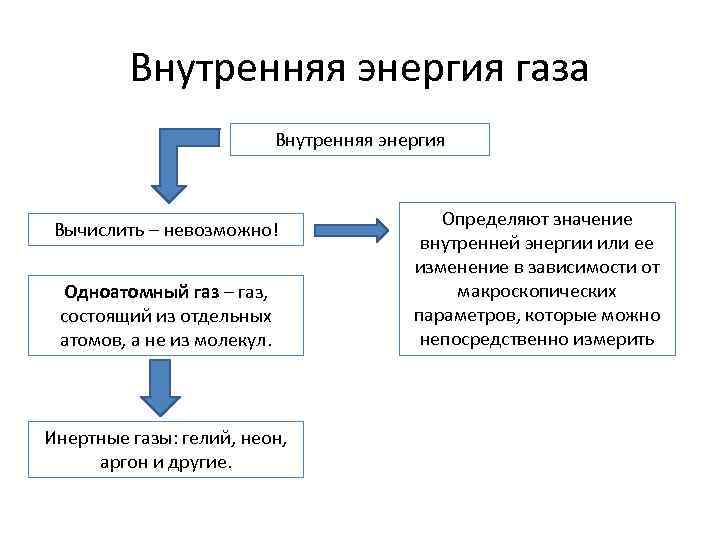 Внутренняя энергия газа Внутренняя энергия Вычислить – невозможно! Одноатомный газ – газ, состоящий из отдельных атомов, а не из молекул. Инертные газы: гелий, неон, аргон и другие. Определяют значение внутренней энергии или ее изменение в зависимости от макроскопических параметров, которые можно непосредственно измерить
Внутренняя энергия газа Внутренняя энергия Вычислить – невозможно! Одноатомный газ – газ, состоящий из отдельных атомов, а не из молекул. Инертные газы: гелий, неон, аргон и другие. Определяют значение внутренней энергии или ее изменение в зависимости от макроскопических параметров, которые можно непосредственно измерить
 Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа Идеальный газ – газ, молекулы которого не взаимодействуют друг с другом, то есть их Eп = 0 Для 1 атома: Число атомов: Получаем: U = Ek - универсальная газовая постоянная
Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа Идеальный газ – газ, молекулы которого не взаимодействуют друг с другом, то есть их Eп = 0 Для 1 атома: Число атомов: Получаем: U = Ek - универсальная газовая постоянная
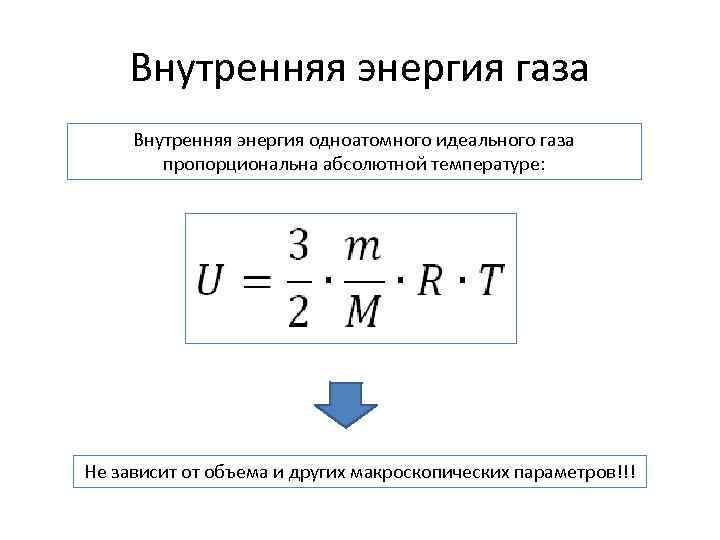 Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа пропорциональна абсолютной температуре: Не зависит от объема и других макроскопических параметров!!!
Внутренняя энергия газа Внутренняя энергия одноатомного идеального газа пропорциональна абсолютной температуре: Не зависит от объема и других макроскопических параметров!!!
 Внутренняя энергия газа Изменение внутренней энергии происходит только при изменении температуры:
Внутренняя энергия газа Изменение внутренней энергии происходит только при изменении температуры:
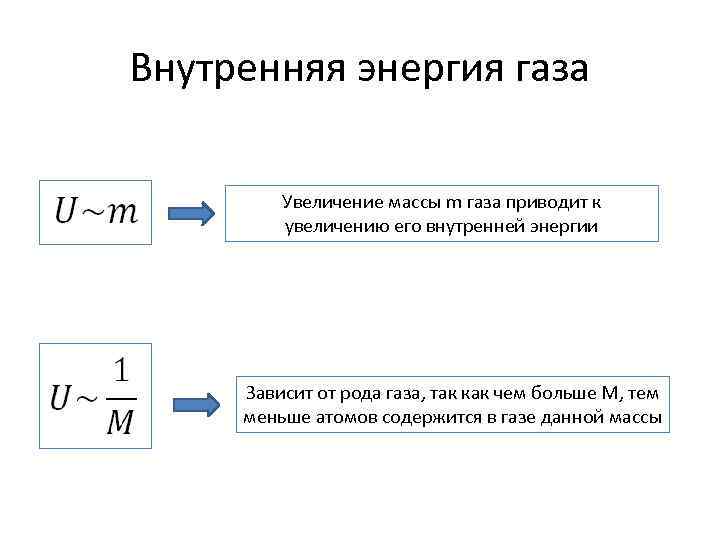 Внутренняя энергия газа Увеличение массы m газа приводит к увеличению его внутренней энергии Зависит от рода газа, так как чем больше M, тем меньше атомов содержится в газе данной массы
Внутренняя энергия газа Увеличение массы m газа приводит к увеличению его внутренней энергии Зависит от рода газа, так как чем больше M, тем меньше атомов содержится в газе данной массы
 Внутренняя энергия газа Если идеальный газ состоит из более сложных молекул, чем одноатомный, то: Изменяется лишь коэффициент пропорциональности между U и T. i – число степеней свободы молекулы Число степеней свободы – число возможных независимых направлений движения молекулы.
Внутренняя энергия газа Если идеальный газ состоит из более сложных молекул, чем одноатомный, то: Изменяется лишь коэффициент пропорциональности между U и T. i – число степеней свободы молекулы Число степеней свободы – число возможных независимых направлений движения молекулы.
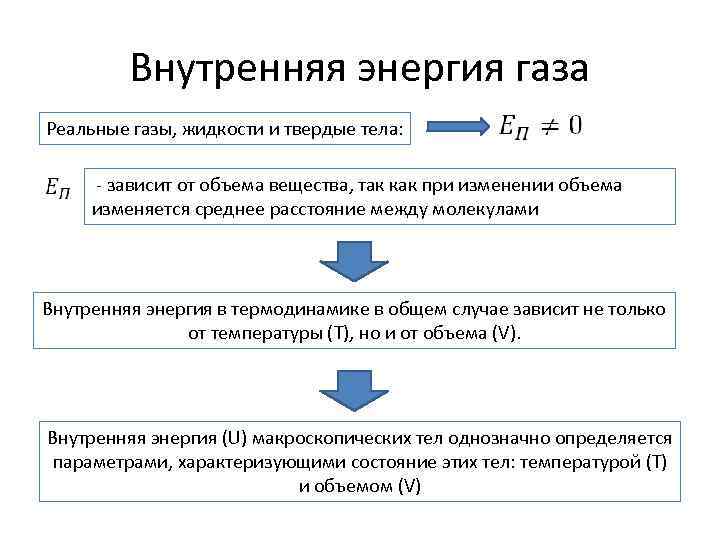 Внутренняя энергия газа Реальные газы, жидкости и твердые тела: - зависит от объема вещества, так как при изменении объема изменяется среднее расстояние между молекулами Внутренняя энергия в термодинамике в общем случае зависит не только от температуры (T), но и от объема (V). Внутренняя энергия (U) макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой (T) и объемом (V)
Внутренняя энергия газа Реальные газы, жидкости и твердые тела: - зависит от объема вещества, так как при изменении объема изменяется среднее расстояние между молекулами Внутренняя энергия в термодинамике в общем случае зависит не только от температуры (T), но и от объема (V). Внутренняя энергия (U) макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой (T) и объемом (V)
 Задание Моль какого газа (водорода или гелия) имеет большую внутреннюю энергию при одинаковой температуре?
Задание Моль какого газа (водорода или гелия) имеет большую внутреннюю энергию при одинаковой температуре?
 Внутренняя энергия газа Может изменяться: При деформации При тепловых процессах Тепловые процессы – процессы, связанные с изменением как температуры тела, так и его агрегатного состояния – плавлением или отвердеванием, испарением или конденсацией. При химических реакциях Силы взаимодействия между атомами изменяются Энергии взаимодействия атомов Характер движения и взаимодействия молекул При ядерных реакциях
Внутренняя энергия газа Может изменяться: При деформации При тепловых процессах Тепловые процессы – процессы, связанные с изменением как температуры тела, так и его агрегатного состояния – плавлением или отвердеванием, испарением или конденсацией. При химических реакциях Силы взаимодействия между атомами изменяются Энергии взаимодействия атомов Характер движения и взаимодействия молекул При ядерных реакциях
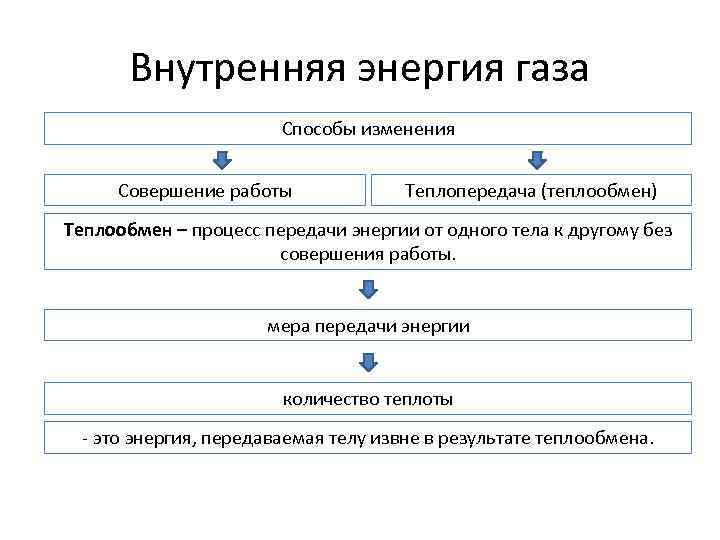 Внутренняя энергия газа Способы изменения Совершение работы Теплопередача (теплообмен) Теплообмен – процесс передачи энергии от одного тела к другому без совершения работы. мера передачи энергии количество теплоты - это энергия, передаваемая телу извне в результате теплообмена.
Внутренняя энергия газа Способы изменения Совершение работы Теплопередача (теплообмен) Теплообмен – процесс передачи энергии от одного тела к другому без совершения работы. мера передачи энергии количество теплоты - это энергия, передаваемая телу извне в результате теплообмена.
 Задачи 1. В одном стакане находится горячая вода, в другом – холодная. В каком случае вода обладает большей внутренней энергией? 2. Спичка воспламеняется при трении ее головки о коробок. Объяснить это явление. 3. Объяснить возрастание скорости диффузии с повышением температуры. 4. Почему радиаторы центрального отопления ставят обычно под окнами? 5. Почему зимой на улице металл на ощупь кажется холоднее дерева? 6. В стакан налит горячий чай. Как осуществляется теплообмен между чаем и стенками стакана? 7. Приведите примеры изменения внутренней энергии тела в процессе теплообмена 8. Почему в безветрие пламя свечи устанавливается вертикально? 9. Зачем канализационные и водопроводные трубы зарывают в землю на значительную глубину? 5. 1. 1 Найдите внутреннюю энергию 5 моль водорода при 20 °С. 5. 1. 2. Как изменится внутренняя энергия 500 г кислорода при его нагревании на 15 °С.
Задачи 1. В одном стакане находится горячая вода, в другом – холодная. В каком случае вода обладает большей внутренней энергией? 2. Спичка воспламеняется при трении ее головки о коробок. Объяснить это явление. 3. Объяснить возрастание скорости диффузии с повышением температуры. 4. Почему радиаторы центрального отопления ставят обычно под окнами? 5. Почему зимой на улице металл на ощупь кажется холоднее дерева? 6. В стакан налит горячий чай. Как осуществляется теплообмен между чаем и стенками стакана? 7. Приведите примеры изменения внутренней энергии тела в процессе теплообмена 8. Почему в безветрие пламя свечи устанавливается вертикально? 9. Зачем канализационные и водопроводные трубы зарывают в землю на значительную глубину? 5. 1. 1 Найдите внутреннюю энергию 5 моль водорода при 20 °С. 5. 1. 2. Как изменится внутренняя энергия 500 г кислорода при его нагревании на 15 °С.
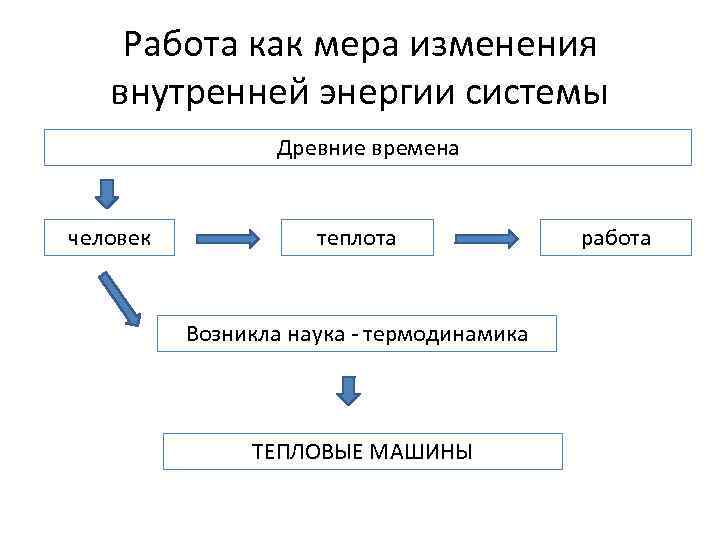 Работа как мера изменения внутренней энергии системы Древние времена человек теплота Возникла наука - термодинамика ТЕПЛОВЫЕ МАШИНЫ работа
Работа как мера изменения внутренней энергии системы Древние времена человек теплота Возникла наука - термодинамика ТЕПЛОВЫЕ МАШИНЫ работа
 Работа как мера изменения внутренней энергии системы Тепловая машина Джеймс Уатт (Ватт) – шотландский изобретатель, создатель универсального парового двигателя. Джеймс Уатт 19. 01. 1736 г. – 19. 08. 1819 г. Исследовал свойства водяного пара, в частности зависимость температуры насыщенного пара от давления. Детальное изучение паровой машины Ньюкомена привело его к введению в неё многих усовершенствований.
Работа как мера изменения внутренней энергии системы Тепловая машина Джеймс Уатт (Ватт) – шотландский изобретатель, создатель универсального парового двигателя. Джеймс Уатт 19. 01. 1736 г. – 19. 08. 1819 г. Исследовал свойства водяного пара, в частности зависимость температуры насыщенного пара от давления. Детальное изучение паровой машины Ньюкомена привело его к введению в неё многих усовершенствований.
 Работа как мера изменения внутренней энергии системы Схема уаттовской паровой машины двойного действия
Работа как мера изменения внутренней энергии системы Схема уаттовской паровой машины двойного действия
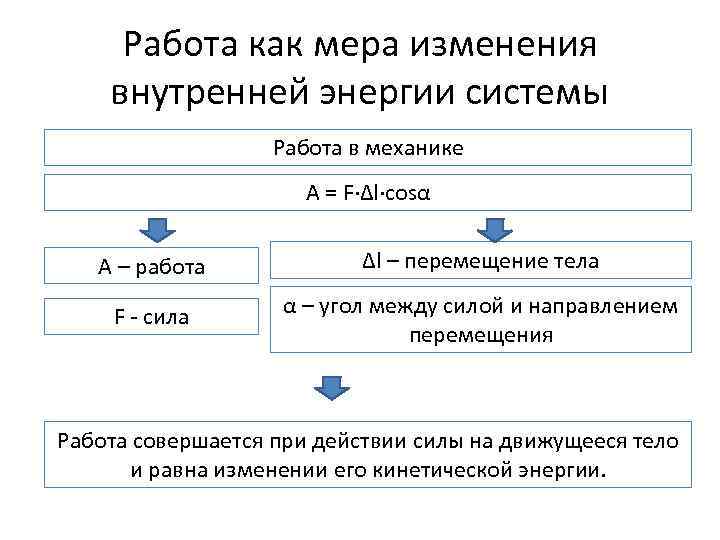 Работа как мера изменения внутренней энергии системы Работа в механике A = F∙∆l∙cosα A – работа ∆l – перемещение тела F - сила α – угол между силой и направлением перемещения Работа совершается при действии силы на движущееся тело и равна изменении его кинетической энергии.
Работа как мера изменения внутренней энергии системы Работа в механике A = F∙∆l∙cosα A – работа ∆l – перемещение тела F - сила α – угол между силой и направлением перемещения Работа совершается при действии силы на движущееся тело и равна изменении его кинетической энергии.
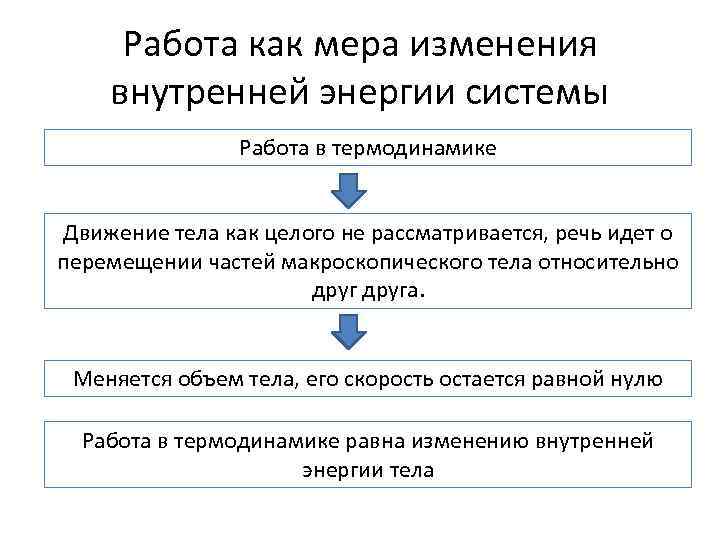 Работа как мера изменения внутренней энергии системы Работа в термодинамике Движение тела как целого не рассматривается, речь идет о перемещении частей макроскопического тела относительно друга. Меняется объем тела, его скорость остается равной нулю Работа в термодинамике равна изменению внутренней энергии тела
Работа как мера изменения внутренней энергии системы Работа в термодинамике Движение тела как целого не рассматривается, речь идет о перемещении частей макроскопического тела относительно друга. Меняется объем тела, его скорость остается равной нулю Работа в термодинамике равна изменению внутренней энергии тела
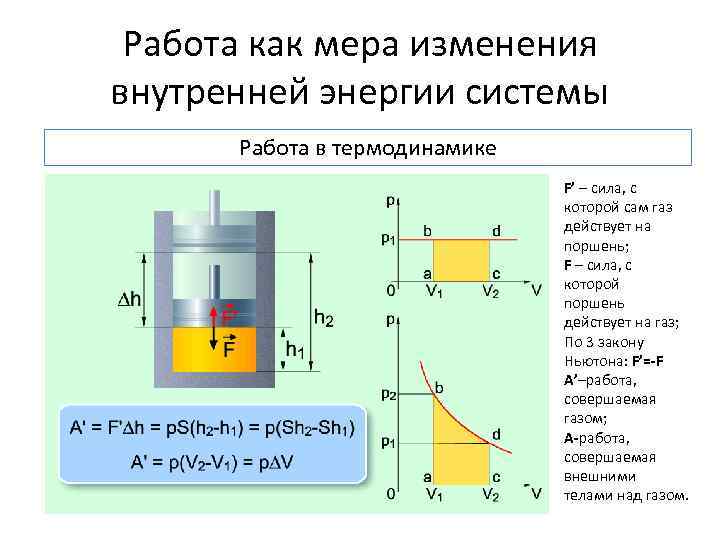 Работа как мера изменения внутренней энергии системы Работа в термодинамике F’ – сила, с которой сам газ действует на поршень; F – сила, с которой поршень действует на газ; По 3 закону Ньютона: F’=-F А’–работа, совершаемая газом; A-работа, совершаемая внешними телами над газом.
Работа как мера изменения внутренней энергии системы Работа в термодинамике F’ – сила, с которой сам газ действует на поршень; F – сила, с которой поршень действует на газ; По 3 закону Ньютона: F’=-F А’–работа, совершаемая газом; A-работа, совершаемая внешними телами над газом.
 Работа как мера изменения внутренней энергии системы Работа в термодинамике A’ = p∙∆V – работа, совершаемая газом. Положительная. A = - p∙∆V – работа, совершаемая внешними телами над газом. Отрицательная.
Работа как мера изменения внутренней энергии системы Работа в термодинамике A’ = p∙∆V – работа, совершаемая газом. Положительная. A = - p∙∆V – работа, совершаемая внешними телами над газом. Отрицательная.
 Домашнее задание
Домашнее задание


