Внеклет_матрикс_2015_Горбачева.ppt
- Количество слайдов: 69

Внеклеточный матрикс и цитоскелет

Гликокаликс (надмембранный компонент, матрикс) В состав гликокаликса входят олигосахариды, протеогликаны, гликопротеиды, гиалуроновая кислота, фибронектин, коллаген, разнообразные ферменты и катионы. Матрикс в соединительной ткани формируют два главных класса макромолекул (1) полисахариды гликозаминогликаны, ковалентно сшитые с белком и формирующие протеогликаны, (2) фибриллярные белки, например коллаген. обычно

внеклеточный матрикс соединительных тканей занимает гораздо больший объем и принимает разнообразные формы Стекловидное тело глаза состоит в Кожа и кровеносные сосуды эластичны основном из желатиновых из-за многочисленных эластичных полисахаридов с несколькими волокон. волокнами Сухожилья, связки - из массивных коллагеновых волокон с относительно небольшим количеством клеток. Состав матрикса определяет свойства ткани Сухожилия обладают большой прочностью на растяжение , в связи с высокой плотностью коллагеновых волокон. Кость несжимаема и жесткая из-за кальцинированная коллагеновой матрицы Самый простой тип внеклеточного матрикса - Базальная мембрана

Фибробласты синтезируют и секретируют макромолекулы, которые образуют внеклеточный матрикс. Фибробласты и экстраклеточный актин В специализированных соединительных тканях (хрящ, кость) компоненты матрикса секеретируют особые клетки, подобные фибробластам и имеющие собственные названия: например, хрящ образуют хондробласты, а кость — остеобласты.

Функции гликокаликса 1. Функции направлены на клеточную адгезию и межклеточные взаимодействия. 2. Гликокаликс способен ограничить доступ определенных молекул к собственно мембране. 3. Гликокаликс является передатчиком механических воздействий (в первую очередь, давления) на клетку, он определяет характер и силу этих воздействий и вызывает адекватную перестройку клеточной структуры и ее функций. В процессе механопередачи участвуют гепаран-сульфат и гиалуроновая кислота. 4. Контроль клеточного микроокружения. Закрепление (docking) за гликокаликс указанных молекул может влиять на локальное микроокружение несколькими способами: А) Связывание рецепторов или ферментов и их лигандов с гликокаликсом ведет к локальному повышению их концентрации, Б) Связывание химических соединений, входящих в состав промежуточного вещества соединительной ткани и плазмы крови, с гликокаликсом ведет к образованию их локального концентрационного градиента, В) Прикрепление (docking) к гликокаликсу ферментов и их агонистов или ингибиторов обеспечивает защиту функциональной активности клетки Г) Гликокаликс связывает катионы Na+, Ca 2+ и K+.
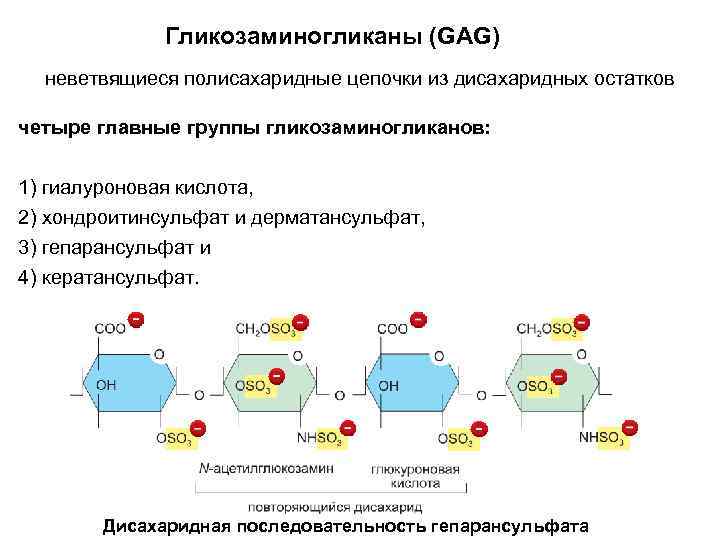
Гликозаминогликаны (GAG) неветвящиеся полисахаридные цепочки из дисахаридных остатков четыре главные группы гликозаминогликанов: 1) гиалуроновая кислота, 2) хондроитинсульфат и дерматансульфат, 3) гепарансульфат и 4) кератансульфат. Дисахаридная последовательность гепарансульфата

Молекулы протеогликанов в тканях образуют гидратированное гелеобразное «основное вещество» Полисахаридный гель обеспечивает механическое сопротивление ткани Коллагеновые волокна усиливают матрикс и упорядочивают его, а другие фибриллярные белки, на пример эластин, придают ему упругость. Белки матрикса помогают клеткам достичь своего места назначения, осесть в нем и дифференцироваться.
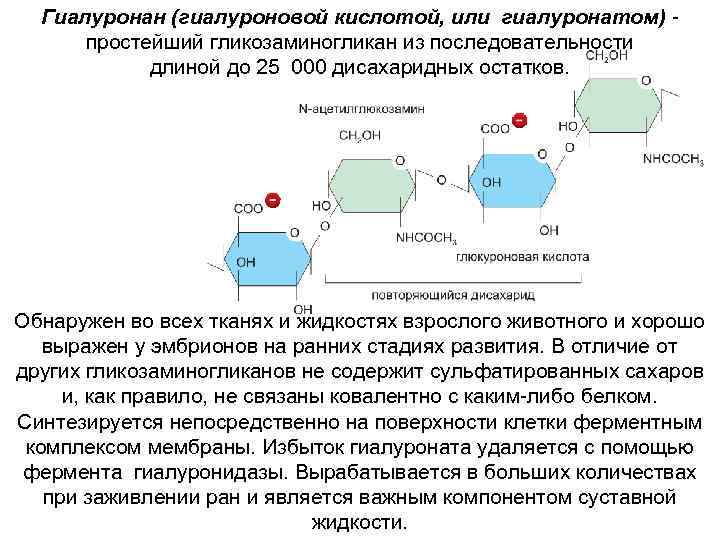
Гиалуронан (гиалуроновой кислотой, или гиалуронатом) простейший гликозаминогликан из последовательности длиной до 25 000 дисахаридных остатков. Обнаружен во всех тканях и жидкостях взрослого животного и хорошо выражен у эмбрионов на ранних стадиях развития. В отличие от других гликозаминогликанов не содержит сульфатированных сахаров и, как правило, не связаны ковалентно с каким-либо белком. Синтезируется непосредственно на поверхности клетки ферментным комплексом мембраны. Избыток гиалуроната удаляется с помощью фермента гиалуронидазы. Вырабатывается в больших количествах при заживлении ран и является важным компонентом суставной жидкости.
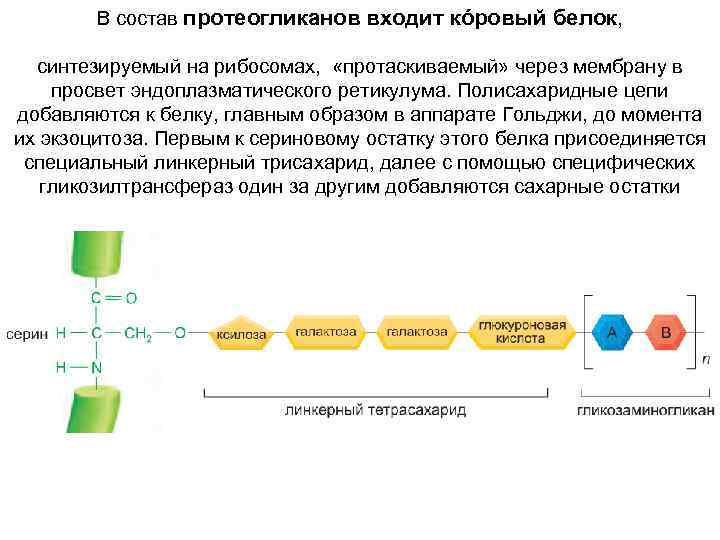
В состав протеогликанов входит кóровый белок, синтезируемый на рибосомах, «протаскиваемый» через мембрану в просвет эндоплазматического ретикулума. Полисахаридные цепи добавляются к белку, главным образом в аппарате Гольджи, до момента их экзоцитоза. Первым к сериновому остатку этого белка присоединяется специальный линкерный трисахарид, далее с помощью специфических гликозилтрансфераз один за другим добавляются сахарные остатки

Протеогликаны матрикса с малой (декорин) и большой (аггрекан) молекулярными массами.

Кóровые белки обладают сходными характерными доменами, например, LINK-доменом, участвующим в связывании гликозаминогликановых цепочек.
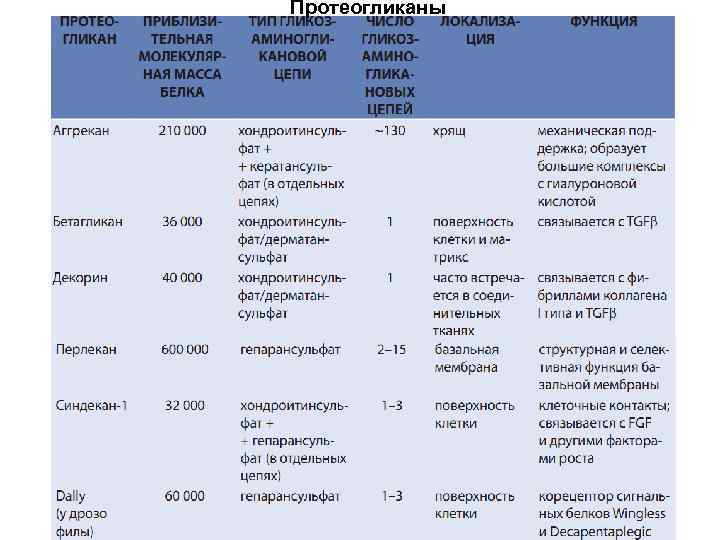
Протеогликаны

Внеклеточный матрикс механическая поддержка тканей многоклеточных организмов. Основной биополимер животные белок коллаген растения полисахарид целлюлоза фибробласты секретируют белковые субъединицы коллагеновых фибрилл и эластических волокон , а также адгезионные белки и сложные полисахариды , которые усиливают белковые волокна внеклеточного матрикса.
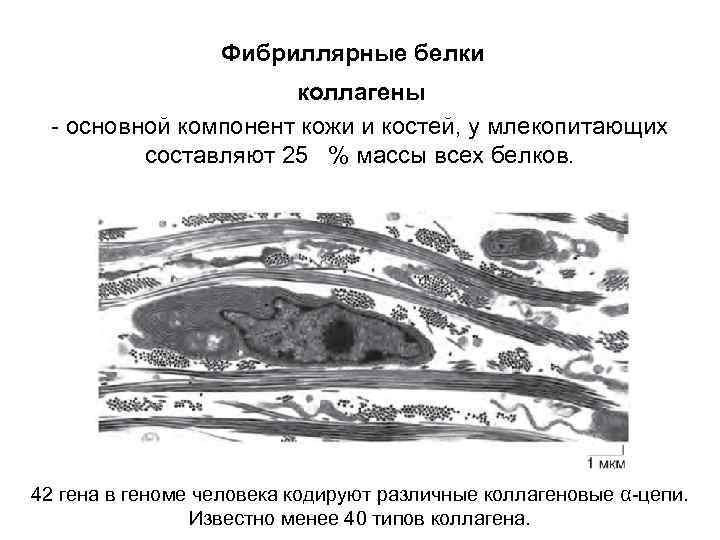
Фибриллярные белки коллагены - основной компонент кожи и костей, у млекопитающих составляют 25 % массы всех белков. 42 гена в геноме человека кодируют различные коллагеновые α-цепи. Известно менее 40 типов коллагена.
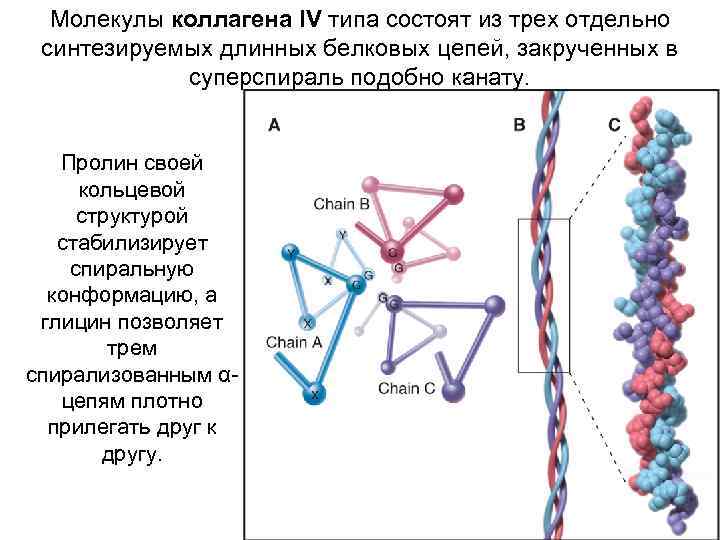
Молекулы коллагена IV типа состоят из трех отдельно синтезируемых длинных белковых цепей, закрученных в суперспираль подобно канату. Пролин своей кольцевой структурой стабилизирует спиральную конформацию, а глицин позволяет трем спирализованным αцепям плотно прилегать друг к другу.
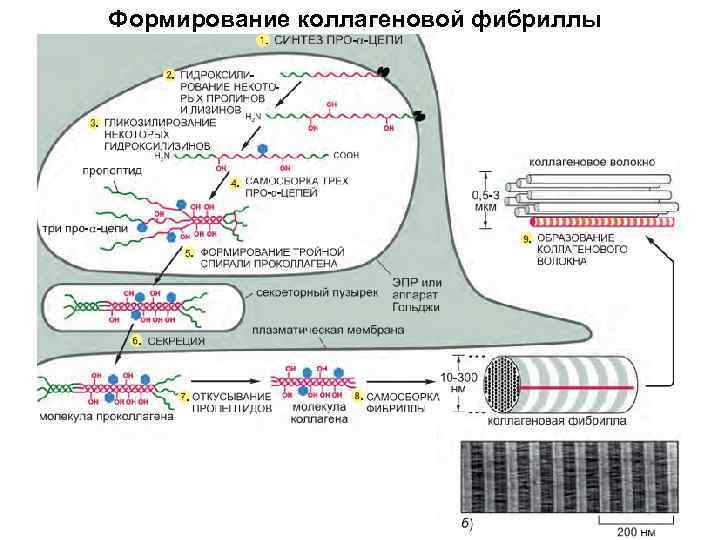
Формирование коллагеновой фибриллы
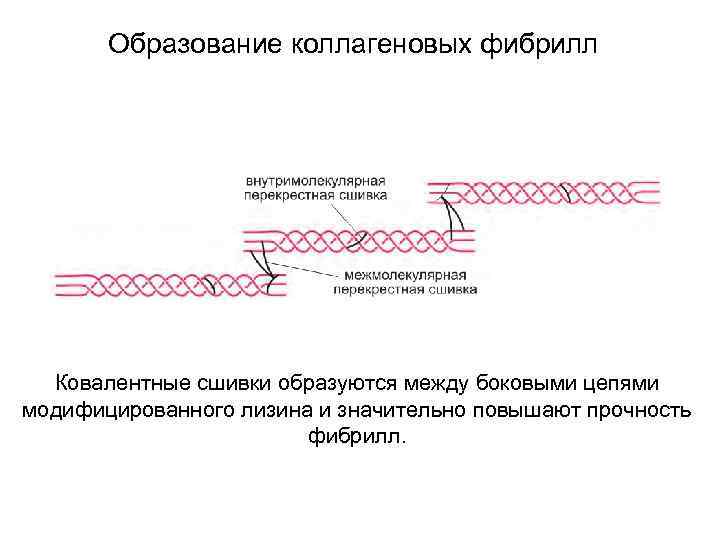
Образование коллагеновых фибрилл Ковалентные сшивки образуются между боковыми цепями модифицированного лизина и значительно повышают прочность фибрилл.

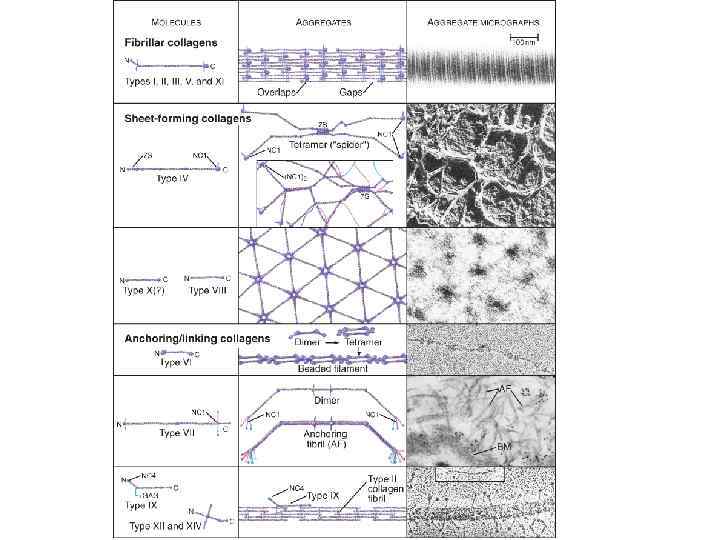
Коллаген I типа (фибриллярный) - основной коллаген кожи и костной ткани. Коллагены IX и XII типов ассоциированы с фибриллами, находятся на поверхности коллагеновых фибрилл. Они связывают фибриллы друг с другом и с другими компонентами внеклеточного матрикса. Коллаген IV типа образует сети и формирует основную часть базальных мембран. Коллаген VII типа образует димеры, которые составляют якорные фибриллы, которые прикрепляют базальную мембрану многослойного эпителия к лежащей под ним соединительной ткани. Коллаген XVII типа имеет трансмембранный домен и обнаружен в полудесмосомах. Коллаген XVIII типа является кóровым белком протеогликанов в базальных мембранах.
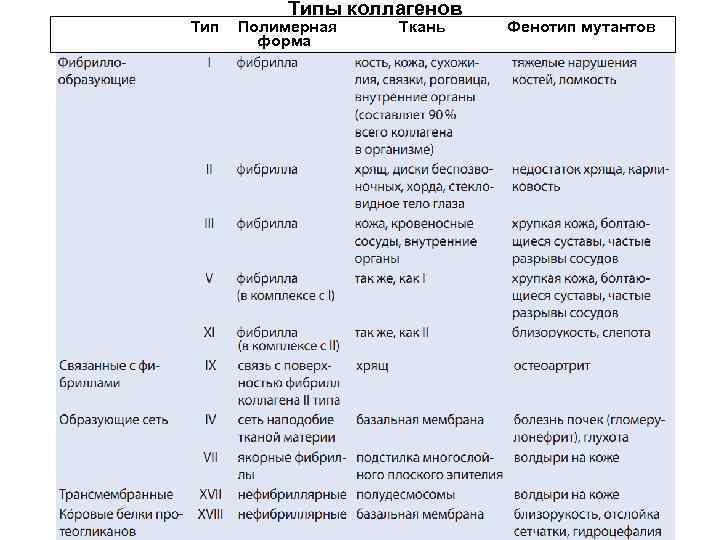
Тип Типы коллагенов Полимерная форма Ткань Фенотип мутантов
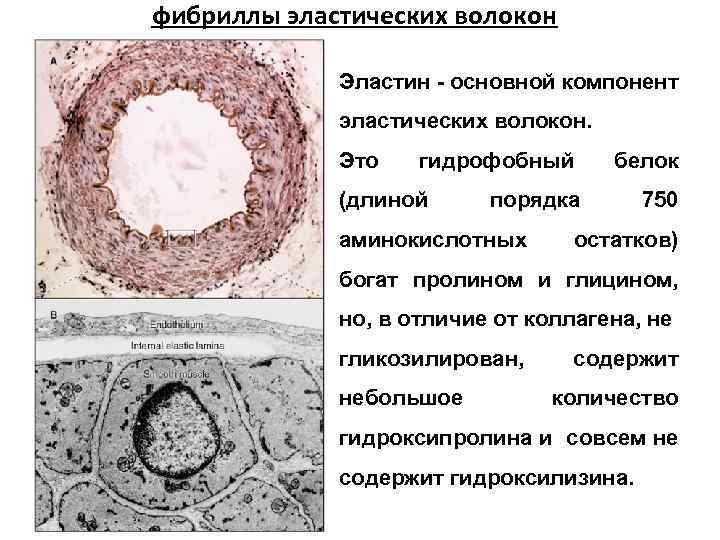
фибриллы эластических волокон Эластин - основной компонент эластических волокон. Это гидрофобный (длиной белок порядка аминокислотных 750 остатков) богат пролином и глицином, но, в отличие от коллагена, не гликозилирован, небольшое содержит количество гидроксипролина и совсем не содержит гидроксилизина.
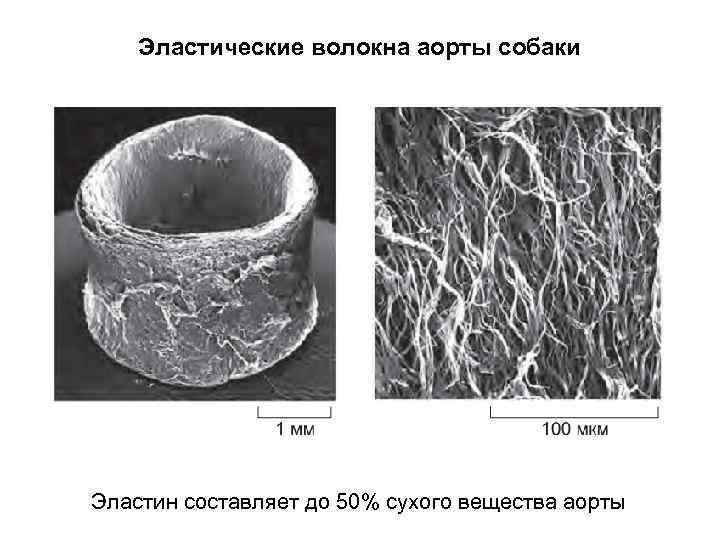
Эластические волокна аорты собаки Эластин составляет до 50% сухого вещества аорты
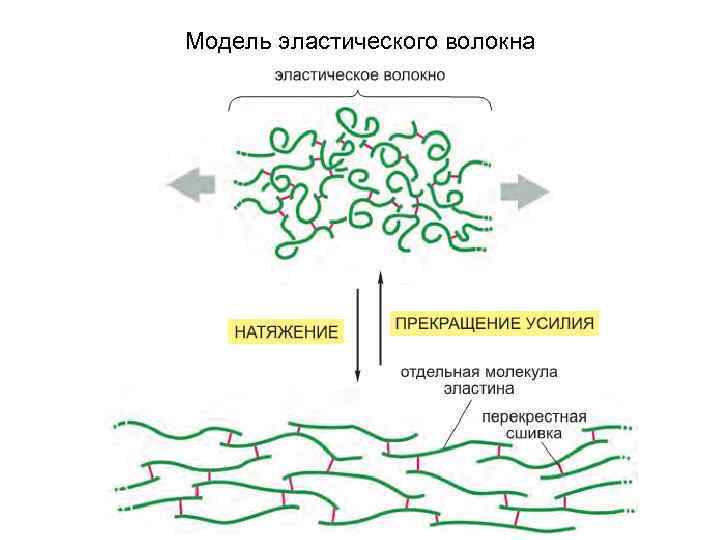
Модель эластического волокна
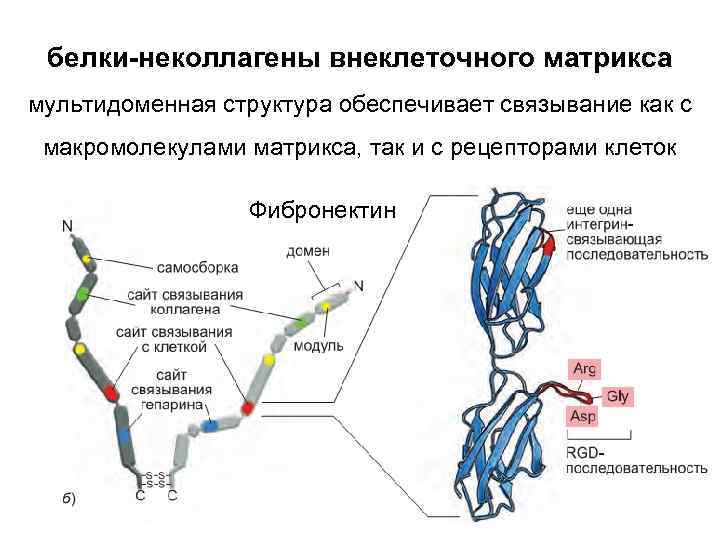
белки-неколлагены внеклеточного матрикса мультидоменная структура обеспечивает связывание как с макромолекулами матрикса, так и с рецепторами клеток Фибронектин
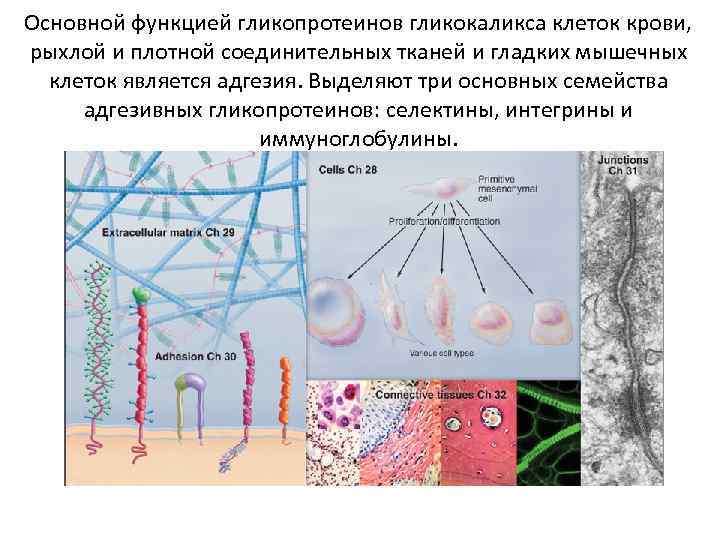
Основной функцией гликопротеинов гликокаликса клеток крови, рыхлой и плотной соединительных тканей и гладких мышечных клеток является адгезия. Выделяют три основных семейства адгезивных гликопротеинов: селектины, интегрины и иммуноглобулины.

Figure 28 -1 CONNECTIVE TISSUE CELLS. A, Indigenous connective tissue cells all originate from a stem cell called a primitive mesenchymal cell. B, Connective tissue near a small blood vessel showing indigenous cells in pink and immigrant cells in green. Poly, polymorphonuclear leukocyte

четыре семейства адгезивных белков Ig. CAMs , кадгерины , интегрины и селектины , составляют большую часть клеточной адгезии Ig. CAMs и кадгерины специфически взаимодействуют с дополнительными белками на поверхности клеток -партнеров. Большинство интегринов связываются с внеклеточными матричными молекулами. Селектины взаимодействуют с гликопротеинами , называемыми муцинами на поверхности клетки примеры динамичной, селективной адгезии : адгезия тромбоцитов друг к другу во время ремонта повреждения мелких кровеносных сосудов и свертывании крови и адгезии лейкоцитов к эндотелиальных клеток, выстилающих кровеносные сосуды воспаленных тканей
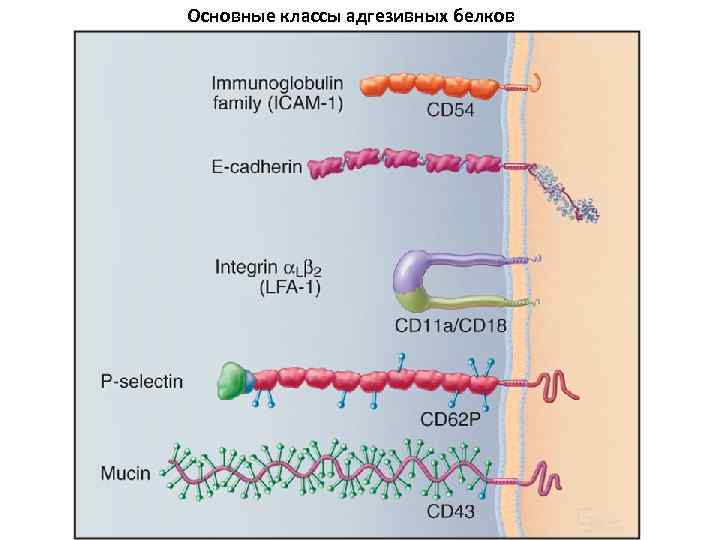
Основные классы адгезивных белков

Ig. CAMs - иммуноглобулины
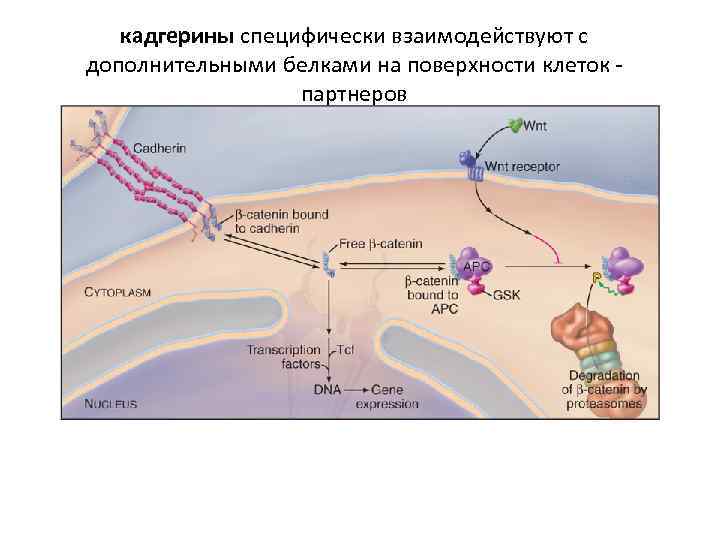
кадгерины специфически взаимодействуют с дополнительными белками на поверхности клеток партнеров

Разные конформации интегринов

Контакты эпителиальной клетки с экстраклеточным матриксом
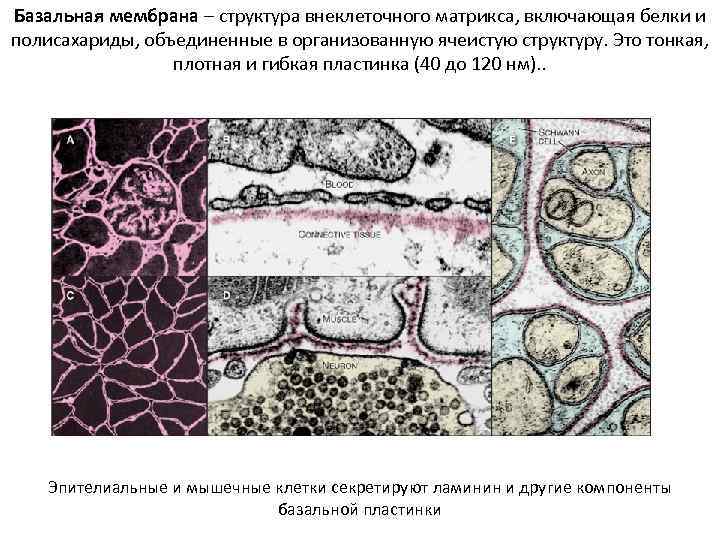
Базальная мембрана – структура внеклеточного матрикса, включающая белки и полисахариды, объединенные в организованную ячеистую структуру. Это тонкая, плотная и гибкая пластинка (40 до 120 нм). . Эпителиальные и мышечные клетки секретируют ламинин и другие компоненты базальной пластинки
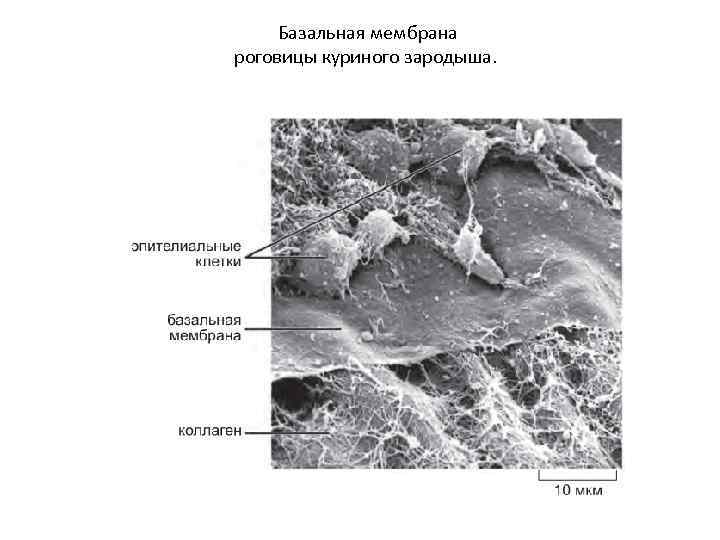
Базальная мембрана роговицы куриного зародыша.

Базальная мембрана подстилает все эпителии, окружает отдельные мышечные клетки, нервные клетки вне ЦНС, клетки жировой ткани и шванновские клетки, выступает селективным фильтром в почечных канальцах. Таким образом, базальная мембрана отделяет эти клетки от окружающей их соединительной ткани, а также устанавливает механическую связь между ними или служит полупроницаемым фильтром
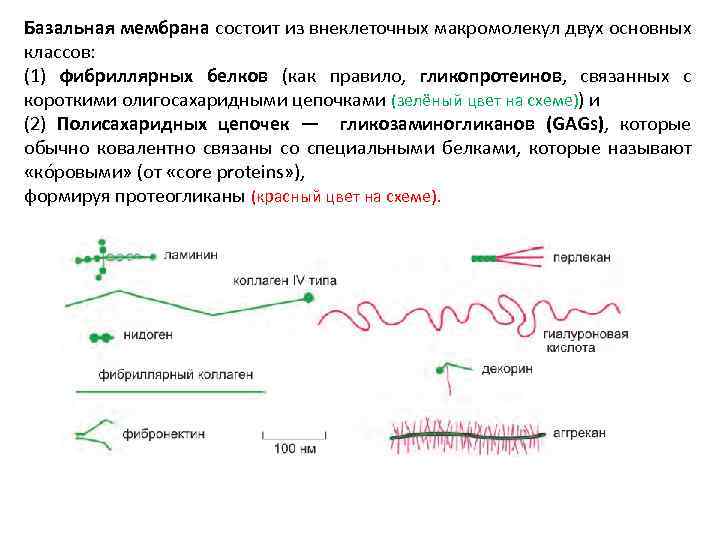
Базальная мембрана состоит из внеклеточных макромолекул двух основных классов: (1) фибриллярных белков (как правило, гликопротеинов, связанных с короткими олигосахаридными цепочками (зелёный цвет на схеме)) и (2) Полисахаридных цепочек — гликозаминогликанов (GAGs), которые обычно ковалентно связаны со специальными белками, которые называют «кóровыми» (от «core proteins» ), формируя протеогликаны (красный цвет на схеме).
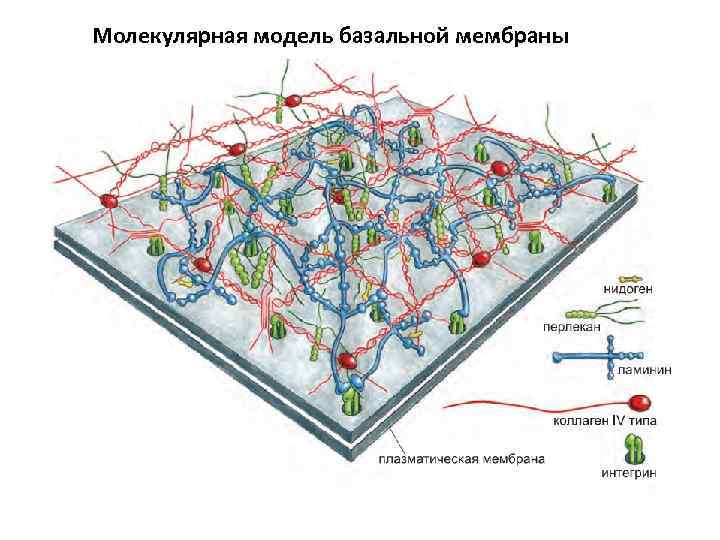
Молекулярная модель базальной мембраны
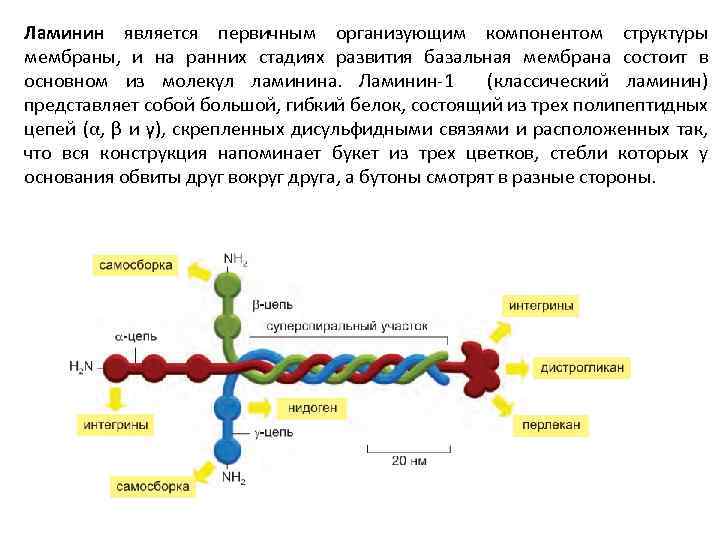
Ламинин является первичным организующим компонентом структуры мембраны, и на ранних стадиях развития базальная мембрана состоит в основном из молекул ламинина. Ламинин-1 (классический ламинин) представляет собой большой, гибкий белок, состоящий из трех полипептидных цепей (α, β и γ), скрепленных дисульфидными связями и расположенных так, что вся конструкция напоминает букет из трех цветков, стебли которых у основания обвиты друг вокруг друга, а бутоны смотрят в разные стороны.
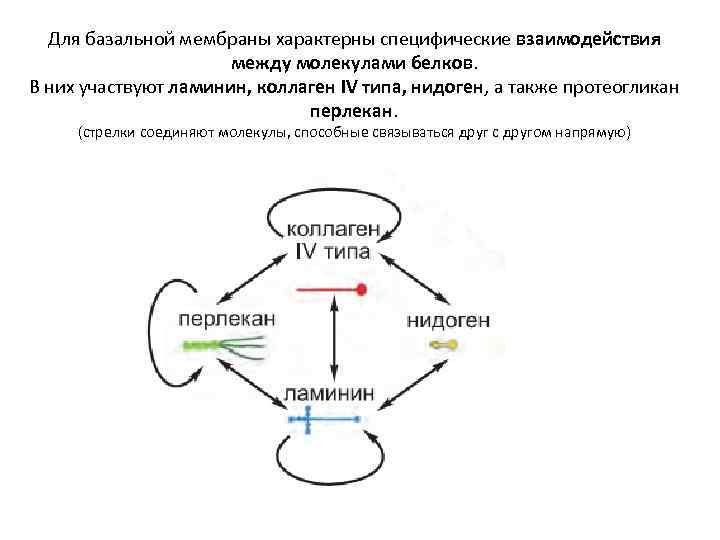
Для базальной мембраны характерны специфические взаимодействия между молекулами белков. В них участвуют ламинин, коллаген IV типа, нидоген, а также протеогликан перлекан. (стрелки соединяют молекулы, способные связываться друг с другом напрямую)

Однако отличие их состоит в том, что их тройная спиральная структура на более чем двадцати участках прерывается, обеспечивая гибкость. Коллаген IV типа придает прочность на разрыв.

Молекулы ламинина, образующие начальную плоскую структуру, сначала соединяются друг с другом, будучи связанными с рецепторами на поверхности клеток, которые их вырабатывают. Эти рецепторы представителями семейства интегринов; другим важным типом ламининовых рецепторов является дистрогликан — протеогликан, чей кóровый белок пронизывает мембрану, а гликозаминогликановые полисахаридные цепи находятся во внеклеточном пространстве. Все эти рецепторы создают структуру базальной мембраны: они фиксируют основания молекул ламинина. Молекулы коллагена IV типа также участвуют в образовании этой структуры, объединяясь в плоскую ячеистую сеть, являющуюся важнейшим компонентом всех зрелых базальных мембран. Коллагеновые и ламининовые сети в сформировавшейся базальной мембране связаны посредством белка нидогена и большого гепарансульфат-содержащего протеогликана перлекана.

Базальные мембраны служат : §механической опорой; §формируют границу между эпителием и соединительной тканью §способствуют их сцеплению друг с другом §выступают в роли фильтров в почках §действуют как барьеры, удерживающие клетки на своем месте; §влияют на полярность клеток и их дифференцировку; §направляют миграцию клеток; §участвуют в образовании таких сложных структур, как нервно-мышечные синапсы. §участвуют в процессах регенерации при повреждении.

Внеклеточный матрикс оказывает влияние на клетки в основном через трансмембранные белки клеточной адгезии, действующие как рецепторы матрикса. Эти рецепторы связывают матрикс, находящийся вне клетки, с внутренним цитоскелетом клетки, однако их роль не сводится к простому механическому прикреплению. Через них компоненты матрикса могут влиять практически на любой аспект поведения клетки. Основными такими рецепторами являются интегрины.

Интегрины (24 формы) – трансмембранные гетеродимеры, связанные с цитоскелетом Структура активной молекулы интегрина, связывающей внеклеточный матрикс с актиновым цитоскелетом.

Большая часть выраженных контактов клетки с матриксом представляет собой полудесмосому, в составе которой особый тип интегрина (α 6β 4) связывает клетки с ламинином базальной мембраны.

Изменение конформации молекулы интегрина при связывании лиганда.

Некоторые типы интегринов

Интегрины (как и другие адгезивные молекулы) отличаются от рецепторов гормонов и других внеклеточных растворимых сигнальных молекул более низким сродством к лиганду и высокой концентрации на поверхности клеток (в 10– 100 раз выше). Также работает принцип «застежки» . Прочное соединение обеспечивается кластеризацией интегринов, формирующих бляшку, на которой заякорено множество филаментов цитоскелета, так же как в случае десмосом в эпидермисе или фокального контакта между фибробластом и днищем чашки Петри.

Сигнальная активность интегринов связана с цитоплазматической тирозинкиназой, называемой протеинкиназой фокальной адгезии (focal adhesion kinase, FAK). При кластеризации интегринов в точках соединения клетки с матриксом FAK связывается внутриклеточными якорными белками, например, талином (связывающимся с βсубъединицей интегрина) или паксиллином, который связывается с одним из видов α-субъединиц. Кластеризованные молекулы FAK взаимно фосфорилируют друга, формируя сайт связывания цитоплазматических тирозинкиназ семейства Src. Эти киназы дополнительно фосфорилируют FAK по еще одному тирозину, создавая сайт связывания для разнообразных внутриклеточных сигнальных белков. Так, внешний сигнал от интегринов через FAK и киназы семейства Src передается внутрь клетки.
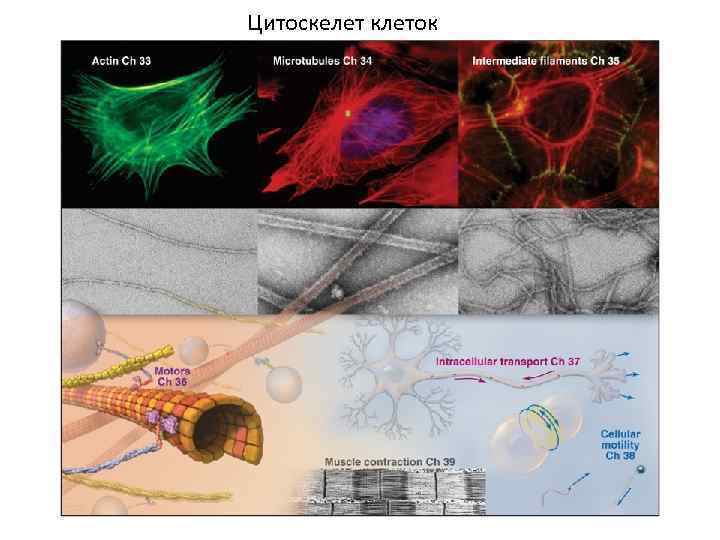
Цитоскелет клеток
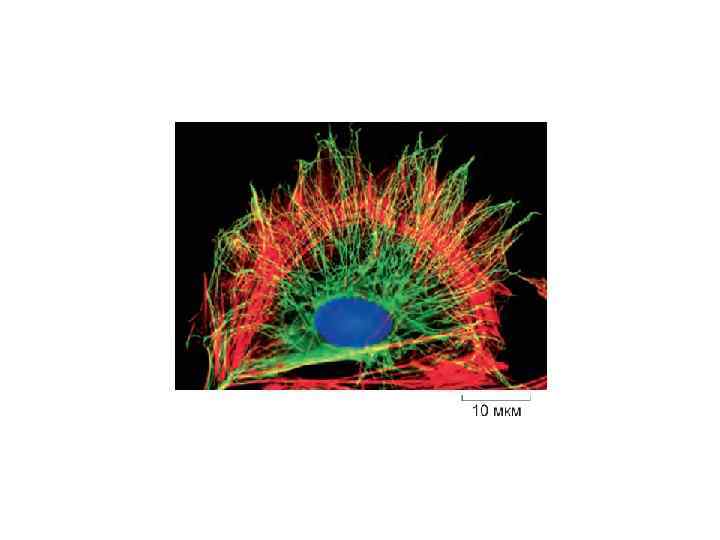
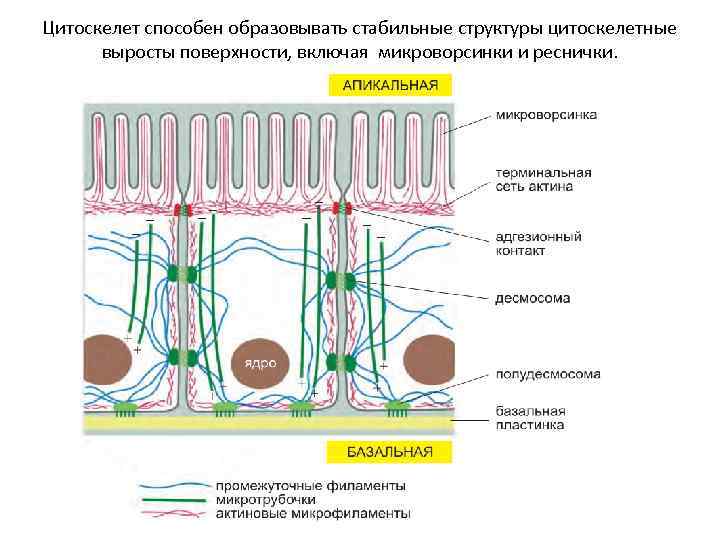
Цитоскелет способен образовывать стабильные структуры цитоскелетные выросты поверхности, включая микроворсинки и реснички.
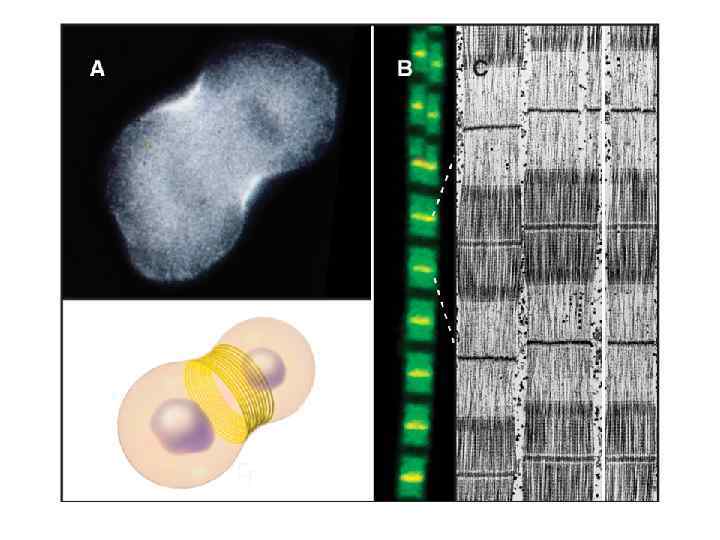
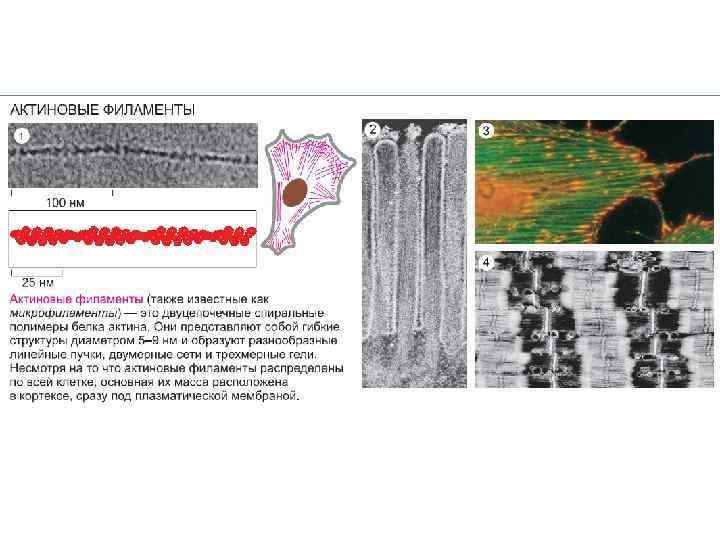

Актиновые филаменты участвуют в формировании цитоскелета

СПЕКРИН-АНКИРИНОВАЯ СИСТЕМА Второй (после актина) по представленности составляющей частью подмембранного компонента является система белков, основную роль в которой играют белки спектрин и анкирин. Спектриновые нити в этом тандеме выполняют скелетную функцию, а анкирин обеспечивает заякоривание спектриновых нитей за плазмолеммальные интегральные белки. Основной функцией, выполняемой спектрин-анкириновой системой, является кластеринг ансамблей ионных каналов и белков, ответственных за клеточную адгезию, в составе микро- и макродоменов цитолеммы.
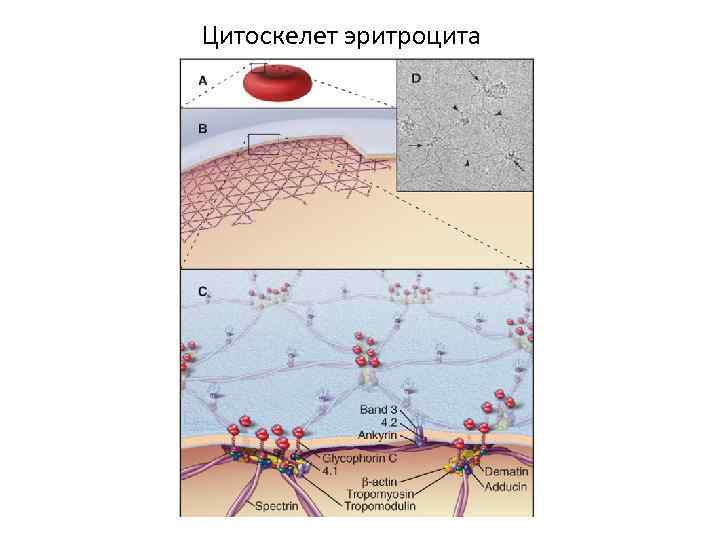
Цитоскелет эритроцита

СПЕКРИН-АНКИРИНОВАЯ СИСТЕМА представляет собой статичную консерватированную часть субплазмолеммального цитоскелета, обеспечивающую сборку и поддержание в составе определенных участков цитолеммы физиологически важных доменов. Спектриновых волокна построены из многочисленных, однотипных, последовательно соединенных триплетов αспиральных участков белковой молекулы (мотифов), называемых спектриновыми повторами. Длина спектринового повтора составляет 106 аминокислот. Структура спектриновых повторов (суперспираль из трех α-спиральных мотифов) и связь α-спиральных мотифов между собой внутри каждого отдельного повтора обеспечивают гибкость и растяжимость спектриновому полимеру. По ряду признаков (в первую очередь, наличию специфичных доменов) спектриновые субъединицы подразделяются на α- и β-субъединицы
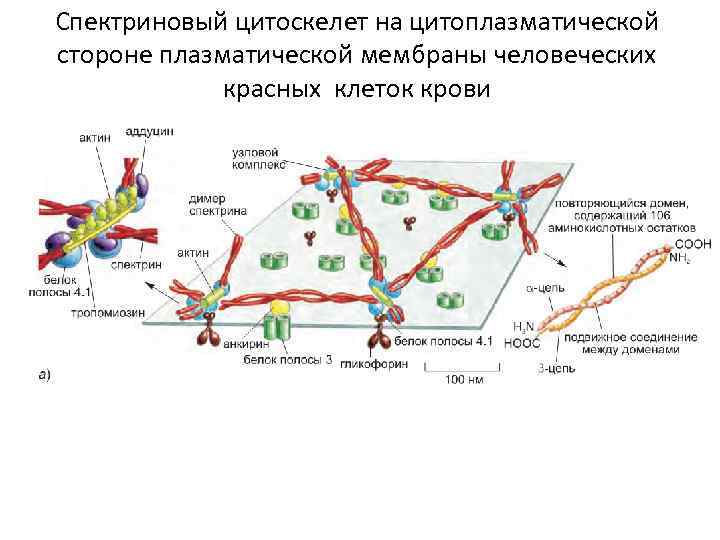
Спектриновый цитоскелет на цитоплазматической стороне плазматической мембраны человеческих красных клеток крови
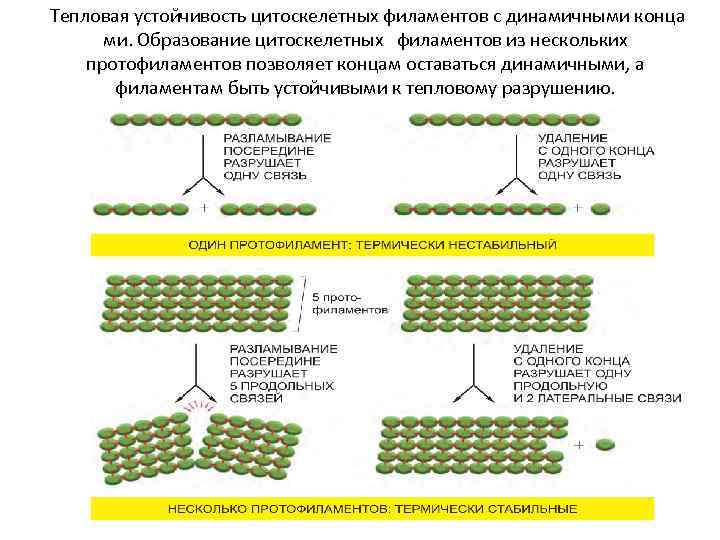
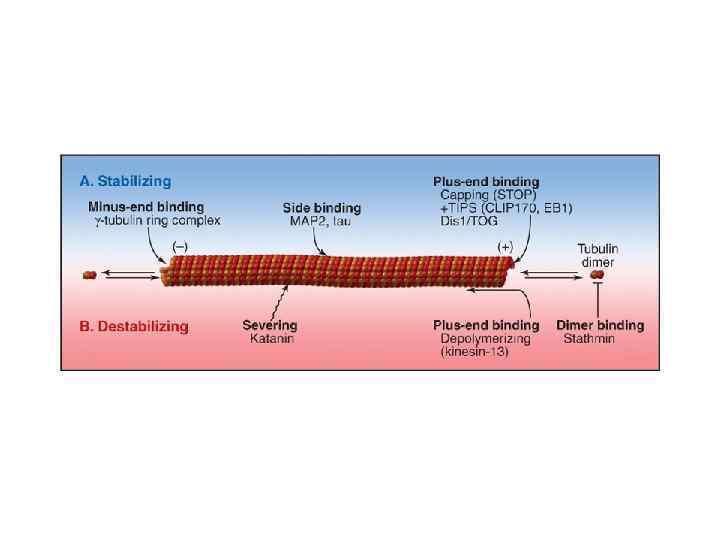
Тепловая устойчивость цитоскелетных филаментов с динамичными конца ми. Образование цитоскелетных филаментов из нескольких протофиламентов позволяет концам оставаться динамичными, а филаментам быть устойчивыми к тепловому разрушению.

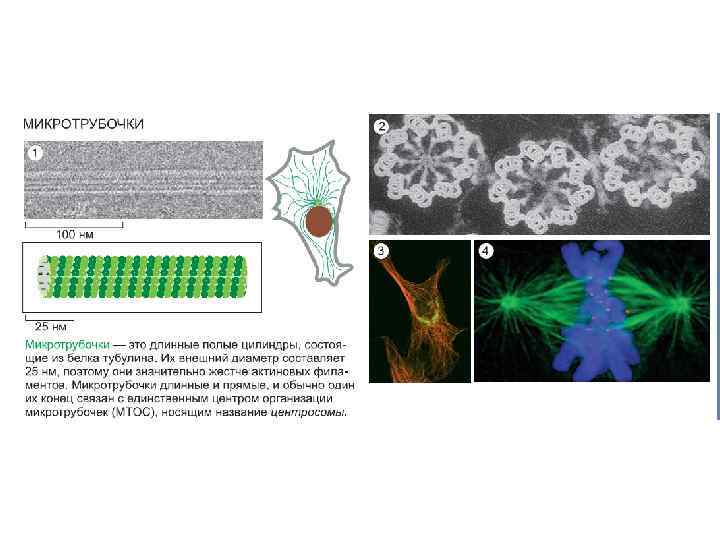
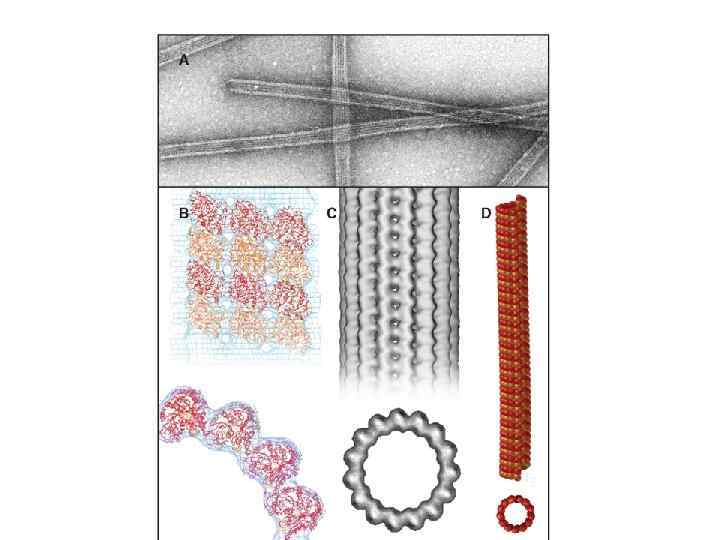
Структура микротрубочки и ее субъединицы.


Внеклет_матрикс_2015_Горбачева.ppt