Л 7.pptx
- Количество слайдов: 30
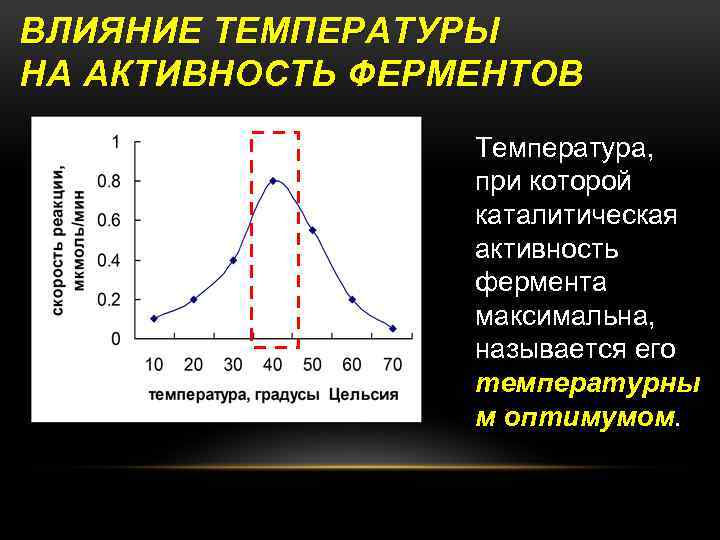 ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ Температура, при которой каталитическая активность фермента максимальна, называется его температурны м оптимумом.
ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ Температура, при которой каталитическая активность фермента максимальна, называется его температурны м оптимумом.
 При увеличении температуры среды выше температурного оптимума активность ферментов уменьшается. Причина – температурная денатурация белка.
При увеличении температуры среды выше температурного оптимума активность ферментов уменьшается. Причина – температурная денатурация белка.
 Температурный оптимум ферментов: животного происхождения - 40 -50 о. С; растительного происхождения - 5060 о. С. Topt папаина = ~80 о. С Topt каталазы = ~5 о. С
Температурный оптимум ферментов: животного происхождения - 40 -50 о. С; растительного происхождения - 5060 о. С. Topt папаина = ~80 о. С Topt каталазы = ~5 о. С
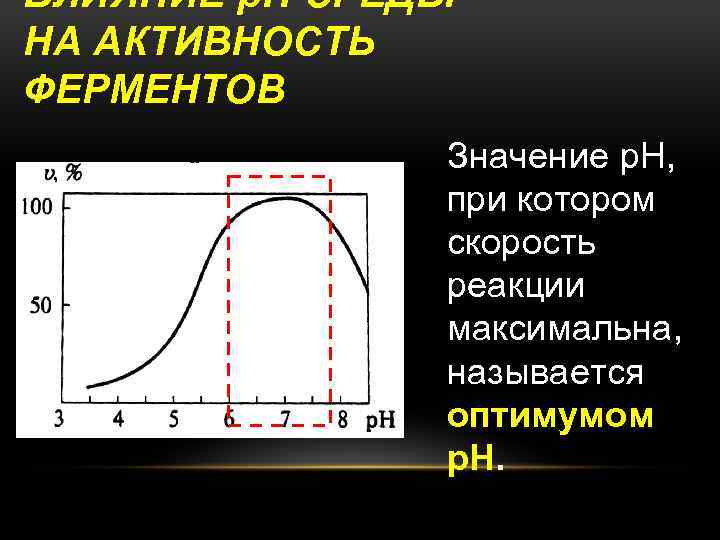 ВЛИЯНИЕ р. Н СРЕДЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ Значение р. Н, при котором скорость реакции максимальна, называется оптимумом р. Н.
ВЛИЯНИЕ р. Н СРЕДЫ НА АКТИВНОСТЬ ФЕРМЕНТОВ Значение р. Н, при котором скорость реакции максимальна, называется оптимумом р. Н.
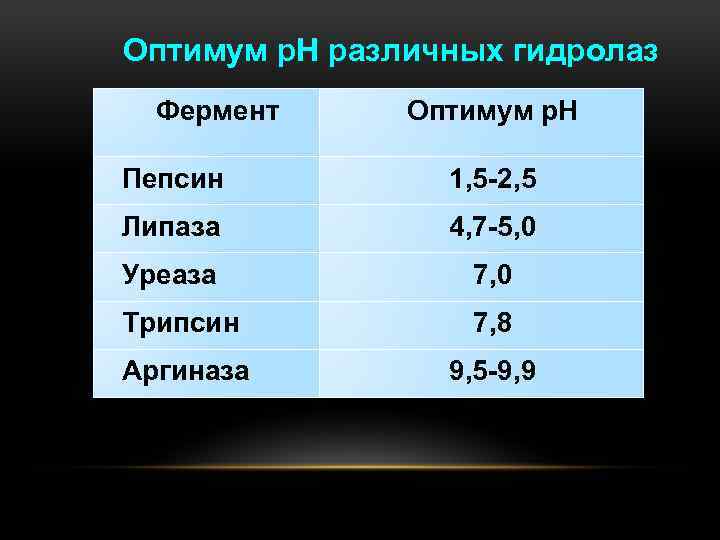 Оптимум р. Н различных гидролаз Фермент Оптимум р. Н Пепсин 1, 5 -2, 5 Липаза 4, 7 -5, 0 Уреаза 7, 0 Трипсин 7, 8 Аргиназа 9, 5 -9, 9
Оптимум р. Н различных гидролаз Фермент Оптимум р. Н Пепсин 1, 5 -2, 5 Липаза 4, 7 -5, 0 Уреаза 7, 0 Трипсин 7, 8 Аргиназа 9, 5 -9, 9
 Чувствительность ферментов к изменению р. Н обусловлено: ü наличием ионогенных групп в активном центре фермента; ü наличием ионогенных групп в молекуле субстрата; ü влиянием р. Н на конформацию ферментв, связь апо- и кофермента, ионное состояние аллостерических регуляторов и ионогенных групп аллостерического центра.
Чувствительность ферментов к изменению р. Н обусловлено: ü наличием ионогенных групп в активном центре фермента; ü наличием ионогенных групп в молекуле субстрата; ü влиянием р. Н на конформацию ферментв, связь апо- и кофермента, ионное состояние аллостерических регуляторов и ионогенных групп аллостерического центра.
 ОРГАНИЗАЦИЯ ФЕРМЕНТОВ В КЛЕТКАХ И ТКАНЯХ
ОРГАНИЗАЦИЯ ФЕРМЕНТОВ В КЛЕТКАХ И ТКАНЯХ
 Органы и ткани многоклеточных организмов отличаются друг от друга по характеру протекающих в них метаболических процессов ü качественным и количественным составом ферментов, ü уровнем активности ферментов.
Органы и ткани многоклеточных организмов отличаются друг от друга по характеру протекающих в них метаболических процессов ü качественным и количественным составом ферментов, ü уровнем активности ферментов.
 ü Фермент: креатинкиназа. Содержится в мышечной ткани. В сыворотке крови в норме содержится в следовых количествах. При повреждении скелетной мускулатуры (мышечная дистрофия) и миокарда (коронарная недостаточность), активность креатинкиназы в крови возрастает в 50 и более раз. ü Фермент: гистидаза. Содержится в печени. Обнаружение активности гистидазы в крови – признак патологии печени (гепатит).
ü Фермент: креатинкиназа. Содержится в мышечной ткани. В сыворотке крови в норме содержится в следовых количествах. При повреждении скелетной мускулатуры (мышечная дистрофия) и миокарда (коронарная недостаточность), активность креатинкиназы в крови возрастает в 50 и более раз. ü Фермент: гистидаза. Содержится в печени. Обнаружение активности гистидазы в крови – признак патологии печени (гепатит).
 ВНУТРИКЛЕТОЧНАЯ ЛОКАЛИЗАЦИЯ ФЕРМЕНТОВ ü ферменты гликолиза, глюконеогенеза, синтеза жирных кислот и холестерина – в цитозоле, ü ферменты цикла Кребса и β-окисления жирных кислот – в матриксе митохондрий, ü ферменты окислительного фосфорилирования – во внутренней мембране митохондрий, ü ферменты репликации и транскрипции – в ядре.
ВНУТРИКЛЕТОЧНАЯ ЛОКАЛИЗАЦИЯ ФЕРМЕНТОВ ü ферменты гликолиза, глюконеогенеза, синтеза жирных кислот и холестерина – в цитозоле, ü ферменты цикла Кребса и β-окисления жирных кислот – в матриксе митохондрий, ü ферменты окислительного фосфорилирования – во внутренней мембране митохондрий, ü ферменты репликации и транскрипции – в ядре.
 Ферменты-маркеры внутриклеточных структур. ü маркеры плазматических мембран - Na+, K+АТФаза и аденилатциклаза; ü маркер цитозоля – лактатдегидрогеназа; ü маркер аппарата Гольджи – галактозилтрансфераза; ü маркер лизосом – кислая фосфатаза; ü маркер пероксисом – каталаза и оксидаза Dаминокислот; ü маркер эндоплазматического ретикулума – глюкозо-6 -фосфатаза и НАДФН-цитохром с – редуктаза; ü маркер митохондрий – глутаматдегидрогеназа.
Ферменты-маркеры внутриклеточных структур. ü маркеры плазматических мембран - Na+, K+АТФаза и аденилатциклаза; ü маркер цитозоля – лактатдегидрогеназа; ü маркер аппарата Гольджи – галактозилтрансфераза; ü маркер лизосом – кислая фосфатаза; ü маркер пероксисом – каталаза и оксидаза Dаминокислот; ü маркер эндоплазматического ретикулума – глюкозо-6 -фосфатаза и НАДФН-цитохром с – редуктаза; ü маркер митохондрий – глутаматдегидрогеназа.
 ФЕРМЕНТНЫЕ СИСТЕМЫ И ПРИНЦИПЫ ИХ ОРГАНИЗАЦИИ Ферментная система (мультимолекулярный ферментный комплекс) – совокупность ферментов, катализирующих последовательные стадии превращения определенного субстрата: ü пируватдегидрогеназная и αкетоглутаратдегидро-геназная системы окислительного декарбоксилирования пирувата и α-кетоглутарата животных, ü синтетаза жирных кислот, ü дыхательная цепь митохондрий и хлоропластов.
ФЕРМЕНТНЫЕ СИСТЕМЫ И ПРИНЦИПЫ ИХ ОРГАНИЗАЦИИ Ферментная система (мультимолекулярный ферментный комплекс) – совокупность ферментов, катализирующих последовательные стадии превращения определенного субстрата: ü пируватдегидрогеназная и αкетоглутаратдегидро-геназная системы окислительного декарбоксилирования пирувата и α-кетоглутарата животных, ü синтетаза жирных кислот, ü дыхательная цепь митохондрий и хлоропластов.
 Особенности ферментных систем: ü пространственная и функциональная ассоциация ферментов в комплексе; ü обеспечение ферментной системой определенной последовательности катализируемых реакций (в пространстве и во времени); ü высокая молекулярная масса комплекса (2· 106 - 10· 106 Да).
Особенности ферментных систем: ü пространственная и функциональная ассоциация ферментов в комплексе; ü обеспечение ферментной системой определенной последовательности катализируемых реакций (в пространстве и во времени); ü высокая молекулярная масса комплекса (2· 106 - 10· 106 Да).
 Типы мультиферментных систем: ü Растворимые мультиферментные системы (цитоплазматические). Небольшие молекулы субстратов, обладающие высокой скоростью диффузии, легко переходят от одного фермента к другому. Ферменты метаболических путей.
Типы мультиферментных систем: ü Растворимые мультиферментные системы (цитоплазматические). Небольшие молекулы субстратов, обладающие высокой скоростью диффузии, легко переходят от одного фермента к другому. Ферменты метаболических путей.
 ü Ассоциированные ферменты, функционирующие совместно. Синтетаза жирных кислот – 7 ферментов, молекулы которых объединены в тесно ассоциированный недиссоциирующий комплекс. ü Ферментные системы, связанные с крупными надмолекулярными структурами (например, мембранами). Дыхательная цепь митохондрий.
ü Ассоциированные ферменты, функционирующие совместно. Синтетаза жирных кислот – 7 ферментов, молекулы которых объединены в тесно ассоциированный недиссоциирующий комплекс. ü Ферментные системы, связанные с крупными надмолекулярными структурами (например, мембранами). Дыхательная цепь митохондрий.
 Регуляция функционирования ферментных систем. Ферментные системы поддерживают суммарную скорость превращения первого (исходного) субстрата. Скорость определяется концентрацией конечного продукта – ингибирование по типу обратной связи, или ретроингибирование.
Регуляция функционирования ферментных систем. Ферментные системы поддерживают суммарную скорость превращения первого (исходного) субстрата. Скорость определяется концентрацией конечного продукта – ингибирование по типу обратной связи, или ретроингибирование.
 ВЫДЕЛЕНИЕ И ОЧИСТКА ФЕРМЕНТОВ
ВЫДЕЛЕНИЕ И ОЧИСТКА ФЕРМЕНТОВ
 1 этап: подбор количественного теста для определения активности фермента. 2 этап: выбор источника фермента. 3 этап: перевод фермента в раствор. • разрушение клеточных мембран (гомогенизация; ультразвук, детергенты, замораживаниеотттаивание и др. ) • экстракция буферными растворами (фосфатный (р. Н 4, 5 -9, 2), ацетатный (р. Н 3, 6 -5, 8), цитратный (р. Н 1, 1 -4, 1), цитратно-фосфатный (р. Н 2, 2 -8, 0), трис (7, 2 -9, 8)).
1 этап: подбор количественного теста для определения активности фермента. 2 этап: выбор источника фермента. 3 этап: перевод фермента в раствор. • разрушение клеточных мембран (гомогенизация; ультразвук, детергенты, замораживаниеотттаивание и др. ) • экстракция буферными растворами (фосфатный (р. Н 4, 5 -9, 2), ацетатный (р. Н 3, 6 -5, 8), цитратный (р. Н 1, 1 -4, 1), цитратно-фосфатный (р. Н 2, 2 -8, 0), трис (7, 2 -9, 8)).
 4 этап: очистка полученного раствора фермента от примесей (диализ, методы фракционирования). Методы фракционирования: • изменение р. Н. • нагревание (при работе с термостабильными ферментами). • использование органических растворителей (ацетон). • использование нейтральных солей (высаливание).
4 этап: очистка полученного раствора фермента от примесей (диализ, методы фракционирования). Методы фракционирования: • изменение р. Н. • нагревание (при работе с термостабильными ферментами). • использование органических растворителей (ацетон). • использование нейтральных солей (высаливание).
 5 этап: получение высокоочищенных ферментных препаратов. Хроматографические методы: • 1. Адсорбционная хроматография. • 2. Распределительная хроматография. • 3. Ионообменная хроматография. • 4. Аффинная хроматография (хроматография по сродству). • 5. Гель-хроматография (метод молекулярных сит).
5 этап: получение высокоочищенных ферментных препаратов. Хроматографические методы: • 1. Адсорбционная хроматография. • 2. Распределительная хроматография. • 3. Ионообменная хроматография. • 4. Аффинная хроматография (хроматография по сродству). • 5. Гель-хроматография (метод молекулярных сит).
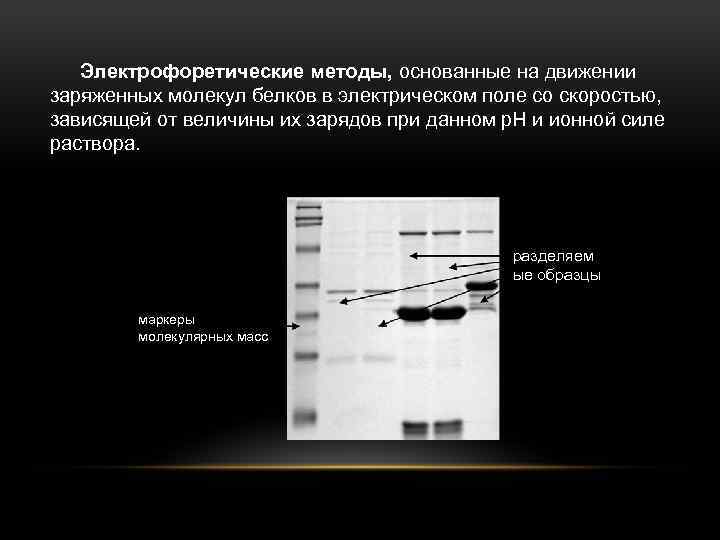 Электрофоретические методы, основанные на движении заряженных молекул белков в электрическом поле со скоростью, зависящей от величины их зарядов при данном р. Н и ионной силе раствора. разделяем ые образцы маркеры молекулярных масс
Электрофоретические методы, основанные на движении заряженных молекул белков в электрическом поле со скоростью, зависящей от величины их зарядов при данном р. Н и ионной силе раствора. разделяем ые образцы маркеры молекулярных масс
 6 этап: хранение очищенных ферментных препаратов. • высушивание (лиофилизация) • замораживание
6 этап: хранение очищенных ферментных препаратов. • высушивание (лиофилизация) • замораживание
 МЕТОДЫ ОЦЕНКИ ГОМОГЕННОСТИ ПОЛУЧЕННОГО ФЕРМЕНТНОГО ПРЕПАРАТА • ультрацентрифугирование в градиенте плотности ; • электрофорез; • изоэлектрическое фокусирование (разделение в градиенте напряжения и градиенте р. Н); • иммунохимические методы (реакция преципитации фермента с соответствующими ему антителами); • определение растворимости белка (растворимость чистого вещества зависит только от температуры, но не зависит от
МЕТОДЫ ОЦЕНКИ ГОМОГЕННОСТИ ПОЛУЧЕННОГО ФЕРМЕНТНОГО ПРЕПАРАТА • ультрацентрифугирование в градиенте плотности ; • электрофорез; • изоэлектрическое фокусирование (разделение в градиенте напряжения и градиенте р. Н); • иммунохимические методы (реакция преципитации фермента с соответствующими ему антителами); • определение растворимости белка (растворимость чистого вещества зависит только от температуры, но не зависит от
 МЕТОДЫ ОПРЕДЕЛЕНИЯ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ 1 КАТАЛ (кат) – количество фермента, способное в течение 1 с обеспечить превращение 1 моля субстрата в стандартных условиях. Единица активности фермента (U, или МЕ) – количество фермента, которое в стандартных условиях катализирует превращение 1 мкмоль субстрата в 1 мин. 1 кат = 6 · 107 МЕ 1 МЕ = 16, 7 нкат
МЕТОДЫ ОПРЕДЕЛЕНИЯ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ 1 КАТАЛ (кат) – количество фермента, способное в течение 1 с обеспечить превращение 1 моля субстрата в стандартных условиях. Единица активности фермента (U, или МЕ) – количество фермента, которое в стандартных условиях катализирует превращение 1 мкмоль субстрата в 1 мин. 1 кат = 6 · 107 МЕ 1 МЕ = 16, 7 нкат
 ü Удельная активность – число единиц ферментативной активности, приходящееся на 1 мг белка (1 мкмоль/мг белка · мин). ü Молекулярная активность – число молей субстрата, которые подвергаются превращению молекулой фермента за 1 мин. ü Активность каталитического центра – число молекул субстрата, которые претерпевают превращение за 1 мин в расчете на 1 каталитический центр. ü Число оборотов фермента – число молекул субстрата, претерпевающих превращение за 1 мин в расчете на 1 молекулу фермента.
ü Удельная активность – число единиц ферментативной активности, приходящееся на 1 мг белка (1 мкмоль/мг белка · мин). ü Молекулярная активность – число молей субстрата, которые подвергаются превращению молекулой фермента за 1 мин. ü Активность каталитического центра – число молекул субстрата, которые претерпевают превращение за 1 мин в расчете на 1 каталитический центр. ü Число оборотов фермента – число молекул субстрата, претерпевающих превращение за 1 мин в расчете на 1 молекулу фермента.
 МЕТОДЫ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ФЕРМЕНТОВ 1. Химические методы отбор проб из реакционной смеси через определенные промежутки времени и определение количества продукта (субстрата) реакции определенными химическими методами. Активность фосфатаз, фосфорилаз, нуклеотидаз – по количеству образующегося Фн. Активность гликозидаз – по количеству образующихся восстанавливающих сахаров.
МЕТОДЫ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ФЕРМЕНТОВ 1. Химические методы отбор проб из реакционной смеси через определенные промежутки времени и определение количества продукта (субстрата) реакции определенными химическими методами. Активность фосфатаз, фосфорилаз, нуклеотидаз – по количеству образующегося Фн. Активность гликозидаз – по количеству образующихся восстанавливающих сахаров.
 2. Поляриметрические методы за ходом реакции следят по изменению величины оптического вращения (накопление оптически активного продукта или убыль субстрата). Фермент сахараза; субстрат – сахароза α, D 20 ºС = + 66, 5º; продукты – глюкоза α, D 20 ºС = + 52, 5º; фруктоза α, D 20 ºС = - 92, 4º
2. Поляриметрические методы за ходом реакции следят по изменению величины оптического вращения (накопление оптически активного продукта или убыль субстрата). Фермент сахараза; субстрат – сахароза α, D 20 ºС = + 66, 5º; продукты – глюкоза α, D 20 ºС = + 52, 5º; фруктоза α, D 20 ºС = - 92, 4º
 3. Хроматографические методы отбор проб из реакционной смеси через определенные промежутки времени и определение содержания веществ с использованием хроматографических методов (разделение, очистка/выделение), т. е. химическое определение наличия продукта (субстрата) реакции. Активность аминотрансфераз, изоферментов цитохрома Р 450 и др.
3. Хроматографические методы отбор проб из реакционной смеси через определенные промежутки времени и определение содержания веществ с использованием хроматографических методов (разделение, очистка/выделение), т. е. химическое определение наличия продукта (субстрата) реакции. Активность аминотрансфераз, изоферментов цитохрома Р 450 и др.
 4. Манометрические методы за ходом реакции наблюдают по изменению давления при образовании или убыли газообразных веществ. глутаматдегидрогеназа Глутамат γ-аминомасляная кислота + СО 2↑ каталаза 2 Н 2 О 2 2 Н 2 О + О 2↑
4. Манометрические методы за ходом реакции наблюдают по изменению давления при образовании или убыли газообразных веществ. глутаматдегидрогеназа Глутамат γ-аминомасляная кислота + СО 2↑ каталаза 2 Н 2 О 2 2 Н 2 О + О 2↑
 5. Спектрофотометрические методы за ходом реакции наблюдают по изменению оптической плотности при λ максимума поглощения продукта, субстрата или кофактора (см. определение активности алкоголльдегидрогеназы – практикум). 6. Флуоресцентные методы за ходом реакции наблюдают по изменению флуоресценции. Флавинзависимые ферменты: ФАД и ФМН флуоресцируют в окисленной форме, в восстановленной – нет. 7. Радиометрические методы метод основан на конкуренции между продуктом реакции и его аналогом, меченым изотопом, за центры связывания на молекуле антитела.
5. Спектрофотометрические методы за ходом реакции наблюдают по изменению оптической плотности при λ максимума поглощения продукта, субстрата или кофактора (см. определение активности алкоголльдегидрогеназы – практикум). 6. Флуоресцентные методы за ходом реакции наблюдают по изменению флуоресценции. Флавинзависимые ферменты: ФАД и ФМН флуоресцируют в окисленной форме, в восстановленной – нет. 7. Радиометрические методы метод основан на конкуренции между продуктом реакции и его аналогом, меченым изотопом, за центры связывания на молекуле антитела.


