Complexes-3-exchange.ppt
- Количество слайдов: 20

Влияние растворителя на процесс комплексообразования Гёрни – шкала мольных долей вместо молярной (моляльной). Если раствор не концентрированный, считается, что в 1 л раствора содержится такое же число молей, что и в 1 л чистого растворителя. NA ≈ [A]/[H 2 O], [H 2 O] – как в чистом растворителе MXi + Y = MY + i. X Энтропия: унитарная составляющая, кратическая составляющая
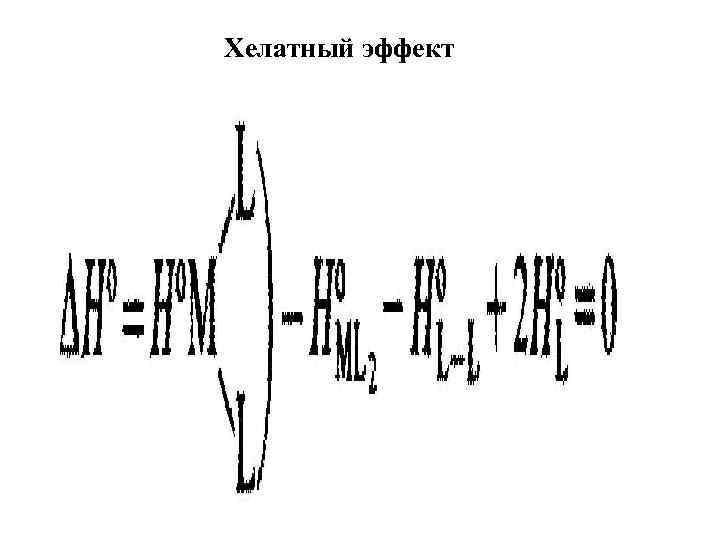
Хелатный эффект

L ML 2 + L-L = M | + 2 L L ΔS 0 = R·ln 55. 5 = 33 Дж·моль-1·К-1 ΔS 0 = 33·n Дж·моль-1·К-1 A. E. Martell, R. D. Hancock, R. J. Motekaitis. Factors affecting stabilities of chelate, macrocyclic and macrobicyclic complexes in solution. Coordination Chemistry Reviews, Volume 133, 1994, Pages 39– 65
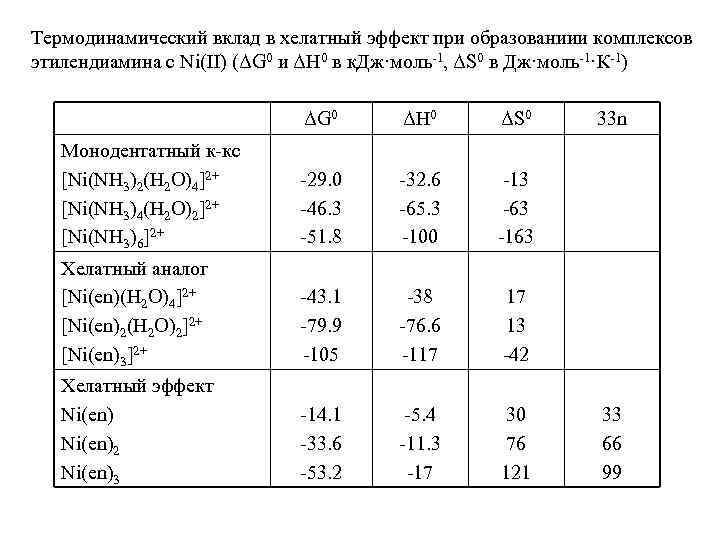
Термодинамический вклад в хелатный эффект при образованиии комплексов этилендиамина с Ni(II) (ΔG 0 и ΔH 0 в к. Дж·моль-1, ΔS 0 в Дж·моль-1·К-1) ΔG 0 ΔH 0 ΔS 0 Монодентатный к-кс [Ni(NH 3)2(H 2 O)4]2+ [Ni(NH 3)4(H 2 O)2]2+ [Ni(NH 3)6]2+ -29. 0 -46. 3 -51. 8 -32. 6 -65. 3 -100 -13 -63 -163 Хелатный аналог [Ni(en)(H 2 O)4]2+ [Ni(en)2(H 2 O)2]2+ [Ni(en)3]2+ -43. 1 -79. 9 -105 -38 -76. 6 -117 17 13 -42 Хелатный эффект Ni(en)2 Ni(en)3 -14. 1 -33. 6 -53. 2 -5. 4 -11. 3 -17 30 76 121 33 n 33 66 99
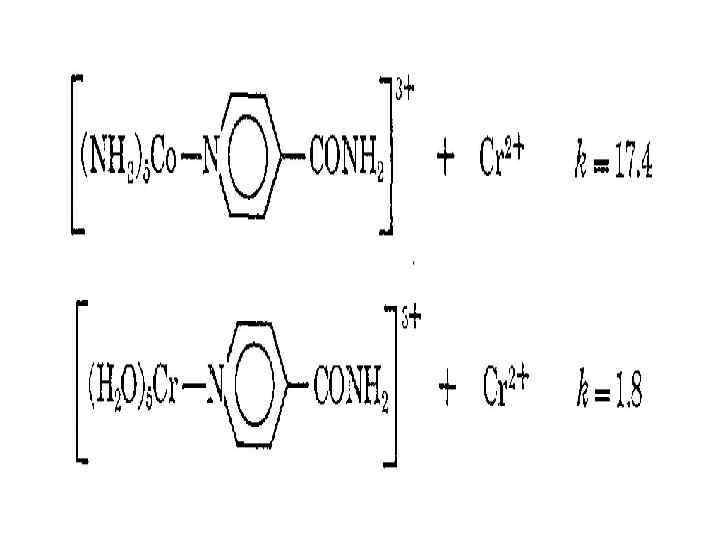
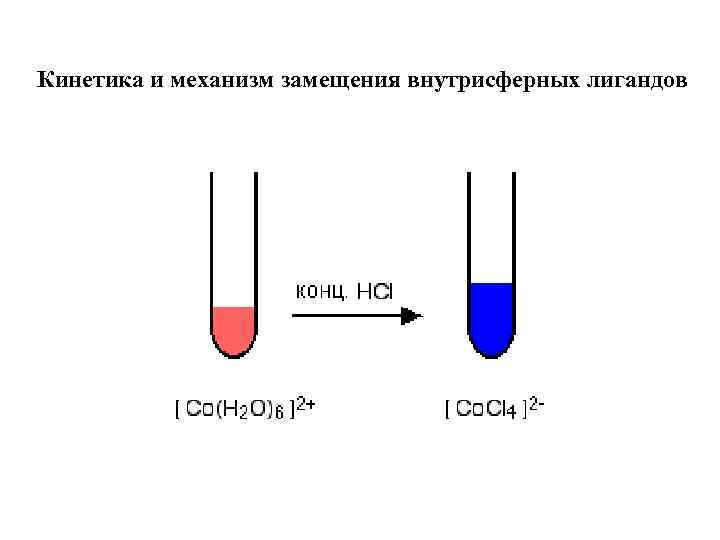
Кинетика и механизм замещения внутрисферных лигандов
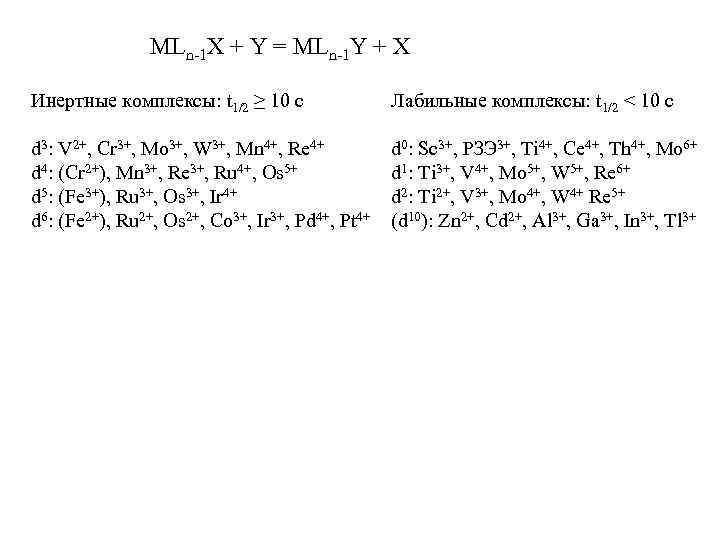
MLn-1 X + Y = MLn-1 Y + X Инертные комплексы: t 1/2 ≥ 10 c Лабильные комплексы: t 1/2 < 10 c d 3: V 2+, Cr 3+, Mo 3+, W 3+, Mn 4+, Re 4+ d 4: (Cr 2+), Mn 3+, Re 3+, Ru 4+, Os 5+ d 5: (Fe 3+), Ru 3+, Os 3+, Ir 4+ d 6: (Fe 2+), Ru 2+, Os 2+, Co 3+, Ir 3+, Pd 4+, Pt 4+ d 0: Sc 3+, РЗЭ 3+, Ti 4+, Ce 4+, Th 4+, Mo 6+ d 1: Ti 3+, V 4+, Mo 5+, W 5+, Re 6+ d 2: Ti 2+, V 3+, Mo 4+, W 4+ Re 5+ (d 10): Zn 2+, Cd 2+, Al 3+, Ga 3+, In 3+, Tl 3+

Механизмы обмена лигандов MLn-1 X + Y = MLn-1 Y + X 1) Ассоциативный механизм (А) MLn-1 X + Y = MLn-1 XY = MLn-1 Y + X 2) Диссоциативный механизм (D) MLn-1 X = MLn-1 + X MLn-1 + Y = MLn-1 Y 3) Механизм взаимного обмена (I) MLn-1 X + Y = MLn-1 X·Y = MLn-1 Y·X = MLn-1 Y + X Ia Id
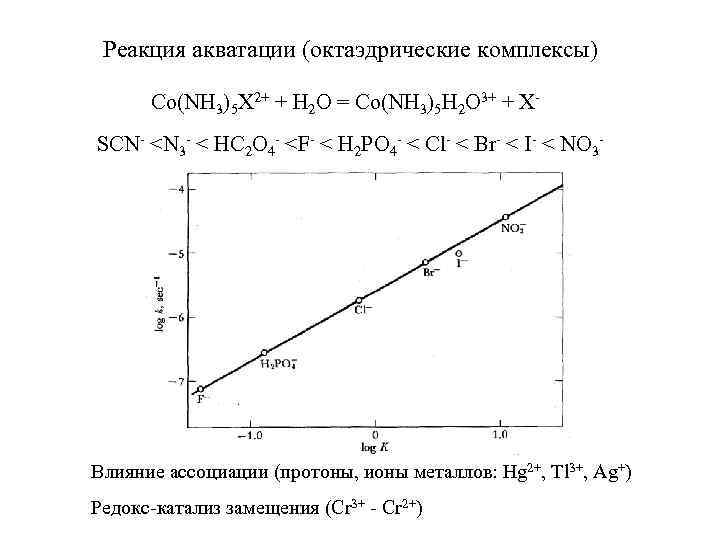
Реакция акватации (октаэдрические комплексы) Co(NH 3)5 X 2+ + H 2 O = Co(NH 3)5 H 2 O 3+ + XSCN- <N 3 - < HC 2 O 4 - <F- < H 2 PO 4 - < Cl- < Br- < I- < NO 3 - Влияние ассоциации (протоны, ионы металлов: Hg 2+, Tl 3+, Ag+) Редокс-катализ замещения (Cr 3+ - Cr 2+)

Langford C. H. , Gray H. B. Ligand Substitution Processes. W. A. Benjamin, Inc. , New York. 1965

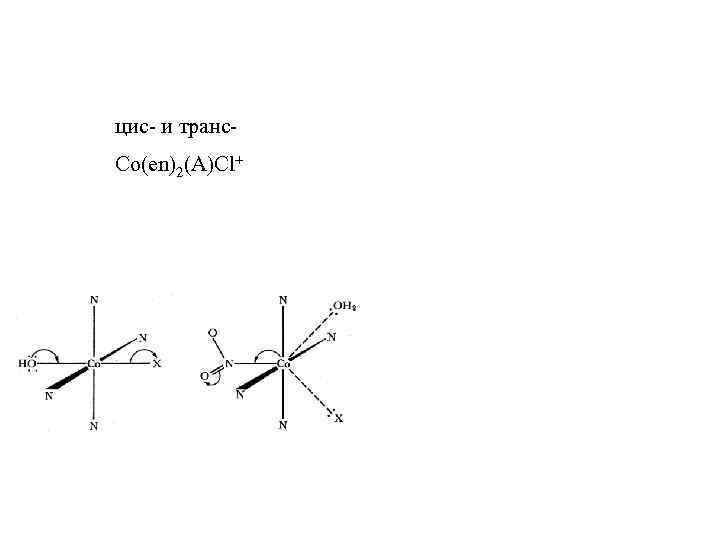
цис- и транс. Co(en)2(A)Cl+

Co(NH 3)5 Cl 2+ + OH- = Co(NH 3)4(NH 2)Cl+ + H 2 O → Co(NH 3)4 OH 2+ + Cl. Co(NH 3)5 F 2+ + H 3 O+ = Co(NH 3)5 FH 3+ + H 2 O → Co(NH 3)5 OH 23+ + HF Co(NH 3)5 CO 3+, Co(NH 3)5 ONO 2+, Co(en)2 F 2+

Процессы обмена лигандов в плоско-квадратных комплексах Ni(II), Rh(I), Pd(II), Ir(I), Pt(II), Au(III), конфигурация d 8 Pt(dien)X+ + Y = Pt(dien)Y + Xdien = H 2 N-C 2 H 4 -NH 2 H 2 O < Cl- < Br- < I-, SCN-, SC(NH 2)2 Pt(dien)Br+
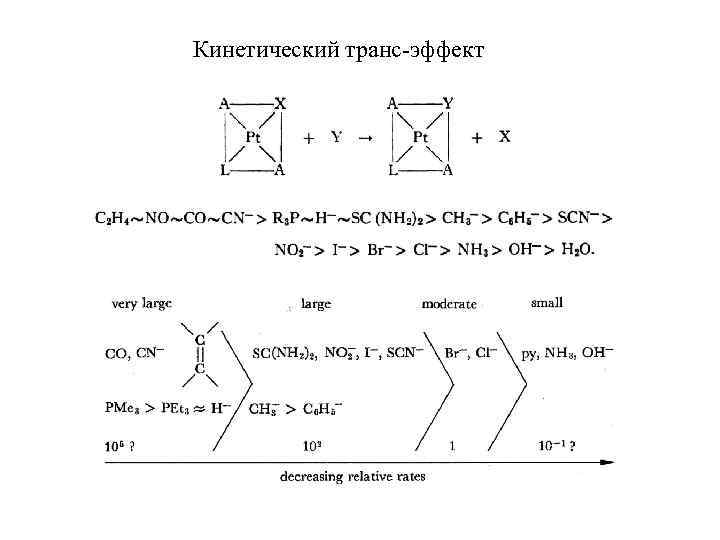
Кинетический транс-эффект

Кинетика и механизм гомогенных окислительновосстановительных реакций комплексов металлов Fe(H 2 O)63+ + Fe(H 2 O)62+ → Fe(H 2 O)62+ + Fe(H 2 O)63+
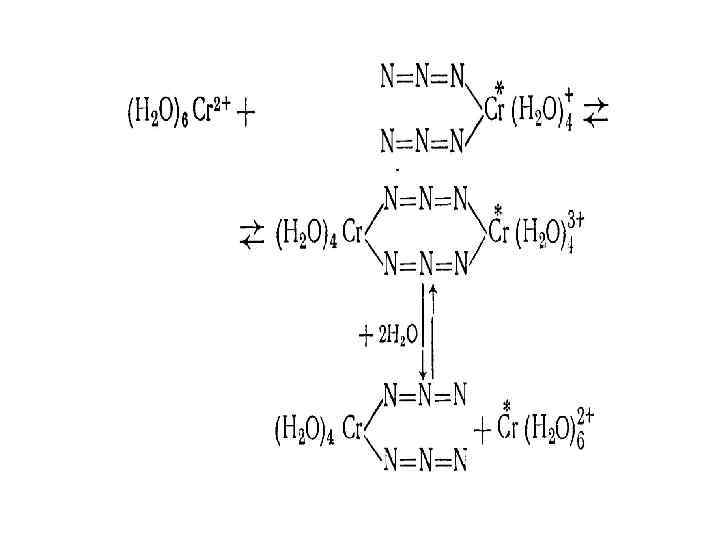

Co(NH 3)63+ + Cr 2+ → Co 2+ + Cr 3+ + 6 NH 3 k = 10 -4 M-1·c-1 внешнесферный механизм Co(NH 3)5 Cl 2+ + Cr 2+ → Co 2+ + Cr. Cl 2+ + 5 NH 3 k = 6· 105 M-1·c-1 внутрисферный механизм [(NH 3)5 Co-X-Cr]4+ - активированный комплекс (NH 3) < (py) < H 2 O < Cl- < Br. Co(NH 3)5 OOCC 6 H 52+ + Cr 2+ → Co 2+ + Cr. OOCC 6 H 52+ + 5 NH 3 k = 0. 15 M-1·c-1
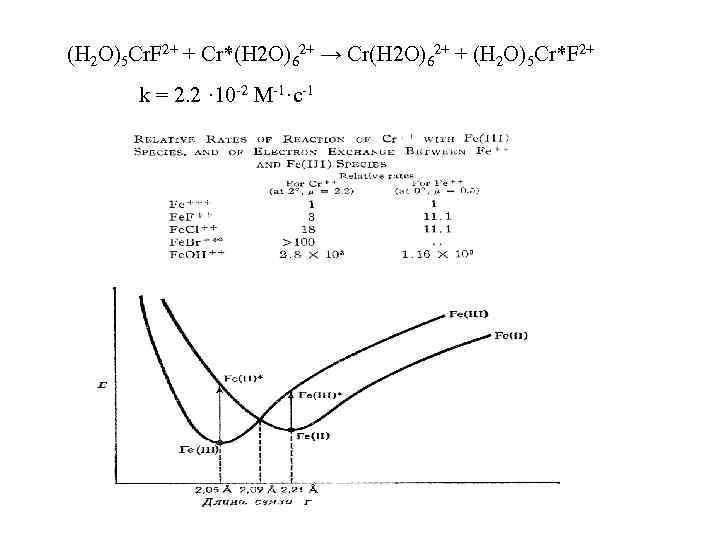
(H 2 O)5 Cr. F 2+ + Cr*(H 2 O)62+ → Cr(H 2 O)62+ + (H 2 O)5 Cr*F 2+ k = 2. 2 · 10 -2 M-1·c-1

Влияние присутствующего противоиона: Fe(CN)64 - - Fe(CN)63 K+, NH 4+ > Na+ > Li+ > H+; Sr 2+ > Ca 2+ > Mg 2+ [Co(en)2 ACl]n+ + Fe 2+ Цис-влияние: NH 3 < NCS- < H 2 O < Cl. Транс-влияние: NH 3 < NCS- < Cl- < N 3 - < H 2 O
Complexes-3-exchange.ppt