BA_ukr2.ppt
- Количество слайдов: 54

Визначення Øвід грецької “ἆσθμα” – тяжке дихання, задишка Ø Бронхіальна астма – це хронічне запальне захворювання дихальних шляхів, провідну роль в якому відіграє багато клітин та їх елементів Ø Хронічне запалення обумовлює розвиток бронхіальної гіперреактивності, яка призводить до повторних епізодів свистячих хрипів, нападів експіраторної задишки, відчуття “закладеності” в грудній клітці, сухого кашлю, зазвичай вночі або вранці Ø Ці епізоди зазвичай пов’язані з генералізованою бронхіальною обструкцією різного ступеня вираженості, зворотньою спонтанно або під дією адекватного лікування GINA 2011: www. ginasthma. org

Поширеність Приблизно 300 млн. хворих в світі За прогнозами до 2025 р. кількість наблизиться до 400 млн. хворих Астма є причиною кожної 250 -ої смерті в світі В Європі за останні 20 років смертність зросла у 2 -3 рази

Ендогенні фактори ризику бронхіальної астми • Гени, які призводять до розвитку атопії (гіперпродукція Ig. E «реагінів» ). Вони локалізуються у 11 -й хромосомі і відповідають за експресію рецепторів на Ig. E • Гени, які призводять до появи бронхіальної гіперреактивності, знижена чутливість β 2 -рецепторів або мутація генів β 2

Фактори, що впливають на розвиток і прояви БА ВНУТРІШНІ ЧИННИКИ Генетичні, наприклад • гени, що схиляють до атопії • гени, що схиляють до бронхіальної гіперреактивності Ожиріння Стать ЗОВНІШНІ ЧИННИКИ алергени • алергени приміщень: кліщі домашнього пилу, шерсть домашніх тварин (собак, кішок, мишей), алергени Тараканів, гриби, в тому числі цвілеві і дріжджові • зовнішні алергени: пилок, гриби, в тому числі цвілеві і дріжджові Інфекції (головним чином, вірусні) Професійні сенсибілізатори Куріння тютюну • пасивне куріння • активне куріння Забруднення повітря всередині і зовні приміщень Харчування

Клітини запалення в дихальних шляхах при БА Тучні клітини. Активовані тучні клітини слизової вивільняють медіатори, що викликають бронхоспазм (гістамін, цистеїнові лейкотрієни, простагландин D 2). Активація тучних клітин відбувається під дією алергенів за участю рецепторів до Ig. E , а також під впливом осмотичних стимулів (цей механізм бере участь у розвитку бронхоспазму при фізичному навантаженні). Підвищення ефективноеї кількость опасистих клітин в гладкій мускулатурі дихальних шляхів може бути пов'язано з бронхіальною гіперреактивністю. Еозинофіли. К-сть еозинофілів у дихальних шляхах підвищена; ці клітини виділяють основні білки, які можуть пошкоджувати епітелій бронхів. Вони також можуть беруть участь- у вивільненні факторів росту і ремоделюванні дихальних шляхів. T- лімфоцити. Кількість T-лімфоцитів у дихальних шляхах підвищена; T-лімфоцити вивільняють специфічні цитокіни, в тому числі IL-4, IL-5, IL-9 і IL-13, які регулюють процес еозинофільного запалення і вироблення Ig. E B-лімфоцитами. Дендритні клітини захоплюють алергени з поверхні слизової бронхів і мігрують в регіональні лімфатічні вузли, де взаємодіють з регуляторними T-клітинами і в кінцевому рахунку стимулюють перетворення недиференційованих T-лімфоцитів в Th 2 -клітини. Макрофаги. Кількість макрофагів в дихальних шляхах підвишена; вони можуть активуватися під дією алергенів за участю рецепторів до Ig. E з низькою афінності; наслідком активації є вивільнення медіаторів запалення і цитокінів, які посилюють запальну реакцію. Нейтрофіли. Кількість нейтрофілів підвищується в дихальних шляхах і мокротинні хворих тяжкою БА, однак патофізіологічна роль цих клітин не з'ясована; підвищення їх кількості, зокрема, може бути наслідком терапії глюкокортикостероїдами.

Основні медіатори при БА Хемокіни експресуються переважно в клітинах бронхіального епітелію і відіграють важливу роль у залученні клітин запалення в дихальні шляхи. Еотоксин селективно впливає на еозинофіли, в той час як хемокінів, регульовані тимусом і активацією (TARC), і макрофагальні хемокінів (MDC) залучають Th 2 -кл. Лейкотрієни є потужними бронхоконстриторами і медіаторами запалення; вони виділяються переважно тучними клітинами і еозинофілами. Це єдиний вид медіаторів, інгібування якого приводить до поліпшення функції легень і зменшення вираженості симптомів БА. Цитокіни регулюють запальну відповідь при БА і визначаючи його вираженість. До найбільш важливих цітокінів відносяться IL-1β і фактор некрозу пухлини (TNF -α), які посилюють запальну реакцію, а також гранулоцитарно-макрофагальний колонієстимулюючий фактор (GM-CSF), що збільшує тривалість життя еозинофілів в дихальних шляхах. До цитокінів відносяться: IL-5, необхідний для диференціації і збільшення тривалості життя еозинофілів; IL-4, що грає важливу роль в диференціюванні по Th 2 -клітинному шляху; IL-13, що бере участь в утворенні Ig. E. Гістамін вивільн. з тучних кл. і бере участь в розвитку бронхоспазму і зап. реакції NO, потужний вазодилататор, синтезується синтазою окису азоту в клітинах бронхіального епітелію. Рівень NO у видихуваному повітрі все частіше використовується для оцінки ефективності лікування БА, так як показано його взаємозв'язок з наявністю запалення при БА. Простагландин D 2 володіє бронхоконстрікторною дією і утворюється переважно в тучних клітинах; бере участь у залученні Th 2 -клітин в дихальні шляхи


Структурні зміни в дихальних шляхах при БА В результаті відкладення волокон колагену і протеогліканів під базальною мембраною розвивається субепітеліальний фіброз, який відмічається у всіх хворих БА, навіть до початку клінічних проявів захворювання; його вираженість може зменшуватись під дією лікування. Розвивається фіброз інших шарів стінки бронха, в яких також відкладаються колаген і протеоглікани. Гладка мускулатура стінки бронха. Товщина гладеньком'язової шару збільшується внаслідок гіпертрофії (збільшення розмірів окремих клітин) і гіперплазії (підвищеного ділення клітин), що сприяє загальному потовщенню стінки бронха. Цей процес може залежати від ступеня тяжкості захворювання і зумовлений дією таких медіаторів запалення, як фактори росту. Кровоносні судини. Під дією факторів росту, наприклад фактора росту ендотелію судин (VEGF), відзначається проліферація судин бронхіальної стінки, що сприяє потовщення стінки бронха. Гіперсекреція слизу зумовлена підвищенням кількості келихоподібних клітин в епітелії дихальних шляхів і збільшенням розмірів підслизових залоз.
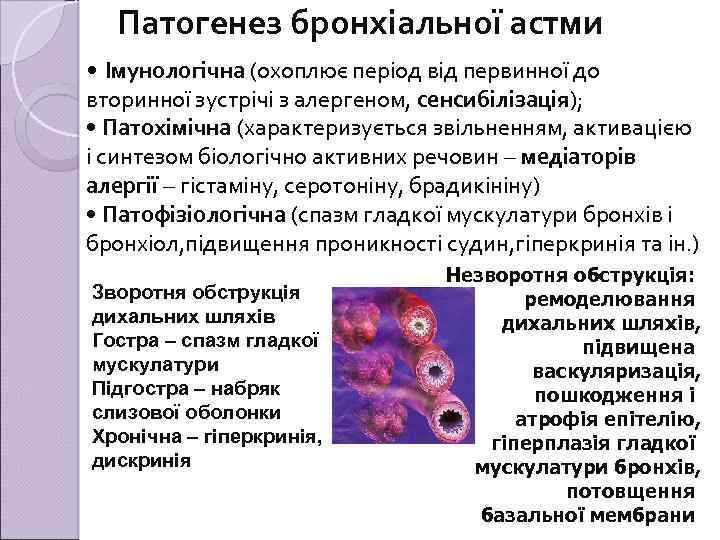
Патогенез бронхіальної астми • Імунологічна (охоплює період від первинної до вторинної зустрічі з алергеном, сенсибілізація); • Патохімічна (характеризується звільненням, активацією і синтезом біологічно активних речовин – медіаторів алергії – гістаміну, серотоніну, брадикініну) • Патофізіологічна (спазм гладкої мускулатури бронхів і бронхіол, підвищення проникності судин, гіперкринія та ін. ) Зворотня обструкція дихальних шляхів Гостра – спазм гладкої мускулатури Підгостра – набряк слизової оболонки Хронічна – гіперкринія, дискринія Незворотня обструкція: ремоделювання дихальних шляхів, підвищена васкуляризація, пошкодження і атрофія епітелію, гіперплазія гладкої мускулатури бронхів, потовщення базальної мембрани
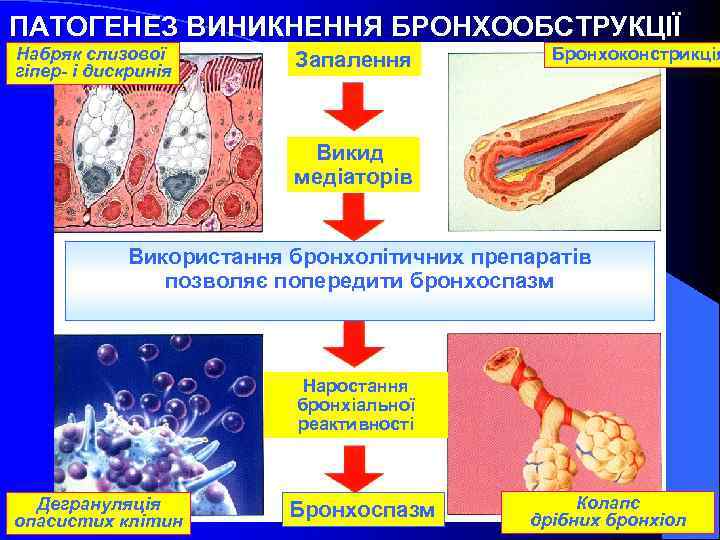
ПАТОГЕНЕЗ ВИНИКНЕННЯ БРОНХООБСТРУКЦІЇ Набряк слизової гіпер- і дискринія Запалення Бронхоконстрикція Викид медіаторів Використання бронхолітичних препаратів позволяє попередити бронхоспазм Наростання бронхіальної реактивності Дегрануляція опасистих клітин Бронхоспазм Колапс дрібних бронхіол

Механізми розвитку бронхіальної гіперреактивності Надмірне скорочення гладких м'язів дихальних шляхів може бути наслідком збільшення обсягу і скоротливості гладких клітин бронхів. Десинхронізація скорочення гладкої мускулатури дихальних шляхів внаслідок запальних змін бронхіальної стінки може призводити до надмірного звуження просвіту бронхів. Потовщення бронхіальної стінки, обумовлене набряком і структурними змінами, збільшує ступінь звуження дихальних шляхів при спазмі гладкої мускулатури бронхів за рахунок трансформаційних змін геометрії бронхів. Запальний процес може сприяти сенсибілізації чутливих нервів, що призводить до надлишкової бронхоконстрикції у відповідь на стимуляцію нервів.
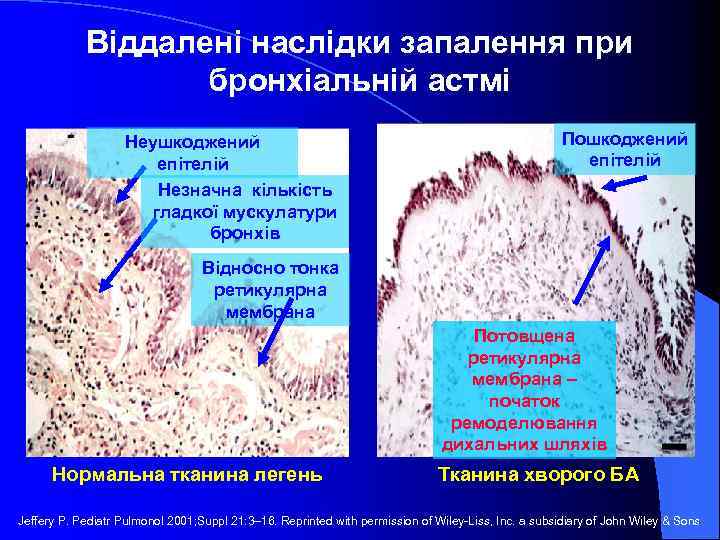
Віддалені наслідки запалення при бронхіальній астмі Неушкоджений епітелій Незначна кількість гладкої мускулатури бронхів Пошкоджений епітелій Відносно тонка ретикулярна мембрана Потовщена ретикулярна мембрана – початок ремоделювання дихальних шляхів Нормальна тканина легень Тканина хворого БА Jeffery P. Pediatr Pulmonol 2001; Suppl 21: 3– 16. Reprinted with permission of Wiley-Liss, Inc. a subsidiary of John Wiley & Sons

Діагностика бронхіальної астми Оцінка алергологічного статусу: алергологічний анамнез (алергічний риніт, атопічний дерматит у хворого або родичів); позитивні шкірні тести з алергенами; підвищений рівень загального і специфічного Ig. E у крові Обстеження ФЗД: наявність ознак бронхіальної обструкції (значення ПОШвид. і ОФВ 1 менше 80% від належних); виражена зворотність бронхіальної обструкції (підвищення ПОШвид. і ОФВ 1 більше 12% (або більше 200 мл) за результатами фармакологічної проби з β 2 -агоністом короткої дії; добова варіабельність ПОШвид. і ОФВ 1 більше 20% Визначення гіперреактивності бронхів. Гіперреактивність бронхів вимірюється за результатами провокаційних тестів з: гістаміном, метахоліном; фізичним зусиллям

ДІАГНОСТИКА БРОНХІАЛЬНОЇ АСТМИ Пікфлоуметрія – це простий і доступний метод вимірювання ПОШвид. Рентгенологічне обстеження. Збільшення легеневих полів, обмеження рухомості, низьке стояння і сплощення куполів діафрагми, розширення ретростернального і ретрокардіального просторів, вертикальне положення серця (“капельне серце”) Дослідження крові: еозинофілія Дослідження мокроти: клітини миготливого епітелію, еозинофіли, спіралі Куршмана, кристали Шарко-Лейдена
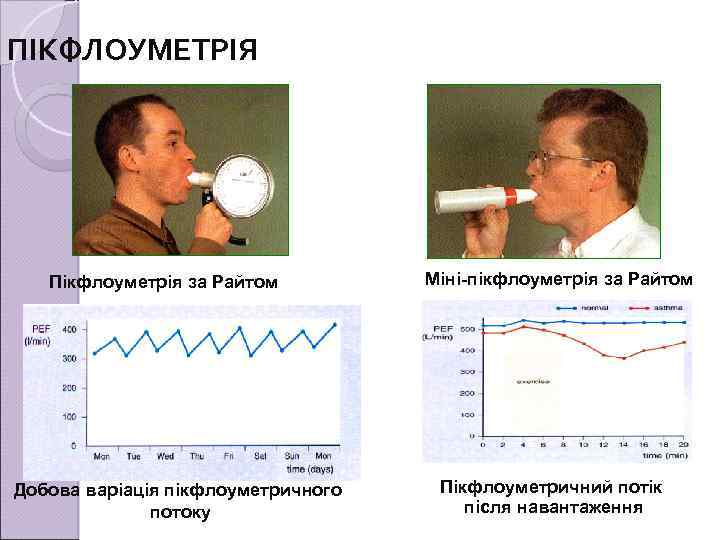
ПІКФЛОУМЕТРІЯ Пікфлоуметрія за Райтом Добова варіація пікфлоуметричного потоку Міні-пікфлоуметрія за Райтом Пікфлоуметричний потік після навантаження

Клінічні прояви бронхіальної астми Симптоми бронхіальної астми включають: Ø Свистячі хрипи (в тому числі дистанційні), зазвичай експіраторного характеру (на видиху) Ø Задишку експіраторного характеру (утруднене дихання) зазвичай у вигляді нападів Ø Відчуття «закладеності» в грудній клітці Ø Кашель, частіше непродуктивний Ø Інколи – виділення білої, «скловидної» мокроти в кінці нападу задишки

ФІЗИКАЛЬНІ ДАНІ • Сухі свистячі експіраторні хрипи (звучність хрипів не завжди відповідає тяжкості захворювання) • При тривалому перебігу – ознаки емфіземи ( «діжкоподібна» грудна клітка, коробковий звук при перкусії) • При загостренні – участь в акті дихання допоміжної мускулатури (м’язів плечового поясу), втягнення податливих ділянок грудної клітки на вдиху • Тахіпное, тахікардія GINA 2011: www. ginasthma. org

Класифікація бронхіальної астми Ступінь І, інтермітуюча (симптоми менше 1 разу в тиждень, короткі загострення, нічні симптоми не більше 2 раз в місяць, ПОШвид. або ОФВ 1 не менше 80% от належних, добова варіабельність до 20%) Ступінь ІІ, легка персистуюча (симптоми від 1 разу в тиждень до 1 разу в день, нічні симптоми 2 рази на місяць, ПОШвид. або ОФВ 1 ≥ 80% від належних, добова варіабельність 20 -30%) Ступінь ІІІ, середньої тяжкості персистуюча (постійні симптоми, нічні симптоми частіше 1 разу на тиждень, ПОШвид. або ОФВ 1 60 -80% від належних, добова варіабельність 30%) Ступінь ІV, тяжка персистуюча (постійні симптоми, часті нічні симптоми, обмеження фізичної активності, ПОШвид. або ОФВ 1 < 60% від належних, добова варіабельність більше 30%)
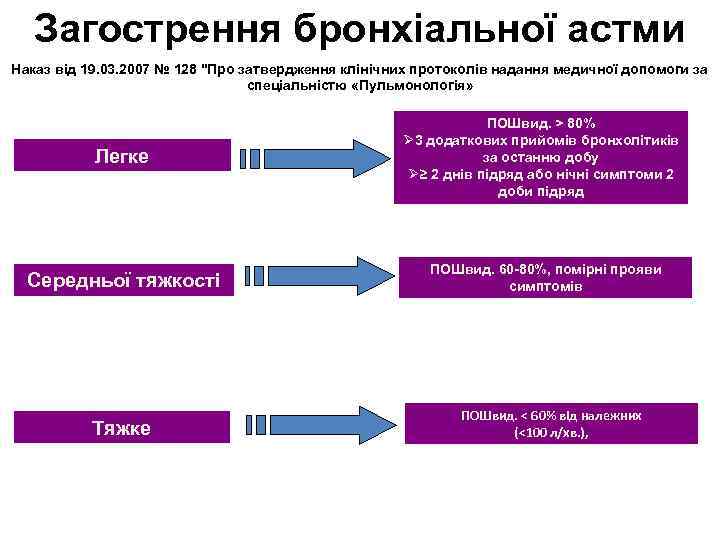
Загострення бронхіальної астми Наказ від 19. 03. 2007 № 128 "Про затвердження клінічних протоколів надання медичної допомоги за спеціальністю «Пульмонологія» Легке Середньої тяжкості Тяжке ПОШвид. > 80% Ø 3 додаткових прийомів бронхолітиків за останню добу Ø≥ 2 днів підряд або нічні симптоми 2 доби підряд ПОШвид. 60 -80%, помірні прояви симптомів ПОШвид. < 60% від належних (<100 л/хв. ),

Астматичний статус – це тяжкий напад бронхіальної астми тривалістю більше 24 годин, який характеризується гострою прогресуючою легеневою недостатністю, яка обумовлена обструкцією повітроносних шляхів на ґрунті розвитку резистентності до β 2 -агоністів Причини розвитку астматичного статусу: бактеріальні інфекції; психо-емоційні стреси; кліматичні фактори; різка відміна ГКС; безконтрольний прийом симпатоміметиків “синдром рикошету”; призначення препаратів, які можуть посилювати бронхообструкцію (психотропні, неселективні НПЗП та бета-блокатори ) Стадії: відносної компенсації, «німа» легеня, гіперкапнічна гіпоксична кома

Приклади формулювання діагнозу Бронхіальна астма, інтермітуючий перебіг, легке загострення. ЛН 0. Бронхіальна астма, легкий персистуючий перебіг, легке загострення. ЛН 0. Бронхіальна астма, персистуючий перебіг, середня важкість, середньо-важке загострення. ЛН ІІ. Бронхіальна астма, важкий персистуючий перебіг, важке загострення. Емфізема легень, пневмосклероз, ЛН ІІ.
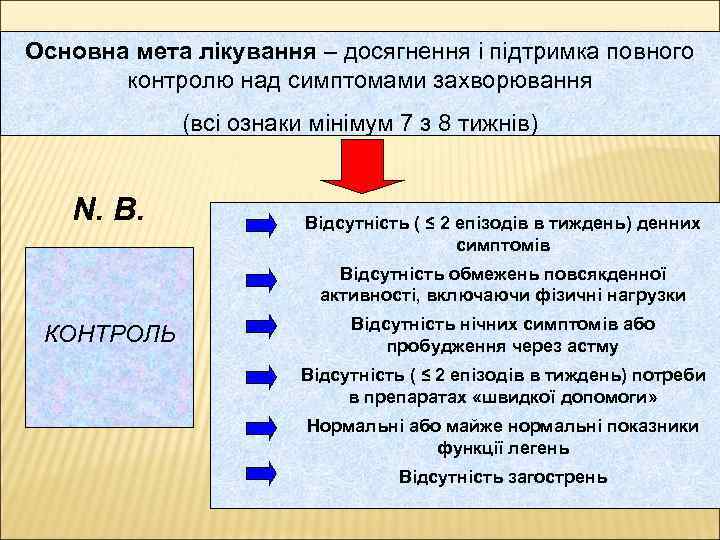
Основна мета лікування – досягнення і підтримка повного контролю над симптомами захворювання (всі ознаки мінімум 7 з 8 тижнів) N. B. Відсутність ( ≤ 2 епізодів в тиждень) денних симптомів Відсутність обмежень повсякденної активності, включаючи фізичні нагрузки КОНТРОЛЬ Відсутність нічних симптомів або пробудження через астму Відсутність ( ≤ 2 епізодів в тиждень) потреби в препаратах «швидкої допомоги» Нормальні або майже нормальні показники функції легень Відсутність загострень
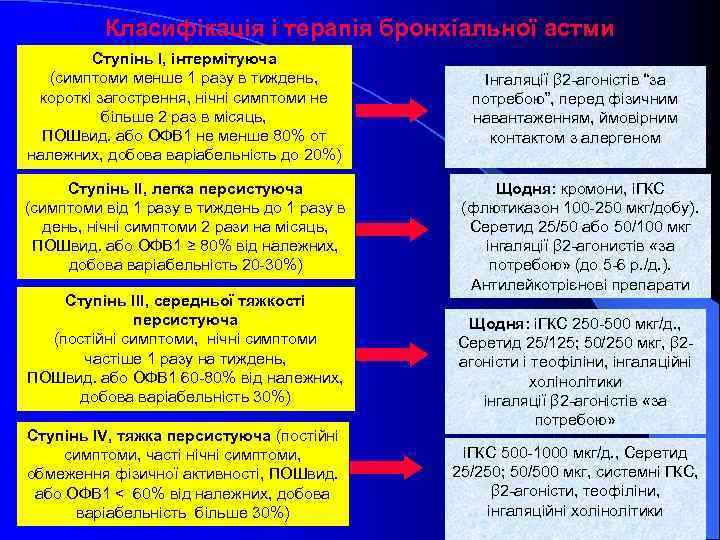
Класифікація і терапія бронхіальної астми Ступінь І, інтермітуюча (симптоми менше 1 разу в тиждень, короткі загострення, нічні симптоми не більше 2 раз в місяць, ПОШвид. або ОФВ 1 не менше 80% от належних, добова варіабельність до 20%) Ступінь ІІ, легка персистуюча (симптоми від 1 разу в тиждень до 1 разу в день, нічні симптоми 2 рази на місяць, ПОШвид. або ОФВ 1 ≥ 80% від належних, добова варіабельність 20 -30%) Ступінь ІІІ, середньої тяжкості персистуюча (постійні симптоми, нічні симптоми частіше 1 разу на тиждень, ПОШвид. або ОФВ 1 60 -80% від належних, добова варіабельність 30%) Ступінь ІV, тяжка персистуюча (постійні симптоми, часті нічні симптоми, обмеження фізичної активності, ПОШвид. або ОФВ 1 < 60% від належних, добова варіабельність більше 30%) Інгаляції β 2 -агоністів “за потребою”, перед фізичним навантаженням, ймовірним контактом з алергеном Щодня: кромони, іГКС (флютиказон 100 -250 мкг/добу). Серетид 25/50 або 50/100 мкг інгаляції β 2 -агонистів «за потребою» (до 5 -6 р. /д. ). Антилейкотрієнові препарати Щодня: іГКС 250 -500 мкг/д. , Серетид 25/125; 50/250 мкг, β 2 агоністи і теофіліни, інгаляційні холінолітики інгаляції β 2 -агоністів «за потребою» іГКС 500 -1000 мкг/д. , Серетид 25/250; 50/500 мкг, системні ГКС, β 2 -агоністи, теофіліни, інгаляційні холінолітики
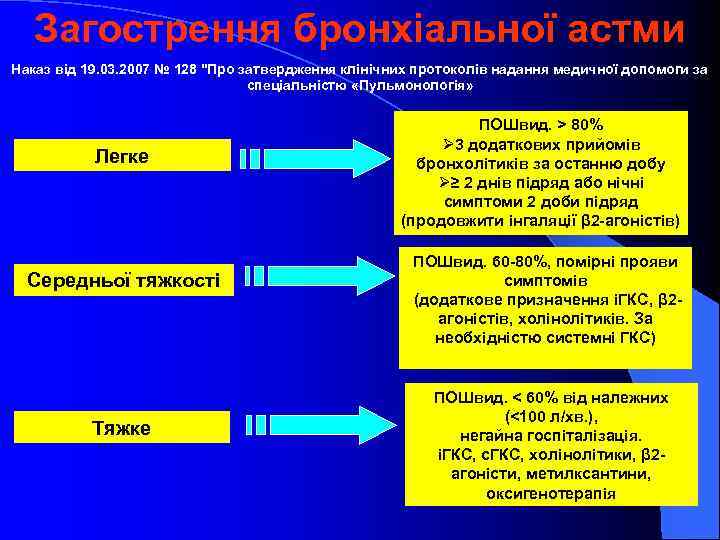
Загострення бронхіальної астми Наказ від 19. 03. 2007 № 128 "Про затвердження клінічних протоколів надання медичної допомоги за спеціальністю «Пульмонологія» Легке Середньої тяжкості Тяжке ПОШвид. > 80% Ø 3 додаткових прийомів бронхолітиків за останню добу Ø≥ 2 днів підряд або нічні симптоми 2 доби підряд (продовжити інгаляції β 2 -агоністів) ПОШвид. 60 -80%, помірні прояви симптомів (додаткове призначення іГКС, β 2 агоністів, холінолітиків. За необхідністю системні ГКС) ПОШвид. < 60% від належних (<100 л/хв. ), негайна госпіталізація. іГКС, с. ГКС, холінолітики, β 2 агоністи, метилксантини, оксигенотерапія
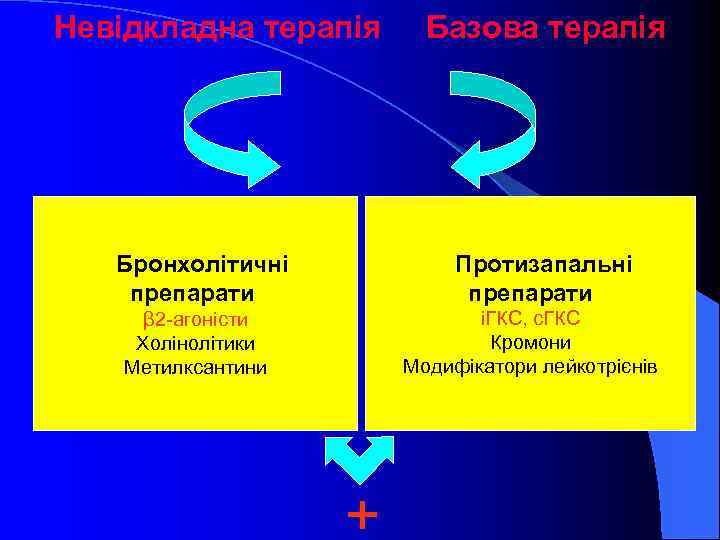
Невідкладна терапія Базова терапія Протизапальні препарати Бронхолітичні препарати іГКС, с. ГКС Кромони Модифікатори лейкотрієнів β 2 -агоністи Холінолітики Метилксантини +
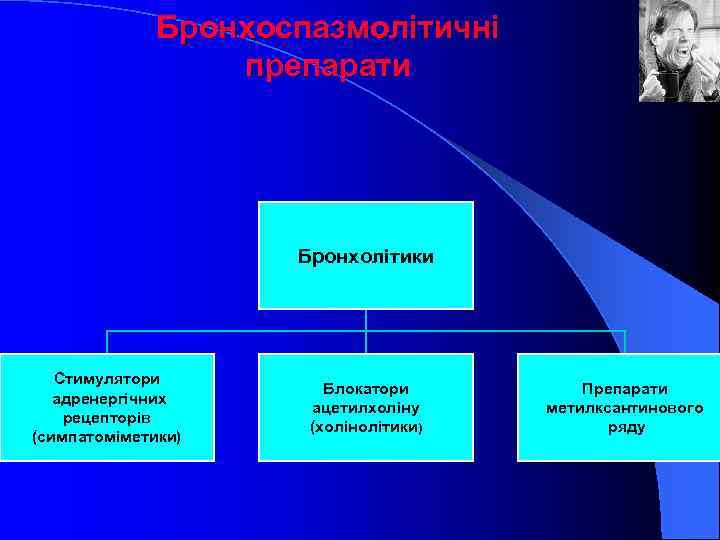
Бронхоспазмолітичні препарати Бронхолітики Стимулятори адренергічних рецепторів (симпатоміметики) Блокатори ацетилхоліну (холінолітики) Препарати метилксантинового ряду

БАЗОВА ТЕРАПІЯ БРОНХІАЛЬНОЇ АСТМИ іГКС (беклометазону діпропіонат, флютиказону пропіонат) β 2 -агоністи пролонгованої дії (сальметерол, формотерол) Комбінація β 2 -агоністів пролонгованої дії і іГКС (Серетид) Кромони (Інтал, Тайлед) Модифікатори лейкотрієнів: Блокатори 5 -ліпооксигенази – Зілеутон 600 мг 3 -4 р/д. Антагоністи лейкотрієнових рецепторів (С 4, D 4, Е 4): Зафірлукаст (Аколат) 20 мг 2 р/д. Монтелукаст (Сінгуляр) 10 мг 1 р/д.
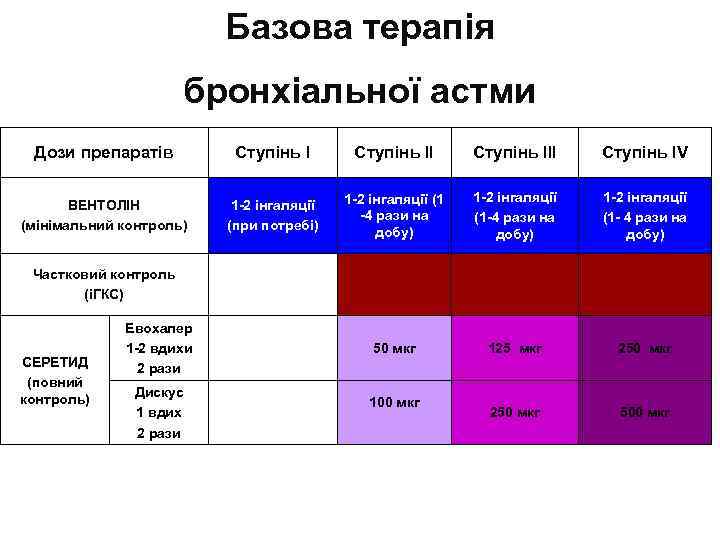
Базова терапія бронхіальної астми Дози препаратів Ступінь ІІІ Ступінь IV ВЕНТОЛІН (мінімальний контроль) 1 -2 інгаляції (при потребі) 1 -2 інгаляції (1 -4 рази на добу) 1 -2 інгаляції (1 - 4 рази на добу) 50 мкг 125 мкг 250 мкг 500 мкг Частковий контроль (іГКС) СЕРЕТИД (повний контроль) Евохалер 1 -2 вдихи 2 рази Дискус 1 вдих 2 рази 100 мкг
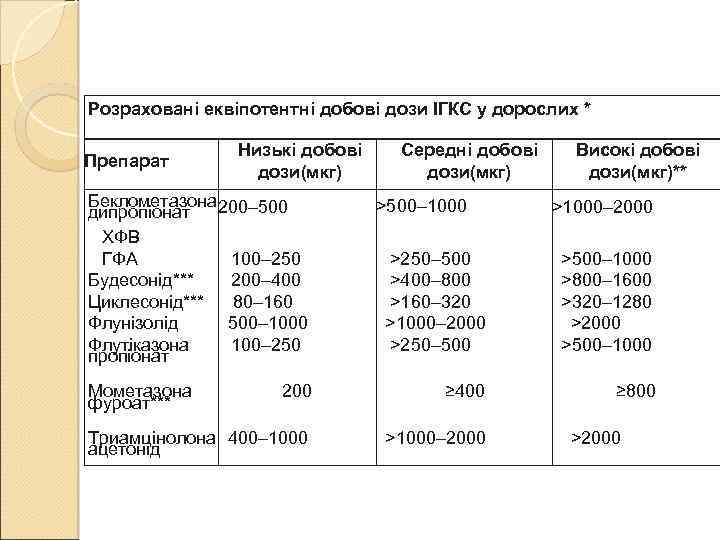
Розраховані еквіпотентні добові дози ІГКС у дорослих * Препарат Низькі добові дози(мкг) Беклометазона 200– 500 дипропіонат ХФВ ГФА 100– 250 Будесонід*** 200– 400 Циклесонід*** 80– 160 Флунізолід 500– 1000 Флутіказона 100– 250 пропіонат Середні добові дози(мкг) >500– 1000 Високі добові дози(мкг)** >1000– 2000 >250– 500 >400– 800 >160– 320 >1000– 2000 >250– 500 >500– 1000 >800– 1600 >320– 1280 >2000 >500– 1000 200 ≥ 400 ≥ 800 Триамцінолона 400– 1000 ацетонід >1000– 2000 Мометазона фуроат*** >2000
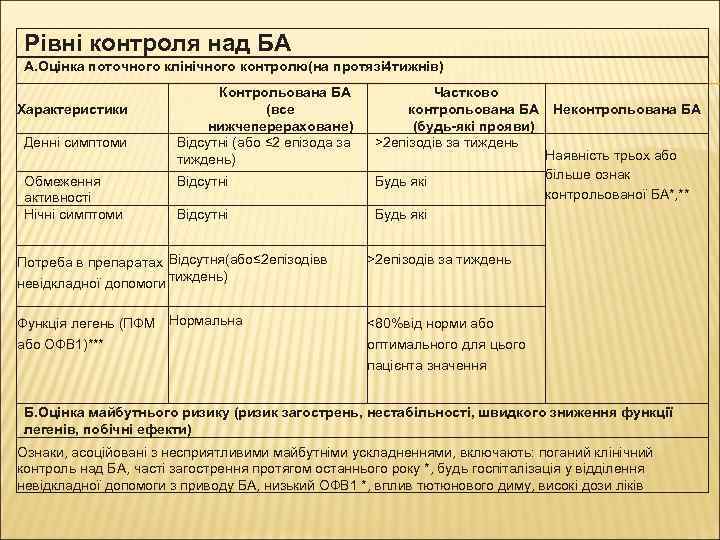
Рівні контроля над БА А. Оцінка поточного клінічного контролю(на протязі 4 тижнів) Характеристики Денні симптоми Обмеження активності Нічні симптоми Контрольована БА (все нижчеперераховане) Відсутні (або ≤ 2 епізода за тиждень) Відсутні Частково контрольована БА Неконтрольована БА (будь-які прояви) >2 епізодів за тиждень Наявність трьох або більше ознак Будь які контрольованої БА*, ** Будь які Потреба в препаратах Відсутня(або≤ 2 епізодівв тиждень) невідкладної допомоги >2 епізодів за тиждень Функція легень (ПФМ Нормальна або ОФВ 1)*** <80%від норми або оптимального для цього пацієнта значення Б. Оцінка майбутнього ризику (ризик загострень, нестабільності, швидкого зниження функції легенів, побічні ефекти) Ознаки, асоційовані з несприятливими майбутніми ускладненнями, включають: поганий клінічний контроль над БА, часті загострення протягом останнього року *, будь госпіталізація у відділення невідкладної допомоги з приводу БА, низький ОФВ 1 *, вплив тютюнового диму, високі дози ліків
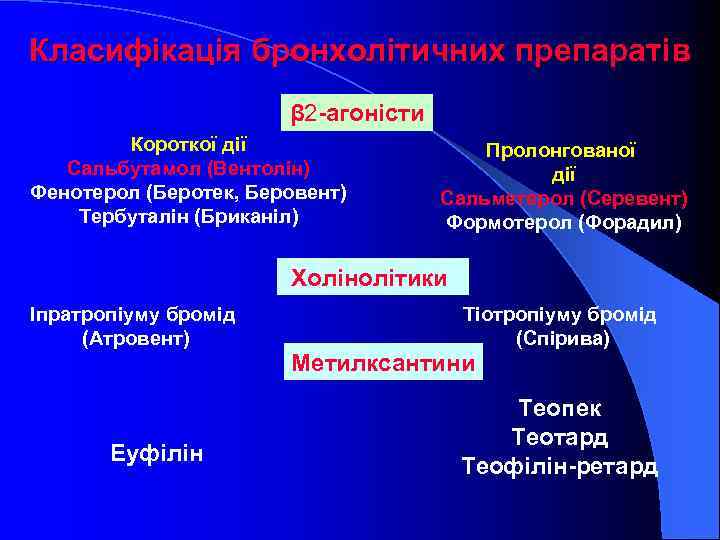
Класифікація бронхолітичних препаратів β 2 -агоністи Короткої дії Сальбутамол (Вентолін) Фенотерол (Беротек, Беровент) Тербуталін (Бриканіл) Пролонгованої дії Сальметерол (Серевент) Формотерол (Форадил) Холінолітики Іпратропіуму бромід (Атровент) Еуфілін Тіотропіуму бромід (Спірива) Метилксантини Теопек Теотард Теофілін-ретард

Бронхолітична терапія Перший селективний β 2 -агоніст короткої дії Не містить фреону (вимоги Монреальского протоколу, 1987 р. ) Використовується для зняття гострого нападу бронхоспазму (100 -200 мкг) Профілактика бронхоспазму перед фізичним навантаженням

Антихолінергічні препарати ІПРАТРОПІУМУ БРОМІД (Атровент) Механізм дії: l усунення/полегшення симптомів завдяки його бронходилятаційному ефекту l усунення/попередження обумовленого ацетилхоліном бронхоспазму; l не впливає на запалення та розвиток алергічних реакцій l Побічні ефекти: сухість і гіркота в роті, погіршення перебігу глаукоми, порушення сечовиділення (при аденомі простати) ТІОТРОПІУМУ БРОМІД (Спірива): препарат для базової терапії, приймається в вигляді інгаляції 1 раз на добу GINA 2007: www. ginasthma. org

Метилксантини l Менш виражена бронхолітична дія, препарати (другого ряду) l Мають незначний протизапальний ефект l Збільшують силу дихальних м’язів та активність дихального центру l Необхідний контроль концентрації (для попередження передозування) препарату в крові

Бекотид, беклофорт (беклометазону діпропіонат) Форма випуску: Бекотид – дозований аерозоль (50 мкг/доза, 200 доз) Беклофорт – дозований аерозоль (250 мкг/доза, 200 доз) Спосіб застосування: дорослим і дітям > 12 років; початкова доза залежить від ступеня тяжкості

Фліксотид (флютиказону пропіонат) Для тривалої терапії ефективний в низьких дозах Форма випуску: 25 мкг; 50 мкг; 125 мкг; 250 мкг – 60 або 120 доз. Спосіб застосування: дорослі і діти > 16 років – по 100 -1000 мкг/добу Діти від 1 -4 років: 100 мкг з допомогою спейсера “Baby haler”

Серетид – (сальметерол/флютиказон) ЕВОХАЛЕР ДИСКУС 25/50 (120 доз) 50/100 (60 доз) 25/125 (120 доз) 50/250 (60 доз) 25/250 (120 доз) 50/500 (60 доз) 2 інгаляції 1 інгаляція 2 рази на добу При досягненні стійкого контролю пацієнти можуть перейти на ОДНУ ІНГАЛЯЦІЮ В ДОБУ
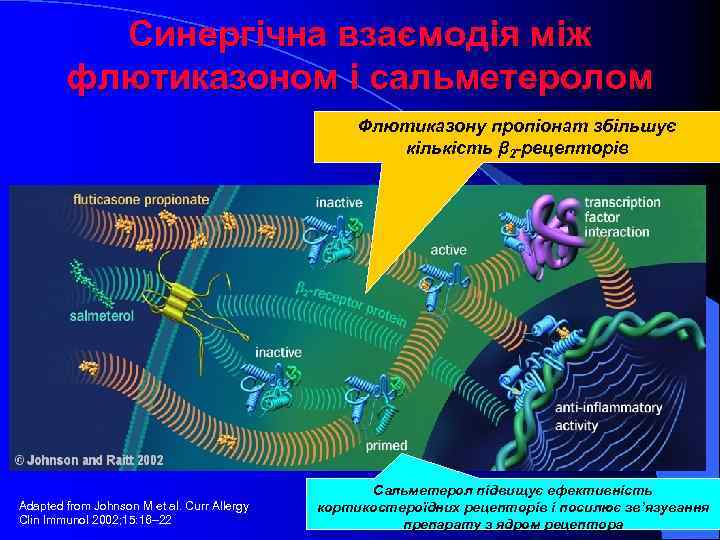
Синергічна взаємодія між флютиказоном і сальметеролом Флютиказону пропіонат збільшує кількість β 2 -рецепторів Adapted from Johnson M et al. Curr Allergy Clin Immunol 2002; 15: 16– 22 Сальметерол підвищує ефективність кортикостероїдних рецепторів і посилює зв’язування препарату з ядром рецептора

Побічні ефекти іГКС Локальні побічні ефекти: l l l дисфонія орофарінгеальний кандидоз кашель Системні побічні ефекти: пригнічення кори наднирників сповільнення росту петехії остеопороз катаракта глаукома метаболічні порушення (глюкоза, інсулін, тригліцериди) психічні порушення
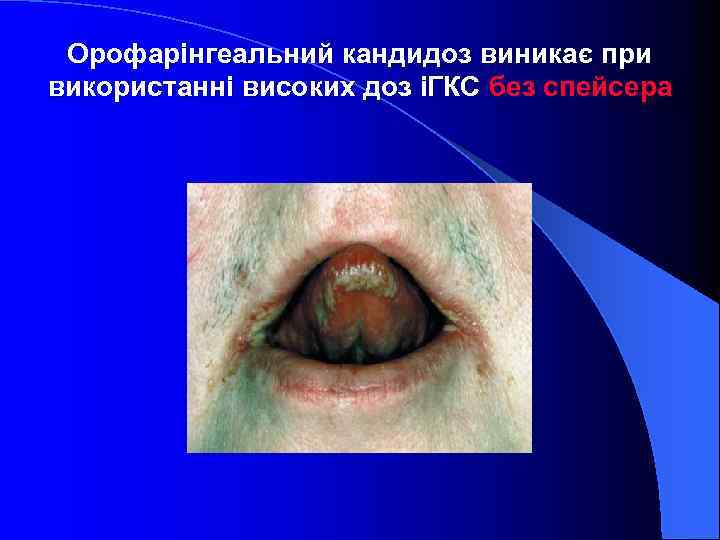
Орофарінгеальний кандидоз виникає при використанні високих доз іГКС без спейсера

Відхаркуючі препарати Муколітики Ацетилцистеїн Карбоцистеїн Стимулятори синтезу сурфактанту АЦЦ 100, 200, 600, Мукобене, Ацетин, Флуїмуцил 3 мл, Мукоміст, Мукосольвін (3 мл для інгаляцій) Амброксол Амбробене

Небулайзерна терапія

НЕБУЛАЙЗЕРНА ТЕРАПІЯ Можливість використання в стаціонарних та амбулаторних умовах; Використання широкого спектру і високих доз медикаментозних препаратів; Можливість підключення в контур подачі кисню, ШВЛ; Не потребує форсованих дихальних маневрів; Можливість використання дітям, літнім особам Бронходилятатори Холінолітики Антибіотики Муколітики Кортикостероїди Антиоксиданти Анальгетики Анестетики (лідокаїн) Провокаційні агенти: (метахолін, гістамін)

Невідкладна допомога при астматичному статусі 60 -90 мг преднізолону в/в з повторними введеннями препарату через 2 -3 години; l регідратація (введення фізіологічного розчину, розчину Рінгера до 2, 0 л/добу); l Парентерально адреналіну гідрохлориду 1%-1 мл в/в; l “агресивне” застосування β 2 -агоністів швидкої дії (сальбутамол) в дозі 0, 3 мл/кг 0, 5% розчину в/в; l теофілін в/в в дозі 6 мг/кг з зменшенням дози до 0, 6 -1 мг/кг; l оксигенотерапія; l ШВЛ при р. Н менше 7, 2; l корекція ацидозу: введення 150 -200 мл 4% розчину натрію гідрокарбонату в/в; l при неефективності лікування госпіталізувати у реанімаційне відділення l

Препарати, які не рекомендовані при бронхіальній астмі l Неселективні бета-блокатори (строго протипоказано) l Неселективні нестероїдні протизапальні препарати (строго протипоказано)

Реабілітація пацієнтів Легенева реабілітація: фізичний тренінг, корекція харчування, навчання та підтримка хворих Оксигенотерапія: залежить від ступеня тяжкості, повноцінності базової терапії, ступеня легеневої недостатності Респіраторна підтримка: штучна вентиляція легень Руководство GOLD. www. goldcopd. com

Емфізема легень l від грецької “ἐμφυσάω» – надуваю, розбухаю l Емфізема легень – захворювання дихальних шляхів, яке характеризується патологічним розширенням повітроносних просторів кінцевих бронхіол та супроводжується деструктивними змінами альвеолярних стінок; одна з частих форм хронічних неспецифічних захворювань легень

Етіологія Виділяють дві групи причин, що приводять до розвитку емфіземи легень. В першу групу входять фактори, що порушують еластичність і міцність елементів структури легень: патологічна мікроциркуляція, зміна властивостей сурфактанту, вроджений дефіцит α 1 -антитрипсину, газоподібні речовини (сполуки кадмію, окись азоту та ін. ), а також тютюновий дим, пилові частки в повітрі. Ці причини можуть привести до розвитку первинної, все дифузної емфіземи. Бронхіальна прохідність при первинній емфіземі не порушується

Етіологія Фактори другої групи сприяють підвищенню тиску в респіраторному відділі легень і посилюють розтягнення альвеол, альвеолярних ходів і респіраторних бронхіол. Найбільше значення має обструкція дихальних шляхів, що виникає при ХОЗЛ Це захворювання є основною причиною розвитку вторинної або обструктивної емфіземи легень, так як власне при ньому створюються всі умови для формування клапанного механізму перерозтягнення альвеол Важливе значення має поширення запального процесу з бронхіол на прилягаючі альвеоли з розвитком альвеоліту і деструкції міжальвеолярних перегородок

Патогенез Центролобулярна емфізема розвивається внаслідок хронічної бронхіальної обструкції, наприклад при ХОЗЛ, БА Панацинарна емфізема може бути того ж походження при більш виражених змінах або мати первинний характер, наприклад, при дефіциті α 1 -антитрипсину. При збільшенні бронхіального опору здавлюються дрібні розгалуження бронхів, звільнення альвеол затрудняється, виникає їх розтягнення, а в подальшому деструкція міжальвеолярних перетинок. Порушення співвідношення вентиляції і кровотоку призводить до зниження насичення артеріальної крові киснем, розвитку дихального ацидозу

Симптоми і перебіг Характерна задишка, «діжкоподібна» грудна клітка, зменшення дихальної екскурсії, розширення міжреберних проміжків, вибухання надключичних ямок, коробковий перкуторний звук, ослаблене дихання, зменшення області відносної тупості серця, низьке стояння куполів діафрагми та зменшення їх рухомості, підвищення прозорості легеневих полів на рентгенограмі. l При первинній емфіземі менше, ніж при вторинній, змінений газовий склад крові l

Лікування первинної емфіземи Симптоматичне лікування первинної емфіземи. Дихальна гімнастика, спрямована на максимальне включення діафрагми в акт дихання; курси кисневої терапії, виключення паління та інших шкідливих факторів, в тому числі професійних; обмеження фізичного навантаження l Впроваджується терапія інгібіторами α 1 антитрипсину l Приєднання бронхолегеневої інфекції потребує призначення антибіотиків l

Лікування вторинної емфіземи l При вторинній емфіземі проводять лікування основного захворювання (ХОЗЛ, БА) і терапію, спрямовану на купування дихальної та серцевої недостатності l Є варіанти хірургічного лікування локальної емфіземи – резекція ушкоджених ділянок легені (булл). Профілактика вторинної емфіземи зводиться до профілактики основного захворювання
BA_ukr2.ppt