ВИТАМИНЫ низкомолекулярные органические вещества различной химической природы и











































19628-lektsia_11_vitamin_i.ppt
- Количество слайдов: 103
 ВИТАМИНЫ низкомолекулярные органические вещества различной химической природы и различного строения; в организме не синтезируются, являются незаменимыми факторами пищи ; требуются в очень малых количествах; выполняют важные функции в процессе метаболизма. не включаются в структуру тканей, т.е. не являются пластическим материалом ; не используются организмом в качестве источника энергии.
ВИТАМИНЫ низкомолекулярные органические вещества различной химической природы и различного строения; в организме не синтезируются, являются незаменимыми факторами пищи ; требуются в очень малых количествах; выполняют важные функции в процессе метаболизма. не включаются в структуру тканей, т.е. не являются пластическим материалом ; не используются организмом в качестве источника энергии.
 ВИТАМИНЫ источники витаминов (пища, синтез микрофлорой кишечника вит. К, биотина, фолиевой, пантотеновой кислот и др.); потребность в них (суточная потребность – мг или доли мг, для вит. С – 100 мг);
ВИТАМИНЫ источники витаминов (пища, синтез микрофлорой кишечника вит. К, биотина, фолиевой, пантотеновой кислот и др.); потребность в них (суточная потребность – мг или доли мг, для вит. С – 100 мг);
 Классификация витаминов водорастворимые витамины (вит.В1, В2, В6, В12 РР, С, Р, фолиевая кислота, пантотеновая кислота, биотин); жирорастворимые витамины (А, Д, Е, К); витаминоподобные вещества (холин, инозит, липоевая кислота, пангамовая кислота, убихинон, парааминобензойная кислота и т.д.).
Классификация витаминов водорастворимые витамины (вит.В1, В2, В6, В12 РР, С, Р, фолиевая кислота, пантотеновая кислота, биотин); жирорастворимые витамины (А, Д, Е, К); витаминоподобные вещества (холин, инозит, липоевая кислота, пангамовая кислота, убихинон, парааминобензойная кислота и т.д.).
 Номенклатура витаминов а) буквенная (вит. А, С, К и т.д.); б) химическая (тиамин, амид никотиновой кислоты и др.); в) по названию авитаминоза с добавлением приставки “анти”, например, антиневритный, антирахитический и т.д.).
Номенклатура витаминов а) буквенная (вит. А, С, К и т.д.); б) химическая (тиамин, амид никотиновой кислоты и др.); в) по названию авитаминоза с добавлением приставки “анти”, например, антиневритный, антирахитический и т.д.).
 Провитамины – предшественники витаминов, способные в организме превращаться в витамины. (7-дегидрохолестерол вит Д3, каротины витамин А и др.).
Провитамины – предшественники витаминов, способные в организме превращаться в витамины. (7-дегидрохолестерол вит Д3, каротины витамин А и др.).
 Антивитамины – вещества, вызывающие снижение или полную потерю биологической активности витамина. 2 группы антивитаминов: антивитамины, имеющие структуру, сходную с витамином и оказывающие действие, основанное на конкурентных взаимоотношениях с ним (сульфаниламиды и ПАСК являются аналогами ПАБК и др.). неспецифические антивитамины, вызывающие расщепление и связывание витамина (тиаминаза, аскорбатоксидаза, авидин).
Антивитамины – вещества, вызывающие снижение или полную потерю биологической активности витамина. 2 группы антивитаминов: антивитамины, имеющие структуру, сходную с витамином и оказывающие действие, основанное на конкурентных взаимоотношениях с ним (сульфаниламиды и ПАСК являются аналогами ПАБК и др.). неспецифические антивитамины, вызывающие расщепление и связывание витамина (тиаминаза, аскорбатоксидаза, авидин).
 Гипо и – авитаминозы. Экзогенные причины гиповитаминозов: недостаточное поступление витаминов или полное их отсутствие в пище. Эндогенные причины: повышенная потребность в витаминах при некоторых физиологических и патологических состояниях; нарушение всасывания витаминов при заболеваниях ЖКТ, печени и поджелудочной железы; дисбактериоз кишечника; действие структурных аналогов витаминов - антивитаминов;
Гипо и – авитаминозы. Экзогенные причины гиповитаминозов: недостаточное поступление витаминов или полное их отсутствие в пище. Эндогенные причины: повышенная потребность в витаминах при некоторых физиологических и патологических состояниях; нарушение всасывания витаминов при заболеваниях ЖКТ, печени и поджелудочной железы; дисбактериоз кишечника; действие структурных аналогов витаминов - антивитаминов;
 Гипо – авитаминозы. Врожденные нарушения обмена и функции витаминов - витаминзависимые и витаминрезистентные состояния. Причина - генетические дефекты в обмене витаминов. Биохимические механизмы этих расстройств: нарушения всасывания витаминов, их транспорта, образования активных форм, взаимодействия с белками-апоферментами. Витаминзависимые и витаминрезистентные состояния развиваются независимо от поступления в организм витаминов.
Гипо – авитаминозы. Врожденные нарушения обмена и функции витаминов - витаминзависимые и витаминрезистентные состояния. Причина - генетические дефекты в обмене витаминов. Биохимические механизмы этих расстройств: нарушения всасывания витаминов, их транспорта, образования активных форм, взаимодействия с белками-апоферментами. Витаминзависимые и витаминрезистентные состояния развиваются независимо от поступления в организм витаминов.
 Гипервитаминозы Жирорастворимые витамины не выделяются с мочой, их избыток в организме оказывает токсический эффект, особенно вит. А и Д.
Гипервитаминозы Жирорастворимые витамины не выделяются с мочой, их избыток в организме оказывает токсический эффект, особенно вит. А и Д.
 Водорастворимые витамины. Основной механизм действия водорастворимых витаминов они - предшественники коферментов, т.е. их производные являются коферментами.
Водорастворимые витамины. Основной механизм действия водорастворимых витаминов они - предшественники коферментов, т.е. их производные являются коферментами.
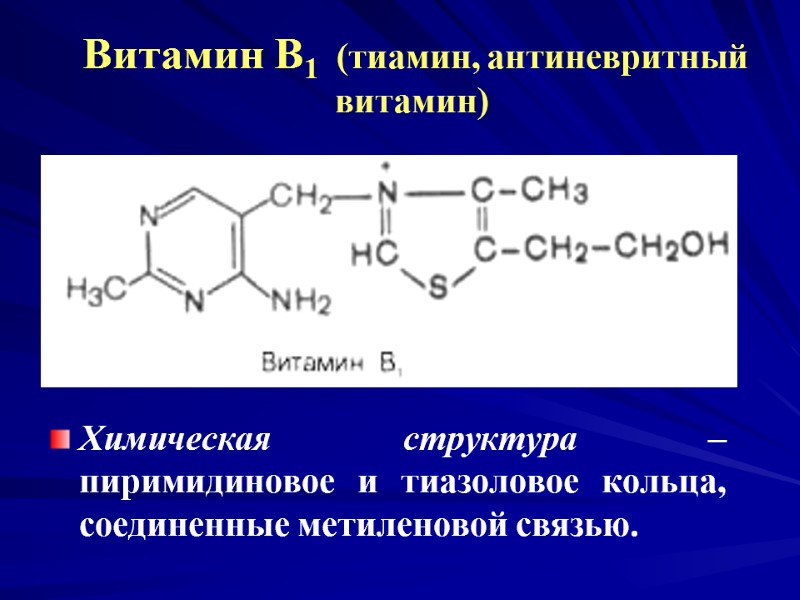
 Витамин В1 (тиамин, антиневритный витамин) Химическая структура – пиримидиновое и тиазоловое кольца, соединенные метиленовой связью.
Витамин В1 (тиамин, антиневритный витамин) Химическая структура – пиримидиновое и тиазоловое кольца, соединенные метиленовой связью.
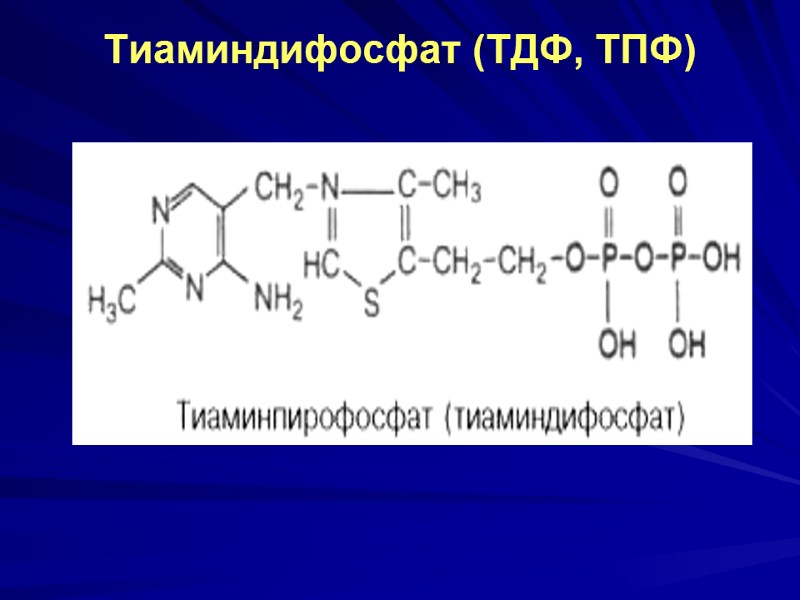
 Тиаминдифосфат (ТДФ, ТПФ)
Тиаминдифосфат (ТДФ, ТПФ)
 Биороль витамина В1 активная форма витамина – ТПФ (ТДФ) входит в состав ферментов: -пируват – и α-кетоглутаратдегидрогеназных комплексов, катализирующих окислительное декарбоксилирование ПВК и α -кетоглутарата; - транскетолазы пентозного цикла; - Авитаминоз: - полиневрит– нарушения в периферической нервной системе (бери-бери); - кардиальная форма болезни; - нарушения секреторной и моторной функции ЖКТ.
Биороль витамина В1 активная форма витамина – ТПФ (ТДФ) входит в состав ферментов: -пируват – и α-кетоглутаратдегидрогеназных комплексов, катализирующих окислительное декарбоксилирование ПВК и α -кетоглутарата; - транскетолазы пентозного цикла; - Авитаминоз: - полиневрит– нарушения в периферической нервной системе (бери-бери); - кардиальная форма болезни; - нарушения секреторной и моторной функции ЖКТ.
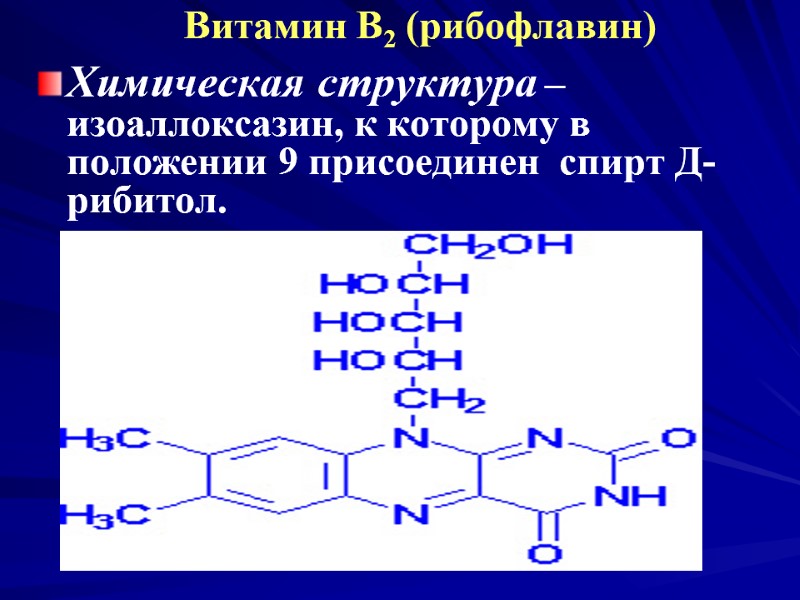
 Витамин В2 (рибофлавин) Химическая структура – изоаллоксазин, к которому в положении 9 присоединен спирт Д- рибитол.
Витамин В2 (рибофлавин) Химическая структура – изоаллоксазин, к которому в положении 9 присоединен спирт Д- рибитол.
 Биороль витамина В2 – участие в построении ФМН и ФАД – коферментов флавиновых ферментов (НАДН-дегидрогеназы дыхательной цепи, ацилКоА-дегидрогеназы, МАО, сукцинатдегидрогеназы, ксантиноксидазы, оксидаз L и D-аминокислот и др). Гипо- и авитаминоз - нарушения ЦТК, ЦПЭ, β-окисления, обмена ЖК, биогенных аминов и т. д. Признаки авитаминоза – ангулярный стоматит, кератиты, катаракта.
Биороль витамина В2 – участие в построении ФМН и ФАД – коферментов флавиновых ферментов (НАДН-дегидрогеназы дыхательной цепи, ацилКоА-дегидрогеназы, МАО, сукцинатдегидрогеназы, ксантиноксидазы, оксидаз L и D-аминокислот и др). Гипо- и авитаминоз - нарушения ЦТК, ЦПЭ, β-окисления, обмена ЖК, биогенных аминов и т. д. Признаки авитаминоза – ангулярный стоматит, кератиты, катаракта.
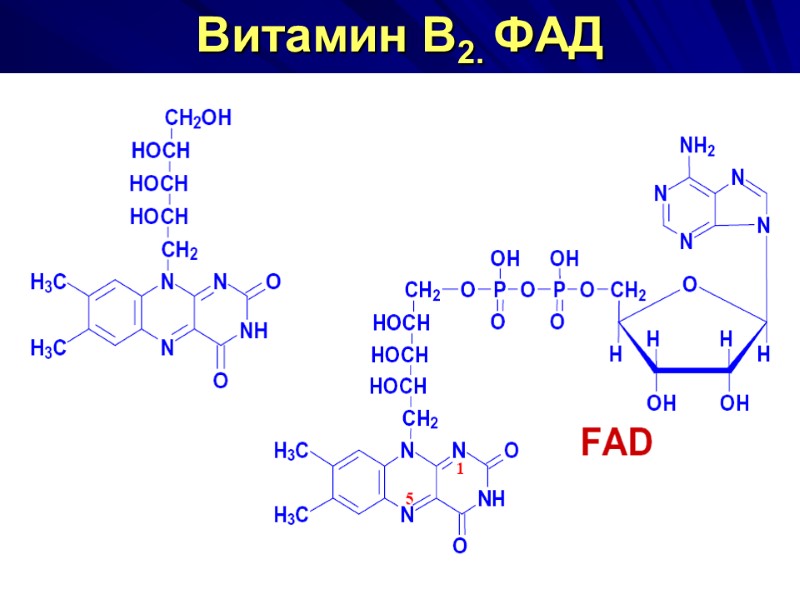
 Витамин В2. ФАД
Витамин В2. ФАД
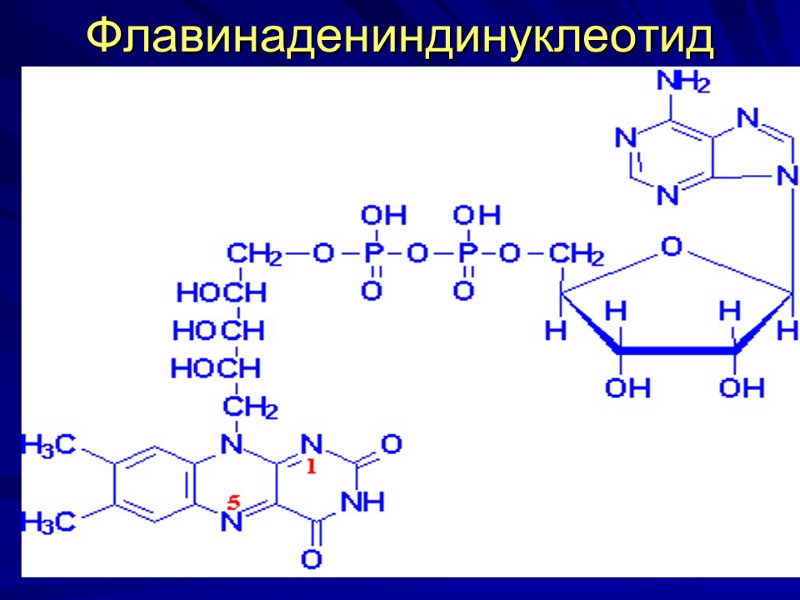
 Флавинадениндинуклеотид
Флавинадениндинуклеотид
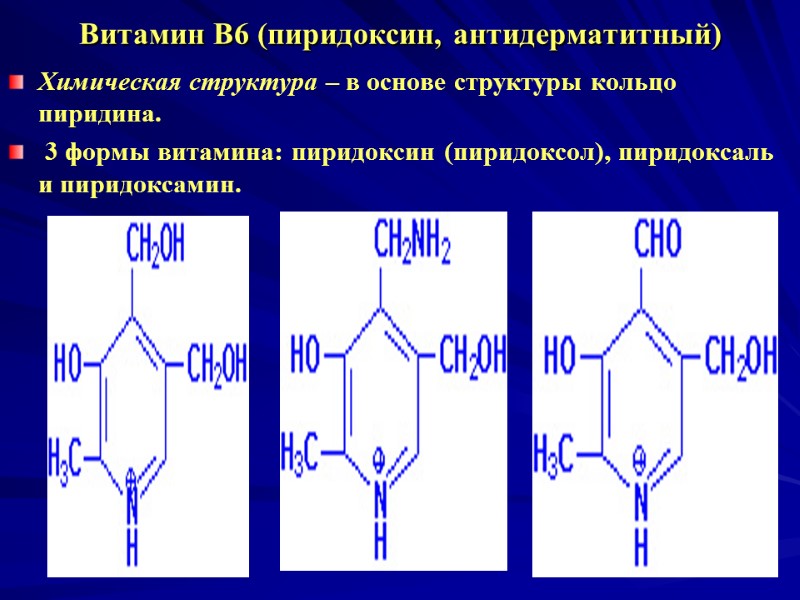
 Витамин В6 (пиридоксин, антидерматитный) Химическая структура – в основе структуры кольцо пиридина. 3 формы витамина: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин.
Витамин В6 (пиридоксин, антидерматитный) Химическая структура – в основе структуры кольцо пиридина. 3 формы витамина: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин.
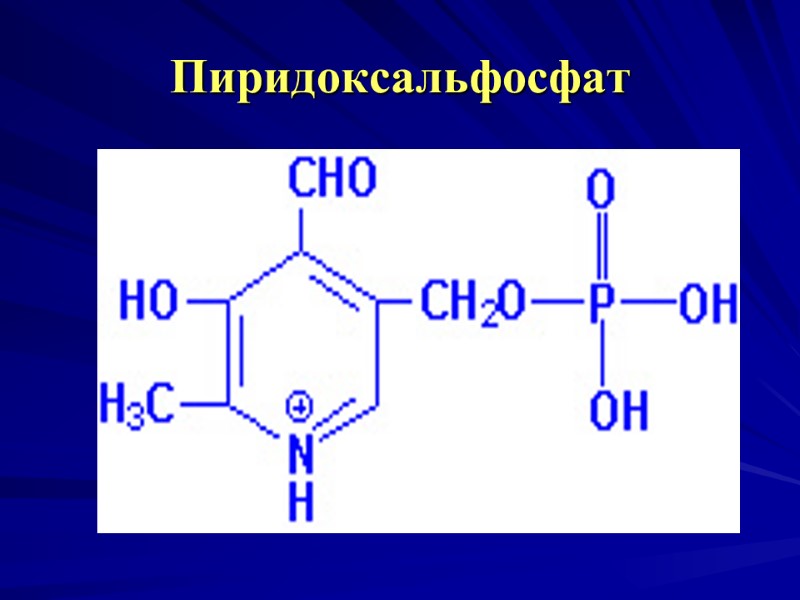
 Пиридоксальфосфат
Пиридоксальфосфат
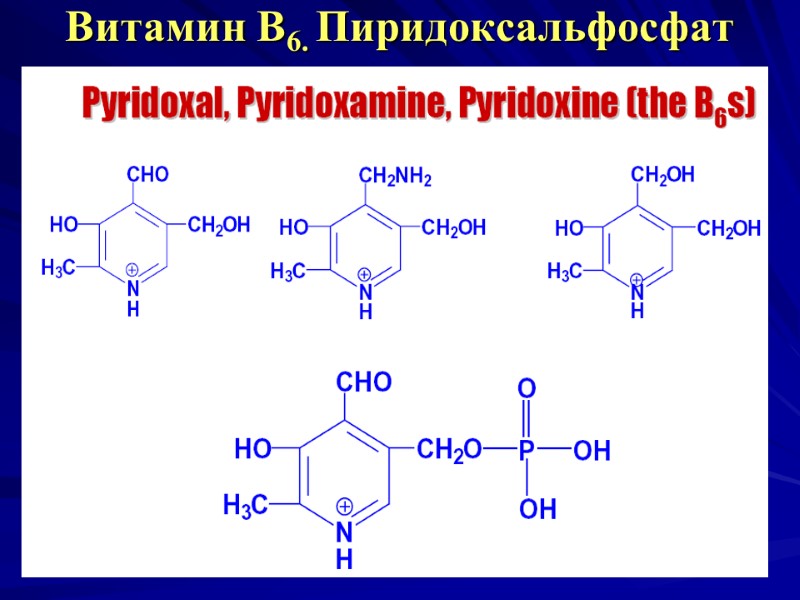
 Витамин В6. Пиридоксальфосфат
Витамин В6. Пиридоксальфосфат
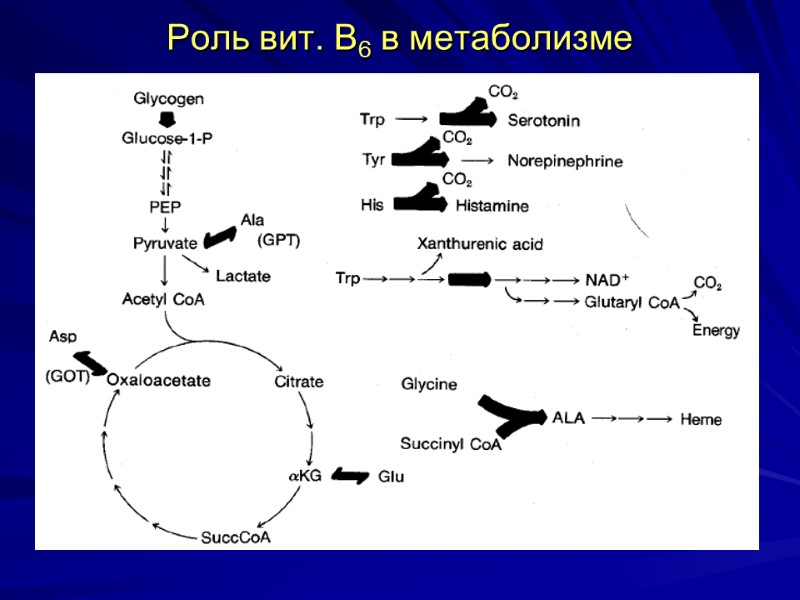
 Биороль витамина В6 Пиридоксальфосфат (ПФ) и фосфопиридоксамин являются коферментами: - аминотрансфераз (трансаминаз), - декарбоксилаз аминокислот, - серин-и треониндегидратаз (неокислительное дезаминирования серина и треонина), - δ-аминолевулинатсинтазы (синтез гема) и др. Гипо- и авитаминоз вит. В6 - нарушение биосинтеза заменимых аминокислот, биогенных аминов, ГАМК, гема и т.д. признаки авитаминоза – специфический дерматит.
Биороль витамина В6 Пиридоксальфосфат (ПФ) и фосфопиридоксамин являются коферментами: - аминотрансфераз (трансаминаз), - декарбоксилаз аминокислот, - серин-и треониндегидратаз (неокислительное дезаминирования серина и треонина), - δ-аминолевулинатсинтазы (синтез гема) и др. Гипо- и авитаминоз вит. В6 - нарушение биосинтеза заменимых аминокислот, биогенных аминов, ГАМК, гема и т.д. признаки авитаминоза – специфический дерматит.
 Роль вит. В6 в метаболизме
Роль вит. В6 в метаболизме
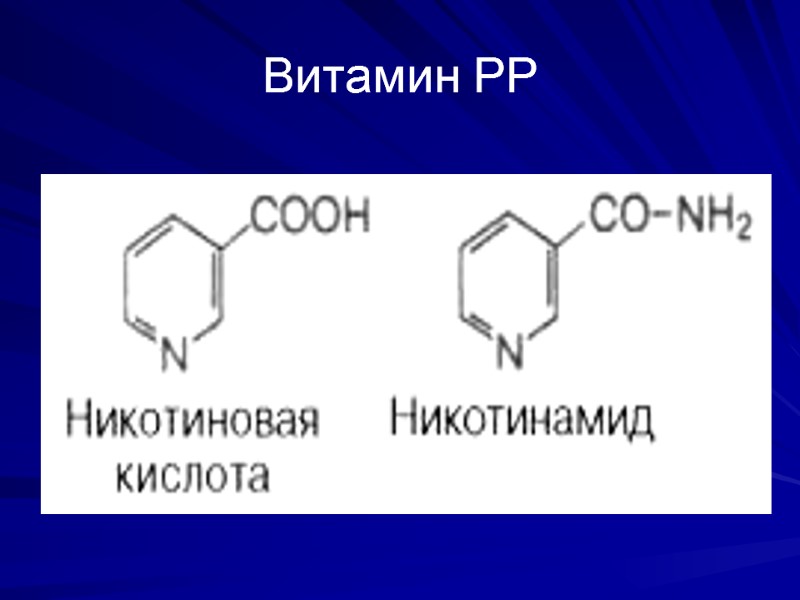
 Витамин РР
Витамин РР
 Витамин РР (ниацин, вит. В3, никотиновая к-та, никотинамид) может синтезироваться из незаменимой АК триптофан. Хим. структура – пиридиновое кольцо, содержащее карбоксильную группу, у никотинамида – амидная группа. Биороль: в составе НАД и НАДФ входит в состав глутаматдегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, изоцитратдегидрогеназы глюкозо-6-фосфатдегидрогеназы и др. Авитаминоз – пеллагра (дерматит, диарея, деменция)
Витамин РР (ниацин, вит. В3, никотиновая к-та, никотинамид) может синтезироваться из незаменимой АК триптофан. Хим. структура – пиридиновое кольцо, содержащее карбоксильную группу, у никотинамида – амидная группа. Биороль: в составе НАД и НАДФ входит в состав глутаматдегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, изоцитратдегидрогеназы глюкозо-6-фосфатдегидрогеназы и др. Авитаминоз – пеллагра (дерматит, диарея, деменция)
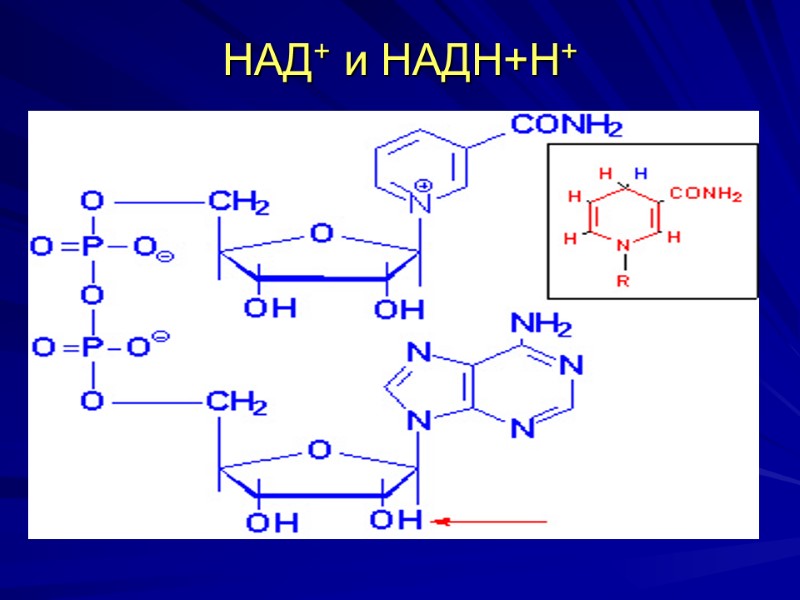
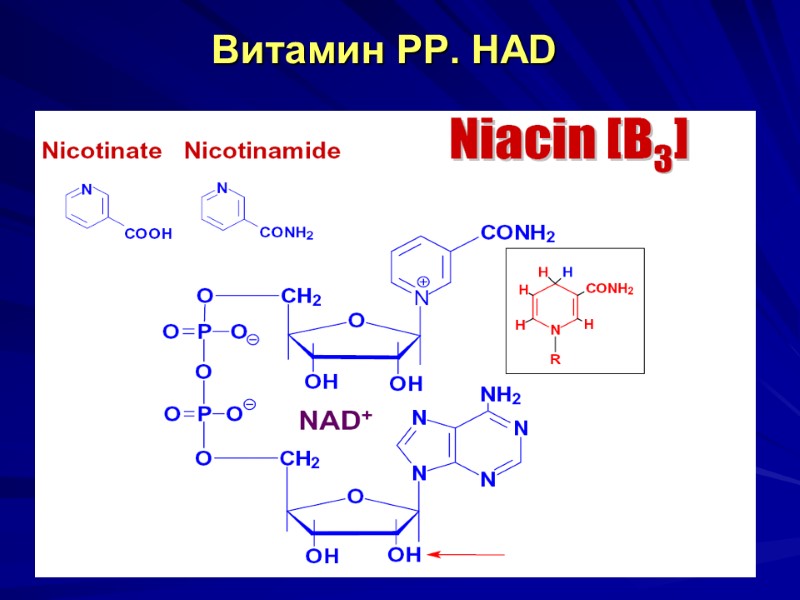
 Витамин РР может синтезироваться из незаменимой АК триптофан. Хим. структура – пиридиновое кольцо, содержащее карбоксильную группу, у никотинамида – амидная группа. Биороль: в составе НАД и НАДФ входит в состав ферментов глутаматдегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, изоцитратдегидрогеназы, глюкозо-6-фосфатдегидрогеназы и др. Авитаминоз – пеллагра (дерматит, диарея, деменция)
Витамин РР может синтезироваться из незаменимой АК триптофан. Хим. структура – пиридиновое кольцо, содержащее карбоксильную группу, у никотинамида – амидная группа. Биороль: в составе НАД и НАДФ входит в состав ферментов глутаматдегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, изоцитратдегидрогеназы, глюкозо-6-фосфатдегидрогеназы и др. Авитаминоз – пеллагра (дерматит, диарея, деменция)
 НАД+ и НАДН+Н+
НАД+ и НАДН+Н+
 Витамин РР. НАD
Витамин РР. НАD
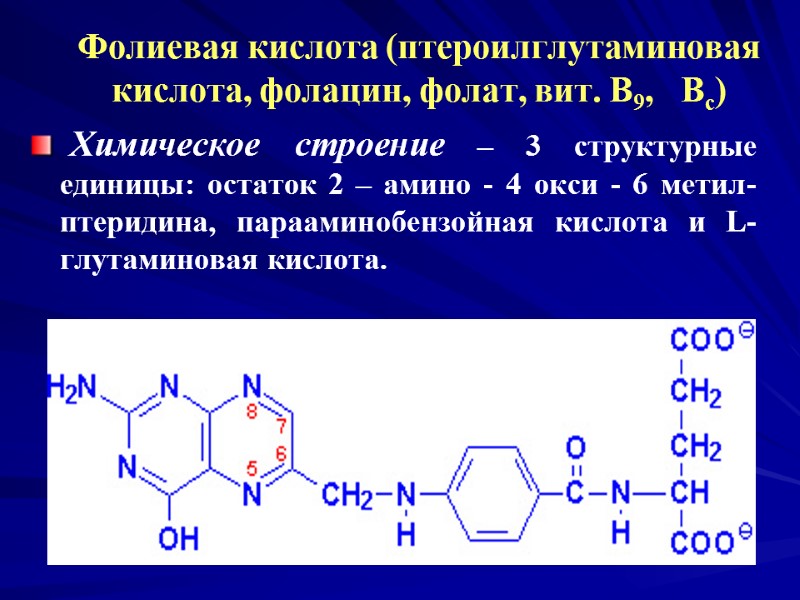
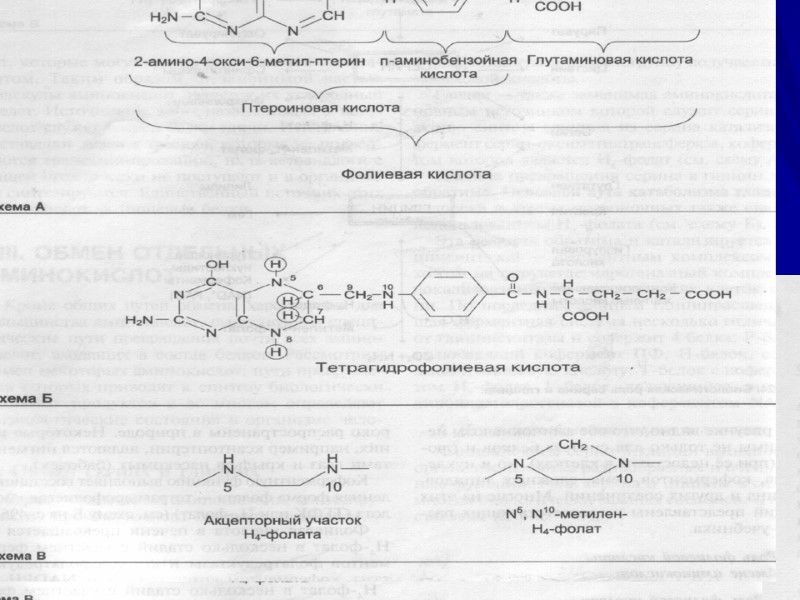
 Фолиевая кислота (птероилглутаминовая кислота, фолацин, фолат, вит. В9, Вс) Химическое строение – 3 структурные единицы: остаток 2 – амино - 4 окси - 6 метил-птеридина, парааминобензойная кислота и L-глутаминовая кислота.
Фолиевая кислота (птероилглутаминовая кислота, фолацин, фолат, вит. В9, Вс) Химическое строение – 3 структурные единицы: остаток 2 – амино - 4 окси - 6 метил-птеридина, парааминобензойная кислота и L-глутаминовая кислота.
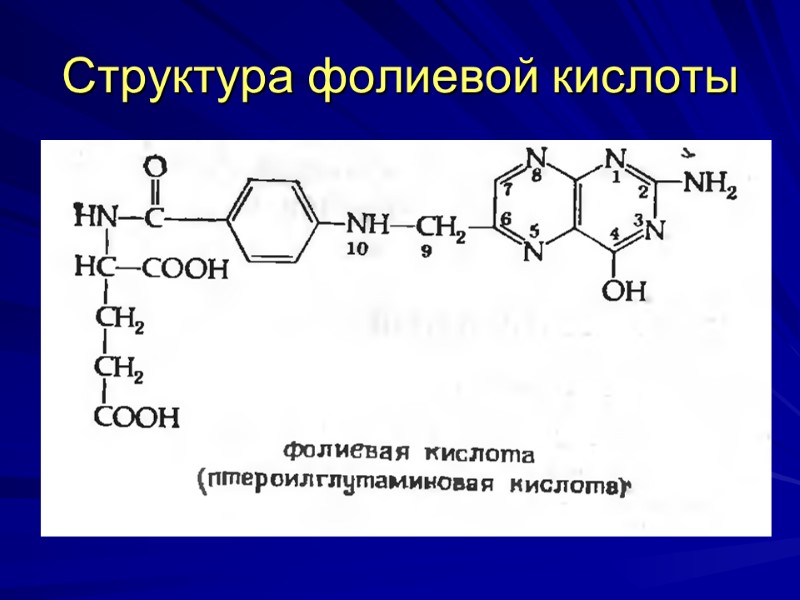
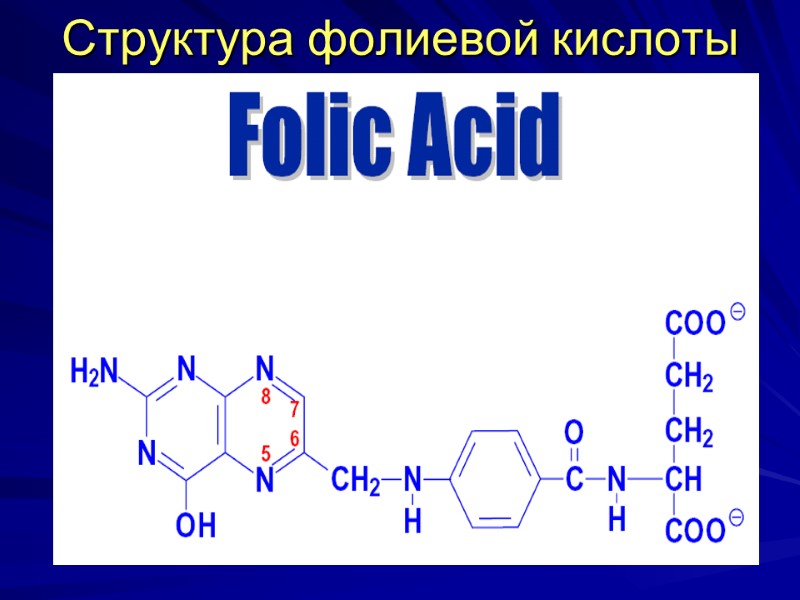
 Структура фолиевой кислоты
Структура фолиевой кислоты

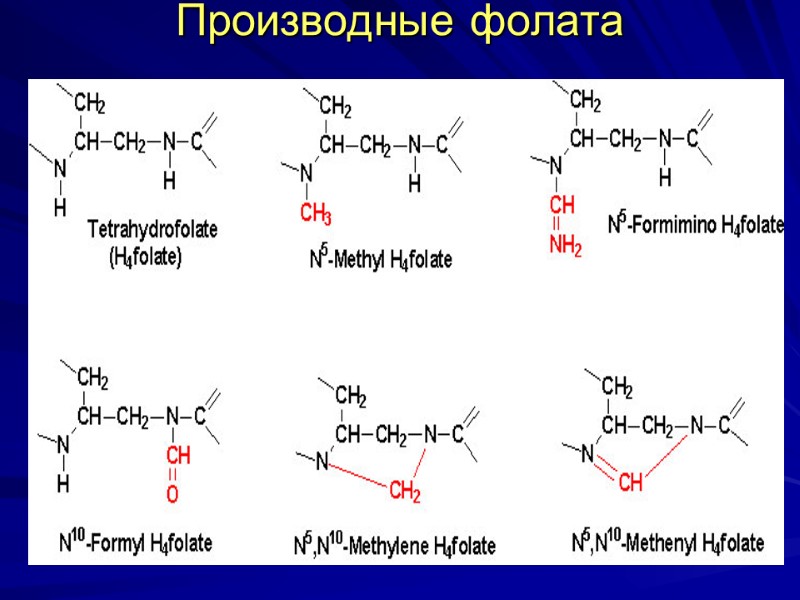
 Биороль ФК входит в состав кофермента ТГФК (Н4-фолат). Все производные Н4-фолата –промежуточные переносчики одноуглеродных фрагментов [C1]. 6 одноуглеродных групп, включающихся в превращения в составе ТГФК: формильная ( -СНО), метенильная (-СН=), метильная ( -СН3) оксиметильная (-СН2ОН), метиленовая ( -СН2-) формиминовая ( -СН=NН).
Биороль ФК входит в состав кофермента ТГФК (Н4-фолат). Все производные Н4-фолата –промежуточные переносчики одноуглеродных фрагментов [C1]. 6 одноуглеродных групп, включающихся в превращения в составе ТГФК: формильная ( -СНО), метенильная (-СН=), метильная ( -СН3) оксиметильная (-СН2ОН), метиленовая ( -СН2-) формиминовая ( -СН=NН).
 Структура фолиевой кислоты
Структура фолиевой кислоты
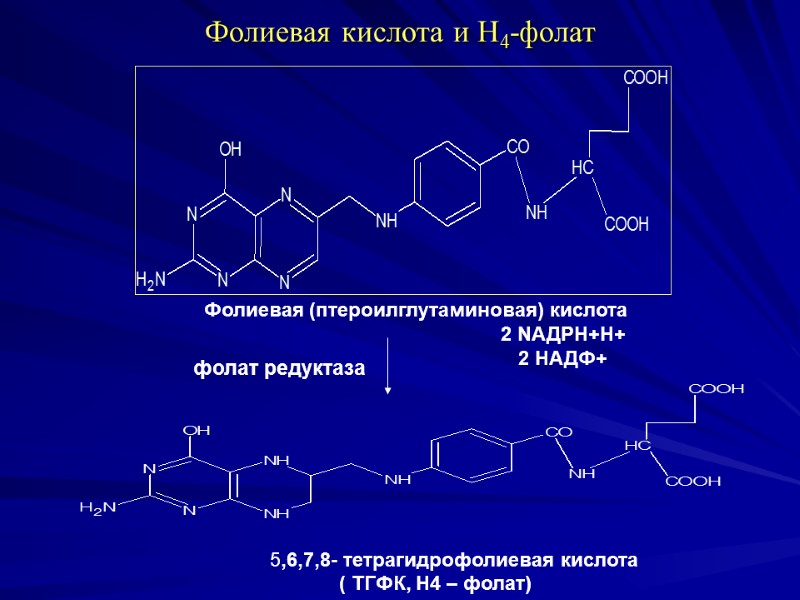
 Фолиевая кислота и Н4-фолат Фолиевая (птероилглутаминовая) кислота 2 NАДРН+Н+ 2 НАДФ+ 5,6,7,8- тетрагидрофолиевая кислота ( ТГФК, Н4 – фолат) фолат редуктаза
Фолиевая кислота и Н4-фолат Фолиевая (птероилглутаминовая) кислота 2 NАДРН+Н+ 2 НАДФ+ 5,6,7,8- тетрагидрофолиевая кислота ( ТГФК, Н4 – фолат) фолат редуктаза
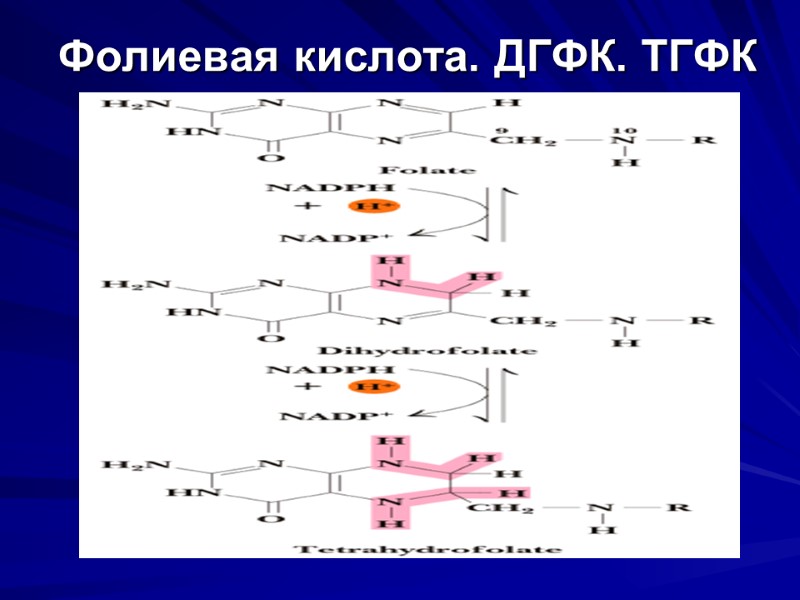
 Фолиевая кислота. ДГФК. ТГФК
Фолиевая кислота. ДГФК. ТГФК
 Биороль Н4-фолата ТГФК образует коферменты, содержащие одноуглеродные фрагменты, присоединенные к атому N в положении 5 или к атому N в положении 10 (или к обоим). Коферменты ТГФК, содержащие одноуглеродные фрагменты, присоединенные к 5 атому N: - N5-формил-ТГФК (N5 СНО-Н4-фолат); - N5-метил-ТГФК (N5-СН3-Н4-фолат) — регенерация мет из гомоцистеина. N5-метил-Н4-фолат Н4-фолат Гомоцистеин метионин гомоцистеинметилтрансфераза
Биороль Н4-фолата ТГФК образует коферменты, содержащие одноуглеродные фрагменты, присоединенные к атому N в положении 5 или к атому N в положении 10 (или к обоим). Коферменты ТГФК, содержащие одноуглеродные фрагменты, присоединенные к 5 атому N: - N5-формил-ТГФК (N5 СНО-Н4-фолат); - N5-метил-ТГФК (N5-СН3-Н4-фолат) — регенерация мет из гомоцистеина. N5-метил-Н4-фолат Н4-фолат Гомоцистеин метионин гомоцистеинметилтрансфераза
 Биороль Н4-фолата к 10 атому N – - N10-формил-ТГФК (N10-СНО-Н4-фолат) — синтез пуриновых нуклеотидов (атом С во 2 положении); - синтез тРНКфМет у прокариот; к 5 и 10 атомам N : - N5,N10-метилен-ТГФК (N5,N10-СН2-Н4-фолат) — синтез тимидиловых нуклеотидов, синтез серина из глицина; - N5,N10-метенил-ТГФК (N5, N10=СН-Н4–фолат) — синтез пуриновых. нуклеотидов (атом С в положении 8). Гиповитаминоз – нарушение синтеза белка и нуклеиновых кислот — макроцитарная анемия.
Биороль Н4-фолата к 10 атому N – - N10-формил-ТГФК (N10-СНО-Н4-фолат) — синтез пуриновых нуклеотидов (атом С во 2 положении); - синтез тРНКфМет у прокариот; к 5 и 10 атомам N : - N5,N10-метилен-ТГФК (N5,N10-СН2-Н4-фолат) — синтез тимидиловых нуклеотидов, синтез серина из глицина; - N5,N10-метенил-ТГФК (N5, N10=СН-Н4–фолат) — синтез пуриновых. нуклеотидов (атом С в положении 8). Гиповитаминоз – нарушение синтеза белка и нуклеиновых кислот — макроцитарная анемия.
 Производные фолата
Производные фолата
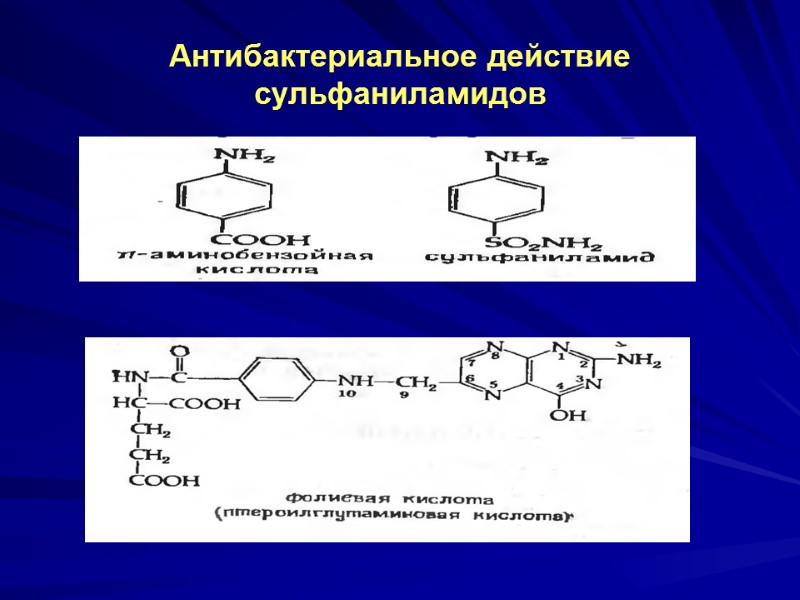
 Антибактериальное действие сульфаниламидов
Антибактериальное действие сульфаниламидов
 Антибактериальное действие сульфаниламидов. Аналоги ФК - цитостатики Антибактериальное действие сульфаниламидов основано на их способности включаться вместо ПАБК (из-за сходства в строении) в структуру ФК, что ведет к блокаде синтеза нуклеиновых кислот у бактерий. Структурные аналоги ФК - 4-аминоптерин и метотрексат (-СН3 у N10) – конкурентные ингибиторы фолатредуктазы, блокируют синтез дТМФ и ДНК, являются цитостатиками, используются в химиотерапии рака.
Антибактериальное действие сульфаниламидов. Аналоги ФК - цитостатики Антибактериальное действие сульфаниламидов основано на их способности включаться вместо ПАБК (из-за сходства в строении) в структуру ФК, что ведет к блокаде синтеза нуклеиновых кислот у бактерий. Структурные аналоги ФК - 4-аминоптерин и метотрексат (-СН3 у N10) – конкурентные ингибиторы фолатредуктазы, блокируют синтез дТМФ и ДНК, являются цитостатиками, используются в химиотерапии рака.
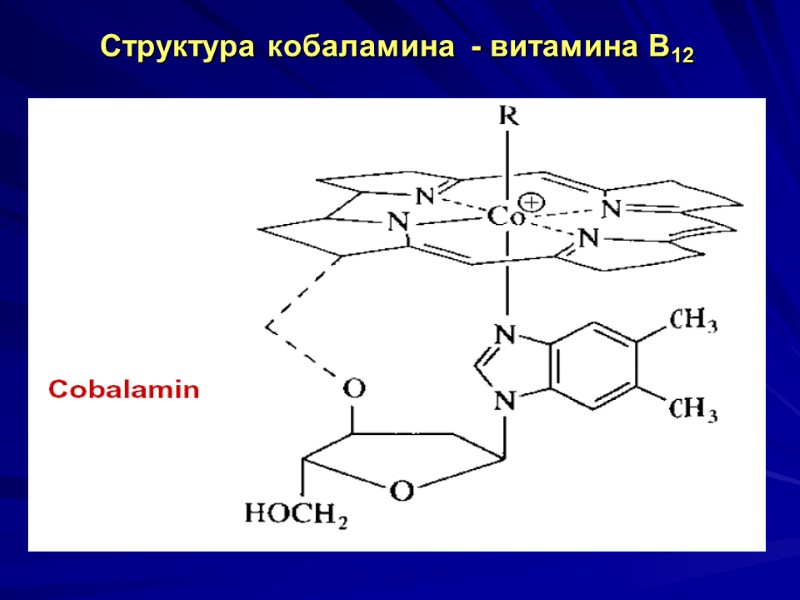
 Структура кобаламина - витамина В12
Структура кобаламина - витамина В12
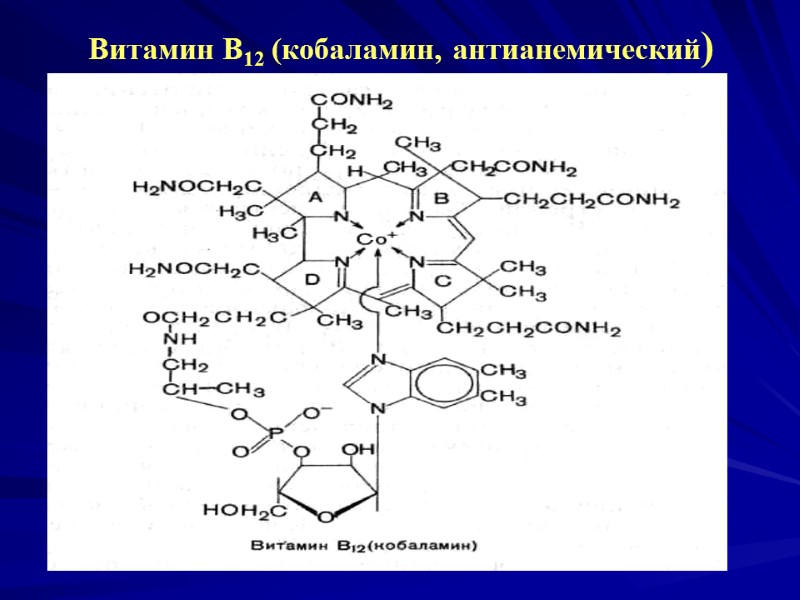
 Витамин В12 (кобаламин, антианемический) Вит.В12 - единственный витамин , содержащий в составе Ме и единственный витамин, синтезирующийся исключительно микроорганизмами. Химическая структура – 2 части: - планарная – порфириноподобное корриновое кольцо с центральным атомом Со; - нуклеотидная часть, содержащая 5,6- диметилбензимидазол, рибозу и остаток фосфата у 3 атома углерода.
Витамин В12 (кобаламин, антианемический) Вит.В12 - единственный витамин , содержащий в составе Ме и единственный витамин, синтезирующийся исключительно микроорганизмами. Химическая структура – 2 части: - планарная – порфириноподобное корриновое кольцо с центральным атомом Со; - нуклеотидная часть, содержащая 5,6- диметилбензимидазол, рибозу и остаток фосфата у 3 атома углерода.
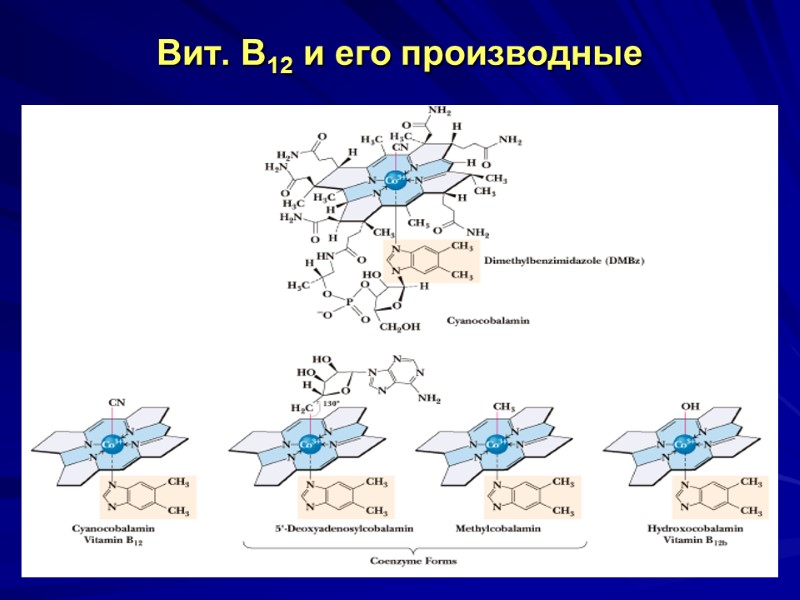
 Вит. В12 и его производные
Вит. В12 и его производные
 Витамин В12 (кобаламин, антианемический) Производные кобаламина – оксикобаламин, хлоркобаламин, цианокобаламин, аквакобаламин, нитритокобаламин, дезоксиаденозилкобаламин и метилкобаламин Два В12–кофермента (кобамидных кофермента) - метилкобаламин (СН3- В12) и дезоксиаденозилкобаламин
Витамин В12 (кобаламин, антианемический) Производные кобаламина – оксикобаламин, хлоркобаламин, цианокобаламин, аквакобаламин, нитритокобаламин, дезоксиаденозилкобаламин и метилкобаламин Два В12–кофермента (кобамидных кофермента) - метилкобаламин (СН3- В12) и дезоксиаденозилкобаламин
 Производные вит. В12
Производные вит. В12
 Витамин В12 (кобаламин, антианемический)
Витамин В12 (кобаламин, антианемический)
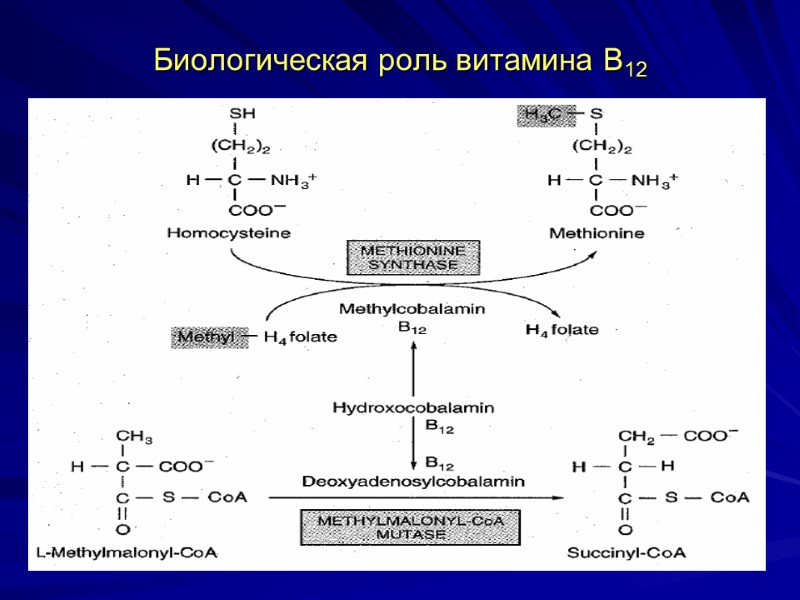
 Участие витамина В12 в обмене метилкобаламин - кофермент в реакциях трансметилирования (регенерация метионина из гомоцистеина), участвует в переносе метильных групп с N5-метил-Н4-фолата на гомоцистеин с образованием метионина и Н4-фолата. Метионин необходим для метилирования различных соединений, например, синтез креатина, адреналина, превращение фосфатидилэтаноламина в фосфатидилхолин. Реакции трансметилирования происходят при синтезе нуклеотидов и нуклеиновых кислот, при недостатке вит. В12 нарушается синтез нуклеиновых кислот, страдает кроветворная система, развивается мегалобластическая анемия.
Участие витамина В12 в обмене метилкобаламин - кофермент в реакциях трансметилирования (регенерация метионина из гомоцистеина), участвует в переносе метильных групп с N5-метил-Н4-фолата на гомоцистеин с образованием метионина и Н4-фолата. Метионин необходим для метилирования различных соединений, например, синтез креатина, адреналина, превращение фосфатидилэтаноламина в фосфатидилхолин. Реакции трансметилирования происходят при синтезе нуклеотидов и нуклеиновых кислот, при недостатке вит. В12 нарушается синтез нуклеиновых кислот, страдает кроветворная система, развивается мегалобластическая анемия.
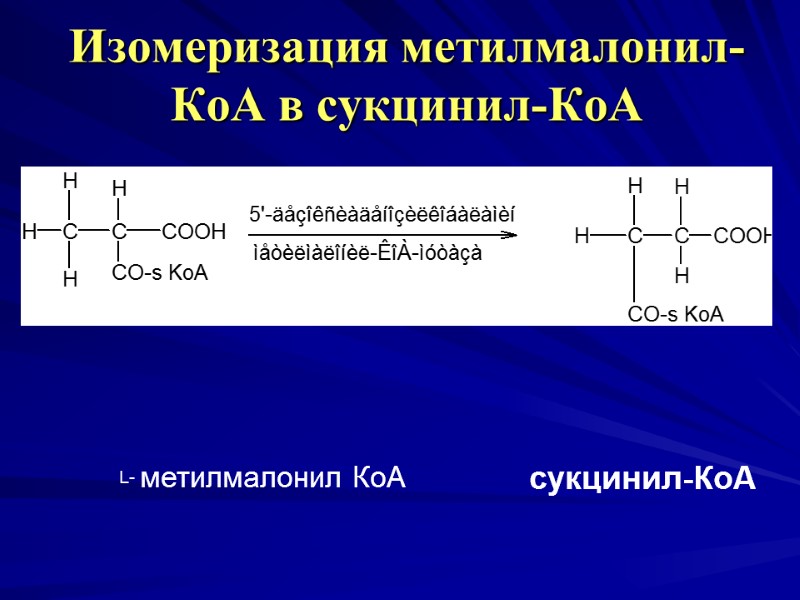
 Участие витамина В12 в обмене 5 дезоксиаденозилкобаламин – кофермент, необходимый для внутримолекулярного переноса водорода в реакциях изомеризации (изомеризация метилмалонил-КоА в сукцинил-КоА с участием метималонил-КоА-мутазы). Метилмалонил-Коа образуется из жирных кислот с нечетным числом атомов С и аминокислот с разветвленным радикалом. При недостатке вит.В12 накапливается метилмалонил-КоА, который токсичен для нервной ткани, возникает поражение задне-боковых столбов спинного мозга.
Участие витамина В12 в обмене 5 дезоксиаденозилкобаламин – кофермент, необходимый для внутримолекулярного переноса водорода в реакциях изомеризации (изомеризация метилмалонил-КоА в сукцинил-КоА с участием метималонил-КоА-мутазы). Метилмалонил-Коа образуется из жирных кислот с нечетным числом атомов С и аминокислот с разветвленным радикалом. При недостатке вит.В12 накапливается метилмалонил-КоА, который токсичен для нервной ткани, возникает поражение задне-боковых столбов спинного мозга.
 Изомеризация метилмалонил-КоА в сукцинил-КоА L- метилмалонил КоА сукцинил-КоА
Изомеризация метилмалонил-КоА в сукцинил-КоА L- метилмалонил КоА сукцинил-КоА
 Биологическая роль витамина В12
Биологическая роль витамина В12
 Гиповитаминоз витамина В12 Наиболее частая причина нарушения всасывания вит. В12 в тонком кишечнике – недостаток гликопротеида внутреннего фактора Касла, который синтезируется париетальными клетками слизистой желудка. транспорт в крови вит. В12 в составе транскобаламина I и II. Транскобаламин I - депо вит. В12. Гиповитаминоз вит. В12 - развитие макроцитарной (мегалобластической) анемии с неврологическими нарушениями.
Гиповитаминоз витамина В12 Наиболее частая причина нарушения всасывания вит. В12 в тонком кишечнике – недостаток гликопротеида внутреннего фактора Касла, который синтезируется париетальными клетками слизистой желудка. транспорт в крови вит. В12 в составе транскобаламина I и II. Транскобаламин I - депо вит. В12. Гиповитаминоз вит. В12 - развитие макроцитарной (мегалобластической) анемии с неврологическими нарушениями.
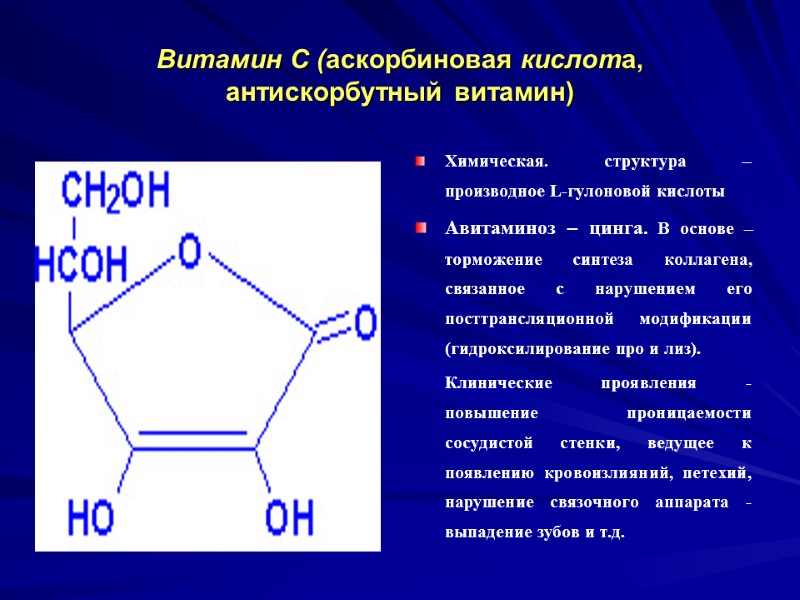
 Витамин С (аскорбиновая кислота, антискорбутный витамин) Химическая. структура – производное L-гулоновой кислоты Авитаминоз – цинга. В основе – торможение синтеза коллагена, связанное с нарушением его посттрансляционной модификации (гидроксилирование про и лиз). Клинические проявления - повышение проницаемости сосудистой стенки, ведущее к появлению кровоизлияний, петехий, нарушение связочного аппарата - выпадение зубов и т.д.
Витамин С (аскорбиновая кислота, антискорбутный витамин) Химическая. структура – производное L-гулоновой кислоты Авитаминоз – цинга. В основе – торможение синтеза коллагена, связанное с нарушением его посттрансляционной модификации (гидроксилирование про и лиз). Клинические проявления - повышение проницаемости сосудистой стенки, ведущее к появлению кровоизлияний, петехий, нарушение связочного аппарата - выпадение зубов и т.д.
 Биороль витамина С Участие в окислительно-восстановительных реакциях; участие в реакциях гидроксилирования: - гидроксилирование про и лиз в проколлагене (синтез коллагена), - синтез норадреналина из дофамина, образующегося из тирозина, - синтез кортикостероидов, - гидроксилирование триптофана в положении 5 (синтез серотонина), - в обмене тирозина (синтез гомогентизиновой кислоты); обладает антиоксидантным действием, предотвращая ПОЛ; в кишечнике восстанавливает Fе3+ в Fе2+, способствуя его всасыванию, ускоряет освобождение Fе из ферритина; способствует освобождению Fе из связанной транспортной формы (из комплекса с трансферрином),
Биороль витамина С Участие в окислительно-восстановительных реакциях; участие в реакциях гидроксилирования: - гидроксилирование про и лиз в проколлагене (синтез коллагена), - синтез норадреналина из дофамина, образующегося из тирозина, - синтез кортикостероидов, - гидроксилирование триптофана в положении 5 (синтез серотонина), - в обмене тирозина (синтез гомогентизиновой кислоты); обладает антиоксидантным действием, предотвращая ПОЛ; в кишечнике восстанавливает Fе3+ в Fе2+, способствуя его всасыванию, ускоряет освобождение Fе из ферритина; способствует освобождению Fе из связанной транспортной формы (из комплекса с трансферрином),
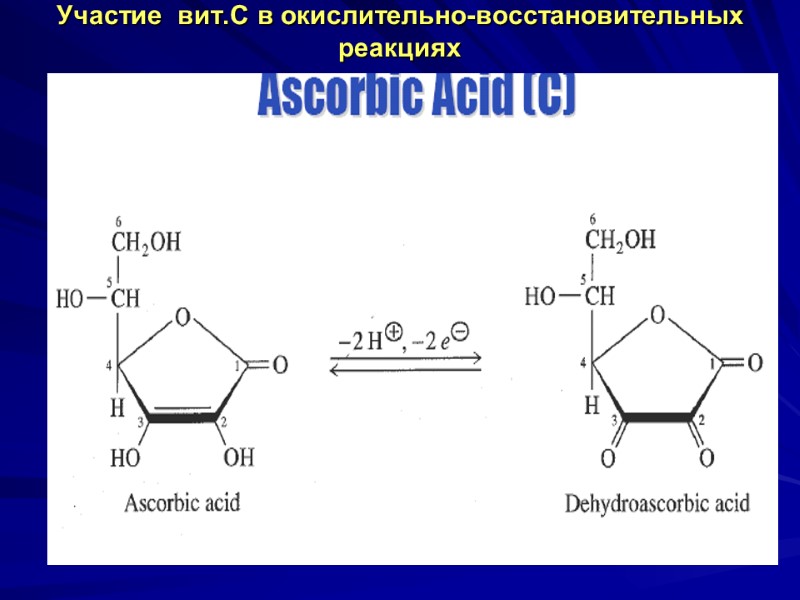
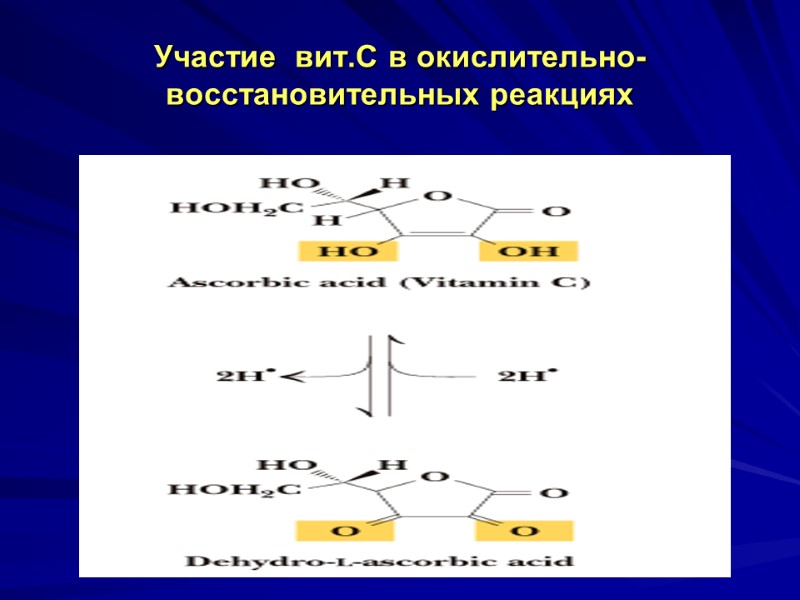
 Участие вит.С в окислительно-восстановительных реакциях
Участие вит.С в окислительно-восстановительных реакциях
 Участие вит.С в окислительно-восстановительных реакциях
Участие вит.С в окислительно-восстановительных реакциях
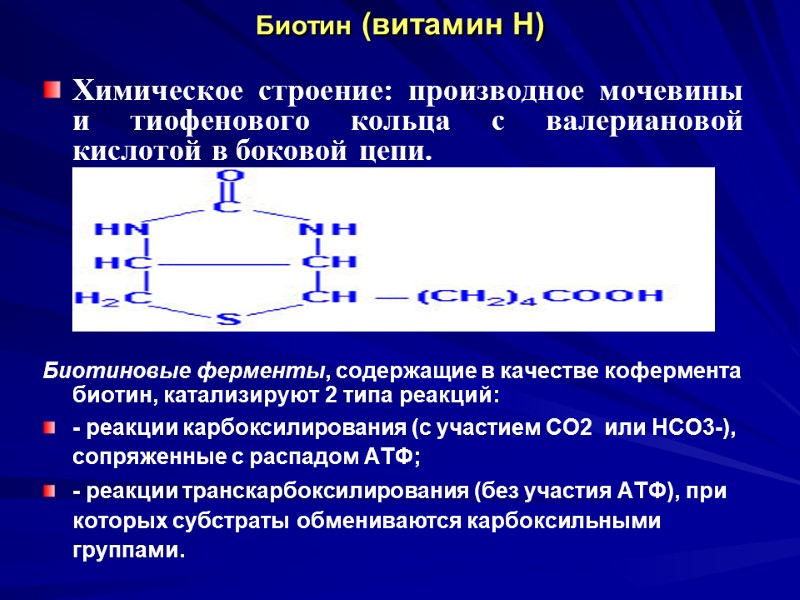
 Биотин (витамин Н) Химическое строение: производное мочевины и тиофенового кольца с валериановой кислотой в боковой цепи. Биотиновые ферменты, содержащие в качестве кофермента биотин, катализируют 2 типа реакций: - реакции карбоксилирования (с участием СО2 или НСО3-), сопряженные с распадом АТФ; - реакции транскарбоксилирования (без участия АТФ), при которых субстраты обмениваются карбоксильными группами.
Биотин (витамин Н) Химическое строение: производное мочевины и тиофенового кольца с валериановой кислотой в боковой цепи. Биотиновые ферменты, содержащие в качестве кофермента биотин, катализируют 2 типа реакций: - реакции карбоксилирования (с участием СО2 или НСО3-), сопряженные с распадом АТФ; - реакции транскарбоксилирования (без участия АТФ), при которых субстраты обмениваются карбоксильными группами.
 Биотин (витамин Н) входит в состав ферментов: - карбамоилфосфатсинтетазы I и II (синтез мочевины, пиримидинов), - пируваткарбоксилазы (ПВК → ЩУК → ФЭП → глю), - ацетил-КоА-- карбоксилазы (ацетил-КоА → малонил-КоА), - пропионил-КоА-карбоксилазы (пропионил-КоА → метилмалонил-КоА → сукцинил-КоА). Антагонист биотина – авидин (гликопротеид). Авитаминоз – нарушение синтеза нуклеиновых кислот, мочевины, ВЖК, а также глюконеогенеза. Клинические проявления - дерматит
Биотин (витамин Н) входит в состав ферментов: - карбамоилфосфатсинтетазы I и II (синтез мочевины, пиримидинов), - пируваткарбоксилазы (ПВК → ЩУК → ФЭП → глю), - ацетил-КоА-- карбоксилазы (ацетил-КоА → малонил-КоА), - пропионил-КоА-карбоксилазы (пропионил-КоА → метилмалонил-КоА → сукцинил-КоА). Антагонист биотина – авидин (гликопротеид). Авитаминоз – нарушение синтеза нуклеиновых кислот, мочевины, ВЖК, а также глюконеогенеза. Клинические проявления - дерматит
 Биотин Антагонист биотина – авидин (гликопротеид). Авитаминоз – нарушение синтеза нуклеиновых кислот, мочевины, ВЖК, а также глюконеогенеза. Клинические проявления -дерматит
Биотин Антагонист биотина – авидин (гликопротеид). Авитаминоз – нарушение синтеза нуклеиновых кислот, мочевины, ВЖК, а также глюконеогенеза. Клинические проявления -дерматит
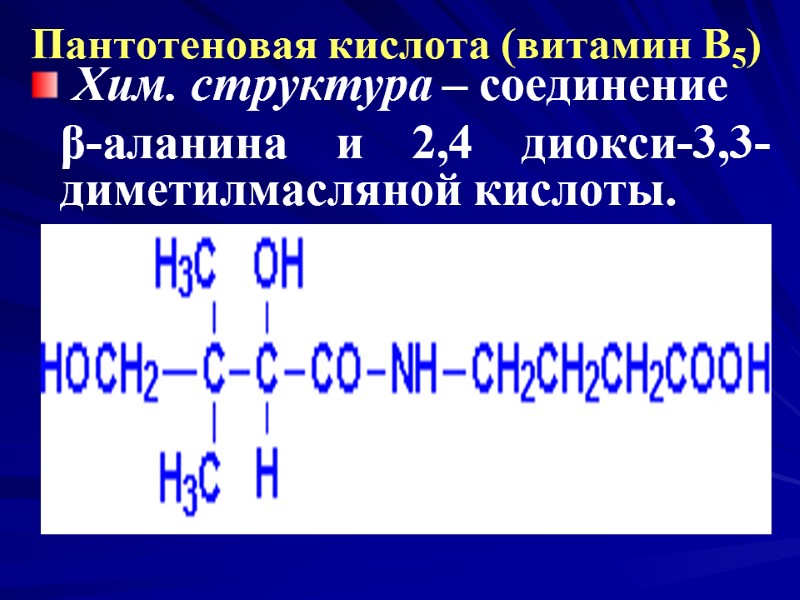
 Пантотеновая кислота (витамин В5) Хим. структура – соединение β-аланина и 2,4 диокси-3,3- диметилмасляной кислоты.
Пантотеновая кислота (витамин В5) Хим. структура – соединение β-аланина и 2,4 диокси-3,3- диметилмасляной кислоты.
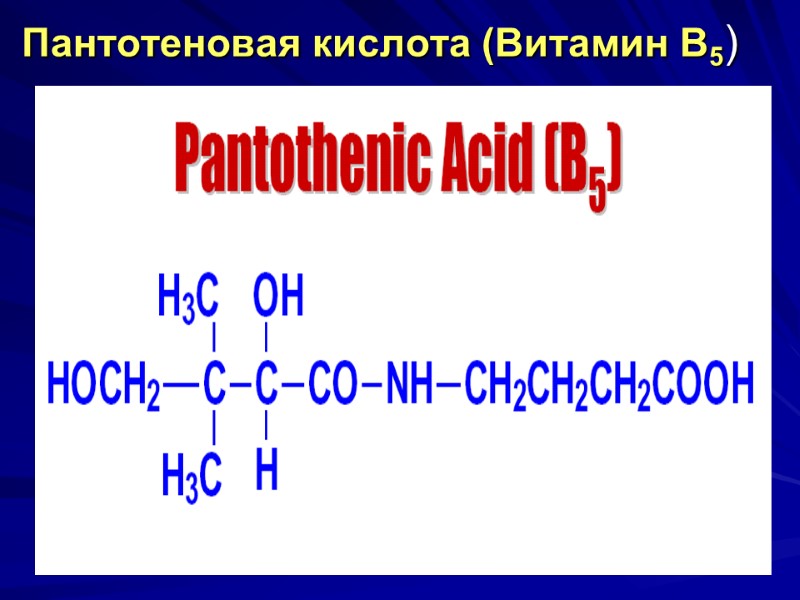
 Пантотеновая кислота (Витамин В5)
Пантотеновая кислота (Витамин В5)
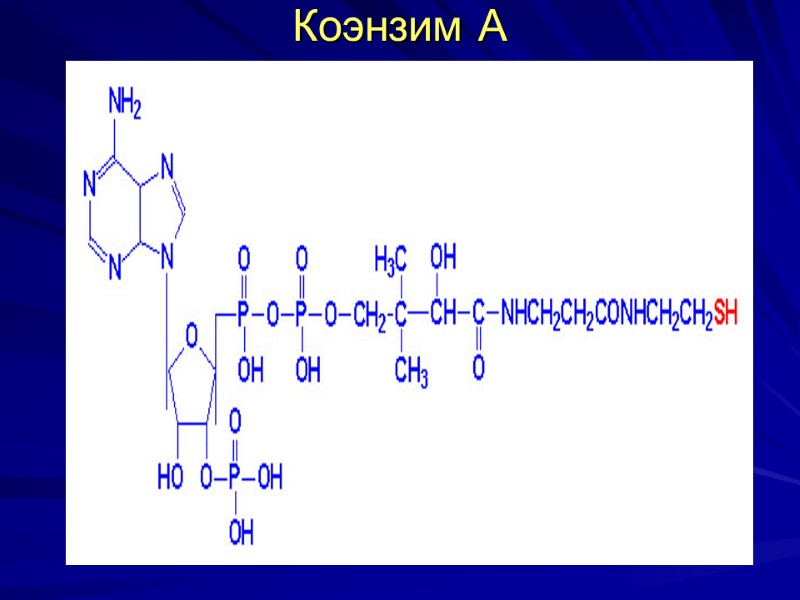
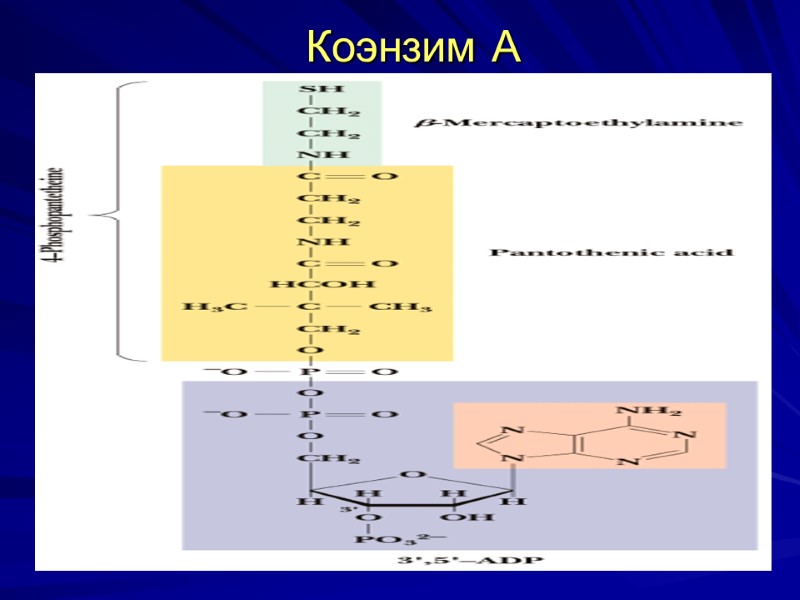
 Коэнзим А
Коэнзим А
 Коэнзим А
Коэнзим А
 Биороль пантотеновой кислоты входит в коэнзим А и 4 фосфопантетеина -простетическую группу АПБ (синтез ЖК). НS-КоА содержит тиоэтаноламин, пантотеновую кислоту, 3фосфоаденозин – 5 дифосфат, участвует в: - окислительном декарбоксилировании α-кетокислот (пирувата и α-кетоглутарата), - активации ЖК, - в окислении и биосинтезе ВЖК, - синтезе холестерина и кетоновых тел и др, Признаки авитаминоза – дерматиты, дистрофические изменения ЖВС и нервной системы, депигментация волос, алопеция и т.д.
Биороль пантотеновой кислоты входит в коэнзим А и 4 фосфопантетеина -простетическую группу АПБ (синтез ЖК). НS-КоА содержит тиоэтаноламин, пантотеновую кислоту, 3фосфоаденозин – 5 дифосфат, участвует в: - окислительном декарбоксилировании α-кетокислот (пирувата и α-кетоглутарата), - активации ЖК, - в окислении и биосинтезе ВЖК, - синтезе холестерина и кетоновых тел и др, Признаки авитаминоза – дерматиты, дистрофические изменения ЖВС и нервной системы, депигментация волос, алопеция и т.д.
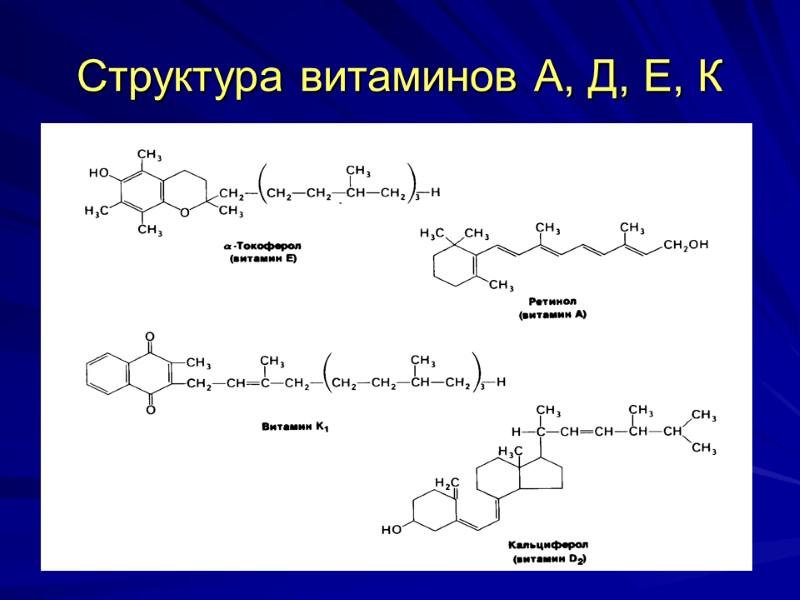
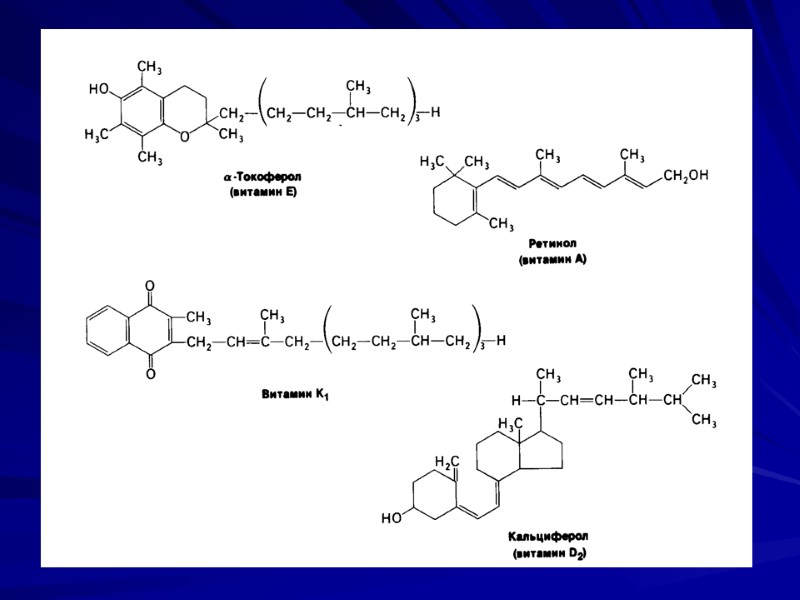
 Структура витаминов А, Д, Е, К
Структура витаминов А, Д, Е, К
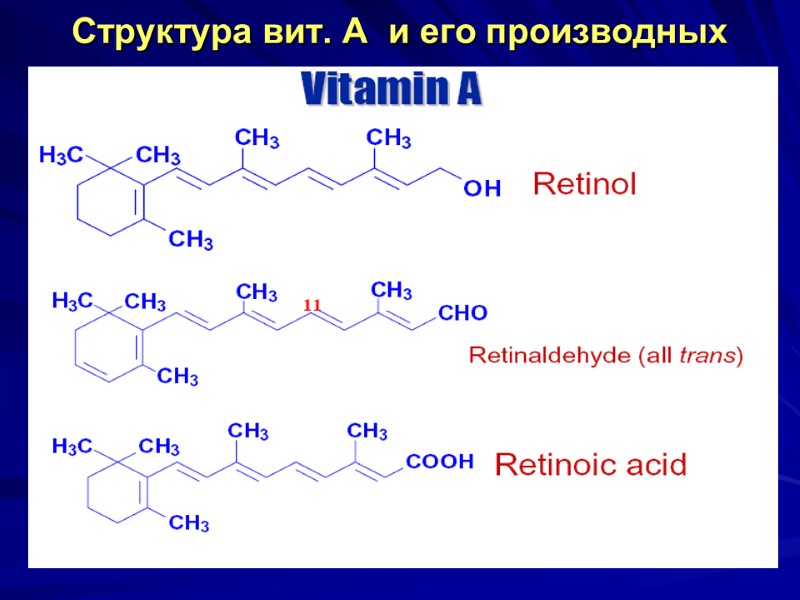
 Витамин А ( ретинол, антиксерофталмический витамин) Хим. строение – циклический непредельный одноатомный С20 спирт, состоит из шестичленного кольца (β - ионон), двух остатков изопрена и первичной спиртовой группы. В организме ретинол окисляется при участии ферментов с образованием цис и– транс-альдегидов – ретиналей, при окислении которых получаются ретиноевые кислоты.
Витамин А ( ретинол, антиксерофталмический витамин) Хим. строение – циклический непредельный одноатомный С20 спирт, состоит из шестичленного кольца (β - ионон), двух остатков изопрена и первичной спиртовой группы. В организме ретинол окисляется при участии ферментов с образованием цис и– транс-альдегидов – ретиналей, при окислении которых получаются ретиноевые кислоты.
 Провитамины вит. А – каротины Наибольшей биологической активностью обладает β-каротин, при расщеплении которого под действием β-каротин-диоксигеназы образуются 2 молекулы ретиналя по схеме: β-каротин 2 ретиналь → ретиноевая кислота тонкий кишечник, печень ↓ ретинол в крови ретинол связан с ретинолсвязывающим белком и преальбумином.
Провитамины вит. А – каротины Наибольшей биологической активностью обладает β-каротин, при расщеплении которого под действием β-каротин-диоксигеназы образуются 2 молекулы ретиналя по схеме: β-каротин 2 ретиналь → ретиноевая кислота тонкий кишечник, печень ↓ ретинол в крови ретинол связан с ретинолсвязывающим белком и преальбумином.
 Структура вит. А и его производных
Структура вит. А и его производных
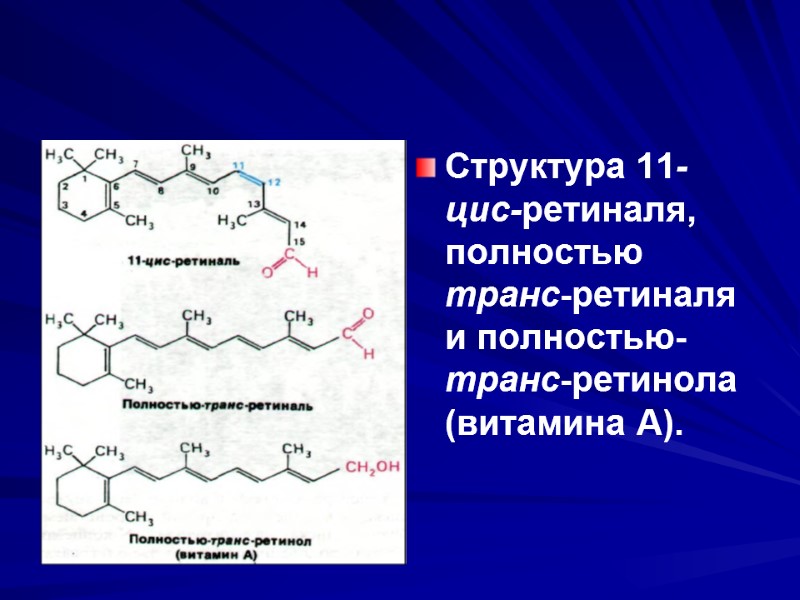
 Структура 11-цис-ретиналя, полностью транс-ретиналя и полностью-транс-ретинола (витамина А).
Структура 11-цис-ретиналя, полностью транс-ретиналя и полностью-транс-ретинола (витамина А).
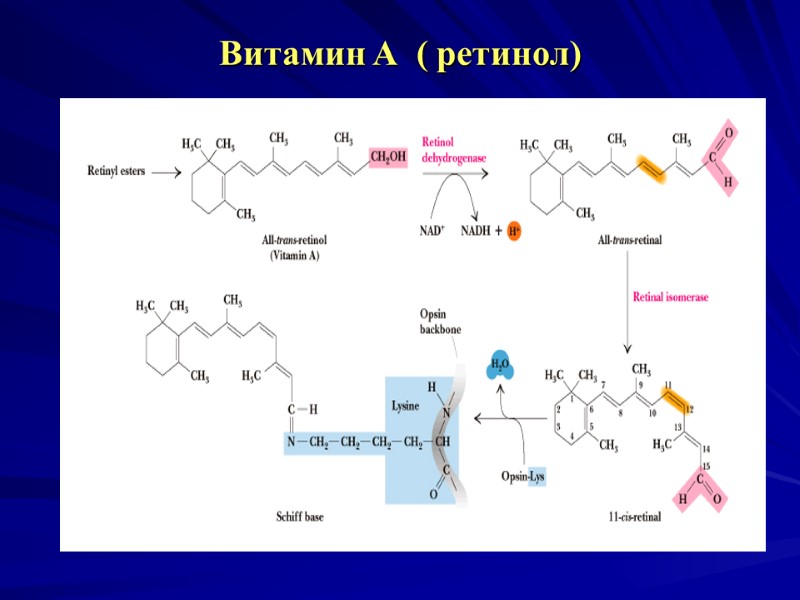
 Витамин А ( ретинол)
Витамин А ( ретинол)
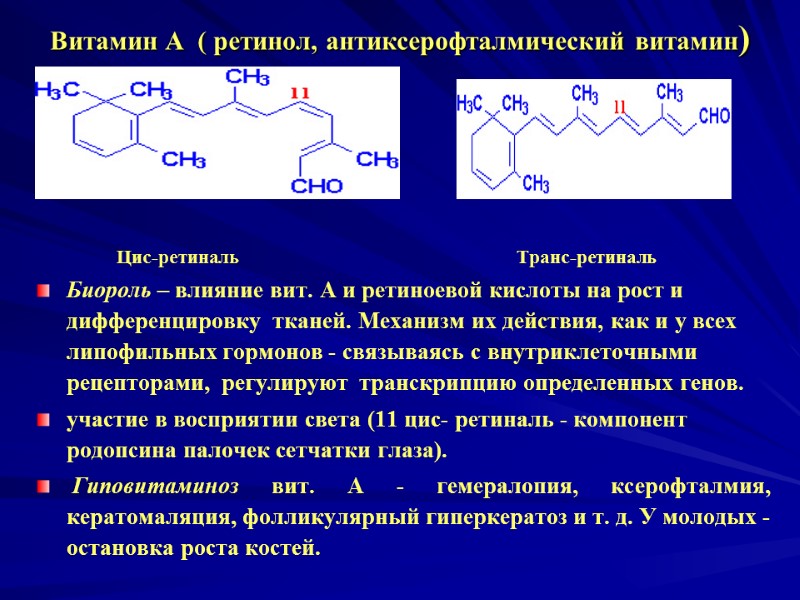
 Витамин А ( ретинол, антиксерофталмический витамин) Цис-ретиналь Транс-ретиналь Биороль – влияние вит. А и ретиноевой кислоты на рост и дифференцировку тканей. Механизм их действия, как и у всех липофильных гормонов - связываясь с внутриклеточными рецепторами, регулируют транскрипцию определенных генов. участие в восприятии света (11 цис- ретиналь - компонент родопсина палочек сетчатки глаза). Гиповитаминоз вит. А - гемералопия, ксерофталмия, кератомаляция, фолликулярный гиперкератоз и т. д. У молодых - остановка роста костей.
Витамин А ( ретинол, антиксерофталмический витамин) Цис-ретиналь Транс-ретиналь Биороль – влияние вит. А и ретиноевой кислоты на рост и дифференцировку тканей. Механизм их действия, как и у всех липофильных гормонов - связываясь с внутриклеточными рецепторами, регулируют транскрипцию определенных генов. участие в восприятии света (11 цис- ретиналь - компонент родопсина палочек сетчатки глаза). Гиповитаминоз вит. А - гемералопия, ксерофталмия, кератомаляция, фолликулярный гиперкератоз и т. д. У молодых - остановка роста костей.
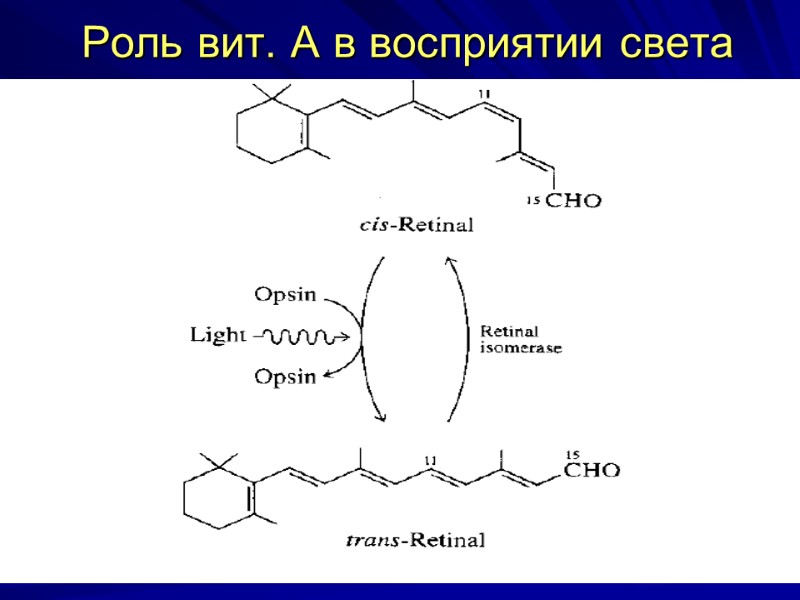
 Роль вит. А в восприятии света
Роль вит. А в восприятии света
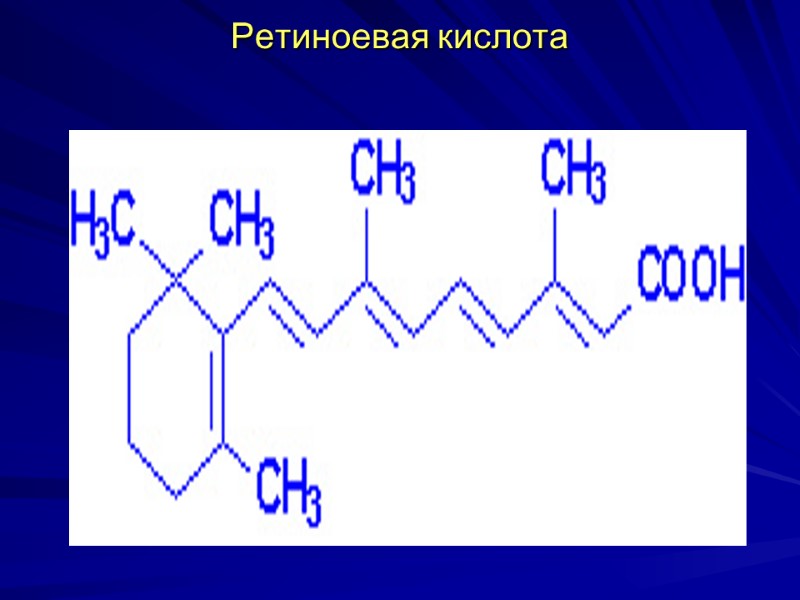
 Ретиноевая кислота
Ретиноевая кислота
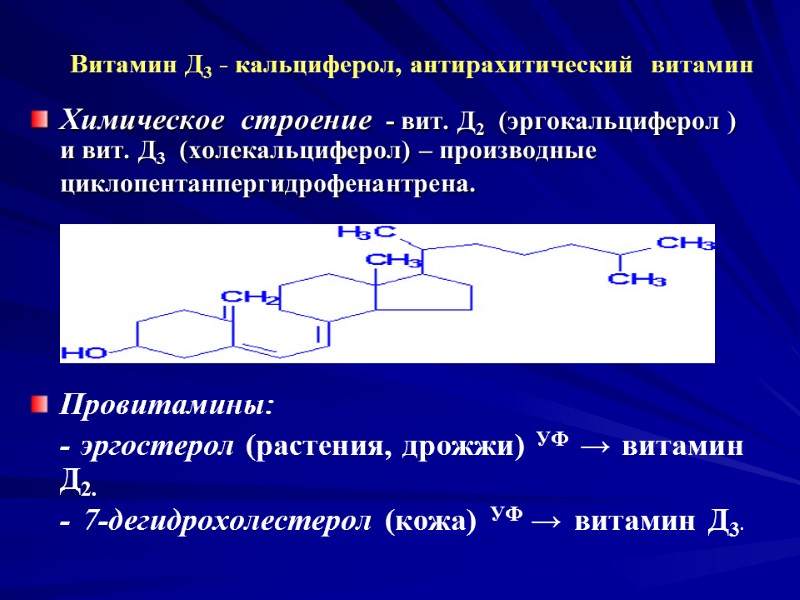
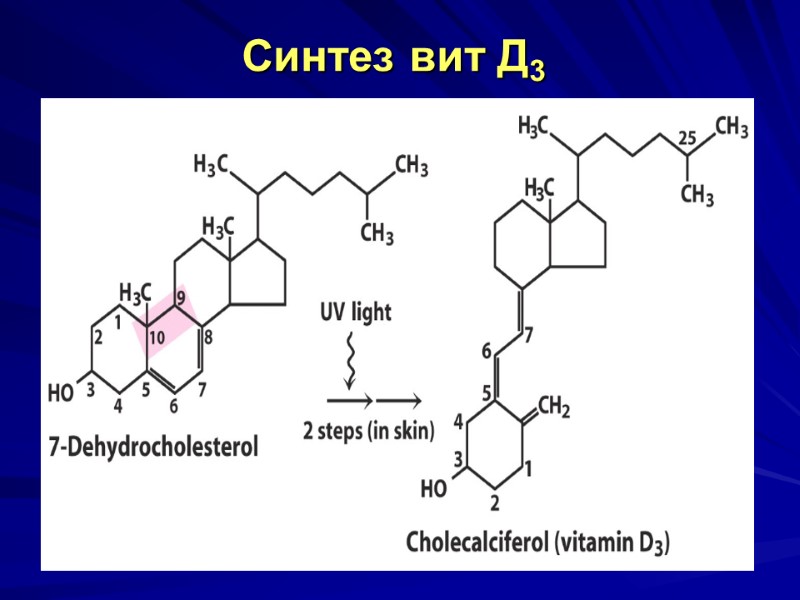
 Витамин Д3 - кальциферол, антирахитический витамин Химическое строение - вит. Д2 (эргокальциферол ) и вит. Д3 (холекальциферол) – производные циклопентанпергидрофенантрена. Провитамины: - эргостерол (растения, дрожжи) УФ → витамин Д2. - 7-дегидрохолестерол (кожа) УФ → витамин Д3.
Витамин Д3 - кальциферол, антирахитический витамин Химическое строение - вит. Д2 (эргокальциферол ) и вит. Д3 (холекальциферол) – производные циклопентанпергидрофенантрена. Провитамины: - эргостерол (растения, дрожжи) УФ → витамин Д2. - 7-дегидрохолестерол (кожа) УФ → витамин Д3.
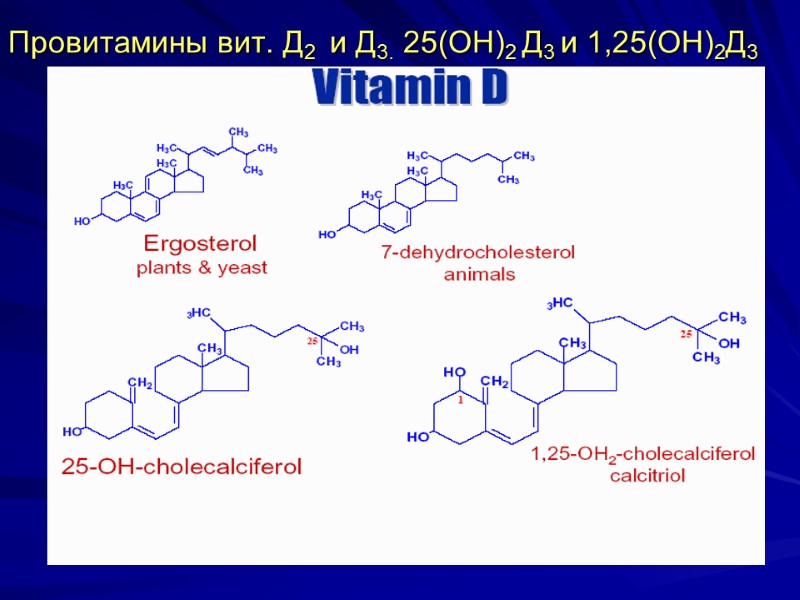
 Провитамины вит. Д2 и Д3. 25(ОН)2 Д3 и 1,25(ОН)2Д3
Провитамины вит. Д2 и Д3. 25(ОН)2 Д3 и 1,25(ОН)2Д3
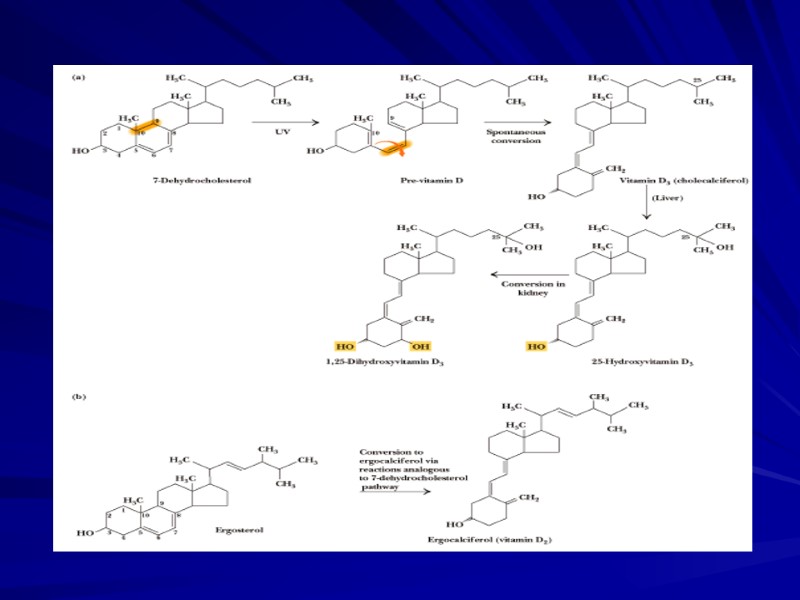
 Активные метаболиты вит Д3 Печень — холекальциферол 25-гидроксилаза25(ОН)Д3 (кальцидиол), Почки - 25(ОН)Д3 24-гидроксилаза 24,25 (ОН)2 Д3 и 25(ОН) Д3 1α-гидроксилаза 1,25 (ОН)2 Д3 (кальцитриол) Активные метаболиты вит. Д3 – 1,25 (ОН)2 Д3 и 24,25(ОН)2 Д3 — гормоны.
Активные метаболиты вит Д3 Печень — холекальциферол 25-гидроксилаза25(ОН)Д3 (кальцидиол), Почки - 25(ОН)Д3 24-гидроксилаза 24,25 (ОН)2 Д3 и 25(ОН) Д3 1α-гидроксилаза 1,25 (ОН)2 Д3 (кальцитриол) Активные метаболиты вит. Д3 – 1,25 (ОН)2 Д3 и 24,25(ОН)2 Д3 — гормоны.

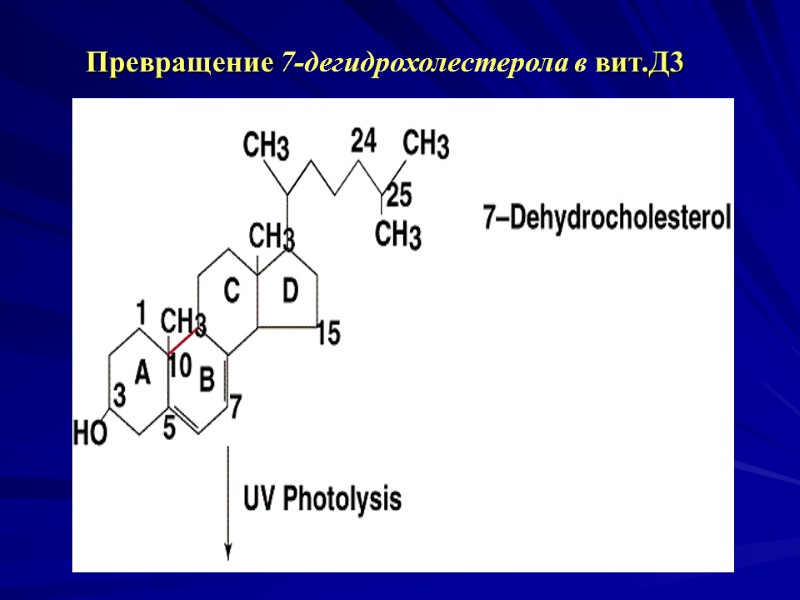
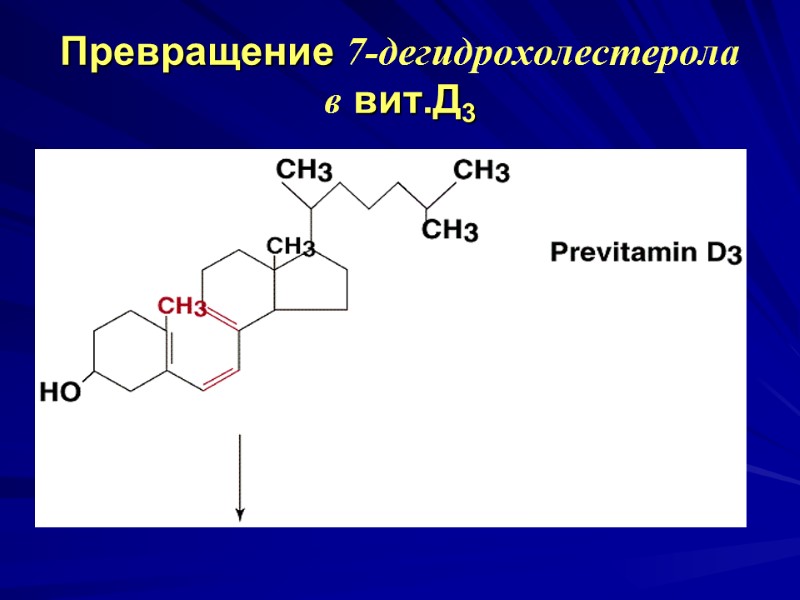
 Превращение 7-дегидрохолестерола в вит.Д3
Превращение 7-дегидрохолестерола в вит.Д3
 Синтез вит Д3
Синтез вит Д3
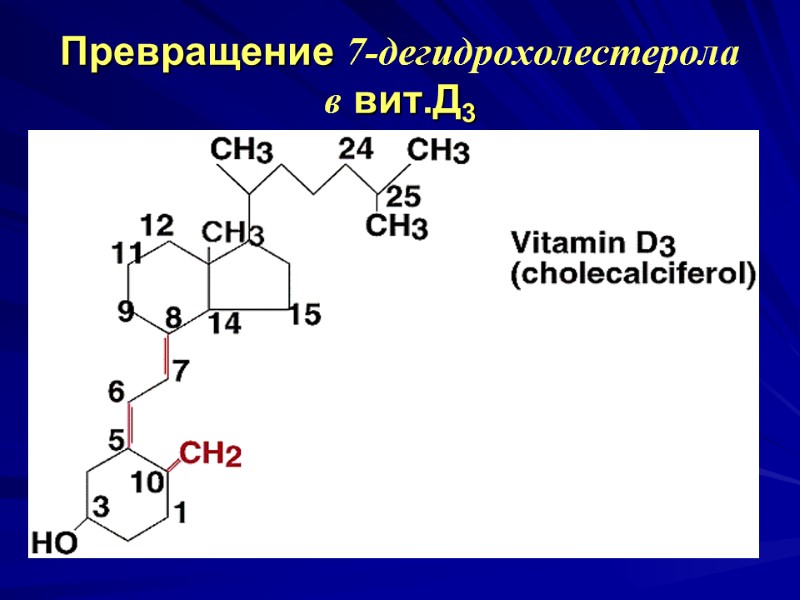
 Превращение 7-дегидрохолестерола в вит.Д3
Превращение 7-дегидрохолестерола в вит.Д3
 Превращение 7-дегидрохолестерола в вит.Д3
Превращение 7-дегидрохолестерола в вит.Д3
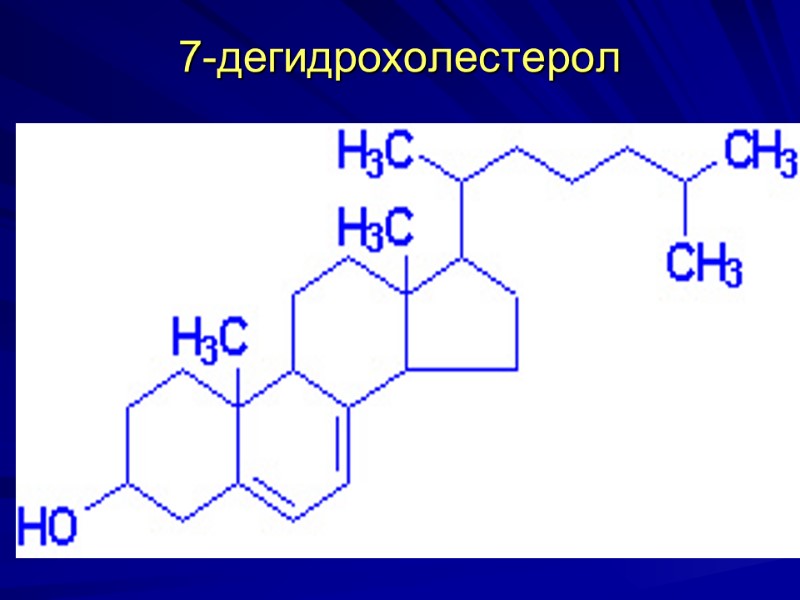
 7-дегидрохолестерол
7-дегидрохолестерол
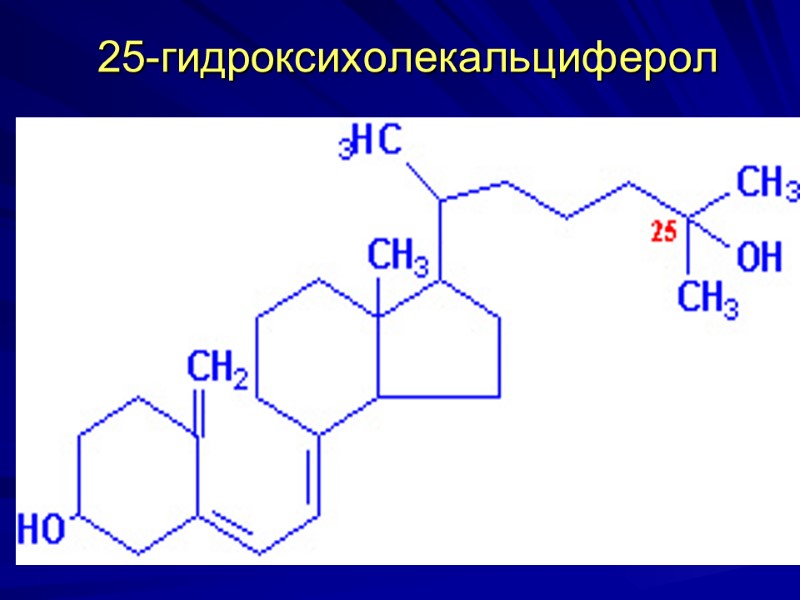
 25-гидроксихолекальциферол
25-гидроксихолекальциферол
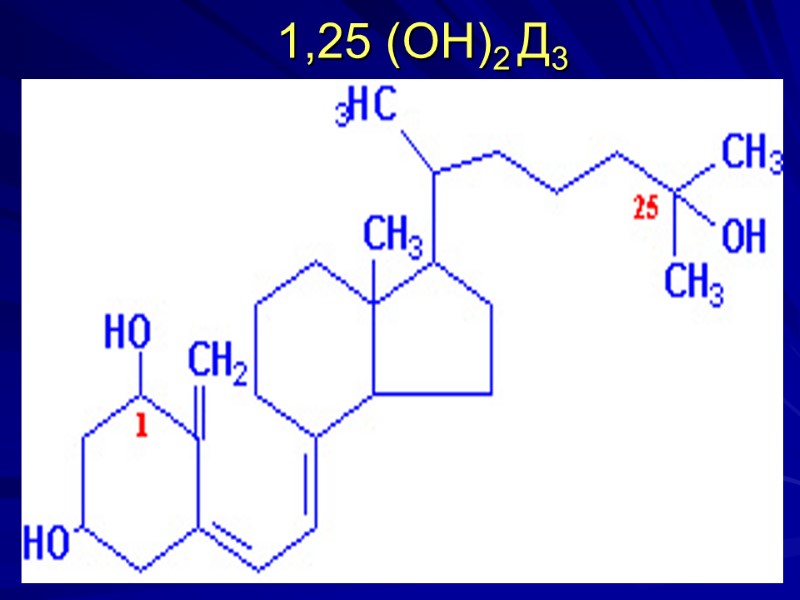
 1,25 (ОН)2 Д3
1,25 (ОН)2 Д3
 Витамин Д - кальциферол, антирахитический витамин Биороль – органы- мишени 1,25(ОН)2Д3: кишечник, почки, кости; тонкий кишечник – увеличение всасывания солей Са и Р; почки – усиление реабсорбции солей Са и Р в дистальных отделах почечных канальцев; кости – увеличение резорбции солей Са и Р при пониженном уровне Са2+ в крови . Итоговый эффект– увеличение уровня Са и Р в плазме крови. 24,25(ОН)2Д3 стимулируют остеогенез.
Витамин Д - кальциферол, антирахитический витамин Биороль – органы- мишени 1,25(ОН)2Д3: кишечник, почки, кости; тонкий кишечник – увеличение всасывания солей Са и Р; почки – усиление реабсорбции солей Са и Р в дистальных отделах почечных канальцев; кости – увеличение резорбции солей Са и Р при пониженном уровне Са2+ в крови . Итоговый эффект– увеличение уровня Са и Р в плазме крови. 24,25(ОН)2Д3 стимулируют остеогенез.
 Активные метаболиты витамина Д3 7-дегидрохолестерол кожа ↓ УФ Витамин Д3 (холекальциферол) печень ↓ 25-гидроксилаза 25 (ОН) Д3 (кальцидиол) почки ↓ 1α-гидроксилаза ПТГ 1,25 (ОН)2 Д3 (кальцитриол).
Активные метаболиты витамина Д3 7-дегидрохолестерол кожа ↓ УФ Витамин Д3 (холекальциферол) печень ↓ 25-гидроксилаза 25 (ОН) Д3 (кальцидиол) почки ↓ 1α-гидроксилаза ПТГ 1,25 (ОН)2 Д3 (кальцитриол).
 Органы –мишени 1,25(ОН)2Д3 1,25 (ОН)2 Д3
Органы –мишени 1,25(ОН)2Д3 1,25 (ОН)2 Д3
 Механизм действия вит. Д3 влияние на генетический аппарат клетки, индукцию синтеза мРНК для кальцийсвязывающих белков. Рецепторы для вит.Д – не только в тканях-мишенях, но и в клетках других тканей, где влияют на рост и дифференцировку тканей.
Механизм действия вит. Д3 влияние на генетический аппарат клетки, индукцию синтеза мРНК для кальцийсвязывающих белков. Рецепторы для вит.Д – не только в тканях-мишенях, но и в клетках других тканей, где влияют на рост и дифференцировку тканей.
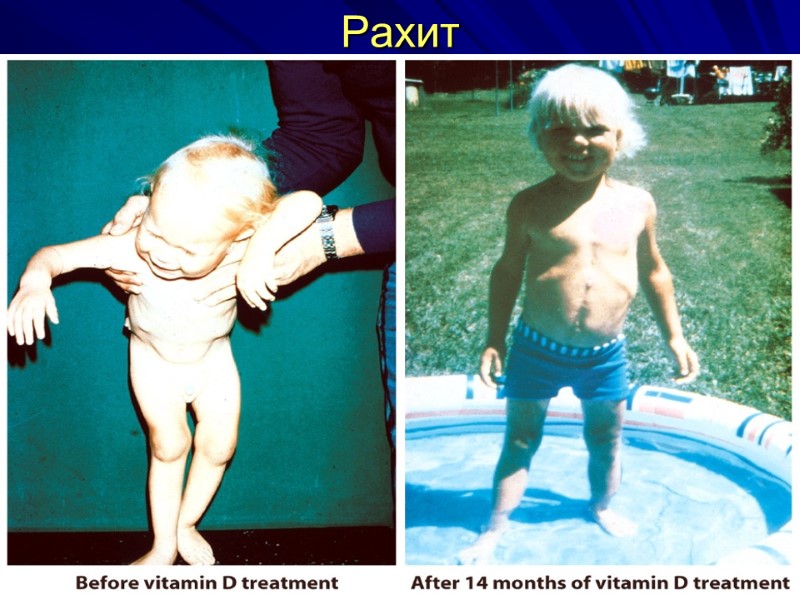
 Витамин Д3 – гипо – и гипервитаминозы Гиповитаминоз вит. Д у детей – рахит – искривление позвоночника, конечностей, деформация костей черепа, грудной клетки, гипотония мышц, повышение нервно--мышечной возбудимости. Причины рахита: ↓ вит. Д3 в рационе; нарушение всасывания вит. Д3 в тонком кишечнике; ↓ синтеза предшественников 1,25(ОН)2Д3 из-за недостаточного пребывания на солнце; дефект 1α гидроксилазы; дефект R кальцитриола в клетках-мишенях.
Витамин Д3 – гипо – и гипервитаминозы Гиповитаминоз вит. Д у детей – рахит – искривление позвоночника, конечностей, деформация костей черепа, грудной клетки, гипотония мышц, повышение нервно--мышечной возбудимости. Причины рахита: ↓ вит. Д3 в рационе; нарушение всасывания вит. Д3 в тонком кишечнике; ↓ синтеза предшественников 1,25(ОН)2Д3 из-за недостаточного пребывания на солнце; дефект 1α гидроксилазы; дефект R кальцитриола в клетках-мишенях.
 Витамин Д3 – гипо – и гипервитаминозы При вит. Д – резистентном рахите нарушен синтез гидроксилаз, переводящих вит. Д3 в активное состояние. У взрослых при недостатке вит. Д – остеомаляция. Гипервитаминоз вит. Д – деминерализация костей, повышение уровня Са в крови, отложение его в мягких тканях, образование камней в мочевых путях.
Витамин Д3 – гипо – и гипервитаминозы При вит. Д – резистентном рахите нарушен синтез гидроксилаз, переводящих вит. Д3 в активное состояние. У взрослых при недостатке вит. Д – остеомаляция. Гипервитаминоз вит. Д – деминерализация костей, повышение уровня Са в крови, отложение его в мягких тканях, образование камней в мочевых путях.
 Рахит
Рахит
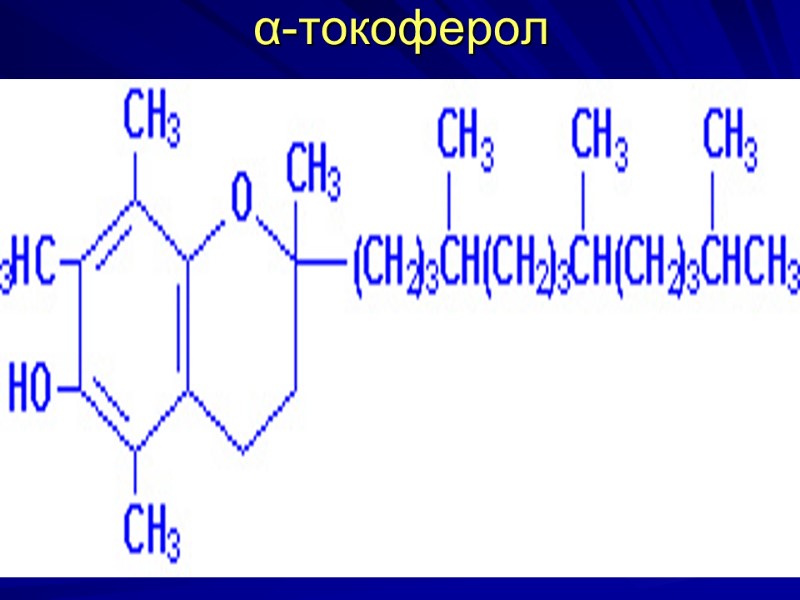
 Витамин Е, токоферолы Химическое строение- производные токола. α-токоферол Биороль–жирорастворимые антиоксиданты, предотвращают аутоокисление липидов биомембран. Дефицит вит Е – дистрофия мышц и гемолитическая анемия, в результате активации ПОЛ в мембранах эритроцитов и мембранах лизосом мышечных клеток. Выходящие в цитозоль ферменты разрушают мышечную ткань, увеличивая креатинурию.
Витамин Е, токоферолы Химическое строение- производные токола. α-токоферол Биороль–жирорастворимые антиоксиданты, предотвращают аутоокисление липидов биомембран. Дефицит вит Е – дистрофия мышц и гемолитическая анемия, в результате активации ПОЛ в мембранах эритроцитов и мембранах лизосом мышечных клеток. Выходящие в цитозоль ферменты разрушают мышечную ткань, увеличивая креатинурию.
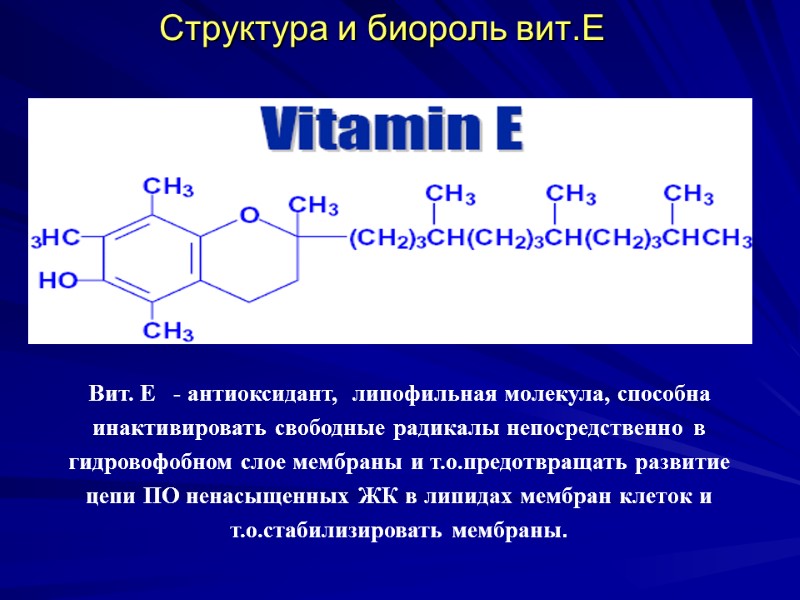
 Структура и биороль вит.Е Вит. Е - антиоксидант, липофильная молекула, способна инактивировать свободные радикалы непосредственно в гидровофобном слое мембраны и т.о.предотвращать развитие цепи ПО ненасыщенных ЖК в липидах мембран клеток и т.о.стабилизировать мембраны.
Структура и биороль вит.Е Вит. Е - антиоксидант, липофильная молекула, способна инактивировать свободные радикалы непосредственно в гидровофобном слое мембраны и т.о.предотвращать развитие цепи ПО ненасыщенных ЖК в липидах мембран клеток и т.о.стабилизировать мембраны.
 α-токоферол
α-токоферол
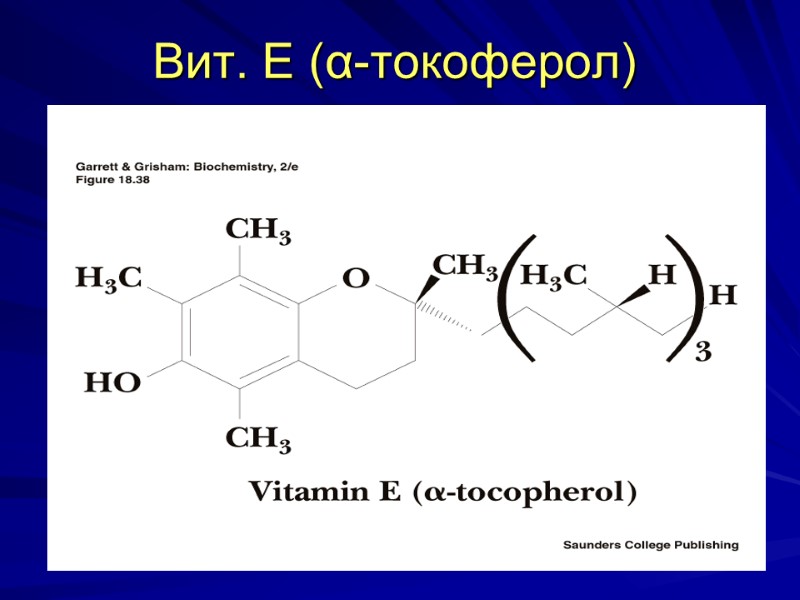
 Вит. Е (α-токоферол)
Вит. Е (α-токоферол)
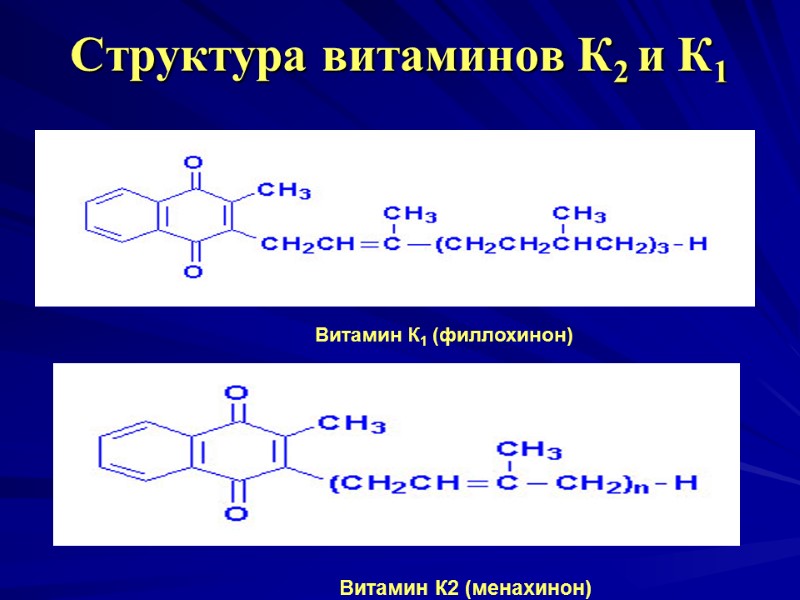
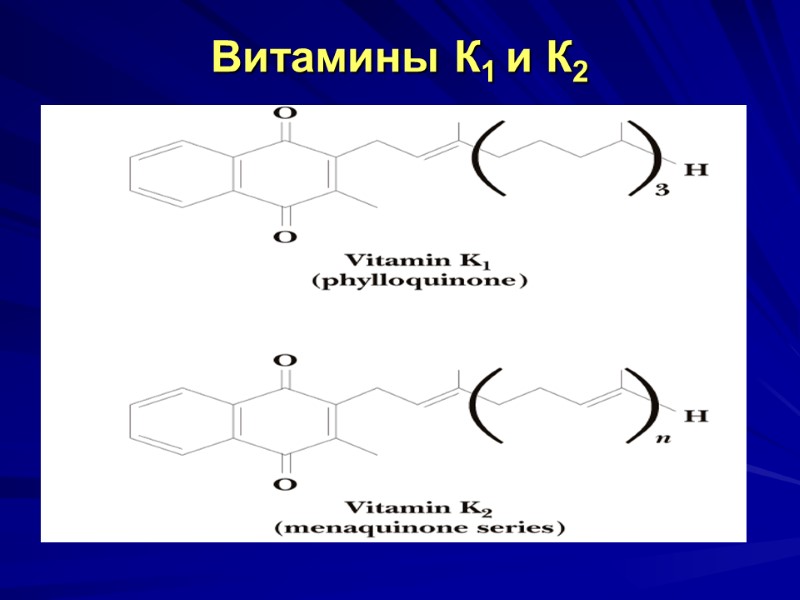
 Витамин К (антигеморрагический) Вит. К1 и К2 - 2 типа хинонов с боковыми цепями, представленными изопреноидными звеньями. В основе структуры — кольцо 1,4- нафтохинона. Вит. К1 (филлохинон) содержится в растениях. Вит. К2 (менахинон) синтезируется микрофлорой кишечника. Вит. К3 - синтетический аналог вит. К. Викасол – синтезированная натриевая соль бисульфитного производного вит. К.
Витамин К (антигеморрагический) Вит. К1 и К2 - 2 типа хинонов с боковыми цепями, представленными изопреноидными звеньями. В основе структуры — кольцо 1,4- нафтохинона. Вит. К1 (филлохинон) содержится в растениях. Вит. К2 (менахинон) синтезируется микрофлорой кишечника. Вит. К3 - синтетический аналог вит. К. Викасол – синтезированная натриевая соль бисульфитного производного вит. К.
 Cтруктура витаминов К2 и К1 Витамин К1 (филлохинон) Витамин К2 (менахинон)
Cтруктура витаминов К2 и К1 Витамин К1 (филлохинон) Витамин К2 (менахинон)
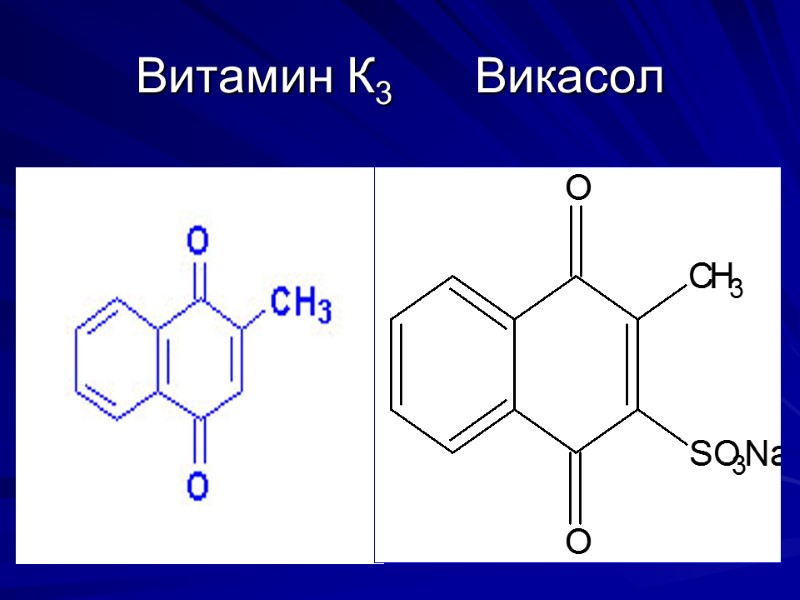
 Витамин К3 Викасол
Витамин К3 Викасол
 Витамины К1 и К2
Витамины К1 и К2
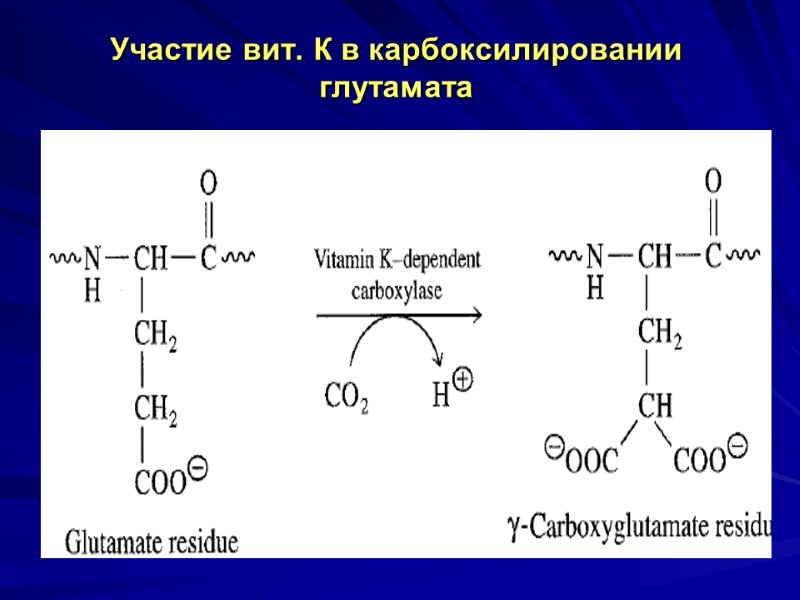
 Биороль вит. К кофермент γ-глутамил-карбоксилазы, (превращение глутамата в γ-карбоксиглутамат, необходимый для биосинтеза 4 факторов свертывания крови – факторов II (протромбина), VII, IX, X. -карбоксиглутаминовая кислота образуется из глутамата в результате посттрансляционной модификации 4 указанных факторов свертывания крови. Дополнительные отрицательно заряженные СООН группы облегчают связывание ионов Са с молекулами белков.
Биороль вит. К кофермент γ-глутамил-карбоксилазы, (превращение глутамата в γ-карбоксиглутамат, необходимый для биосинтеза 4 факторов свертывания крови – факторов II (протромбина), VII, IX, X. -карбоксиглутаминовая кислота образуется из глутамата в результате посттрансляционной модификации 4 указанных факторов свертывания крови. Дополнительные отрицательно заряженные СООН группы облегчают связывание ионов Са с молекулами белков.
 Участие вит. К в карбоксилировании глутамата
Участие вит. К в карбоксилировании глутамата
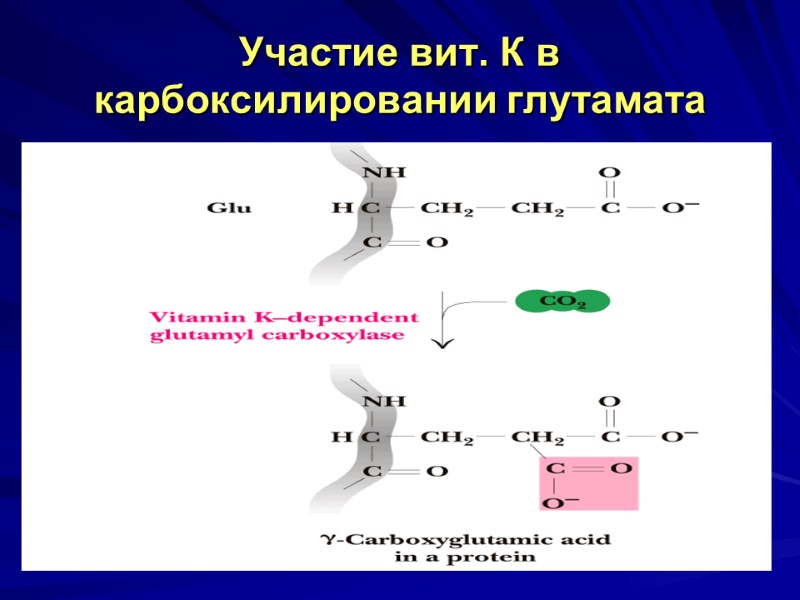
 Участие вит. К в карбоксилировании глутамата
Участие вит. К в карбоксилировании глутамата
 Витамин К Антивитамины вит. К – природный антикоагулянт дикумарол и синтетические аналоги вит. К — конкурентные ингибиторы γ-глутамилкарбоксилазы, препятствуют тромбообразованию. дефицит вит.К - при нарушении всасывания жиров, применении антибиотиков, нарушающих нормальный состав микрофлоры кишечника; возможны нарушения свертывания крови.
Витамин К Антивитамины вит. К – природный антикоагулянт дикумарол и синтетические аналоги вит. К — конкурентные ингибиторы γ-глутамилкарбоксилазы, препятствуют тромбообразованию. дефицит вит.К - при нарушении всасывания жиров, применении антибиотиков, нарушающих нормальный состав микрофлоры кишечника; возможны нарушения свертывания крови.

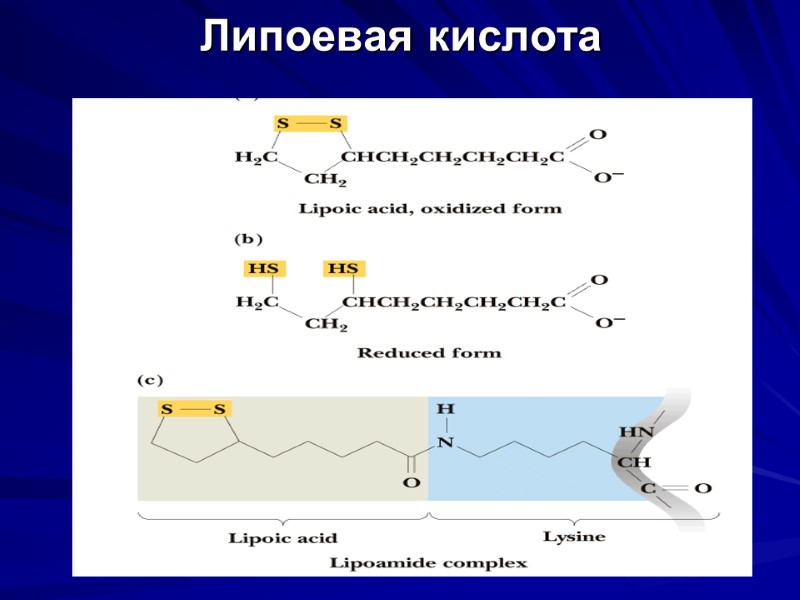
 Липоевая кислота
Липоевая кислота

