Ильичева_Алтай 2014.ppt
- Количество слайдов: 41
 ВИРУСЫ ГРИППА И ВАКЦИНОПРОФИЛАКТИК А Татьяна Николаевна Ильичёва Доктор биологических наук, доцент каф. молекулярной биологии НГУ, зав. лабораторией гриппа человека ФБУН ГНЦ ВБ «Вектор»
ВИРУСЫ ГРИППА И ВАКЦИНОПРОФИЛАКТИК А Татьяна Николаевна Ильичёва Доктор биологических наук, доцент каф. молекулярной биологии НГУ, зав. лабораторией гриппа человека ФБУН ГНЦ ВБ «Вектор»
 Грипп – острое респираторное вирусное заболевание, вызываемое вирусами гриппа А, В и С, принадлежащими к семейству Оrthomyxoviridae. Симптомы: повышение температуры тела до 39°С и выше, интоксикация (головная боль, «ломота» в мышцах и суставах, слабость), заложенность носа, боль в горле, кашель. В общей структуре инфекционных болезней на долю гриппа и острых инфекций дыхательных путей приходится до 92%. Вирусы гриппа вызывают ежегодные эпидемии и периодические пандемии, которые уносят миллионы жизней. Сезонные эпидемии гриппа поражают до 15% населения и ежегодно уносят 250 000 – 500 000 человеческих жизней во всем мире.
Грипп – острое респираторное вирусное заболевание, вызываемое вирусами гриппа А, В и С, принадлежащими к семейству Оrthomyxoviridae. Симптомы: повышение температуры тела до 39°С и выше, интоксикация (головная боль, «ломота» в мышцах и суставах, слабость), заложенность носа, боль в горле, кашель. В общей структуре инфекционных болезней на долю гриппа и острых инфекций дыхательных путей приходится до 92%. Вирусы гриппа вызывают ежегодные эпидемии и периодические пандемии, которые уносят миллионы жизней. Сезонные эпидемии гриппа поражают до 15% населения и ежегодно уносят 250 000 – 500 000 человеческих жизней во всем мире.
 Грипп передается воздушно-капельным путем, причем очень эффективно. Кашель приводит к появлению нескольких сотен капель аэрозоля, при чихании их количество в среднем достигает 20000.
Грипп передается воздушно-капельным путем, причем очень эффективно. Кашель приводит к появлению нескольких сотен капель аэрозоля, при чихании их количество в среднем достигает 20000.
 РАННИЕ ПАНДЕМИИ ГРИППА 1580 г. - Европа, Североамериканский континент, Африка, Восточные страны 1626 г. - Италия, южная часть Франции 1729 – 1730 гг. - Европа, Россия (По смертности сравнивали с чумой) 1836 – 1837 гг. - Австралия, о. Ява, Индия, южная Африка, Европа, Россия (По смертности сравнивали с холерой) 1889 – 1892 гг. - Китай, Россия, Европа, Северная Америка, Африка, Австралия
РАННИЕ ПАНДЕМИИ ГРИППА 1580 г. - Европа, Североамериканский континент, Африка, Восточные страны 1626 г. - Италия, южная часть Франции 1729 – 1730 гг. - Европа, Россия (По смертности сравнивали с чумой) 1836 – 1837 гг. - Австралия, о. Ява, Индия, южная Африка, Европа, Россия (По смертности сравнивали с холерой) 1889 – 1892 гг. - Китай, Россия, Европа, Северная Америка, Африка, Австралия
 В начале 20 века причиной гриппа называли H. influenzae и другие бактерии. В 1933 Smith, Andrewes и Laidlaw изолировали из хорьков вирус гриппа и доказали, что он является причиной заболевания людей. В 1940 -е годы, когда еще не применялись культуры клеток для выращивания вирусов, иммунология была примитивна и мало вирусов было известно, были исследованы свойства гемагглютинина, открыта способность вируса размножаться в развивающихся куриных эмбрионах (после адаптации). Все это позволило стать вирусу гриппа самым изученным вирусом этого времени и наиболее удобной моделью для изучения патогенеза. В 40 -60 годы многие другие вирусы со сходными свойствами были добавлены в группу Myxoviridae, но в 1970 -е годы группу разделили на 2 семейства: Paramyxoviridae и Orthmyxoviridae.
В начале 20 века причиной гриппа называли H. influenzae и другие бактерии. В 1933 Smith, Andrewes и Laidlaw изолировали из хорьков вирус гриппа и доказали, что он является причиной заболевания людей. В 1940 -е годы, когда еще не применялись культуры клеток для выращивания вирусов, иммунология была примитивна и мало вирусов было известно, были исследованы свойства гемагглютинина, открыта способность вируса размножаться в развивающихся куриных эмбрионах (после адаптации). Все это позволило стать вирусу гриппа самым изученным вирусом этого времени и наиболее удобной моделью для изучения патогенеза. В 40 -60 годы многие другие вирусы со сходными свойствами были добавлены в группу Myxoviridae, но в 1970 -е годы группу разделили на 2 семейства: Paramyxoviridae и Orthmyxoviridae.
 ХАРАКТЕРИСТИКА РОДОВ СЕМЕЙСТВА ORTHОMYXOVIRIDAE Вирусы гриппа А инфицируют широкий спектр млекопитающих, включая человека, лошадей, свиней, хорьков, и птиц. Этот патоген вызывает эпидемии и пандемии. Вирусы гриппа В инфицируют людей и тюленей. В отличие от вирусов гриппа А не имеют серотипов, вызывают эпидемии, но не пандемии. Вирусы гриппа С инфицируют людей и свиней. Генетически и морфологически отличаются от вирусов гриппа А и В. Isaviruses инфицируют лосося. Thogotoviruses вызывают заболевание у беспозвоночных животных.
ХАРАКТЕРИСТИКА РОДОВ СЕМЕЙСТВА ORTHОMYXOVIRIDAE Вирусы гриппа А инфицируют широкий спектр млекопитающих, включая человека, лошадей, свиней, хорьков, и птиц. Этот патоген вызывает эпидемии и пандемии. Вирусы гриппа В инфицируют людей и тюленей. В отличие от вирусов гриппа А не имеют серотипов, вызывают эпидемии, но не пандемии. Вирусы гриппа С инфицируют людей и свиней. Генетически и морфологически отличаются от вирусов гриппа А и В. Isaviruses инфицируют лосося. Thogotoviruses вызывают заболевание у беспозвоночных животных.
 КЛАССИФИКАЦИЯ ВИРУСОВ ГРИППА А Вирусы гриппа А классифицируют на основании атигенных свойств двух поверхностных гликопротеинов вирусной частицы – гемагглютинина (НА) и нейраминидазы (NA). К настоящему моменту выделены вирусы гриппа А 17 -ти подтипов НА и 10 -ти подтипов NA Пандемии вызывали вирусы гриппа А трех подтипов гемагглютинина (H 1, H 2, H 3) и двух подтипов нейраминидазы(N 1, N 2).
КЛАССИФИКАЦИЯ ВИРУСОВ ГРИППА А Вирусы гриппа А классифицируют на основании атигенных свойств двух поверхностных гликопротеинов вирусной частицы – гемагглютинина (НА) и нейраминидазы (NA). К настоящему моменту выделены вирусы гриппа А 17 -ти подтипов НА и 10 -ти подтипов NA Пандемии вызывали вирусы гриппа А трех подтипов гемагглютинина (H 1, H 2, H 3) и двух подтипов нейраминидазы(N 1, N 2).
 ОБОЗНАЧЕНИЕ ШТАММА ВИРУСА ГРИППА Согласно Международной номенклатуре штаммы вируса гриппа обозначаются по следующей схеме: Род/источник изоляции/место изоляции/собственный номер изолята/год изоляции. Антигенное описание подтипов НА и NA для вирусов гриппа рода А дается далее в скобках. Пример: A/Chicken/Pennsylvania/1370/83 (H 5 N 2). Если штамм выделен от человека, источник изоляции опускается. Пример: A/Hong Kong/156/97 (H 5 N 1)
ОБОЗНАЧЕНИЕ ШТАММА ВИРУСА ГРИППА Согласно Международной номенклатуре штаммы вируса гриппа обозначаются по следующей схеме: Род/источник изоляции/место изоляции/собственный номер изолята/год изоляции. Антигенное описание подтипов НА и NA для вирусов гриппа рода А дается далее в скобках. Пример: A/Chicken/Pennsylvania/1370/83 (H 5 N 2). Если штамм выделен от человека, источник изоляции опускается. Пример: A/Hong Kong/156/97 (H 5 N 1)
 ЭЛЕКТРОННАЯ МИКРОФОТОГРАФИЯ ВИРУСНОЙ ЧАСТИЦЫ ВИРУСА ГРИППА
ЭЛЕКТРОННАЯ МИКРОФОТОГРАФИЯ ВИРУСНОЙ ЧАСТИЦЫ ВИРУСА ГРИППА
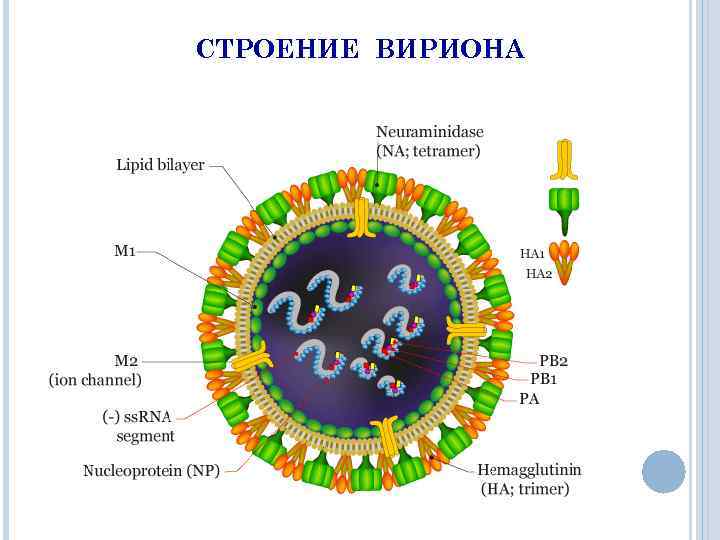 СТРОЕНИЕ ВИРИОНА
СТРОЕНИЕ ВИРИОНА
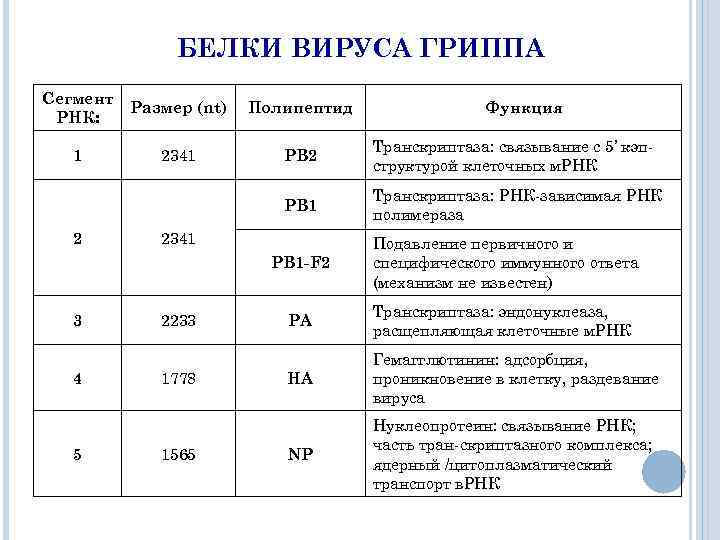 БЕЛКИ ВИРУСА ГРИППА Сегмент РНК: Размер (nt) Полипептид 1 2341 PB 2 Транскриптаза: связывание с 5’ кэпструктурой клеточных м. РНК PB 1 Транскриптаза: РНК-зависимая РНК полимераза 2 2341 Функция PB 1 -F 2 3 4 5 2233 1778 1565 Подавление первичного и специфического иммунного ответа (механизм не известен) PA Транскриптаза: эндонуклеаза, расщепляющая клеточные м. РНК HA Гемагглютинин: адсорбция, проникновение в клетку, раздевание вируса NP Нуклеопротеин: связывание РНК; часть тран-скриптазного комплекса; ядерный /цитоплазматический транспорт в. РНК
БЕЛКИ ВИРУСА ГРИППА Сегмент РНК: Размер (nt) Полипептид 1 2341 PB 2 Транскриптаза: связывание с 5’ кэпструктурой клеточных м. РНК PB 1 Транскриптаза: РНК-зависимая РНК полимераза 2 2341 Функция PB 1 -F 2 3 4 5 2233 1778 1565 Подавление первичного и специфического иммунного ответа (механизм не известен) PA Транскриптаза: эндонуклеаза, расщепляющая клеточные м. РНК HA Гемагглютинин: адсорбция, проникновение в клетку, раздевание вируса NP Нуклеопротеин: связывание РНК; часть тран-скриптазного комплекса; ядерный /цитоплазматический транспорт в. РНК
 БЕЛКИ ВИРУСА ГРИППА (ПРОДОЛЖЕНИЕ) Сегмент РНК Размер (nt) Полипептид 6 1413 NA Нейраминидаза: освобождение вируса (выход из клетки) M 1 Матриксный белок: вирусная оболочка, г. о. защитная функция M 2 Интегральный мембранный белок, выстилающий ионные каналыl NEP Сплайсинг, трансляция. Антиинтерфероновая активность (другое название - NS 1) NS 2 Неструктурный белок: в ядре + цитоплазме, функция неизвестна. 7 8 Функция 1027 890
БЕЛКИ ВИРУСА ГРИППА (ПРОДОЛЖЕНИЕ) Сегмент РНК Размер (nt) Полипептид 6 1413 NA Нейраминидаза: освобождение вируса (выход из клетки) M 1 Матриксный белок: вирусная оболочка, г. о. защитная функция M 2 Интегральный мембранный белок, выстилающий ионные каналыl NEP Сплайсинг, трансляция. Антиинтерфероновая активность (другое название - NS 1) NS 2 Неструктурный белок: в ядре + цитоплазме, функция неизвестна. 7 8 Функция 1027 890
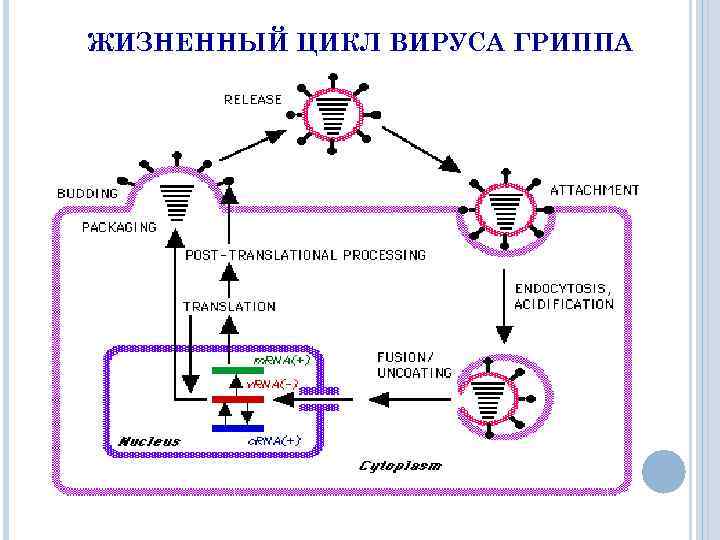 ЖИЗНЕННЫЙ ЦИКЛ ВИРУСА ГРИППА
ЖИЗНЕННЫЙ ЦИКЛ ВИРУСА ГРИППА
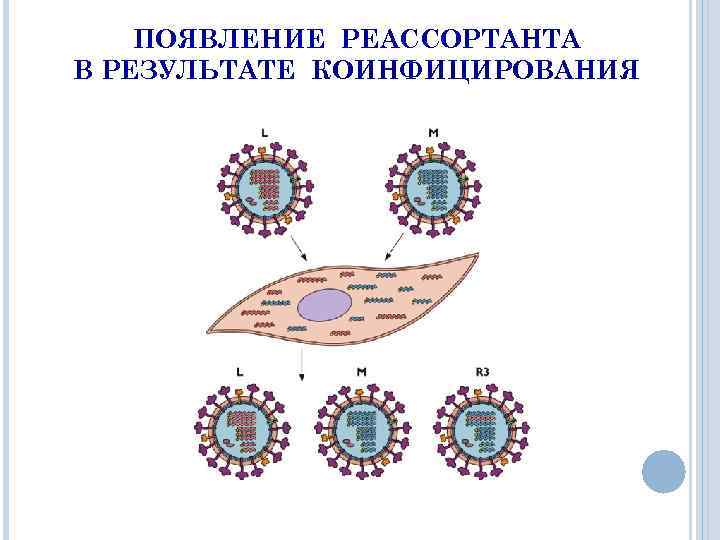 ПОЯВЛЕНИЕ РЕАССОРТАНТА В РЕЗУЛЬТАТЕ КОИНФИЦИРОВАНИЯ
ПОЯВЛЕНИЕ РЕАССОРТАНТА В РЕЗУЛЬТАТЕ КОИНФИЦИРОВАНИЯ
 ПАНДЕМИИ ГРИППА В XX ВЕКЕ: 1918 -1919 – Испанский грипп, «испанка» : ◦ вирус гриппа A(H 1 N 1) ◦ погибло от 20 до 50 млн. чел. в мире, 500 тыс. чел. – в США 1957 -1958 – Азиатский грипп: ◦ вирус гриппа A(H 2 N 2). ◦ погибло около 70 тыс. чел. в США 1968 -1969 – Гонконгский грипп: ◦ вирус гриппа A(H 3 N 2) ◦ погибло около 34 тыс. чел. В США 1977 – Русский грипп: ◦ вирус гриппа А(Н 1 N 1)
ПАНДЕМИИ ГРИППА В XX ВЕКЕ: 1918 -1919 – Испанский грипп, «испанка» : ◦ вирус гриппа A(H 1 N 1) ◦ погибло от 20 до 50 млн. чел. в мире, 500 тыс. чел. – в США 1957 -1958 – Азиатский грипп: ◦ вирус гриппа A(H 2 N 2). ◦ погибло около 70 тыс. чел. в США 1968 -1969 – Гонконгский грипп: ◦ вирус гриппа A(H 3 N 2) ◦ погибло около 34 тыс. чел. В США 1977 – Русский грипп: ◦ вирус гриппа А(Н 1 N 1)
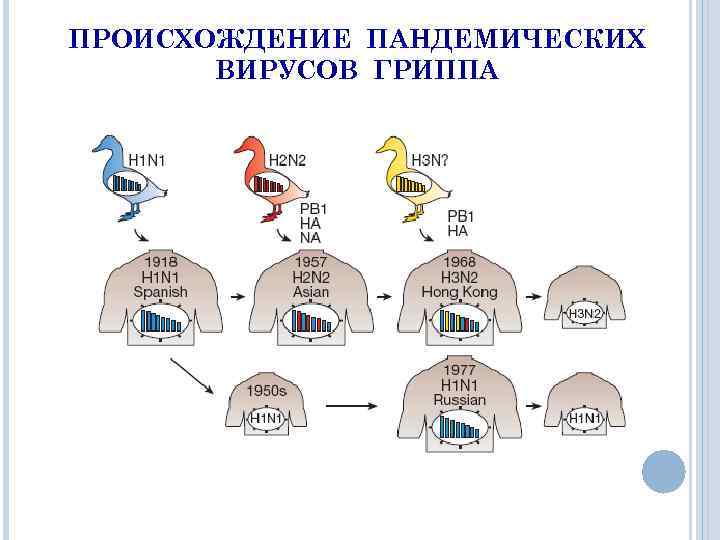 ПРОИСХОЖДЕНИЕ ПАНДЕМИЧЕСКИХ ВИРУСОВ ГРИППА
ПРОИСХОЖДЕНИЕ ПАНДЕМИЧЕСКИХ ВИРУСОВ ГРИППА
 ФАКТЫ, КОТОРЫЕ ПРОТИВОРЕЧАТ ТЕОРИИ ПРОИСХОЖДЕНИЯ ПАНДЕМИЧЕСКИХ ШТАММОВ ПУТЕМ РЕАССОРТАЦИИ ВИРУСОВ ГРИППА ЧЕЛОВЕКА И ПТИЦ Пандемии вызывали только подтипы вируса гриппа A(H 1 N 1), A(H 2 N 2), A(H 3 N 2), в то время как в популяциях птиц циркулируют вирусы 16 подтипов НА и 9 подтипов NA. К началу пандемии в крови пожилых людей обнаруживаются антитела к новому вирусу, следовательно, эти люди ранее были инфицированы родственным вариантом вируса.
ФАКТЫ, КОТОРЫЕ ПРОТИВОРЕЧАТ ТЕОРИИ ПРОИСХОЖДЕНИЯ ПАНДЕМИЧЕСКИХ ШТАММОВ ПУТЕМ РЕАССОРТАЦИИ ВИРУСОВ ГРИППА ЧЕЛОВЕКА И ПТИЦ Пандемии вызывали только подтипы вируса гриппа A(H 1 N 1), A(H 2 N 2), A(H 3 N 2), в то время как в популяциях птиц циркулируют вирусы 16 подтипов НА и 9 подтипов NA. К началу пандемии в крови пожилых людей обнаруживаются антитела к новому вирусу, следовательно, эти люди ранее были инфицированы родственным вариантом вируса.
 ВЫСОКОПАТОГЕННЫЙ ВИРУС ГРИППА A/H 5 N 1 Первые случаи инфицирования людей высокопатогенным вирусом гриппа птиц субтипа H 5 N 1 – Гонконг, 1997 г. : 18 инфицированных, 6 летальных исходов. Эта вспышка была взята под контроль с помощью поголовного уничтожения живых птиц на рынках Гонконга. После периода локальных и спорадических вспышек, новый вариант вируса H 5 N 1 начал быстро распространяться с 2003 г. Начиная с 2005 г. вирусы H 5 N 1 появились в Сибири среди дикой и домашней птицы, отсюда проникли в Европу и Африку. В это же время они стали эндемичными в популяции домашних птиц во многих странах Юго-восточной Азии.
ВЫСОКОПАТОГЕННЫЙ ВИРУС ГРИППА A/H 5 N 1 Первые случаи инфицирования людей высокопатогенным вирусом гриппа птиц субтипа H 5 N 1 – Гонконг, 1997 г. : 18 инфицированных, 6 летальных исходов. Эта вспышка была взята под контроль с помощью поголовного уничтожения живых птиц на рынках Гонконга. После периода локальных и спорадических вспышек, новый вариант вируса H 5 N 1 начал быстро распространяться с 2003 г. Начиная с 2005 г. вирусы H 5 N 1 появились в Сибири среди дикой и домашней птицы, отсюда проникли в Европу и Африку. В это же время они стали эндемичными в популяции домашних птиц во многих странах Юго-восточной Азии.
 ПОДТВЕРЖДЕННЫЕ СЛУЧАИ ИНФИЦИРОВАНИЯ ЧЕЛОВЕКА ВИРУСОМ ГРИППА A/H 5 N 1 (С 2003 Г. ) 637 СЛУЧАЕВ, ИЗ НИХ 378 С ЛЕТАЛЬНЫМ ИСХОДОМ
ПОДТВЕРЖДЕННЫЕ СЛУЧАИ ИНФИЦИРОВАНИЯ ЧЕЛОВЕКА ВИРУСОМ ГРИППА A/H 5 N 1 (С 2003 Г. ) 637 СЛУЧАЕВ, ИЗ НИХ 378 С ЛЕТАЛЬНЫМ ИСХОДОМ
 ПЕРВАЯ ПАНДЕМИЯ ГРИППА В XXI В. Вирус А(H 1 N 1)pdm 09 свиного происхождения первоначально вызвал вспышку заболеваемости в Мексике и США в марте и апреле 2009 г. Вирус распространился по планете с такой быстротой, что 11 июня 2009 г. ВОЗ официально объявила первую пандемию гриппа в XXI в. Через несколько дней после первых сообщений из Мексики и США были расшифрованы полные геномы нескольких изолятов, филогенетики определили комплексное происхождение вируса. В течение нескольких недель был получен вакцинный штамм, и началось производство вакцины.
ПЕРВАЯ ПАНДЕМИЯ ГРИППА В XXI В. Вирус А(H 1 N 1)pdm 09 свиного происхождения первоначально вызвал вспышку заболеваемости в Мексике и США в марте и апреле 2009 г. Вирус распространился по планете с такой быстротой, что 11 июня 2009 г. ВОЗ официально объявила первую пандемию гриппа в XXI в. Через несколько дней после первых сообщений из Мексики и США были расшифрованы полные геномы нескольких изолятов, филогенетики определили комплексное происхождение вируса. В течение нескольких недель был получен вакцинный штамм, и началось производство вакцины.
 С помощью молекулярного анализа было выяснено, что пандемический вирус гриппа A(H 1 N 1)pdm 09 – это результат генетической реассортации вирусов человека, свиньи и птиц, которая произошла в организме свиньи, хотя свидетельств прямой передачи этого вируса от свиньи к человеку нет. В 2010 г. заболеваемость пошла на спад, и 10 августа Генеральный секретарь ВОЗ М. Чен объявила об окончании пандемии и наступлении постпандемического периода. Меньше чем за полтора года пандемия затронула 214 стран и территорий мира и стала причиной смерти по меньшей мере 18449 человек.
С помощью молекулярного анализа было выяснено, что пандемический вирус гриппа A(H 1 N 1)pdm 09 – это результат генетической реассортации вирусов человека, свиньи и птиц, которая произошла в организме свиньи, хотя свидетельств прямой передачи этого вируса от свиньи к человеку нет. В 2010 г. заболеваемость пошла на спад, и 10 августа Генеральный секретарь ВОЗ М. Чен объявила об окончании пандемии и наступлении постпандемического периода. Меньше чем за полтора года пандемия затронула 214 стран и территорий мира и стала причиной смерти по меньшей мере 18449 человек.
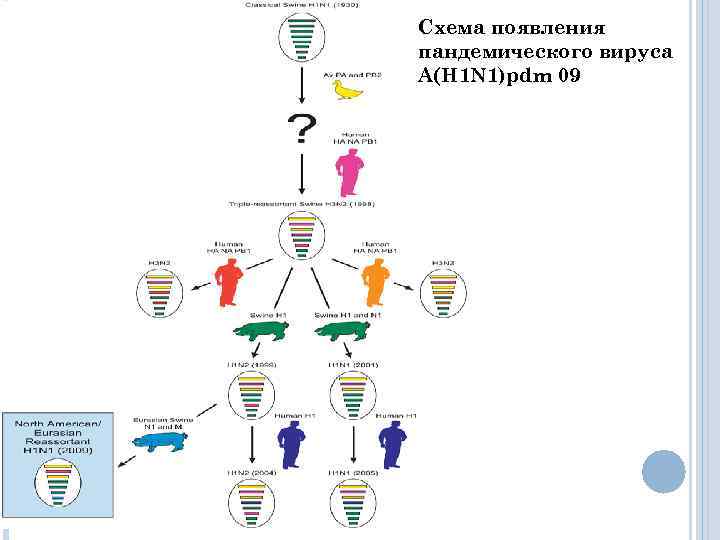 Схема появления пандемического вируса А(H 1 N 1)pdm 09
Схема появления пандемического вируса А(H 1 N 1)pdm 09
 ГРИППОЗНЫЕ ВАКЦИНЫ Существующие гриппозные вакцины можно разделить на два вида: аттенуированные (живые) и инактивированные, включая субъединичные. Аттенуированные вакцины представляют собой вирусы гриппа с ослабленной вирулентностью. При приготовлении инактивированных субъединичных вакцин также используются эпидемически актуальные штаммы вируса, хотя применение высокопатогенных штаммов ограничено высокими требованиями к биологической безопасности производства.
ГРИППОЗНЫЕ ВАКЦИНЫ Существующие гриппозные вакцины можно разделить на два вида: аттенуированные (живые) и инактивированные, включая субъединичные. Аттенуированные вакцины представляют собой вирусы гриппа с ослабленной вирулентностью. При приготовлении инактивированных субъединичных вакцин также используются эпидемически актуальные штаммы вируса, хотя применение высокопатогенных штаммов ограничено высокими требованиями к биологической безопасности производства.
 КОНСТРУИРОВАНИЕ ВИРУСА ГРИППА С ПОМОЩЬЮ ОБРАТНОЙ ГЕНЕТИКИ
КОНСТРУИРОВАНИЕ ВИРУСА ГРИППА С ПОМОЩЬЮ ОБРАТНОЙ ГЕНЕТИКИ
 Благодаря обратной генетике: удалось получить и исследовать вирус гриппа А (H 1 N 1), вызвавший в 1918 году пандемию ( «испанка» ); можно снижать вирулентность вируса путем введения мутаций в различные вирусные гены. Недостатки вакцин, полученных с помощью обратной генетики: возможность мутаций, восстанавливающих или повышающих вирулентность вируса; возможность реассортации живой вакцины с циркулирующими штаммами вирусов гриппа; вакцинные штаммы чаще всего получают в куриных эмбрионах, что делает невозможным вакцинацию лиц с аллергией на куриный белок; зависимость технологического процесса от продуктивности куриного стада.
Благодаря обратной генетике: удалось получить и исследовать вирус гриппа А (H 1 N 1), вызвавший в 1918 году пандемию ( «испанка» ); можно снижать вирулентность вируса путем введения мутаций в различные вирусные гены. Недостатки вакцин, полученных с помощью обратной генетики: возможность мутаций, восстанавливающих или повышающих вирулентность вируса; возможность реассортации живой вакцины с циркулирующими штаммами вирусов гриппа; вакцинные штаммы чаще всего получают в куриных эмбрионах, что делает невозможным вакцинацию лиц с аллергией на куриный белок; зависимость технологического процесса от продуктивности куриного стада.
 РЕКОМБИНАНТНЫЕ СУБЪЕДИНИЧНЫЕ ВАКЦИНЫ Гриппозные белки продуцируют в клетках насекомых при помощи бакуловирусных векторов, несущих гены целевых антигенов. Наиболее широко используют вирус множественного ядерного полиэдроза калифорнийской совки (Ac. MNPV). Для работы с Ac. MNPV обычно используют линии клеток Sf 9, полученные из яичника гусениц Spodoptera frugiperda. Иммунизация мышей рекомбинантным НА вируса гриппа H 5 N 1 приводила к индукции высокого уровня вируснейтрализующих антител. Однако для достижения значимых уровней антител требовалось либо применение адъюванта, либо праймбуст-иммунизация с помощью инактивированного вируса гриппа H 5 N 1 или рекомбинантного аденовируса, несущего ген НА вируса гриппа.
РЕКОМБИНАНТНЫЕ СУБЪЕДИНИЧНЫЕ ВАКЦИНЫ Гриппозные белки продуцируют в клетках насекомых при помощи бакуловирусных векторов, несущих гены целевых антигенов. Наиболее широко используют вирус множественного ядерного полиэдроза калифорнийской совки (Ac. MNPV). Для работы с Ac. MNPV обычно используют линии клеток Sf 9, полученные из яичника гусениц Spodoptera frugiperda. Иммунизация мышей рекомбинантным НА вируса гриппа H 5 N 1 приводила к индукции высокого уровня вируснейтрализующих антител. Однако для достижения значимых уровней антител требовалось либо применение адъюванта, либо праймбуст-иммунизация с помощью инактивированного вируса гриппа H 5 N 1 или рекомбинантного аденовируса, несущего ген НА вируса гриппа.
 Одним из наиболее перспективных кандидатов для создания субъединичных вакцин против вируса гриппа считается белок М 2, формирующий ионный канал. М 2 – один из трех белков вируса гриппа А, экспрессируемых на поверхности вириона, и, в отличие от НА и N A, высококонсервативный. В вирусах, циркулирующих в человеческой популяции, эктодомен белка М 2 (М 2 е) практически не претерпел изменений с 1933 года. Недостатки: низкая иммуногенность. Один из способов решения этой проблемы - включение в состав субъединичных вакцин молекулярных адъювантов – лигандов различных рецепторов системы врожденного иммунитета.
Одним из наиболее перспективных кандидатов для создания субъединичных вакцин против вируса гриппа считается белок М 2, формирующий ионный канал. М 2 – один из трех белков вируса гриппа А, экспрессируемых на поверхности вириона, и, в отличие от НА и N A, высококонсервативный. В вирусах, циркулирующих в человеческой популяции, эктодомен белка М 2 (М 2 е) практически не претерпел изменений с 1933 года. Недостатки: низкая иммуногенность. Один из способов решения этой проблемы - включение в состав субъединичных вакцин молекулярных адъювантов – лигандов различных рецепторов системы врожденного иммунитета.
 Рекомбинантный белок STF 2. 4×M 2 e, продуцируемый в клетках Escherichia coli и включающий флагеллин, лиганд для Toll-подобного рецептора 5 (TLR-5), позволял защитить иммунизированных мышей от летальной дозы вируса гриппа. Безопасность и эффективность вакцины на основе полученной конструкции показаны на взрослых добровольцах. Внутримышечная иммунизация мышей полученным в E. coli рекомбинантным слитым белком 4×M 2 e۰HSP 70 c, состоящим из последовательных повторов белков M 2 e и HSP 70 Mycobacterium tuberculosis, приводила к значительному снижению падения веса, уменьшению титра вируса в легких и менее выраженному проявлению симптомов заболевания при заражении летальной дозой вирусов гриппа А H 1 N 1, H 3 N 2 или H 9 N 2 (Ebrahimi et al. , 2012).
Рекомбинантный белок STF 2. 4×M 2 e, продуцируемый в клетках Escherichia coli и включающий флагеллин, лиганд для Toll-подобного рецептора 5 (TLR-5), позволял защитить иммунизированных мышей от летальной дозы вируса гриппа. Безопасность и эффективность вакцины на основе полученной конструкции показаны на взрослых добровольцах. Внутримышечная иммунизация мышей полученным в E. coli рекомбинантным слитым белком 4×M 2 e۰HSP 70 c, состоящим из последовательных повторов белков M 2 e и HSP 70 Mycobacterium tuberculosis, приводила к значительному снижению падения веса, уменьшению титра вируса в легких и менее выраженному проявлению симптомов заболевания при заражении летальной дозой вирусов гриппа А H 1 N 1, H 3 N 2 или H 9 N 2 (Ebrahimi et al. , 2012).
 ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ Вирусоподобные частицы (ВПЧ) представляют собой антигенные детерминанты вирионов без фрагментов геномной РНК. Благодаря отсутствию генетического материала ВПЧ не способны инфицировать клетки человека и животных, что обеспечивает их безопасность. Поверхностные белки гриппозных ВПЧ могут представлять конформационные эпитопы клеткам иммунной системы как нативные вирионы. Показано, что в формировании гриппозных ВПЧ ключевую роль играет участие внутреннего белка вируса гриппа – M 1. Он инициирует сборку и почкование ВПЧ, содержащих липидную мембрану клетки-хозяина с инкорпорированными в нее тремя трансмембранными белками вируса гриппа
ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ Вирусоподобные частицы (ВПЧ) представляют собой антигенные детерминанты вирионов без фрагментов геномной РНК. Благодаря отсутствию генетического материала ВПЧ не способны инфицировать клетки человека и животных, что обеспечивает их безопасность. Поверхностные белки гриппозных ВПЧ могут представлять конформационные эпитопы клеткам иммунной системы как нативные вирионы. Показано, что в формировании гриппозных ВПЧ ключевую роль играет участие внутреннего белка вируса гриппа – M 1. Он инициирует сборку и почкование ВПЧ, содержащих липидную мембрану клетки-хозяина с инкорпорированными в нее тремя трансмембранными белками вируса гриппа
 Один из подходов к получению гриппозных ВПЧ в клетках насекомых предполагает использование рекомбинантных бакуловирусов. На животных моделях показано, что поверхностные гриппозные антигены в составе ВПЧ, полученные при помощи рекомбинантных бакуловирусов, индуцировали выработку как антигемагглютинирующих и вируснейтрализующих антител, так и эффекторов клеточного иммунного ответа. Вакцина на основе гриппозных ВПЧ индуцировала протективный иммунитет против гомологичных и гетерологичных штаммов вируса гриппа А. Вакцина на основе ВПЧ, несущих антигены пандемичного вируса гриппа A H 1 N 1(2009), прошла вторую фазу клинических испытаний на 4563 здоровых взрослых добровольцах и показала безопасность и иммуногенность
Один из подходов к получению гриппозных ВПЧ в клетках насекомых предполагает использование рекомбинантных бакуловирусов. На животных моделях показано, что поверхностные гриппозные антигены в составе ВПЧ, полученные при помощи рекомбинантных бакуловирусов, индуцировали выработку как антигемагглютинирующих и вируснейтрализующих антител, так и эффекторов клеточного иммунного ответа. Вакцина на основе гриппозных ВПЧ индуцировала протективный иммунитет против гомологичных и гетерологичных штаммов вируса гриппа А. Вакцина на основе ВПЧ, несущих антигены пандемичного вируса гриппа A H 1 N 1(2009), прошла вторую фазу клинических испытаний на 4563 здоровых взрослых добровольцах и показала безопасность и иммуногенность
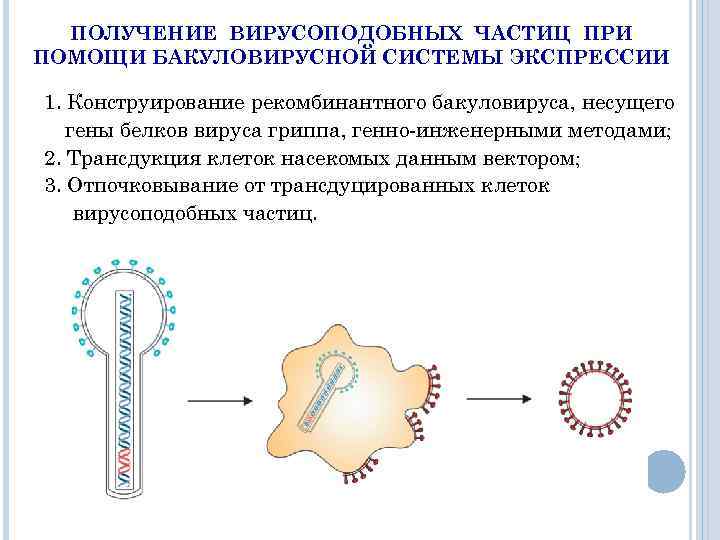 ПОЛУЧЕНИЕ ВИРУСOПОДОБНЫХ ЧАСТИЦ ПРИ ПОМОЩИ БАКУЛОВИРУСНОЙ СИСТЕМЫ ЭКСПРЕССИИ 1. Конструирование рекомбинантного бакуловируса, несущего гены белков вируса гриппа, генно-инженерными методами; 2. Трансдукция клеток насекомых данным вектором; 3. Отпочковывание от трансдуцированных клеток вирусoподобных частиц.
ПОЛУЧЕНИЕ ВИРУСOПОДОБНЫХ ЧАСТИЦ ПРИ ПОМОЩИ БАКУЛОВИРУСНОЙ СИСТЕМЫ ЭКСПРЕССИИ 1. Конструирование рекомбинантного бакуловируса, несущего гены белков вируса гриппа, генно-инженерными методами; 2. Трансдукция клеток насекомых данным вектором; 3. Отпочковывание от трансдуцированных клеток вирусoподобных частиц.
 ПРОТЕОСОМЫ Методами генной инженерии можно получить наноразмерные структуры, в состав которых входит целевой антиген, соединенный с носителем, состоящим из макромолекул биологического происхождения. В результате самосборки таких макромолекул могут быть получены так называемые протеосомы, представляющие собой комплекс белков, диаметром около 30 -60 нм, несущий на своей поверхности целевой антиген. В отличие от ВПЧ, основой для образования протеосом служит белок-носитель. Наиболее часто в качестве основы для создания протеосом используют белки вирусной оболочки, например пентон аденовируса, белок L 1 папилломавируса человека,
ПРОТЕОСОМЫ Методами генной инженерии можно получить наноразмерные структуры, в состав которых входит целевой антиген, соединенный с носителем, состоящим из макромолекул биологического происхождения. В результате самосборки таких макромолекул могут быть получены так называемые протеосомы, представляющие собой комплекс белков, диаметром около 30 -60 нм, несущий на своей поверхности целевой антиген. В отличие от ВПЧ, основой для образования протеосом служит белок-носитель. Наиболее часто в качестве основы для создания протеосом используют белки вирусной оболочки, например пентон аденовируса, белок L 1 папилломавируса человека,
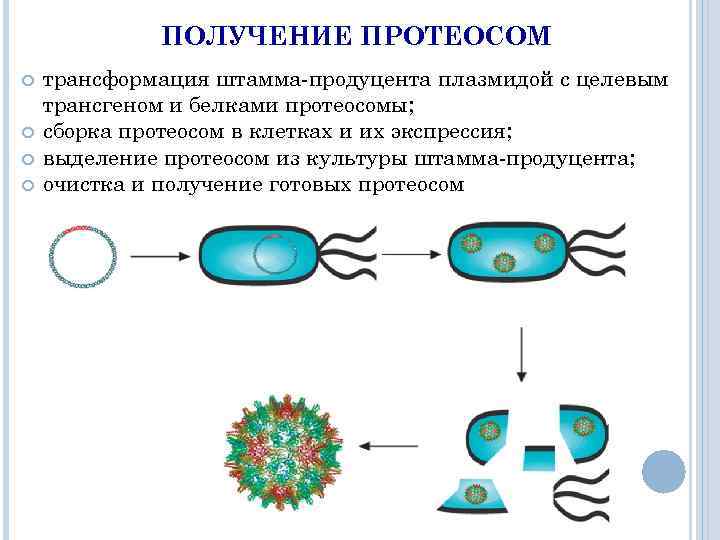 ПОЛУЧЕНИЕ ПРОТЕОСОМ трансформация штамма-продуцента плазмидой с целевым трансгеном и белками протеосомы; сборка протеосом в клетках и их экспрессия; выделение протеосом из культуры штамма-продуцента; очистка и получение готовых протеосом
ПОЛУЧЕНИЕ ПРОТЕОСОМ трансформация штамма-продуцента плазмидой с целевым трансгеном и белками протеосомы; сборка протеосом в клетках и их экспрессия; выделение протеосом из культуры штамма-продуцента; очистка и получение готовых протеосом
 ГЕНЕТИЧЕСКИЕ ВАКЦИНЫ Принцип создания любой генетической вакцины заключается в том, что определенный ген или участок генома патогена встраивается в вектор-носитель, который затем используется для вакцинации. Такие вакцины обеспечивают попадание генетического материала в клетки хозяина и экспрессию в них генов белков патогена. В результате экспрессируемые клетками организма антигены патогена распознаются иммунной системой, что приводит к индукции как гуморального, так и клеточного иммунного ответа. Структура целевых антигенов максимально близка к структуре, формируемой при вирусной инфекции.
ГЕНЕТИЧЕСКИЕ ВАКЦИНЫ Принцип создания любой генетической вакцины заключается в том, что определенный ген или участок генома патогена встраивается в вектор-носитель, который затем используется для вакцинации. Такие вакцины обеспечивают попадание генетического материала в клетки хозяина и экспрессию в них генов белков патогена. В результате экспрессируемые клетками организма антигены патогена распознаются иммунной системой, что приводит к индукции как гуморального, так и клеточного иммунного ответа. Структура целевых антигенов максимально близка к структуре, формируемой при вирусной инфекции.
 ДНК-ВАКЦИНЫ ДНК-вакцины – это бактериальные плазмиды, в которые включен целевой ген и регуляторные элементы, обеспечивающие его экспрессию после введения такой конструкции в организм. При использовании ДНК-вакцин, как правило, требуется применение адъювантов для повышения иммуногенности, а также таких процедур, как электропорация и gen-gun для лучшего проникновения генетического материала в клетки. Первая фаза клинических испытаний ДНК-вакцины, экспрессирующей НА вируса гриппа птиц A/Vietnam/1203/04 (H 5 N 1) с применением адъюванта, выявила образование гемагглютининингибирующих антител у 47– 67% и индукцию Т-клеточного ответа у 75– 100% иммунизированных добровольцев.
ДНК-ВАКЦИНЫ ДНК-вакцины – это бактериальные плазмиды, в которые включен целевой ген и регуляторные элементы, обеспечивающие его экспрессию после введения такой конструкции в организм. При использовании ДНК-вакцин, как правило, требуется применение адъювантов для повышения иммуногенности, а также таких процедур, как электропорация и gen-gun для лучшего проникновения генетического материала в клетки. Первая фаза клинических испытаний ДНК-вакцины, экспрессирующей НА вируса гриппа птиц A/Vietnam/1203/04 (H 5 N 1) с применением адъюванта, выявила образование гемагглютининингибирующих антител у 47– 67% и индукцию Т-клеточного ответа у 75– 100% иммунизированных добровольцев.
 ВАКЦИНЫ НА ОСНОВЕ РЕКОМБИНАНТНЫХ ВИРУСНЫХ ВЕКТОРОВ Вирусные векторы представляют собой рекомбинантные вирусы, в геном которых встроен целевой ген с набором регуляторных элементов. Вирусные векторы обладают следующими особенностями: o имеют природный механизм взаимодействия с клеткой и проникновения в нее; o переносят чужеродный генетический материал в ядро клетки; o способны обеспечивать длительную экспрессию антигена; o вирусная оболочка защищает генетический материал, кодирующий антиген.
ВАКЦИНЫ НА ОСНОВЕ РЕКОМБИНАНТНЫХ ВИРУСНЫХ ВЕКТОРОВ Вирусные векторы представляют собой рекомбинантные вирусы, в геном которых встроен целевой ген с набором регуляторных элементов. Вирусные векторы обладают следующими особенностями: o имеют природный механизм взаимодействия с клеткой и проникновения в нее; o переносят чужеродный генетический материал в ядро клетки; o способны обеспечивать длительную экспрессию антигена; o вирусная оболочка защищает генетический материал, кодирующий антиген.
 СХЕМА ПОЛУЧЕНИЯ РЕКОМБИНАНТНЫХ АДЕНОВИРУСОВ o получение геномной ДНК рекомбинантного аденовируса человека, несущей гены вируса гриппа, с помощью генно-инженерных методов; o трансфекция пермиссивной линии клеток ДНК рекомбинантного вируса; o экспрессия вирусных генов в клетках и сборка рекомбинантных аденовирусных частиц; o очистка аденовирусных вирионов из суспензии клеток
СХЕМА ПОЛУЧЕНИЯ РЕКОМБИНАНТНЫХ АДЕНОВИРУСОВ o получение геномной ДНК рекомбинантного аденовируса человека, несущей гены вируса гриппа, с помощью генно-инженерных методов; o трансфекция пермиссивной линии клеток ДНК рекомбинантного вируса; o экспрессия вирусных генов в клетках и сборка рекомбинантных аденовирусных частиц; o очистка аденовирусных вирионов из суспензии клеток
 Вирусные векторы обладают способностью активировать врожденный иммунитет путем связывания генетического материала или белков их оболочки с паттерн-распознающими рецепторами (TLR, RIG-1 и др. ). Вирусные векторы распознаются TLR 2, TLR 3, TLR 4, TLR 7, TLR 8, TLR 9. При взаимодействии этих рецепторов с лигандами активируются различные факторы транскрипции, что приводит к формированию очага воспаления и быстрой активации защитных реакций организма. Не все вирусы обладают свойствами, необходимыми для создания эффективных векторов. Для создания гриппозных вакцин на основе вирусных векторов в настоящее время наиболее широко используются поксвирусы, вирус болезни Ньюкасла и аденовирусы.
Вирусные векторы обладают способностью активировать врожденный иммунитет путем связывания генетического материала или белков их оболочки с паттерн-распознающими рецепторами (TLR, RIG-1 и др. ). Вирусные векторы распознаются TLR 2, TLR 3, TLR 4, TLR 7, TLR 8, TLR 9. При взаимодействии этих рецепторов с лигандами активируются различные факторы транскрипции, что приводит к формированию очага воспаления и быстрой активации защитных реакций организма. Не все вирусы обладают свойствами, необходимыми для создания эффективных векторов. Для создания гриппозных вакцин на основе вирусных векторов в настоящее время наиболее широко используются поксвирусы, вирус болезни Ньюкасла и аденовирусы.
 При выборе вирусного вектора для генетической иммунизации необходимо руководствоваться следующими критериями: такая вакцина не должна вызывать симптомов заболевания, она должна быть безопасной для людей с ослабленным иммунитетом, пожилых и детей; собственные белки рекомбинантного вируса не должны вызывать сильного иммунного ответа; вирусный вектор должен быть простым для генетических манипуляций и позволять включать большие фрагменты чужеродной ДНК; полученные препараты должны иметь высокий титр и обеспечивать высокий уровень экспрессии целевых антигенов; при иммунизации ДНК вирусного вектора не должна интегрировать в геном клетки-хозяина, и сам вектор должен полностью выводиться из организма после индукции иммунного ответа; нежелательно наличие предсуществующего иммунного ответа к белкам вирусного вектора у иммунизируемых индивидов, так как он может существенно снизить уровень иммунного ответа на целевой антиген
При выборе вирусного вектора для генетической иммунизации необходимо руководствоваться следующими критериями: такая вакцина не должна вызывать симптомов заболевания, она должна быть безопасной для людей с ослабленным иммунитетом, пожилых и детей; собственные белки рекомбинантного вируса не должны вызывать сильного иммунного ответа; вирусный вектор должен быть простым для генетических манипуляций и позволять включать большие фрагменты чужеродной ДНК; полученные препараты должны иметь высокий титр и обеспечивать высокий уровень экспрессии целевых антигенов; при иммунизации ДНК вирусного вектора не должна интегрировать в геном клетки-хозяина, и сам вектор должен полностью выводиться из организма после индукции иммунного ответа; нежелательно наличие предсуществующего иммунного ответа к белкам вирусного вектора у иммунизируемых индивидов, так как он может существенно снизить уровень иммунного ответа на целевой антиген
 ЗАКЛЮЧЕНИЕ Таким образом, в настоящее время идут широкомасштабные работы, направленные на конструирование гриппозных вакцин при помощи новых подходов, использующих возможности обратной генетики и рекомбинантные технологии, получение ВПЧ, протеосом и субъединичных вакцин в различных системах экспрессии. Новые подходы позволили существенно продвинуться в создании гриппозных вакцин нового типа. Некоторые из этих вакцин в настоящее время проходят либо доклинические исследования, либо клинические испытания. Тем не менее, до создания универсальной гриппозной вакцины, способной защитить человека от широкого спектра вирусных субтипов, к сожалению, еще далеко.
ЗАКЛЮЧЕНИЕ Таким образом, в настоящее время идут широкомасштабные работы, направленные на конструирование гриппозных вакцин при помощи новых подходов, использующих возможности обратной генетики и рекомбинантные технологии, получение ВПЧ, протеосом и субъединичных вакцин в различных системах экспрессии. Новые подходы позволили существенно продвинуться в создании гриппозных вакцин нового типа. Некоторые из этих вакцин в настоящее время проходят либо доклинические исследования, либо клинические испытания. Тем не менее, до создания универсальной гриппозной вакцины, способной защитить человека от широкого спектра вирусных субтипов, к сожалению, еще далеко.
 СПАСИБО ЗА ВНИМАНИЕ Образ развития НГУ до 2030 года
СПАСИБО ЗА ВНИМАНИЕ Образ развития НГУ до 2030 года


