Миокардиты Этиология и Лечение.pptx
- Количество слайдов: 16


*Вирусы: аденовирус, арбовирус, ареновирус, вирус Коксаки, вирус Эпштейна-Барр, цитомегаловирус, , вирус энцефаломиокардита, гепатита В, вирус герпеса человека 6, вирус иммунодефицита человека-1, вирус гриппа В, вирус паротита, парвовирус В 19, вирус полиомиелита, бешенства, респираторно-синцитиальный вирус, вирус краснухи, вирус коровьей оспы, вирус натуральной оспы

*Бактерии: Brucellosis, Clostridia, Diphtheria, Francisella, Gonococcus, Haemophilus, Legionella, Meningococcus, Mycobacterium, Mycoplasma, Pneumococcus, Psittacosis, Salmonella, Staphylococcus, Streptococcus, Tropheryma whippleii

*Грибки: Actinomyces, Aspergillus, Blastomyces, Candida, Coccidioides, Cryptococcus, Histoplasma, Nocardia, Sporothrix *Риккетсии: Пятнистая лихорадка Скалистых гор, лихорадка Q, сыпной тиф, тиф

*Спирохеты: Borrelia, Leptospira, Syphilis *Гельминты: Cysticercus, Echinococcus, Schistosoma, Toxocara, Trichinella *Протозойные: Entamoeba, Leishmania, Trypanosoma, Toxoplasmosis

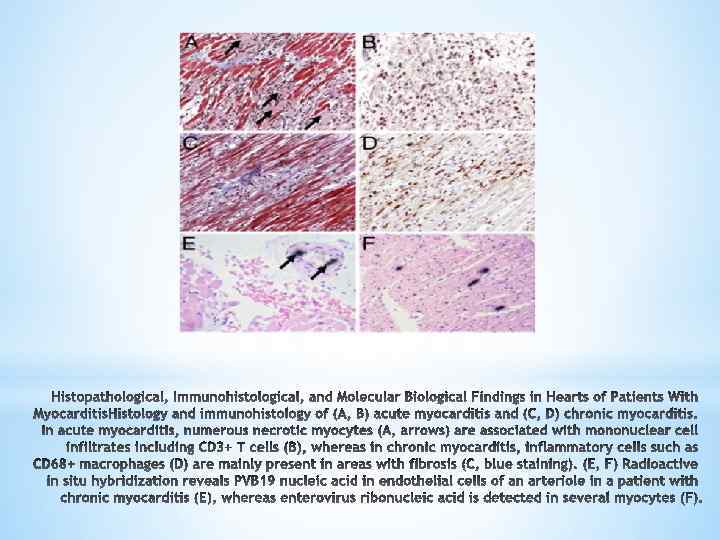
* ЭМБ до сих пор остается золотым стандартом в диагностике миокардитов. В соответствии с критериями Даллас, острый миокардит определяется лимфоцитарной инфильтрацией с некрозом миоцитов (рис. 4 А и 4 В ). Пограничный миокардит характеризуется воспалительными инфильтратами без признаков некроза миоцитов. Критерии Даллас ограничены высокой вариабельность в интерпретации биопсии ( в частности, в отношении пограничного миокардита ) и потому неклеточные воспалительные процессы не могут быть обнаружены. Таким образом, иммуногистохимия ( рис. 4 В и рис 4 D) набирает дальнейшее распространение в диагностике миокардита. Моноклональные антитела позволяют характеризовать и локализовать инфильтраты мононуклеарных клеток : например, CD 3 для Т-клетки, PGM 1 ( CD 68 ) для активированных макрофагов , а человеческого лейкоцитарного антигена (HLA) -DR- α для оценки выраженности HLA класс II в антиген-презентирующих иммунных клетках.

С использованием этих иммуногистологических методов количество выявления миокардита с помощью ЭМБ заметно увеличилось. С помощью ЭМБ возможно обнаружение иммуногистохимически очаговых или диффузных мононуклеарных инфильтратов ( Т-лимфоцитов и макрофагов) с > 14 клеток/mm 2 , в дополнение к повышенной экспрессии молекул HLA класса II. Молекулярно-биологических обнаружение кардиотропных вирусов могут быть выполнены встроенной ПЦР в реальном времени. Методы гибридизации позволяют идентифицировать типы клеток реплицирующихся вирусных геномов , как показано на PVB 19 и энтеровирусов на рисунке 4 E и рис 4 F. Из-за отсутствия доступных объектов и клинического опыта ЭМБ, по-видимому, редко используется для диагностики миокардита. Однако, когда исследование выполняется опытными специалистами, ЭМБ левого и правого желудочков является безопасной процедурой, с количеством крупных осложнений < 1%. Недавние исследования показали, не только диагностическое , но и прогностическое значение ЭМБ у пациентов с подозрением на миокардит.


* *Хотя лечение миокардита должно быть сосредоточено на этиопатофизиологическом аспекте, эффект от терапии конкретного возбудителя был подтвержден только в нескольких исследованиях по воспалительным заболеваниям сердца, таким как саркоидоз и гигантоклеточный миокардит. Из-за высокой заболеваемости дисфункцией ЛЖ, на основе фактических данных терапия сердечной недостаточности является обязательной у таких пациентов.

В терапии конкретных видов миокардита, основанных на аутоиммунитете используют метод иммуносупрессии, например, у пациентов с гигантоклеточным миокардитом или кардиосаркоидозом. В случае гигантоклеточным миокардитом, комбинированное лечение с иммунодепрессантами ( циклоспорин и кортикостероидов с или без азатиоприном или muronomab -CDs ) может улучшить прогноз, и дает среднюю выживаемость 12 месяцев по сравнению с 3 -мя месяцами для неполучавших терапию пациентов. Тем не менее, малое количество пациентов требует поддержки механического кровообращения или трансплантации сердца в течение 1 года. Снижение иммунитета может приводить к повторяющимся и иногда со смертельным исходом гигантоклеточным миокардитаи. В случае кардиосаркоидоза, ранняя иммуносупрессивная терапия высокими дозами кортикостероидов была связана с улучшением функции сердца. Прогноз для пациентов с лечением является переменной величиной, с выживанием в диапазоне от 60 % до 90% в течение 5 лет. Конкретные варианты лечения вирусного миокардита пока не установлены.

* *Обоснованием для использования иммуноглобулина при вирусной этиологии миокардитов являются их противовирусные и иммуномодулирующие эффекты. В ранних проявлениях миокардита или ДКМП, не было никакого различия в функции ЛЖ у пациентов, получавших внутривенно иммуноглобулин и пациентов, получавших плацебо. Однако дети с острыми миокардитами показали улучшение функции ЛЖ и выживания в первый год после лечения.

* * Целью иммуноадсорбции является устранение anticardiac антител против различных белков клеток сердца, которые были выявлены у пациентов с ДКМП и миокардитом. Существует доказательство того, что удаление циркулирующих антител при иммуноадсорбции у пациентов с ДКМП улучшило сердечную функцию и клинические и гуморальный маркеры тяжести сердечной недостаточности (толерантность к физической нагрузке, N-терминальный про-В-типа натрийуретический пептид (NT-про-BNP), а также показатели гемодинамики ( индекс ударного объема, системное сосудистое сопротивление). Кроме того, при иммуноадсорбции снижалось воспаление миокарда. У пациентов с воспалительной кардиомиопатией, систолическая функция ЛЖ улучшилась после иммуноадсорбции А протеина. В настоящее время многоцентровое, рандомизированное, двойное плацебоконтролируемое, проспективное исследование по вопросу о влияниях иммуноадсорбции на функцию сердца у 200 пациентов с ДКМП продолжается (NCT 00558584)

* Лечение иммунодепрессантами (циклоспорин, преднизолон, азатиоприн) острого миокардита показали противоречивые результаты. При ДКМП азатиоприн и преднизолон привели к улучшению функции ЛЖ и класса NYHA. TIMIC(Immunosuppressive Therapy in Patients With Virus Negative Inflammatory Cardiomyopathy) исследование было первое рандомизированное, плацебо-контролируемое исследование, в котором все ДКМП были изучены на предмет воспаления с помощью гистологических и иммуногистологических критериев. Молекулярно-биологические исследования были выполнены во всех биоптатах, чтобы исключить вирусную инфекцию. Было доказано значительное улучшение ФВ ЛЖ и уменьшение размеров ЛЖ в результате иммуносупрессивной терапии с преднизолоном и азатиоприном.

* Обоснованием для использования противовирусных препаратов является результаты исследований, показывающих, что наиболее распространенные случаи миокардита, вызванны вирусными инфекциями. В мышиной модели Коксаки В 3 – индуцированного миокардита , терапия интерферон (IFN) бета и IFN- альфа-2 защищала миоциты от повреждения и снижалось количество воспалительных инфильтратов. Тем не менее, использование только IFN- бета привело к устранению вирусной нагрузки на сердце. Лечение IFN- бета у пациентов с инфарктом энтеровирусной или аденовирусной природы и дисфункцией ЛЖ показали ликвидацию вирусных геномов у всех пациентов и улучшение функции ЛЖ в 15 из 22 больных.

* В последующем плацебо-контролируемое , рандомизированное, двойное слепое , по всей Европе многоцентровое BICC(Betaferon in patients with chronic viral cardiomyopathy ) исследование, 143 больных с воспалительной ДКМП и подтвержденной вирусной инфекцией миокарда лечили Бетафероном (IFN- бета-1 b ) по сравнению с плацебо. При лечении Бетафероном значительно снижалась вирусная нагрузка ( энтеровирусы ) в миокарде , однако полного вирусного устранения ( PVB 19 ) не было достигнуто у всех больных. Многочисленные параметры были оценены , но только функциональный класс по NYHA и общее самочувствие пациентов улучшались.
Миокардиты Этиология и Лечение.pptx