12_ВИРУСНЫЕ ИНФЕКЦИИ.ppt
- Количество слайдов: 76
 Вирусные инфекции Противовирусный иммунитет Профилактика и терапия вирусных инфекций Шабан Ж. Г.
Вирусные инфекции Противовирусный иммунитет Профилактика и терапия вирусных инфекций Шабан Ж. Г.
 Вирусные инфекции
Вирусные инфекции
 Особенности физиологии вирусов 1. Вирусы – облигатные внутриклеточные паразиты, размножаются в живых клетках. Строгий паразитизм вирусов (неспособность вирусов к размножению вне клетки-хозяина) обусловлен: - отсутствием у вирусов белоксинтезирующих систем; вирусы используют белоксинтезирующие системы клетки-хозяина - Использованием для репликации НК клеточных ферментов 2. Строгий цитотропизм вирусов (репликация в определённых клетках) обусловлен возможностью вируса поразить клетку, имеющие соответствующие этому вирусу: - рецепторы для адсорбции - ферменты депротеинизации Вирусы, репродуцирующиеся в клетках печени - гепатотропные, в нейронах – нейротропные и т. д.
Особенности физиологии вирусов 1. Вирусы – облигатные внутриклеточные паразиты, размножаются в живых клетках. Строгий паразитизм вирусов (неспособность вирусов к размножению вне клетки-хозяина) обусловлен: - отсутствием у вирусов белоксинтезирующих систем; вирусы используют белоксинтезирующие системы клетки-хозяина - Использованием для репликации НК клеточных ферментов 2. Строгий цитотропизм вирусов (репликация в определённых клетках) обусловлен возможностью вируса поразить клетку, имеющие соответствующие этому вирусу: - рецепторы для адсорбции - ферменты депротеинизации Вирусы, репродуцирующиеся в клетках печени - гепатотропные, в нейронах – нейротропные и т. д.
 Типы вирусной инфекции клеток 1. Автономная – вирусный геном реплицируется независимо от клеточного: продуктивная – осуществляется в результате размножения (репродукции) вируса (англ. reproduce – воспроизводить), в вирусинфицированных клетках образуется новое поколение вирионов и развивается литическая инфекция: - вирионы выходят из клетки при её лизисе - множественное отпочковывание вирионов от ЦПМ клетки приводит к её лизису абортивная – синтез вирусных частиц в клетке-хозяине останавливается на любом из этапов, инфекционный процесс обрывается, новых вирионов мало или нет
Типы вирусной инфекции клеток 1. Автономная – вирусный геном реплицируется независимо от клеточного: продуктивная – осуществляется в результате размножения (репродукции) вируса (англ. reproduce – воспроизводить), в вирусинфицированных клетках образуется новое поколение вирионов и развивается литическая инфекция: - вирионы выходят из клетки при её лизисе - множественное отпочковывание вирионов от ЦПМ клетки приводит к её лизису абортивная – синтез вирусных частиц в клетке-хозяине останавливается на любом из этапов, инфекционный процесс обрывается, новых вирионов мало или нет
 Продуктивная и абортивная инфекция может быть: А) острая, в зависимости от исхода: - цитолитическая – завершается деструктивными изменениями вирусинфицированных клеток и их гибелью - нецитолитическая – не сопровождается деструктивными изменениями вирусинфицированных клеток и их гибелью Б) хроническая – клетки быстро не погибают, долго жизнеспособны и внешне могут не отличаться от вирусинфицированных
Продуктивная и абортивная инфекция может быть: А) острая, в зависимости от исхода: - цитолитическая – завершается деструктивными изменениями вирусинфицированных клеток и их гибелью - нецитолитическая – не сопровождается деструктивными изменениями вирусинфицированных клеток и их гибелью Б) хроническая – клетки быстро не погибают, долго жизнеспособны и внешне могут не отличаться от вирусинфицированных
 2. Интеграционная (вирогения) – вирусный геном включается в состав клеточного Для интеграции с клеточным геномом необходима кольцевая форма двунитевой в. ДНК Провирус (встроенная в состав хромосомы клетки в. ДНК) реплицируется в составе хромосомы и переходит в геном дочерних клеток, т. е. состояние вирогении наследуется При вирогении отсутствуют стадии: репродукции выхода вируса из клетки
2. Интеграционная (вирогения) – вирусный геном включается в состав клеточного Для интеграции с клеточным геномом необходима кольцевая форма двунитевой в. ДНК Провирус (встроенная в состав хромосомы клетки в. ДНК) реплицируется в составе хромосомы и переходит в геном дочерних клеток, т. е. состояние вирогении наследуется При вирогении отсутствуют стадии: репродукции выхода вируса из клетки
 На способности вирусов к интеграции с геномом клетки основана персистенция (лат. persisto - постоянно пребывать, оставаться) вирусов в организме (ВГВ способен вызывать персистирующие поражения с развитием хр. гепатита и рака печени) Дополнительная генетическая информация провируса при вирогении сообщает клетке новые свойства развитие опухолей, аутоиммунных и хронических заболеваний Под влиянием физических или химических факторов провирус может перейти в автономное состояние продуктивный тип взаимодействия с клеткой синтез полноценных вирусных частиц
На способности вирусов к интеграции с геномом клетки основана персистенция (лат. persisto - постоянно пребывать, оставаться) вирусов в организме (ВГВ способен вызывать персистирующие поражения с развитием хр. гепатита и рака печени) Дополнительная генетическая информация провируса при вирогении сообщает клетке новые свойства развитие опухолей, аутоиммунных и хронических заболеваний Под влиянием физических или химических факторов провирус может перейти в автономное состояние продуктивный тип взаимодействия с клеткой синтез полноценных вирусных частиц
 Типы вирусной инфекции клеток
Типы вирусной инфекции клеток
 Механизмы поражения вирусами клеток организма По отношению к клеткам, в которых репродуцируются, вирусы могут вызывать действие: Цитопатическое – изменение клеток (образование включений, изменение формы и размеров клеток) без их гибели Цитотоксическое – гибель клеток в результате размножения в них вируса Иммуноопосредованное – вирусинфицированные клетки могут погибать в результате аутоиммунного процесса, индуцированного вирусными АГ, экспрессированными на поверхности поражённых клеток Механизмы гибели клеток: - действие цитотоксических Т-л комплементзависимый лизис АЗКЦ
Механизмы поражения вирусами клеток организма По отношению к клеткам, в которых репродуцируются, вирусы могут вызывать действие: Цитопатическое – изменение клеток (образование включений, изменение формы и размеров клеток) без их гибели Цитотоксическое – гибель клеток в результате размножения в них вируса Иммуноопосредованное – вирусинфицированные клетки могут погибать в результате аутоиммунного процесса, индуцированного вирусными АГ, экспрессированными на поверхности поражённых клеток Механизмы гибели клеток: - действие цитотоксических Т-л комплементзависимый лизис АЗКЦ
 Типы вирусной инфекции организма По уровню охвата организма: 1) очаговая – вирус репродуцируется в клетках локально в месте входных ворот (ОРВИ, ОКВИ) 2) генерализованная – вирус локально репродуцируется, затем гематогенно или лимфогенно разносится в различные органы и ткани вторичные очаги инфекции (полиомиелит, корь, оспа)
Типы вирусной инфекции организма По уровню охвата организма: 1) очаговая – вирус репродуцируется в клетках локально в месте входных ворот (ОРВИ, ОКВИ) 2) генерализованная – вирус локально репродуцируется, затем гематогенно или лимфогенно разносится в различные органы и ткани вторичные очаги инфекции (полиомиелит, корь, оспа)
 Типы вирусной инфекции организма По характеру течения: 1) острая – непродолжительная, сопровождается выделением вируса в окружающую среду, чаще заканчивается реконвалесценцией. Может проявляться типичными симптомами (манифестная), а может быть бессимптомной (инаппарантная). 2) персистентная (ПИ) возникает при длительном взаимодействии вируса с организмом. Клинические проявления выражены, слабо выражены или отсутствуют. Вирус выделяется в окружающую среду или нет. Виды ПИ: - латентные – скрытые, без клинических проявлений и без выделения вируса (онкогенные вирусы, ВИЧ, в. герпеса, аденовирусы) - хронические – с периодами обострений (когда вирус выделяется в окружающую среду) и ремиссий (герпетическая и аденовирусная инфекции, ВГВ, ВГС) - медленные – длительный инкубационный период, медленное прогрессирующее развитие симптомов тяжёлое нарушение функций организма и летальный исход (ПСПЭ)
Типы вирусной инфекции организма По характеру течения: 1) острая – непродолжительная, сопровождается выделением вируса в окружающую среду, чаще заканчивается реконвалесценцией. Может проявляться типичными симптомами (манифестная), а может быть бессимптомной (инаппарантная). 2) персистентная (ПИ) возникает при длительном взаимодействии вируса с организмом. Клинические проявления выражены, слабо выражены или отсутствуют. Вирус выделяется в окружающую среду или нет. Виды ПИ: - латентные – скрытые, без клинических проявлений и без выделения вируса (онкогенные вирусы, ВИЧ, в. герпеса, аденовирусы) - хронические – с периодами обострений (когда вирус выделяется в окружающую среду) и ремиссий (герпетическая и аденовирусная инфекции, ВГВ, ВГС) - медленные – длительный инкубационный период, медленное прогрессирующее развитие симптомов тяжёлое нарушение функций организма и летальный исход (ПСПЭ)
 Объяснения длительной персистенции вирусов в мозговых тканях или внутренних органах (в иммунном организме): переход вируса или субвирусных структур непосредственно из клетки в клетку, минуя барьер АТ геном вируса переписан в ДНК и интегрирован в геноме вирусинфицированных клеток. Продукция такими клетками вирусоспецифических белков делает их чужеродными для организма, они становятся предметом атаки ИКК аутоиммунное заболевание При активации персистирующего вируса может развиваться: рецидив того же заболевания другое заболевание, вызываемое тем же самым вирусом другое заболевание, вызванное другим вирусом, который активизировался в организме хозяина под влиянием персистирующего вируса иммунопатологические процессы в связи с накоплением преципитатов АГ-АТ в почках и печени (часть хр. нефропатий и гепатопатий имеет такую природу)
Объяснения длительной персистенции вирусов в мозговых тканях или внутренних органах (в иммунном организме): переход вируса или субвирусных структур непосредственно из клетки в клетку, минуя барьер АТ геном вируса переписан в ДНК и интегрирован в геноме вирусинфицированных клеток. Продукция такими клетками вирусоспецифических белков делает их чужеродными для организма, они становятся предметом атаки ИКК аутоиммунное заболевание При активации персистирующего вируса может развиваться: рецидив того же заболевания другое заболевание, вызываемое тем же самым вирусом другое заболевание, вызванное другим вирусом, который активизировался в организме хозяина под влиянием персистирующего вируса иммунопатологические процессы в связи с накоплением преципитатов АГ-АТ в почках и печени (часть хр. нефропатий и гепатопатий имеет такую природу)
 Типы вирусной инфекции организма
Типы вирусной инфекции организма
 Особенности вирусных инфекций 1. 2. 3. 4. Убиквитарность (встречаются повсеместно). Широко распространены, их удельный вес в структуре инфекционной заболеваемости – 75% Внутриклеточная репродукция вирусов массовая гибель клеток поражённых органов Иммунотропное действие вирусов обусловлено их лимфотропностью. Факультативно лимфотропные вирусы - количества Т-л (в. герпеса, ветряной оспы, цитомегалии) - активация Т-л (в. клещевого энцефалита) - функции Т-л (в. гриппа, кори, герпеса, полиомиелита, ротавирусы) Облигатно лимфотропные вирусы Т-лимфотропные: - вызывают трансформацию и пролиферацию Т-л лейкоз (HTLV-I, HTLV-II) - вызывает деструкцию Т-л (ВИЧ ВИДС) B-лимфотропный: вызывает трансформацию и пролиферацию В-л лейкоз (ВЭБ)
Особенности вирусных инфекций 1. 2. 3. 4. Убиквитарность (встречаются повсеместно). Широко распространены, их удельный вес в структуре инфекционной заболеваемости – 75% Внутриклеточная репродукция вирусов массовая гибель клеток поражённых органов Иммунотропное действие вирусов обусловлено их лимфотропностью. Факультативно лимфотропные вирусы - количества Т-л (в. герпеса, ветряной оспы, цитомегалии) - активация Т-л (в. клещевого энцефалита) - функции Т-л (в. гриппа, кори, герпеса, полиомиелита, ротавирусы) Облигатно лимфотропные вирусы Т-лимфотропные: - вызывают трансформацию и пролиферацию Т-л лейкоз (HTLV-I, HTLV-II) - вызывает деструкцию Т-л (ВИЧ ВИДС) B-лимфотропный: вызывает трансформацию и пролиферацию В-л лейкоз (ВЭБ)
 5. Тератогенные свойства некоторых вирусов (краснухи, цитомегалии) – поражение ими плода при проникновении ч/з плаценту. Реализуется при вирусемии у беременной, особенно в I триместре 6. Онкогенное действие вирусов – индуцирование ими опухолевой трансформации клеток при хр. вирусных инфекциях (аденовирусы, герпесвирусы, в. гепатитов В, С, G) 7. Вирусы могут вызывать медленные инфекции (ВИЧ, в. кори) 8. Толерогенное действие вирусов – индуцируют иммунологическую толерантность к своим и к гетерологичным АГ
5. Тератогенные свойства некоторых вирусов (краснухи, цитомегалии) – поражение ими плода при проникновении ч/з плаценту. Реализуется при вирусемии у беременной, особенно в I триместре 6. Онкогенное действие вирусов – индуцирование ими опухолевой трансформации клеток при хр. вирусных инфекциях (аденовирусы, герпесвирусы, в. гепатитов В, С, G) 7. Вирусы могут вызывать медленные инфекции (ВИЧ, в. кори) 8. Толерогенное действие вирусов – индуцируют иммунологическую толерантность к своим и к гетерологичным АГ
 9. Интеграция некоторых вирусов с геномом клетки-хозяина (ВИЧ, ВГВ, онкогенные РНК-вирусы) влияние на экспрессию генов клетки-хозяина 10. При одновременном заражении чувствительной клетки несколькими штаммами вируса возможны рекомбинации – обмен генетическим материалом между штаммами вируса различные варианты одного и того же вируса (ВИЧ) 11. Отсутствие препаратов для специфической иммунопрофилактики и этиотропной химиотерапии многих вирусных инфекций 12. Этиологическая диагностика вирусных инфекций трудоёмка, из-за массовости ряда инфекций применяется редко
9. Интеграция некоторых вирусов с геномом клетки-хозяина (ВИЧ, ВГВ, онкогенные РНК-вирусы) влияние на экспрессию генов клетки-хозяина 10. При одновременном заражении чувствительной клетки несколькими штаммами вируса возможны рекомбинации – обмен генетическим материалом между штаммами вируса различные варианты одного и того же вируса (ВИЧ) 11. Отсутствие препаратов для специфической иммунопрофилактики и этиотропной химиотерапии многих вирусных инфекций 12. Этиологическая диагностика вирусных инфекций трудоёмка, из-за массовости ряда инфекций применяется редко
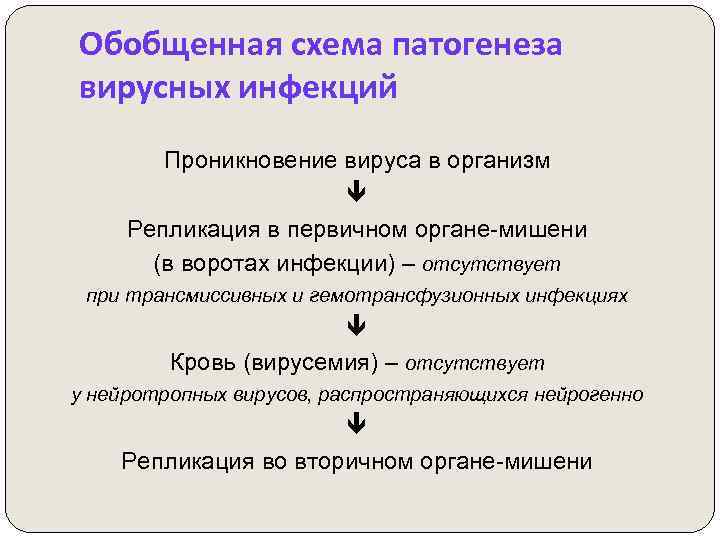 Обобщенная схема патогенеза вирусных инфекций Проникновение вируса в организм Репликация в первичном органе-мишени (в воротах инфекции) – отсутствует при трансмиссивных и гемотрансфузионных инфекциях Кровь (вирусемия) – отсутствует у нейротропных вирусов, распространяющихся нейрогенно Репликация во вторичном органе-мишени
Обобщенная схема патогенеза вирусных инфекций Проникновение вируса в организм Репликация в первичном органе-мишени (в воротах инфекции) – отсутствует при трансмиссивных и гемотрансфузионных инфекциях Кровь (вирусемия) – отсутствует у нейротропных вирусов, распространяющихся нейрогенно Репликация во вторичном органе-мишени
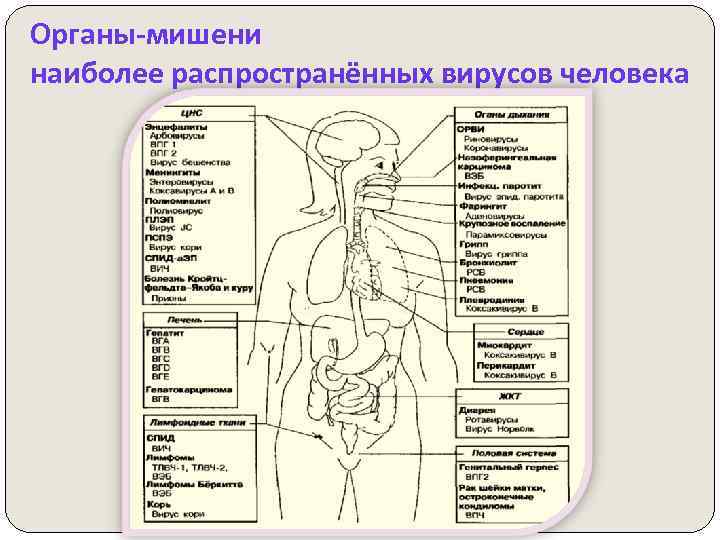 Органы-мишени наиболее распространённых вирусов человека
Органы-мишени наиболее распространённых вирусов человека
 Противовирусный иммунитет
Противовирусный иммунитет
 Особенности противовирусного иммунитета обусловлены Особенностями строения вирусов Небольшим набором поверхностных АГ оболочек вирусов Возможностью дрейфа поверхностных АГ Строгим внутриклеточным паразитизмом вирусов Особенностью взаимодействия вирусов с чувствительными клетками
Особенности противовирусного иммунитета обусловлены Особенностями строения вирусов Небольшим набором поверхностных АГ оболочек вирусов Возможностью дрейфа поверхностных АГ Строгим внутриклеточным паразитизмом вирусов Особенностью взаимодействия вирусов с чувствительными клетками
 Неиммунные механизмы врождённого противовирусного иммунитета 1. Ареактивность клеток – отсутствие на клеточной мембране специфических рецепторов, комплементарных поверхностным белкам вириона вирусов 2. Механическая защита: целостные слизистые оболочки и кожные покровв препятствуют внедрению вируса в организм
Неиммунные механизмы врождённого противовирусного иммунитета 1. Ареактивность клеток – отсутствие на клеточной мембране специфических рецепторов, комплементарных поверхностным белкам вириона вирусов 2. Механическая защита: целостные слизистые оболочки и кожные покровв препятствуют внедрению вируса в организм
 Иммунные механизмы врождённого противовирусного иммунитета 1. Гуморальные: - сывороточные противовирусные ингибиторы неспецифически связываются с вирусной частицей, нейтрализуют её препятствие адсорбции вируса на клетках-мишенях - интерфероны - система комплемента комлементзависимый лизис инфицированных клеток 2. Клеточные: ЕКК уничтожают инфицированные вирусами клетки, распознавая экпрессированные на их поверхности вирусспецифические АГ Мф: фагоцитоз при вирусных инфекциях играет двоякую роль: - фагоциты не инактивируют вирусные частицы и разносят их по организму - фагоцитирующие клетки презентируют вирусные АГ Т-лимфоцитам и дают начало иммунному ответу на проникновение вируса
Иммунные механизмы врождённого противовирусного иммунитета 1. Гуморальные: - сывороточные противовирусные ингибиторы неспецифически связываются с вирусной частицей, нейтрализуют её препятствие адсорбции вируса на клетках-мишенях - интерфероны - система комплемента комлементзависимый лизис инфицированных клеток 2. Клеточные: ЕКК уничтожают инфицированные вирусами клетки, распознавая экпрессированные на их поверхности вирусспецифические АГ Мф: фагоцитоз при вирусных инфекциях играет двоякую роль: - фагоциты не инактивируют вирусные частицы и разносят их по организму - фагоцитирующие клетки презентируют вирусные АГ Т-лимфоцитам и дают начало иммунному ответу на проникновение вируса
 Механизмы приобретённого противовирусного иммунитета Если инфицирующая доза вируса достаточно велика и ему удаётся преодолеть барьеры врождённого неспецифического иммунитета, вирус репродуцируется в месте входных ворот развитие АГспецифического иммунного ответа с формированием специфических эффекторных механизмов: 1. Т-клеточных: цитотоксических CD 8+ и хелперных CD 4+ Т-л 2. Гуморальных: биосинтез противовирусных АТ
Механизмы приобретённого противовирусного иммунитета Если инфицирующая доза вируса достаточно велика и ему удаётся преодолеть барьеры врождённого неспецифического иммунитета, вирус репродуцируется в месте входных ворот развитие АГспецифического иммунного ответа с формированием специфических эффекторных механизмов: 1. Т-клеточных: цитотоксических CD 8+ и хелперных CD 4+ Т-л 2. Гуморальных: биосинтез противовирусных АТ
 Цитотоксические Т-л уничтожают собственные инфицированные вирусом клетки-мишени Вирусинфицированные клетки, приступившие к репликации вируса, - экспрессируют вирусные белки на поверхности ЦПМ в составе молекул ГКГС I класса. Цитотоксические Т-л: специфически распознают вирусинфицированные клетки (АГ + ГКГС I) активируются выделяют гранзимы или цитолизины изменение мембранной проницаемости клетки-мишени: осмотическое набухание, разрыв мембраны и выход содержимого цитоплазмы ДНК-вирусы и ретровирусы интегрируют вирусную НК в геном клеткимишени. Потомство вирусинфицированной клетки наследует провирус. Вирусные антигены (белки) в клетке не синтезируются, они не представлены на ГКГС I. Иммунному надзору такая клетка не поддаётся.
Цитотоксические Т-л уничтожают собственные инфицированные вирусом клетки-мишени Вирусинфицированные клетки, приступившие к репликации вируса, - экспрессируют вирусные белки на поверхности ЦПМ в составе молекул ГКГС I класса. Цитотоксические Т-л: специфически распознают вирусинфицированные клетки (АГ + ГКГС I) активируются выделяют гранзимы или цитолизины изменение мембранной проницаемости клетки-мишени: осмотическое набухание, разрыв мембраны и выход содержимого цитоплазмы ДНК-вирусы и ретровирусы интегрируют вирусную НК в геном клеткимишени. Потомство вирусинфицированной клетки наследует провирус. Вирусные антигены (белки) в клетке не синтезируются, они не представлены на ГКГС I. Иммунному надзору такая клетка не поддаётся.
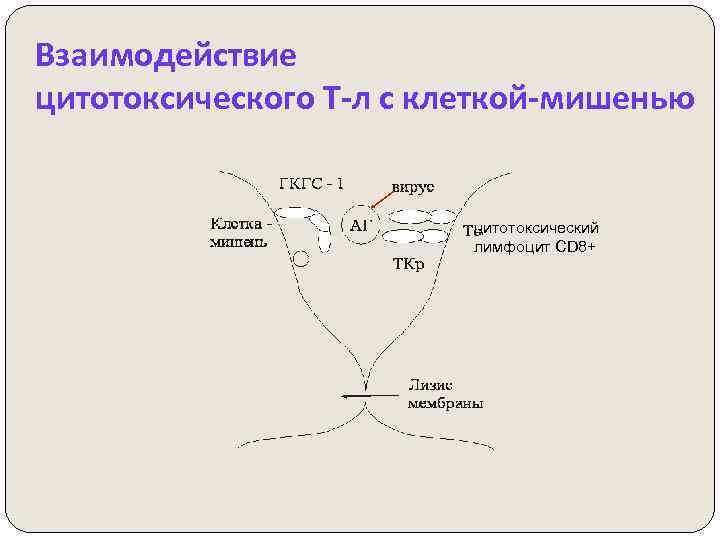 Взаимодействие цитотоксического Т-л с клеткой-мишенью цитотоксический лимфоцит CD 8+
Взаимодействие цитотоксического Т-л с клеткой-мишенью цитотоксический лимфоцит CD 8+
 Противовирусные АТ взаимодействуют с вирионами (внеклеточными вирусными частицами), нейтрализуют инвазивные свойства вирионов, препятствуют их адсорбции на клетках-мишенях, инфицированию клеток-мишеней, генерализации инфекции с вирусными белками и НК, которые попадают в межклеточную среду и секреты после разрушения вирусинфицированных клеток
Противовирусные АТ взаимодействуют с вирионами (внеклеточными вирусными частицами), нейтрализуют инвазивные свойства вирионов, препятствуют их адсорбции на клетках-мишенях, инфицированию клеток-мишеней, генерализации инфекции с вирусными белками и НК, которые попадают в межклеточную среду и секреты после разрушения вирусинфицированных клеток
 Механизмы элиминации вирусных частиц с участием АТ А) иммунный фагоцитоз «маркированных» антителами вирусных частиц. Комплекс вирион+АТ связывается с поверхностью Мф за счёт его Fcрецепторов. Поглощение комплекса гибель вируса. Непоглощённые ИК могут диссоциировать, а освободившиеся вирионы заражают чувствительные клетки. Длительная циркуляция непоглощённых и недиссоциированных ИК по организму депонирование их в тканях и фиксация клетками, имеющими рецептор к Fcфрагменту АТ местные воспалительные реакции ч/з активацию системы комплемента или ИЛ (гепатит В, инфекционный мононуклеоз, ПСПЭ) Б) АТ-опосредованный комплемент-зависимый цитолиз заражённых вирусом клеток-мишеней: лизис мембраны заражённой клетки за счёт МАК комплемента. Освободившиеся вирионы подвергаются воздействию АТ. В) АЗКЦ = АТ-опосредованный цитолиз клеток-мишеней макрофагами и гранулоцитами при выделении ими в момент контакта с поражённой клеткой гранзимов и цитолизинов. Такие Мф и гранулоциты должны иметь Fc-рецепторы.
Механизмы элиминации вирусных частиц с участием АТ А) иммунный фагоцитоз «маркированных» антителами вирусных частиц. Комплекс вирион+АТ связывается с поверхностью Мф за счёт его Fcрецепторов. Поглощение комплекса гибель вируса. Непоглощённые ИК могут диссоциировать, а освободившиеся вирионы заражают чувствительные клетки. Длительная циркуляция непоглощённых и недиссоциированных ИК по организму депонирование их в тканях и фиксация клетками, имеющими рецептор к Fcфрагменту АТ местные воспалительные реакции ч/з активацию системы комплемента или ИЛ (гепатит В, инфекционный мононуклеоз, ПСПЭ) Б) АТ-опосредованный комплемент-зависимый цитолиз заражённых вирусом клеток-мишеней: лизис мембраны заражённой клетки за счёт МАК комплемента. Освободившиеся вирионы подвергаются воздействию АТ. В) АЗКЦ = АТ-опосредованный цитолиз клеток-мишеней макрофагами и гранулоцитами при выделении ими в момент контакта с поражённой клеткой гранзимов и цитолизинов. Такие Мф и гранулоциты должны иметь Fc-рецепторы.
 Участие АТ в противовирусном иммунитете а) Нейтрализация антителами свободных вирионов и иммунный фагоцитоз б) АТ-опосредованный комплементзависимый цитоз клетки-мишени в) АЗКЦ
Участие АТ в противовирусном иммунитете а) Нейтрализация антителами свободных вирионов и иммунный фагоцитоз б) АТ-опосредованный комплементзависимый цитоз клетки-мишени в) АЗКЦ
 Лабораторная диагностика вирусных инфекций
Лабораторная диагностика вирусных инфекций
 ПРИНЦИПЫ ДИАГНОСТИКИ ВИРУСНЫХ ИНФЕКЦИЙ Экспресс-методы – выявление самого вируса, вирусных включений, АГ, специфических нуклетидных последовательностей генома II. Вирусологические методы – выделение вируса в клеточных системах (культура клеток, КЭ, лаб. животные), его индикация и идентификация III. Серологический метод – выявление АТ к вирусу I. Выбор метода зависит от: биологических свойств вируса периода заболевания технической оснащённости лаборатории
ПРИНЦИПЫ ДИАГНОСТИКИ ВИРУСНЫХ ИНФЕКЦИЙ Экспресс-методы – выявление самого вируса, вирусных включений, АГ, специфических нуклетидных последовательностей генома II. Вирусологические методы – выделение вируса в клеточных системах (культура клеток, КЭ, лаб. животные), его индикация и идентификация III. Серологический метод – выявление АТ к вирусу I. Выбор метода зависит от: биологических свойств вируса периода заболевания технической оснащённости лаборатории
 I. ЭКСПРЕСС-МЕТОДЫ 1. Электронная микроскопия - прямое обнаружение и идентификация вируса в клиническом материале: ИЭМ – вируссодержащий материал обрабатывают специфическими АТ, меченными ферритином (железосодержащим белком), что контрастность вируса, реагирующего с ними на электронограмме Метод негативного контрастирования – смешивают суспензию вирусных частиц с раствором соли тяжёлого Ме, наносят тонкий слой полученной суспензии на сетку из вольфрамовой плёнки, высушивают. Соль проникает в различные компоненты вирусной частицы неодинаково контраст выявление тончайших деталей структуры вирусной частицы Метод тонких срезов для изучения структуры вирусов и установления локализации специфических белков в вирусной частице (используют вспомогательные методы: радиоавтографию, обработку тонких срезов мечеными АТ)
I. ЭКСПРЕСС-МЕТОДЫ 1. Электронная микроскопия - прямое обнаружение и идентификация вируса в клиническом материале: ИЭМ – вируссодержащий материал обрабатывают специфическими АТ, меченными ферритином (железосодержащим белком), что контрастность вируса, реагирующего с ними на электронограмме Метод негативного контрастирования – смешивают суспензию вирусных частиц с раствором соли тяжёлого Ме, наносят тонкий слой полученной суспензии на сетку из вольфрамовой плёнки, высушивают. Соль проникает в различные компоненты вирусной частицы неодинаково контраст выявление тончайших деталей структуры вирусной частицы Метод тонких срезов для изучения структуры вирусов и установления локализации специфических белков в вирусной частице (используют вспомогательные методы: радиоавтографию, обработку тонких срезов мечеными АТ)
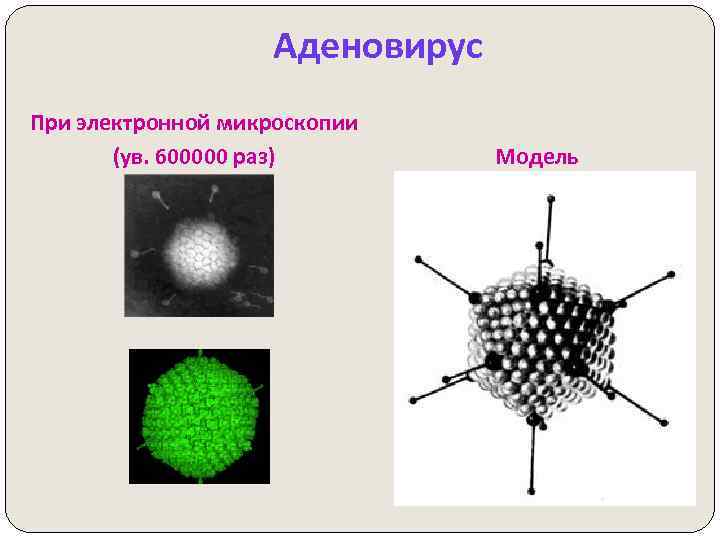 Аденовирус При электронной микроскопии (ув. 600000 раз) Модель
Аденовирус При электронной микроскопии (ув. 600000 раз) Модель
 2. Световая микроскопия - выявление включений в вирусинфицированных клетках КЛЕТКИ, инфицированные вирусами, образующими включения в ЦП: 1 - в. оспы (тельца Гварниери) 5 - реовирусом 6 - в. бешенства (тельца Бабеша-Негри) образующими включения в ядре: 2 - в. герпеса (тельца Каудри) 3 - аденовирусом 4 - паповавирусом SV 40 образующими включения в ЦП и ядре: Включения обозначены чёрным цветом 7 - в. гриппа 8 - в. кори
2. Световая микроскопия - выявление включений в вирусинфицированных клетках КЛЕТКИ, инфицированные вирусами, образующими включения в ЦП: 1 - в. оспы (тельца Гварниери) 5 - реовирусом 6 - в. бешенства (тельца Бабеша-Негри) образующими включения в ядре: 2 - в. герпеса (тельца Каудри) 3 - аденовирусом 4 - паповавирусом SV 40 образующими включения в ЦП и ядре: Включения обозначены чёрным цветом 7 - в. гриппа 8 - в. кори
 Цитоплазматические включения Бабеша-Негри при бешенстве Обнаруживаются у 70% погибших людей в гистологических срезах или мазках-отпечатках слюнных желёз и мозга (кора больших полушарий, мозжечок, аммонов рог, продолговатый и спинной мозг) Ø за 3 -4 дня до появления клиники Ø размер 4 -10 мкм, зернистая структура Ø количество и величина их в течение болезни, в одной клетке может быть несколько включений Недостатки метода: Ø постмортальный Ø некоторые биовары вируса не образуют включений Ø при коротком инкубационном периоде (2 -3 нед) телец мало или нет
Цитоплазматические включения Бабеша-Негри при бешенстве Обнаруживаются у 70% погибших людей в гистологических срезах или мазках-отпечатках слюнных желёз и мозга (кора больших полушарий, мозжечок, аммонов рог, продолговатый и спинной мозг) Ø за 3 -4 дня до появления клиники Ø размер 4 -10 мкм, зернистая структура Ø количество и величина их в течение болезни, в одной клетке может быть несколько включений Недостатки метода: Ø постмортальный Ø некоторые биовары вируса не образуют включений Ø при коротком инкубационном периоде (2 -3 нед) телец мало или нет
 3. Серологический метод для выявления вирусных АГ в клиническом материале (мазки-отпечатки, биоптаты, эпителий осадка, лейкоциты, гистологические срезы, секционный материал) с помощью диагностических противовирусных сывороток (РИФ, ИФА, РИА, ВИЭФ, РОПГА, РТГА) (ОРВИ, ротавирусная инфекция) 4. Молекулярно-генетические методы – выявление специфических нуклеотидных последовательностей вируса без выделения вируса МГ – гибридизация комплементарных нитей НК вируса и зонда. Зонд мечен радиоактивным изотопом или ферментом. Выявление степени гибридизации по радиоактивности или колориметрически. ПЦР обнаруживает нуклеотидные последовательности вируса, присутствующие в ничтожно малом количестве в исследуемом материале. Для этого амплифицируют специфический для данного вируса ген. Детекция – аналогично МГ. Основной метод подтверждения диагнозов герпетического менингоэнцефалита ВИЧ, ВГ Установление вирусной нагрузки для определения тяжести ВИЧ-инфекции и прогноза заболевания
3. Серологический метод для выявления вирусных АГ в клиническом материале (мазки-отпечатки, биоптаты, эпителий осадка, лейкоциты, гистологические срезы, секционный материал) с помощью диагностических противовирусных сывороток (РИФ, ИФА, РИА, ВИЭФ, РОПГА, РТГА) (ОРВИ, ротавирусная инфекция) 4. Молекулярно-генетические методы – выявление специфических нуклеотидных последовательностей вируса без выделения вируса МГ – гибридизация комплементарных нитей НК вируса и зонда. Зонд мечен радиоактивным изотопом или ферментом. Выявление степени гибридизации по радиоактивности или колориметрически. ПЦР обнаруживает нуклеотидные последовательности вируса, присутствующие в ничтожно малом количестве в исследуемом материале. Для этого амплифицируют специфический для данного вируса ген. Детекция – аналогично МГ. Основной метод подтверждения диагнозов герпетического менингоэнцефалита ВИЧ, ВГ Установление вирусной нагрузки для определения тяжести ВИЧ-инфекции и прогноза заболевания
 II. ВИРУСОЛОГИЧЕСКИЙ МЕТОД - выделение вируса из клинического материала путём культивирования на чувствительных клеточных системах (культура клеток, КЭ, лабораторные животные) Этапы метода: 1. Забор исследуемого материала. 2. Выбор и получение чувствительной тест-системы, определение её жизнеспособности. 3. Заражение её по принципу цитотропизма. 4. Индикация вируса – выявление наличия вируса. 5. Идентификация вируса – определение типа вируса. Достоинства: - ранний метод - высокая чувствительность Недостатки: - трудоёмкий, длительный, дорогой, не везде доступный - не все вирусы культивируются - сложность интерпретации результатов при выделении персистирующих вирусов
II. ВИРУСОЛОГИЧЕСКИЙ МЕТОД - выделение вируса из клинического материала путём культивирования на чувствительных клеточных системах (культура клеток, КЭ, лабораторные животные) Этапы метода: 1. Забор исследуемого материала. 2. Выбор и получение чувствительной тест-системы, определение её жизнеспособности. 3. Заражение её по принципу цитотропизма. 4. Индикация вируса – выявление наличия вируса. 5. Идентификация вируса – определение типа вируса. Достоинства: - ранний метод - высокая чувствительность Недостатки: - трудоёмкий, длительный, дорогой, не везде доступный - не все вирусы культивируются - сложность интерпретации результатов при выделении персистирующих вирусов
 А. Культивирование вирусов в культурах клеток Культуры клеток 1. По технике приготовления: - однослойные – прикрепляются и размножаются на поверхности химически нейтрального стекла лабораторной посуды в виде монослоя - суспензионные – размножаются во всём объёме питательной среды при постоянном её перемешивании - органные – цельные кусочки органов и тканей, сохраняющие исходную структуру вне организма (применяются ограничено) 2. По происхождению: - эмбриональные - опухолевые - из взрослых организмов
А. Культивирование вирусов в культурах клеток Культуры клеток 1. По технике приготовления: - однослойные – прикрепляются и размножаются на поверхности химически нейтрального стекла лабораторной посуды в виде монослоя - суспензионные – размножаются во всём объёме питательной среды при постоянном её перемешивании - органные – цельные кусочки органов и тканей, сохраняющие исходную структуру вне организма (применяются ограничено) 2. По происхождению: - эмбриональные - опухолевые - из взрослых организмов
 3. По морфогенезу: - фибробластные - эпителиальные 4. По числу жизнеспособных генераций: - первичные (первично трипсинизированные) - перевиваемые (стабильные) линии - полуперевиваемые штаммы - трансфецированные
3. По морфогенезу: - фибробластные - эпителиальные 4. По числу жизнеспособных генераций: - первичные (первично трипсинизированные) - перевиваемые (стабильные) линии - полуперевиваемые штаммы - трансфецированные
 Первичные (первично трипсинизированные) Получены в эмбриональном или постнатальном периоде из тканей человека (из почек эмбриона человека, амниона человека) или животных (из почек обезьян, куриных эмбрионов) Однослойные Размножаются только на первых генерациях (несколько пассажей после выделения из тканей), к длительному размножению неспособны Ч/з определённое время в них возникают явления неспецифической дегенерации (грануляция и вакуолизация ЦП, округление клеток, утрата связи между клетками и твёрдой поверхностью, на которой они выращивались) гибель Используют: - для выделения и накопления вирусов - производства противовирусных вакцин - источник перевиваемых и полуперевиваемых клеток: отдельные клетки первичных культур сохраняют способность к росту и размножению, при многократных перевивках дают начало перевиваемым линиям и полуперевиваемым штаммам клеток
Первичные (первично трипсинизированные) Получены в эмбриональном или постнатальном периоде из тканей человека (из почек эмбриона человека, амниона человека) или животных (из почек обезьян, куриных эмбрионов) Однослойные Размножаются только на первых генерациях (несколько пассажей после выделения из тканей), к длительному размножению неспособны Ч/з определённое время в них возникают явления неспецифической дегенерации (грануляция и вакуолизация ЦП, округление клеток, утрата связи между клетками и твёрдой поверхностью, на которой они выращивались) гибель Используют: - для выделения и накопления вирусов - производства противовирусных вакцин - источник перевиваемых и полуперевиваемых клеток: отдельные клетки первичных культур сохраняют способность к росту и размножению, при многократных перевивках дают начало перевиваемым линиям и полуперевиваемым штаммам клеток
 Перевиваемые (стабильные) линии Гетероплоидный кариотип Бессмертны: размножаются в лабораторных условиях неопределённо долго при постоянном пассировании Относительно автономны Изменения, приводящие к появлению в клетках таких свойств – трансформация. Клетки перевиваемых тканевых культур – трансформированные. Источники перевиваемых линий клеток: А) злокачественные новообразования – трансформация клеток происходит in vivo: - He. La из карциномы шейки матки - Hep-2 из карциномы гортани - Hep-3 из лимфоидной карциномы - Детройт-6 из метастаза рака легкого в костный мозг - RH из опухоли почки человека Б) первичные клеточные культуры, отдельные клетки которых обнаруживают тенденцию к бесконечному размножению in vitro в определённых условиях: - СОЦ из сердца обезьяны циномольгус - ПЭС из почек эмбриона свиньи - ВНК-21 из почек однодневных сирийских хомяков - ПМС из почки морской свинки
Перевиваемые (стабильные) линии Гетероплоидный кариотип Бессмертны: размножаются в лабораторных условиях неопределённо долго при постоянном пассировании Относительно автономны Изменения, приводящие к появлению в клетках таких свойств – трансформация. Клетки перевиваемых тканевых культур – трансформированные. Источники перевиваемых линий клеток: А) злокачественные новообразования – трансформация клеток происходит in vivo: - He. La из карциномы шейки матки - Hep-2 из карциномы гортани - Hep-3 из лимфоидной карциномы - Детройт-6 из метастаза рака легкого в костный мозг - RH из опухоли почки человека Б) первичные клеточные культуры, отдельные клетки которых обнаруживают тенденцию к бесконечному размножению in vitro в определённых условиях: - СОЦ из сердца обезьяны циномольгус - ПЭС из почек эмбриона свиньи - ВНК-21 из почек однодневных сирийских хомяков - ПМС из почки морской свинки
 Полуперевиваемые штаммы: - диплоидный набор хромосом - ограниченная продолжительность жизни in vitro: 40 -100 пассажей (до года) - не претерпевают злокачественного перерождения - используются для диагностики вирусных инфекций и производстве вирусных вакцин Трансфецированные: - получены методом трансфекции (переноса) генов вирусов, контролирующих биосинтез поверхностных АГ - на мембране экспрессируют поверхностный белок определённого вируса (HBs-АГ, gp 120) - используются для изучения механизмов патогенеза вирусных инфекций, разработки химиотерапевтических препаратов
Полуперевиваемые штаммы: - диплоидный набор хромосом - ограниченная продолжительность жизни in vitro: 40 -100 пассажей (до года) - не претерпевают злокачественного перерождения - используются для диагностики вирусных инфекций и производстве вирусных вакцин Трансфецированные: - получены методом трансфекции (переноса) генов вирусов, контролирующих биосинтез поверхностных АГ - на мембране экспрессируют поверхностный белок определённого вируса (HBs-АГ, gp 120) - используются для изучения механизмов патогенеза вирусных инфекций, разработки химиотерапевтических препаратов
 Использование культур клеток 1. Изучение особенностей взаимодействия «вирус-клетка» 2. Диагностика – золотой стандарт вирусологии 3. Производство препаратов для профилактики вирусных инфекций Выбор клеточных культур определяется их чувствительностью к отдельным группам вирусов
Использование культур клеток 1. Изучение особенностей взаимодействия «вирус-клетка» 2. Диагностика – золотой стандарт вирусологии 3. Производство препаратов для профилактики вирусных инфекций Выбор клеточных культур определяется их чувствительностью к отдельным группам вирусов
 Феномены, указывающие на наличие вируса в культуре клеток 1. Специфическая дегенерация клеток цитопатическое действие вируса (ЦПД) - видимые под световым микроскопом морфологические изменения клеток, которые возникают в результате внутриклеточной репродукции вирусов. Типы ЦПД: кругло- или мелкоклеточная дегенерация (в. гриппа, энтеровирусы, реовирусы аденовирусы) образование многоядерных гигантских клеток (симпластов, синцития) (парамиксовирусы, герпесвирусы) развитие очагов клеточной пролиферации из нескольких слоёв клеток (опухольиндуцирующие в. )
Феномены, указывающие на наличие вируса в культуре клеток 1. Специфическая дегенерация клеток цитопатическое действие вируса (ЦПД) - видимые под световым микроскопом морфологические изменения клеток, которые возникают в результате внутриклеточной репродукции вирусов. Типы ЦПД: кругло- или мелкоклеточная дегенерация (в. гриппа, энтеровирусы, реовирусы аденовирусы) образование многоядерных гигантских клеток (симпластов, синцития) (парамиксовирусы, герпесвирусы) развитие очагов клеточной пролиферации из нескольких слоёв клеток (опухольиндуцирующие в. )
 Индикация репродукции вируса в культуре ткани по цитопатическому действию (ЦПД) Интактная монослойная культура клеток Зараженная культура (ЦПД, дегенерация)
Индикация репродукции вируса в культуре ткани по цитопатическому действию (ЦПД) Интактная монослойная культура клеток Зараженная культура (ЦПД, дегенерация)
 2. Внутриклеточные включения в ЦП и/или в ядрах поражённых клеток скопление вирусных частиц или отдельных компонентов вирусов, выявляемые под микроскопом при специальном окрашивании. Включения различаются по величине, форме, численности. 3. +РГА 4. +РГАдс способность культур клеток, инфицированных вирусами, адсорбировать на своей поверхности эритроциты определённых видов животных и птиц. Гемадсорбция проявляется скоплением в виде гроздей эритроцитов, адсорбированных на инфицированных вирусом клетках. 5. Цветная проба. Если вирусы не размножаются в культуре клеток, то живые клетки в процессе метаболизма выделяют кислые продукты изменение р. Н среды и цвета индикатора фенолового красного на жёлтый. При продукции вирусов нормальный метаболизм клеток нарушается, клетки гибнут, и среда сохраняет свой первоначальный (красный) цвет. Красный цвет среды указывает на наличие вируса и прекращение жизнедеятельности клеток.
2. Внутриклеточные включения в ЦП и/или в ядрах поражённых клеток скопление вирусных частиц или отдельных компонентов вирусов, выявляемые под микроскопом при специальном окрашивании. Включения различаются по величине, форме, численности. 3. +РГА 4. +РГАдс способность культур клеток, инфицированных вирусами, адсорбировать на своей поверхности эритроциты определённых видов животных и птиц. Гемадсорбция проявляется скоплением в виде гроздей эритроцитов, адсорбированных на инфицированных вирусом клетках. 5. Цветная проба. Если вирусы не размножаются в культуре клеток, то живые клетки в процессе метаболизма выделяют кислые продукты изменение р. Н среды и цвета индикатора фенолового красного на жёлтый. При продукции вирусов нормальный метаболизм клеток нарушается, клетки гибнут, и среда сохраняет свой первоначальный (красный) цвет. Красный цвет среды указывает на наличие вируса и прекращение жизнедеятельности клеток.
 6. Бляшки (негативные колонии). Монослой заражённых вирусом клеток покрывают тонким слоем агара с добавлением индикатора нейтрального красного (фон розовый). При наличии вируса в клетках образуются бесцветные зоны ( «бляшки» ) на розовом фоне агара. Одна бляшка соответствует потомству одного вириона. Негативные колонии разных вирусов отличаются по размеру, форме. Бляшкообразование используют для дифференциации, селекции вирусов, определения их концентрации в исследуемом материале. Титр вируса выражают числом бляшкообразующих единиц (БОЕ) в 1 мл. 7. При отсутствии ЦПД, ГА или Гадс используют реакцию интерференции: исследуемую культуру повторно заражают вирусом, вызывающим ЦПД. В положительном случае ЦПД будет отсутствовать (реакция интерференции положительная). Если в исследуемом материале вируса не было, наблюдается ЦПД. ИДЕНТИФИКАЦИЯ ВИРУСА в серологических реакциях (РН, РТГАдс, РСК, РИФ)
6. Бляшки (негативные колонии). Монослой заражённых вирусом клеток покрывают тонким слоем агара с добавлением индикатора нейтрального красного (фон розовый). При наличии вируса в клетках образуются бесцветные зоны ( «бляшки» ) на розовом фоне агара. Одна бляшка соответствует потомству одного вириона. Негативные колонии разных вирусов отличаются по размеру, форме. Бляшкообразование используют для дифференциации, селекции вирусов, определения их концентрации в исследуемом материале. Титр вируса выражают числом бляшкообразующих единиц (БОЕ) в 1 мл. 7. При отсутствии ЦПД, ГА или Гадс используют реакцию интерференции: исследуемую культуру повторно заражают вирусом, вызывающим ЦПД. В положительном случае ЦПД будет отсутствовать (реакция интерференции положительная). Если в исследуемом материале вируса не было, наблюдается ЦПД. ИДЕНТИФИКАЦИЯ ВИРУСА в серологических реакциях (РН, РТГАдс, РСК, РИФ)
 Б. Культивирование вирусов в курином эмбрионе (КЭ) Большинство вирусов способны размножаться в КЭ Методику широко используют при промышленном культивировании и получении вакцин Используют жизнеспособные КЭ в возрасте 8 -14 дней (в зависимости от вида вируса, способа заражения и задач исследования, в. гриппа культивируются в 9 -10, паротита - в 7 -дневных КЭ) Размножение вирусов в КЭ происходит в разных частях зародыша в зависимости от тропизма культивируемого вируса методы заражения КЭ: - на хорионаллантоисную оболочку (в. простого герпеса) - в аллантоисную полость (в. гриппа) - в в желточный мешок - в амниотическую полость - в тело эмбриона
Б. Культивирование вирусов в курином эмбрионе (КЭ) Большинство вирусов способны размножаться в КЭ Методику широко используют при промышленном культивировании и получении вакцин Используют жизнеспособные КЭ в возрасте 8 -14 дней (в зависимости от вида вируса, способа заражения и задач исследования, в. гриппа культивируются в 9 -10, паротита - в 7 -дневных КЭ) Размножение вирусов в КЭ происходит в разных частях зародыша в зависимости от тропизма культивируемого вируса методы заражения КЭ: - на хорионаллантоисную оболочку (в. простого герпеса) - в аллантоисную полость (в. гриппа) - в в желточный мешок - в амниотическую полость - в тело эмбриона
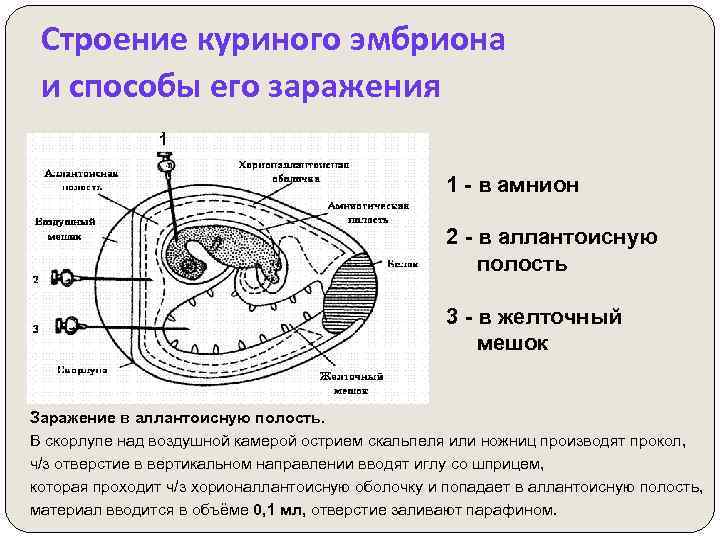 Строение куриного эмбриона и способы его заражения 1 1 - в амнион 2 - в аллантоисную полость 3 - в желточный мешок Заражение в аллантоисную полость. В скорлупе над воздушной камерой острием скальпеля или ножниц производят прокол, ч/з отверстие в вертикальном направлении вводят иглу со шприцем, которая проходит ч/з хорионаллантоисную оболочку и попадает в аллантоисную полость, материал вводится в объёме 0, 1 мл, отверстие заливают парафином.
Строение куриного эмбриона и способы его заражения 1 1 - в амнион 2 - в аллантоисную полость 3 - в желточный мешок Заражение в аллантоисную полость. В скорлупе над воздушной камерой острием скальпеля или ножниц производят прокол, ч/з отверстие в вертикальном направлении вводят иглу со шприцем, которая проходит ч/з хорионаллантоисную оболочку и попадает в аллантоисную полость, материал вводится в объёме 0, 1 мл, отверстие заливают парафином.
 Культивирование вирусов в курином эмбрионе (КЭ) Индикация вируса: гибель эмбриона морфологические изменения эмбриона или его оболочек +РГА с аллантоисной или амниотической жидкостью Идентификация вируса: РТГА, РСК, РН
Культивирование вирусов в курином эмбрионе (КЭ) Индикация вируса: гибель эмбриона морфологические изменения эмбриона или его оболочек +РГА с аллантоисной или амниотической жидкостью Идентификация вируса: РТГА, РСК, РН
 В. Культивирование вирусов в организме лабораторных животных Ограничено: когда невозможно использовать более удобные системы Преимущественно новорожденные (белые мыши и крысята, кролики, морские свинки, хомячки, обезьяны) Вид животного зависит от видовой чувствительности к вирусу Заражение животных по принципу цитотропизма вируса: - нейротропные (в. бешенства, КЭ) – интрацеребрально - респираторные (в. гриппа) – интраназально - дерматотропные (в. герпеса) – на кожу Индикация вируса: - заболевание животного - гибель животного. При первичном заражении животное может не заболеть, поэтому ч/з 5 -7 дней внешне здоровых животных убивают, из их органов готовят суспензию, которой заражают следующее животное ( «пассажи» ). - патоморфологические и патогистологические изменения в тканях и органах - + РГА с экстрактами из органов Идентификация вируса: РН
В. Культивирование вирусов в организме лабораторных животных Ограничено: когда невозможно использовать более удобные системы Преимущественно новорожденные (белые мыши и крысята, кролики, морские свинки, хомячки, обезьяны) Вид животного зависит от видовой чувствительности к вирусу Заражение животных по принципу цитотропизма вируса: - нейротропные (в. бешенства, КЭ) – интрацеребрально - респираторные (в. гриппа) – интраназально - дерматотропные (в. герпеса) – на кожу Индикация вируса: - заболевание животного - гибель животного. При первичном заражении животное может не заболеть, поэтому ч/з 5 -7 дней внешне здоровых животных убивают, из их органов готовят суспензию, которой заражают следующее животное ( «пассажи» ). - патоморфологические и патогистологические изменения в тканях и органах - + РГА с экстрактами из органов Идентификация вируса: РН
 III. СЕРОЛОГИЧЕСКИЙ МЕТОД – ОБНАРУЖЕНИЕ АТ К ВИРУСУ 1. Определение класса специфических противовирусных АТ для определения давности инфицирования (вирусные гепатиты, краснуха) методом ИФА Интерпретация результатов: Ig. M – свежий случай заболевания Ig. G – анамнестическая реакция
III. СЕРОЛОГИЧЕСКИЙ МЕТОД – ОБНАРУЖЕНИЕ АТ К ВИРУСУ 1. Определение класса специфических противовирусных АТ для определения давности инфицирования (вирусные гепатиты, краснуха) методом ИФА Интерпретация результатов: Ig. M – свежий случай заболевания Ig. G – анамнестическая реакция
 2. Определение динамики Т противовирусных АТ в парных сыворотках больного или переболевшего человека с помощью набора вирусных диагностикумов Парные сыворотки - две сыворотки, взятые от одного больного в начале заболевания и ч/з 1 -4 нед. Серологические реакции (РПГА, РСК, РТГА, РН, ИФА) ставят одновременно с двумя сыворотками для определения АТ и сравнения их титров. Интерпретация результатов: свежий случай заболевания, если наблюдается: 4 -кратный прирост Т АТ или 2 -кратный прирост Т АТ при наличии дополнительных клинич. или эпидемиологич. данных
2. Определение динамики Т противовирусных АТ в парных сыворотках больного или переболевшего человека с помощью набора вирусных диагностикумов Парные сыворотки - две сыворотки, взятые от одного больного в начале заболевания и ч/з 1 -4 нед. Серологические реакции (РПГА, РСК, РТГА, РН, ИФА) ставят одновременно с двумя сыворотками для определения АТ и сравнения их титров. Интерпретация результатов: свежий случай заболевания, если наблюдается: 4 -кратный прирост Т АТ или 2 -кратный прирост Т АТ при наличии дополнительных клинич. или эпидемиологич. данных
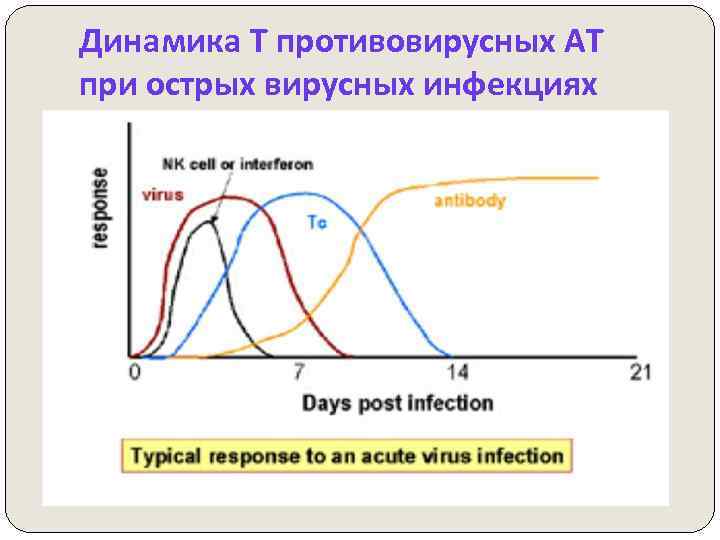 Динамика Т противовирусных АТ при острых вирусных инфекциях
Динамика Т противовирусных АТ при острых вирусных инфекциях
 3. Выявление АТ при некоторых вирусных инфекциях указывает на заболевание – ВИЧ ИФА-тест-системы III поколения АТ к ВИЧ в период о. фазы не обнаруживают 90 -95% пациентов – АТ в первые 3 мес после заражения 5 -9 % пациентов – АТ ч/з 6 мес требуемый период карантинизации донорской плазмы, повторные доноры!!! 0, 5 -1% – АТ позже
3. Выявление АТ при некоторых вирусных инфекциях указывает на заболевание – ВИЧ ИФА-тест-системы III поколения АТ к ВИЧ в период о. фазы не обнаруживают 90 -95% пациентов – АТ в первые 3 мес после заражения 5 -9 % пациентов – АТ ч/з 6 мес требуемый период карантинизации донорской плазмы, повторные доноры!!! 0, 5 -1% – АТ позже
 Серодиагностика ВИЧ - ИФА-тест-системы IV поколения: ВИЧ 1 АГ p 24 + АТ к ВИЧ 1 + АТ к ВИЧ 2 + рез-т ч/з 2 нед после инфицирования Проблемы: 1. ! очень низкий титр АГ или АТ не выявляется на 1 -ом этапе инфекции «-» рез-т: указывает, что тестированный образец не содержит ВИЧ АГ или АТ, определяемых с помощью данной тест-системы (по сути это ЛОР) - не может исключать развития ВИЧ инфекции в дальнейшем - 2. Некоторые варианты ВИЧ 1 имеют только 70% гомологичных участков генома ЛОР 3. Гомология ВИЧ 1 и ВИЧ 2 <40% ЛОР 4. Высокое содержание в сыворотке липидов, гемоглобина ЛПР подготовка обследуемого для серологического обследования
Серодиагностика ВИЧ - ИФА-тест-системы IV поколения: ВИЧ 1 АГ p 24 + АТ к ВИЧ 1 + АТ к ВИЧ 2 + рез-т ч/з 2 нед после инфицирования Проблемы: 1. ! очень низкий титр АГ или АТ не выявляется на 1 -ом этапе инфекции «-» рез-т: указывает, что тестированный образец не содержит ВИЧ АГ или АТ, определяемых с помощью данной тест-системы (по сути это ЛОР) - не может исключать развития ВИЧ инфекции в дальнейшем - 2. Некоторые варианты ВИЧ 1 имеют только 70% гомологичных участков генома ЛОР 3. Гомология ВИЧ 1 и ВИЧ 2 <40% ЛОР 4. Высокое содержание в сыворотке липидов, гемоглобина ЛПР подготовка обследуемого для серологического обследования
 Серодиагностика ВИЧ - постановка диагноза: 1. Повторно ИФА-тест-системы IV поколения 2. Или конфирматорный (подтверждающий) ИФА тест на АГ ВИЧ с последующей реакцией нейтрализации 3. Иммуноблотинг – определение АТ к различным АГ ВИЧ 1 и ВИЧ 2 диагноз 4. ПЦР диагноз Детям, родившимся от ВИЧ-инфицированных матерей, при наличии АТ устанавливается диагноз «ВИЧ-экспонированный» (18 мес) периодический серологический контроль в ИФА окончательное подтверждение или снятие диагноза (редко) ч/з 18 мес, быстрее - ПЦР
Серодиагностика ВИЧ - постановка диагноза: 1. Повторно ИФА-тест-системы IV поколения 2. Или конфирматорный (подтверждающий) ИФА тест на АГ ВИЧ с последующей реакцией нейтрализации 3. Иммуноблотинг – определение АТ к различным АГ ВИЧ 1 и ВИЧ 2 диагноз 4. ПЦР диагноз Детям, родившимся от ВИЧ-инфицированных матерей, при наличии АТ устанавливается диагноз «ВИЧ-экспонированный» (18 мес) периодический серологический контроль в ИФА окончательное подтверждение или снятие диагноза (редко) ч/з 18 мес, быстрее - ПЦР
 Профилактика вирусных инфекций
Профилактика вирусных инфекций
 Принципы профилактики вирусных инфекций 1. Неспецифическая 2. Специфическая активная 3. Специфическая пассивная 4. Химиопрофилактика 5. Интерферонопрофилактика
Принципы профилактики вирусных инфекций 1. Неспецифическая 2. Специфическая активная 3. Специфическая пассивная 4. Химиопрофилактика 5. Интерферонопрофилактика
 Неспецифическая профилактика вирусных инфекций Оптимальная, не всегда реальная, точки приложения: - источник инфекции - механизм передачи - восприимчивый организм Единственный вид профилактики инфекций, в отношении которых специфическая и химиопрофилактика отсутствуют
Неспецифическая профилактика вирусных инфекций Оптимальная, не всегда реальная, точки приложения: - источник инфекции - механизм передачи - восприимчивый организм Единственный вид профилактики инфекций, в отношении которых специфическая и химиопрофилактика отсутствуют
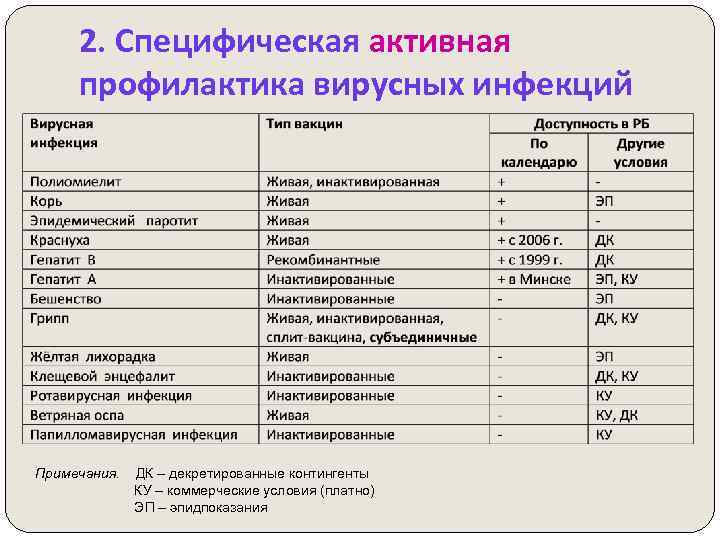 2. Специфическая активная профилактика вирусных инфекций Примечания. ДК – декретированные контингенты КУ – коммерческие условия (платно) ЭП – эпидпоказания
2. Специфическая активная профилактика вирусных инфекций Примечания. ДК – декретированные контингенты КУ – коммерческие условия (платно) ЭП – эпидпоказания
 3. Специфическая пассивная профилактика вирусных инфекций 1. Нормальный иммуноглобулин контактным лицам для профилактики кори, гриппа, ВГА, полиомиелита, эпидпаротита 2. Антирабический иммуноглобулин – для профилактики бешенства (безусловный курс) при высокой угрозе развития заболевания 3. Ig против клещевого энцефалита: - укушенным клещом, инфицированным в. КЭ срочно выезжающим на неблагополучные по КЭ территории (Сибирь, Дальний Восток, Карпаты)
3. Специфическая пассивная профилактика вирусных инфекций 1. Нормальный иммуноглобулин контактным лицам для профилактики кори, гриппа, ВГА, полиомиелита, эпидпаротита 2. Антирабический иммуноглобулин – для профилактики бешенства (безусловный курс) при высокой угрозе развития заболевания 3. Ig против клещевого энцефалита: - укушенным клещом, инфицированным в. КЭ срочно выезжающим на неблагополучные по КЭ территории (Сибирь, Дальний Восток, Карпаты)
 4. Химиопрофилактика (ХП) вирусных инфекций Крайне ограничена, используют: - озетальмивир (тамифлю) – профилактика гриппа А и В у детей > 1 года и взрослых из группах риска инфицирования (в/части, большие коллективы, ослабленные больные). Профилактическое действие продолжается сколько длится приём. >12 лет – по 75 мг (1 капсуле) 1 раз/сут: - во время сезонной эпидемии – в течение 6 нед - после контакта с инфицированным – не < 10 дней; начинать не позже 2 дней после контакта < 40 кг – рекомендованную дозу (суспензия) - амантадин (ремантадин) - профилактика гриппа А - интерфероногены (индукторы INF)
4. Химиопрофилактика (ХП) вирусных инфекций Крайне ограничена, используют: - озетальмивир (тамифлю) – профилактика гриппа А и В у детей > 1 года и взрослых из группах риска инфицирования (в/части, большие коллективы, ослабленные больные). Профилактическое действие продолжается сколько длится приём. >12 лет – по 75 мг (1 капсуле) 1 раз/сут: - во время сезонной эпидемии – в течение 6 нед - после контакта с инфицированным – не < 10 дней; начинать не позже 2 дней после контакта < 40 кг – рекомендованную дозу (суспензия) - амантадин (ремантадин) - профилактика гриппа А - интерфероногены (индукторы INF)
 5. Интерферонопрофилактика вирусных инфекций Гены INF найдены в клетках всех позвоночных, но в нормальных условиях молчат и начинают работать лишь в ответ на сигналы тревоги. В природе роль таких сигналов чаще всего играют вирусы. Образование INF - первая реакция организма на их внедрение. Применение INF атуально: - когда вакцинация неприменима (вспышка уже началась или человек уже инфицировался, но до температуры) - при вирусных инфекциях, против которых вакцины ещё не созданы (цитомегалия) или практически не могут быть созданы (ОРВИ, вызываемые , чем 150 вирусами)
5. Интерферонопрофилактика вирусных инфекций Гены INF найдены в клетках всех позвоночных, но в нормальных условиях молчат и начинают работать лишь в ответ на сигналы тревоги. В природе роль таких сигналов чаще всего играют вирусы. Образование INF - первая реакция организма на их внедрение. Применение INF атуально: - когда вакцинация неприменима (вспышка уже началась или человек уже инфицировался, но до температуры) - при вирусных инфекциях, против которых вакцины ещё не созданы (цитомегалия) или практически не могут быть созданы (ОРВИ, вызываемые , чем 150 вирусами)
 Терапия вирусных инфекций
Терапия вирусных инфекций
 Группы препаратов для лечения вирусных инфекций 1. Этиотропные – против в. гриппа, ВГ, ВИЧ, герпесвирусов, ДНК-вирусов 2. Патогенетические – детоксикация, регидратация, ингибирование протеолитической активации (трасилол, контрикал, ε-аминокапроновая кислота), профилактика бактериальных вторичных инфекций (антибиотики), борьба с сосудистыми и органными поражениями, аллергическими реакциями. 3. Симптоматические – купирующие сопутствующую симптоматику (головную боль, кашель и др. ) Препараты 2 -3 групп используются при всех вирусных инфекциях
Группы препаратов для лечения вирусных инфекций 1. Этиотропные – против в. гриппа, ВГ, ВИЧ, герпесвирусов, ДНК-вирусов 2. Патогенетические – детоксикация, регидратация, ингибирование протеолитической активации (трасилол, контрикал, ε-аминокапроновая кислота), профилактика бактериальных вторичных инфекций (антибиотики), борьба с сосудистыми и органными поражениями, аллергическими реакциями. 3. Симптоматические – купирующие сопутствующую симптоматику (головную боль, кашель и др. ) Препараты 2 -3 групп используются при всех вирусных инфекциях
 Принципы действия противовирусных препаратов 1. На отдельные стадии репродукции вируса 2. На вирусинфицированную клетку, которая в генетическом и функциональном отношении отличается от здоровых клеток: А) с помощью мк. АТ (в перспективе) Б) в результате проницаемости вирусинфицированной клетки к ряду соединений В) использование пролекарств (протоксинов), которые в вирусинфицированных клетках превращаются в токсины под действием вирусспецифических ферментов
Принципы действия противовирусных препаратов 1. На отдельные стадии репродукции вируса 2. На вирусинфицированную клетку, которая в генетическом и функциональном отношении отличается от здоровых клеток: А) с помощью мк. АТ (в перспективе) Б) в результате проницаемости вирусинфицированной клетки к ряду соединений В) использование пролекарств (протоксинов), которые в вирусинфицированных клетках превращаются в токсины под действием вирусспецифических ферментов
 1. Группы противовирусных препаратов 1. Интерфероны: Эндогенного происхождения из лейкоцитов крови доноров – местно Рекомбинантные, получаемые геннонженерным путём – хорошо очищены, в/м, п/к или per rectum Производные INF и их аналоги - пэгинтерфероны (α 2 a, α 2 b) – присоединение полиэтиленгликоля к молекуле INF > период полувыведения, клиническая эффективность
1. Группы противовирусных препаратов 1. Интерфероны: Эндогенного происхождения из лейкоцитов крови доноров – местно Рекомбинантные, получаемые геннонженерным путём – хорошо очищены, в/м, п/к или per rectum Производные INF и их аналоги - пэгинтерфероны (α 2 a, α 2 b) – присоединение полиэтиленгликоля к молекуле INF > период полувыведения, клиническая эффективность
 Интерфероны (INF) цитокины (гликопротеины с Ммассой 17 -80 к. Д), вырабатываемые ИС под влиянием индукторов: - МИО (вирусов, бактерий, простейших) - НК - синтетических соединений Наиболее эффективные индукторы INF – двунитчатые РНК или синтетические аналоги 3 класса INF: α – лейкоцитарный max противовирусная активность β – фибробластный противовирусная активность γ – иммунный, продуцируют Т-л, ЕКК, активированные Мф иммуномоделирующее и противоопухолевое действие
Интерфероны (INF) цитокины (гликопротеины с Ммассой 17 -80 к. Д), вырабатываемые ИС под влиянием индукторов: - МИО (вирусов, бактерий, простейших) - НК - синтетических соединений Наиболее эффективные индукторы INF – двунитчатые РНК или синтетические аналоги 3 класса INF: α – лейкоцитарный max противовирусная активность β – фибробластный противовирусная активность γ – иммунный, продуцируют Т-л, ЕКК, активированные Мф иммуномоделирующее и противоопухолевое действие
 Противовирусная активность - INF α/β Видоспецифичность Действие универсально: вирусспецифичность отсутствует Наибольшая противовирусная активность у αINF – 20 субтипов, из них 70% – α 2 -INF (2 a, 2 b, 2 c) INF: - не взаимодействуют непосредственно с вирусами - не препятствуют адсорбции вирусов на клетках Противовирусный эффект INF: - подавление внутриклеточной репродукции вирусов - индукция резистентности клетки к последующему инфицированию вирусами - чувствительность разных вирусов к INF неодинакова
Противовирусная активность - INF α/β Видоспецифичность Действие универсально: вирусспецифичность отсутствует Наибольшая противовирусная активность у αINF – 20 субтипов, из них 70% – α 2 -INF (2 a, 2 b, 2 c) INF: - не взаимодействуют непосредственно с вирусами - не препятствуют адсорбции вирусов на клетках Противовирусный эффект INF: - подавление внутриклеточной репродукции вирусов - индукция резистентности клетки к последующему инфицированию вирусами - чувствительность разных вирусов к INF неодинакова
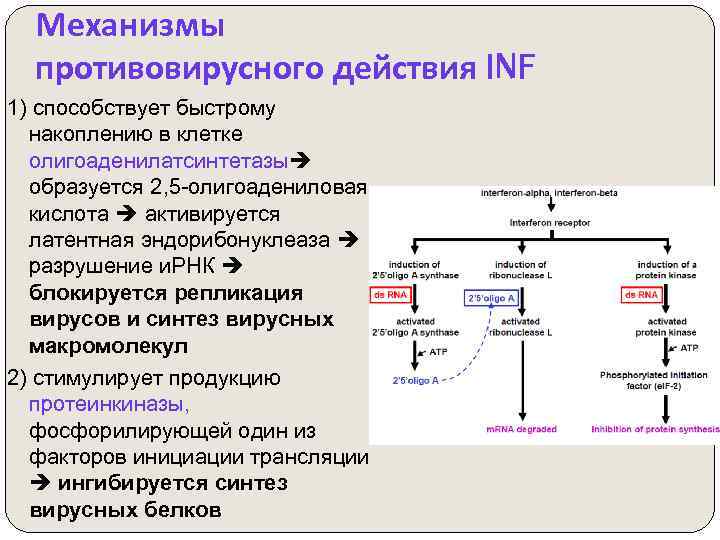 Механизмы противовирусного действия INF 1) способствует быстрому накоплению в клетке олигоаденилатсинтетазы образуется 2, 5 -олигоадениловая кислота активируется латентная эндорибонуклеаза разрушение и. РНК блокируется репликация вирусов и синтез вирусных макромолекул 2) стимулирует продукцию протеинкиназы, фосфорилирующей один из факторов инициации трансляции ингибируется синтез вирусных белков
Механизмы противовирусного действия INF 1) способствует быстрому накоплению в клетке олигоаденилатсинтетазы образуется 2, 5 -олигоадениловая кислота активируется латентная эндорибонуклеаза разрушение и. РНК блокируется репликация вирусов и синтез вирусных макромолекул 2) стимулирует продукцию протеинкиназы, фосфорилирующей один из факторов инициации трансляции ингибируется синтез вирусных белков
 Иммуномодулирующее и противоопухолевое действие γ-INF На систему врождённого иммунитета: стимулирует ЕКК активирует Мф активирует систему комплемента стимулирует образование молекул ГКГС класса II На систему приобретённого иммунитета: стимулирует активность цитотоксических Т-л и чувствительность к ним клеток-мишеней кофактор дифференцировки и активации В-л и антагонист действия на них ИЛ 4, стимулирует образование АТ влияет на процессы переключения биосинтеза Ig
Иммуномодулирующее и противоопухолевое действие γ-INF На систему врождённого иммунитета: стимулирует ЕКК активирует Мф активирует систему комплемента стимулирует образование молекул ГКГС класса II На систему приобретённого иммунитета: стимулирует активность цитотоксических Т-л и чувствительность к ним клеток-мишеней кофактор дифференцировки и активации В-л и антагонист действия на них ИЛ 4, стимулирует образование АТ влияет на процессы переключения биосинтеза Ig
 2. Группы противовирусных препаратов 2. Индукторы INF (арбидол, циклоферон, неовир, полудан, продигиозан) – интерфероногены – экзогенные вещества, стимулирующие при введении в организм синтез эндогенных INF, которые сохраняются длительно: - часто > эффективны, чем сам INF - обладают широким спектром противовирусной активности - стимулируют механизмы специфического иммунитета - эффективны при лечении опухолей
2. Группы противовирусных препаратов 2. Индукторы INF (арбидол, циклоферон, неовир, полудан, продигиозан) – интерфероногены – экзогенные вещества, стимулирующие при введении в организм синтез эндогенных INF, которые сохраняются длительно: - часто > эффективны, чем сам INF - обладают широким спектром противовирусной активности - стимулируют механизмы специфического иммунитета - эффективны при лечении опухолей
 3 -4. Группы противовирусных препаратов 3. Синтетические соединения: А. Производные адамантамина гидрохлорида (амантадин, ремантадин) Б. Производное тетрагидронафталина (оксолин) В. Тиосемикарбазоны (метисазон) Г. Ингибиторы проникновения, ОТ, интегразы, протеазы (препараты для лечения ВИЧ-инфекции) 4. Аномальные нуклеозиды А. Аналоги пиримидина (идоксуридин) Б. Аналоги пурина (рибавирин, видарабин, ацикловир, виразол)
3 -4. Группы противовирусных препаратов 3. Синтетические соединения: А. Производные адамантамина гидрохлорида (амантадин, ремантадин) Б. Производное тетрагидронафталина (оксолин) В. Тиосемикарбазоны (метисазон) Г. Ингибиторы проникновения, ОТ, интегразы, протеазы (препараты для лечения ВИЧ-инфекции) 4. Аномальные нуклеозиды А. Аналоги пиримидина (идоксуридин) Б. Аналоги пурина (рибавирин, видарабин, ацикловир, виразол)
 Поиск противовирусных препаратов сложная задача, т. к. репродукция вирусов тесно связана с функционированием эукариотической клетки Скрининг большого количества соединений на предмет противовирусной активности (ремантадин, метисазон) Направленный синтез химиопрепаратов, действующих на определённые стадии репродукции вируса
Поиск противовирусных препаратов сложная задача, т. к. репродукция вирусов тесно связана с функционированием эукариотической клетки Скрининг большого количества соединений на предмет противовирусной активности (ремантадин, метисазон) Направленный синтез химиопрепаратов, действующих на определённые стадии репродукции вируса
 Принцип противовирусной фармакотерапии раннее начало терапии, до развития необратимого повреждения тканей, т. к. противовирусные препараты препятствуют воспроизводству вирусов, а не уничтожают их Высокая токсичность противовирусных препаратов этиотропная терапия при большинстве вирусных инфекций отсутствует Антибиотики и другие антимикробные препараты не действуют на вирусы!
Принцип противовирусной фармакотерапии раннее начало терапии, до развития необратимого повреждения тканей, т. к. противовирусные препараты препятствуют воспроизводству вирусов, а не уничтожают их Высокая токсичность противовирусных препаратов этиотропная терапия при большинстве вирусных инфекций отсутствует Антибиотики и другие антимикробные препараты не действуют на вирусы!
 Благодарю за внимание !
Благодарю за внимание !


