сталь.ppt
- Количество слайдов: 17

Виробництво сталі Технологічні та хімічні особливості процесів

Загальна інформація про сталь • Сталь – сплав заліза з Карбоном (до 1, 7%) та деяких інших елементів (Si, Mn, P, S) у дуже малих кількостях. • Збільшення вмісту Сульфуру призводить до крихкості сталі при високих температурах (червоноламкість) • Збільшення вмісту Фосфору – до крихкості при низьких температурах (холодноламкість)

Загальна інформація про сталь • Сталь з великим вмістом Карбону (2%) називають твердою. Вона йде на виготовлення інструментів • Сталь з мінімальним вмістом Карбону (~0, 3%) називають м’якою або ковкою.

Домішки, що містяться в сталі • Корисні домішки: • Шкідливі домішки: 1) Mn та Si містяться в сталі всіх марок. Вони надають їй зносостійкості та жаростійкості 2) Легуючі добавки, які спеціально вводяться в сталь: Cr, Mo, W, Ni, V, Ti, Al. 1) S, P, As, Sb, Sn, Zn, Pb, O 2↑, N 2 ↑ , H 2 ↑. 2) Деякі домішки (S, P) видаляють в процесі плавки за допомогою флюсів 3) Гази (О 2, N 2, H 2) видаляють після виплавки продувкою аргоном
Апарати сталелітейного виробництва • МАРТЕН • КОНВЕРТОР • ЕЛЕКТРОПІЧЬ
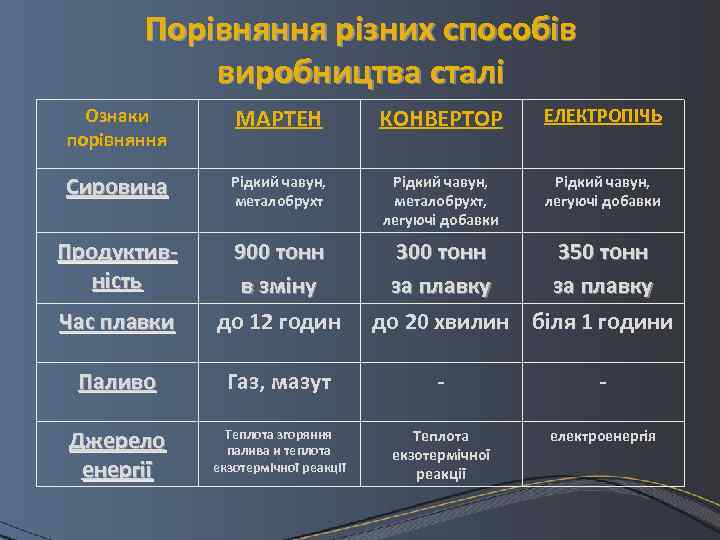
Порівняння різних способів виробництва сталі Ознаки порівняння МАРТЕН КОНВЕРТОР ЕЛЕКТРОПІЧЬ Сировина Рідкий чавун, металобрухт, легуючі добавки Рідкий чавун, легуючі добавки Продуктивність Час плавки 900 тонн в зміну до 12 годин Паливо Газ, мазут - - Джерело енергії Теплота згоряння палива и теплота екзотермічної реакції Теплота екзотермічної реакції електроенергія 300 тонн 350 тонн за плавку до 20 хвилин біля 1 години

ОСНОВНІ ХІМІЧНІ ПРОЦЕСИ ВИРОБНИЦТВА СТАЛІ

1 стадія Небажані реакції окиснення заліза • 1) Чавун: 2 Fe + O 2 = 2 Fe. O + Q • 2) Металобрухт (Fe 2 O 3 и Fe 3 O 4): Fe + Fe 3 O 4 = 4 Fe. O + Q

2 Стадія Окиснення домішок ферум (II) оксидом Si + 2 Fe. O = Si. O 2 + 2 Fe + Q Mn + Fe. O = Mn. O + Fe + Q 2 P + 5 Fe. O = P 2 O 5 + 5 Fe + Q C + Fe. O = CO + Fe - Q

3 Стадія Утворення шлаку (видалення Фосфору та Сульфуру флюсами) 3 Ca. O + P 2 O 5 = Ca 3(PO 4)2 Ca. O + Fe. S = Ca. S + Fe. O

4 Стадія Розкислення сталі (відновлення Fe. O до заліза) • Розкислювачі: Fe-Mn, Fe-Si, Fe-Al Mn + Fe. O = Mn. O + Fe Si + 2 Fe. O = Si. O 2 + 2 Fe 2 Al + 3 Fe. O = Al 2 O 3 + 3 Fe • Основний продукт: сталь • Побічний продукт: шлак, відхідні гази

Переваги процесів МАРТЕН • Утилізація металобрухту • Незначна вимогливість до хімічного складу сировини, висока якість та широкий асортимент сталі КОНВЕРТОР • Висока продуктивність апарату • Добування легованої сталі високої якості • Автоматизація процесу • Відносно низька собівартість продукту ЭЛЕКТРОПЕЧЬ • Дуже висока якість сталі, яка містить тугоплавкі легуючі добавки

Недоліки процесів МАРТЕН • Довготривалість процесу • Низька продуктивність • Забруднення атмосфери • Преривність процесу (щоб піч не остила, у період випуску сталі не припиняють спалювання палива) • Важко отримати високолеговану сталь, оскільки в атмосфері печі містяться окислювачі КОНВЕРТОР • Періодичність процесу • Частина металу губиться при вигорянні ЭЛЕКТРОПЕЧЬ • Висока вартість електроенергії • Не можна отримати сорти сталі, в яких Карбону міститься менше 0, 1%, оскільки частина Карбону обов’язково переходить у сталь при згорянні електродів • Потрібно час від часу нарощувати електроди
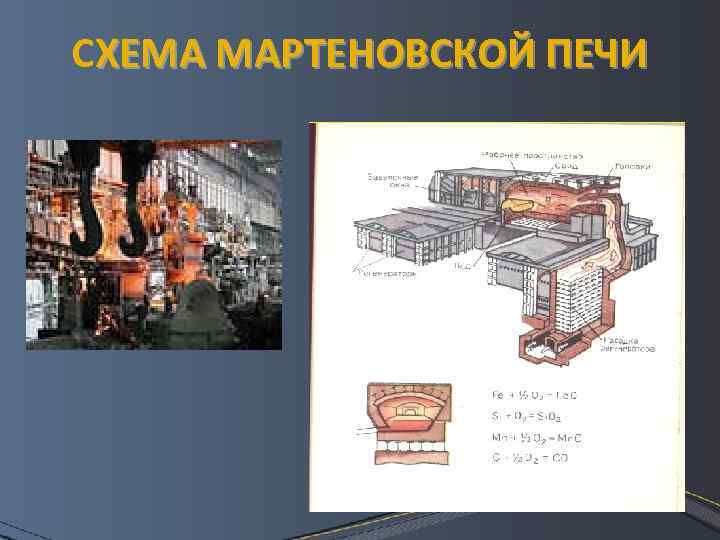
СХЕМА МАРТЕНОВСКОЙ ПЕЧИ
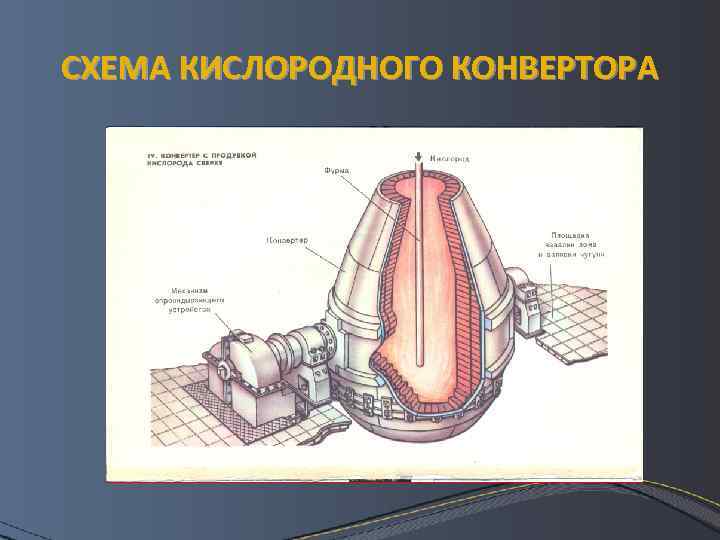
СХЕМА КИСЛОРОДНОГО КОНВЕРТОРА

СХЕМА УСТРОЙСТВА ЭЛЕКТРОДУГОВОЙ ПЕЧИ

Домашнє завдання • Попель с. 183 -186 № 255 – письм. • Ярошенко с. 199 -202 • Задача При спалюванні 2, 4 г залізного порошку зібрано 56 мл вуглекислого газу (н. у. ). Яка масова частка карбону в залізі? Зі сталі чи чавуну виготовлено цей порошок?
сталь.ppt