Prezentation 2 ukr.PPT
- Количество слайдов: 159
 ВІЛ–інфекція і СНІД Червона стрічка — символ солідарності з ВІЛ-позитивними та хворими на СНІД
ВІЛ–інфекція і СНІД Червона стрічка — символ солідарності з ВІЛ-позитивними та хворими на СНІД
 СНІД НАБУВАЄ МАСШТАБІВ ПАНДЕМІЇ
СНІД НАБУВАЄ МАСШТАБІВ ПАНДЕМІЇ
 ВІЛ - вірус імунодефіциту людини HIV – human immunodeficiency virus СНІД – синдром набутого імунодефіциту AIDS – acquired immunodeficiency syndrome
ВІЛ - вірус імунодефіциту людини HIV – human immunodeficiency virus СНІД – синдром набутого імунодефіциту AIDS – acquired immunodeficiency syndrome
 ВІЛ-інфекція – не вирок
ВІЛ-інфекція – не вирок
 Африканська зелена мартишка – головний резервуар вірусу імунодефіциту мавп (SIV), спорідненого до вірусу, що викликає СНІД у людини. У популяціях зелених мавп звичайно є зараженим від 30 до 70 % особин. Хоча SIV не викликає хворобу у мартишок, він може бути причиною СІНДу в інших видів мавп.
Африканська зелена мартишка – головний резервуар вірусу імунодефіциту мавп (SIV), спорідненого до вірусу, що викликає СНІД у людини. У популяціях зелених мавп звичайно є зараженим від 30 до 70 % особин. Хоча SIV не викликає хворобу у мартишок, він може бути причиною СІНДу в інших видів мавп.

 Ретровіруси - РНК-вмісні пухлинні віруси. Мають фермент - зворотну транскриптазу (ревертазу), яка визначає передачу генетичної інформації від РНК на ДНК. У заражених ретровірусами клітинах синтезується провірусна ДНК, комплементарна віріонній РНК, яка інтегрує у клітинний геном.
Ретровіруси - РНК-вмісні пухлинні віруси. Мають фермент - зворотну транскриптазу (ревертазу), яка визначає передачу генетичної інформації від РНК на ДНК. У заражених ретровірусами клітинах синтезується провірусна ДНК, комплементарна віріонній РНК, яка інтегрує у клітинний геном.
 Родина ретровірусів поділяється на 7 родів. Рід Lentivirinae (“повільні” віруси): - збудники повільних інфекцій овець, корів та коней, хронічних захворювань мозку, пневмонії, артриту й анемії (меді-вісна); - Т-лімфотропні віруси 1 -го і 2 -го типу; - ВІЛ.
Родина ретровірусів поділяється на 7 родів. Рід Lentivirinae (“повільні” віруси): - збудники повільних інфекцій овець, корів та коней, хронічних захворювань мозку, пневмонії, артриту й анемії (меді-вісна); - Т-лімфотропні віруси 1 -го і 2 -го типу; - ВІЛ.
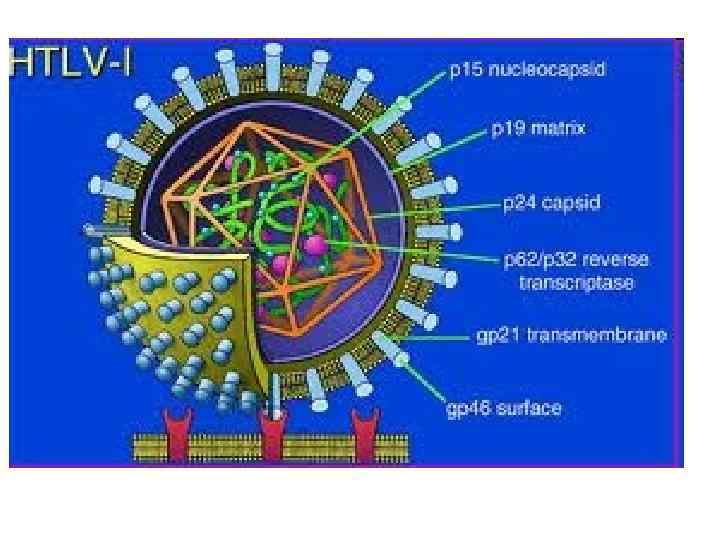
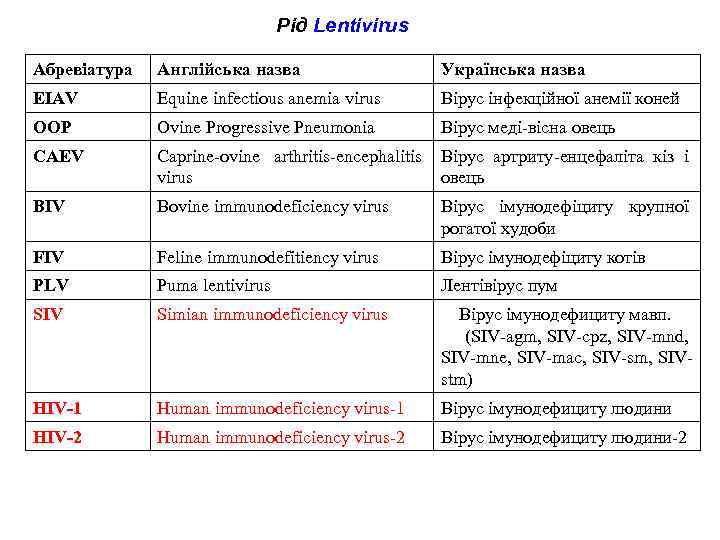 Рід Lentivirus Абревіатура Англійська назва Українська назва EIAV Equine infectious anemia virus Вірус інфекційної анемії коней OOP Ovine Progressive Pneumonia Вірус меді-вісна овець CAEV Caprine-ovine arthritis-encephalitis virus Вірус артриту-енцефаліта кіз і овець BIV Bovine immunodeficiency virus Вірус імунодефіциту крупної рогатої худоби FIV Feline immunodefitiency virus Вірус імунодефіциту котів PLV Puma lentivirus Лентівірус пум SIV Simian immunodeficiency virus Вірус імунодефициту мавп. (SIV-agm, SIV-cpz, SIV-mnd, SIV-mne, SIV-mac, SIV-sm, SIVstm) HIV-1 Human immunodeficiency virus-1 Вірус імунодефициту людини HIV-2 Human immunodeficiency virus-2 Вірус імунодефициту людини-2
Рід Lentivirus Абревіатура Англійська назва Українська назва EIAV Equine infectious anemia virus Вірус інфекційної анемії коней OOP Ovine Progressive Pneumonia Вірус меді-вісна овець CAEV Caprine-ovine arthritis-encephalitis virus Вірус артриту-енцефаліта кіз і овець BIV Bovine immunodeficiency virus Вірус імунодефіциту крупної рогатої худоби FIV Feline immunodefitiency virus Вірус імунодефіциту котів PLV Puma lentivirus Лентівірус пум SIV Simian immunodeficiency virus Вірус імунодефициту мавп. (SIV-agm, SIV-cpz, SIV-mnd, SIV-mne, SIV-mac, SIV-sm, SIVstm) HIV-1 Human immunodeficiency virus-1 Вірус імунодефициту людини HIV-2 Human immunodeficiency virus-2 Вірус імунодефициту людини-2
 Різновиди ВІЛ: -ВІЛ-1 – відкрито у 1983 р. , найбільш розповсюджений, штами: M (major), O (outlier), N (new); - ВІЛ-2 – відкрито у 1986 р. , відрізняється за структурою геному, менш патогенний; - ВІЛ-3 (підтип O ВІЛ-1) - відкрито у 1988 р. , рідкий різновид, значно відрізняється за структурою геному; - ВІЛ-4 - відкрито у 1986 р. , рідкий різновид.
Різновиди ВІЛ: -ВІЛ-1 – відкрито у 1983 р. , найбільш розповсюджений, штами: M (major), O (outlier), N (new); - ВІЛ-2 – відкрито у 1986 р. , відрізняється за структурою геному, менш патогенний; - ВІЛ-3 (підтип O ВІЛ-1) - відкрито у 1988 р. , рідкий різновид, значно відрізняється за структурою геному; - ВІЛ-4 - відкрито у 1986 р. , рідкий різновид.
 Особливості вірусу ВІЛ - має спорідненість до Т-лімфоцитів-хелперів з молекулоюрецептором CD 4+ на поверхні; - вбиває Т-хелпери; - генетичний аппарат ВІЛ має ряд додаткових генів, відсутніх в інших ретровірусів. Наслідок – у тисячу разів швидша транскрипція геному, ніж у клітинних генів. Швидкість розмноження ВІЛ величезна; - надзвичайна мінливість – у 30– 100 разів (за деякимим даними в мільйони разів) вища, ніж у вірусу грипу.
Особливості вірусу ВІЛ - має спорідненість до Т-лімфоцитів-хелперів з молекулоюрецептором CD 4+ на поверхні; - вбиває Т-хелпери; - генетичний аппарат ВІЛ має ряд додаткових генів, відсутніх в інших ретровірусів. Наслідок – у тисячу разів швидша транскрипція геному, ніж у клітинних генів. Швидкість розмноження ВІЛ величезна; - надзвичайна мінливість – у 30– 100 разів (за деякимим даними в мільйони разів) вища, ніж у вірусу грипу.
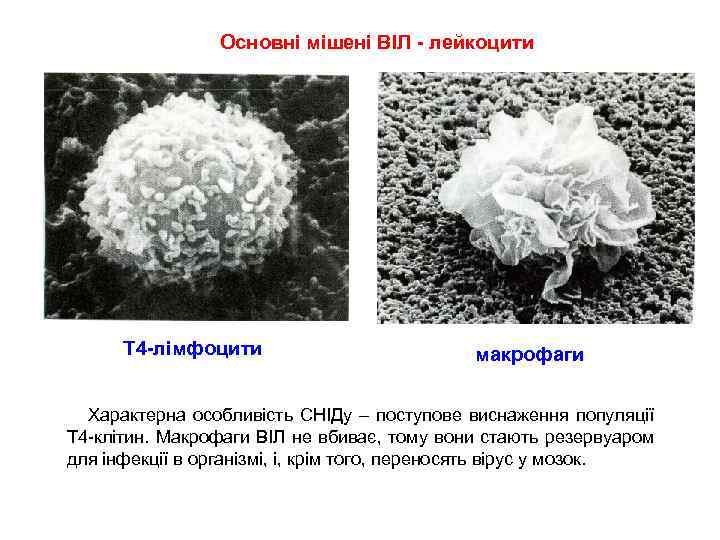 Основні мішені ВІЛ - лейкоцити Т 4 -лімфоцити макрофаги Характерна особливість СНІДу – поступове виснаження популяції Т 4 -клітин. Макрофаги ВІЛ не вбиває, тому вони стають резервуаром для інфекції в організмі, і, крім того, переносять вірус у мозок.
Основні мішені ВІЛ - лейкоцити Т 4 -лімфоцити макрофаги Характерна особливість СНІДу – поступове виснаження популяції Т 4 -клітин. Макрофаги ВІЛ не вбиває, тому вони стають резервуаром для інфекції в організмі, і, крім того, переносять вірус у мозок.
 Стадії СНІДу - латентна інфекція – від декількох місяців до 5 років; - синдром лімфоаденопатії – (СПНЛ – синдром пролонгованої немотивованої лімфоаденопатії або пре. СНІД), тривалість 1 – 2 роки (в окремих випадках до 7 років); - клінічно виражений СНІД – з різноманітною картиною хвороби та ураженням різних органів і тканин (шкіра, лімфатична система, органи дихання, шлунково-кишковий тракт, нервова система та ін. ).
Стадії СНІДу - латентна інфекція – від декількох місяців до 5 років; - синдром лімфоаденопатії – (СПНЛ – синдром пролонгованої немотивованої лімфоаденопатії або пре. СНІД), тривалість 1 – 2 роки (в окремих випадках до 7 років); - клінічно виражений СНІД – з різноманітною картиною хвороби та ураженням різних органів і тканин (шкіра, лімфатична система, органи дихання, шлунково-кишковий тракт, нервова система та ін. ).
 Біохімічна і молекулярнобіологічна структура вірусу імунодефіциту людини
Біохімічна і молекулярнобіологічна структура вірусу імунодефіциту людини
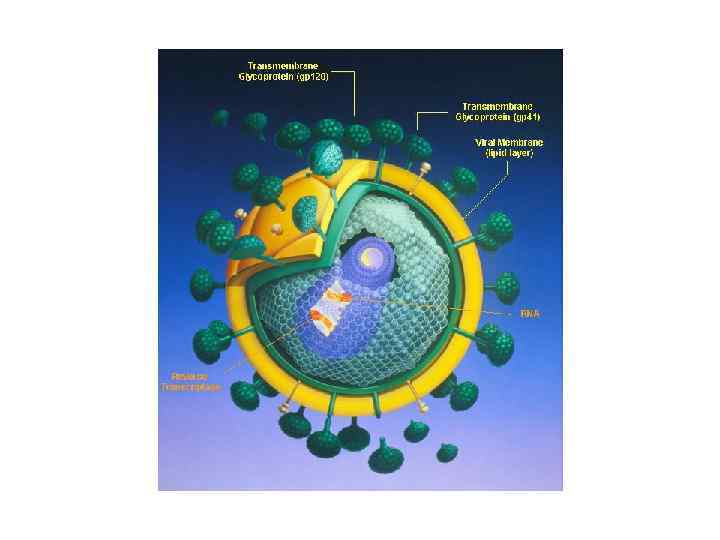
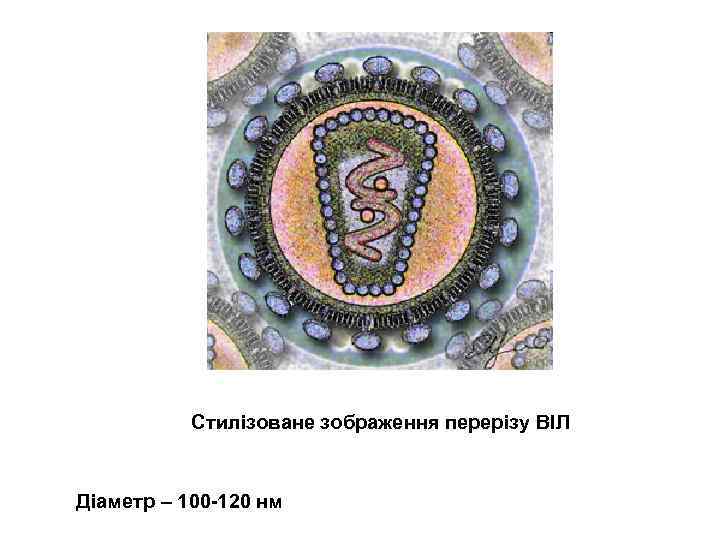 Стилізоване зображення перерізу ВІЛ Діаметр – 100 -120 нм
Стилізоване зображення перерізу ВІЛ Діаметр – 100 -120 нм
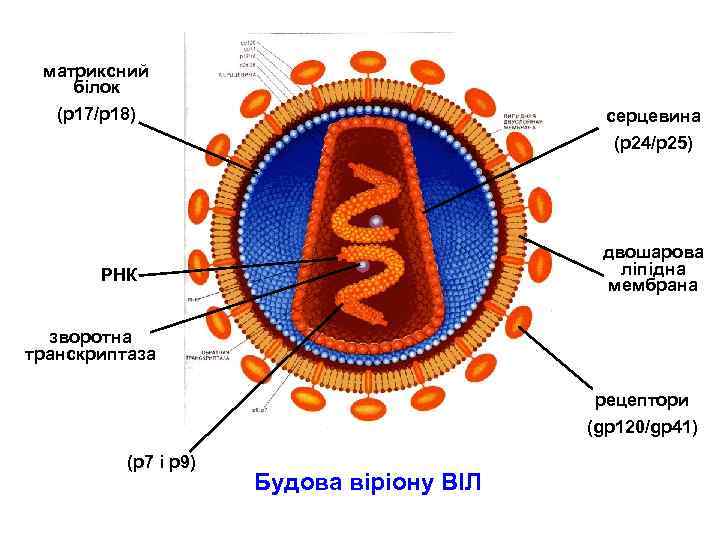 матриксний білок (р17/р18) серцевина (р24/р25) двошарова ліпідна мембрана РНК зворотна транскриптаза рецептори (gр120/gр41) (р7 і р9) Будова віріону ВІЛ
матриксний білок (р17/р18) серцевина (р24/р25) двошарова ліпідна мембрана РНК зворотна транскриптаза рецептори (gр120/gр41) (р7 і р9) Будова віріону ВІЛ
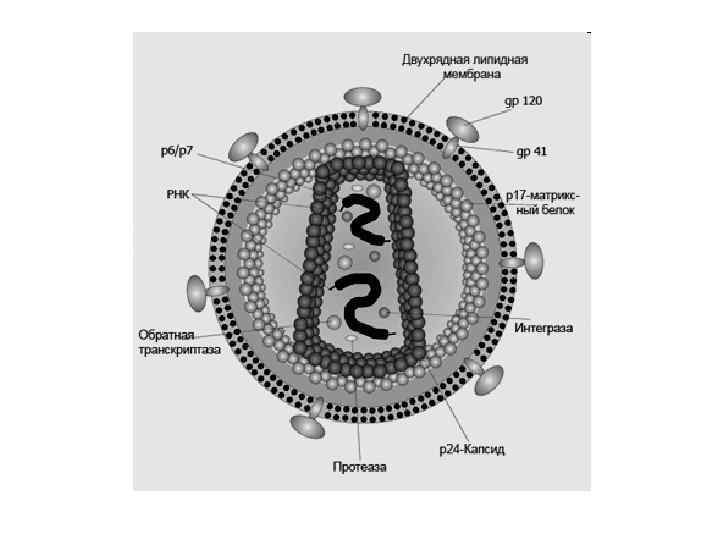
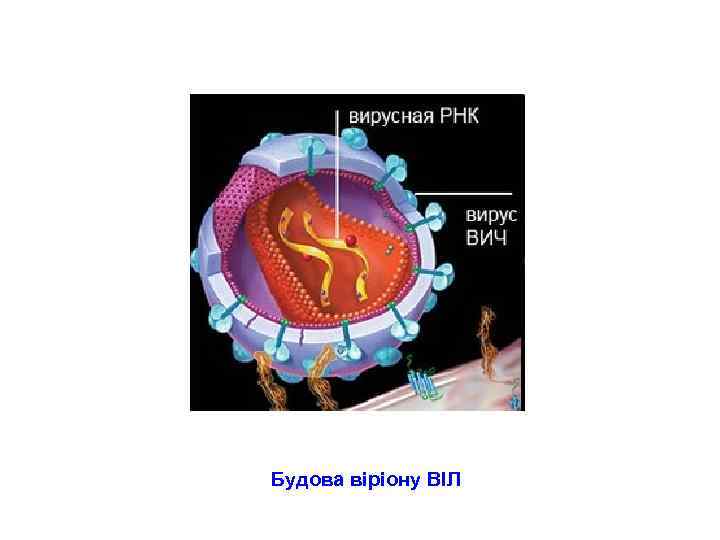 Будова віріону ВІЛ
Будова віріону ВІЛ
 Зображення ВІЛ, отримане за допомогою трансмісійного електронного мікроскопу
Зображення ВІЛ, отримане за допомогою трансмісійного електронного мікроскопу
 Мікрофотографія віріонів ВІЛ (х 200 000)
Мікрофотографія віріонів ВІЛ (х 200 000)
 Структура частки ВІЛ 1. Суперкапсид або зовнішня оболонка вірусу (“конверт”) - бімолекулярний шар ліпідів, походить з клітинної мембрани хазяїна, із вбудованими рецепторами - глікопротеїнами gp 120 (SU, surface) та gp 41 (TM, transmembrane), 1 gp 41 + 3 -5 gp 120. 2. Матриксний білок р17 (MA, matrix) – між зовнішньою вірусною мембраною і серцевиною вірусу, ~ 2 тис. молекул білка утворюють шар товщиною 5 -7 нм. 3. Нуклеокапсид або серцевина вірусу (кор) – під зовнішньою оболонкою, має форму зрізаного конусу й утворена білком р24 (CA, capsid). 4. Геном - дві молекули позитивно-смислової (positive-sense, або (+)) РНК, з’єднані з низькомолекулярними білками р9 і р7 (NC, nucleocapsid) основного характеру - всередині серцевини. 5. Білки-ферменти - у серцевині віріону: р66, RT – зворотна транскриптаза, р34, IN – ендонуклеаза або інтеграза, Р 22, PR – протеаза.
Структура частки ВІЛ 1. Суперкапсид або зовнішня оболонка вірусу (“конверт”) - бімолекулярний шар ліпідів, походить з клітинної мембрани хазяїна, із вбудованими рецепторами - глікопротеїнами gp 120 (SU, surface) та gp 41 (TM, transmembrane), 1 gp 41 + 3 -5 gp 120. 2. Матриксний білок р17 (MA, matrix) – між зовнішньою вірусною мембраною і серцевиною вірусу, ~ 2 тис. молекул білка утворюють шар товщиною 5 -7 нм. 3. Нуклеокапсид або серцевина вірусу (кор) – під зовнішньою оболонкою, має форму зрізаного конусу й утворена білком р24 (CA, capsid). 4. Геном - дві молекули позитивно-смислової (positive-sense, або (+)) РНК, з’єднані з низькомолекулярними білками р9 і р7 (NC, nucleocapsid) основного характеру - всередині серцевини. 5. Білки-ферменти - у серцевині віріону: р66, RT – зворотна транскриптаза, р34, IN – ендонуклеаза або інтеграза, Р 22, PR – протеаза.
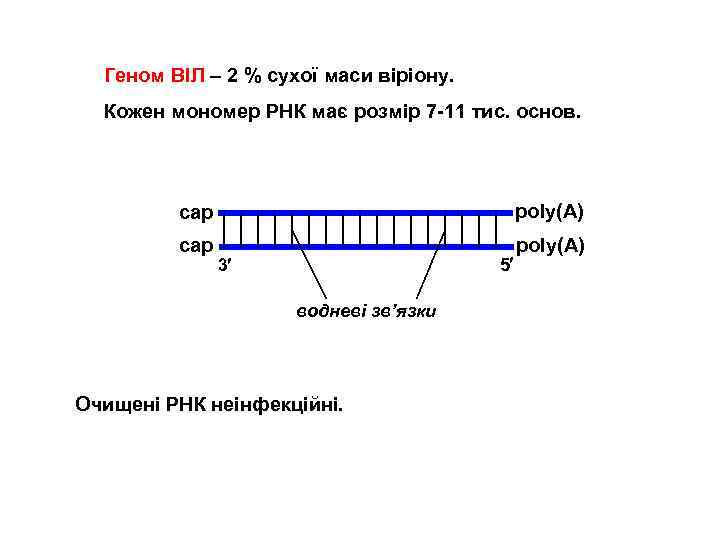 Геном ВІЛ – 2 % сухої маси віріону. Кожен мономер РНК має розмір 7 -11 тис. основ. cap poly(A) 5 3 водневі зв’язки Очищені РНК неінфекційні.
Геном ВІЛ – 2 % сухої маси віріону. Кожен мономер РНК має розмір 7 -11 тис. основ. cap poly(A) 5 3 водневі зв’язки Очищені РНК неінфекційні.
 З капсидом асоційовані білки: - nef; - vif (7 -20 молекул vif на віріон). Всередині віріону (можливо, за межами капсиду) виявлений білок vpr. Капсид утворено ~2 тис. копій білка p 24: gp 120 у віріоні - 60 -100: 1 p 24: pol ~ 10 -20: 1. У ліпідній мембрані ВІЛ також знаходяться мембранні білки клітин: - лейкоцитарні антигени людини (HLA) класів I і II; - молекули адгезії.
З капсидом асоційовані білки: - nef; - vif (7 -20 молекул vif на віріон). Всередині віріону (можливо, за межами капсиду) виявлений білок vpr. Капсид утворено ~2 тис. копій білка p 24: gp 120 у віріоні - 60 -100: 1 p 24: pol ~ 10 -20: 1. У ліпідній мембрані ВІЛ також знаходяться мембранні білки клітин: - лейкоцитарні антигени людини (HLA) класів I і II; - молекули адгезії.
 Protein p 6 Локалізація у віріоні невідома, може сприяти введенню білку Vpr у віріон Three proteins are associated with HIV capsid : - nef; - vif (7 -20 molecules per virion). Protein vpr is located inside of the virion. HIV membrane (envelope) also contains host cell proteins: - Human Leucocyte Antigens (HLA) I and II; - Cellular adhesion molecules.
Protein p 6 Локалізація у віріоні невідома, може сприяти введенню білку Vpr у віріон Three proteins are associated with HIV capsid : - nef; - vif (7 -20 molecules per virion). Protein vpr is located inside of the virion. HIV membrane (envelope) also contains host cell proteins: - Human Leucocyte Antigens (HLA) I and II; - Cellular adhesion molecules.
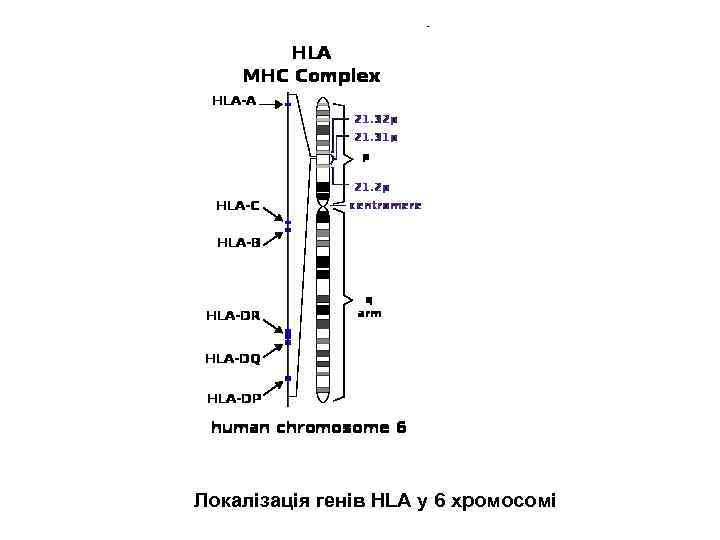 Локалізація генів HLA у 6 хромосомі
Локалізація генів HLA у 6 хромосомі
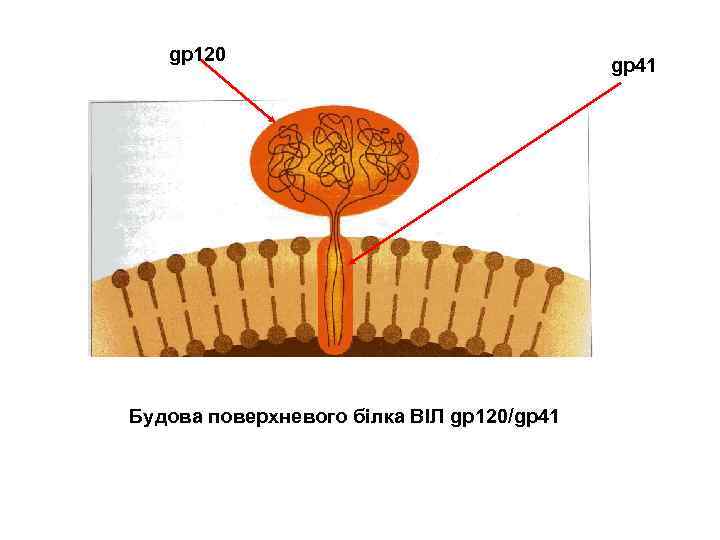 gp 120 Будова поверхневого білка ВІЛ gp 120/gp 41
gp 120 Будова поверхневого білка ВІЛ gp 120/gp 41
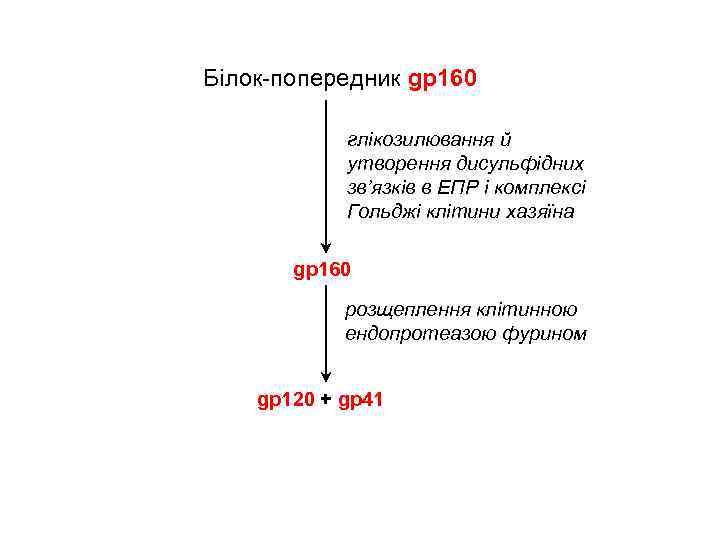 Білок-попередник gp 160 глікозилювання й утворення дисульфідних зв’язків в ЕПР і комплексі Гольджі клітини хазяїна gp 160 розщеплення клітинною ендопротеазою фурином gp 120 + gp 41
Білок-попередник gp 160 глікозилювання й утворення дисульфідних зв’язків в ЕПР і комплексі Гольджі клітини хазяїна gp 160 розщеплення клітинною ендопротеазою фурином gp 120 + gp 41
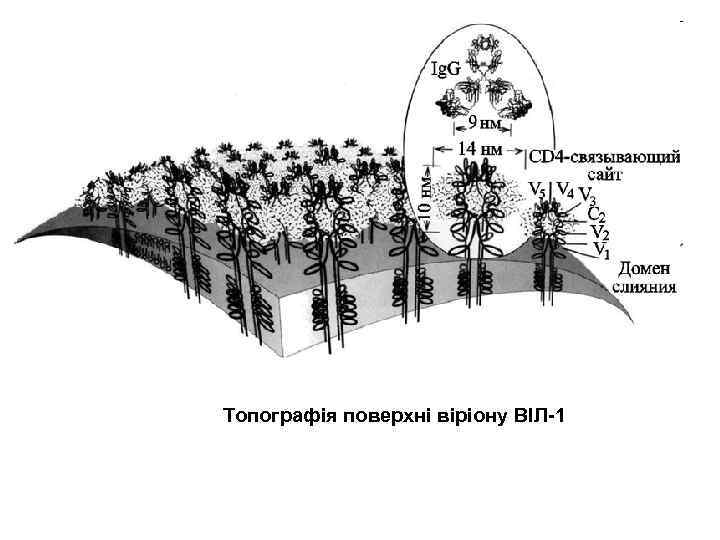 Топографія поверхні віріону ВІЛ-1
Топографія поверхні віріону ВІЛ-1
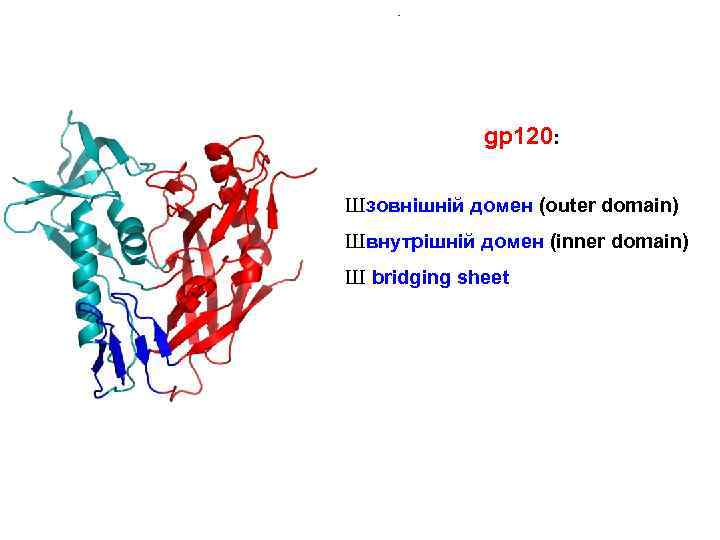 gp 120: Ш зовнішній домен (outer domain) Ш внутрішній домен (inner domain) Ш bridging sheet
gp 120: Ш зовнішній домен (outer domain) Ш внутрішній домен (inner domain) Ш bridging sheet
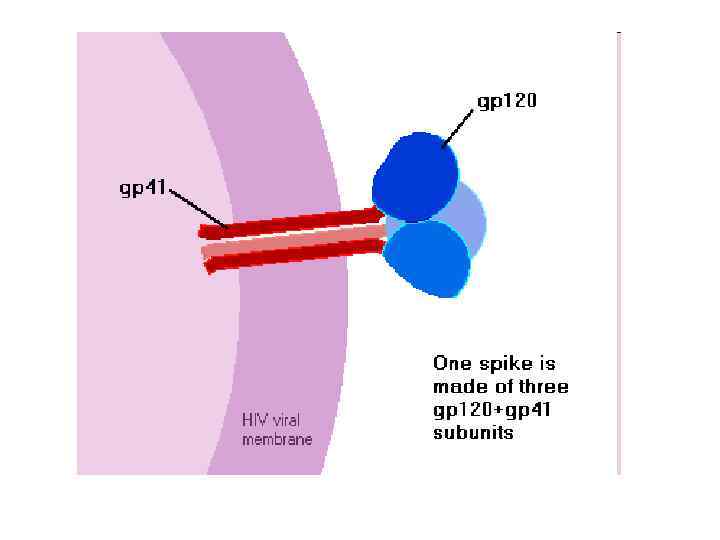
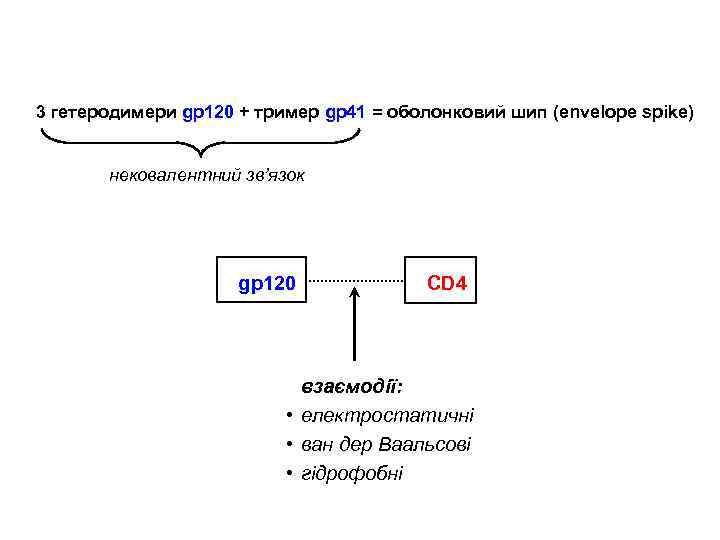 3 гетеродимери gp 120 + тример gp 41 = оболонковий шип (envelope spike) нековалентний зв’язок gp 120 CD 4 взаємодії: • електростатичні • ван дер Ваальсові • гідрофобні
3 гетеродимери gp 120 + тример gp 41 = оболонковий шип (envelope spike) нековалентний зв’язок gp 120 CD 4 взаємодії: • електростатичні • ван дер Ваальсові • гідрофобні
 Ділянки gp 120 : Ш варіабельні (V 1 -V 5) Ш консервативні (С 1 -С 5) До N-кінця gp 120 приєднані вуглеводи (1/2 маси), переважно олігоманоза. 2 рецепторні сайти gp 120: v для рецептору CD 4 v для корецепторів CCR 5 і CXCR 4
Ділянки gp 120 : Ш варіабельні (V 1 -V 5) Ш консервативні (С 1 -С 5) До N-кінця gp 120 приєднані вуглеводи (1/2 маси), переважно олігоманоза. 2 рецепторні сайти gp 120: v для рецептору CD 4 v для корецепторів CCR 5 і CXCR 4
 Кор gp 120 екранований вуглеводами. Неекранована частина gp 120 взаємодіє з gp 41. Консервативний сайт зв’язування з CD 4 «заглиблений» і важко доступний для антитіл. Варіабельні послідовності gp 120 ВІЛ (петлі V 1 — V 4) – головна мішень для нейтралізуючих антитіл імунної системи людини.
Кор gp 120 екранований вуглеводами. Неекранована частина gp 120 взаємодіє з gp 41. Консервативний сайт зв’язування з CD 4 «заглиблений» і важко доступний для антитіл. Варіабельні послідовності gp 120 ВІЛ (петлі V 1 — V 4) – головна мішень для нейтралізуючих антитіл імунної системи людини.
 HIV Env v Env складається з тримерів нековалентно зв’язаних gp 120 іgp 41. v Під час реплікації транскрибується m. RNA гену Env, на клітинниз прибосомах синтезується попередник 845 -870 а. к. v Він глікозилюється за залишком Асп – приєднуються поліцукри, що складаються з манози, утворюється білок gp 160.
HIV Env v Env складається з тримерів нековалентно зв’язаних gp 120 іgp 41. v Під час реплікації транскрибується m. RNA гену Env, на клітинниз прибосомах синтезується попередник 845 -870 а. к. v Він глікозилюється за залишком Асп – приєднуються поліцукри, що складаються з манози, утворюється білок gp 160.
 Домени gp 120 здатні прикріплюватися до: - рецепторів клітин-мішеней (поверхневих глікопротеїнів Т -лімфоцитів і макрофагів); - зв’язуватися з нейтралізуючими антитілами. При відокремленні поверхневої субодиниці gp 120 від віріону інгібується інфекційна здатність ВІЛ.
Домени gp 120 здатні прикріплюватися до: - рецепторів клітин-мішеней (поверхневих глікопротеїнів Т -лімфоцитів і макрофагів); - зв’язуватися з нейтралізуючими антитілами. При відокремленні поверхневої субодиниці gp 120 від віріону інгібується інфекційна здатність ВІЛ.
 HIV Env v gp 160 утворює гомотример, експортується в апарат Гольджі, розщеплюється клітинною протеазю фурином, утворюються гомотримери gp 120 і gp 41. v gp 120 і gp 41 далі підлягають N-глікозилюванню v Білок gp 120 глікозилюється в різних місцях (має 24 потенційних сайтів глікозилювання). Це глікозилювання (окрім мутацій гену Env), другою є причиною утворення різних варіантів структури gp 120. Ці нові варіанти білка gp 120 не впізнаються антитілами проти попередньо утворених варіантів цього білка.
HIV Env v gp 160 утворює гомотример, експортується в апарат Гольджі, розщеплюється клітинною протеазю фурином, утворюються гомотримери gp 120 і gp 41. v gp 120 і gp 41 далі підлягають N-глікозилюванню v Білок gp 120 глікозилюється в різних місцях (має 24 потенційних сайтів глікозилювання). Це глікозилювання (окрім мутацій гену Env), другою є причиною утворення різних варіантів структури gp 120. Ці нові варіанти білка gp 120 не впізнаються антитілами проти попередньо утворених варіантів цього білка.
 HIV Env v Після N-глікозилювання тример gp 120 нековалентно зв’язується з тримером gp 41 з утворенням гетеродимеру gp 41 -gp 120. v Дозрілі білки Env надходять до мембрани клітини, розщеплюються клітинними ферментами до на gp 120 і gp 41 і включаються до мембрани віріону. Gp 120 знаходиться на зовнішній поверхні мембрани, а gp 41 заякорений у ліпідний бішар. Після цього віріон відбуньковується від клітини-хазяїна. v Серед мутацій ВІЛ найчастіші саме мутації гену Env. Тому утворюються нащадки вірусу з порушеною структурою глікопротеїнових комплексів. Вони не можуть дозріти і навіть “випадають” з оболонки віріону.
HIV Env v Після N-глікозилювання тример gp 120 нековалентно зв’язується з тримером gp 41 з утворенням гетеродимеру gp 41 -gp 120. v Дозрілі білки Env надходять до мембрани клітини, розщеплюються клітинними ферментами до на gp 120 і gp 41 і включаються до мембрани віріону. Gp 120 знаходиться на зовнішній поверхні мембрани, а gp 41 заякорений у ліпідний бішар. Після цього віріон відбуньковується від клітини-хазяїна. v Серед мутацій ВІЛ найчастіші саме мутації гену Env. Тому утворюються нащадки вірусу з порушеною структурою глікопротеїнових комплексів. Вони не можуть дозріти і навіть “випадають” з оболонки віріону.
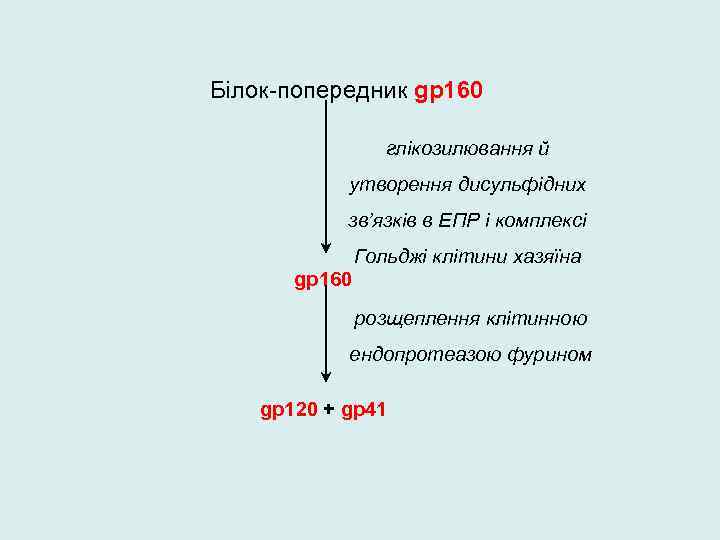 Білок-попередник gp 160 глікозилювання й утворення дисульфідних зв’язків в ЕПР і комплексі Гольджі клітини хазяїна gp 160 розщеплення клітинною ендопротеазою фурином gp 120 + gp 41
Білок-попередник gp 160 глікозилювання й утворення дисульфідних зв’язків в ЕПР і комплексі Гольджі клітини хазяїна gp 160 розщеплення клітинною ендопротеазою фурином gp 120 + gp 41
 Коли gp 160 синтезується в клітині, клітинний фермент приєднує вуглеводи до add complex carbohydrates and turn it from a protein into a glycoprotein – hence the name “gp 160″ rather than “p 160″. ) gp 160 мігрує до клітинної поверхні, де клітинні ферменти where cellular enzymes again attack it, this time chopping into two pieces – gp 120, and gp 41. When new virus particles bud off from the host cell, gp 120, and gp 41 lie on opposite sides of the virus membrane. gp 120 sits on the outside of the virus particle, forming the virus’s spikes, while gp 41 sits just on the
Коли gp 160 синтезується в клітині, клітинний фермент приєднує вуглеводи до add complex carbohydrates and turn it from a protein into a glycoprotein – hence the name “gp 160″ rather than “p 160″. ) gp 160 мігрує до клітинної поверхні, де клітинні ферменти where cellular enzymes again attack it, this time chopping into two pieces – gp 120, and gp 41. When new virus particles bud off from the host cell, gp 120, and gp 41 lie on opposite sides of the virus membrane. gp 120 sits on the outside of the virus particle, forming the virus’s spikes, while gp 41 sits just on the
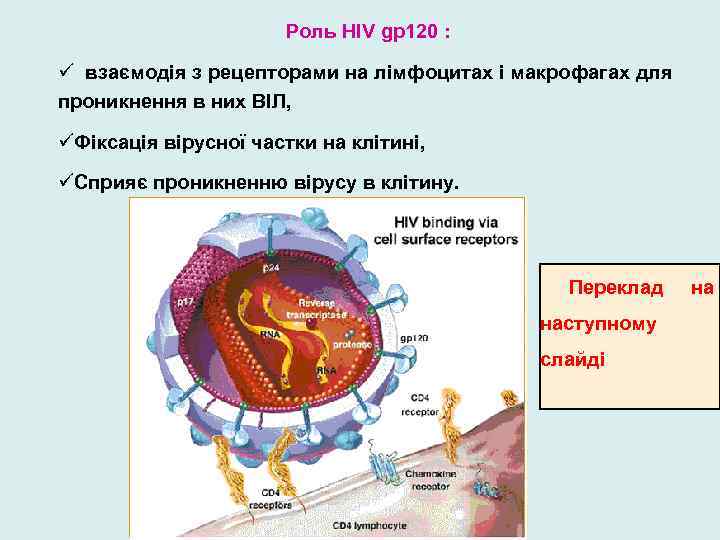 Роль HIV gp 120 : ü взаємодія з рецепторами на лімфоцитах і макрофагах для проникнення в них ВІЛ, üФіксація вірусної частки на клітині, üСприяє проникненню вірусу в клітину. Переклад наступному слайді на
Роль HIV gp 120 : ü взаємодія з рецепторами на лімфоцитах і макрофагах для проникнення в них ВІЛ, üФіксація вірусної частки на клітині, üСприяє проникненню вірусу в клітину. Переклад наступному слайді на
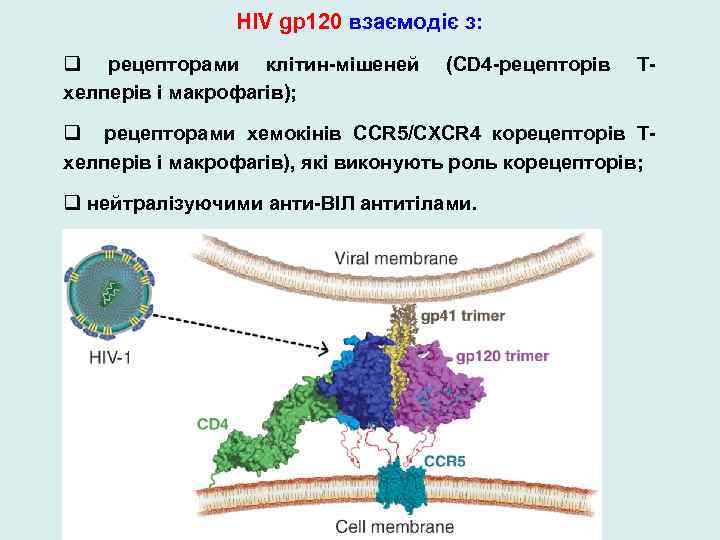 HIV gp 120 взаємодіє з: q рецепторами клітин-мішеней хелперів і макрофагів); (CD 4 -рецепторів Т- q рецепторами хемокінів CCR 5/CXCR 4 корецепторів Тхелперів і макрофагів), які виконують роль корецепторів; q нейтралізуючими анти-ВІЛ антитілами.
HIV gp 120 взаємодіє з: q рецепторами клітин-мішеней хелперів і макрофагів); (CD 4 -рецепторів Т- q рецепторами хемокінів CCR 5/CXCR 4 корецепторів Тхелперів і макрофагів), які виконують роль корецепторів; q нейтралізуючими анти-ВІЛ антитілами.
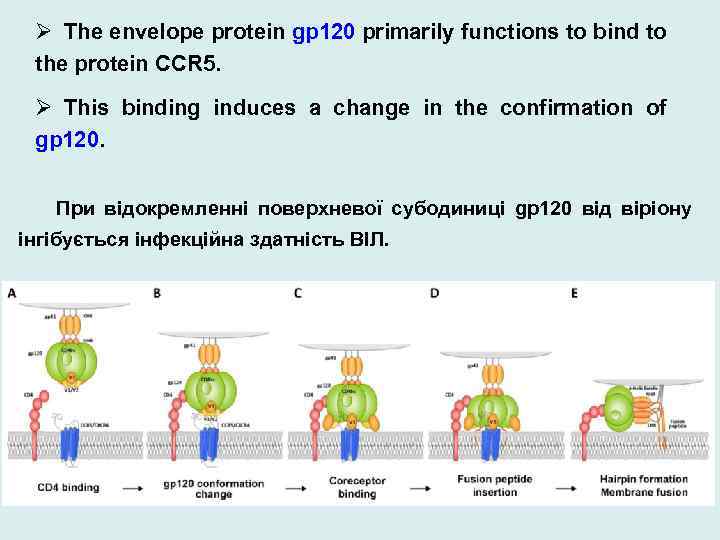 Ø The envelope protein gp 120 primarily functions to bind to the protein CCR 5. Ø This binding induces a change in the confirmation of gp 120. При відокремленні поверхневої субодиниці gp 120 від віріону інгібується інфекційна здатність ВІЛ.
Ø The envelope protein gp 120 primarily functions to bind to the protein CCR 5. Ø This binding induces a change in the confirmation of gp 120. При відокремленні поверхневої субодиниці gp 120 від віріону інгібується інфекційна здатність ВІЛ.
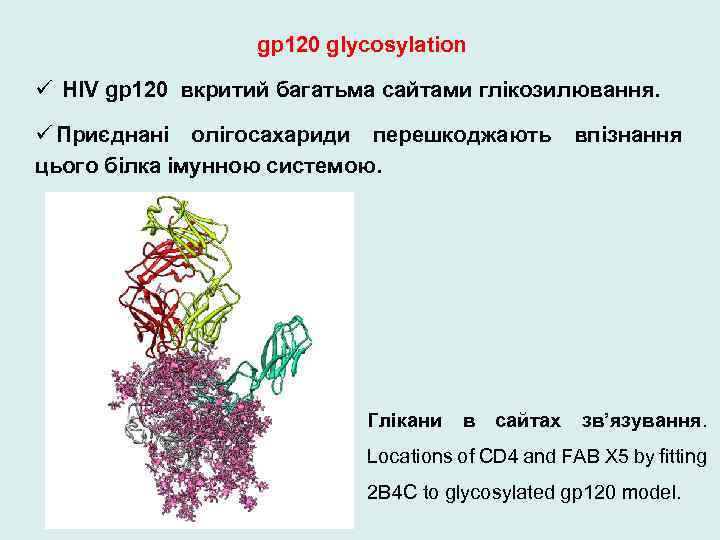 gp 120 glycosylation ü HIV gp 120 вкритий багатьма сайтами глікозилювання. ü Приєднані олігосахариди перешкоджають впізнання цього білка імунною системою. Глікани в сайтах зв’язування. Locations of CD 4 and FAB X 5 by fitting 2 B 4 C to glycosylated gp 120 model.
gp 120 glycosylation ü HIV gp 120 вкритий багатьма сайтами глікозилювання. ü Приєднані олігосахариди перешкоджають впізнання цього білка імунною системою. Глікани в сайтах зв’язування. Locations of CD 4 and FAB X 5 by fitting 2 B 4 C to glycosylated gp 120 model.
 Env gp 120 необхідний для впізнавання клітин-мішеней та зв’язування ВІЛ з ними Зовнійшній домен gp 120 взаємодіє з CD 4 -рецептором. This interaction occurs within a largely hydrophobic binding pocket composed of β-ribbon components β 20 -β 21, the CD 4 binding loop, and the α-helices of the outer domain. Це викликає конформаційні зміни внутрішнього домену gp 120. That bring together the β-sheets of the so-called "bridging sheet", which connects the outer and inner domains. Компактний зв’язуючий місток є сайтом зв’язування хемокінового рецептора CCR 5 або рідше CXCR 4. Завдяки цій взаємодії віріон приєднується до клітини-мішені й експонується білок gp 41.
Env gp 120 необхідний для впізнавання клітин-мішеней та зв’язування ВІЛ з ними Зовнійшній домен gp 120 взаємодіє з CD 4 -рецептором. This interaction occurs within a largely hydrophobic binding pocket composed of β-ribbon components β 20 -β 21, the CD 4 binding loop, and the α-helices of the outer domain. Це викликає конформаційні зміни внутрішнього домену gp 120. That bring together the β-sheets of the so-called "bridging sheet", which connects the outer and inner domains. Компактний зв’язуючий місток є сайтом зв’язування хемокінового рецептора CCR 5 або рідше CXCR 4. Завдяки цій взаємодії віріон приєднується до клітини-мішені й експонується білок gp 41.
 Структура gp 120 : ШВаріабельні ділянки – петлі (V 1 -V 5) – прямо взаємодіють з білками мембрани клітини-мішені. ШКонсервативні ділянки (С 1 -С 5) 2 рецпторні сайти gp 120: v for CD 4 рецептор v Корецептори CCR 5 і CXCR 4
Структура gp 120 : ШВаріабельні ділянки – петлі (V 1 -V 5) – прямо взаємодіють з білками мембрани клітини-мішені. ШКонсервативні ділянки (С 1 -С 5) 2 рецпторні сайти gp 120: v for CD 4 рецептор v Корецептори CCR 5 і CXCR 4
 Висока ступінь мітацій HIV визначаєтьсятакими факторами: Ø Варіації довжини варіабельних петель gp 120. Ø Ступінь N-глікозилювання варіабельних петель gp 120 визначається мутаціями (додаються чи видаляються ділянки – потенційні місця N-глікозилювання). Отже, висока варіабельність довжини та ступеню Nглікозилювання варіабельних петель gp 120 випливають на специфічність ВІЛ щодо зв’язування з клітинами-мішенями та їх інфікування.
Висока ступінь мітацій HIV визначаєтьсятакими факторами: Ø Варіації довжини варіабельних петель gp 120. Ø Ступінь N-глікозилювання варіабельних петель gp 120 визначається мутаціями (додаються чи видаляються ділянки – потенційні місця N-глікозилювання). Отже, висока варіабельність довжини та ступеню Nглікозилювання варіабельних петель gp 120 випливають на специфічність ВІЛ щодо зв’язування з клітинами-мішенями та їх інфікування.
 Механізм, за яким імунна система не впізає варіабельні петлі gp 120 Хоча петлі V 1 і V 2 є мішенню анти-ВІЛ антитіл, які продукуються організмом у відповідь на ВІЛ-інфекцію, висока ступінь мутацій gp 120 призводить до того, що нові покоління вірусу із зміненими петлями gp 120 не впізнаються наявними на той момент в організмі анти-ВІЛ “конформаційного маскування”. антитілами. Явище
Механізм, за яким імунна система не впізає варіабельні петлі gp 120 Хоча петлі V 1 і V 2 є мішенню анти-ВІЛ антитіл, які продукуються організмом у відповідь на ВІЛ-інфекцію, висока ступінь мутацій gp 120 призводить до того, що нові покоління вірусу із зміненими петлями gp 120 не впізнаються наявними на той момент в організмі анти-ВІЛ “конформаційного маскування”. антитілами. Явище
 Два механізми “конформаційного маскування”. : q Додаткове N-глікозилювання петель V 1 і V 2; q Перегрупування вже існуючих потенційних сайтів Nглікозилювання (potential N-glycosylation sites, PNGs) у петлях V 1 and V 2. Ці зміни у N-глікозилюванні петель V 1 і V 2 маскують білок Env (gp 120), й антитіла проти послідовностей у петлях V 1 і V 2 «старих» (попередніх) штамів ВІЛ не впізнають їх.
Два механізми “конформаційного маскування”. : q Додаткове N-глікозилювання петель V 1 і V 2; q Перегрупування вже існуючих потенційних сайтів Nглікозилювання (potential N-glycosylation sites, PNGs) у петлях V 1 and V 2. Ці зміни у N-глікозилюванні петель V 1 і V 2 маскують білок Env (gp 120), й антитіла проти послідовностей у петлях V 1 і V 2 «старих» (попередніх) штамів ВІЛ не впізнають їх.
 HIV infection of CD 4+ T cells in the gut
HIV infection of CD 4+ T cells in the gut
 Інфікування ВІЛ CD 4+ T клітин у кишечнику § HIV віріони можуть взаємодіяти з α 4β 7 інтегрином на поверхні CD 4+ T клітин у кишечнику. § Тому ВІЛ має кращі шанси зв’язатися та інфікувати ці CD 4+ T клітини. Природний ліганд α 4β 7 інтегрину є молекули MAd. CAM-1 (mucosal addressin cell adhesion molecule-1). α 4β 7 інтегрин призводить до міграції Т-клітин у лімфоїдну тканину, асоційовану з кишечником (gut-associated lymphoid tissue, GALT), що є важливим центром продукції Т-клітин у шлунково-кишковому тракті. • Висока щільність CD 4+ T клітин у цій ділянці сприяє швидкому поширенню ВІЛ, і тому кишечник стає “гарячою точкою” розмноження ВІЛ.
Інфікування ВІЛ CD 4+ T клітин у кишечнику § HIV віріони можуть взаємодіяти з α 4β 7 інтегрином на поверхні CD 4+ T клітин у кишечнику. § Тому ВІЛ має кращі шанси зв’язатися та інфікувати ці CD 4+ T клітини. Природний ліганд α 4β 7 інтегрину є молекули MAd. CAM-1 (mucosal addressin cell adhesion molecule-1). α 4β 7 інтегрин призводить до міграції Т-клітин у лімфоїдну тканину, асоційовану з кишечником (gut-associated lymphoid tissue, GALT), що є важливим центром продукції Т-клітин у шлунково-кишковому тракті. • Висока щільність CD 4+ T клітин у цій ділянці сприяє швидкому поширенню ВІЛ, і тому кишечник стає “гарячою точкою” розмноження ВІЛ.
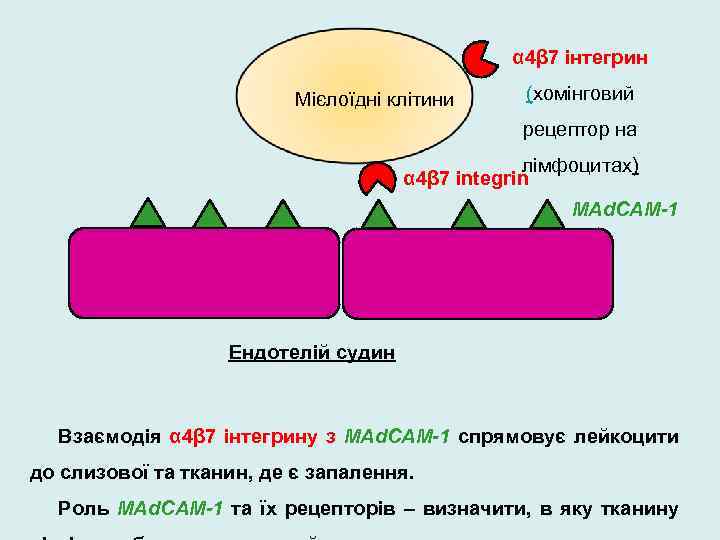 α 4β 7 інтегрин Мієлоїдні клітини (хомінговий рецептор на лімфоцитах) α 4β 7 integrin MAd. CAM-1 Ендотелій судин Взаємодія α 4β 7 інтегрину з MAd. CAM-1 спрямовує лейкоцити до слизової та тканин, де є запалення. Роль MAd. CAM-1 та їх рецепторів – визначити, в яку тканину
α 4β 7 інтегрин Мієлоїдні клітини (хомінговий рецептор на лімфоцитах) α 4β 7 integrin MAd. CAM-1 Ендотелій судин Взаємодія α 4β 7 інтегрину з MAd. CAM-1 спрямовує лейкоцити до слизової та тканин, де є запалення. Роль MAd. CAM-1 та їх рецепторів – визначити, в яку тканину
 Інфікування ВІЛ CD 4+ T клітин у кишечнику § gp 120 зв’язується з α 4β 7 інтегрином за допомогою трипептидної послідовності у петлі V 2. § V 2 петля подібна до структур, які містяться у природних лігандах інтегринів. Тому α 4β 7 може сприяти розповсюдженню ВІЛ-інфекції в кишечнику. J Virol. 2014 Sep; 88(18): 10767 -77. Envelope glycoprotein binding to the integrin α 4β 7 is not a general property of most HIV-1 strains.
Інфікування ВІЛ CD 4+ T клітин у кишечнику § gp 120 зв’язується з α 4β 7 інтегрином за допомогою трипептидної послідовності у петлі V 2. § V 2 петля подібна до структур, які містяться у природних лігандах інтегринів. Тому α 4β 7 може сприяти розповсюдженню ВІЛ-інфекції в кишечнику. J Virol. 2014 Sep; 88(18): 10767 -77. Envelope glycoprotein binding to the integrin α 4β 7 is not a general property of most HIV-1 strains.
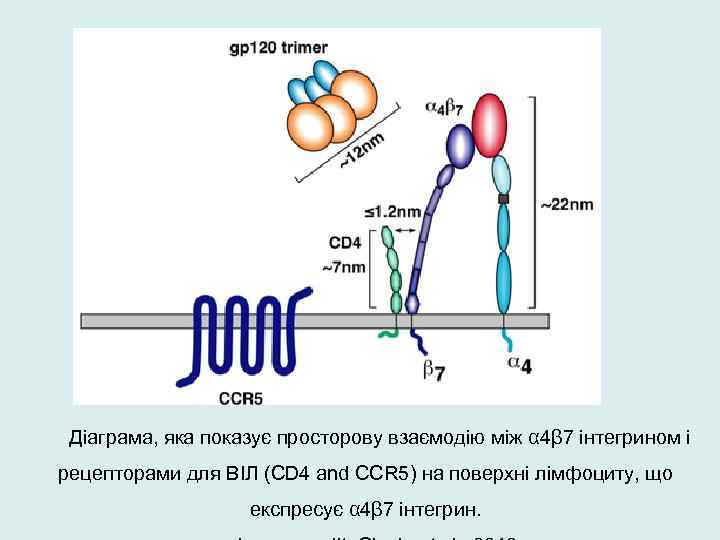 Діаграма, яка показує просторову взаємодію між α 4β 7 інтегрином і рецепторами для ВІЛ (CD 4 and CCR 5) на поверхні лімфоциту, що експресує α 4β 7 інтегрин.
Діаграма, яка показує просторову взаємодію між α 4β 7 інтегрином і рецепторами для ВІЛ (CD 4 and CCR 5) на поверхні лімфоциту, що експресує α 4β 7 інтегрин.
 gp 41 – глікопротеїн, який нековалентно зв’язаний з gp 120 і заякорений у мембрану ВІЛ. gp 41 забезпечує другий етап проникнення ВІЛ у лімфоцит: 1. gp 120 зв’язується з CD 4 -рецептором, 2. gp 120 змінює конформацію, що призводить до gp 41 експонування gp 41. 3. Викликає злиття мембран ВІЛ і лімфоцита.
gp 41 – глікопротеїн, який нековалентно зв’язаний з gp 120 і заякорений у мембрану ВІЛ. gp 41 забезпечує другий етап проникнення ВІЛ у лімфоцит: 1. gp 120 зв’язується з CD 4 -рецептором, 2. gp 120 змінює конформацію, що призводить до gp 41 експонування gp 41. 3. Викликає злиття мембран ВІЛ і лімфоцита.
 Процес, під час якого gp 41 опосередковує злиття мембран ВІЛ і клітини під час інфікування http: //www. molecularmovies. com/movies/view/120
Процес, під час якого gp 41 опосередковує злиття мембран ВІЛ і клітини під час інфікування http: //www. molecularmovies. com/movies/view/120
 Білки оболонки ВІЛ вкривають поверхню віріону (1, 2) і зв’язуються к клітиною-хазяїном http: //medicalxpress. com/news/2014 -01 -tricky-protein-hiv-vaccine. html
Білки оболонки ВІЛ вкривають поверхню віріону (1, 2) і зв’язуються к клітиною-хазяїном http: //medicalxpress. com/news/2014 -01 -tricky-protein-hiv-vaccine. html
 У складі gp 41 є 3 домени: q ектодомен, q трансмембранний домен, q цитоплазматичний домен Тример ектодоменів gp 41 складається з 3 -х паралельних N –кінцевих α-спіралей у біспіральній конформації, які оточені 3 ма антипаралельними С-кінцевими α-спіралями, зв’язаними одна з одною за допомогою гнучких петлевих ділянок. Біспіральний ектодомен зв’язаний з гідрофільним трансмембранним доменом, за яким знаходиться гідрофільний цитоплазматичний домен.
У складі gp 41 є 3 домени: q ектодомен, q трансмембранний домен, q цитоплазматичний домен Тример ектодоменів gp 41 складається з 3 -х паралельних N –кінцевих α-спіралей у біспіральній конформації, які оточені 3 ма антипаралельними С-кінцевими α-спіралями, зв’язаними одна з одною за допомогою гнучких петлевих ділянок. Біспіральний ектодомен зв’язаний з гідрофільним трансмембранним доменом, за яким знаходиться гідрофільний цитоплазматичний домен.
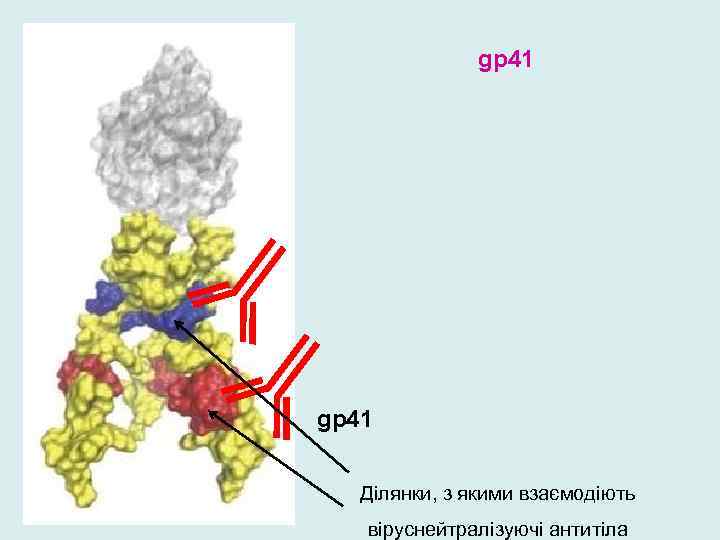 gp 41 Ділянки, з якими взаємодіють віруснейтралізуючі антитіла
gp 41 Ділянки, з якими взаємодіють віруснейтралізуючі антитіла
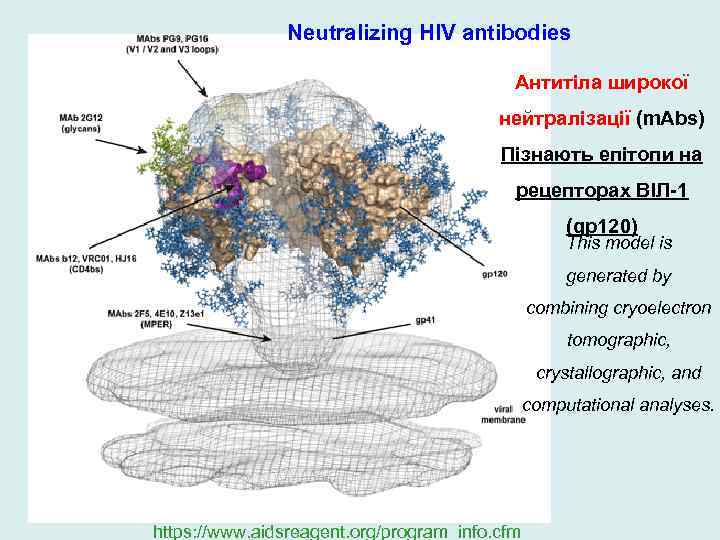 Neutralizing HIV antibodies Антитіла широкої нейтралізації (m. Abs) Пізнають епітопи на рецепторах ВІЛ-1 (gp 120) This model is generated by combining cryoelectron tomographic, crystallographic, and computational analyses. https: //www. aidsreagent. org/program_info. cfm
Neutralizing HIV antibodies Антитіла широкої нейтралізації (m. Abs) Пізнають епітопи на рецепторах ВІЛ-1 (gp 120) This model is generated by combining cryoelectron tomographic, crystallographic, and computational analyses. https: //www. aidsreagent. org/program_info. cfm
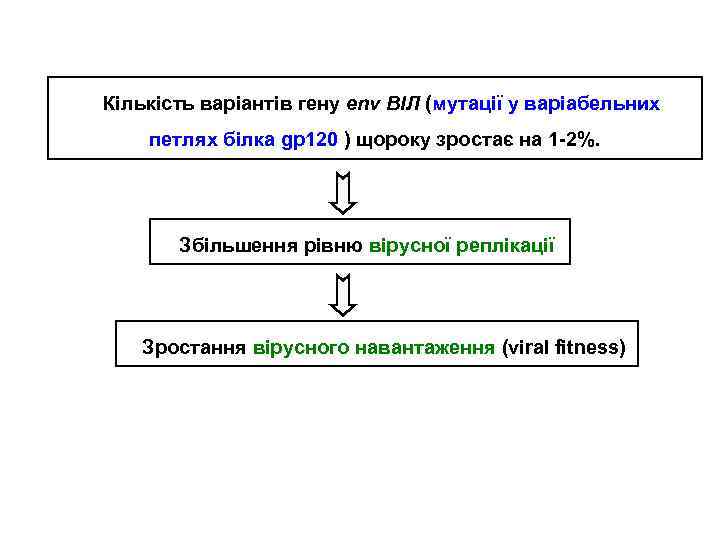 Кількість варіантів гену env ВІЛ (мутації у варіабельних петлях білка gp 120 ) щороку зростає на 1 -2%. Збільшення рівню вірусної реплікації Зростання вірусного навантаження (viral fitness)
Кількість варіантів гену env ВІЛ (мутації у варіабельних петлях білка gp 120 ) щороку зростає на 1 -2%. Збільшення рівню вірусної реплікації Зростання вірусного навантаження (viral fitness)
 Гіпотеза Wood N. *: Варіабельність у потенційних місцях N-глікозилювання gp 120 – PNGSs (potential N-linked glycosylation sites) вірусного навантаження чутливості до нейтралізуючих АТ Великі вуглеводні ланцюги, зв’язані з gp 120, можуть екранувати ділянки зв’язування з АТ. * - Wood, N. , Bhattacharya, T. , Keele, B. , Giorgi, E. , Liu, M. , Gaschen, B. , Daniels, M. , Ferrari, G. , Haynes, B. , Mc. Michael, A. , Shaw, G. , Hahn, B. , Korber, B. , and Seoighe, C. (2009). "HIV evolution in early infection: selection pressures, patterns of insertion and deletion, and the impact of APOBEC". PLOS Pathogens 5: 1– 16.
Гіпотеза Wood N. *: Варіабельність у потенційних місцях N-глікозилювання gp 120 – PNGSs (potential N-linked glycosylation sites) вірусного навантаження чутливості до нейтралізуючих АТ Великі вуглеводні ланцюги, зв’язані з gp 120, можуть екранувати ділянки зв’язування з АТ. * - Wood, N. , Bhattacharya, T. , Keele, B. , Giorgi, E. , Liu, M. , Gaschen, B. , Daniels, M. , Ferrari, G. , Haynes, B. , Mc. Michael, A. , Shaw, G. , Hahn, B. , Korber, B. , and Seoighe, C. (2009). "HIV evolution in early infection: selection pressures, patterns of insertion and deletion, and the impact of APOBEC". PLOS Pathogens 5: 1– 16.
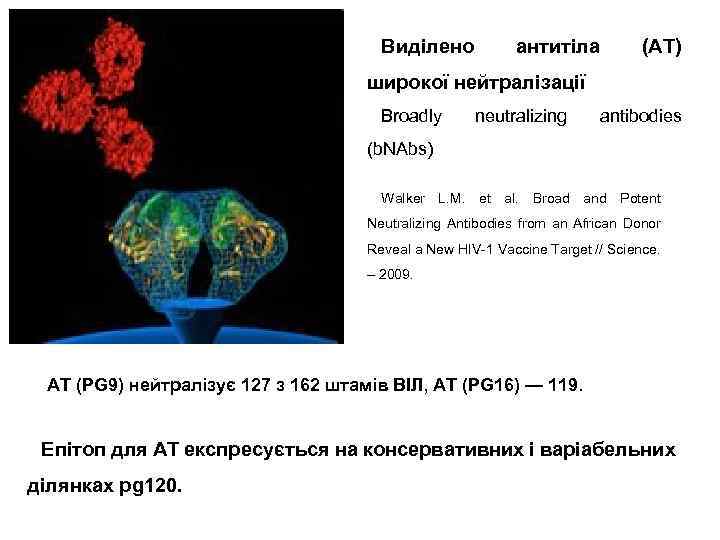 Виділено антитіла (АТ) широкої нейтралізації Broadly neutralizing antibodies (b. NAbs) Walker L. M. et al. Broad and Potent Neutralizing Antibodies from an African Donor Reveal a New HIV-1 Vaccine Target // Science. – 2009. АТ (PG 9) нейтралізує 127 з 162 штамів ВІЛ, АТ (PG 16) — 119. Епітоп для АТ експресується на консервативних і варіабельних ділянках pg 120.
Виділено антитіла (АТ) широкої нейтралізації Broadly neutralizing antibodies (b. NAbs) Walker L. M. et al. Broad and Potent Neutralizing Antibodies from an African Donor Reveal a New HIV-1 Vaccine Target // Science. – 2009. АТ (PG 9) нейтралізує 127 з 162 штамів ВІЛ, АТ (PG 16) — 119. Епітоп для АТ експресується на консервативних і варіабельних ділянках pg 120.
 Консервативна ділянка gp 120, яка бере участь у зв’язуванні з CD 4 - мішень для дії АТ широкої нейтралізації. Нова вакцина*: Ig. A з плазми і слини людини розщеплювали gp 120 втрачав здатність зв’язуватися з лімфоцитами * - Planque, S. , Mitsuda, Y. , Taguchi, H. , et al. (2007). "Characterization of gp 120 Hydrolysis by Ig. A Antibodies from Humans without HIV Infection". AIDS Research and Human Retroviruses 23 (12): 1541– 1554.
Консервативна ділянка gp 120, яка бере участь у зв’язуванні з CD 4 - мішень для дії АТ широкої нейтралізації. Нова вакцина*: Ig. A з плазми і слини людини розщеплювали gp 120 втрачав здатність зв’язуватися з лімфоцитами * - Planque, S. , Mitsuda, Y. , Taguchi, H. , et al. (2007). "Characterization of gp 120 Hydrolysis by Ig. A Antibodies from Humans without HIV Infection". AIDS Research and Human Retroviruses 23 (12): 1541– 1554.
 Ферменти ВІЛ зворотна транскриптаза (р66) - складається з двох субодиниць. Має 2 ферментативні активності: - ДНК-полімеразну - синтезує дволанцюгову ДНК, комплементарну вірусній РНК; -рибонуклеазну - розщеплює вихідну РНК. протеаза (р22) - бере участь у “нарізанні” попередників вірусних білків при дозріванні нової вірусної частки; інтеграза (р34) або ендонуклеаза - здійснює інтеграцію вірусної ДНК у геном клітини-хазяїна з утворенням провірусу.
Ферменти ВІЛ зворотна транскриптаза (р66) - складається з двох субодиниць. Має 2 ферментативні активності: - ДНК-полімеразну - синтезує дволанцюгову ДНК, комплементарну вірусній РНК; -рибонуклеазну - розщеплює вихідну РНК. протеаза (р22) - бере участь у “нарізанні” попередників вірусних білків при дозріванні нової вірусної частки; інтеграза (р34) або ендонуклеаза - здійснює інтеграцію вірусної ДНК у геном клітини-хазяїна з утворенням провірусу.
 Структуру інтегрази ВІЛ вченим не вдавалося змоделювати упродовж більш ніж 20 років (ілюстрація Peter Cherepanov et al. /Nature)
Структуру інтегрази ВІЛ вченим не вдавалося змоделювати упродовж більш ніж 20 років (ілюстрація Peter Cherepanov et al. /Nature)
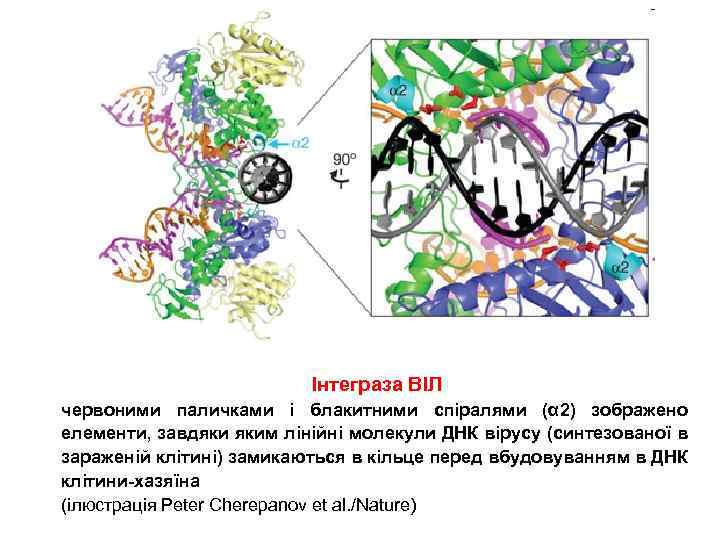 Інтеграза ВІЛ червоними паличками і блакитними спіралями (α 2) зображено елементи, завдяки яким лінійні молекули ДНК вірусу (синтезованої в зараженій клітині) замикаються в кільце перед вбудовуванням в ДНК клітини-хазяїна (ілюстрація Peter Cherepanov et al. /Nature)
Інтеграза ВІЛ червоними паличками і блакитними спіралями (α 2) зображено елементи, завдяки яким лінійні молекули ДНК вірусу (синтезованої в зараженій клітині) замикаються в кільце перед вбудовуванням в ДНК клітини-хазяїна (ілюстрація Peter Cherepanov et al. /Nature)
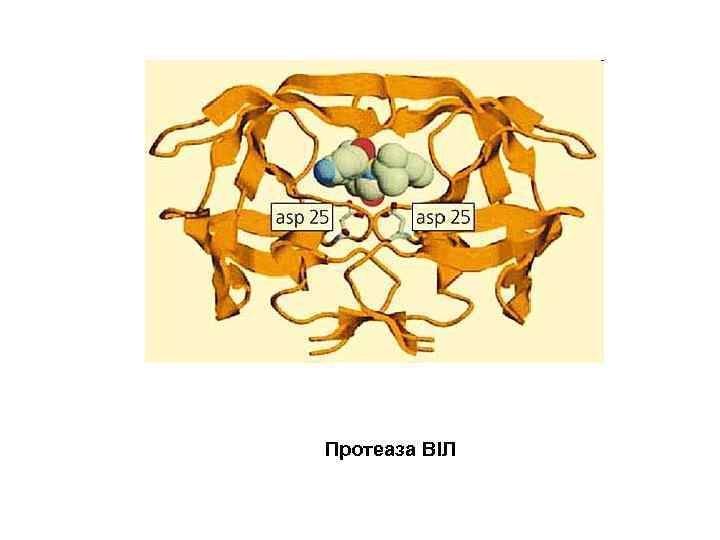 Протеаза ВІЛ
Протеаза ВІЛ
 Життєвий цикл ВІЛ
Життєвий цикл ВІЛ
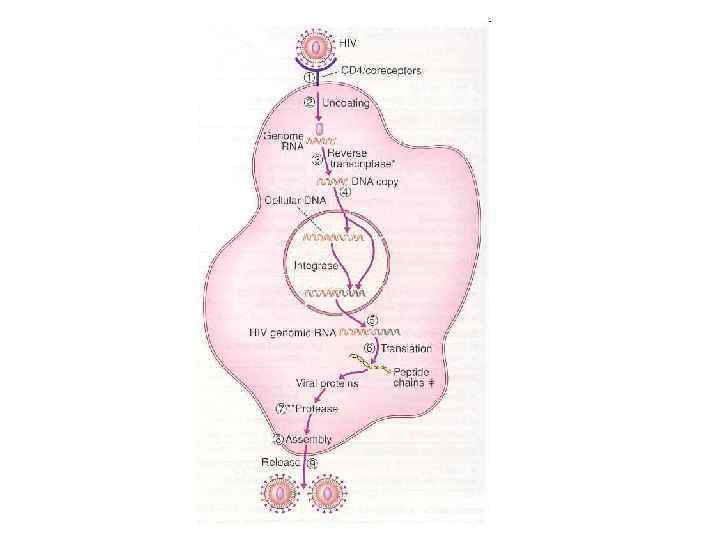
 Відбиток поверхні клітини, зараженої ВІЛ мікрофотографія (х 40 000) Для отримання препарату клітину зневоднюють, заморожують, наносять на її поверхню платину і вуглець. Очищають кислотою, промивають і досліджують в електронному мікроскопі.
Відбиток поверхні клітини, зараженої ВІЛ мікрофотографія (х 40 000) Для отримання препарату клітину зневоднюють, заморожують, наносять на її поверхню платину і вуглець. Очищають кислотою, промивають і досліджують в електронному мікроскопі.
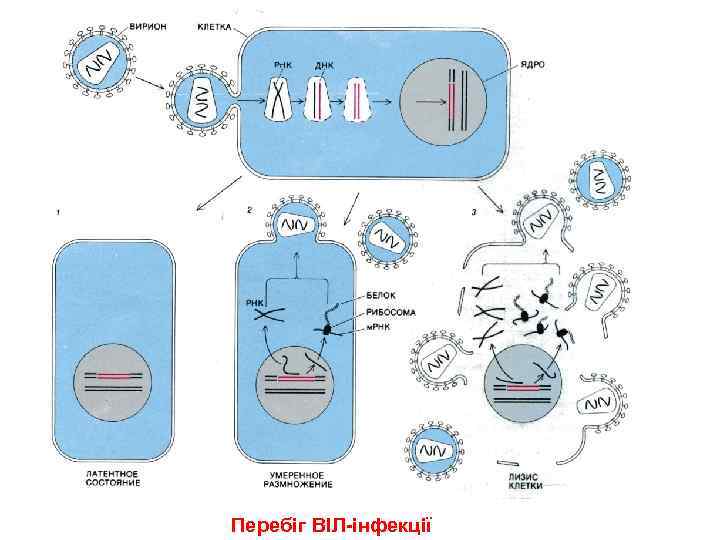 Перебіг ВІЛ-інфекції
Перебіг ВІЛ-інфекції
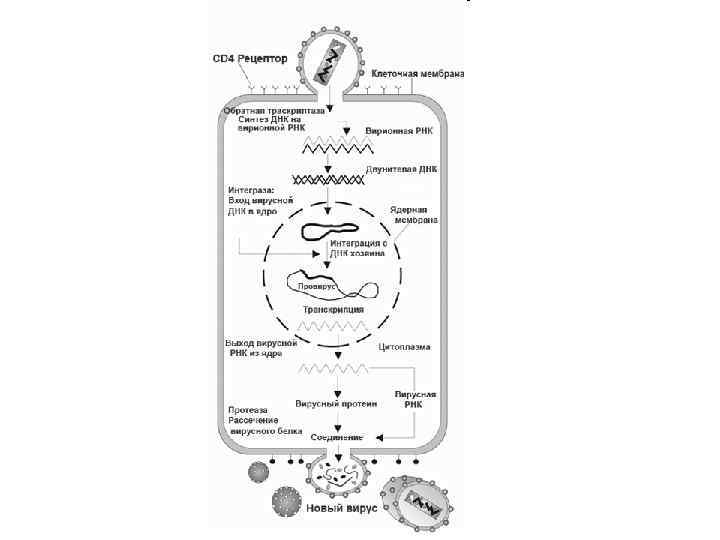
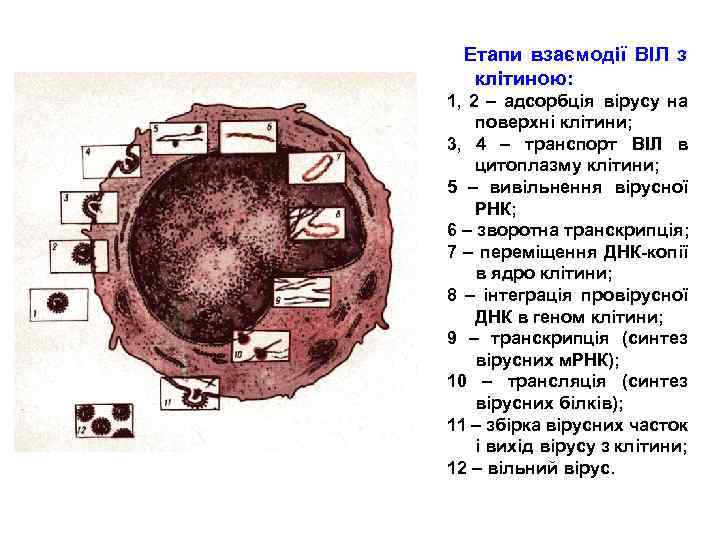 Етапи взаємодії ВІЛ з клітиною: 1, 2 – адсорбція вірусу на поверхні клітини; 3, 4 – транспорт ВІЛ в цитоплазму клітини; 5 – вивільнення вірусної РНК; 6 – зворотна транскрипція; 7 – переміщення ДНК-копії в ядро клітини; 8 – інтеграція провірусної ДНК в геном клітини; 9 – транскрипція (синтез вірусних м. РНК); 10 – трансляція (синтез вірусних білків); 11 – збірка вірусних часток і вихід вірусу з клітини; 12 – вільний вірус.
Етапи взаємодії ВІЛ з клітиною: 1, 2 – адсорбція вірусу на поверхні клітини; 3, 4 – транспорт ВІЛ в цитоплазму клітини; 5 – вивільнення вірусної РНК; 6 – зворотна транскрипція; 7 – переміщення ДНК-копії в ядро клітини; 8 – інтеграція провірусної ДНК в геном клітини; 9 – транскрипція (синтез вірусних м. РНК); 10 – трансляція (синтез вірусних білків); 11 – збірка вірусних часток і вихід вірусу з клітини; 12 – вільний вірус.
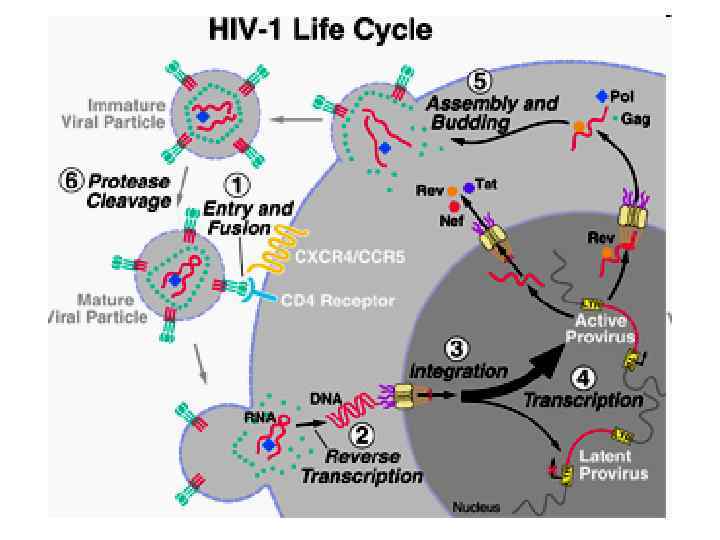
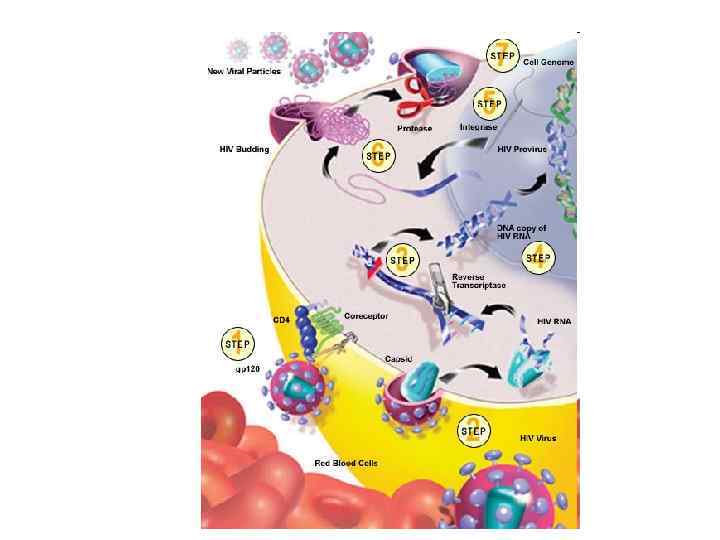
 Життєвий цикл ВІЛ 1. Вірусна частка приєднується до поверхні клітини. Глікопротеїн gp 120 зв’язується з CD 4 -рецептором і CCR 5/CXCR 4 -корецептором на Т-клітині. 2. Оболонка вірусу і мембрана клітини зливаються, серцевина віріону (білки та РНК) проникає в цитоплазму клітини (uncoated virus). 3. Зворотна транскриптаза (знаходиться в серцевині) синтезує одноланцюгову ДНК, комплементарну вірусній РНК. Після розщеплення вірусної РНК синтезується другий ланцюг ДНК. 4. Дволанцюгова вірусна ДНК (провірус), за сприяння інтегрази, проникає в ядро клітини і вбудовується в хромосомну ДНК. Далі може бути літична або прихована (латентна) фаза. Це залежить від вірусних білків або клітинних факторів. 5. Коли провірус активується, за допомогою клітинного механізму транскрипції утворюються м. РНК (РНК-копії провірусу). 6. З м. РНК на рибосомах клітини синтезуються вірусні білки і модифікуються за участю вірусних протеаз. З білків і РНК-копій формуються нові вірусні частки, що залишають клітину, відбруньковуючись від її поверхні. 7. Якщо реплікація вірусу дуже інтенсивна, відбувається лізис клітини, вона розривається і гине.
Життєвий цикл ВІЛ 1. Вірусна частка приєднується до поверхні клітини. Глікопротеїн gp 120 зв’язується з CD 4 -рецептором і CCR 5/CXCR 4 -корецептором на Т-клітині. 2. Оболонка вірусу і мембрана клітини зливаються, серцевина віріону (білки та РНК) проникає в цитоплазму клітини (uncoated virus). 3. Зворотна транскриптаза (знаходиться в серцевині) синтезує одноланцюгову ДНК, комплементарну вірусній РНК. Після розщеплення вірусної РНК синтезується другий ланцюг ДНК. 4. Дволанцюгова вірусна ДНК (провірус), за сприяння інтегрази, проникає в ядро клітини і вбудовується в хромосомну ДНК. Далі може бути літична або прихована (латентна) фаза. Це залежить від вірусних білків або клітинних факторів. 5. Коли провірус активується, за допомогою клітинного механізму транскрипції утворюються м. РНК (РНК-копії провірусу). 6. З м. РНК на рибосомах клітини синтезуються вірусні білки і модифікуються за участю вірусних протеаз. З білків і РНК-копій формуються нові вірусні частки, що залишають клітину, відбруньковуючись від її поверхні. 7. Якщо реплікація вірусу дуже інтенсивна, відбувається лізис клітини, вона розривається і гине.
 Події у цитоплазмі клітини 1. Депротеїнізація нуклеокапсиду і вивільнення геномної РНК ВІЛ. Див. слайд англ. Комплекс зворотної транскрипції: • • • 2 молекули РНК ВІЛ т. РНКліз 2 молекули зворотної транскриптази та інтегрази білок Vpr ВІЛ матриксні та нуклеокапсидні білки ВІЛ. Асоційований з актиновими мікрофібрилами клітини. Стабілізується білком Vif ВІЛ.
Події у цитоплазмі клітини 1. Депротеїнізація нуклеокапсиду і вивільнення геномної РНК ВІЛ. Див. слайд англ. Комплекс зворотної транскрипції: • • • 2 молекули РНК ВІЛ т. РНКліз 2 молекули зворотної транскриптази та інтегрази білок Vpr ВІЛ матриксні та нуклеокапсидні білки ВІЛ. Асоційований з актиновими мікрофібрилами клітини. Стабілізується білком Vif ВІЛ.
 2. Утворення комплексу передінтеграції: • дволанцюгова к. ДНК ВІЛ • інтеграза • матриксний білок • Vpr в комплексі з клітинним білком (HMGI). Комплекс переміщується до ядра.
2. Утворення комплексу передінтеграції: • дволанцюгова к. ДНК ВІЛ • інтеграза • матриксний білок • Vpr в комплексі з клітинним білком (HMGI). Комплекс переміщується до ядра.
 Проникнення в ядро Передінтеграційний комплекс вдвічі більший за розмір ядерної пори. Наслідок: вірусна ДНК повинна зазнати структурних змін. Проникненню в ядро передінтеграційного комплексу сприяють білки: • матриксний білок – має сигнал ядерної локалізації, подібний до клітинних імпортинів (компонентів класичного шляху ядерного імпорту); • Vpr – здатен ігнорувати імпортинову систему й ініціювати прямий контакт передінтеграційного комплексу з компонентами комплексу ядерної пори.
Проникнення в ядро Передінтеграційний комплекс вдвічі більший за розмір ядерної пори. Наслідок: вірусна ДНК повинна зазнати структурних змін. Проникненню в ядро передінтеграційного комплексу сприяють білки: • матриксний білок – має сигнал ядерної локалізації, подібний до клітинних імпортинів (компонентів класичного шляху ядерного імпорту); • Vpr – здатен ігнорувати імпортинову систему й ініціювати прямий контакт передінтеграційного комплексу з компонентами комплексу ядерної пори.
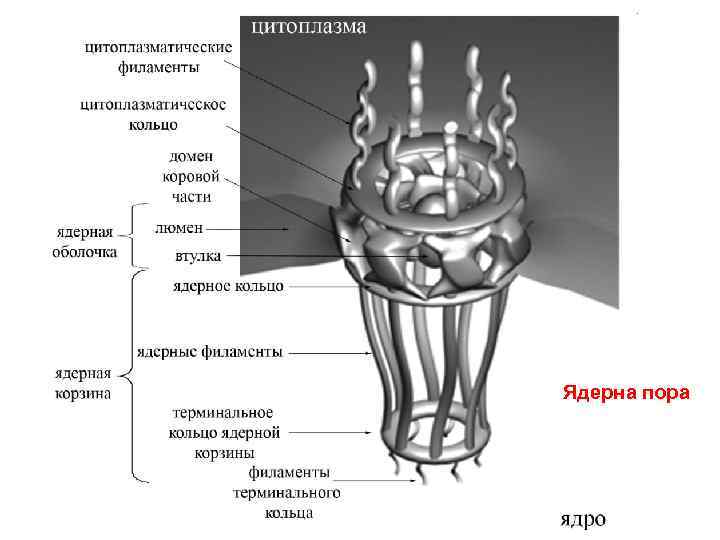 Ядерна пора
Ядерна пора
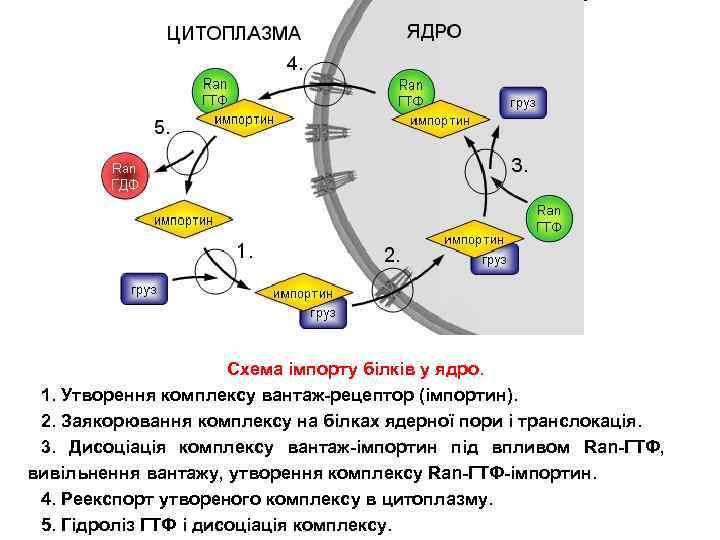 Схема імпорту білків у ядро. 1. Утворення комплексу вантаж-рецептор (імпортин). 2. Заякорювання комплексу на білках ядерної пори і транслокація. 3. Дисоціація комплексу вантаж-імпортин під впливом Ran-ГТФ, вивільнення вантажу, утворення комплексу Ran-ГТФ-імпортин. 4. Реекспорт утвореного комплексу в цитоплазму. 5. Гідроліз ГТФ і дисоціація комплексу.
Схема імпорту білків у ядро. 1. Утворення комплексу вантаж-рецептор (імпортин). 2. Заякорювання комплексу на білках ядерної пори і транслокація. 3. Дисоціація комплексу вантаж-імпортин під впливом Ran-ГТФ, вивільнення вантажу, утворення комплексу Ran-ГТФ-імпортин. 4. Реекспорт утвореного комплексу в цитоплазму. 5. Гідроліз ГТФ і дисоціація комплексу.
 Інтеграція За участю інтегрази, яка зв’язує кінці вірусної ДНК. Необхідні також: • клітинні білки HMGI • фактор автоінтеграції. Інтеграза виділяє з LTR на кінцях ДНК ВІЛ кінцеві нуклеотиди та каталізує реакцію вбудовування вірусної ДНК в хромосому клітини (сайт-специфічна інтеграція).
Інтеграція За участю інтегрази, яка зв’язує кінці вірусної ДНК. Необхідні також: • клітинні білки HMGI • фактор автоінтеграції. Інтеграза виділяє з LTR на кінцях ДНК ВІЛ кінцеві нуклеотиди та каталізує реакцію вбудовування вірусної ДНК в хромосому клітини (сайт-специфічна інтеграція).
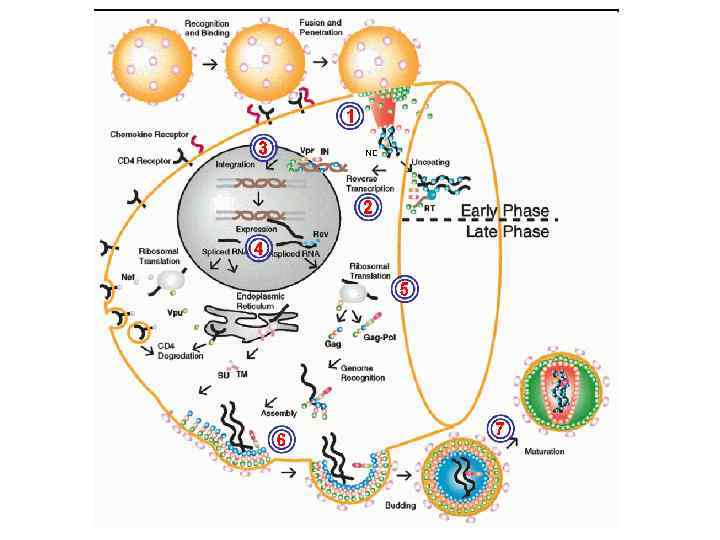
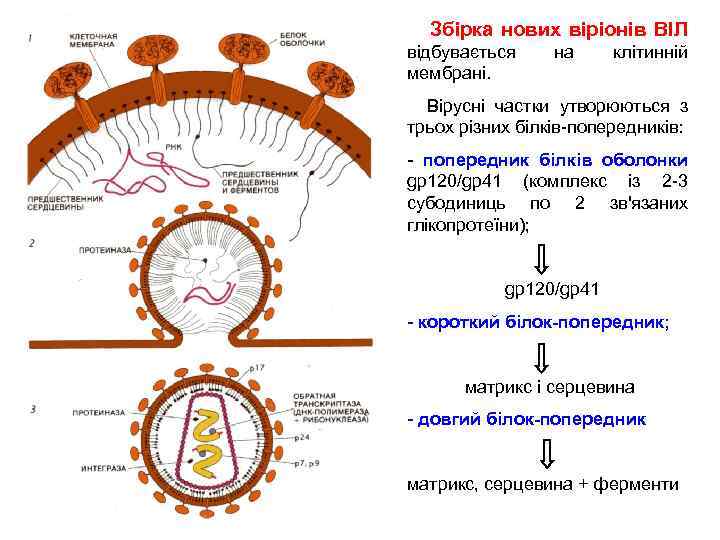 Збірка нових віріонів ВІЛ відбувається мембрані. на клітинній Вірусні частки утворюються з трьох різних білків-попередників: - попередник білків оболонки gp 120/gp 41 (комплекс із 2 -3 субодиниць по 2 зв'язаних глікопротеїни); gp 120/gp 41 - короткий білок-попередник; матрикс і серцевина - довгий білок-попередник матрикс, серцевина + ферменти
Збірка нових віріонів ВІЛ відбувається мембрані. на клітинній Вірусні частки утворюються з трьох різних білків-попередників: - попередник білків оболонки gp 120/gp 41 (комплекс із 2 -3 субодиниць по 2 зв'язаних глікопротеїни); gp 120/gp 41 - короткий білок-попередник; матрикс і серцевина - довгий білок-попередник матрикс, серцевина + ферменти
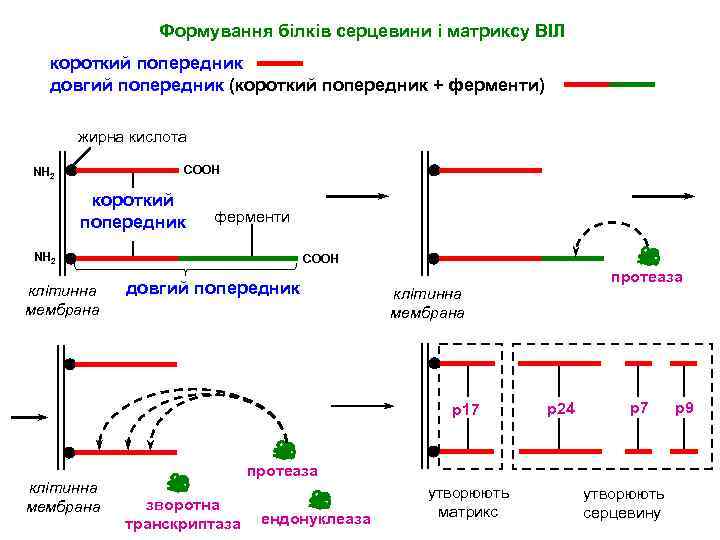 Формування білків серцевини і матриксу ВІЛ короткий попередник довгий попередник (короткий попередник + ферменти) жирна кислота СООН NH 2 короткий попередник ферменти NH 2 клітинна мембрана СООН довгий попередник клітинна мембрана р17 клітинна мембрана протеаза р24 р7 протеаза зворотна транскриптаза ендонуклеаза утворюють матрикс утворюють серцевину р9
Формування білків серцевини і матриксу ВІЛ короткий попередник довгий попередник (короткий попередник + ферменти) жирна кислота СООН NH 2 короткий попередник ферменти NH 2 клітинна мембрана СООН довгий попередник клітинна мембрана р17 клітинна мембрана протеаза р24 р7 протеаза зворотна транскриптаза ендонуклеаза утворюють матрикс утворюють серцевину р9
 Формування віріонів ВІЛ 1. У процесі агрегації вірусних білків на клітинній мембрані вона випинається. 2. Короткий білок-попередник втягує в щойно сформований віріон два ланцюги вірусної РНК. 3. Від довгого білка-попередника відрізається протеаза, що завершує формування віріону: вона відщеплює від довгого попередника ще молекули протеази, зворотну транскриптазу та ендорибонуклеазу. 4. Протеаза розрізає кожний з попередників на чотири частини. Одна частина (р17) залишається зв'язаною з клітинною мембраною, що оточує віріон, а три (р24, р7 і р9) утворюють кулеподібну серцевину. 5. У клітинну мембрану вбудовуються білки оболонки gp 41 і gp 120 незалежно від серцевинних (корових, від англ. core — серцевина) білків. 6. Віріон відбруньковується від клітини хазяїна.
Формування віріонів ВІЛ 1. У процесі агрегації вірусних білків на клітинній мембрані вона випинається. 2. Короткий білок-попередник втягує в щойно сформований віріон два ланцюги вірусної РНК. 3. Від довгого білка-попередника відрізається протеаза, що завершує формування віріону: вона відщеплює від довгого попередника ще молекули протеази, зворотну транскриптазу та ендорибонуклеазу. 4. Протеаза розрізає кожний з попередників на чотири частини. Одна частина (р17) залишається зв'язаною з клітинною мембраною, що оточує віріон, а три (р24, р7 і р9) утворюють кулеподібну серцевину. 5. У клітинну мембрану вбудовуються білки оболонки gp 41 і gp 120 незалежно від серцевинних (корових, від англ. core — серцевина) білків. 6. Віріон відбруньковується від клітини хазяїна.
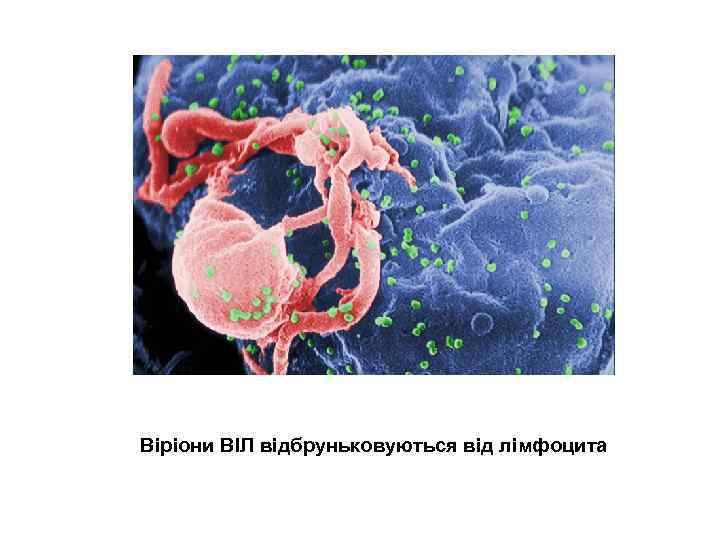 Віріони ВІЛ відбруньковуються від лімфоцита
Віріони ВІЛ відбруньковуються від лімфоцита
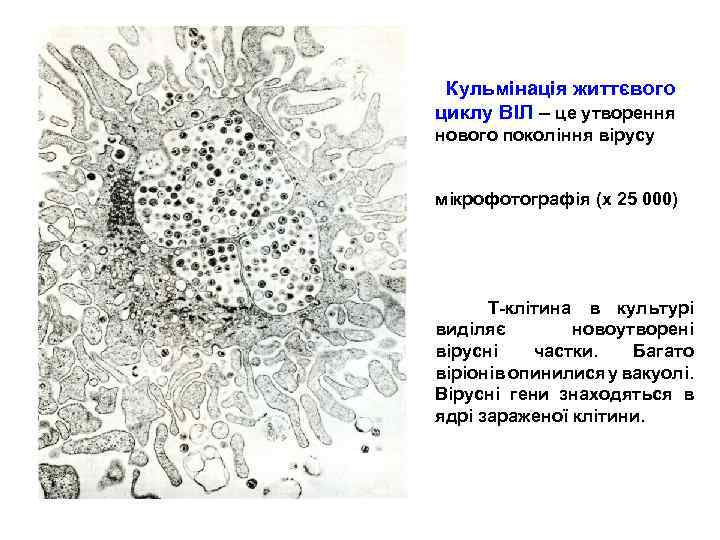 Кульмінація життєвого циклу ВІЛ – це утворення нового покоління вірусу мікрофотографія (х 25 000) Т-клітина в культурі виділяє новоутворені вірусні частки. Багато віріонів опинилися у вакуолі. Вірусні гени знаходяться в ядрі зараженої клітини.
Кульмінація життєвого циклу ВІЛ – це утворення нового покоління вірусу мікрофотографія (х 25 000) Т-клітина в культурі виділяє новоутворені вірусні частки. Багато віріонів опинилися у вакуолі. Вірусні гени знаходяться в ядрі зараженої клітини.
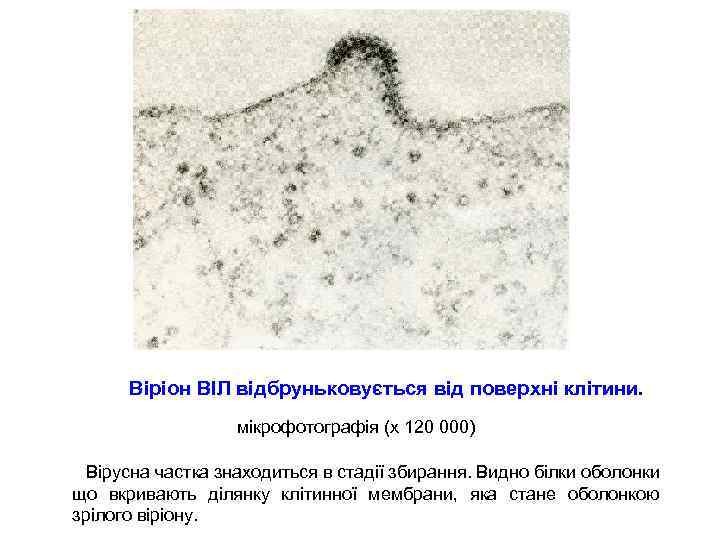 Віріон ВІЛ відбруньковується від поверхні клітини. мікрофотографія (х 120 000) Вірусна частка знаходиться в стадії збирання. Видно білки оболонки що вкривають ділянку клітинної мембрани, яка стане оболонкою зрілого віріону.
Віріон ВІЛ відбруньковується від поверхні клітини. мікрофотографія (х 120 000) Вірусна частка знаходиться в стадії збирання. Видно білки оболонки що вкривають ділянку клітинної мембрани, яка стане оболонкою зрілого віріону.
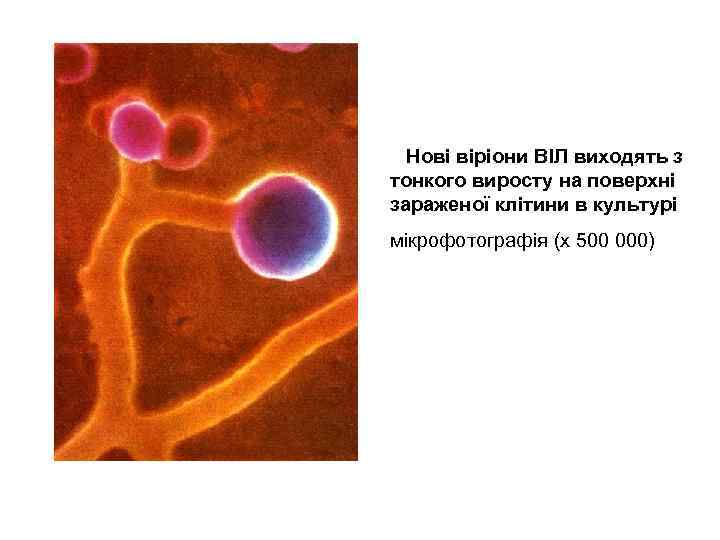 Нові віріони ВІЛ виходять з тонкого виросту на поверхні зараженої клітини в культурі мікрофотографія (х 500 000)
Нові віріони ВІЛ виходять з тонкого виросту на поверхні зараженої клітини в культурі мікрофотографія (х 500 000)
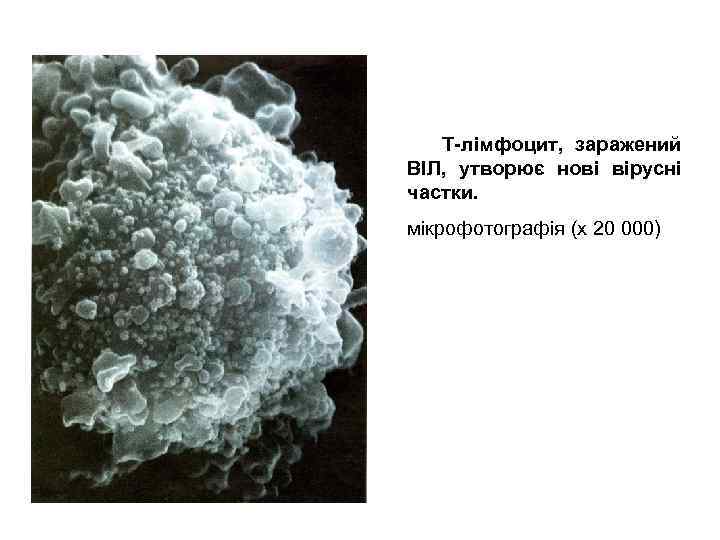 Т-лімфоцит, заражений ВІЛ, утворює нові вірусні частки. мікрофотографія (х 20 000)
Т-лімфоцит, заражений ВІЛ, утворює нові вірусні частки. мікрофотографія (х 20 000)
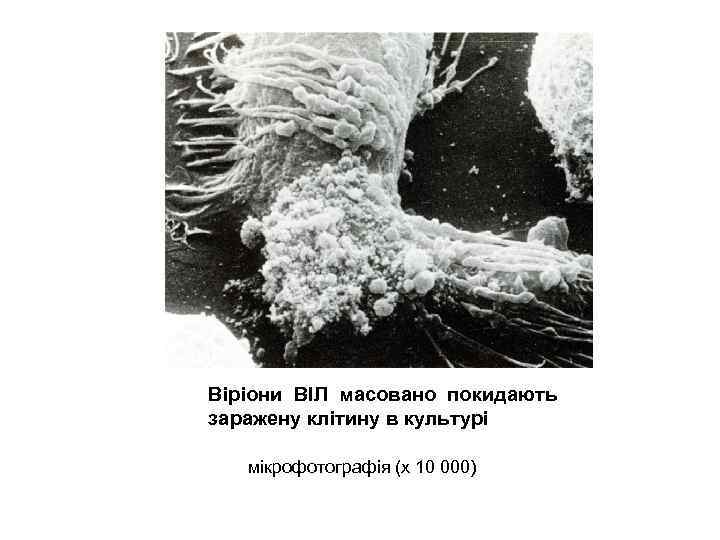 Віріони ВІЛ масовано покидають заражену клітину в культурі мікрофотографія (х 10 000)
Віріони ВІЛ масовано покидають заражену клітину в культурі мікрофотографія (х 10 000)
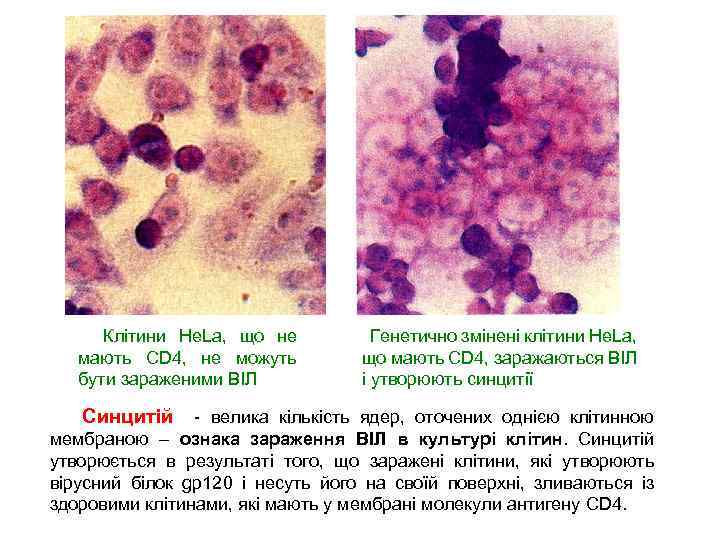 Клітини He. La, що не мають CD 4, не можуть бути зараженими ВІЛ Генетично змінені клітини He. La, що мають CD 4, заражаються ВІЛ і утворюють синцитії Синцитій - велика кількість ядер, оточених однією клітинною мембраною – ознака зараження ВІЛ в культурі клітин. Синцитій утворюється в результаті того, що заражені клітини, які утворюють вірусний білок gp 120 і несуть його на своїй поверхні, зливаються із здоровими клітинами, які мають у мембрані молекули антигену CD 4.
Клітини He. La, що не мають CD 4, не можуть бути зараженими ВІЛ Генетично змінені клітини He. La, що мають CD 4, заражаються ВІЛ і утворюють синцитії Синцитій - велика кількість ядер, оточених однією клітинною мембраною – ознака зараження ВІЛ в культурі клітин. Синцитій утворюється в результаті того, що заражені клітини, які утворюють вірусний білок gp 120 і несуть його на своїй поверхні, зливаються із здоровими клітинами, які мають у мембрані молекули антигену CD 4.
 ВЗАЄМОДІЯ ВІЛ З КЛІТИНОЮ
ВЗАЄМОДІЯ ВІЛ З КЛІТИНОЮ
 З’ясування механізму проникнення ВІЛ у клітину дає основу для розробки вакцин чи захисних препаратів, здатних блокувати дію вірусу на найбільш ранніх стадіях — ще до зараження першої клітини-хазяїна. Перший крок будь-якої вірусної інфекції — зв'язування вірусної частки з компонентом мембрани клітини, що заражається. Спектр клітин і тканин організму, що заражаються ВІЛ, відповідає розподілу CD 4 -рецепторів.
З’ясування механізму проникнення ВІЛ у клітину дає основу для розробки вакцин чи захисних препаратів, здатних блокувати дію вірусу на найбільш ранніх стадіях — ще до зараження першої клітини-хазяїна. Перший крок будь-якої вірусної інфекції — зв'язування вірусної частки з компонентом мембрани клітини, що заражається. Спектр клітин і тканин організму, що заражаються ВІЛ, відповідає розподілу CD 4 -рецепторів.
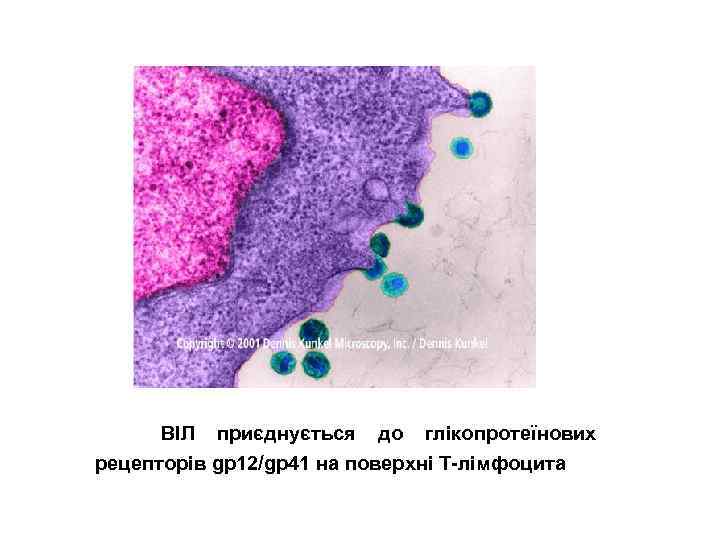 ВІЛ приєднується до глікопротеїнових рецепторів gp 12/gp 41 на поверхні Т-лімфоцита
ВІЛ приєднується до глікопротеїнових рецепторів gp 12/gp 41 на поверхні Т-лімфоцита
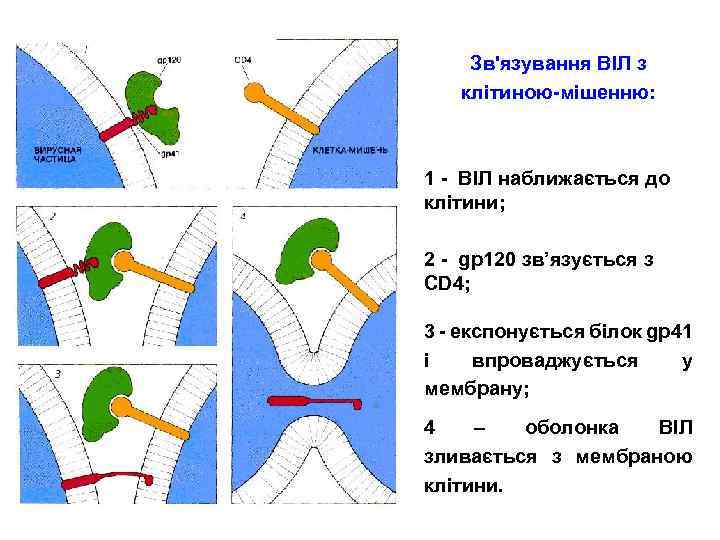 Зв'язування ВІЛ з клітиною-мішенню: 1 - ВІЛ наближається до клітини; 2 - gp 120 зв’язується з CD 4; 3 - експонується білок gp 41 і впроваджується у мембрану; 4 – оболонка ВІЛ зливається з мембраною клітини.
Зв'язування ВІЛ з клітиною-мішенню: 1 - ВІЛ наближається до клітини; 2 - gp 120 зв’язується з CD 4; 3 - експонується білок gp 41 і впроваджується у мембрану; 4 – оболонка ВІЛ зливається з мембраною клітини.
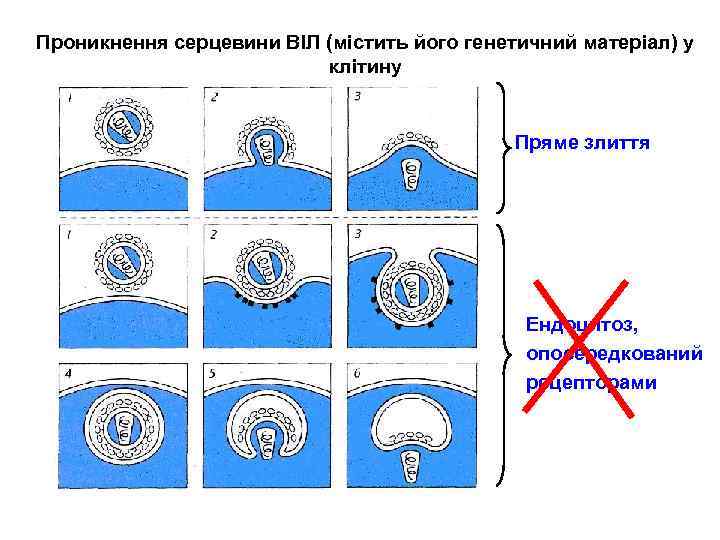 Проникнення серцевини ВІЛ (містить його генетичний матеріал) у клітину Пряме злиття Ендоцитоз, опосередкований рецепторами
Проникнення серцевини ВІЛ (містить його генетичний матеріал) у клітину Пряме злиття Ендоцитоз, опосередкований рецепторами
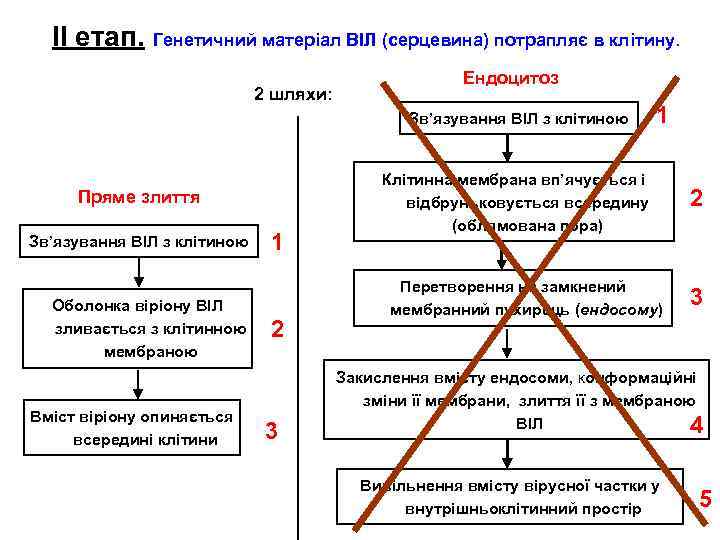 ІІ етап. Генетичний матеріал ВІЛ (серцевина) потрапляє в клітину. 2 шляхи: Ендоцитоз Зв’язування ВІЛ з клітиною Пряме злиття Зв’язування ВІЛ з клітиною Оболонка віріону ВІЛ зливається з клітинною мембраною Вміст віріону опиняється всередині клітини 1 2 3 1 Клітинна мембрана вп’ячується і відбруньковується всередину (облямована пора) Перетворення на замкнений мембранний пухирець (ендосому) 2 3 Закислення вмісту ендосоми, конформаційні зміни її мембрани, злиття її з мембраною ВІЛ 4 Вивільнення вмісту вірусної частки у внутрішньоклітинний простір 5
ІІ етап. Генетичний матеріал ВІЛ (серцевина) потрапляє в клітину. 2 шляхи: Ендоцитоз Зв’язування ВІЛ з клітиною Пряме злиття Зв’язування ВІЛ з клітиною Оболонка віріону ВІЛ зливається з клітинною мембраною Вміст віріону опиняється всередині клітини 1 2 3 1 Клітинна мембрана вп’ячується і відбруньковується всередину (облямована пора) Перетворення на замкнений мембранний пухирець (ендосому) 2 3 Закислення вмісту ендосоми, конформаційні зміни її мембрани, злиття її з мембраною ВІЛ 4 Вивільнення вмісту вірусної частки у внутрішньоклітинний простір 5
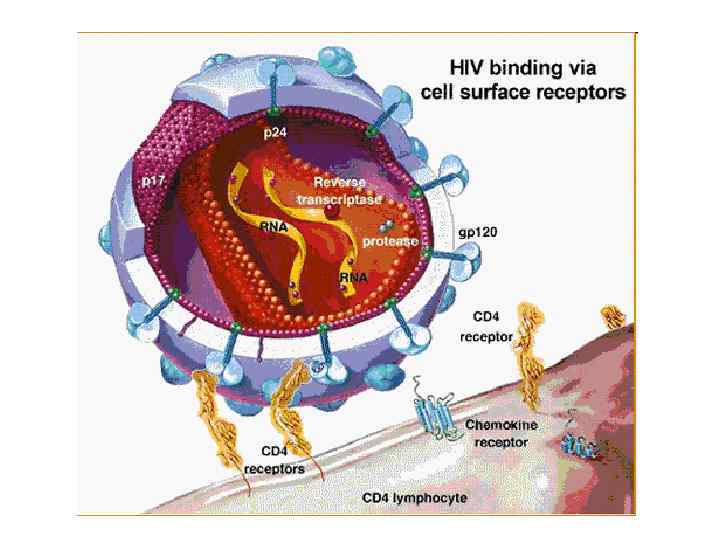
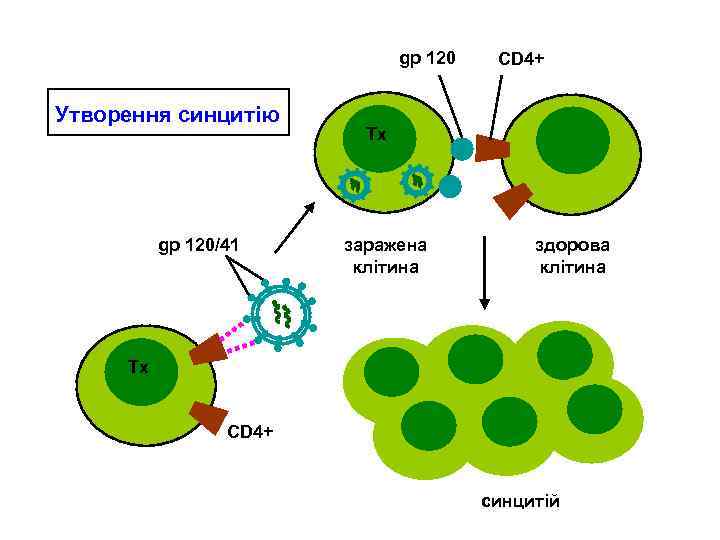 gp 120 Утворення синцитію gp 120/41 CD 4+ Тх заражена клітина Тх здорова клітина Тх CD 4+ синцитій
gp 120 Утворення синцитію gp 120/41 CD 4+ Тх заражена клітина Тх здорова клітина Тх CD 4+ синцитій
 Механізм утворення синцитію: Клітини, заражені ВІЛ, синтезують gp 120 і несуть його на своїй мембрані. Заражена клітина (має gp 120) зв’язується із здоровою клітиною (має CD 4+), вони зливаються з утворенням синцитію. Синцитій здатний далі зливатися із здоровими клітинами. Одна заражена клітина може в результаті приєднати до 50 клітин.
Механізм утворення синцитію: Клітини, заражені ВІЛ, синтезують gp 120 і несуть його на своїй мембрані. Заражена клітина (має gp 120) зв’язується із здоровою клітиною (має CD 4+), вони зливаються з утворенням синцитію. Синцитій здатний далі зливатися із здоровими клітинами. Одна заражена клітина може в результаті приєднати до 50 клітин.
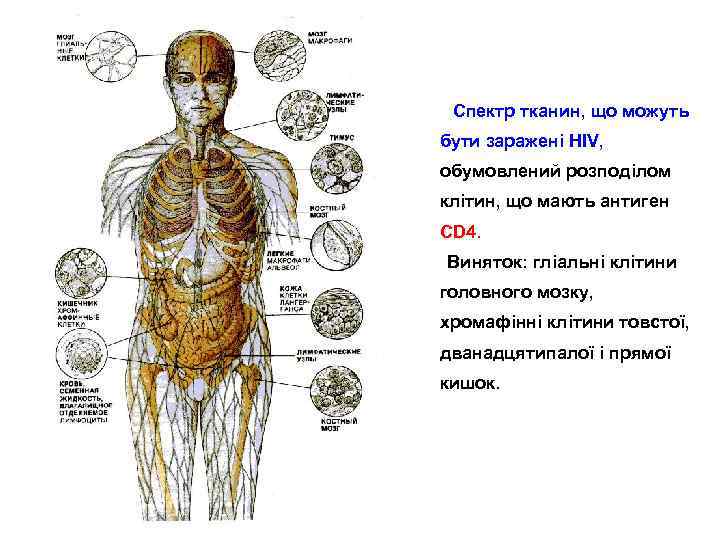 Спектр тканин, що можуть бути заражені HIV, обумовлений розподілом клітин, що мають антиген CD 4. Виняток: гліальні клітини головного мозку, хромафінні клітини товстої, дванадцятипалої і прямої кишок.
Спектр тканин, що можуть бути заражені HIV, обумовлений розподілом клітин, що мають антиген CD 4. Виняток: гліальні клітини головного мозку, хромафінні клітини товстої, дванадцятипалої і прямої кишок.
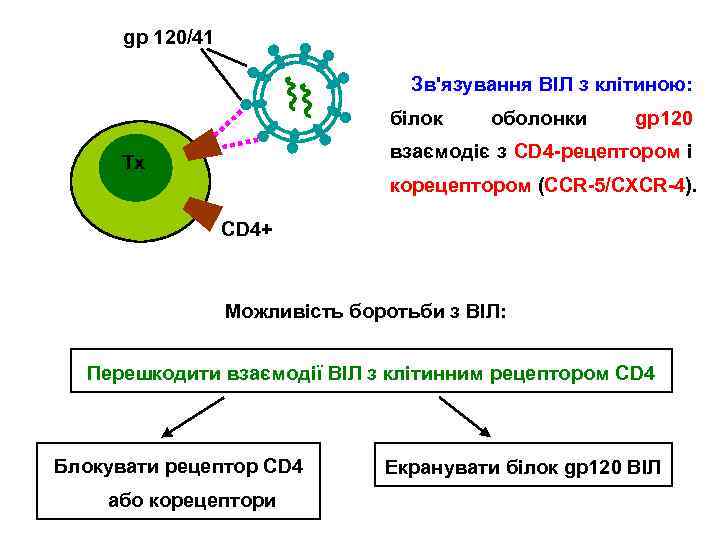 gp 120/41 Зв'язування ВІЛ з клітиною: білок оболонки gp 120 взаємодіє з CD 4 -рецептором і Тх корецептором (CCR-5/CXCR-4). CD 4+ Можливість боротьби з ВІЛ: Перешкодити взаємодії ВІЛ з клітинним рецептором CD 4 Блокувати рецептор CD 4 або корецептори Екранувати білок gp 120 ВІЛ
gp 120/41 Зв'язування ВІЛ з клітиною: білок оболонки gp 120 взаємодіє з CD 4 -рецептором і Тх корецептором (CCR-5/CXCR-4). CD 4+ Можливість боротьби з ВІЛ: Перешкодити взаємодії ВІЛ з клітинним рецептором CD 4 Блокувати рецептор CD 4 або корецептори Екранувати білок gp 120 ВІЛ
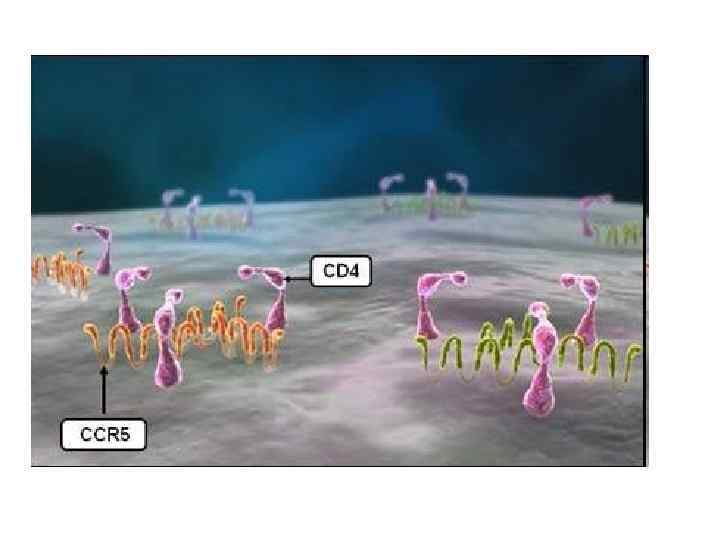
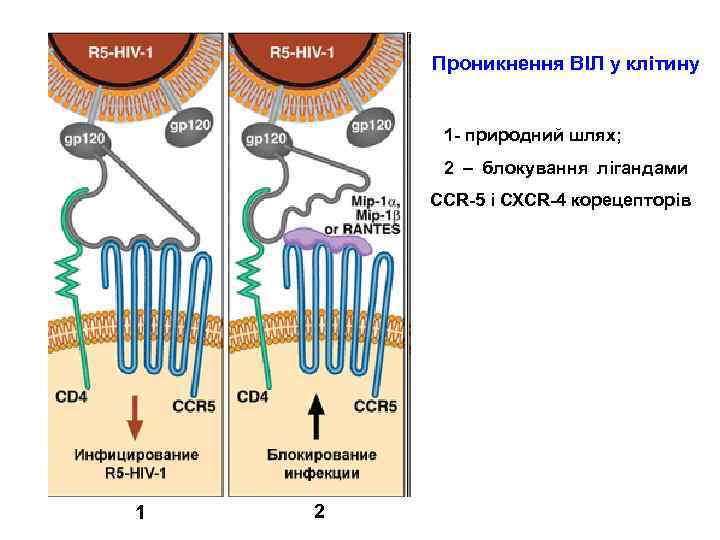 Проникнення ВІЛ у клітину 1 - природний шлях; 2 – блокування лігандами CCR-5 і CXCR-4 корецепторів 1 2
Проникнення ВІЛ у клітину 1 - природний шлях; 2 – блокування лігандами CCR-5 і CXCR-4 корецепторів 1 2
 Проникнення ВІЛ у клітину Забезпечується 2 рецепторами: CD 4 і CCR-5: 1. Адсорбція ВІЛ: Ш CD 4 необхідний для первинного закріплення, захоплює тример gp 120 ВІЛ, який змінює конформацію; Ш наближення і зв’язування хемокінового рецептору CCR-5 з gp 120 у комплексі CD 4 -ВІЛ; Ш зміна конформації gp 41, його експонування і проникнення в клітинну мембрану; 2. Злиття: утворення шпилькоподібних структур, що з’єднують суперкапсидну оболонку віріону та клітинну мембрану, злиття вірусних часток з мембраною, проникнення нуклеокапсиду в цитоплазму клітини (інфікування).
Проникнення ВІЛ у клітину Забезпечується 2 рецепторами: CD 4 і CCR-5: 1. Адсорбція ВІЛ: Ш CD 4 необхідний для первинного закріплення, захоплює тример gp 120 ВІЛ, який змінює конформацію; Ш наближення і зв’язування хемокінового рецептору CCR-5 з gp 120 у комплексі CD 4 -ВІЛ; Ш зміна конформації gp 41, його експонування і проникнення в клітинну мембрану; 2. Злиття: утворення шпилькоподібних структур, що з’єднують суперкапсидну оболонку віріону та клітинну мембрану, злиття вірусних часток з мембраною, проникнення нуклеокапсиду в цитоплазму клітини (інфікування).
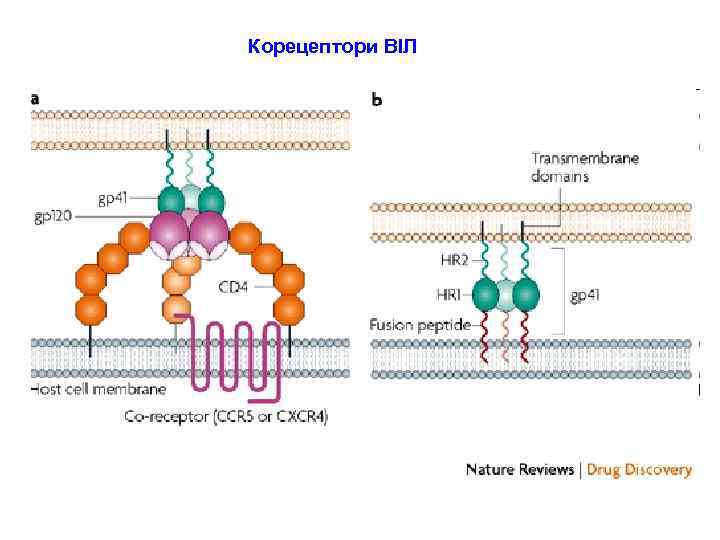 Корецептори ВІЛ
Корецептори ВІЛ
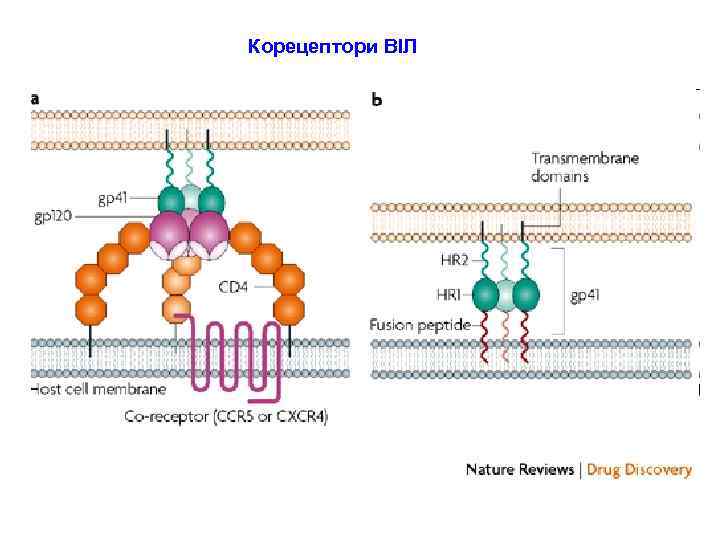 Корецептори ВІЛ
Корецептори ВІЛ
 Хемокінові рецептори (chemokine receptors) Ліганди – хемокіни (chemokines) або хемотактичні цитокіни (chemotactic cytokines) Здатні індукувати: üспрямований хемотаксис найближчих чутливих клітин; üІмунну відповід ь на інфекцію та запалення
Хемокінові рецептори (chemokine receptors) Ліганди – хемокіни (chemokines) або хемотактичні цитокіни (chemotactic cytokines) Здатні індукувати: üспрямований хемотаксис найближчих чутливих клітин; üІмунну відповід ь на інфекцію та запалення
 Хемокінові рецептори (chemokine receptors) Ліганди - chemokines (chemotactic cytokines) üability to induce directed chemotaxis in nearby responsive cells ücrucial for immune responses towards infection and inflammation
Хемокінові рецептори (chemokine receptors) Ліганди - chemokines (chemotactic cytokines) üability to induce directed chemotaxis in nearby responsive cells ücrucial for immune responses towards infection and inflammation
 β-хемокіни: RANTES (Regulated upon Activation, Normal T-cell Expressed, and Secreted) (CCL 5) Ø Викликає хемотаксис Т-клітин, еозинофілів та базофілів, Ø Активна роль у рекрутуванні лейкоцитів до вогни ща запалення; Ø Індукує проліферацію та активацію певних натуральних кілерів; Ø ВІЛ-супресивний фактор, що вивільнюється з CD 8+ -клітин. MIP (macrophage inflammatory proteins) - MIP-1α (CCL 3 ) і MIP-1β (CCL 4) Продукується макрофагами бактеріальними ендотксинами. після їх стимуляції
β-хемокіни: RANTES (Regulated upon Activation, Normal T-cell Expressed, and Secreted) (CCL 5) Ø Викликає хемотаксис Т-клітин, еозинофілів та базофілів, Ø Активна роль у рекрутуванні лейкоцитів до вогни ща запалення; Ø Індукує проліферацію та активацію певних натуральних кілерів; Ø ВІЛ-супресивний фактор, що вивільнюється з CD 8+ -клітин. MIP (macrophage inflammatory proteins) - MIP-1α (CCL 3 ) і MIP-1β (CCL 4) Продукується макрофагами бактеріальними ендотксинами. після їх стимуляції
 β chemokines: RANTES (Regulated upon Activation, Normal T-cell Expressed, and Secreted) (CCL 5) chemotactic for T cells, eosinophils, and basophils, and plays an active role in recruiting leukocytes into inflammatory sites induces the proliferation and activation of certain natural-killer (NK) cells HIV-suppressive factor released from CD 8+ T cells MIP (macrophage inflammatory proteins) - MIP-1α (CCL 3 ) і MIP-1β (CCL 4) major factors produced by macrophages after they are stimulated with bacterial endotoxins
β chemokines: RANTES (Regulated upon Activation, Normal T-cell Expressed, and Secreted) (CCL 5) chemotactic for T cells, eosinophils, and basophils, and plays an active role in recruiting leukocytes into inflammatory sites induces the proliferation and activation of certain natural-killer (NK) cells HIV-suppressive factor released from CD 8+ T cells MIP (macrophage inflammatory proteins) - MIP-1α (CCL 3 ) і MIP-1β (CCL 4) major factors produced by macrophages after they are stimulated with bacterial endotoxins
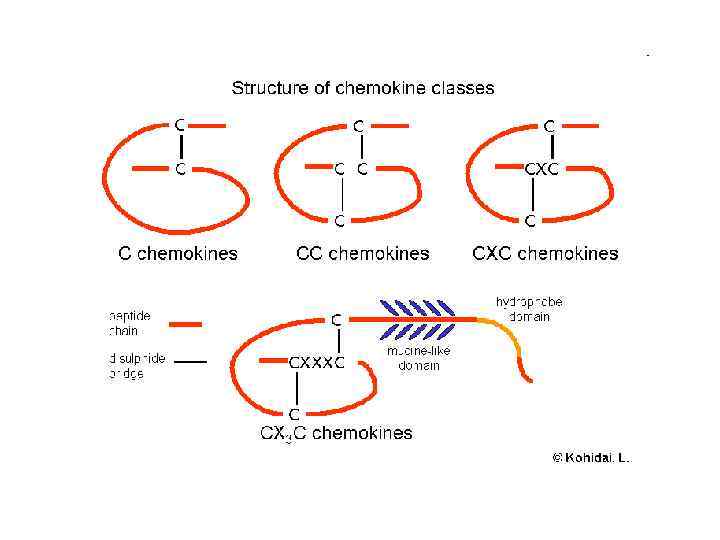
 19 різних хемокінових рецепторів Рецептори, зв’язані з G-білками, містять 7 трансмембранних доменів, згнаходяться на поверхні лейкоцитів. 4 родини (залежно від типу хемокінів, що зв’язуються) CXCR –зв’язуються з CXC хемокінами, CCR - зв’язуються з CCхемокінами, CX 3 CR 1 - зв’язуються з CX 3 C хемокінами (CX 3 CL 1), XCR 1 - зв’язуються з двома XC хемокінами (XCL 1 and XCL 2). Трансдукція сигналу – через фосфатидилінозитол (4, 5)- дифосфатну (PIP 2) систему Відповідь - хемотаксис, дегрануляція, вивільнення супероксид аніонів і зміни авідності молекул міжклітинної адгезії (інтегринів) у клітинах, що містять хемокінові рецептори
19 різних хемокінових рецепторів Рецептори, зв’язані з G-білками, містять 7 трансмембранних доменів, згнаходяться на поверхні лейкоцитів. 4 родини (залежно від типу хемокінів, що зв’язуються) CXCR –зв’язуються з CXC хемокінами, CCR - зв’язуються з CCхемокінами, CX 3 CR 1 - зв’язуються з CX 3 C хемокінами (CX 3 CL 1), XCR 1 - зв’язуються з двома XC хемокінами (XCL 1 and XCL 2). Трансдукція сигналу – через фосфатидилінозитол (4, 5)- дифосфатну (PIP 2) систему Відповідь - хемотаксис, дегрануляція, вивільнення супероксид аніонів і зміни авідності молекул міжклітинної адгезії (інтегринів) у клітинах, що містять хемокінові рецептори
 19 different chemokine receptors G protein-coupled receptors containing 7 transmembrane domains that are found on the surface of leukocytes 4 families depending on the type of chemokine they bind CXCR -bind the CXC chemokines, CCR - bind the CC chemokines, CX 3 CR 1 - binds the CX 3 C chemokine (CX 3 CL 1), XCR 1 - binds the two XC chemokines (XCL 1 and XCL 2). Signal transduction – via phosphatidylinositol (4, 5)-bisphosphate (PIP 2) system Responses - chemotaxis, degranulation, release of superoxide anions and changes in the avidity of cell adhesion molecules called integrins within the cell harbouring the chemokine receptor
19 different chemokine receptors G protein-coupled receptors containing 7 transmembrane domains that are found on the surface of leukocytes 4 families depending on the type of chemokine they bind CXCR -bind the CXC chemokines, CCR - bind the CC chemokines, CX 3 CR 1 - binds the CX 3 C chemokine (CX 3 CL 1), XCR 1 - binds the two XC chemokines (XCL 1 and XCL 2). Signal transduction – via phosphatidylinositol (4, 5)-bisphosphate (PIP 2) system Responses - chemotaxis, degranulation, release of superoxide anions and changes in the avidity of cell adhesion molecules called integrins within the cell harbouring the chemokine receptor
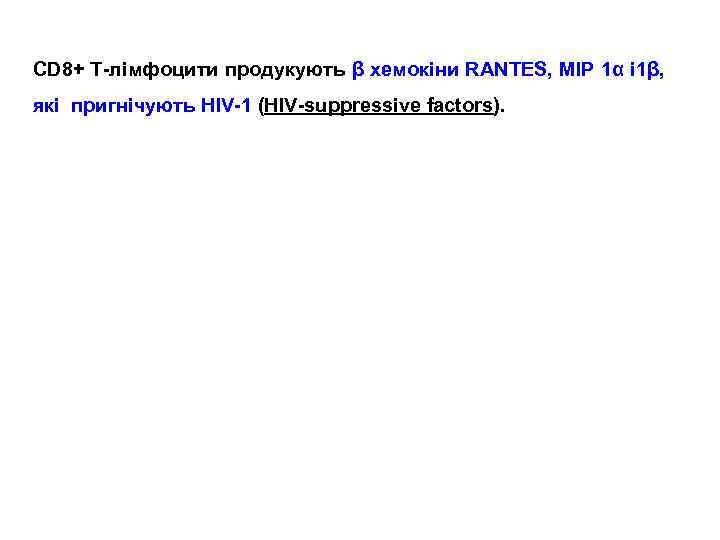 CD 8+ T-лімфоцити продукують β хемокіни RANTES, MIP 1α і 1β, які пригнічують HIV-1 (HIV-suppressive factors).
CD 8+ T-лімфоцити продукують β хемокіни RANTES, MIP 1α і 1β, які пригнічують HIV-1 (HIV-suppressive factors).
 Корецептори ВІЛ Взаємодія з gp 120 ВІЛ з хемокіновим рецептором запускає конформаційні зміни, що призводять до злиття оболонки вірусу та клітинної мембрани. CCR 5 - -хемокіновий рецептор, є корецептором штамів ВІЛ, що уражують макрофаги. -CXCR 4 - -хемокіновий рецептор, є корецептором штамів ВІЛ, що мають тропізм до Т-лімфоцитів. CXCR 4 -корецептор – експресується на мієлоїдних клітинах, Т- і В-клітинах, макрофагах, епітеліальних, ендотеліальних і дендритних клітинах. Різні варіанти ВІЛ використовують: v або CCR-5 – штам R 5 -HIV-1 (M-tropic) v або CXCR-4 - штам X 4 -HIV-1 (T-tropic) v обидва корецептори відразу - штам X 4 R 5 -HIV-1 або R 3 -HIV-1
Корецептори ВІЛ Взаємодія з gp 120 ВІЛ з хемокіновим рецептором запускає конформаційні зміни, що призводять до злиття оболонки вірусу та клітинної мембрани. CCR 5 - -хемокіновий рецептор, є корецептором штамів ВІЛ, що уражують макрофаги. -CXCR 4 - -хемокіновий рецептор, є корецептором штамів ВІЛ, що мають тропізм до Т-лімфоцитів. CXCR 4 -корецептор – експресується на мієлоїдних клітинах, Т- і В-клітинах, макрофагах, епітеліальних, ендотеліальних і дендритних клітинах. Різні варіанти ВІЛ використовують: v або CCR-5 – штам R 5 -HIV-1 (M-tropic) v або CXCR-4 - штам X 4 -HIV-1 (T-tropic) v обидва корецептори відразу - штам X 4 R 5 -HIV-1 або R 3 -HIV-1
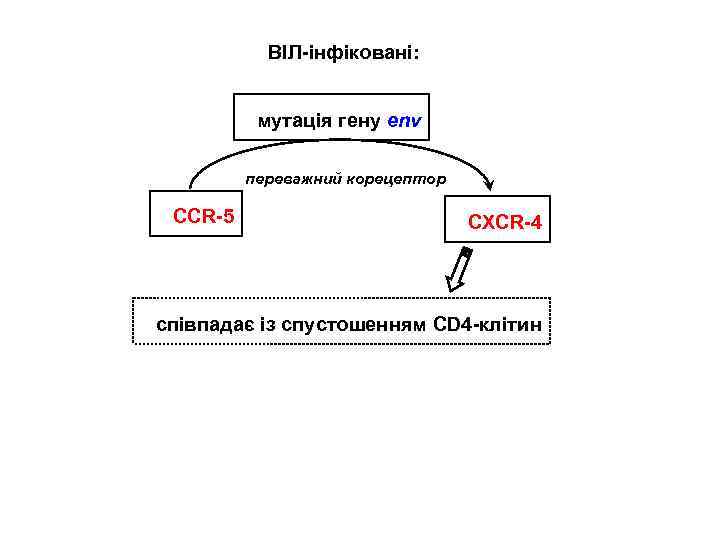 ВІЛ-інфіковані: мутація гену env переважний корецептор CCR-5 CXCR-4 співпадає із спустошенням CD 4 -клітин
ВІЛ-інфіковані: мутація гену env переважний корецептор CCR-5 CXCR-4 співпадає із спустошенням CD 4 -клітин
 Інігбування проникнення ВІЛ у клітину: 1. стеричний ефект – конкурентна блокада рецептора шляхом прямого зв’язування з ним ліганду; 2. інактивація рецептора після зв’язування хемокіну. Вивільнення хемокінів – рання реакція на інфікування ВІЛ. Дослідження показали: Високий рівень хемокінів (рецептор - CCR-5) пов’язаний з повільним прогресуванням ВІЛ-інфекції.
Інігбування проникнення ВІЛ у клітину: 1. стеричний ефект – конкурентна блокада рецептора шляхом прямого зв’язування з ним ліганду; 2. інактивація рецептора після зв’язування хемокіну. Вивільнення хемокінів – рання реакція на інфікування ВІЛ. Дослідження показали: Високий рівень хемокінів (рецептор - CCR-5) пов’язаний з повільним прогресуванням ВІЛ-інфекції.
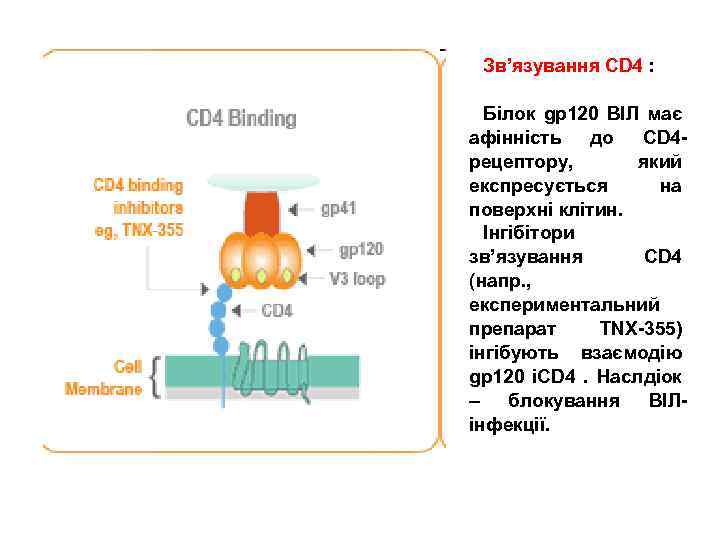 Зв’язування CD 4 : Білок gp 120 ВІЛ має афінність до CD 4 рецептору, який експресується на поверхні клітин. Інгібітори зв’язування CD 4 (напр. , експериментальний препарат TNX-355) інгібують взаємодію gp 120 іCD 4 . Наслдіок – блокування ВІЛінфекції.
Зв’язування CD 4 : Білок gp 120 ВІЛ має афінність до CD 4 рецептору, який експресується на поверхні клітин. Інгібітори зв’язування CD 4 (напр. , експериментальний препарат TNX-355) інгібують взаємодію gp 120 іCD 4 . Наслдіок – блокування ВІЛінфекції.
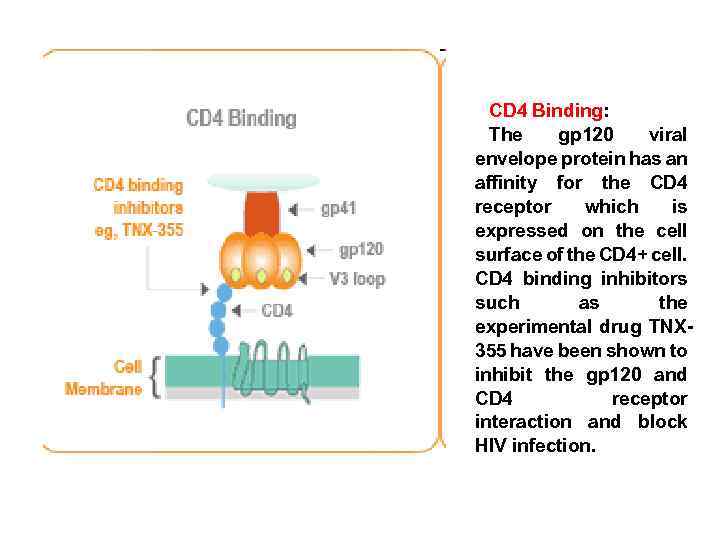 CD 4 Binding: The gp 120 viral envelope protein has an affinity for the CD 4 receptor which is expressed on the cell surface of the CD 4+ cell. CD 4 binding inhibitors such as the experimental drug TNX 355 have been shown to inhibit the gp 120 and CD 4 receptor interaction and block HIV infection.
CD 4 Binding: The gp 120 viral envelope protein has an affinity for the CD 4 receptor which is expressed on the cell surface of the CD 4+ cell. CD 4 binding inhibitors such as the experimental drug TNX 355 have been shown to inhibit the gp 120 and CD 4 receptor interaction and block HIV infection.
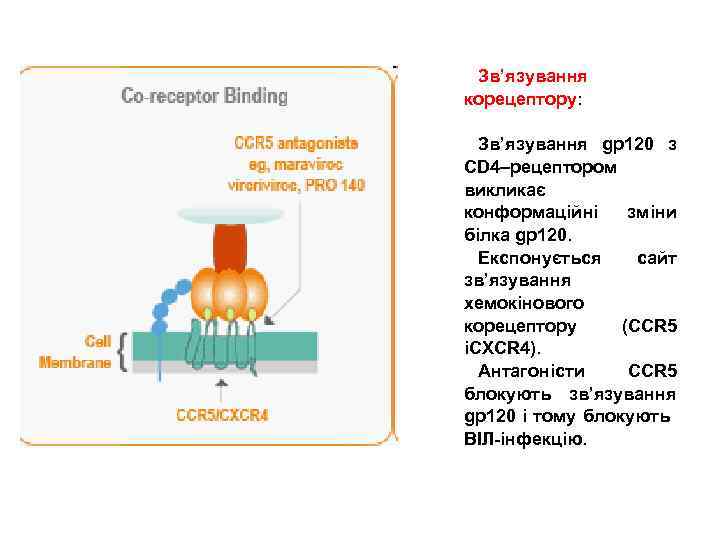 Зв’язування корецептору: Зв’язування gp 120 з CD 4–рецептором викликає конформаційні зміни білка gp 120. Експонується сайт зв’язування хемокінового корецептору (CCR 5 іCXCR 4). Антагоністи CCR 5 блокують зв’язування gp 120 і тому блокують ВІЛ-інфекцію.
Зв’язування корецептору: Зв’язування gp 120 з CD 4–рецептором викликає конформаційні зміни білка gp 120. Експонується сайт зв’язування хемокінового корецептору (CCR 5 іCXCR 4). Антагоністи CCR 5 блокують зв’язування gp 120 і тому блокують ВІЛ-інфекцію.
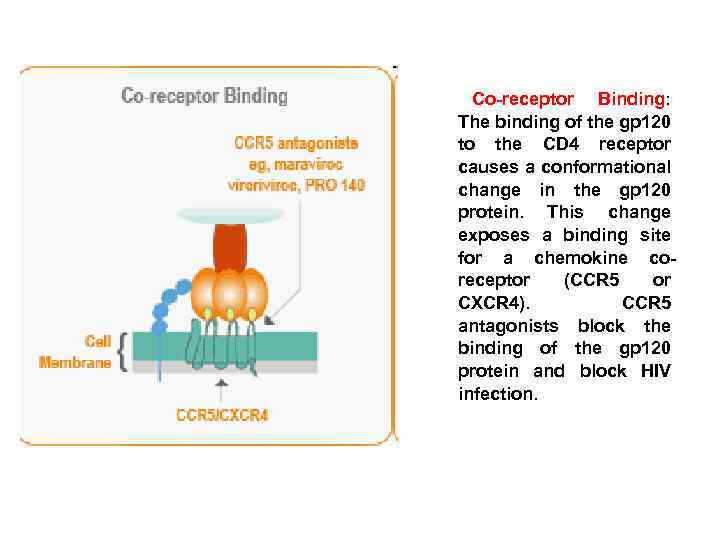 Co-receptor Binding: The binding of the gp 120 to the CD 4 receptor causes a conformational change in the gp 120 protein. This change exposes a binding site for a chemokine coreceptor (CCR 5 or CXCR 4). CCR 5 antagonists block the binding of the gp 120 protein and block HIV infection.
Co-receptor Binding: The binding of the gp 120 to the CD 4 receptor causes a conformational change in the gp 120 protein. This change exposes a binding site for a chemokine coreceptor (CCR 5 or CXCR 4). CCR 5 antagonists block the binding of the gp 120 protein and block HIV infection.
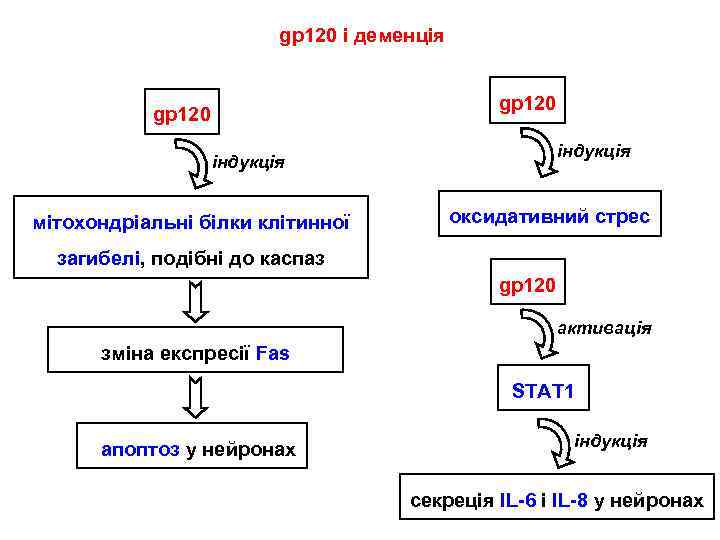 gp 120 і деменція gp 120 індукція мітохондріальні білки клітинної оксидативний стрес загибелі, подібні до каспаз gp 120 активація зміна експресії Fas STAT 1 апоптоз у нейронах індукція секреція IL-6 і IL-8 у нейронах
gp 120 і деменція gp 120 індукція мітохондріальні білки клітинної оксидативний стрес загибелі, подібні до каспаз gp 120 активація зміна експресії Fas STAT 1 апоптоз у нейронах індукція секреція IL-6 і IL-8 у нейронах
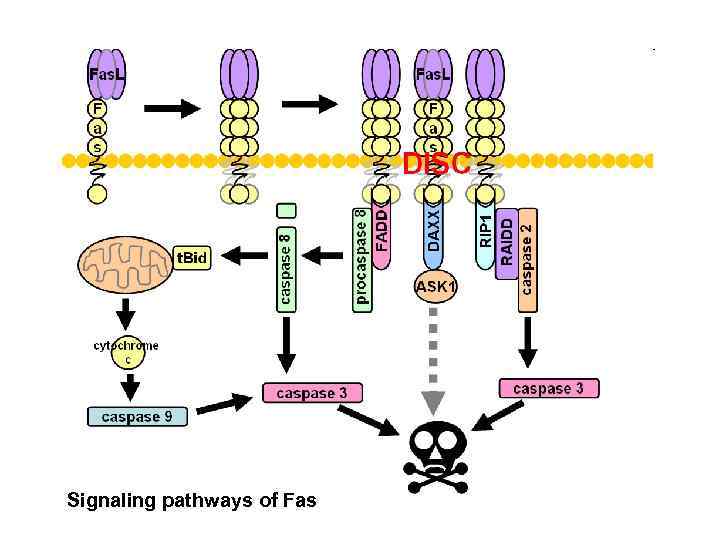 Signaling pathways of Fas
Signaling pathways of Fas
 Вплив gp 120 на імунокомпетентні клітини ь викликає дисбаланс у системі цитокінів; ь підвищує концентрацію Са, індукує синтез інозитолтрифосфату; ь інгібує мітогенну або антигенну активацію Т-клітин; ь змінює продукцію цитокінів шляхом активації субпопуляцій мононуклеарних клітин периферійної крові (PBMC); ь впливає на активність АГ-представляючих клітин; ь порушує цитотоксичність і хемотаксис у відповідь на АГ; ь стимулює поліклональну активацію В-клітин; ь посилює продукцію певних цитокінів (IL 6, TNF-alpha, IL 1 alpha and IL 1 -beta, IL 10 and IL 8).
Вплив gp 120 на імунокомпетентні клітини ь викликає дисбаланс у системі цитокінів; ь підвищує концентрацію Са, індукує синтез інозитолтрифосфату; ь інгібує мітогенну або антигенну активацію Т-клітин; ь змінює продукцію цитокінів шляхом активації субпопуляцій мононуклеарних клітин периферійної крові (PBMC); ь впливає на активність АГ-представляючих клітин; ь порушує цитотоксичність і хемотаксис у відповідь на АГ; ь стимулює поліклональну активацію В-клітин; ь посилює продукцію певних цитокінів (IL 6, TNF-alpha, IL 1 alpha and IL 1 -beta, IL 10 and IL 8).
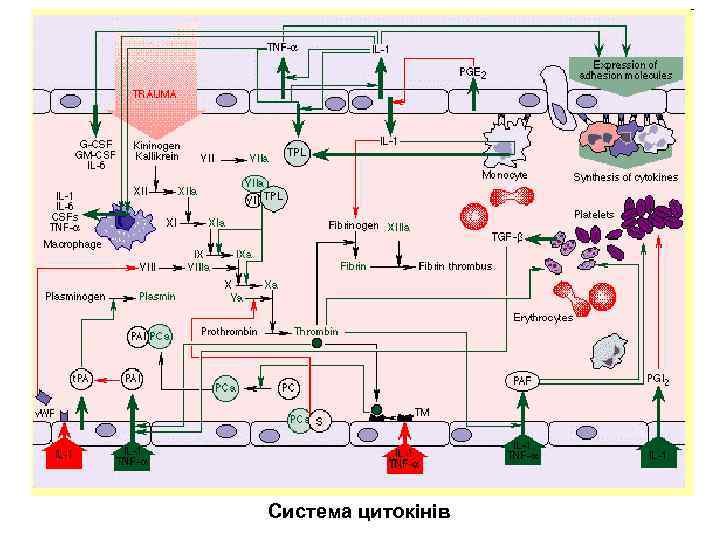 Система цитокінів
Система цитокінів
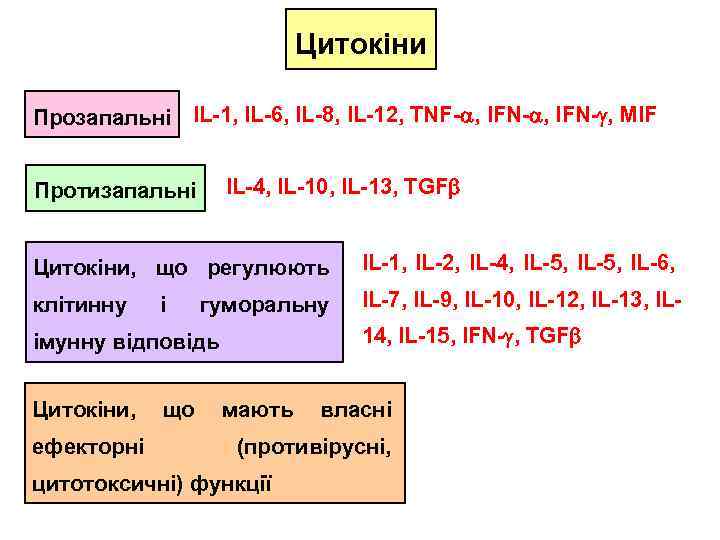 Цитокіни Прозапальні IL-1, IL-6, IL-8, IL-12, TNF- , IFN- , MIF IL-4, IL-10, IL-13, TGF Протизапальні Цитокіни, що регулюють IL-1, IL-2, IL-4, IL-5, IL-6, клітинну IL-7, IL-9, IL-10, IL-12, IL-13, IL- і гуморальну 14, IL-15, IFN- , TGF імунну відповідь Цитокіни, що мають власні ефекторні (противірусні, цитотоксичні) функції
Цитокіни Прозапальні IL-1, IL-6, IL-8, IL-12, TNF- , IFN- , MIF IL-4, IL-10, IL-13, TGF Протизапальні Цитокіни, що регулюють IL-1, IL-2, IL-4, IL-5, IL-6, клітинну IL-7, IL-9, IL-10, IL-12, IL-13, IL- і гуморальну 14, IL-15, IFN- , TGF імунну відповідь Цитокіни, що мають власні ефекторні (противірусні, цитотоксичні) функції
 Прозапальні цитокіни IL-1 і IL-1 Клітини-продуценти: гемопоетичні, епітеліальні, нервові клітини. Продукується не спонтанно, а у відповідь на: інфекцію, мікробні токсини, запальні агенти, білки комплементу, білки зсідання крові. Функція: широкий спектр прозапальної, метаболічної, фізіологічної, гемопоетичної та імунологічної активності.
Прозапальні цитокіни IL-1 і IL-1 Клітини-продуценти: гемопоетичні, епітеліальні, нервові клітини. Продукується не спонтанно, а у відповідь на: інфекцію, мікробні токсини, запальні агенти, білки комплементу, білки зсідання крові. Функція: широкий спектр прозапальної, метаболічної, фізіологічної, гемопоетичної та імунологічної активності.
 Синергізм: IL-1 + TNF- + IL-6 – прозапальні ефекти: Шстимулюють Т- і В-лімфоцити, Шпосилюють клітинну проліферацію, Швпливають на експресію певних генів; IL-1 – медіатор запалення: опосередковує розвиток системної гострофазної відповіді. Підвищення рівню IL-1: лихоманка, анорексія, нейтрофілія, активація ендотеліальних клітин і пдвищення експресії на них молекул адгезії, активація нейтрофілів, підвищення синтезу білків гострої фази і комплементу. IL-1 – індукує власний синтез й експресію рецепторів для IL-2.
Синергізм: IL-1 + TNF- + IL-6 – прозапальні ефекти: Шстимулюють Т- і В-лімфоцити, Шпосилюють клітинну проліферацію, Швпливають на експресію певних генів; IL-1 – медіатор запалення: опосередковує розвиток системної гострофазної відповіді. Підвищення рівню IL-1: лихоманка, анорексія, нейтрофілія, активація ендотеліальних клітин і пдвищення експресії на них молекул адгезії, активація нейтрофілів, підвищення синтезу білків гострої фази і комплементу. IL-1 – індукує власний синтез й експресію рецепторів для IL-2.
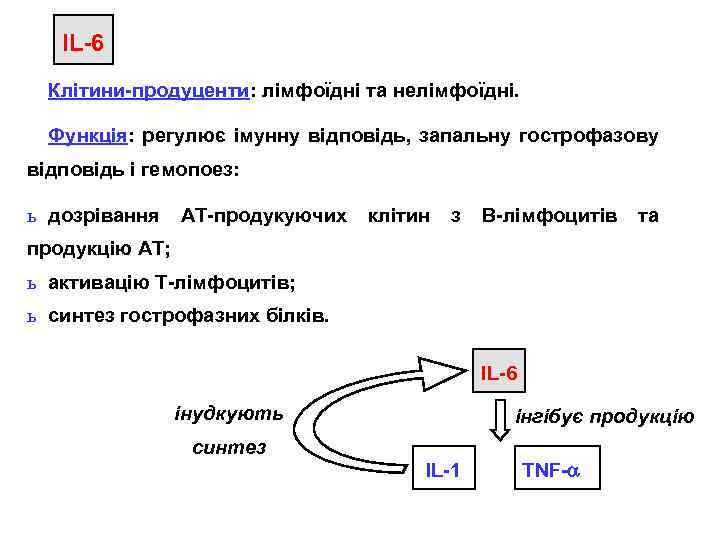 IL-6 Клітини-продуценти: лімфоїдні та нелімфоїдні. Функція: регулює імунну відповідь, запальну гострофазову відповідь і гемопоез: ь дозрівання АТ-продукуючих клітин з В-лімфоцитів та продукцію АТ; ь активацію Т-лімфоцитів; ь синтез гострофазних білків. IL-6 інудкують інгібує продукцію синтез IL-1 TNF-
IL-6 Клітини-продуценти: лімфоїдні та нелімфоїдні. Функція: регулює імунну відповідь, запальну гострофазову відповідь і гемопоез: ь дозрівання АТ-продукуючих клітин з В-лімфоцитів та продукцію АТ; ь активацію Т-лімфоцитів; ь синтез гострофазних білків. IL-6 інудкують інгібує продукцію синтез IL-1 TNF-
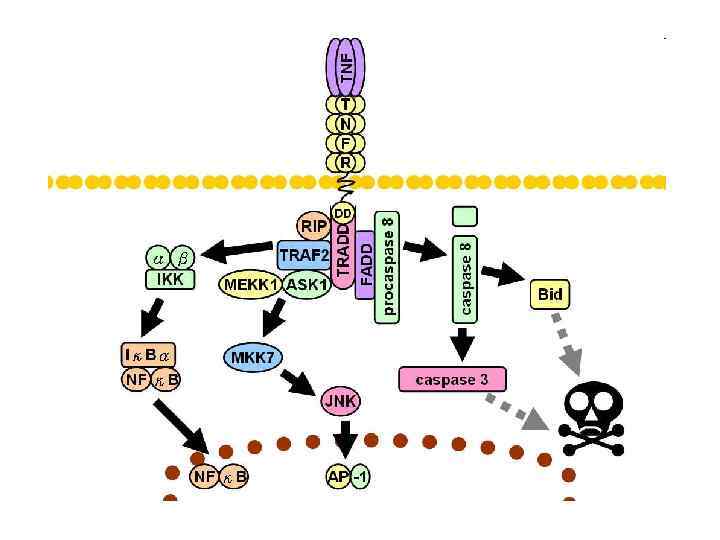
 TNF- Клітини-продуценти: моноцити і макрофаги, лімфоцити крові, натуральні кілери, гранулоцити крові, Т-лімфоцитарні клітинні лінії. Індуктори синтезу: бактеріальні ліполісахариди (ЛПС), цитокіни (IL-1, IL-2, IFN- і - ). Функція: активація або інгібування експресії генів, напр. , інших прозапальних цитокінів (через фактор NF B). Біологічна активність: ь цитотоксичність по відношенню до деяких пухлинних клітин; ь пригнічення ліпопротеїнкінази; ь участь у регуляції імунної відповіді і запалення.
TNF- Клітини-продуценти: моноцити і макрофаги, лімфоцити крові, натуральні кілери, гранулоцити крові, Т-лімфоцитарні клітинні лінії. Індуктори синтезу: бактеріальні ліполісахариди (ЛПС), цитокіни (IL-1, IL-2, IFN- і - ). Функція: активація або інгібування експресії генів, напр. , інших прозапальних цитокінів (через фактор NF B). Біологічна активність: ь цитотоксичність по відношенню до деяких пухлинних клітин; ь пригнічення ліпопротеїнкінази; ь участь у регуляції імунної відповіді і запалення.
 Запуск запалення: Ш активує ендотелій; TNF- Ш сприяє адгезії лейкоцитів до ендотелію через індукцію на ньому експресії молекул адгезії і міграції лейкоцитів до вогнища запалення; Ш активує лейкоцити (гранулоцити, моноцити, лімфоцити); Ш індукує продукцію інших прозапальних цитокінів (IL-1, IL-6, IFN ), що виявляють синергізм з TNF-. Місцева продукція TNF- у вогнищі запалення викликає: v хемотаксис гранулоцитів і моноцитів, v посилення фагоцитозу; v дегрануляцію фагоцитів; v продукцію і секрецію реактивних кисневих радикалів; v збільшену цитотоксичність фагоцитів; v Т-лімфоцити посилюють експресію рецепторів для IL-2 і TNF-.
Запуск запалення: Ш активує ендотелій; TNF- Ш сприяє адгезії лейкоцитів до ендотелію через індукцію на ньому експресії молекул адгезії і міграції лейкоцитів до вогнища запалення; Ш активує лейкоцити (гранулоцити, моноцити, лімфоцити); Ш індукує продукцію інших прозапальних цитокінів (IL-1, IL-6, IFN ), що виявляють синергізм з TNF-. Місцева продукція TNF- у вогнищі запалення викликає: v хемотаксис гранулоцитів і моноцитів, v посилення фагоцитозу; v дегрануляцію фагоцитів; v продукцію і секрецію реактивних кисневих радикалів; v збільшену цитотоксичність фагоцитів; v Т-лімфоцити посилюють експресію рецепторів для IL-2 і TNF-.
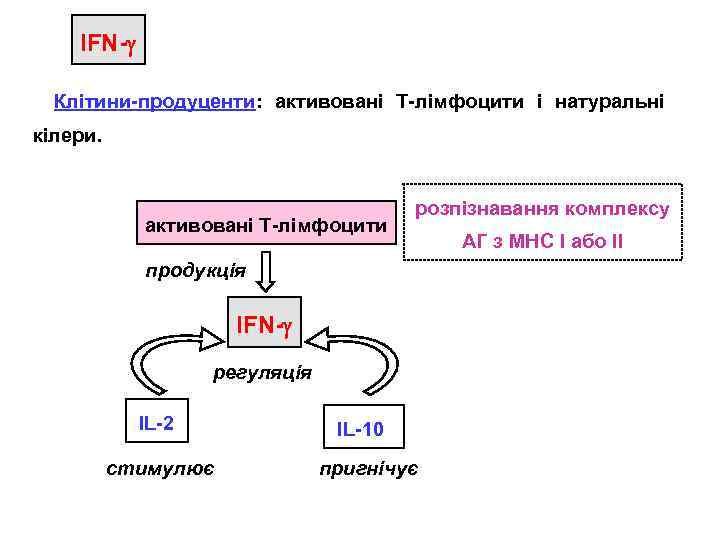 IFN- Клітини-продуценти: активовані Т-лімфоцити і натуральні кілери. активовані Т-лімфоцити розпізнавання комплексу продукція IFN- регуляція IL-2 стимулює IL-10 пригнічує АГ з МНС І або ІІ
IFN- Клітини-продуценти: активовані Т-лімфоцити і натуральні кілери. активовані Т-лімфоцити розпізнавання комплексу продукція IFN- регуляція IL-2 стимулює IL-10 пригнічує АГ з МНС І або ІІ
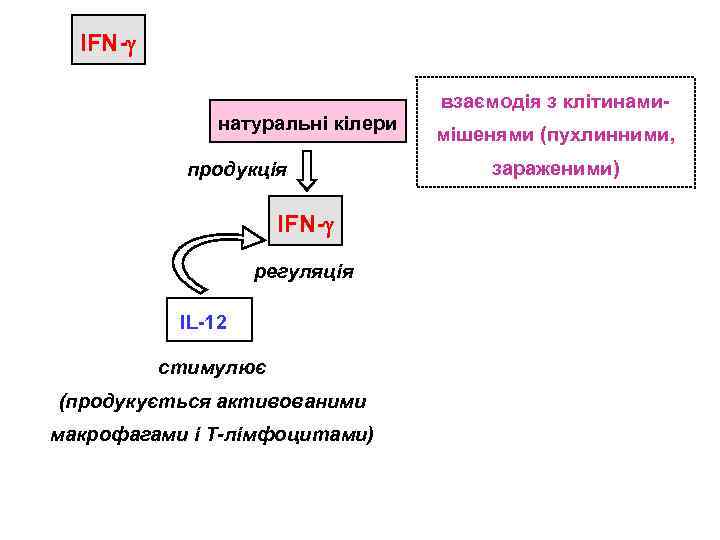 IFN- взаємодія з клітинаминатуральні кілери продукція IFN- регуляція IL-12 стимулює (продукується активованими макрофагами і Т-лімфоцитами) мішенями (пухлинними, зараженими)
IFN- взаємодія з клітинаминатуральні кілери продукція IFN- регуляція IL-12 стимулює (продукується активованими макрофагами і Т-лімфоцитами) мішенями (пухлинними, зараженими)
 IFN- Функції IFN- : Ш активація секреторних функцій макрофагів (мікробіцидності й цитотоксичності), продукції ними цитокінів, кисневих радикалів, простагнландинів; Ш підвищення експресії МНС І і ІІ на різних клітинах підвищення ефективності презентації АГ і їх розпізнавання Т-лімфоцитами; Ш участь в адгезії лімфоцитів до ендотеліальних клітин у посткапілярних венах; Ш сумісно з TNF- індукує продукцію хемокінів (напр. , RANTES); Ш збільшує лімфоцитів. функціональну активність цитотоксичних Т-
IFN- Функції IFN- : Ш активація секреторних функцій макрофагів (мікробіцидності й цитотоксичності), продукції ними цитокінів, кисневих радикалів, простагнландинів; Ш підвищення експресії МНС І і ІІ на різних клітинах підвищення ефективності презентації АГ і їх розпізнавання Т-лімфоцитами; Ш участь в адгезії лімфоцитів до ендотеліальних клітин у посткапілярних венах; Ш сумісно з TNF- індукує продукцію хемокінів (напр. , RANTES); Ш збільшує лімфоцитів. функціональну активність цитотоксичних Т-
 Протизапальні цитокіни IL-4 Клітини-продуценти: Т-хелпери 2 порядку (TH 2), частково тучні клітини, базофіли, В-лімфоцити, сторомальні клітини кістковго мозку. Функція: ь контроль проліферації, диференціювання і функцій Влімфоцитів (антитільної відповіді); ь інгібування моноцитів/макрофагів; ь блокування продукції прозапальних цитокінів (IL-1, IL-8, TNF- ) моноцитами і макрофагами; ь блокування продукції супероксидних радикалів і ПГ Е 2.
Протизапальні цитокіни IL-4 Клітини-продуценти: Т-хелпери 2 порядку (TH 2), частково тучні клітини, базофіли, В-лімфоцити, сторомальні клітини кістковго мозку. Функція: ь контроль проліферації, диференціювання і функцій Влімфоцитів (антитільної відповіді); ь інгібування моноцитів/макрофагів; ь блокування продукції прозапальних цитокінів (IL-1, IL-8, TNF- ) моноцитами і макрофагами; ь блокування продукції супероксидних радикалів і ПГ Е 2.
 Протизапальні цитокіни IL-13 Клітини-продуценти: активовані CD 4+- (Th 1 і Th 2) і CD 8+-Тлімфоцити. Функція: Спільна з IL-4 дія на моноцити, макрофаги і Влімфоцити, але не діє на Т-лімфоцити. ь підвищує адгезію і виживання моноцитів, ь підвищує експресію на моноцитах молекул адгезії, МНС ІІ, посилює їх АГ-презентуючу функцію; ь інгібує продукцію макрофагами цитокінів IL-1, IL-6, IL-8, IL-10, TNF- ; ь підвищує експресію на В-лімфоцитах МНС ІІ, поверхневих Ig, сприяяє переключення синтезу з Ig. G 4 на Ig. E; ь індукує синтез IFN- натуральними кілерами.
Протизапальні цитокіни IL-13 Клітини-продуценти: активовані CD 4+- (Th 1 і Th 2) і CD 8+-Тлімфоцити. Функція: Спільна з IL-4 дія на моноцити, макрофаги і Влімфоцити, але не діє на Т-лімфоцити. ь підвищує адгезію і виживання моноцитів, ь підвищує експресію на моноцитах молекул адгезії, МНС ІІ, посилює їх АГ-презентуючу функцію; ь інгібує продукцію макрофагами цитокінів IL-1, IL-6, IL-8, IL-10, TNF- ; ь підвищує експресію на В-лімфоцитах МНС ІІ, поверхневих Ig, сприяяє переключення синтезу з Ig. G 4 на Ig. E; ь індукує синтез IFN- натуральними кілерами.
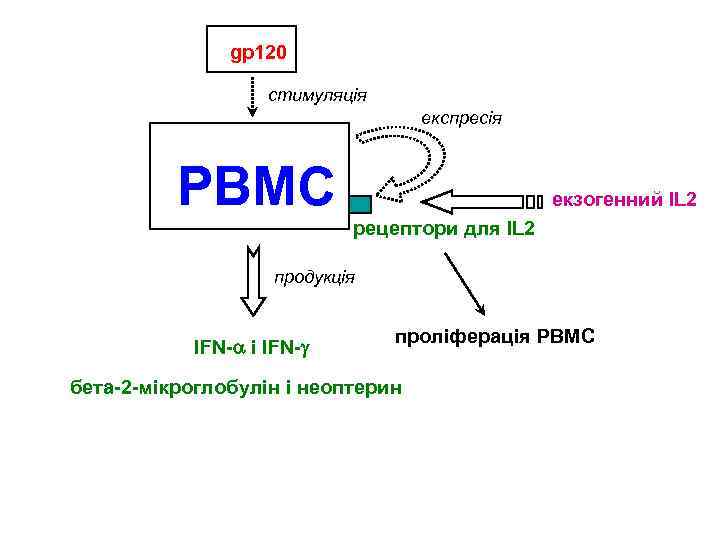 gp 120 стимуляція експресія PBMC екзогенний IL 2 рецептори для IL 2 продукція IFN- і IFN- проліферація PBMC бета-2 -мікроглобулін і неоптерин
gp 120 стимуляція експресія PBMC екзогенний IL 2 рецептори для IL 2 продукція IFN- і IFN- проліферація PBMC бета-2 -мікроглобулін і неоптерин
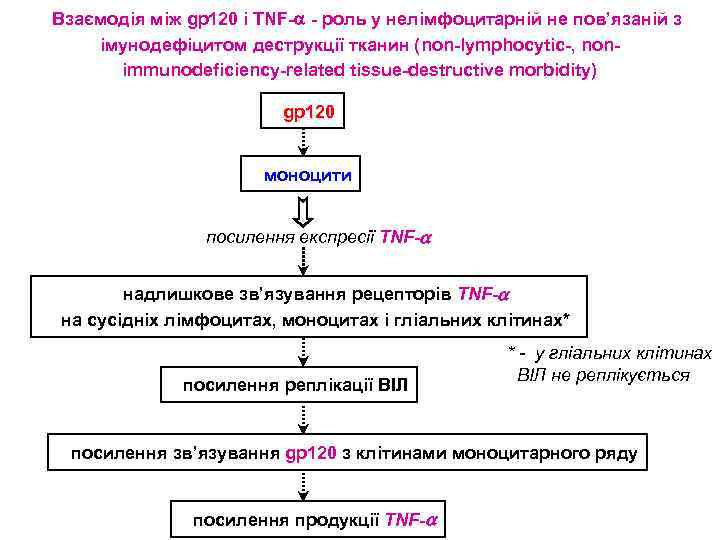 Взаємодія між gp 120 і TNF- - роль у нелімфоцитарній не пов’язаній з імунодефіцитом деструкції тканин (non-lymphocytic-, nonimmunodeficiency-related tissue-destructive morbidity) gp 120 моноцити посилення експресії TNF- надлишкове зв’язування рецепторів TNF- на сусідніх лімфоцитах, моноцитах і гліальних клітинах* посилення реплікації ВІЛ * - у гліальних клітинах ВІЛ не реплікується посилення зв’язування gp 120 з клітинами моноцитарного ряду посилення продукції TNF-
Взаємодія між gp 120 і TNF- - роль у нелімфоцитарній не пов’язаній з імунодефіцитом деструкції тканин (non-lymphocytic-, nonimmunodeficiency-related tissue-destructive morbidity) gp 120 моноцити посилення експресії TNF- надлишкове зв’язування рецепторів TNF- на сусідніх лімфоцитах, моноцитах і гліальних клітинах* посилення реплікації ВІЛ * - у гліальних клітинах ВІЛ не реплікується посилення зв’язування gp 120 з клітинами моноцитарного ряду посилення продукції TNF-
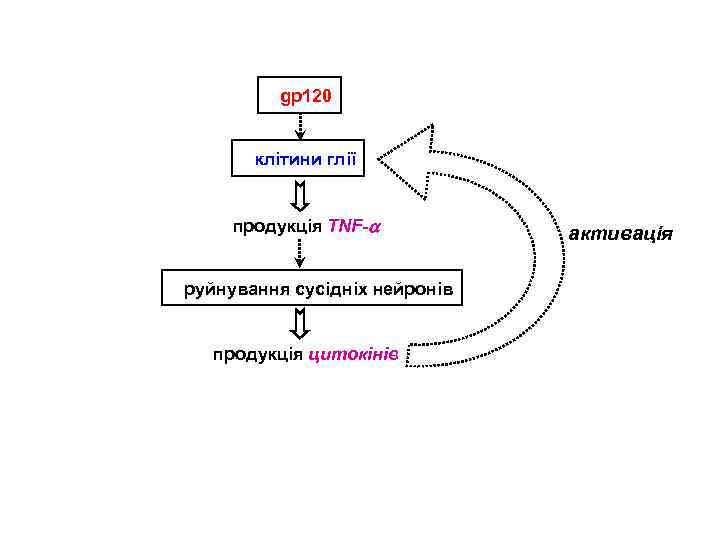 gp 120 клітини глії продукція TNF- руйнування сусідніх нейронів продукція цитокінів активація
gp 120 клітини глії продукція TNF- руйнування сусідніх нейронів продукція цитокінів активація
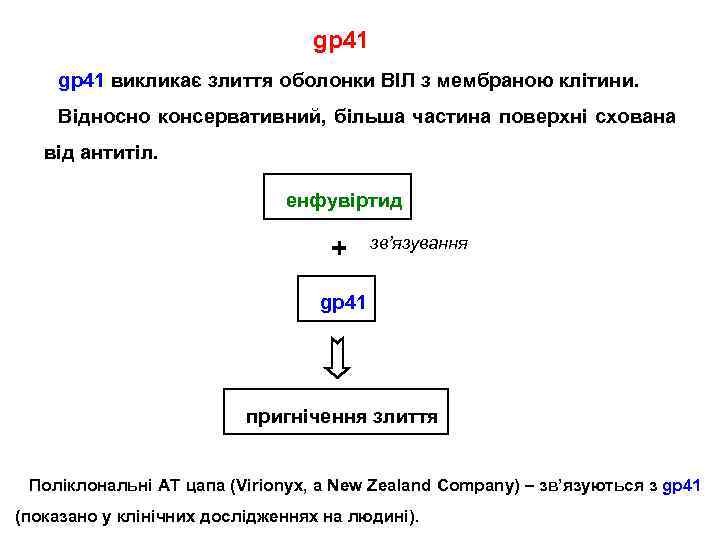 gp 41 викликає злиття оболонки ВІЛ з мембраною клітини. Відносно консервативний, більша частина поверхні схована від антитіл. енфувіртид + зв’язування gp 41 пригнічення злиття Поліклональні АТ цапа (Virionyx, a New Zealand Company) – зв’язуються з gp 41 (показано у клінічних дослідженнях на людині).
gp 41 викликає злиття оболонки ВІЛ з мембраною клітини. Відносно консервативний, більша частина поверхні схована від антитіл. енфувіртид + зв’язування gp 41 пригнічення злиття Поліклональні АТ цапа (Virionyx, a New Zealand Company) – зв’язуються з gp 41 (показано у клінічних дослідженнях на людині).
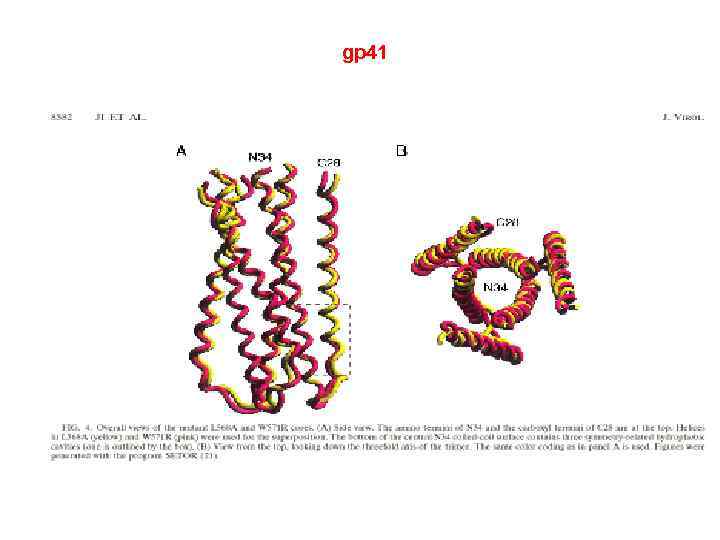 gp 41
gp 41
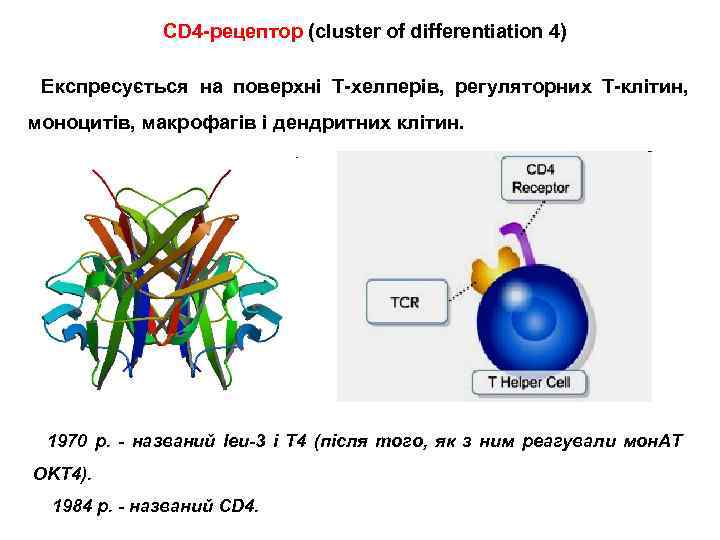 CD 4 -рецептор (cluster of differentiation 4) Експресується на поверхні Т-хелперів, регуляторних Т-клітин, моноцитів, макрофагів і дендритних клітин. 1970 р. - названий leu-3 і T 4 (після того, як з ним реагували мон. АТ OKT 4). 1984 р. - названий CD 4.
CD 4 -рецептор (cluster of differentiation 4) Експресується на поверхні Т-хелперів, регуляторних Т-клітин, моноцитів, макрофагів і дендритних клітин. 1970 р. - названий leu-3 і T 4 (після того, як з ним реагували мон. АТ OKT 4). 1984 р. - названий CD 4.
 gp 120 CD 4 Залишок Phe 43 CD 4 знаходиться у зв’язуючій “кишені” gp 120
gp 120 CD 4 Залишок Phe 43 CD 4 знаходиться у зв’язуючій “кишені” gp 120
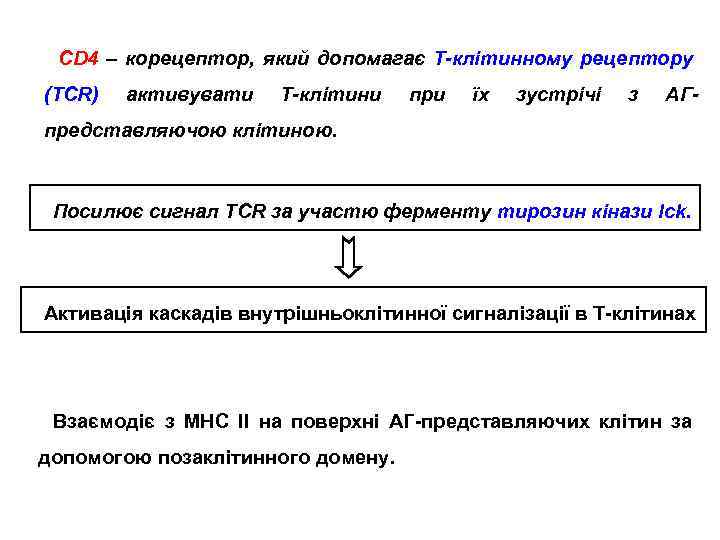 CD 4 – корецептор, який допомагає Т-клітинному рецептору (TCR) активувати Т-клітини при їх зустрічі з АГ- представляючою клітиною. Посилює сигнал TCR за участю ферменту тирозин кінази lck. Активація каскадів внутрішньоклітинної сигналізації в Т-клітинах Взаємодіє з МНС ІІ на поверхні АГ-представляючих клітин за допомогою позаклітинного домену.
CD 4 – корецептор, який допомагає Т-клітинному рецептору (TCR) активувати Т-клітини при їх зустрічі з АГ- представляючою клітиною. Посилює сигнал TCR за участю ферменту тирозин кінази lck. Активація каскадів внутрішньоклітинної сигналізації в Т-клітинах Взаємодіє з МНС ІІ на поверхні АГ-представляючих клітин за допомогою позаклітинного домену.
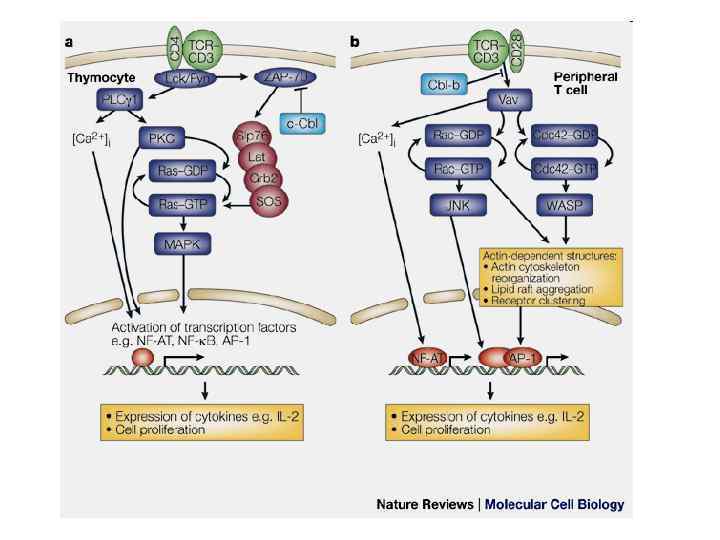
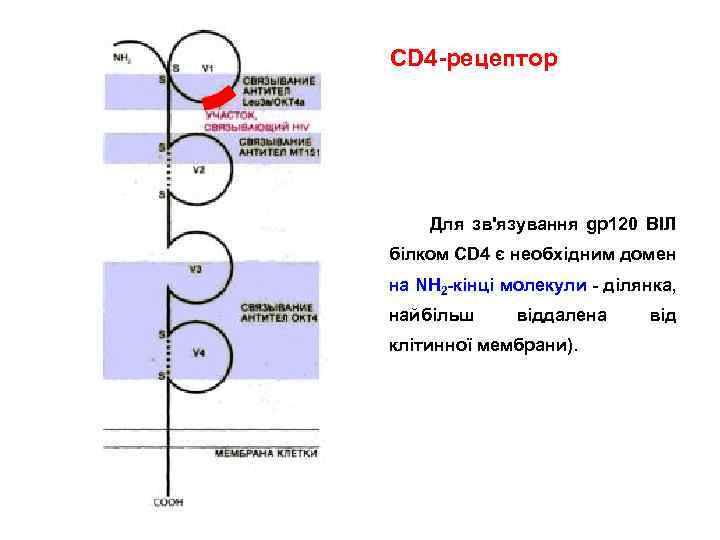 CD 4 -рецептор Для зв'язування gp 120 ВІЛ білком CD 4 є необхідним домен на ΝΗ 2 -кінці молекули - ділянка, найбільш віддалена клітинної мембрани). від
CD 4 -рецептор Для зв'язування gp 120 ВІЛ білком CD 4 є необхідним домен на ΝΗ 2 -кінці молекули - ділянка, найбільш віддалена клітинної мембрани). від
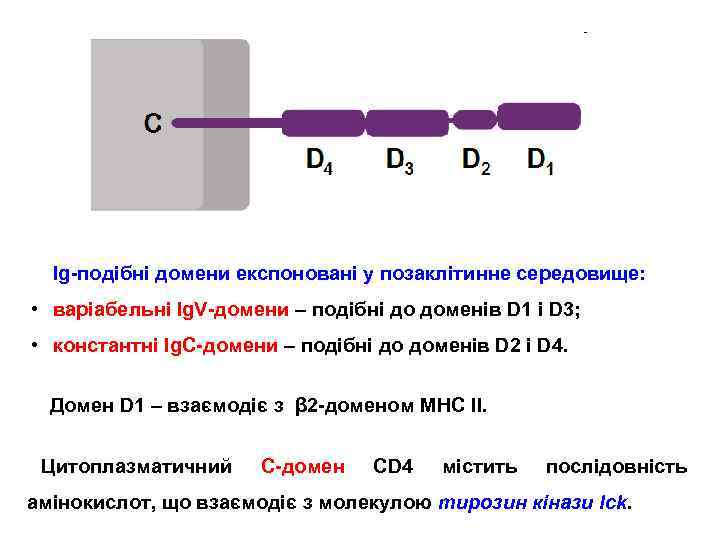 Ig-подібні домени експоновані у позаклітинне середовище: • варіабельні Ig. V-домени – подібні до доменів D 1 і D 3; • константні Ig. C-домени – подібні до доменів D 2 і D 4. Домен D 1 – взаємодіє з β 2 -доменом MHC II. Цитоплазматичний С-домен CD 4 містить послідовність амінокислот, що взаємодіє з молекулою тирозин кінази lck.
Ig-подібні домени експоновані у позаклітинне середовище: • варіабельні Ig. V-домени – подібні до доменів D 1 і D 3; • константні Ig. C-домени – подібні до доменів D 2 і D 4. Домен D 1 – взаємодіє з β 2 -доменом MHC II. Цитоплазматичний С-домен CD 4 містить послідовність амінокислот, що взаємодіє з молекулою тирозин кінази lck.
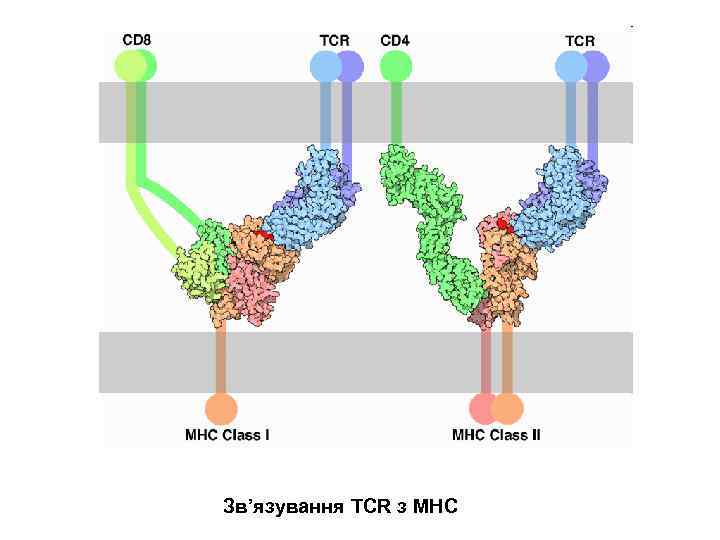 Зв’язування TCR з MHC
Зв’язування TCR з MHC
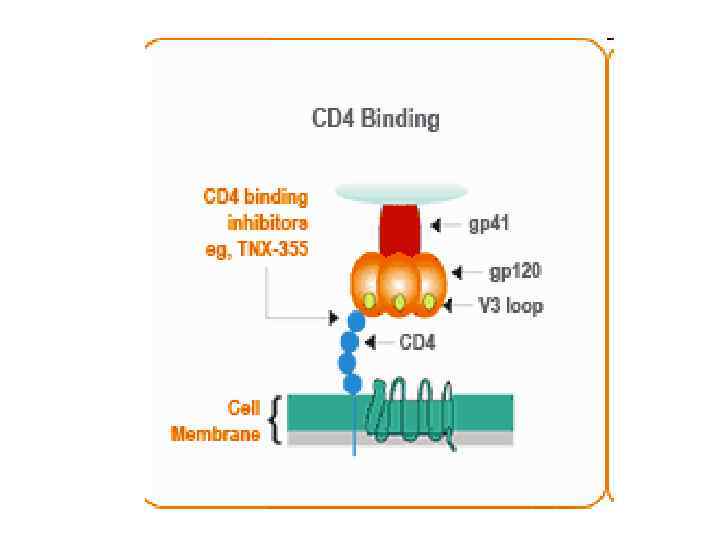
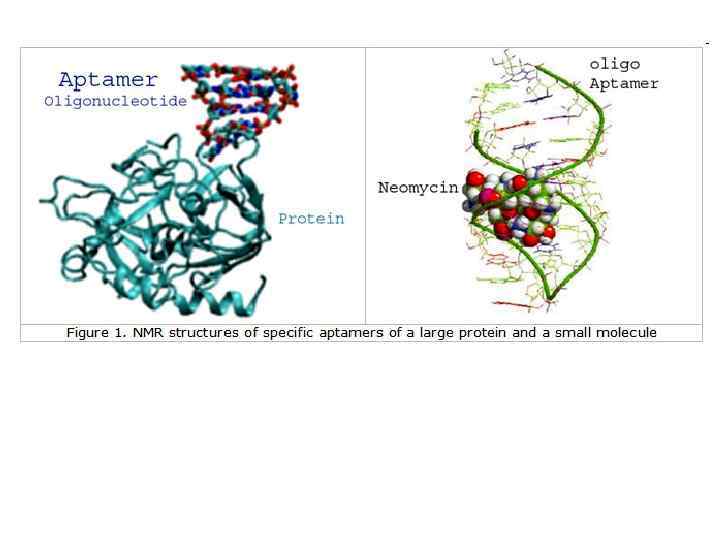
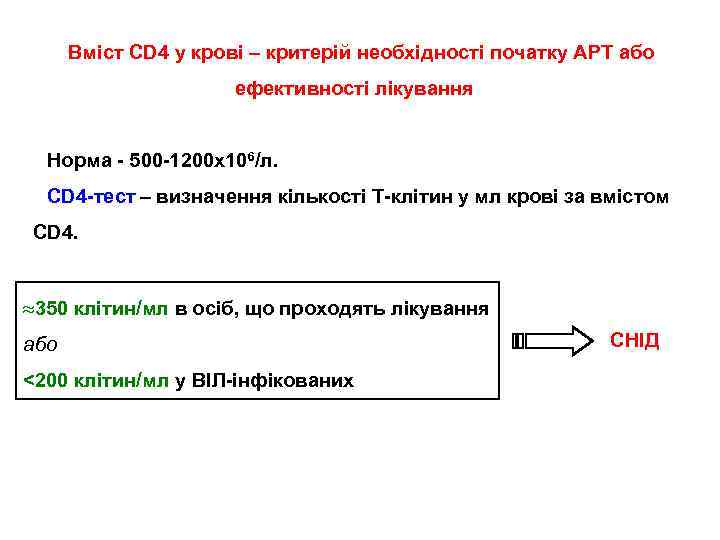 Вміст CD 4 у крові – критерій необхідності початку АРТ або ефективності лікування Норма - 500 -1200 x 106/л. CD 4 -тест – визначення кількості Т-клітин у мл крові за вмістом CD 4. » 350 клітин/мл в осіб, що проходять лікування або <200 клітин/мл у ВІЛ-інфікованих СНІД
Вміст CD 4 у крові – критерій необхідності початку АРТ або ефективності лікування Норма - 500 -1200 x 106/л. CD 4 -тест – визначення кількості Т-клітин у мл крові за вмістом CD 4. » 350 клітин/мл в осіб, що проходять лікування або <200 клітин/мл у ВІЛ-інфікованих СНІД


