VI группа побочная подгруппа 1. Характеристика элементов В


VI группа побочная подгруппа
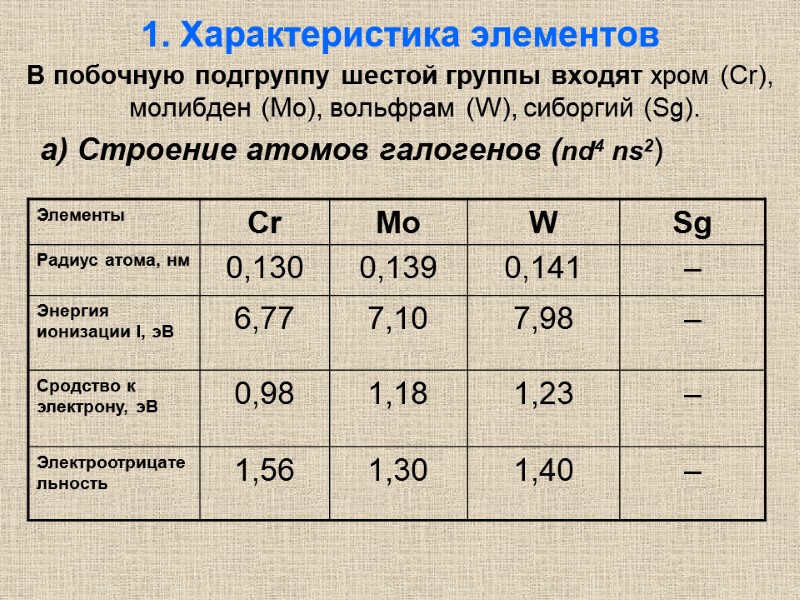
1. Характеристика элементов В побочную подгруппу шестой группы входят хром (Cr), молибден (Мо), вольфрам (W), сиборгий (Sg). а) Строение атомов галогенов (nd4 ns2)
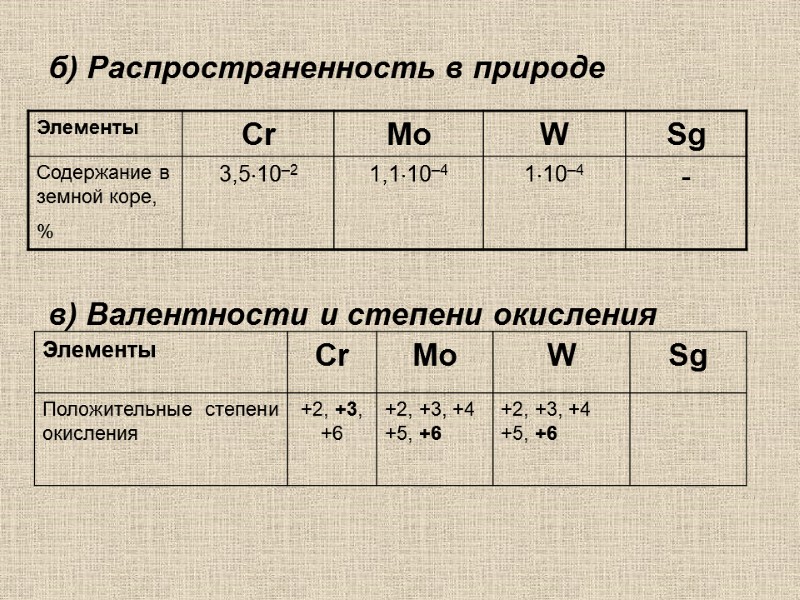
б) Распространенность в природе в) Валентности и степени окисления
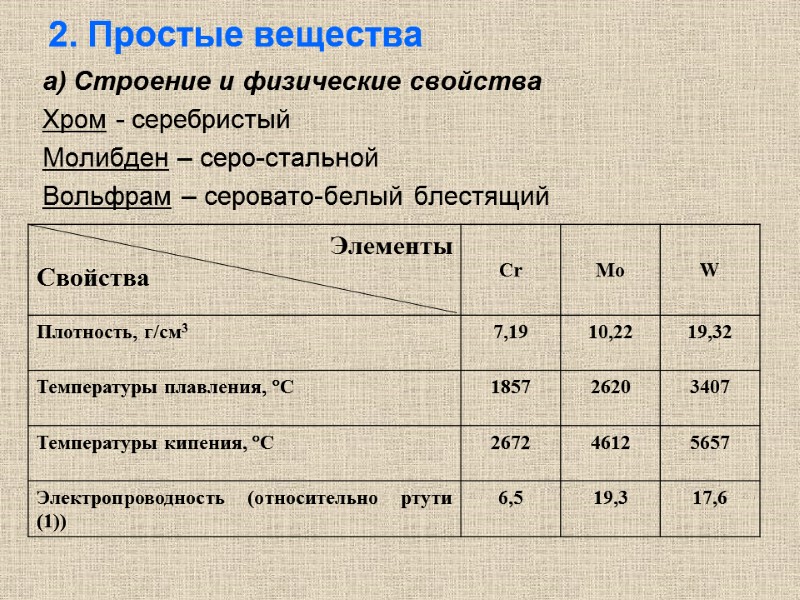
2. Простые вещества а) Строение и физические свойства Хром - серебристый Молибден – серо-стальной Вольфрам – серовато-белый блестящий

Способы получения 1.Восстановление оксидов Cr2O3, MoO3 и WO3 Cr2О3 + 2Al 2Cr + Al2O3 MoO3 (WO3) + 3H2 Мо (W) + 3H2О 2. Восстановление галогенидов MoF6 + 3H2 Mo + 6HF 3. Электролизом расплавов 4. Сиборгий получен путем ядерного синтеза

Химические свойства С простыми веществами – с кислородом: 2Мо + 3О2 → 2МоО3 (хром - Cr2О3) – с галогенами: хром – CrHal2, CrHal3; молибден и вольфрам – ЭHal2, ЭHal3, ЭHal4, ЭHal5, ЭHal6 – с серой: ЭхSу – с азотом: Э2N, ЭN – с водородом не реагируют – с углеродом ЭхСу

Со сложными веществами с водой хром – Cr2O3, молибден и вольфрам – ЭО3 с плавиковой и соляной кислотами CrF2 CrCl2 со смесью плавиковой и азотной кислот Н2[ЭF8] с разбавленной серной кислотой CrSO4 с концентрированной серной кислотой Н2ЭО4 (кроме Cr) с азотной кислотой металлы подгруппы не реагируют со щелочами в расплаве в присутствии натриевой селитры

2Сr + 3H2O Cr2O3 + 3H2 Cr + H2SО4(разб.) → CrSО4 + Н2 W + 8HF + 2HNO3 → H2[WF8] + 2NO + 4H2O Mo + 3NaNO3 + 2NaOH → Na2MoO4 + 3NaNO2 + H2O Соединения Бинарные соединения С водородом не дают соединений Оксиды W18O19, Мо17О47, Cr3O8 и т. д. Устойчивы - Cr2O3, а у молибдена и вольфрама – МоО3 и WO3

Оксиды элементов побочной подгруппы VI группы
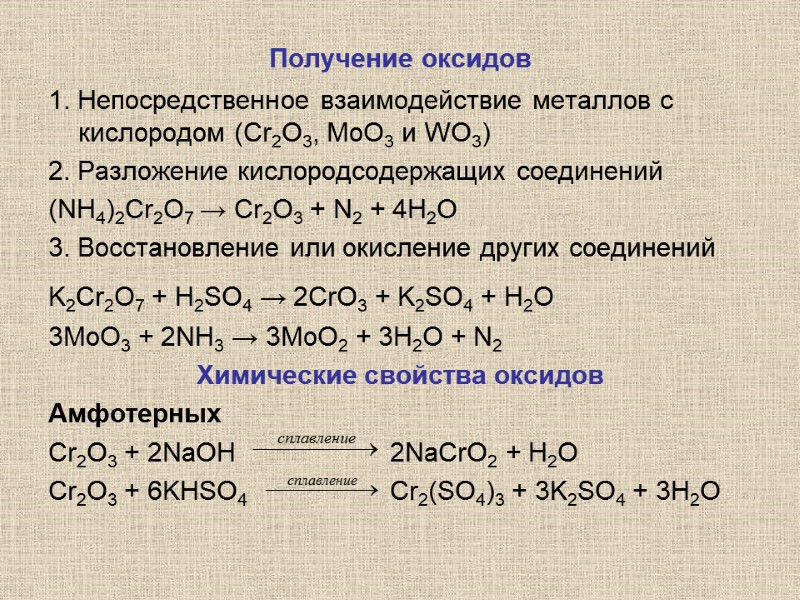
Получение оксидов 1. Непосредственное взаимодействие металлов с кислородом (Cr2O3, МоО3 и WО3) 2. Разложение кислородсодержащих соединений (NH4)2Cr2O7 → Cr2O3 + N2 + 4H2O 3. Восстановление или окисление других соединений K2Cr2O7 + H2SO4 → 2CrO3 + K2SO4 + H2O 3МоО3 + 2NH3 → 3MoO2 + 3H2O + N2 Химические свойства оксидов Амфотерных Cr2O3 + 2NaOH 2NaCrO2 + H2O Cr2O3 + 6KHSO4 Cr2(SO4)3 + 3K2SO4 + 3H2O

Кислотных CrO3 + H2O → H2CrO4 H2Cr2O7 2KOH + ЭО3 → К2ЭО4 + Н2О Гидроксиды
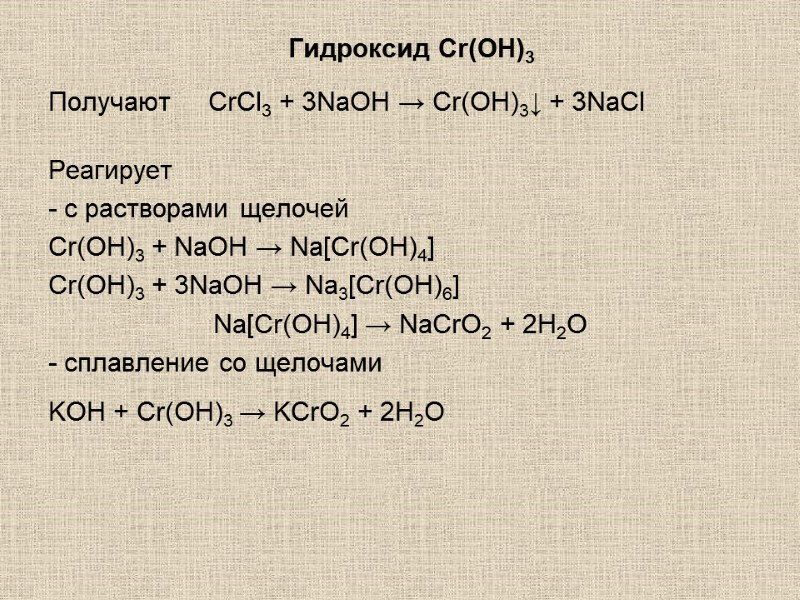
Гидроксид Cr(OH)3 Получают CrCl3 + 3NaOH → Cr(OH)3↓ + 3NaСl Реагирует - с растворами щелочей Cr(OH)3 + NaOH → Na[Cr(OH)4] Cr(OH)3 + 3NaOH → Na3[Cr(OH)6] Na[Cr(OH)4] → NaCrO2 + 2H2O - сплавление со щелочами KOH + Cr(OH)3 → KCrO2 + 2H2O
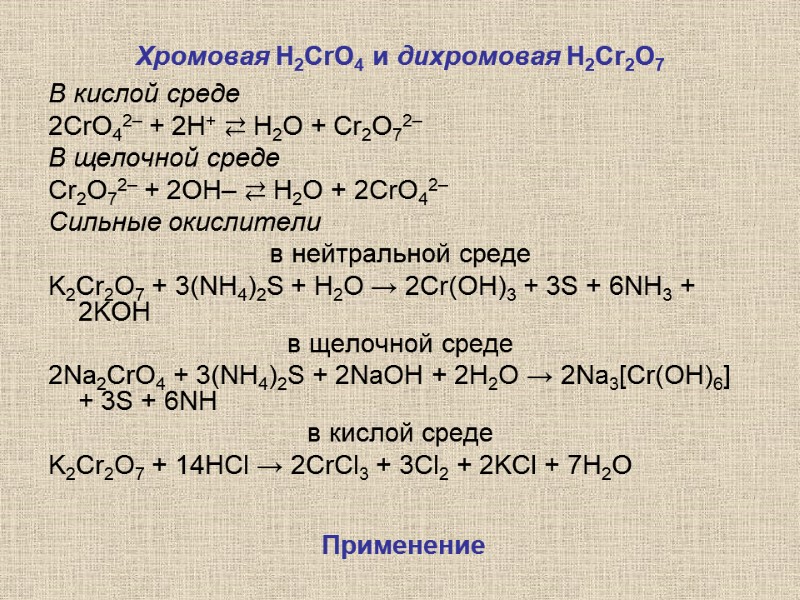
Хромовая Н2CrO4 и дихромовая Н2Cr2О7 В кислой среде 2CrO42– + 2H+ ⇄ H2O + Cr2O72– В щелочной среде Cr2O72– + 2OH– ⇄ H2O + 2CrO42– Сильные окислители в нейтральной среде K2Cr2O7 + 3(NH4)2S + H2O → 2Cr(OH)3 + 3S + 6NH3 + 2KOH в щелочной среде 2Na2CrO4 + 3(NH4)2S + 2NaOH + 2H2O → 2Na3[Cr(OH)6] + 3S + 6NH в кислой среде K2Cr2O7 + 14HCl → 2CrCl3 + 3Cl2 + 2KCl + 7H2O Применение
18822-vi_poboch.ppt
- Количество слайдов: 13

