1. Строение вещества.pptx
- Количество слайдов: 20
 Вещество Энергия Структура и превращения Часть I Структура материи
Вещество Энергия Структура и превращения Часть I Структура материи
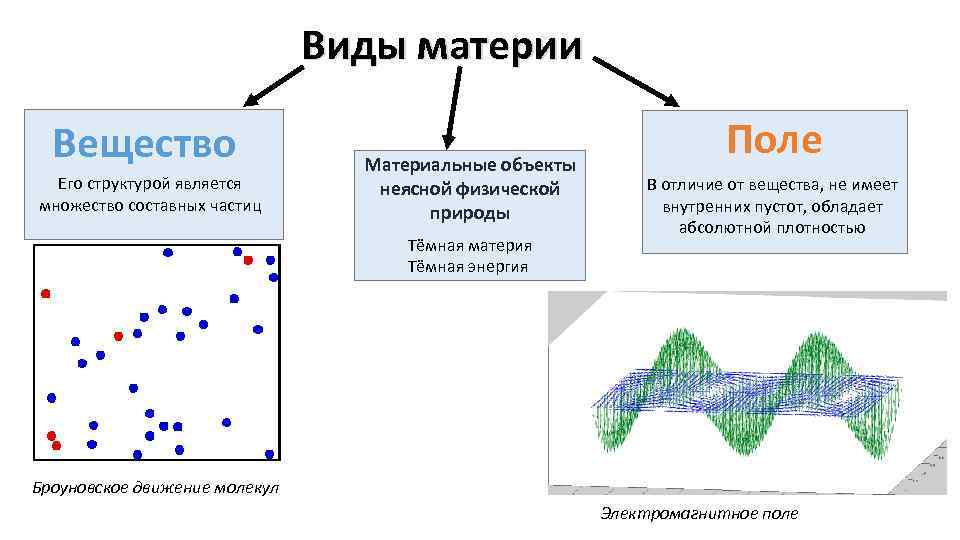 Виды материи Вещество Его структурой является множество составных частиц Материальные объекты неясной физической природы Тёмная материя Тёмная энергия Поле В отличие от вещества, не имеет внутренних пустот, обладает абсолютной плотностью Броуновское движение молекул Электромагнитное поле
Виды материи Вещество Его структурой является множество составных частиц Материальные объекты неясной физической природы Тёмная материя Тёмная энергия Поле В отличие от вещества, не имеет внутренних пустот, обладает абсолютной плотностью Броуновское движение молекул Электромагнитное поле
 Молекулярно-кинетическая теория (МКТ) 1. Любое вещество состоит из мельчайших частиц - молекул и атомов. Они расположены в пространстве дискретно, то есть на некоторых расстояниях друг от друга. 2. Атомы или молекулы вещества находятся в состоянии беспорядочного движения, которое никогда не прекращается. 3. Атомы или молекулы вещества взаимодействуют друг с другом силами притяжения и отталкивания, которые зависят от расстояний между частицами.
Молекулярно-кинетическая теория (МКТ) 1. Любое вещество состоит из мельчайших частиц - молекул и атомов. Они расположены в пространстве дискретно, то есть на некоторых расстояниях друг от друга. 2. Атомы или молекулы вещества находятся в состоянии беспорядочного движения, которое никогда не прекращается. 3. Атомы или молекулы вещества взаимодействуют друг с другом силами притяжения и отталкивания, которые зависят от расстояний между частицами.
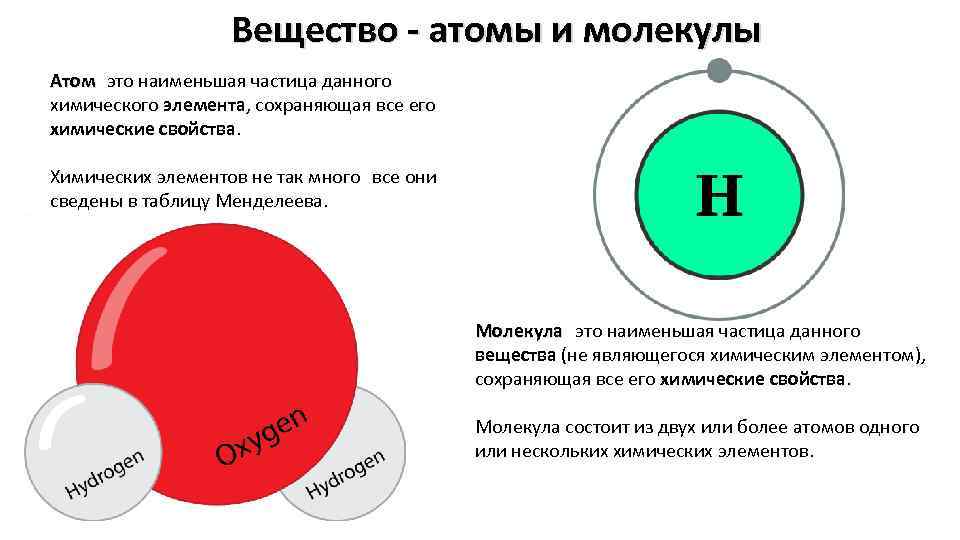 Вещество - атомы и молекулы Атом это наименьшая частица данного химического элемента, сохраняющая все его химические свойства. Химических элементов не так много все они сведены в таблицу Менделеева. Молекула это наименьшая частица данного вещества (не являющегося химическим элементом), сохраняющая все его химические свойства. Молекула состоит из двух или более атомов одного или нескольких химических элементов.
Вещество - атомы и молекулы Атом это наименьшая частица данного химического элемента, сохраняющая все его химические свойства. Химических элементов не так много все они сведены в таблицу Менделеева. Молекула это наименьшая частица данного вещества (не являющегося химическим элементом), сохраняющая все его химические свойства. Молекула состоит из двух или более атомов одного или нескольких химических элементов.
 Атомы и молекулы • Размер атома или молекулы (состоящей из небольшого числа атомов) составляет порядка 10− 8 см. • Это настолько малая величина, что атом невозможно разглядеть ни в какой оптический микроскоп. • Атомы и молекулы называются для краткости просто частицами вещества. • Чем именно является частица атомом или молекулой в каждом конкретном случае установить нетрудно. Но с помощью электронного микроскопа можно увидеть отдельные молекулы! • Если речь идёт о химическом элементе, то частицей будет атом; если же рассматривается сложное вещество, то его частица - это молекула, состоящая из нескольких атомов.
Атомы и молекулы • Размер атома или молекулы (состоящей из небольшого числа атомов) составляет порядка 10− 8 см. • Это настолько малая величина, что атом невозможно разглядеть ни в какой оптический микроскоп. • Атомы и молекулы называются для краткости просто частицами вещества. • Чем именно является частица атомом или молекулой в каждом конкретном случае установить нетрудно. Но с помощью электронного микроскопа можно увидеть отдельные молекулы! • Если речь идёт о химическом элементе, то частицей будет атом; если же рассматривается сложное вещество, то его частица - это молекула, состоящая из нескольких атомов.
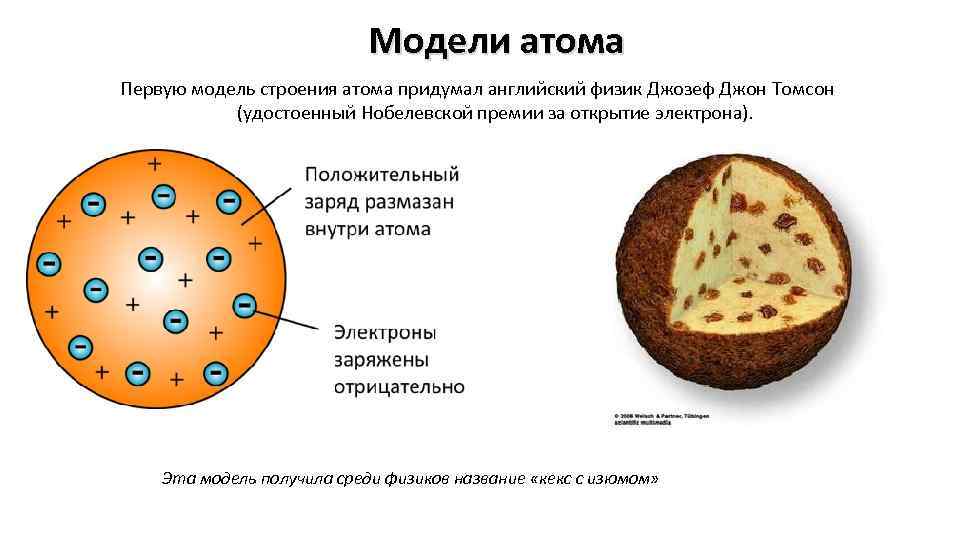 Модели атома Первую модель строения атома придумал английский физик Джозеф Джон Томсон (удостоенный Нобелевской премии за открытие электрона). Эта модель получила среди физиков название «кекс с изюмом»
Модели атома Первую модель строения атома придумал английский физик Джозеф Джон Томсон (удостоенный Нобелевской премии за открытие электрона). Эта модель получила среди физиков название «кекс с изюмом»
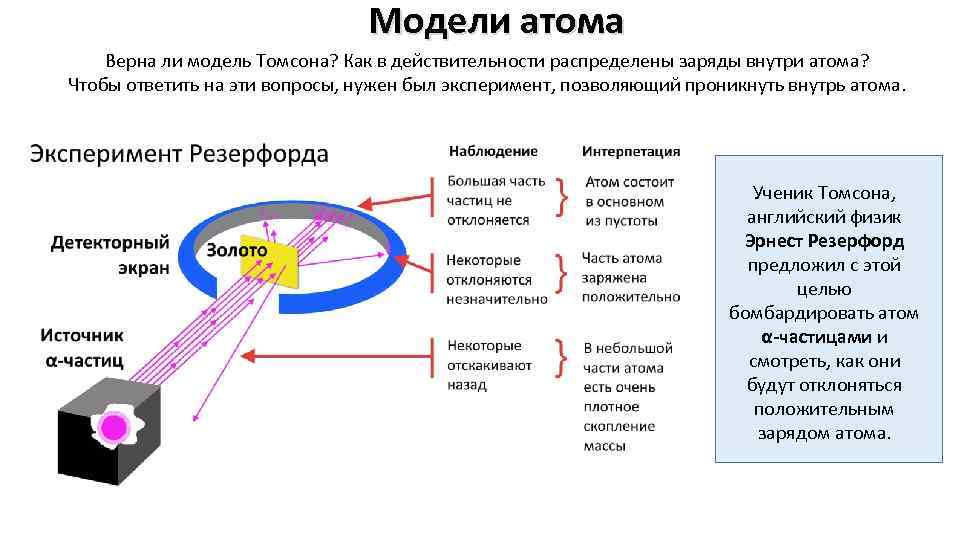 Модели атома Верна ли модель Томсона? Как в действительности распределены заряды внутри атома? Чтобы ответить на эти вопросы, нужен был эксперимент, позволяющий проникнуть внутрь атома. Ученик Томсона, английский физик Эрнест Резерфорд предложил с этой целью бомбардировать атом α-частицами и смотреть, как они будут отклоняться положительным зарядом атома.
Модели атома Верна ли модель Томсона? Как в действительности распределены заряды внутри атома? Чтобы ответить на эти вопросы, нужен был эксперимент, позволяющий проникнуть внутрь атома. Ученик Томсона, английский физик Эрнест Резерфорд предложил с этой целью бомбардировать атом α-частицами и смотреть, как они будут отклоняться положительным зарядом атома.
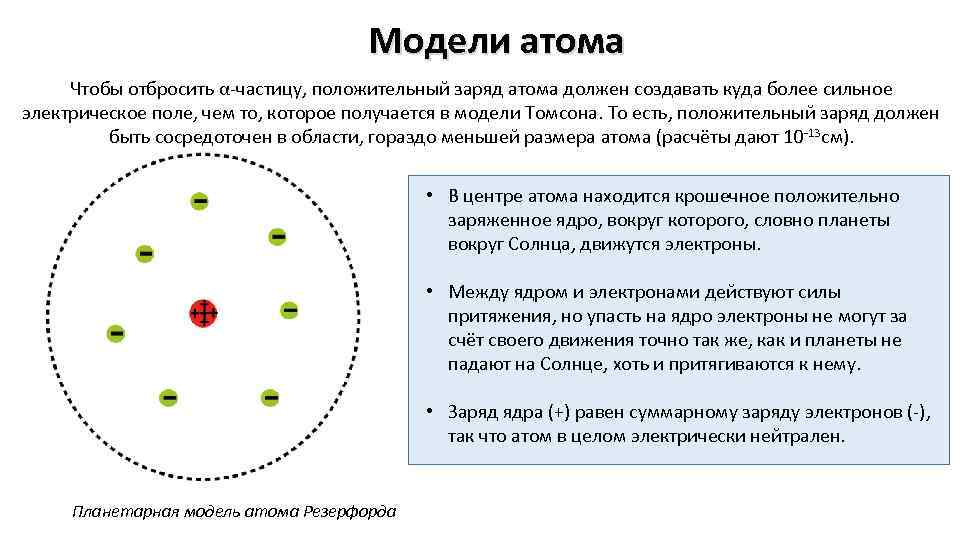 Модели атома Чтобы отбросить α-частицу, положительный заряд атома должен создавать куда более сильное электрическое поле, чем то, которое получается в модели Томсона. То есть, положительный заряд должен быть сосредоточен в области, гораздо меньшей размера атома (расчёты дают 10 -13 см). • В центре атома находится крошечное положительно заряженное ядро, вокруг которого, словно планеты вокруг Солнца, движутся электроны. • Между ядром и электронами действуют силы притяжения, но упасть на ядро электроны не могут за счёт своего движения точно так же, как и планеты не падают на Солнце, хоть и притягиваются к нему. • Заряд ядра (+) равен суммарному заряду электронов (-), так что атом в целом электрически нейтрален. Планетарная модель атома Резерфорда
Модели атома Чтобы отбросить α-частицу, положительный заряд атома должен создавать куда более сильное электрическое поле, чем то, которое получается в модели Томсона. То есть, положительный заряд должен быть сосредоточен в области, гораздо меньшей размера атома (расчёты дают 10 -13 см). • В центре атома находится крошечное положительно заряженное ядро, вокруг которого, словно планеты вокруг Солнца, движутся электроны. • Между ядром и электронами действуют силы притяжения, но упасть на ядро электроны не могут за счёт своего движения точно так же, как и планеты не падают на Солнце, хоть и притягиваются к нему. • Заряд ядра (+) равен суммарному заряду электронов (-), так что атом в целом электрически нейтрален. Планетарная модель атома Резерфорда
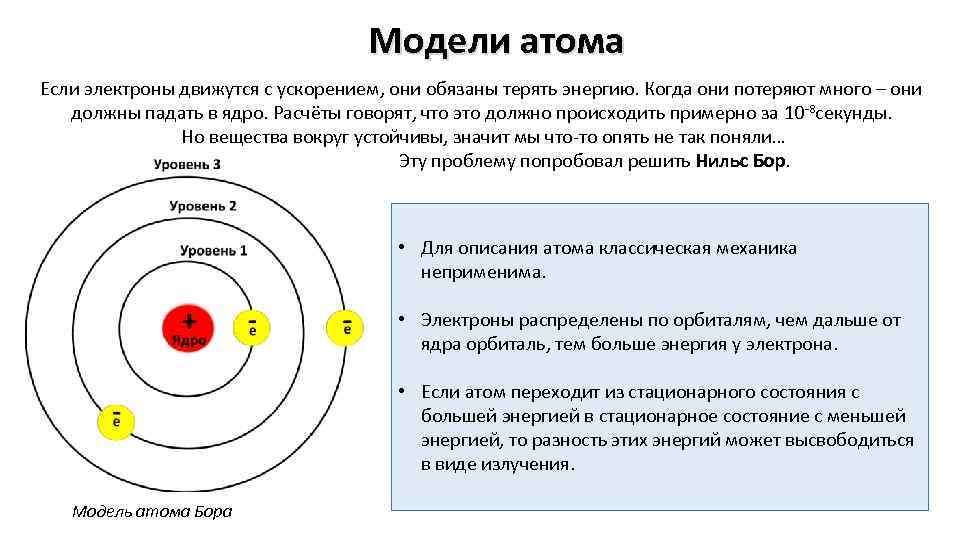 Модели атома Если электроны движутся с ускорением, они обязаны терять энергию. Когда они потеряют много – они должны падать в ядро. Расчёты говорят, что это должно происходить примерно за 10 -8 секунды. Но вещества вокруг устойчивы, значит мы что-то опять не так поняли… Эту проблему попробовал решить Нильс Бор. • Для описания атома классическая механика неприменима. • Электроны распределены по орбиталям, чем дальше от ядра орбиталь, тем больше энергия у электрона. • Если атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией, то разность этих энергий может высвободиться в виде излучения. Модель атома Бора
Модели атома Если электроны движутся с ускорением, они обязаны терять энергию. Когда они потеряют много – они должны падать в ядро. Расчёты говорят, что это должно происходить примерно за 10 -8 секунды. Но вещества вокруг устойчивы, значит мы что-то опять не так поняли… Эту проблему попробовал решить Нильс Бор. • Для описания атома классическая механика неприменима. • Электроны распределены по орбиталям, чем дальше от ядра орбиталь, тем больше энергия у электрона. • Если атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией, то разность этих энергий может высвободиться в виде излучения. Модель атома Бора
 Модели атома Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Современные представления не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома). Орбиталь – место где с вероятностью около 90 -99% есть электрон.
Модели атома Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Современные представления не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома). Орбиталь – место где с вероятностью около 90 -99% есть электрон.
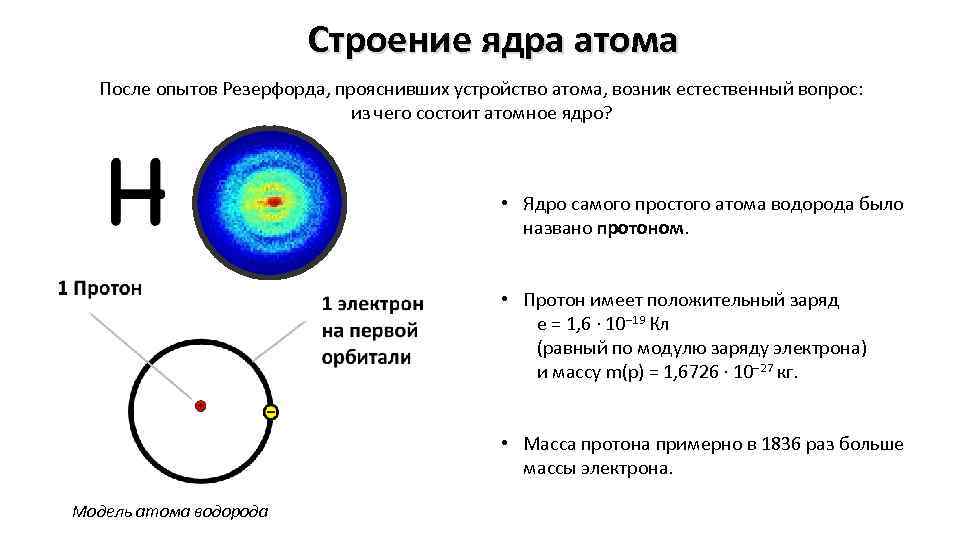 Строение ядра атома После опытов Резерфорда, прояснивших устройство атома, возник естественный вопрос: из чего состоит атомное ядро? • Ядро самого простого атома водорода было названо протоном. • Протон имеет положительный заряд e = 1, 6 · 10− 19 Кл (равный по модулю заряду электрона) и массу m(p) = 1, 6726 · 10− 27 кг. • Масса протона примерно в 1836 раз больше массы электрона. Модель атома водорода
Строение ядра атома После опытов Резерфорда, прояснивших устройство атома, возник естественный вопрос: из чего состоит атомное ядро? • Ядро самого простого атома водорода было названо протоном. • Протон имеет положительный заряд e = 1, 6 · 10− 19 Кл (равный по модулю заряду электрона) и массу m(p) = 1, 6726 · 10− 27 кг. • Масса протона примерно в 1836 раз больше массы электрона. Модель атома водорода
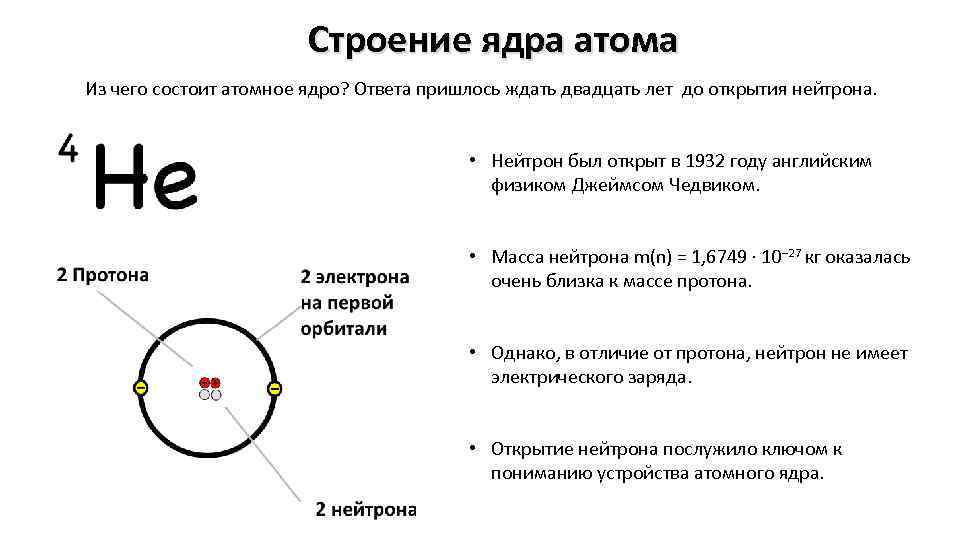 Строение ядра атома Из чего состоит атомное ядро? Ответа пришлось ждать двадцать лет до открытия нейтрона. • Нейтрон был открыт в 1932 году английским физиком Джеймсом Чедвиком. • Масса нейтрона m(n) = 1, 6749 · 10− 27 кг оказалась очень близка к массе протона. • Однако, в отличие от протона, нейтрон не имеет электрического заряда. • Открытие нейтрона послужило ключом к пониманию устройства атомного ядра.
Строение ядра атома Из чего состоит атомное ядро? Ответа пришлось ждать двадцать лет до открытия нейтрона. • Нейтрон был открыт в 1932 году английским физиком Джеймсом Чедвиком. • Масса нейтрона m(n) = 1, 6749 · 10− 27 кг оказалась очень близка к массе протона. • Однако, в отличие от протона, нейтрон не имеет электрического заряда. • Открытие нейтрона послужило ключом к пониманию устройства атомного ядра.
 Строение ядра атома Протон • масса ~ 1 а. е. м (атомная единица массы) • Заряд +1 Нейтрон • масса ~ 1 а. е. м • Заряд 0 Электрон • масса ~ 5, 4*10 -4 а. е. м (можно пренебречь) • Заряд -1
Строение ядра атома Протон • масса ~ 1 а. е. м (атомная единица массы) • Заряд +1 Нейтрон • масса ~ 1 а. е. м • Заряд 0 Электрон • масса ~ 5, 4*10 -4 а. е. м (можно пренебречь) • Заряд -1
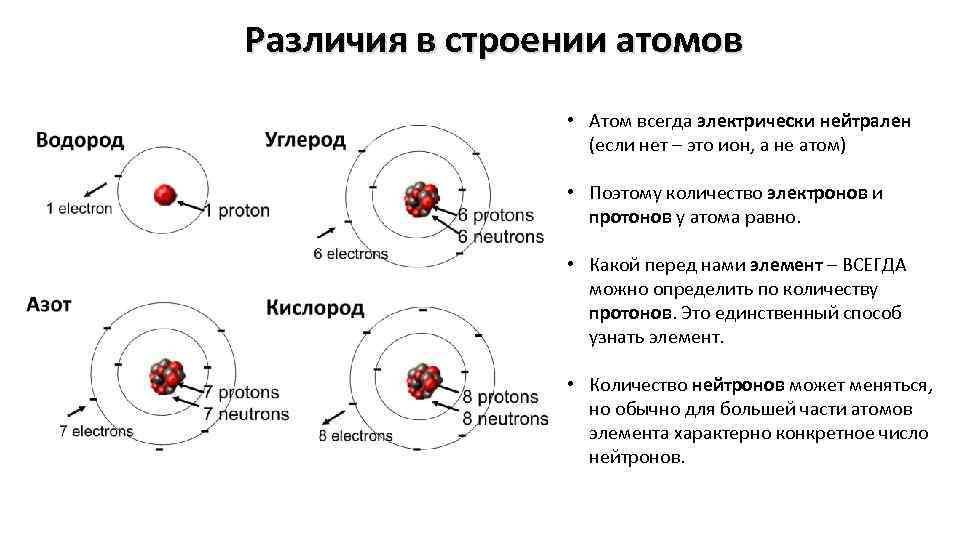 Различия в строении атомов • Атом всегда электрически нейтрален (если нет – это ион, а не атом) • Поэтому количество электронов и протонов у атома равно. • Какой перед нами элемент – ВСЕГДА можно определить по количеству протонов. Это единственный способ узнать элемент. • Количество нейтронов может меняться, но обычно для большей части атомов элемента характерно конкретное число нейтронов.
Различия в строении атомов • Атом всегда электрически нейтрален (если нет – это ион, а не атом) • Поэтому количество электронов и протонов у атома равно. • Какой перед нами элемент – ВСЕГДА можно определить по количеству протонов. Это единственный способ узнать элемент. • Количество нейтронов может меняться, но обычно для большей части атомов элемента характерно конкретное число нейтронов.
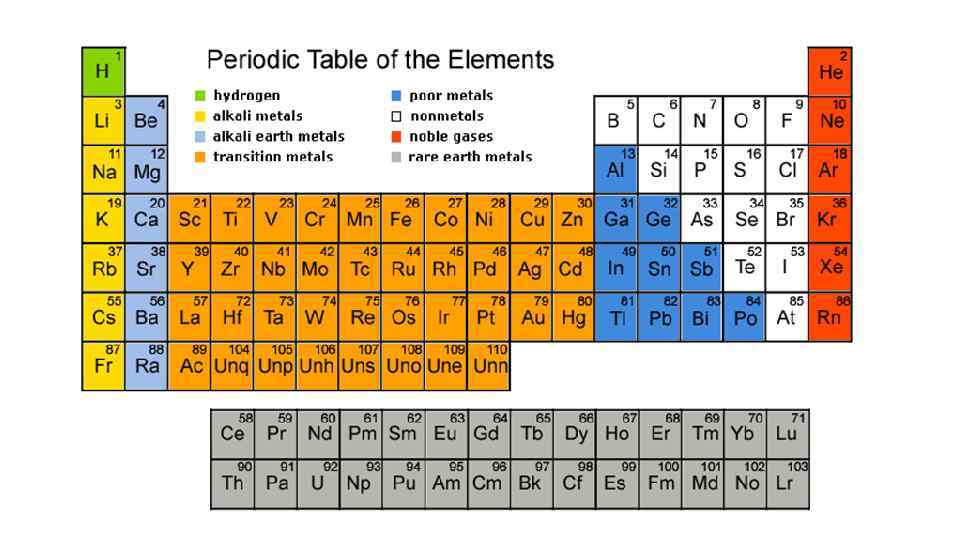
 Периодическая таблица • Порядковый номер = количество протонов • Относительная масса. 1 = 1/12 массы атома углерода (раньше 1 = массе атома водорода) • Вообще-то из положения элемента в таблице можно много сказать о его свойствах. Но это позже. • Количество электронов = количеству протонов. • Количество нейтронов = атомная масса округленная до целого – количество протонов (электроны почти ничего не весят)
Периодическая таблица • Порядковый номер = количество протонов • Относительная масса. 1 = 1/12 массы атома углерода (раньше 1 = массе атома водорода) • Вообще-то из положения элемента в таблице можно много сказать о его свойствах. Но это позже. • Количество электронов = количеству протонов. • Количество нейтронов = атомная масса округленная до целого – количество протонов (электроны почти ничего не весят)
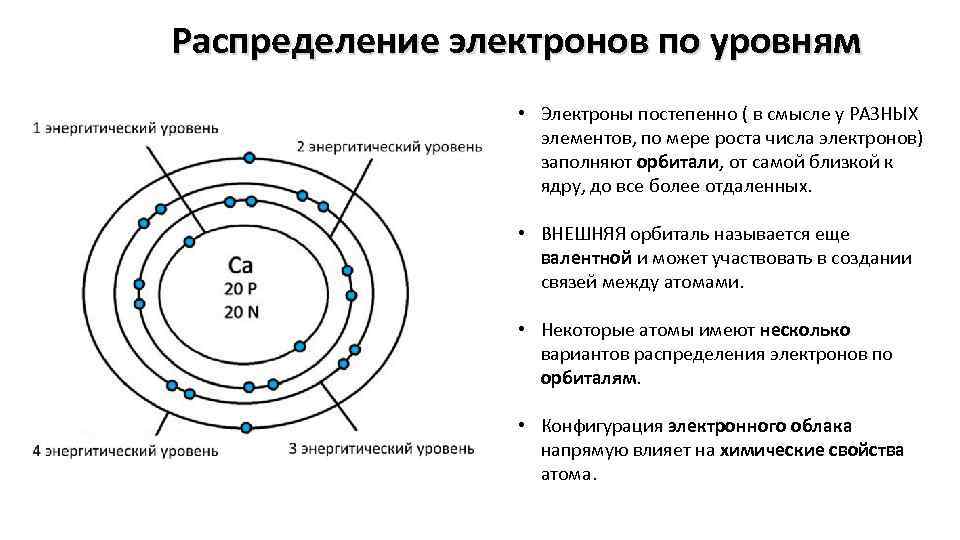 Распределение электронов по уровням • Электроны постепенно ( в смысле у РАЗНЫХ элементов, по мере роста числа электронов) заполняют орбитали, от самой близкой к ядру, до все более отдаленных. • ВНЕШНЯЯ орбиталь называется еще валентной и может участвовать в создании связей между атомами. • Некоторые атомы имеют несколько вариантов распределения электронов по орбиталям. • Конфигурация электронного облака напрямую влияет на химические свойства атома.
Распределение электронов по уровням • Электроны постепенно ( в смысле у РАЗНЫХ элементов, по мере роста числа электронов) заполняют орбитали, от самой близкой к ядру, до все более отдаленных. • ВНЕШНЯЯ орбиталь называется еще валентной и может участвовать в создании связей между атомами. • Некоторые атомы имеют несколько вариантов распределения электронов по орбиталям. • Конфигурация электронного облака напрямую влияет на химические свойства атома.
 Распределение электронов по уровням • Первая орбиталь включает только S подуровень • Вторая – S и P подуровни • Третья S, P и D подуровни • Четвертая – S, P, D и F подуровни • Они заполняются так, чтобы суммарная энергия была минимальна. • S вмещает 2 электрона • P вмещает 6 электронов • D вмещает 10 электронов
Распределение электронов по уровням • Первая орбиталь включает только S подуровень • Вторая – S и P подуровни • Третья S, P и D подуровни • Четвертая – S, P, D и F подуровни • Они заполняются так, чтобы суммарная энергия была минимальна. • S вмещает 2 электрона • P вмещает 6 электронов • D вмещает 10 электронов
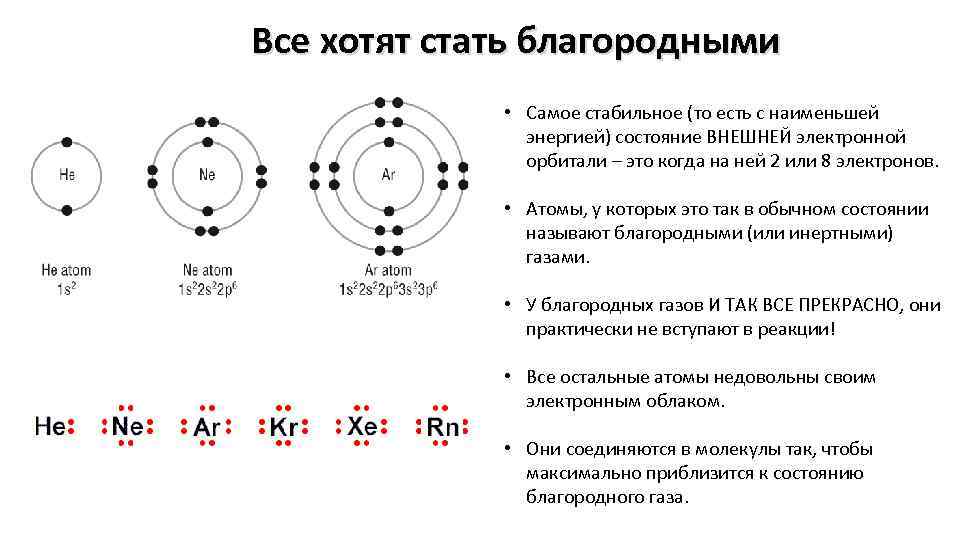 Все хотят стать благородными • Самое стабильное (то есть с наименьшей энергией) состояние ВНЕШНЕЙ электронной орбитали – это когда на ней 2 или 8 электронов. • Атомы, у которых это так в обычном состоянии называют благородными (или инертными) газами. • У благородных газов И ТАК ВСЕ ПРЕКРАСНО, они практически не вступают в реакции! • Все остальные атомы недовольны своим электронным облаком. • Они соединяются в молекулы так, чтобы максимально приблизится к состоянию благородного газа.
Все хотят стать благородными • Самое стабильное (то есть с наименьшей энергией) состояние ВНЕШНЕЙ электронной орбитали – это когда на ней 2 или 8 электронов. • Атомы, у которых это так в обычном состоянии называют благородными (или инертными) газами. • У благородных газов И ТАК ВСЕ ПРЕКРАСНО, они практически не вступают в реакции! • Все остальные атомы недовольны своим электронным облаком. • Они соединяются в молекулы так, чтобы максимально приблизится к состоянию благородного газа.
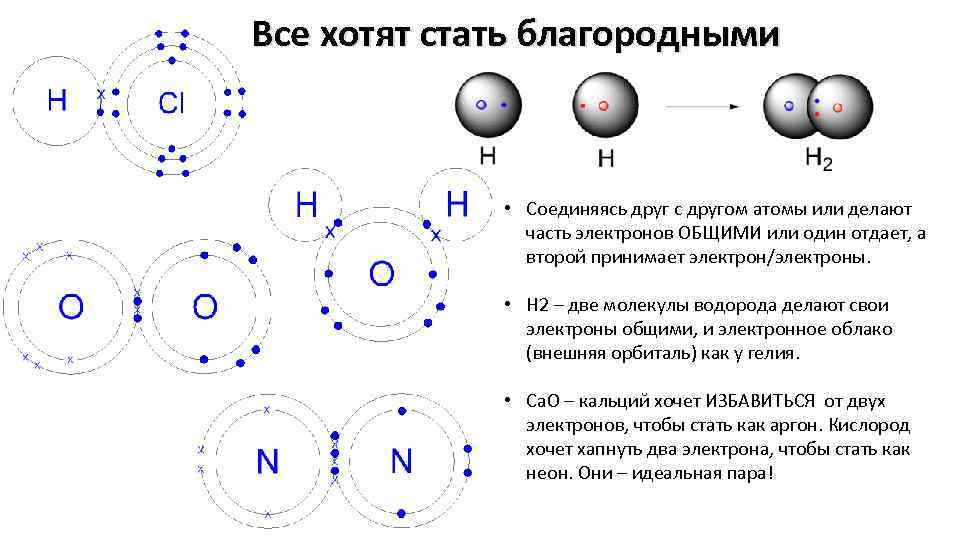 Все хотят стать благородными • Соединяясь друг с другом атомы или делают часть электронов ОБЩИМИ или один отдает, а второй принимает электрон/электроны. • H 2 – две молекулы водорода делают свои электроны общими, и электронное облако (внешняя орбиталь) как у гелия. • Сa. O – кальций хочет ИЗБАВИТЬСЯ от двух электронов, чтобы стать как аргон. Кислород хочет хапнуть два электрона, чтобы стать как неон. Они – идеальная пара!
Все хотят стать благородными • Соединяясь друг с другом атомы или делают часть электронов ОБЩИМИ или один отдает, а второй принимает электрон/электроны. • H 2 – две молекулы водорода делают свои электроны общими, и электронное облако (внешняя орбиталь) как у гелия. • Сa. O – кальций хочет ИЗБАВИТЬСЯ от двух электронов, чтобы стать как аргон. Кислород хочет хапнуть два электрона, чтобы стать как неон. Они – идеальная пара!


