Строение вещества 4 л 2016.ppt
- Количество слайдов: 38
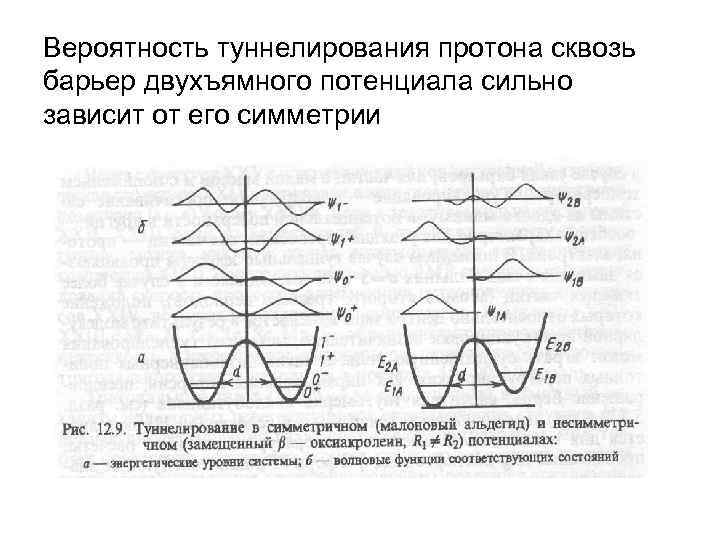
Вероятность туннелирования протона сквозь барьер двухъямного потенциала сильно зависит от его симметрии

• При симметричном профиле ППЭ волновые функции системы делокализованы по двум ямам, тогда как ассиметричный потенциал (R 1≠R 2) характеризуется локализацией собственных функций вблизи минимума. • Следовательно, при симметричном профиле ППЭ вероятность туннелирования протона сквозь барьер выше.
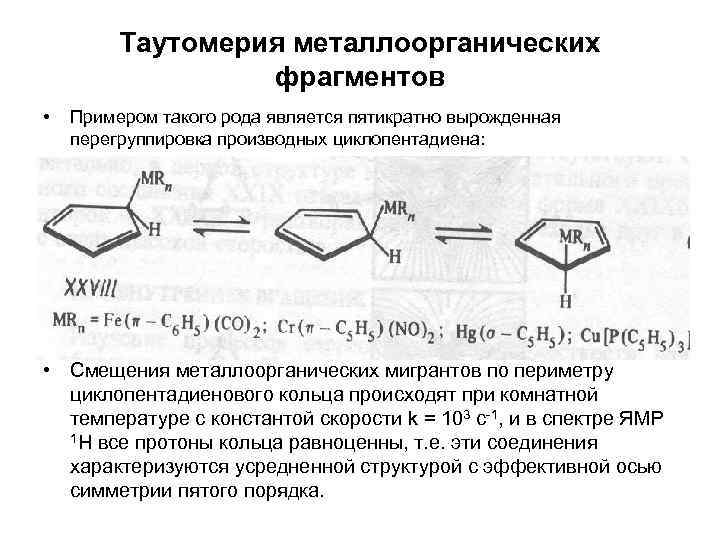
Таутомерия металлоорганических фрагментов • Примером такого рода является пятикратно вырожденная перегруппировка производных циклопентадиена: • Смещения металлоорганических мигрантов по периметру циклопентадиенового кольца происходят при комнатной температуре с константой скорости k = 103 c-1, и в спектре ЯМР 1 Н все протоны кольца равноценны, т. е. эти соединения характеризуются усредненной структурой с эффективной осью симметрии пятого порядка.
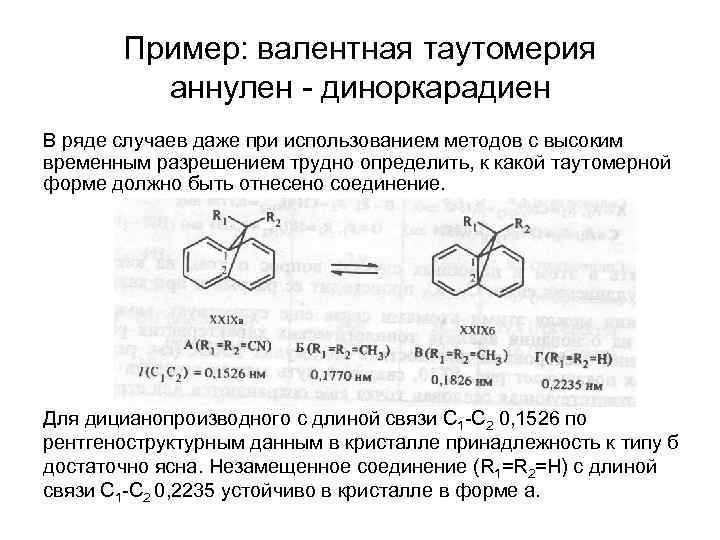
Пример: валентная таутомерия аннулен - диноркарадиен В ряде случаев даже при использованием методов с высоким временным разрешением трудно определить, к какой таутомерной форме должно быть отнесено соединение. Для дицианопроизводного с длиной связи С 1 -С 2 0, 1526 по рентгеноструктурным данным в кристалле принадлежность к типу б достаточно ясна. Незамещенное соединение (R 1=R 2=H) c длиной связи С 1 -С 2 0, 2235 устойчиво в кристалле в форме а.
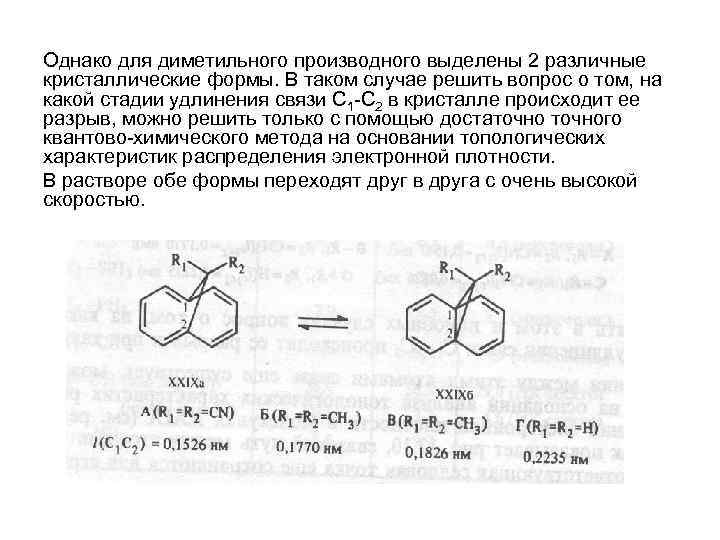
Однако для диметильного производного выделены 2 различные кристаллические формы. В таком случае решить вопрос о том, на какой стадии удлинения связи С 1 -С 2 в кристалле происходит ее разрыв, можно решить только с помощью достаточного квантово-химического метода на основании топологических характеристик распределения электронной плотности. В растворе обе формы переходят друг в друга с очень высокой скоростью.

• Приведенные примеры показывают, что туннельные процессы в явном и ярком виде наблюдаются в эксперименте при низких, чаще всего гелиевых температурах. Это, однако, не означает, что туннельные процессы не происходят при более высоких температурах. В обычных условиях значительно труднее отделить квантовые эффекты от движений по классическим траекториям, которые происходят одновременно. Поэтому при высоких температурах туннельные явления описываются как поправки к классическому рассмотрению.

Зависимость спектра ЯМР нежестких молекул от температуры • Поскольку константа скорости взаимного превращения изомеров в таких структурах является функцией температуры, для одного и того же процесса при разных температурах можно выполнить условия как быстрого, так и медленного превращения.
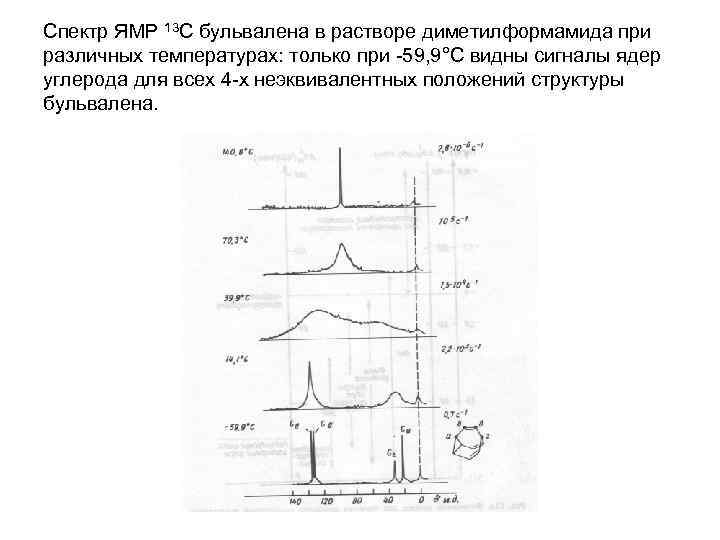
Спектр ЯМР 13 С бульвалена в растворе диметилформамида при различных температурах: только при -59, 9°С видны сигналы ядер углерода для всех 4 -х неэквивалентных положений структуры бульвалена.
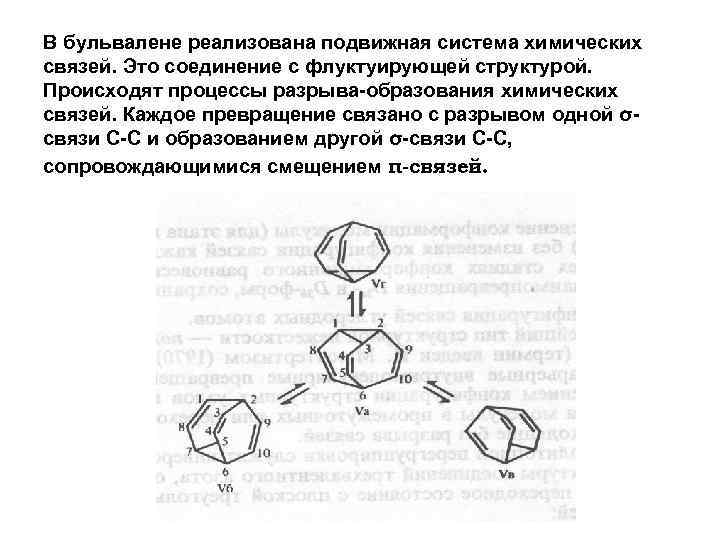
В бульвалене реализована подвижная система химических связей. Это соединение с флуктуирующей структурой. Происходят процессы разрыва-образования химических связей. Каждое превращение связано с разрывом одной σсвязи С-С и образованием другой σ-связи С-С, сопровождающимися смещением π-связей.

Температурная зависимость превращений бульвалена в спектре ЯМР • При низкой температуре скорость (частота) взаимопревращений изомеров мала по сравнению с разностью резонансных частот любой пары неэквивалентных ядер углерода. При повышении температуры раствора скорость перегруппировок растет, достигает и превосходит диапазон химических сдвигов неэквивалентных ядер 13 С. Выше 70°С в спектре ЯМР 13 С фиксируется только один сигнал от ядер 13 С. Это означает, что в рамках метода ЯМР 13 С все группы СН в бульвалене при этих температурах эквивалентны.
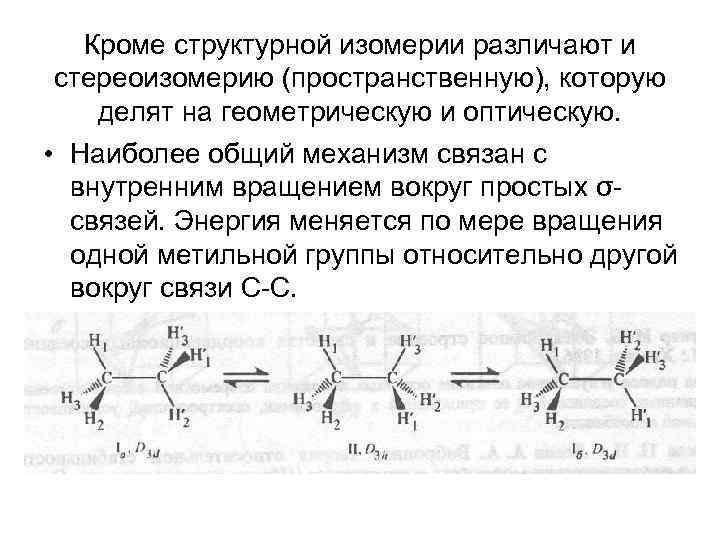
Кроме структурной изомерии различают и стереоизомерию (пространственную), которую делят на геометрическую и оптическую. • Наиболее общий механизм связан с внутренним вращением вокруг простых σсвязей. Энергия меняется по мере вращения одной метильной группы относительно другой вокруг связи С-С.
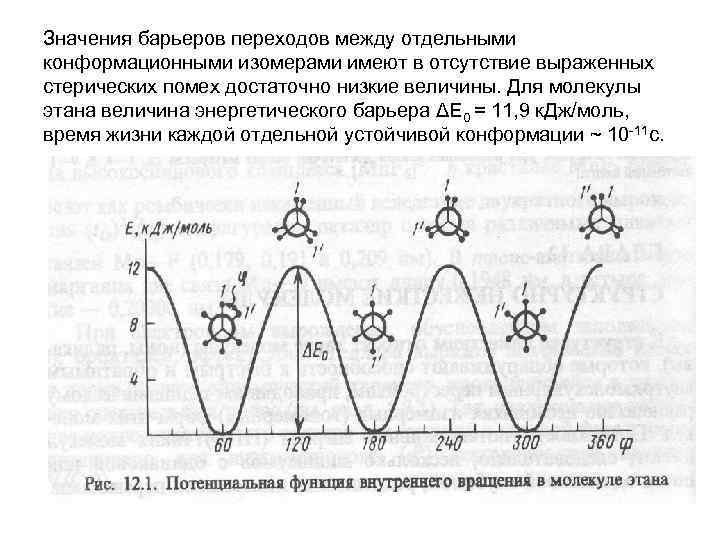
Значения барьеров переходов между отдельными конформационными изомерами имеют в отсутствие выраженных стерических помех достаточно низкие величины. Для молекулы этана величина энергетического барьера ΔЕ 0 = 11, 9 к. Дж/моль, время жизни каждой отдельной устойчивой конформации ~ 10 -11 с.
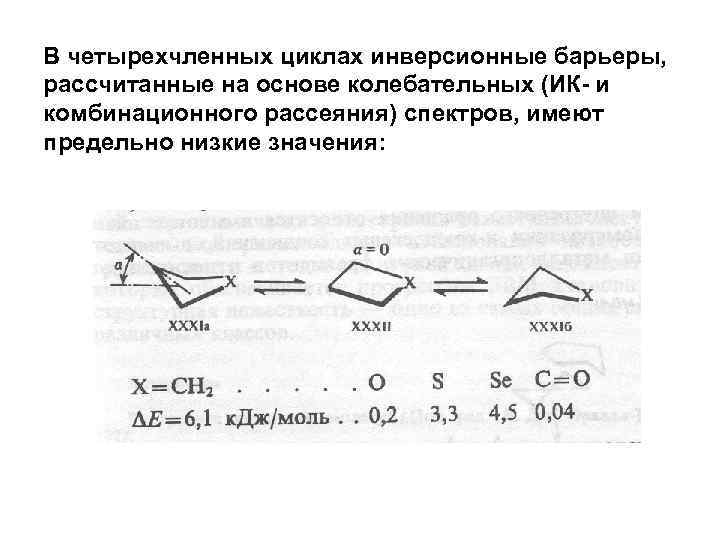
В четырехчленных циклах инверсионные барьеры, рассчитанные на основе колебательных (ИК- и комбинационного рассеяния) спектров, имеют предельно низкие значения:

Политопные перегруппировки – это низкобарьерные внутримолекулярные превращения, связанные с изменением конфигурации структурных узлов молекулы, происходящие без разрыва связей • Пример – инверсия пирамидальной структуры соединений трехвалентного азота, осуществляющаяся через переходное плоское состояние. В этом процессе молекула аммиака выворачивается подобно зонтику на ветру.
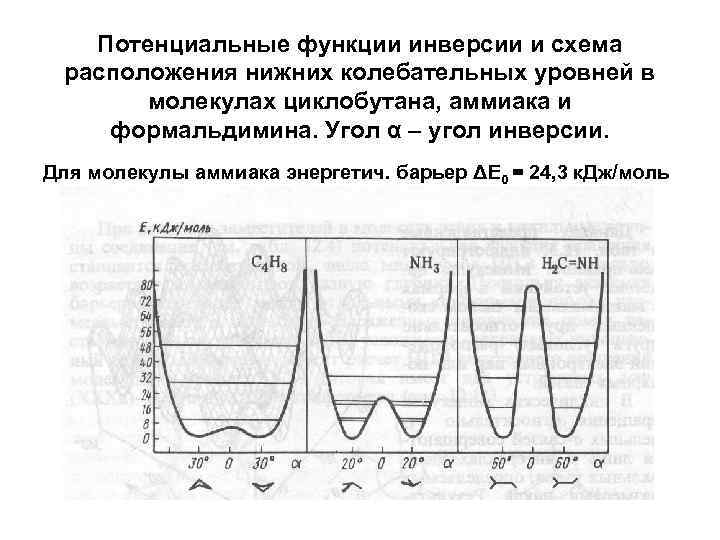
Потенциальные функции инверсии и схема расположения нижних колебательных уровней в молекулах циклобутана, аммиака и формальдимина. Угол α – угол инверсии. Для молекулы аммиака энергетич. барьер ΔЕ 0 = 24, 3 к. Дж/моль

• Процесс инверсии для аммиака проявляется в эксперименте как расщепление полосы зонтичного колебания в ИК-спектрах. • В общем случае для тригональнопирамидальных молекул AL 3 барьер инверсии зависит от индивидуальной природы А и L и может достигать высоких значений, что сразу делает молекулу жесткой: 240 к. Дж/моль для NF 3 против 24, 3 к. Дж/моль для NH 3 Молекула жесткая – т. е. энергетический барьер практически непреодолим.

Как видно из табл. , значения барьеров инверсии охватывают чрезвычайно широкий диапазон – от 3 -9 к. Дж/моль для отличающейся исключительной структурной нежесткостью метиланиона, катиона гидроксония и аммиака до 140 -690 к. Дж/моль в структурно жестких молекулах фосфина, трифторида азота и трифторида фосфора.

Цис-транс изомерия • Для изомеров, переходящих друг в друга при вращении вокруг двойной связи, обычно обеспечивается стабильность и возможность разделения (это связано с большой величиной энергетических барьеров). «Транс» по-латыни – это «через» , «за» . Приставка «цис» так и переводится с латыни – «по одну сторону» . • При наличии нескольких двойных связей число возможных изомеров быстро увеличивается: для несимметричной цепи с n двойными связями возможно 2 n стереоизомеров.
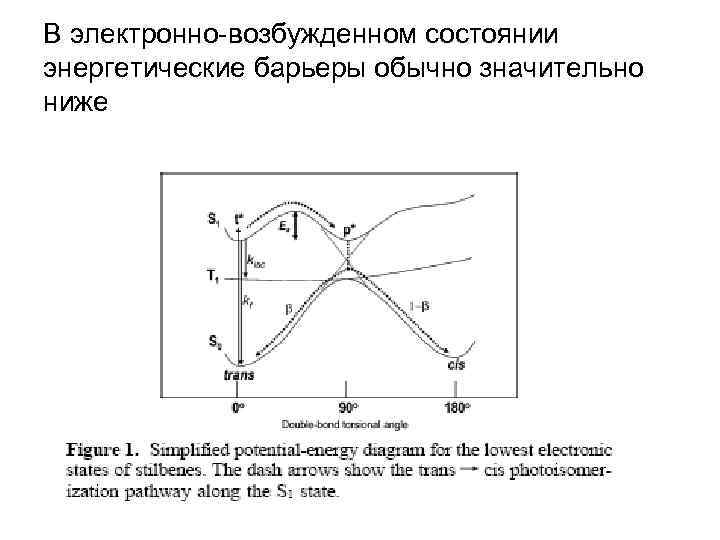
В электронно-возбужденном состоянии энергетические барьеры обычно значительно ниже
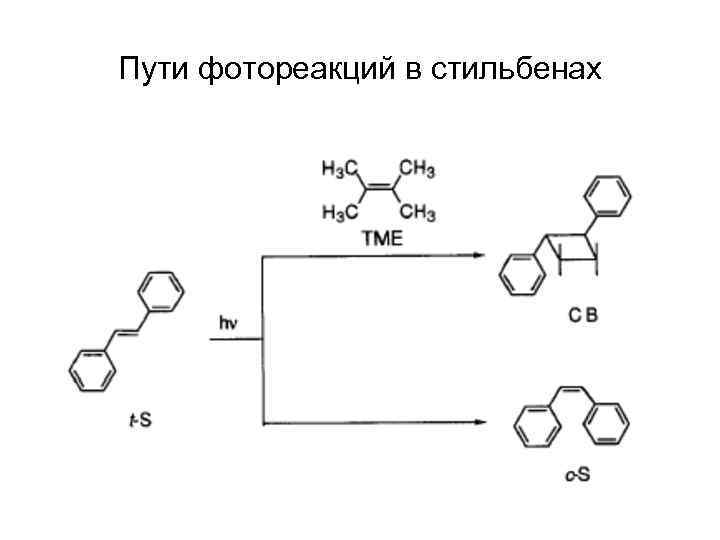
Пути фотореакций в стильбенах
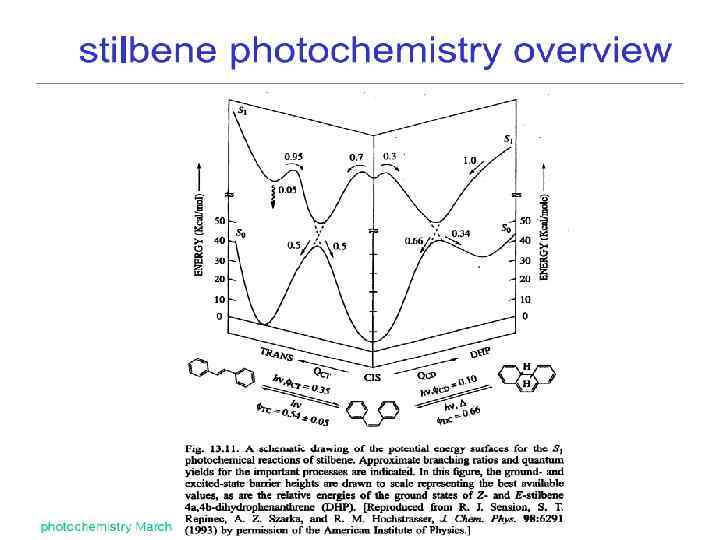

Экспериментальные данные свидетельствуют о том, что обычно транс-изомеры более стабильны, однако, например, в случае природных жирных кислот (олеиновая, линолевая и т. д. ) преобладают структуры с полностью цис-конфигурацией. Можно прочитать информацию о вредном воздействии на организм маргарина в связи с тем, что в нем содержатся транс-изомеры ненасыщенных жирных кислот. Между тем их цис-изомеры необходимы человеку как клеточный строительный материал. Но в процессе превращения растительного масла в маргарин по технологии промышленного производства происходит частичное превращение цис-изомеров во вредные транс-изомеры. Попытки изменения технологии приготовления маргарина существенно удорожают продукт.

Изомерия координационных соединений • В таких системах проявления изомерии расширяются, возникают новые варианты. • Существует координационная изомерия, когда изомеры отличаются химическим составом двух координационных сфер. • Лигандная изомерия, когда двойники различаются химическим составом лигандов лишь в одной координационной сфере.
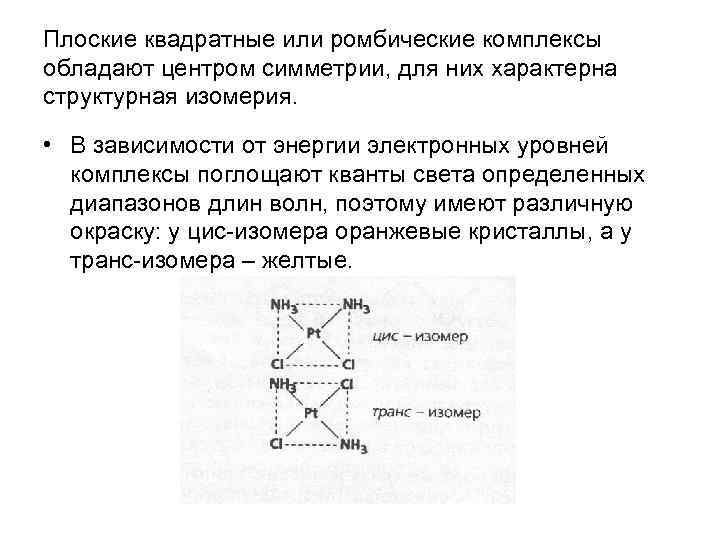
Плоские квадратные или ромбические комплексы обладают центром симметрии, для них характерна структурная изомерия. • В зависимости от энергии электронных уровней комплексы поглощают кванты света определенных диапазонов длин волн, поэтому имеют различную окраску: у цис-изомера оранжевые кристаллы, а у транс-изомера – желтые.

Практически важный момент • Существование изомерии приходится принимать во внимание при создании новых лекарственных препаратов. В 1969 г. было установлено, что цис[Pt(NH 3)2 Cl 2] обладает отчетливо выраженными противоопухолевыми свойствами, тогда как у транс-изомера они полностью отсутствуют.
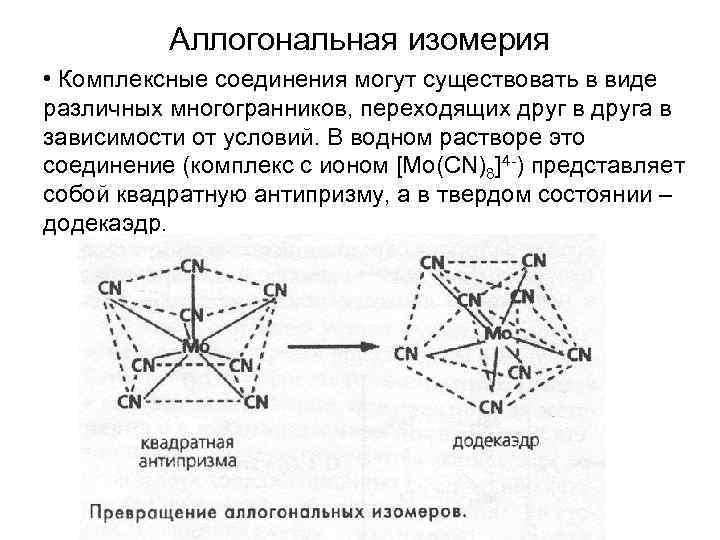
Аллогональная изомерия • Комплексные соединения могут существовать в виде различных многогранников, переходящих друг в друга в зависимости от условий. В водном растворе это соединение (комплекс с ионом [Mo(CN)8]4 -) представляет собой квадратную антипризму, а в твердом состоянии – додекаэдр.
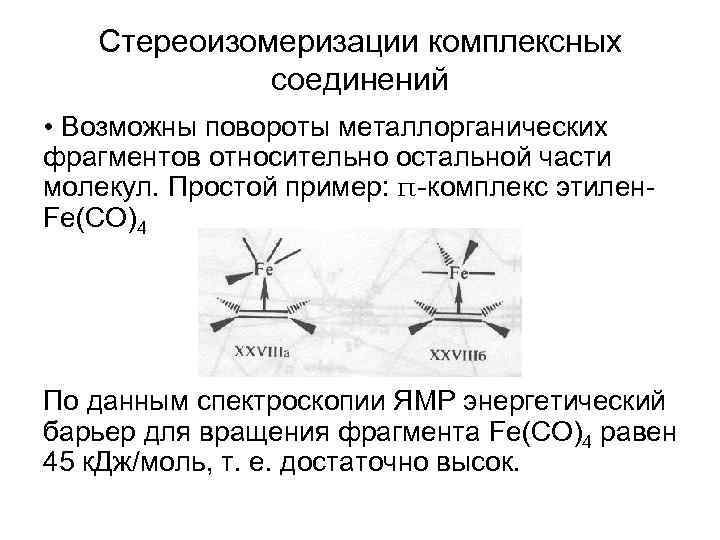
Стереоизомеризации комплексных соединений • Возможны повороты металлорганических фрагментов относительно остальной части молекул. Простой пример: π-комплекс этилен. Fe(CO)4 По данным спектроскопии ЯМР энергетический барьер для вращения фрагмента Fe(CO)4 равен 45 к. Дж/моль, т. е. достаточно высок.
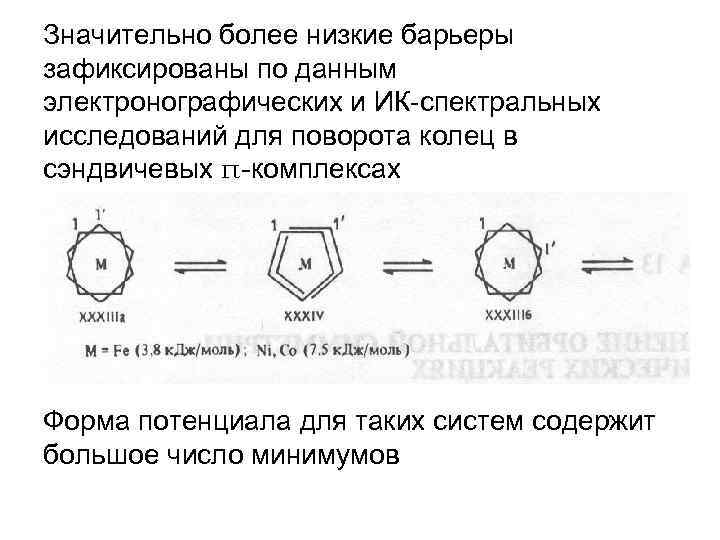
Значительно более низкие барьеры зафиксированы по данным электронографических и ИК-спектральных исследований для поворота колец в сэндвичевых π-комплексах Форма потенциала для таких систем содержит большое число минимумов

Спиновые изомеры Это координационные соединения, у которых в зависимости от температуры или иных факторов изменяется лишь число неспаренных электронов, тогда как все остальное (стехиометрический состав, лиганды, их взаимное расположение, даже геометрия координационного многогранника) одинаково. Изомер хелата железа, содержащий один неспаренный электрон, существует при низкой температуре (< 270 К), а с 5 такими электронами – при высокой. Окраской эти изомеры также отличаются, т. к. набор разрешенных электронных переходов, ответственных за цвет в видимой области спектра, у них резко различен.

Электронная природа структурной нежесткости молекул В случае жесткой молекулы, отвечающей устойчивой структуре, минимум потенциальной поверхности имеет значительную глубину (ΔЕ > 90 -100 к. Дж/моль). В случае структурно нежестких молекул существует по крайней мере одна из внутренних координат, смещение по которой в сторону ближайшего минимума ППЭ сопряжено с преодолением достаточно малого энергетического барьера.
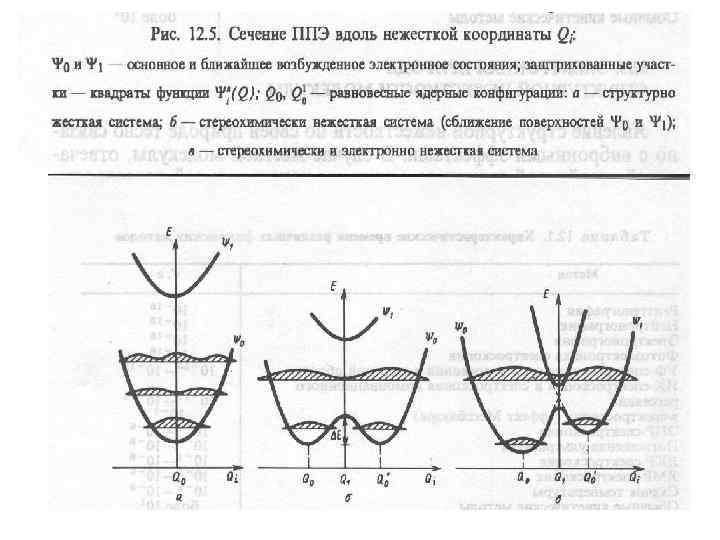

• Стереохимическая нежесткость (рис. б) характерна для систем с внутренним вращениям, а также для систем, способных к политопным и таутомерным перегруппировкам. • Если движение по нежесткой координате сопряжено с пересечением поверхностей электронных состояний, то это приводит к появлению электронно нежестких систем (рис. в). • Многочисленные примеры электронной нежесткости, сопряженной со стереохимической, обнаружены в координационных соединениях переходных металлов с не полностью заполненными dоболочками.

Волновая функция для электронно нежестких систем Она представляется как суперпозиция всех n вырожденных электронных состояний: Вклад отдельного электронного состояния зависит от колебательных состояний. Изменяя при варьировании температуры заселенность колебательных уровней, можно варьировать одновременно и ядерную конфигурацию, и электронные свойства молекулярной системы.
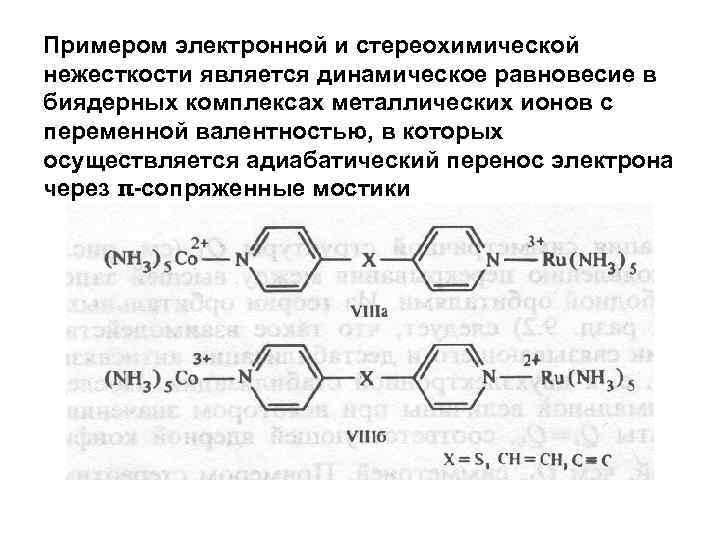
Примером электронной и стереохимической нежесткости является динамическое равновесие в биядерных комплексах металлических ионов с переменной валентностью, в которых осуществляется адиабатический перенос электрона через π-сопряженные мостики

Наряду с геометрической перестройкой при этих процессах резко перестраивается электронная конфигурация, что четко отражается изменениями в электронных спектрах поглощения и люминесценции. Величины энергетических барьеров меняются в широких пределах в зависимости от природы мостиковой группы. С развитием техники экспериментальных исследований низкобарьерных перегруппировок и методов квантовой химии, надежность предсказаний которых повышается, становится ясно, что нежесткость – одно из самых общих свойств молекул различных классов.

Оптическая изомерия Луи Пастер, 1850 г. ; при кристаллизации натрий -аммониевой соли виноградной кислоты из водного раствора. Он сумел под лупой с помощью пинцета разделить два типа кристаллов, различающихся ориентацией одной из граней. Водные растворы двух типов кристаллов отличались только тем, что по разному вращали плоскость поляризации (плоскость колебаний) световых волн (дисперсия оптического вращения). Различная оптическая активность.

Оптические изомеры или энантиомеры представляют собой стереоизомеры, структуры которых несовместимы с их зеркальными отражениями. Это один из самых сложных типов изомерии. • Такие молекулы называются хиральными. • Как и в общей проблеме определения структуры изомеров, возможность обнаружения хиральности зависит от характеристического времени соответствующего физического метода. • При простом изменении температуры одна и та же структура может вести себя в одном случае как хиральная, а в другом – как ахиральная.

• При данных условиях наблюдения молекула является хиральной, если существует её мгновенная геометрия, которая не может быть совмещена со своим зеркальным отражением при вращении и поступательном движении молекулы как целого, а также при внутримолекулярных движениях, которые допустимы в указанных условиях. • Свойства хиральности обусловлены внутренней асимметрией молекул. Эти молекулы отличаются огромным структурным разнообразием. Такое количество вариантов структуры может быть одним из источников значительного разнообразия биологических веществ, построенных именно из хиральных молекул.
Строение вещества 4 л 2016.ppt