Лекция Кинетика ферментативных реакций.ppt
- Количество слайдов: 16


Ведущую роль в механизме ферментативного катализа играет образование ферментсубстратных комплексов.

I фаза Между субстратом и ферментом возникает соединение, в котором первый и второй связаны друг с другом ковалентной или иного типа связью.

II фаза Cубстрат под действием присоединенного к нему фермента претерпевает изменение, делающее его более доступным для соответствующей химической реакции.

III фаза Происходит сама химическая реакция (на поверхности фермента)

IV фаза Образовавшийся продукт реакции освобождается из ферментсубстратного комплекса.

Если обозначить фермент буквой Е, субстрат – S, активированный субстрат – S и продукт реакции – Р, то последовательность процессов выразится схемой:

Одним из примеров может служить реакция переаминирования аминокислот с кетокислотами (переноса NH 2 -группы с аминокислоты на кетокислоту) под действием ферментов аминотранфераз. Эти ферменты двухкомпонентны: простетической группой во всех случаях является пиридоксальфосфат. Различные аминотранферазы отличаются друг от друга белковой частью.

Примером реакции переаминирования может служить следующий процесс:
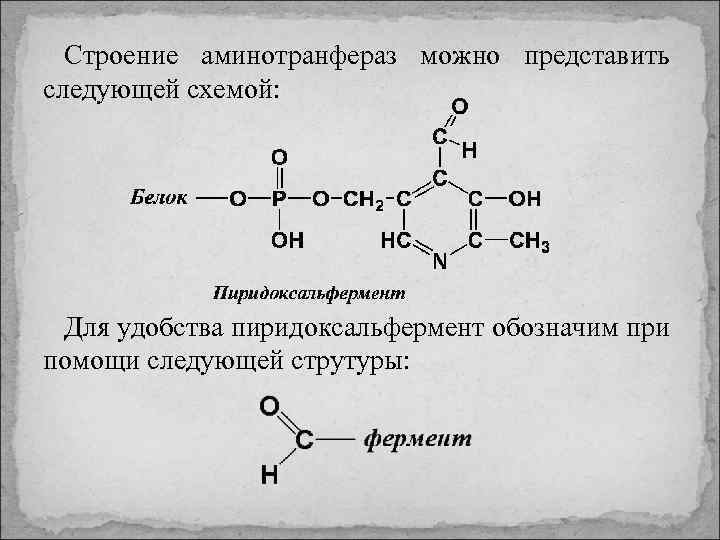
Строение аминотранфераз можно представить следующей схемой: Для удобства пиридоксальфермент обозначим при помощи следующей струтуры:
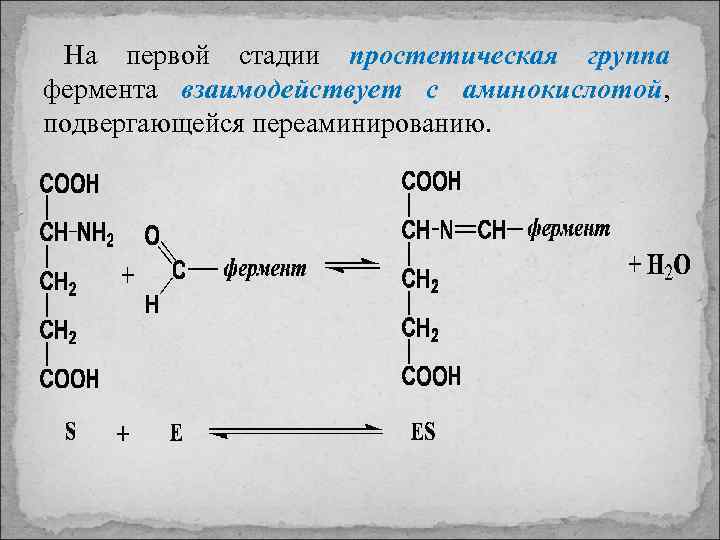
На первой стадии простетическая группа фермента взаимодействует с аминокислотой, подвергающейся переаминированию.
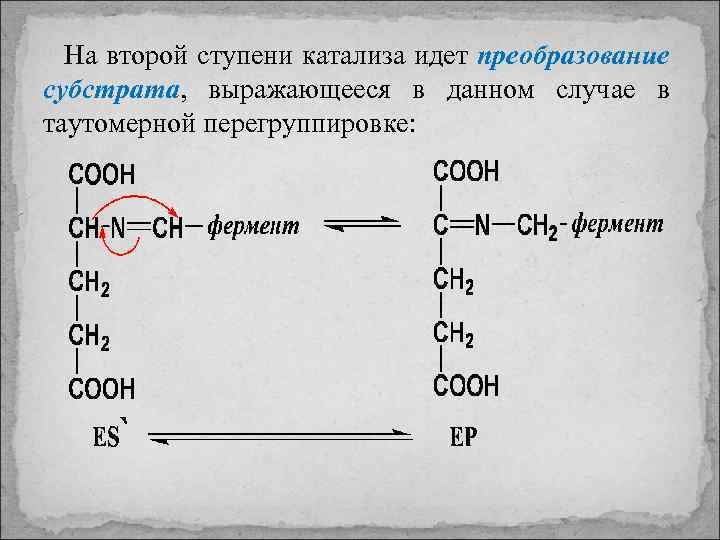
На второй ступени катализа идет преобразование субстрата, выражающееся в данном случае в таутомерной перегруппировке:
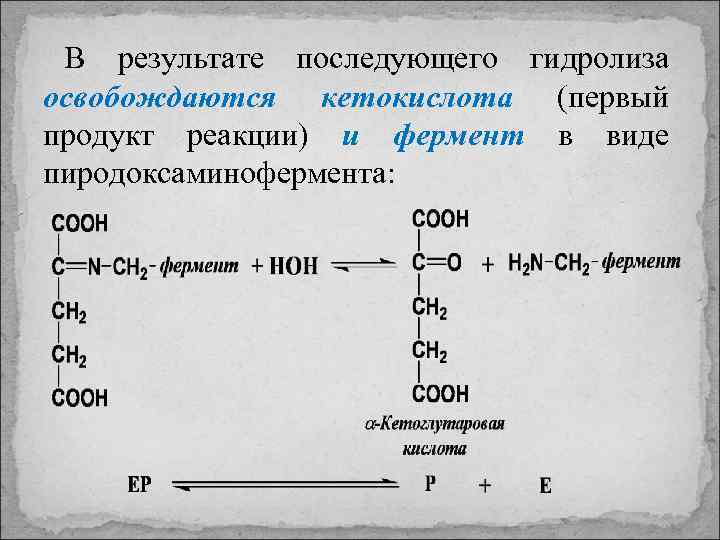
В результате последующего гидролиза освобождаются кетокислота (первый продукт реакции) и фермент в виде пиродоксаминофермента:

Далее между пиридоксаминоферментом и другой кетокислотой вновь возникает ферментсубстратный комплекс:
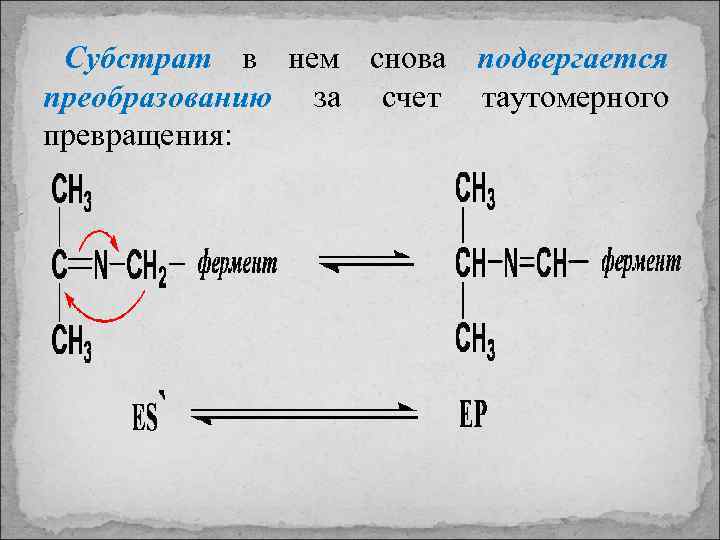
Субстрат в нем снова подвергается преобразованию за счет таутомерного превращения:

Полученное соединение гидролизуется и возникает новая аминокислота (2 -ой продукт реакции переаминирования):
Лекция Кинетика ферментативных реакций.ppt