важнейшие понятия и законы химии1.pptx
- Количество слайдов: 50

Важнейшие понятия и законы химии 11 класс базовый уровень Шкатова Е. В.

Основные понятия ü химический элемент ü вещество ü химическая реакция ü атом ü молекула ü простое вещество ü сложное вещество и др.
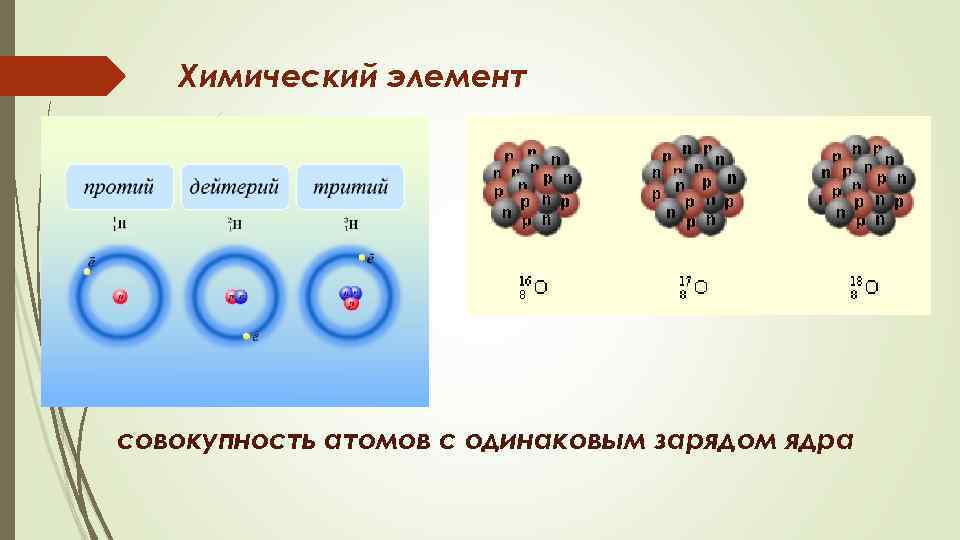
Химический элемент совокупность атомов с одинаковым зарядом ядра

Решение задач Рассчитайте относительную атомную массу меди, если известно, что мольная доля изотопа 63 Cu составляет приблизительно 69% от общего числа атомов меди, а доля изотопов 65 Cu – 31%.

Для самостоятельного решения Рассчитайте относительную атомную массу иридия, если известно, что доля нуклида 191 Ir составляет 37, 3% от общего количества атомов иридия, а доля нуклидов 193 Ir – 62, 7%
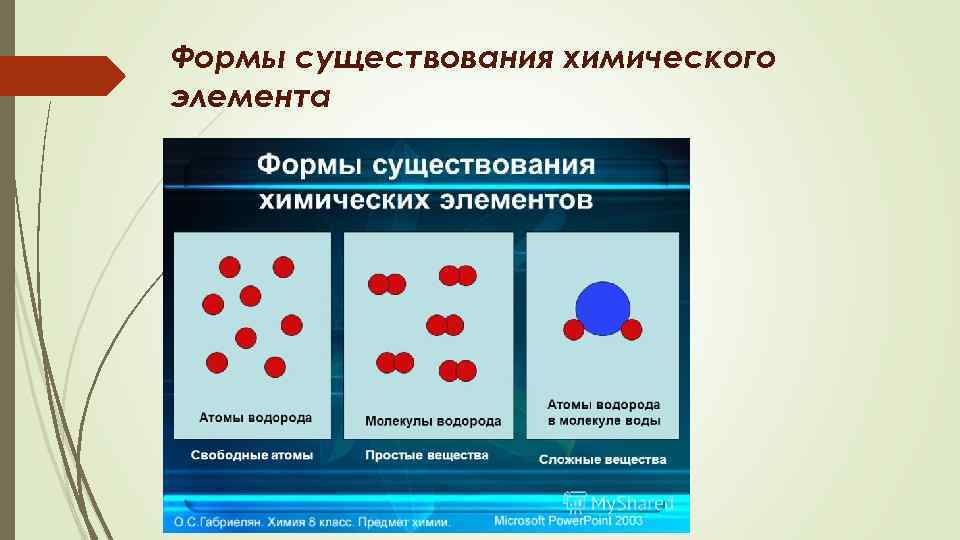
Формы существования химического элемента

Вещество – то, из чего состоят физические тела. Толковый словарь русского языка, 1982 Вещество, вид материи, которая обладает массой покоя. Состоит из элементарных частиц. Химическая энциклопедия, 1988 Вещество – совокупность дискретных образований, обладающих массой покоя (атомы, молекулы) и то, что из них состоит. Философский словарь Вещество - это нечто, занимающее пространство и имеющее массу. Химия в центре наук. Браун, Лемей

Свойства веществ Физические агрегатное состояние цвет запах растворимость температуры плавления и кипения теплопроводность электропроводность Химические проявляются в химических реакциях и характеризуют способность вещества взаимодействовать с другими веществами и превращаться в новые

Химическая реакция

Признаки химической реакции ü ü выделение или поглощение теплоты выпадение или исчезновение осадка изменение окраски или запаха выделение газа или света

Лабораторный эксперимент Cu. SO 4 + Na. OH Na 2 CO 3 + HCl Na. OH + ф/ф + HCl Какие признаки химических реакций вы наблюдали?

Уравнение химической реакции Cu. SO 4 + 2 Na. OH → Cu(OH)2 + Na 2 SO 4 Cu 2+ + 2 OH- →Cu(OH)2↓

Атомно – молекулярное учение ü Вещества состоят из частиц. ü Атомы - мельчайшие химически неделимые частицы. ü Многие вещества состоят из молекул. ü Молекулы образованы химически связанными атомами. ü Атомы, ионы, молекулы находятся в непрерывном движении.

Относительная атомная масса

Решение задач Масса молекулы белого фосфора составляет 2, 06*10 -22 г. Сколько атомов фосфора Образуют молекулу белого фосфора?

Для самостоятельного решения Используя периодическую систему, вычислите массу атомов А) натрия Б) серы

Относительная молекулярная масса

Решение задач Рассчитайте относительную молекулярную массу Ортофосфорной кислоты H 3 PO 4 Соляной кислоты HCl Оксида магния Mg. O Оксида серы (IV) SO 2 Оксида серы (VI) SO 3

Количество вещества

Решение задач В какой массе железа содержится столько же атомов, сколько их содержится в 119 г олова?

Для самостоятельного решения Какова масса кусочка платины, в котором содержится столько же атомов, сколько их содержится в 19, 7 г золота?
![Молярная масса [ г/моль ] М = Mr Молярная масса [ г/моль ] М = Mr](https://present5.com/presentation/9299796_326149475/image-22.jpg)
Молярная масса [ г/моль ] М = Mr

Решение задач Рассчитайте количество вещества и число частиц в порции натрия массой 46 г.

Для самостоятельного решения Рассчитайте количество вещества и число частиц, которое содержится в порции серы массой 16 г.

Примеры тестовых заданий Укажите формулы сложных веществ: А)C 2 H 5 OH Б)Cu В)O 2 Г)HCl При каких процессах протекают химические реакции? А)Фильтрование Б)Перегонка нефти В)Гидратация этилена Г)Разложение карбоната кальция Укажите единицу измерения количества вещества: А)г Б)кг В)а. е. м. Г)моль

Отметьте правильные утверждения: Относительная атомная масса А)показывает, во сколько раз масса атома больше 1/12 массы атома углерода 12 С Б)имеет размерность г/моль В)безразмерная величина Г)приведена в Периодической системе

Отметьте правильные утверждения: Постоянная Авогадро А)показывает число структурных единиц в 1 г вещества Б)показывает число структурных единиц в 1 моль вещества В)имеет размерность моль-1 Г)равна 22, 4 л

Домашнее задание § 1 В. 1, 2, 3, 4, 5 Творческое задание в. 8 - кроссворд

Закон постоянства состава вещества Ж. Пруст 1799 Качественный и количественный состав индивидуального химического соединения строго постоянен и не зависит от способа его получения теоретическая основа для выражения состава соединений с помощью химических формул

Дальтониды – вещества постоянного состава Бертоллиды – вещества переменного состава (оксиды титана Ti. O 0, 8 Ti. O 1, 2) Д. Дальтон К. -Л. Бертолле

Закон сохранения массы веществ Ломоносов 1748 Лавуазье Масса всех веществ, вступивших в реакцию равна массе всех веществ, образующихся в результате реакции. Теоретическая основа для составления уравнений химических реакций и расчетов по ним

Какая масса водорода потребуется для получения 36 г воды?

Для самостоятельного решения Какая масса оксида кальция образуется при разложении 50 г карбоната кальция? Ca. CO 3 → Ca. O + CO 2

Закон сохранения материи и её движения Е= 2 mc

Закон Авогадро 1811 В равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится равное число молекул.

Следствия из закона Авогадро Порции разных газов, в которых содержится одинаковое число молекул, при одинаковых условиях займут одинаковый объём

н. у. 0ºС, 101, 3 к. Па Vm = 22, 4 л/моль n = V/Vm

Некоторый газ массой 1 г занимает объём 0, 7 л (н. у. ). Определите, о каком газе идёт речь, если известно, что это простое вещество, молекула которого двухатомна.

Для самостоятельного решения Некоторый газ массой 10 г занимает объём 8 л (н. у. ). Определите, о каком газе идёт речь, если известно, что это простое вещество, молекула которого двухатомна.

Отношение объёмов реагирующих веществ, измеренных при одинаковых условиях, равно отношению стехиометрических коэффициентов, то есть равно отношению количеств веществ 3 H 2 + N 2 = 2 NH 3 3 моль 1 моль 2 моль

Вычислите, какой объём кислорода потребуется для полного сгорания 5 л пропана (объёмы газов приведены при одних и тех же условиях). C 3 H 8 + 5 O 2 → 3 CO 2 + 4 H 2 O

Для самостоятельного решения Вычислите, какой объём кислорода потребуется для полного сгорания 4 л бутана (объёмы газов приведены при одних и тех же условиях).

При одинаковых условиях отношение масс равных объёмов газов (то есть отношение значений плотностей газов) будет равно отношению их молярных масс ρ1/ρ2 = М 1/М 2 ρ1/ρ2 = D D – относительная плотность газа 1 по газу2

Вычислите относительную плотность по водороду: А) углекислого газа Б) метана

Для самостоятельного решения Найдите относительную плотность А) по водороду Б) по воздуху аммиака, оксида азота (IV) Среднюю молярную массу воздуха считать равной 29.

Примеры тестовых заданий Укажите молекулярную формулу газа, для которого относительная плотность по воздуху составляет 1, 586: а) SO 2; б) NO 2; в) N 2 O; г) NO.

Домашнее задание § 2 В. 1, 2, 3, 4 В. 1 - 5 Творческое задание сообщение о Ломоносове, Лавуазье, Авогадро, Прусте (по выбору) Кроссворд «Знаменитые химики»

Задачи повышенного уровня сложности В ходе качественного анализа некоторой соли выяснено, что в её состав входят атомы бария, хлора и молекулы воды. Результаты анализа следующие: массовая доля бария 56, 03% хлора – 28, 84% воды – 15, 02% Найдите формулу данного вещества.

важнейшие понятия и законы химии1.pptx