Молекулярная биотехнология 3.ppt
- Количество слайдов: 169

Важнейшие методы молекулярной биотехнологии http: //molbiotech. ucoz. ru/

Важнейшие методы молекулярной биотехнологии • Химический синтез дезоксирибополинуклеотидов • Молекулярная гибридизация • Полимеразная цепная реакция • Секвенирование ДНК

Химический синтез ДНК • Общий принцип • ДНК-синтезаторы • Подход удобен для синтеза олигонуклеотидов, используемых в различных работах по генетической инженерии • Возможен химический синтез генов
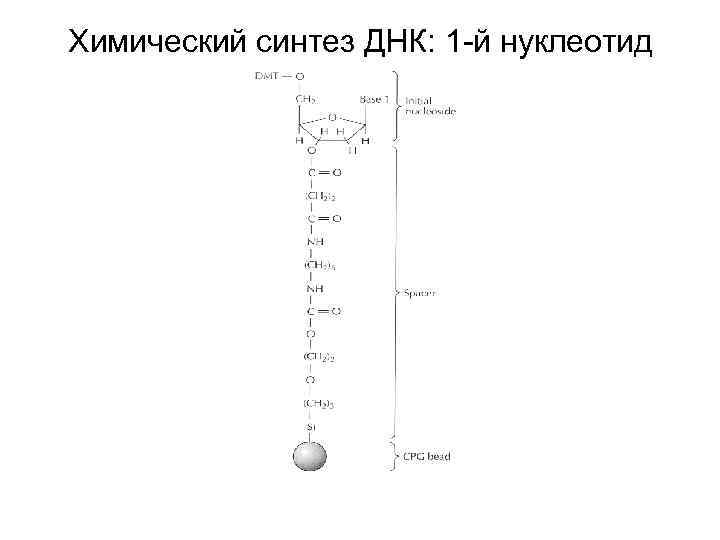
Химический синтез ДНК: 1 -й нуклеотид
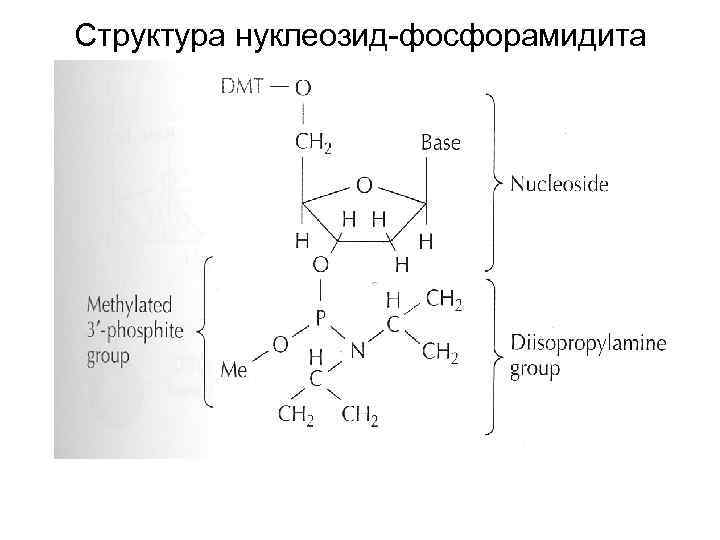
Структура нуклеозид-фосфорамидита
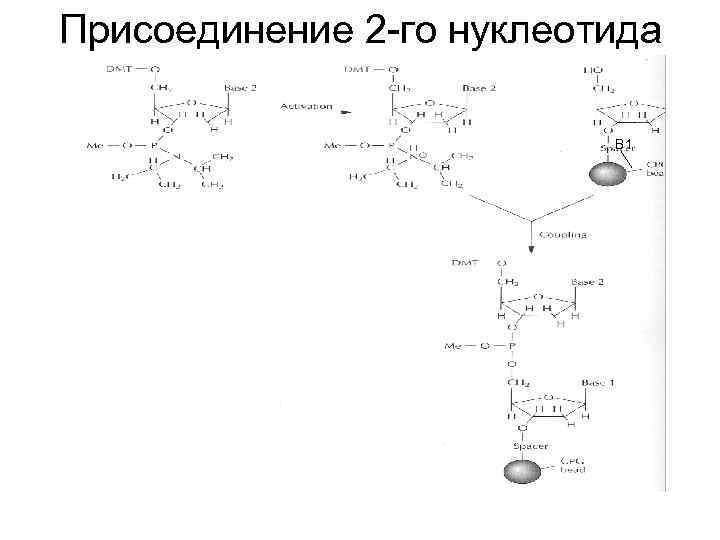
Присоединение 2 -го нуклеотида В 1

ДНК-синтезаторы • Это аппараты, в которых синтез ДНК осуществляется автоматически под контролем компьютера

Для чего нужен химический синтез ДНК? 1) Праймеры 2) Зонды 3) Линкеры 4) Адапторы 5) Синтетические гены

Синтетические праймеры Олигонуклеотиды (20 -25 нт), используемые для старта матричного синтеза ДНК с помощью ДНК-полимераз 3’ 5’

Синтетические зонды • Зонд – меченый олигонуклеотид, специфически связывающийся с определённой нуклеотидной последовательностью и позволяющий ее обнаружить • Радиоактивные зонды • Флуоресцирующие зонды * 5’ ___________ 3’

Синтетические линкеры • Короткие двуцепочечные олигонуклеотиды, позволяющие соединить две молекулы ДНК, имеющие разные концы • ___________

Синтетические адапторы • Короткие дц олигонуклеотиды, позволяющие создать липкий конец в молекуле ДНК _________

Синтетические гены • Химический синтез ДНК с помощью ДНКсинтезаторов (олигонуклеотиды до 50 нт) • Сборка молекулы из фрагментов d. NTP, ДНК-полимераза, лигаза • Включение синтетического гена в плазмиду

Работы К. Вентера по синтетической геномике • Синтез генома микоплазмы (1000 тпн) • Синтез митохондриального генома (20 тпн)

Полимеразная цепная реакция (ПЦР) Это метод амплификации (увеличения количества) определённой нуклеотидной последовательности

Разработка ПЦР • Химический синтез праймеров • Выделение термостабильной ДНКполимеразы из термофильной бактерии Thermus aquaticus – Taq I – А. Каледин и С. Городецкий (1980) • Разработка принципа ПЦР К. Муллисом (1986)

Главные реактивы для ПЦР • • • Исходная ДНК Праймеры Термостабильная ДНК-полимераза Дезоксирибонуклеотиды (d. NTP) Буферный раствор
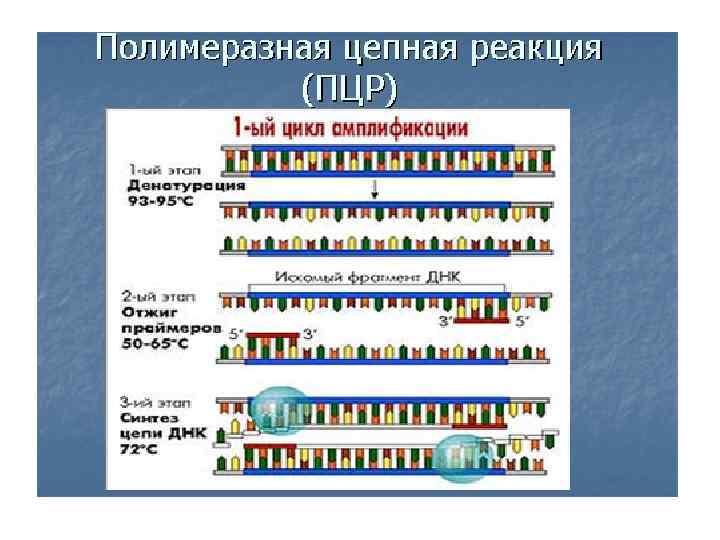

Принцип ПЦР

• pcr_animation. MOV

Электрофорез продуктов ПЦР в агарозе 1 - маркер 2, 3, 4, 5 – gag 1/gag 2 6, 7, 8, 9 – pol 1/pol 2

ПЦР в реальном времени Это ПЦР, продукты которой выявляют не электрофоретическим методом, а с помощью флуоресцирующей метки, которая нарастает по мере увеличения продуктов реакции

Варианты ПЦР в реальном времени: метод интеркаляции • Используется флуоресцентный краситель (SYBR), который флуоресцирует после интеркаляции в дц. ДНК (чем больше ДНК, тем сильнее флуоресценция)
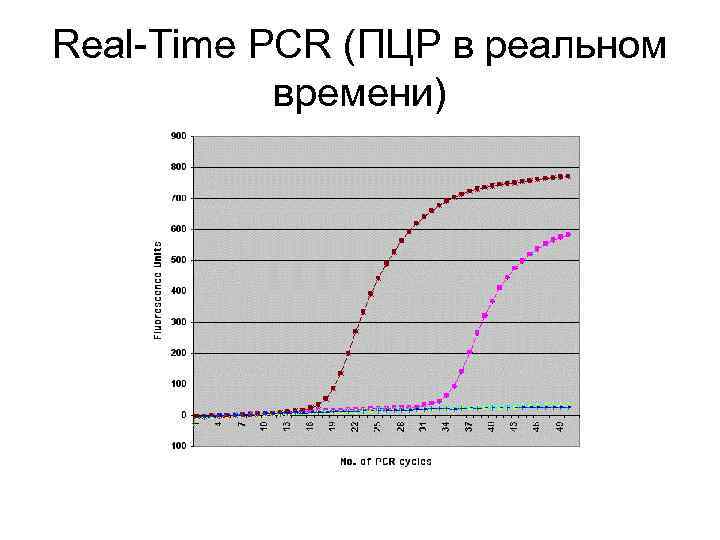
Real-Time PCR (ПЦР в реальном времени)

Варианты ПЦР в реальном времени: метод зондов • Использование меченых зондов, флуоресценция которых проявляется после связывания с ДНК (чем больше ДНК, тем сильнее флуоресценция)
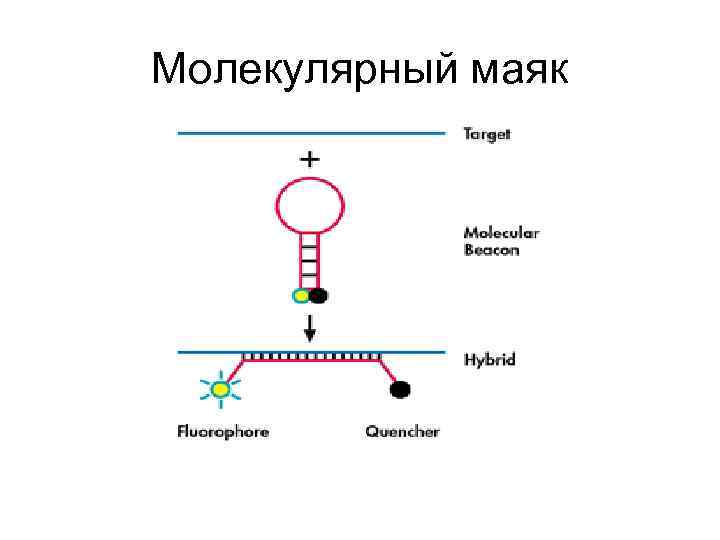
Молекулярный маяк

ОТ(RT)-ПЦР • С помощью обратной транскриптазы синтезируют к. ДНК-копии молекул РНК • В смеси образовавшихся молекул к. ДНК с помощью ПЦР амплифицируется заданная последовательность с помощью подобранной пары праймеров РНК оц. ДНК дц. ДНК амплификация определённого фрагмента ДНК

Возможности ПЦР • Получение нужных вставок для генетической инженерии и клонирование генов, введение нужных сайтов рестрикции в концы амплифицированной последовательности • Получение материала для секвенирования ДНК

Клонирование генов с помощью ПЦР • Выбор праймеров на основании данных банка нуклеотидных последовательностей • Приготовление препарата РНК • Постановка ОТ-ПЦР с праймерами, содержащими нужный сайт рестрикции • Клонирование полученного продукта в нужный вектор

Диагностическое значение ПЦР • Индикация определённых фрагментов ДНК • Диагностика инфекционных болезней • Определение вида пищевого сырья
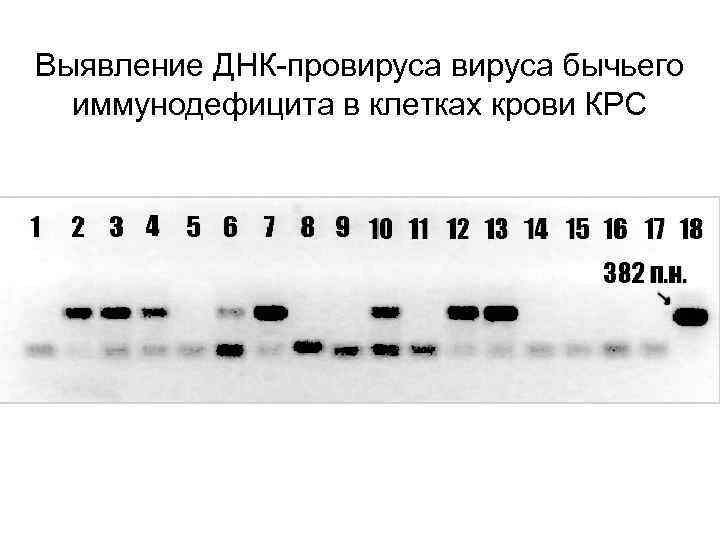
Выявление ДНК-провируса бычьего иммунодефицита в клетках крови КРС

Секвенирование ДНК Это определение порядка нуклеотидов в молекуле ДНК (чтение генетического текста)
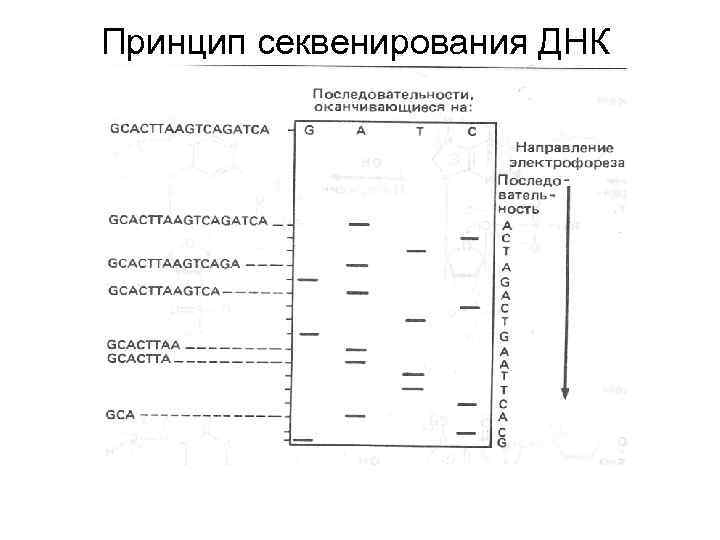
Принцип секвенирования ДНК
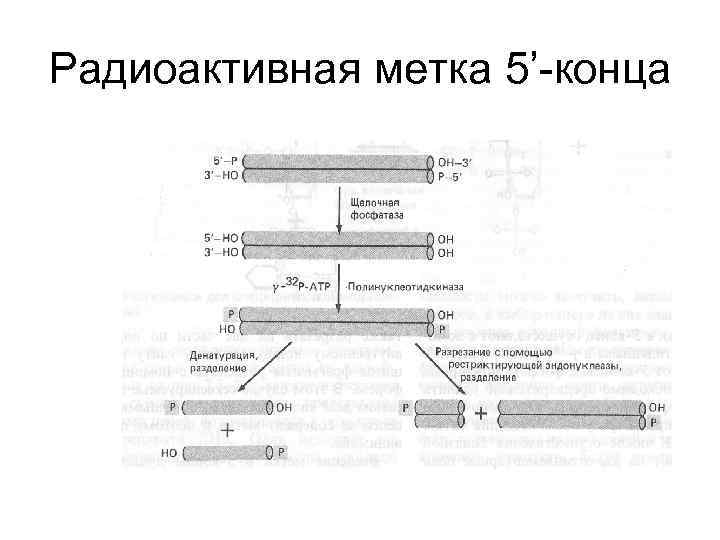
Радиоактивная метка 5’-конца

Химическое секвенирование ДНК (метод Максама-Гилберта) • Модификация пуринов (G+A) – пиперидинформат • Модификация гуанина (G) – диметилсульфат • Модификация пиримидинов (C+T) - гидразин • Модификация цитозина (C) – гидразин +Na. Cl
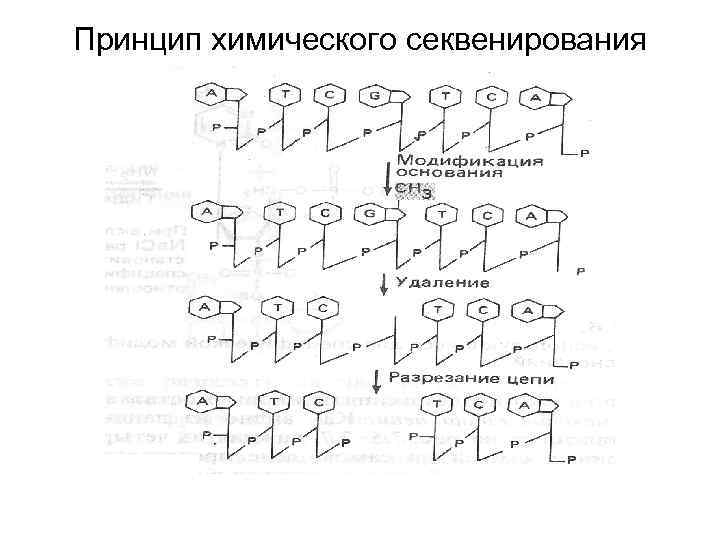
Принцип химического секвенирования

Результат химического секвенирования

Ферментативное секвенирование ДНК (метод Сэнгера) Для секвенирования необходимы: • ДНК-полимераза • d. NTP (A, G, C, T) • Дидезоксинуклеотиды (dd. ATP, dd. GTP, dd. CTP, dd. TTP)
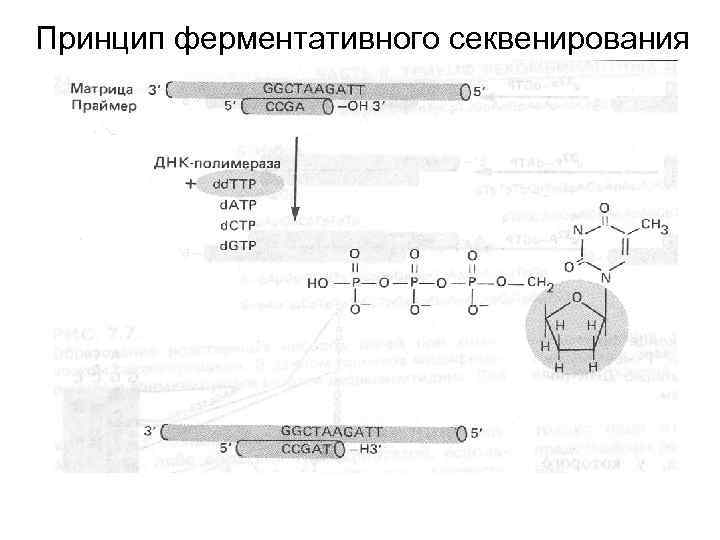
Принцип ферментативного секвенирования
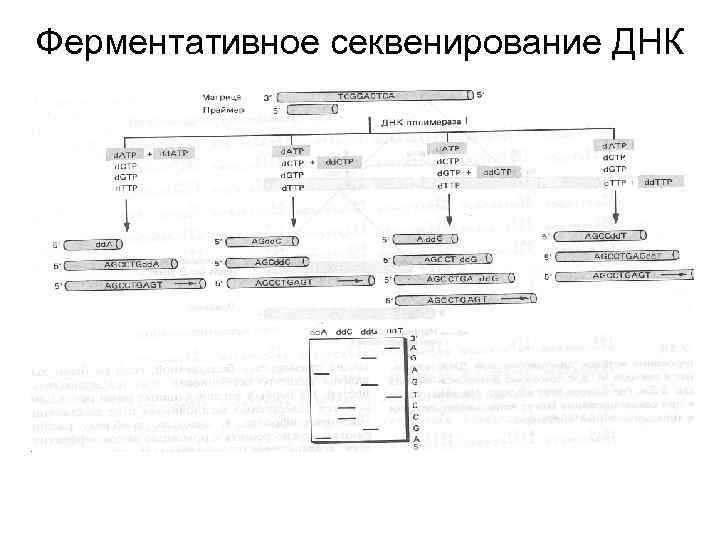
Ферментативное секвенирование ДНК

Метка dd. NTP • Радиоактивная • Флуоресцентная

ДНК-секвенаторы • Аппараты для автоматического секвенирования ДНК

ГЕНОМНЫЕ ПРОЕКТЫ • • ГЕНОМ ДРОЗОФИЛЫ ГЕНОМ H. INFLUENZAE ГЕНОМ ЧЕЛОВЕКА ГЕНОМ МЫШИ ГЕНОМ E. COLI ГЕНОМ ДРОЖЖЕЙ ГЕНОМ C. ELEGANS ГЕНОМЫ МНОГИХ ВИРУСОВ
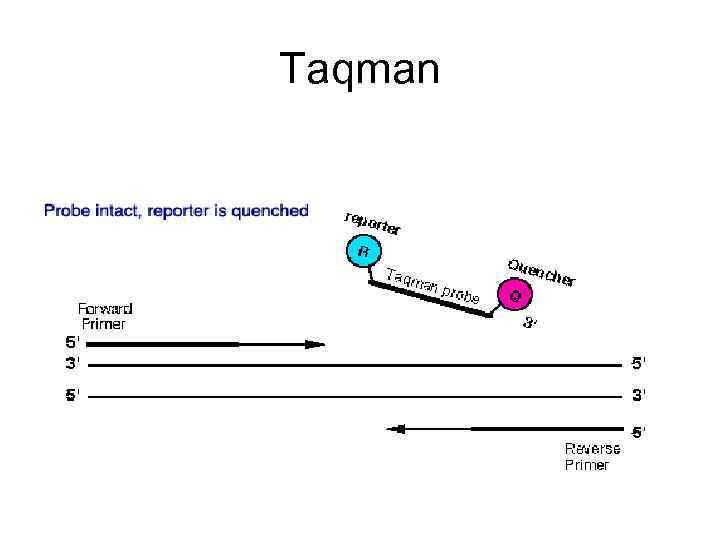
Тaqman

Экспрессия рекомбинантных генов в прокариотических клетках

Одна из главных целей молекулярной биотехнологии – получение продуцентов биологически активных белков с помощью генетической инженерии

Рекомбинантная ДНК и рекомбинантные гены • Рекомбинантная ДНК – это ДНК, состоящая из вектора и вставки • Встроенные гены в составе рекомбинантной ДНК называются рекомбинантными генами

Экспрессия рекомбинантных генов • Синтез м. РНК на матрице рекомбинантных генов (транскрипция) • Синтез белков, кодируемых рекомбинантными генами (трансляция)

Рекомбинантные белки • Белки, экспрессируемые генами в составе рекомбинантной ДНК • Некоторые из этих белков полностью соответствуют природному белку • Некоторые рекомбинантные белки являются слитыми белками • Некоторые рекомбинантные белки имеют замены по отдельным аминокислотам

Что необходимо для эффективного получения рекомбинантных белков • Правильная биологическая система, позволяющая использовать ферментёры (биореакторы) • Эффективный аппарат транскрипции и трансляции • Правильная посттрансляционная модификация рекомбинантного белка • Эффективные методы очистки рекомбинантного белка

Ферментёры, или биореакторы • Это аппараты для промышленного культивирования микроорганизмов или клеток многоклеточных организмов • В ферментёрах поддерживается оптимальная температура, аэрация, р. Н, обеспечивается автоматическая подача питательной среды, получение и сбор клеток, подготовка аппарата к следующему циклу

Биологические системы, пригодные для использования в ферментёрах • Прокариоты (микроорганизмы) • Эукариоты (дрожжи) • Эукариотические клетки многоклеточных организмов в культуре

Прокариоты • Наиболее удобная биологическая система для промышленного получения продуктов – прокариоты • Наиболее отработанные прокариотические системы – E. coli (кишечная палочка) и B. subtilis (сенная палочка)
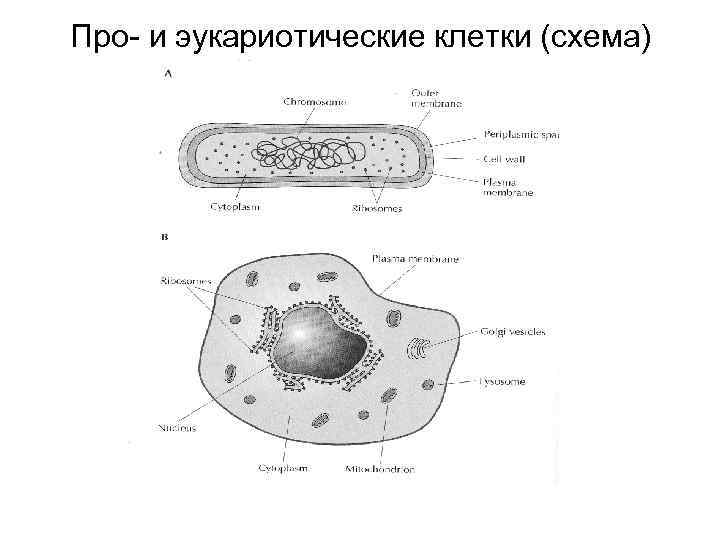
Про- и эукариотические клетки (схема)

Преимущества прокариотических систем • Дешёвая питательная среда • Быстрое размножение клеток • Возможность культивирования в больших объёмах среды • Максимальный экономический эффект

Недостатки прокариотических систем • Невозможность экспрессии интронированных эукариотических генов из-за отсутствия сплайсинга у прокариот • Невозможность правильной посттрансляционной модификации некоторых белков (протеолиз, фосфорилирование, гликозилирование, ацетилирование и др. ) • Нестабильность многих чужеродных белков в прокариотах

Е. coli • • Грамотрицательная бактерия, 1 х0. 5 мкм Геном – кольцевая дц. ДНК, 4 х106 п. н. Время деления – от 30 мин. Хорошо охарактеризована генетически, имеются коллекции мутантов • Имеются плазмиды и вирусы (фаги) для работы с Е. coli

Штамм E. coli K 12 • Специальный штамм E. coli, неспособный сохраняться во внешней среде • Имеется коллекция мутантов • Используется в работах по генетической инженерии

Этапы получения рекомбинантных белков • Подготовка гена • Подготовка вектора с необходимыми регуляторными элементами • Получение и накопление рекомбинантной плазмиды • Трансфекция, трансформация и селекция трансформированных клеток • Получение рекомбинанта-продуцента • Наращивание бактериальной массы • Индукция синтеза целевого белка • Очистка рекомбинантного белка

Как подготовить гены для их экспрессии в прокариотах • Используют клонированные гены • Прокариотические гены используются в их натуральном виде (за исключением промотора) • Эукариотические гены используются в виде к. ДНК • Гены получают из соответствующих библиотек или с помощью ПЦР

Два типа векторов • Клонирующие векторы • Экспрессирующие векторы

Векторы экспрессии • Для экспрессии генов используют те же векторы, что и для клонирования генов (плазмиды, фаги) • Специальное внимание уделяется регуляторным элементам, которые должны обеспечивать эффективную экспрессию целевого гена
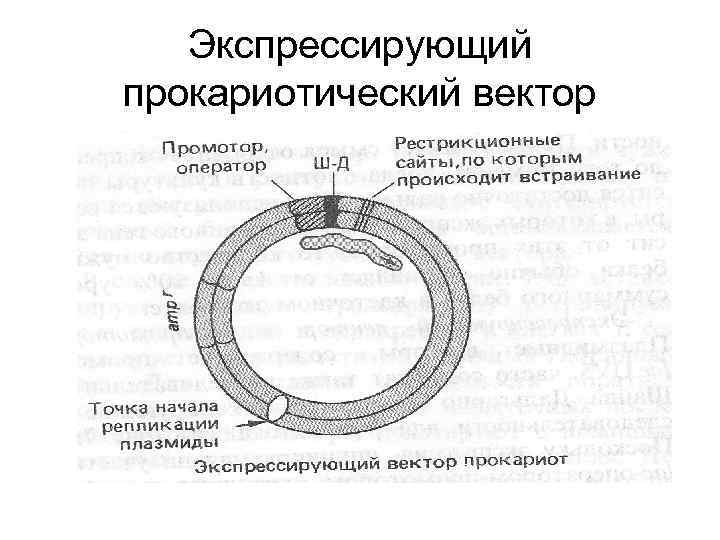
Экспрессирующий прокариотический вектор

Регуляторные элементы для экспрессии генов в прокариотах • • • Промотор Оператор Последовательность Шайн-Дельгарно Инициаторный ATG кодон Терминирующий кодон (ТАА, ТАG, ТGА) Терминатор транскрипции
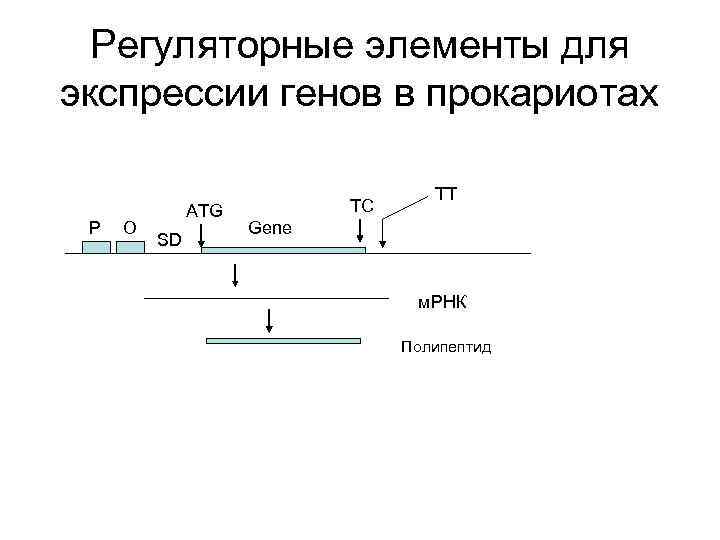
Регуляторные элементы для экспрессии генов в прокариотах P O ATG SD TC TT Gene м. РНК Полипептид
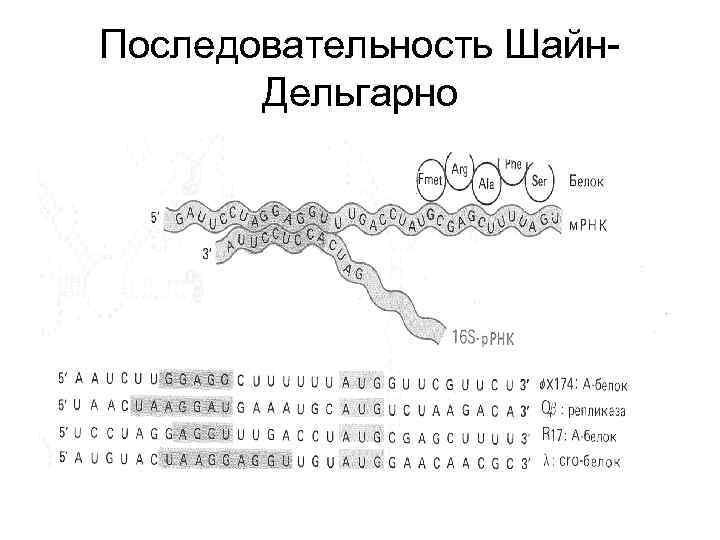
Последовательность Шайн. Дельгарно

Прокариотический промотор старт 5’TAGTG TATTGACA TGATAGAAGCACTCTAC TATATT CTCAATAACG 3’ -35 последов. -10 последов. Прибнов бокс -1 +1
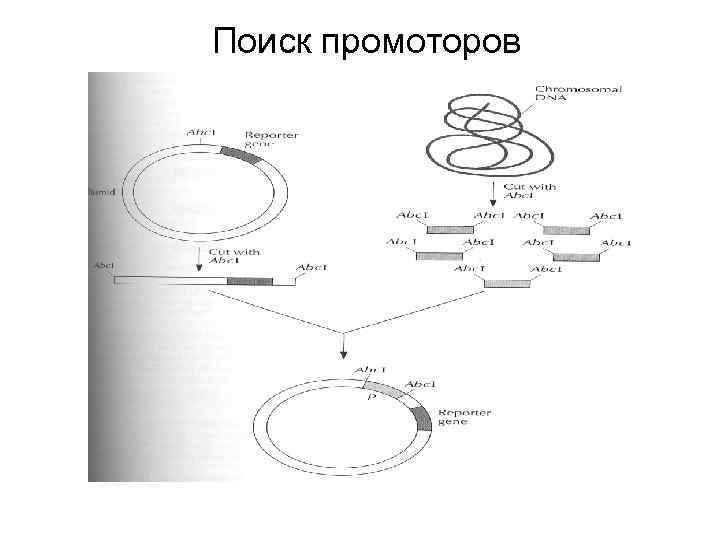
Поиск промоторов

Два типа промоторов • Конститутивные – работают постоянно • Индуцибельные – работают при определенных условиях • Для наработки белков необходимо использовать индуцибельные промоторы, потому что накапливаемый в большом количестве белок помешает бактериям размножаться

Индуцибельные прокариотические промоторы • Lac (промотор lac-оперона) • UV 5 (модифицированный промотор lacоперона) • Trp (промотор триптофанового оперона) • Tac (-35 область из trp, -10 из lacпромотора • PL (промотор фага лямбда)
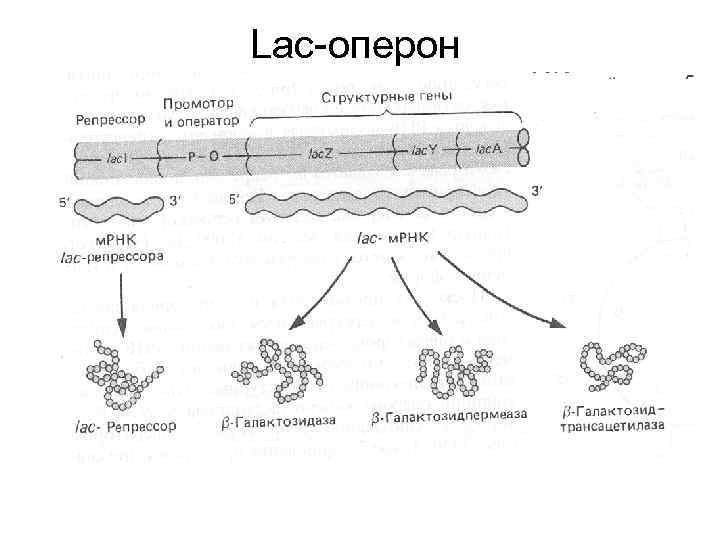
Lac-оперон

Два способа регуляции lacоперона • Негативная регуляция – lac-репрессор (ингибитор, I) • Позитивная регуляция – CAP-c. AMP (комплекс белка, активирующего катаболизм, с циклическим АМФ)
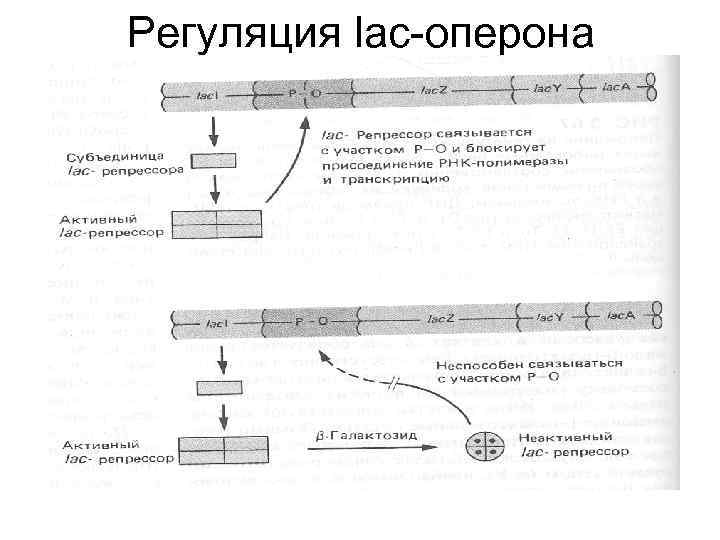
Регуляция lac-оперона
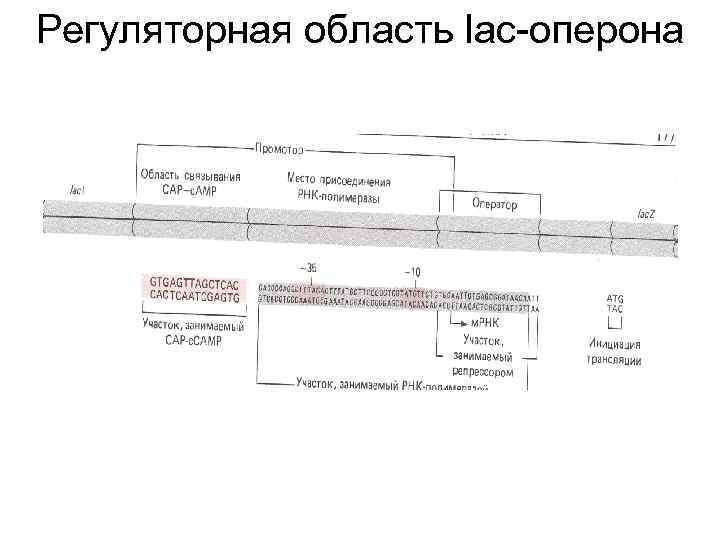
Регуляторная область lac-оперона
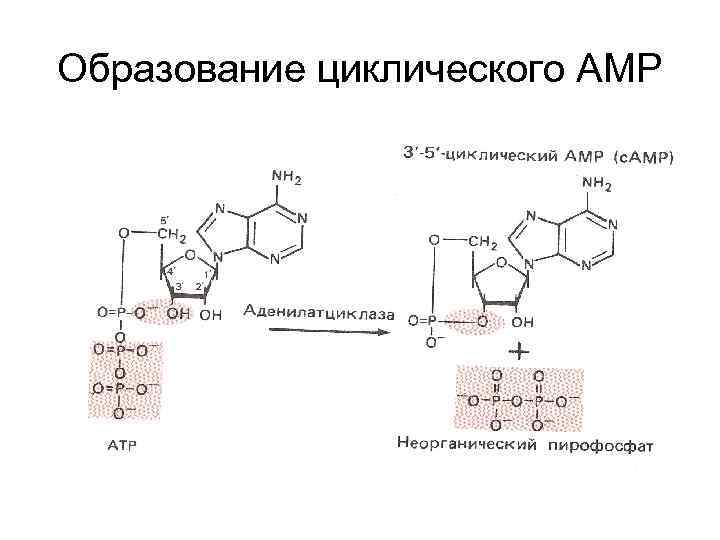
Образование циклического АМР
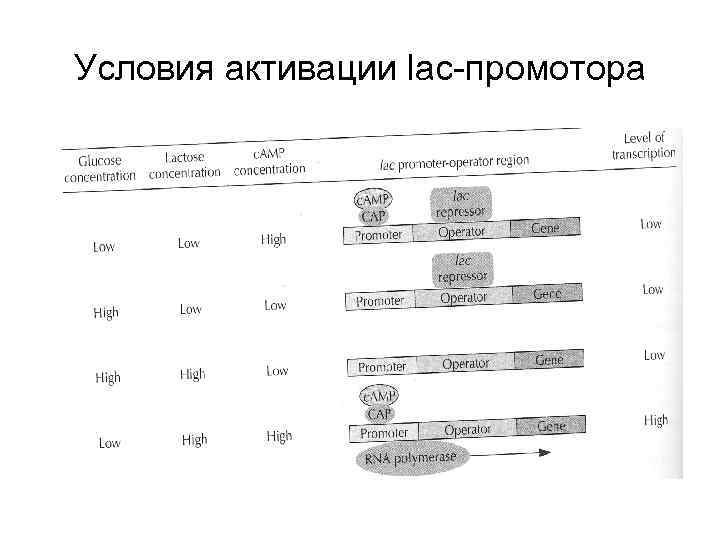
Условия активации lac-промотора

Фаговые PL - промотор и с. I-репрессор • Активность PL - промотора подавляется с. I-репрессором • Используют мутантный с. I-репрессор, теряющий активность при 420

Триптофановый промотор • Индуцибельный промотор, содержит оператор • Контролирует работу триптофанового оперона, продукты которого осуществляют синтез триптофана • Ген ингибитора находится далеко от оперона • При наличии триптофана в среде ингибитор+Trp выключает оперон

Искусственное выключение промотора • Lac-промотор: среда с глюкозой и без лактозы • Trp-промотор: среда с триптофаном • PL -промотор – культивирование при 370

Искусственная индукция промоторов • Lac-промотор: изопропил-β -Dтиогалактозид (IPTG) • Trp-промотор: 3 -β-индолилакриловая кислота • PL -промотор – нагревание до 420

Нестабильность рекомбинантных белков в бактериях • Многие рекомбинантные белки в бактериях подвергаются ускоренному протеолитическому распаду • Для устранения ускоренного протеолиза заменяют аминокислоту на N-конце полипептидной цепи (правило N-конца) или • Получают т. н. слитый белок
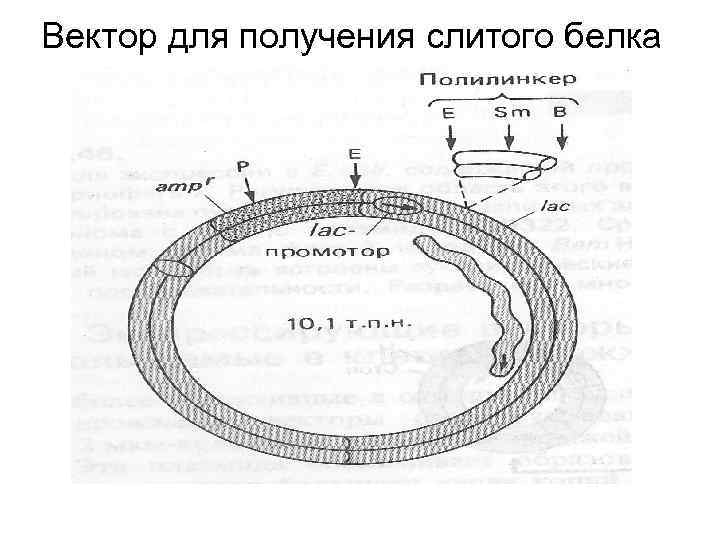
Вектор для получения слитого белка

Очистка рекомбинантного белка • При накоплении белка в бактериях их нужно разрушить ультразвуком • Осадить дебрис центрифугированием • Фракционировать смесь полученных белков с помощью колоночной хроматографии

Виды хроматографии • Ионообменная хроматография (делит молекулы белка по заряду) • Гель-фильтрация (делит молекулы белка по размеру) • Аффинная хроматография (делит по сродству к определённому веществулиганду, закреплённому на матрице)

Ионообменная хроматография • Разделение по заряду • Анионообменники (ДЕАЕ-целлюлоза) • Катионообменники (фосфоцеллюлоза)

Гель-фильтрация • • Разделение по размеру Гели на основе декстрана (сефадексы) Гели на основе агарозы Гели на основе синтетических веществ (полиакриламид, трисакрил и др. )

Аффинная хроматография • Разделение по связыванию с лигандом, фиксированным на матрице • Матрицы (целлюлоза, агароза и др. ) • Лиганды (нуклеиновые к-ты, антитела и др. )

Прокариотические белки, получаемые в рекомбинантных бактериях • ДНК-полимераза I Е. coli • ДНК-лигаза Е. coli • Рестриктазы и др.

Эукариотические белки, получаемые в рекомбинантных бактериях • • Обратная транскриптаза Гормоны роста Интерфероны (альфа-, бета-, гамма-) Инсулин Цитокины (IL-2, TNF и др. ) Факторы свёртываемости крови Тканевой активатор плазминогена и урокиназа • Вирусные антигены и др.

Экспрессия рекомбинантных генов в эукариотических клетках
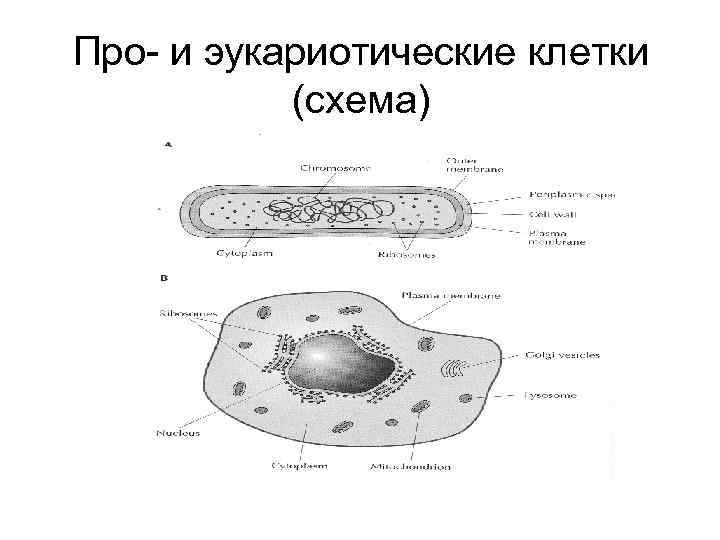
Про- и эукариотические клетки (схема)

Недостатки прокариотических систем • Невозможность экспрессии интронированных эукариотических генов из-за отсутствия сплайсинга у прокариот • Невозможность правильной пострансляционной модификации белков (протеолиз, фосфорилирование, гликозилирование, ацетилирование и др. ) • Нестабильность многих чужеродных белков в прокариотах

Эукариотические клетки, используемые как продуценты рекомбинантных белков • Дрожжи (пекарские дрожжи, метилотрофные дрожжи) • Культуры клеток насекомых • Культуры клеток млекопитающих и птиц

Преимущества эукариотических клеток • Обеспечивается правильное посттрансляционное процессирование рекомбинантных белков, особенно в клетках животных • Дрожжи сочетают достоинства эукариотических и прокариотических клеток

Недостатки эукариотических клеток • Использование эукариотических клеток, особенно клеток животных, менее технологично из-за более медленного размножения клеток и требует больших затрат Время удвоения: • Бактерии – 20 -30 мин • Дрожжи – 1, 5 -2, 5 ч. • Клетки животных – 8 -12 ч.

Пекарские дрожжи. Saccharomyces cerevisiae • • Размер клетки ~10 мкм Геном 1. 4 x 107 пн 16 хромосом Размножается почкованием и половым способом • Время удвоения – 1, 5 -2, 5 ч. • Образует колонии на агаре, легко культивируется в биореакторах

Векторы для дрожжевой системы • Вирусы дрожжей не описаны • Обнаружен один вид плазмиды – 2 мкм ДНК • На основе этой плазмиды получены векторы для дрожжей, в том числе челночные плазмиды

Челночный вектор • Способен размножаться и в бактерии и в эукариотической клетке • Содержит два участка ori – про- и эукариотический • Содержит селективные маркеры для прокариотических и для эукариотических клеток
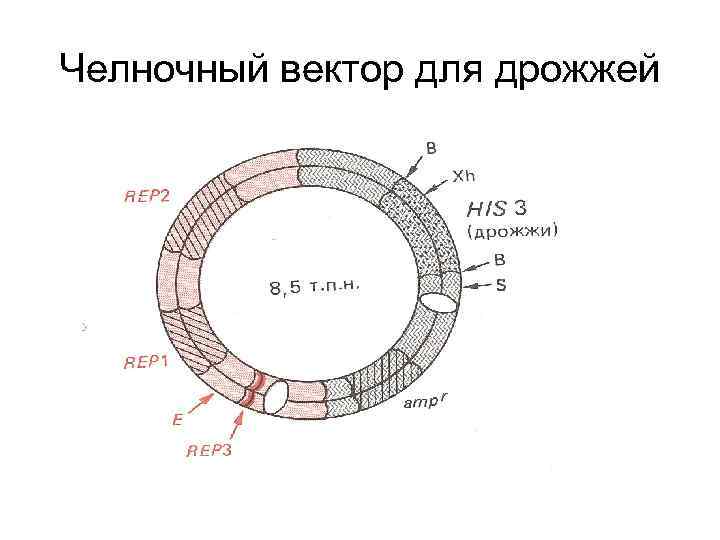
Челночный вектор для дрожжей
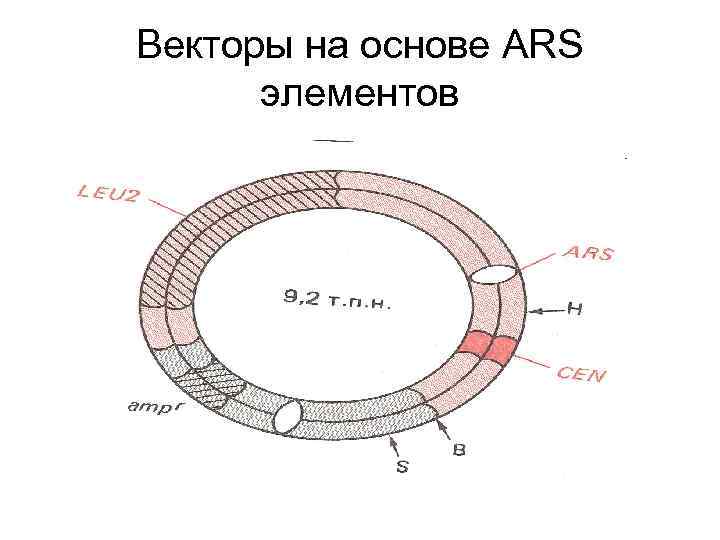
Векторы на основе ARS элементов

Трансфекция дрожжевых клеток • Клетки дрожжей имеют полисахаридную клеточную стенку, окружающую цитоплазматическую мембрану. Эта стенка не пропускает молекулы ДНК. • Клеточную стенку разрушают полисахаридрасщепляющим ферментом и получают сферопласты, которые обрабатывают Ca. Cl 2 и трансфицируют ДНК. Клеточная стенка восстанавливается при культивировании.

Неинтегративная и интегративная трансформация • Неинтегративная трансформация клетки достигается за счет размножения плазмиды в клеточном ядре. • Интегративная трансформация – результат интеграции части плазмиды с интересующим геном в хромосому.

Стабильная и нестабильная трансформация клеток • В отсутствие селективного давления автономные плазмиды легко утрачиваются (нестабильная трансформация) • Интегрированный ген обычно стабильно сохраняется в геноме, если не влияет негативно на жизнеспособность клетки (стабильная трансформация)
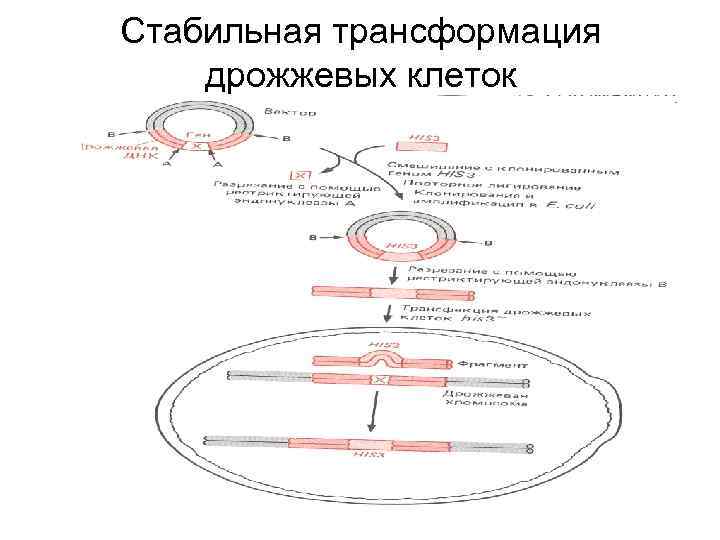
Стабильная трансформация дрожжевых клеток
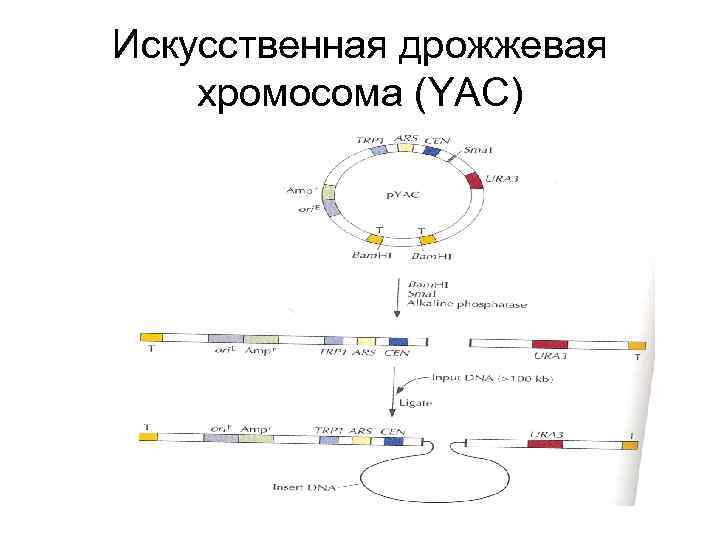
Искусственная дрожжевая хромосома (YAC)

Системы селекции для дрожжей • Использование мутантов дрожжей, дефектных по генам синтеза аминокислот (лейцин, гистидин, триптофан) и азотистых оснований. Маркерами являются гены LEU, HIS, TRP, URA и др. • Использование гена NEO устойчивости к антибиотику G 418 (генетицину)
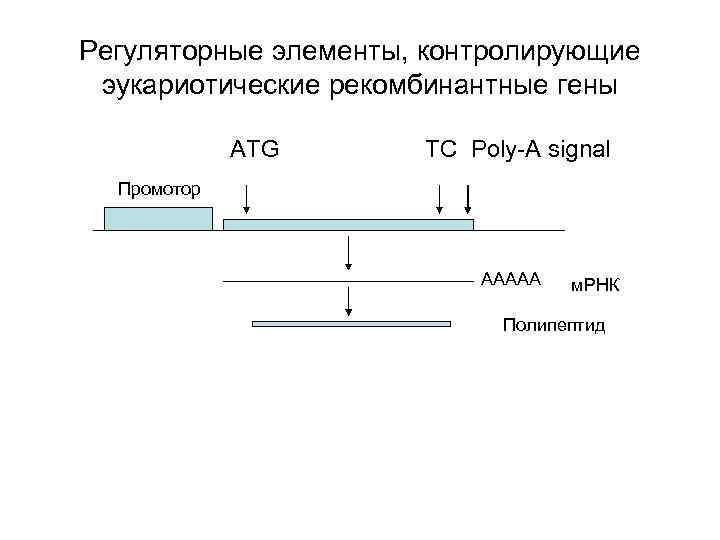
Регуляторные элементы, контролирующие эукариотические рекомбинантные гены ATG TC Poly-A signal Промотор AAAAA м. РНК Полипептид
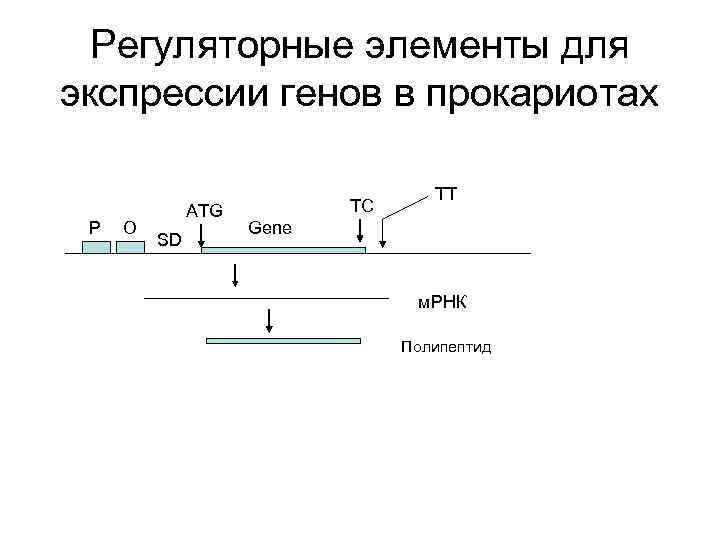
Регуляторные элементы для экспрессии генов в прокариотах P O ATG SD TC TT Gene м. РНК Полипептид

Дрожжевые промоторы • Промотор гена CYC 1 (кодирует цитохром С) • Промотор гена алкоголь-оксидазы (AOX 1)

Метилотрофные дрожжи • Метилотрофные дрожжи используют метиловый спирт в качестве источника углерода • Они накапливаются в большом количестве • Удобны для наработки рекомбинантных белков под контролем промотора гена алкоголь-оксидазы (АОХ 1)

Использование метилотрофных дрожжей Pichia pastoris для наработки белков
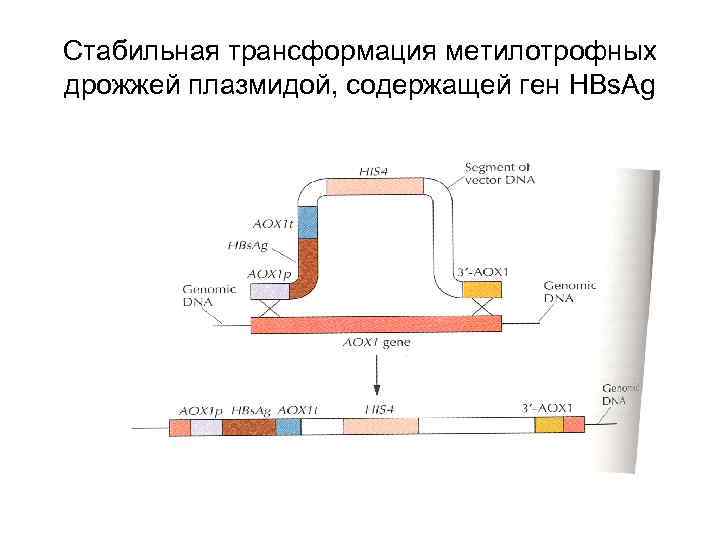
Стабильная трансформация метилотрофных дрожжей плазмидой, содержащей ген HBs. Ag

Рекомбинантные продукты, полученные в дрожжевых системах • • HBs. Ag (вакцина против гепатита В) Белки малярийного плазмодия Оболочечный антиген HIV Лекарственные белки человека (эпидермальный фактор роста, альфа 1 антитрипсин, факторы свёртываемости крови и др. )

Клетки животных в культуре • Первичные и вторичные культуры • Диплоидные штаммы клеток • Перевиваемые линии клеток

Векторы для клеток животных • Вирусы (поксвирусы, аденовирусы, полиома- и папилломавирусы, ретровирусы, бакуловирусы и др. ) • Прокариотические плазмиды
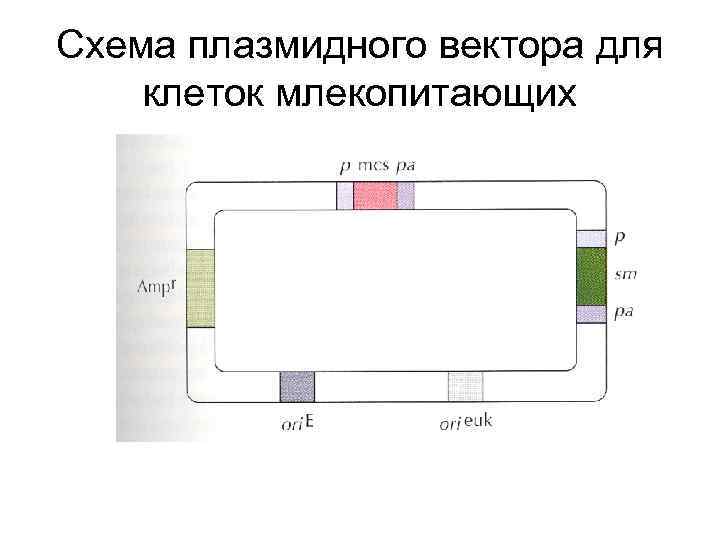
Схема плазмидного вектора для клеток млекопитающих

Введение плазмидных векторов в клетки • Кальций-фосфатный метод (Ca. Cl 2+ Na 3 PO 4 Ca 3(PO 4)2 • Полибрен, ДЕАЕ-декстран • Липосомы • Электропорация • Бомбардировка частичками золота

Селекция трансформированных клеток • Ген устойчивости к G 418 (генетицину) • Ген устойчивости к пуромицину • Устойчивость к аминоптерину или метотрексату • Устойчивость к микофеноловой кислоте • Окраска (lac. Z) или флуоресценция (флуоресцентные белки)

Транзиторная экспрессия генов в эукариотических клетках • В большинстве трансфицированных клеток происходит транзиторная (временная, проходящая) экспрессия трансфицированного гена, достигающая максимума через 2 -3 дня и спадающая к 6 -7 дню после трансфекции. • Небольшая часть трансфицированных клеток становится стабильно трансформированной.

Стабильная трансформация клеток животных рекомбинантными плазмидами • Попав в клеточное ядро, рекомбинантные плазмиды способны встраиваться в геном клетки, что ведет к стабильной трансформации • Встройка обычно происходит по принципу случайной рекомбинации • Существуют способы увеличения числа копий встроенного гена
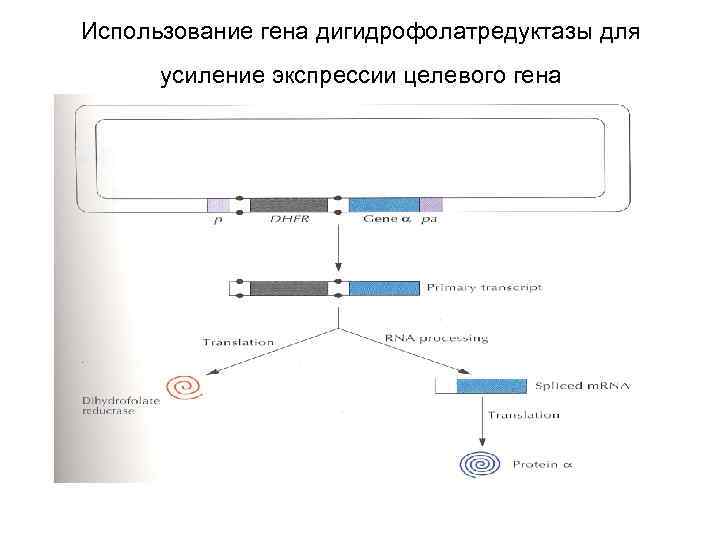
Использование гена дигидрофолатредуктазы для усиление экспрессии целевого гена

Увеличения числа копий введенного гена • Выращивание клеток в присутствии аминоптерина ведет к амплификации участка генома, содержащего ген дигидрофолатредуктазы (ДГФР) и прилежащие гены • При этом резко увеличивается число копий гена ДГФР и расположенных рядом с ним генов. Количество продукта значительно увеличивается.

Эритропоэтин • Важное лекарство – эритропоэтин – было получено в клетках СНО после амплификации гена эритропоэтина, встроенного рядом с геном ДГФР
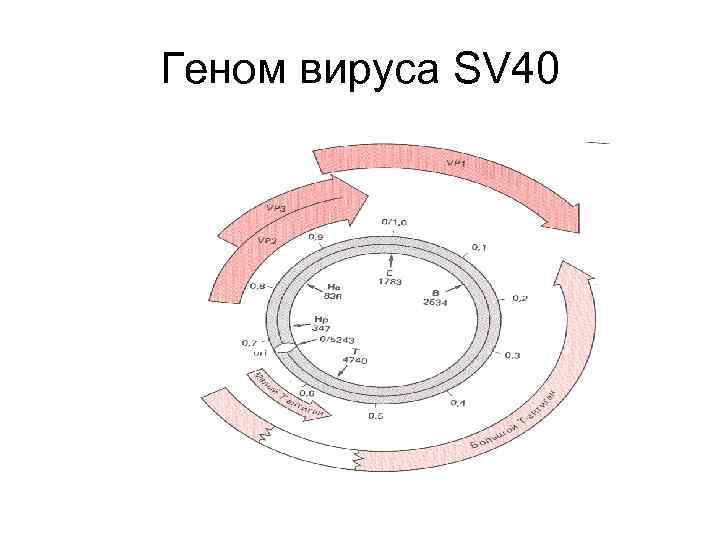
Геном вируса SV 40

Размножение плазмид в клетках животных • Обезьяньи СOS клетки Я. Глузмана • Эти клетки продуцируют Т антиген вируса SV 40 • T антиген, связываясь с ori SV 40, вызывает репликацию вирусной ДНК клеточной репликационной машиной • Если ori SV 40 включен в плазмиду, она будет реплицироваться в COS клетках

Бакуловирусная система • Вирус множественного ядерного полиэдроза – ДНК-содержащий вирус с кольцевой дц. ДНК ~120 тпн, поражает насекомых свыше 30 видов, вызывает образование полиэдров в ядрах клеток • Полиэдры построены из вирусного белка полиэдрина. • Ген полиэдрина имеет мощный промотор
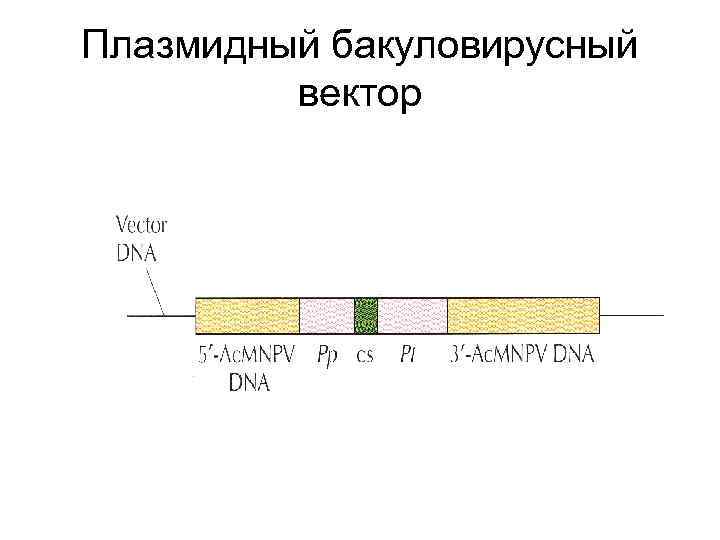
Плазмидный бакуловирусный вектор

Получение рекомбинантного бакуловируса • Клетки заражают «диким» бакуловирусом • Трансфицируют зараженные клетки плазмидой, содержащей участок вирусной ДНК и ген интереса • В результате гомологичной рекомбинации ген интереса встраивается в вирусную ДНК • Затем отбирают и клонируют рекомбинантные вирионы методом бляшек
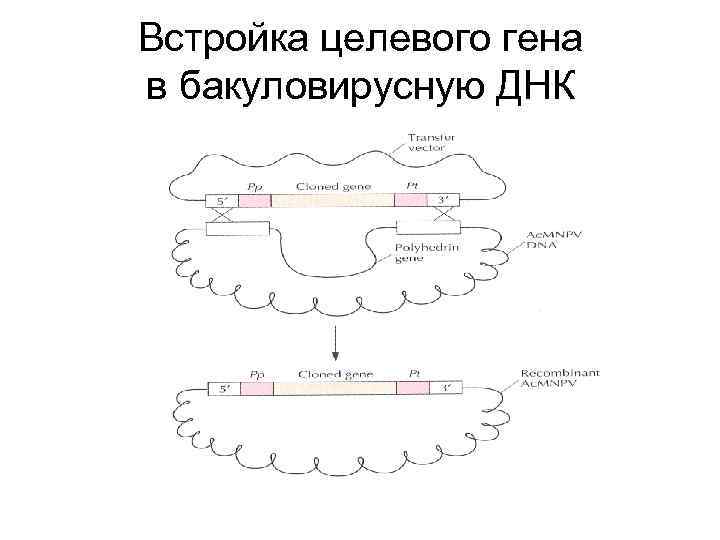
Встройка целевого гена в бакуловирусную ДНК

Получение рекомбинантного белка в бакуловирусной системе • Культуру клеток насекомых заражают рекомбинантным бакуловирусом • Целевой белок образуется в заражённых клетках и может быть выделен и очищен из культуральной жидкости или клеточного экстракта

Рекомбинантные белки, полученные в бакуловирусной системе • В системе получены сотни рекомбинантных белков различного назначения • Недавно была разработана вакцина против папилломавирусных инфекций, вызывающих рак шейки матки (антигены для этой вакцины нарабатываются в бакуловирусной системе)

Трансгенные животные

Биологические системы, используемые молекулярной биотехнологией • • Вирусы Прокариоты Дрожжи Культура клеток животных и человека (клетки насекомых, птиц, млекопитающих), растений • Животные • Растения

Трансгенные животные • Трансгенные животные - это животные, в геном которых искусственно встроен чужеродный генетический материал • Чужеродный ген содержится во всех клетках трансгенного организма

ТРАНСГЕНЫ И ТРАНСГЕНЕЗ • ТРАНСГЕНЫ: ВСТРОЕННЫЙ ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ ОБОЗНАЧАЕТСЯ ТЕРМИНОМ “ТРАНСГЕН” • ТРАНСГЕНЕЗ: ПРОЦЕСС ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ОРГАНИЗМОВ ОБОЗНАЧАЕТСЯ ТЕРМИНОМ “ТРАНСГЕНЕЗ”

Подготовка генной конструкции для трансгенеза • Экспрессирующие векторы (плазмиды) – такие же, как для экспрессии генов в клетках животных. Они должны содержать регуляторные элементы (промоторы, энхенсеры и др. ), соответствующие поставленной задаче • Специальные конструкции для введения гена в заданную область генома
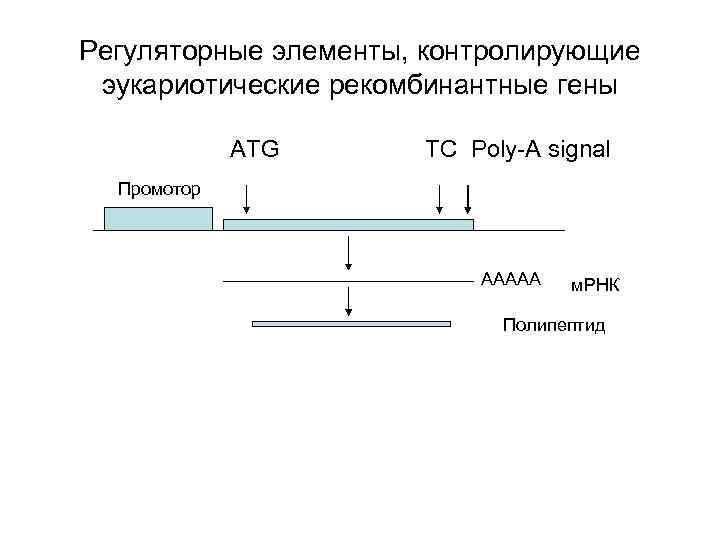
Регуляторные элементы, контролирующие эукариотические рекомбинантные гены ATG TC Poly-A signal Промотор AAAAA м. РНК Полипептид

Стабильная трансформация клеток животных трансгеном • В качестве трансгенов используют линейную ДНК, освобожденную от плазмидных последовательностей • Попав в клеточное ядро, трансгены способны встроиться в геном клетки, что ведет к стабильной трансформации трансфицированной клетки • Встройка обычно происходит по принципу случайной (негомологичной) рекомбинации

ВИДЫ ЖИВОТНЫХ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ТРАНСГЕНЕЗА • • • ДРОЗОФИЛЫ ЗЕМНОВОДНЫЕ МЫШИ КРОЛИКИ КОЗЫ ОВЦЫ СВИНЬИ КОРОВЫ КУРЫ РЫБЫ

ОБЩАЯ СХЕМА ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ЖИВОТНЫХ • • • ПОЛУЧЕНИЕ ОПЛОДОТВОРЕННЫХ ЯЙЦЕКЛЕТОК ВВЕДЕНИЕ КЛОНИРОВАННОГО ГЕНА В ЯДРО ОПЛОДОТВОРЕННОЙ ЯЙЦЕКЛЕТКИ ИМПЛАНТАЦИЯ ТАКИХ ЯЙЦЕКЛЕТОК В МАТКУ ПОДГОТОВЛЕННОЙ САМКИ ВЫЯВЛЕНИЕ ЖИВОТНЫХ, СОДЕРЖАЩИХ ТРАНСГЕН, СРЕДИ РОДИВШЕГОСЯ ПОТОМСТВА СКРЕЩИВАНИЕ ОСОБЕЙ, СОДЕРЖАЩИХ ТРАНСГЕН, ДЛЯ ВЫВЕДЕНИЯ ЛИНИИ ТРАНСГЕННЫХ ЖИВОТНЫХ

Введение трансгена • Введение трансгена с помощью ретровируса • Микроинъекции трансгена в яйцеклетку, микроманипуляторы

ТРАНСГЕННЫЕ МЫШИ • • ПОЛУЧЕНИЕ ОПЛОДОТВОРЕННЫХ ЯЙЦЕКЛЕТОК ОТ СУПЕРОВУЛИРОВАННЫХ САМОК (ДО 35 ЯЙЦЕКЛЕТОК ВМЕСТО ОБЫЧНЫХ 5 -10) МИКРОИНЪЕКЦИЯ ТРАНСГЕНА В МУЖСКОЙ ПРОНУКЛЕУС ИМПЛАНТАЦИЯ ИНОКУЛИРОВАННЫХ ЯЙЦЕКЛЕТОК В МАТКУ ПОДГОТОВЛЕННЫХ САМОК ПОЛУЧЕНИЕ И АНАЛИЗ ПОТОМСТВА НА НАЛИЧИЕ ТРАНСГЕНА (БЛОТГИБРИДИЗАЦИЯ И ПЦР)
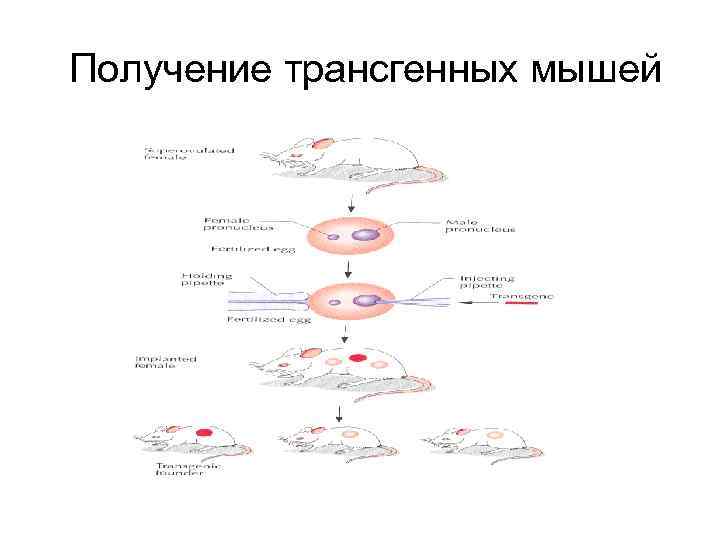
Получение трансгенных мышей

ЭМБРИОНАЛЬНЫЕ СТВОЛОВЫЕ (ЭС) КЛЕТКИ • ЭС КЛЕТКИ – НЕДИФФЕРЕНЦИРОВАННЫЕ КЛЕТКИ, ДАЮЩИЕ НАЧАЛО ВСЕМ ТКАНЯМ ОРГАНИЗМА • ИСПОЛЬЗОВАНИЕ ДЛЯ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ МЫШЕЙ • ВВЕДЕНИЕ ТРАНСГЕНА В ЗАДАННОЕ МЕСТО ГЕНОМА

ПОЛУЧЕНИЕ ЭС КЛЕТОК • • ЭС КЛЕТКИ ПОЛУЧАЮТ ИЗ ВНУТРЕННЕЙ КЛЕТОЧНОЙ МАССЫ БЛАСТОЦИСТА КУЛЬТИВИРОВАНИЕ ЭТИХ КЛЕТОК ПОЗВОЛЯЕТ ПОЛУЧИТЬ ПЕРЕВИВАЕМЫЕ КЛЕТОЧНЫЕ ЛИНИИ, ПРИГОДНЫЕ ДЛЯ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ЖИВОТНЫХ
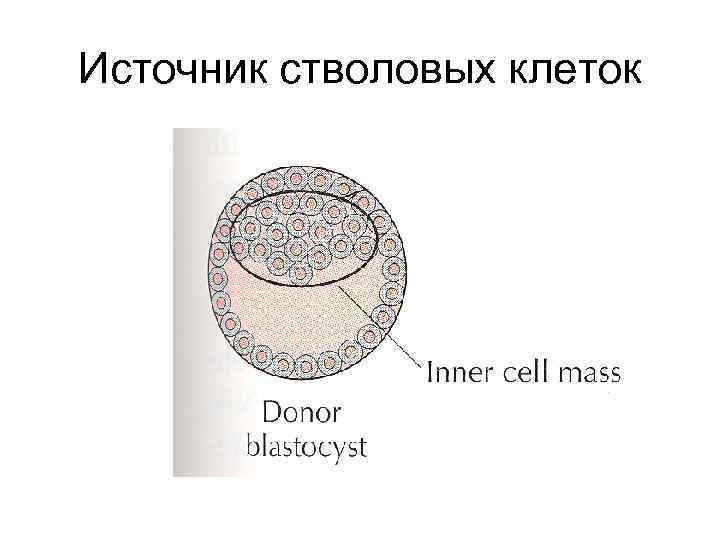
Источник стволовых клеток

ИСПОЛЬЗОВАНИЕ ЭС КЛЕТОК ДЛЯ ТРАНСГЕНЕЗА • ПОДГОТОВКА ЭС КЛЕТОК • ТРАНСФЕКЦИЯ ЭС КЛЕТОК ТРАНСГЕНОМ, ОТБОР ТРАНСФОРМИРОВАННЫХ КЛЕТОК • ВВЕДЕНИЕ ТРАНСФОРМИРОВАННЫХ ТРАНСГЕНОМ ЭС КЛЕТОК В БЛАСТОЦИСТЫ • ИМПЛАНТАЦИЯ БЛАСТОЦИСТОВ ПОДГОТОВЛЕННЫМ САМКАМ • ПОЛУЧЕНИЕ ПОТОМСТВА И ЕГО АНАЛИЗ НА НАЛИЧИЕ ТРАНСГЕНА

Введение трансгенов в ЭС клетки • Кальций-фосфатный метод (Ca. Cl 2+ Na 3 PO 4 Ca 3(PO 4)2 • Полибрен, ДЕАЕ-декстран • Липосомы • Электропорация
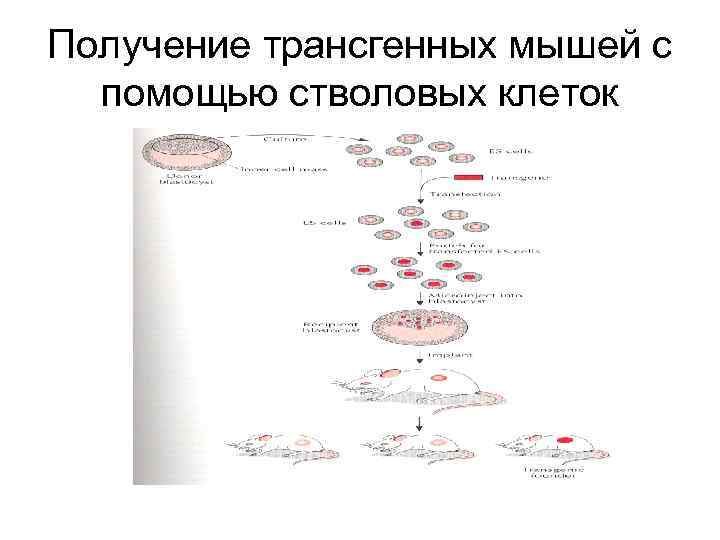
Получение трансгенных мышей с помощью стволовых клеток

ВВЕДЕНИЕ ТРАНСГЕНА В ЗАДАННОЕ МЕСТО ГЕНОМА • ОБЫЧНО ТРАНСГЕН НЕ ИМЕЕТ ОПРЕДЕЛЕННОГО АДРЕСА ДЛЯ ВСТРОЙКИ • ДЛЯ ВВЕДЕНИЯ ТРАНСГЕНА В ЗАДАННЫЙ УЧАСТОК ГЕНОМА ИСПОЛЬЗУЮТ ПРИНЦИП ГОМОЛОГИЧНОЙ РЕКОМБИНАЦИИ

ГЕН ТИМИДИНКИНАЗЫ (tk) ВИРУСА ПРОСТОГО ГЕРПЕСА • TK ГЕНЫ ФОСФОРИЛИРУЮТ ТИМИДИН, ПРЕВРАЩАЯ ЕГО В ТМР (Td. R-PO 4) • TK ГЕН ВПГ ОТЛИЧАЕТСЯ НИЗКОЙ СПЕЦИФИЧНОСТЬЮ И СПОСОБЕН ФОСФОРИЛИРОВАТЬ ЦИТИДИН И «НЕПРАВИЛЬНЫЕ» НУКЛЕОЗИДЫ (НАПР. , ГАНЦИКЛОВИР). • ФОСФОРИЛИРОВАННЫЙ ГАНЦИКЛОВИР УБИВАЕТ КЛЕТКУ
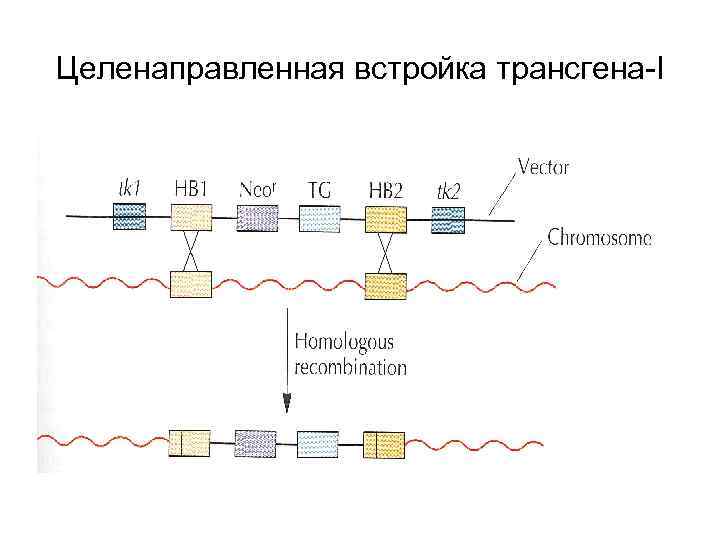
Целенаправленная встройка трансгена-I
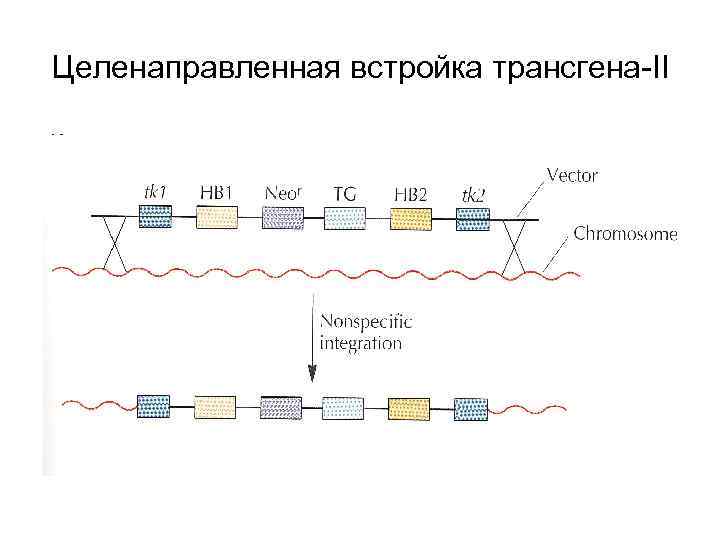
Целенаправленная встройка трансгена-II

Позитивная и негативная селекция Ген Ингибитор Рост клеток (позитивная селекция) Neo G 418 Neo + G 418 + (негативная селекция) tk HSV ганцикловир + tk HSV+ ганцикловир -

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ

НОКАУТ ГЕНОВ У МЫШЕЙ • Нокаут гена – это его инактивация во всех клетках организма • Это достигается встройкой маркерного гена внутрь нокаутируемого гена

ТКАНЕСПЕЦИФИЧЕСКАЯ ЭКСПРЕССИЯ ГЕНОВ У ТРАНСГЕННЫХ МЫШЕЙ • Выявление промоторов, способных экспрессироваться в строго определенных тканях (в поджелудочной железе, в мозгу, в молочной железе и т. д. ) • Поставив онкоген под соответствующий промотор, можно вызвать опухоли у трансгенных мышей в определенной ткани или органе

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ • ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ • СОЗДАНИЕ МОДЕЛЕЙ БОЛЕЗНЕЙ ЧЕЛОВЕКА (БОЛЕЗНЬ АЛЬЦГЕЙМЕРА ГЕН ПРЕДШЕСТВЕННИКА БЕТААМИЛОИДНОГО БЕЛКА; МЫШИ, ЧУВСТВИТЕЛЬНЫЕ К ВИРУСУ ПОЛИОМИЕЛИТА)

Болезнь Альцгеймера • Накопление сенильных бляшек в синапсисах нейронов • Бляшки содержат амилоид бета (Аβ), 4 к. Д • Ген предшественника Аβ кодирует белок предшественник Аβ (АРР) • Мутации в гене АРР ведут к накоплению Аβ • Мыши, трансгенные по мутантному гену АРР, проявляют симптомы болезни и характерные патологические изменения

МЫШИ, ЧУВСТВИТЕЛЬНЫЕ К ВИРУСУ ПОЛИОМИЕЛИТА • Рецептор полиовируса отсутствует в клетках мышей, поэтому они нечувствительны к этому вирусу • Мыши, трансгенные по гену рецептора полиовируса, чувствительны к нему и могут использоваться для контроля полиомиелитной вакцины вместо обезьян

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ • ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ • СОЗДАНИЕ МОДЕЛЕЙ БОЛЕЗНЕЙ ЧЕЛОВЕКА (БОЛЕЗНЬ АЛЬЦГЕЙМЕРА - ГЕН ПРЕДШЕСТВЕННИКА БЕТА-АМИЛОИДНОГО БЕЛКА; МЫШИ, ЧУВСТВИТЕЛЬНЫЕ К ВИРУСУ ПОЛИОМИЕЛИТА) • МОДЕЛЬНЫЕ ЭКСПЕРИМЕНТЫ ПО ПРОДУКЦИИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ (БАВ)

ПРОДУКЦИЯ БАВ В МОЛОЧНОЙ ЖЕЛЕЗЕ ТРАНСГЕННЫХ ЖИВОТНЫХ • МОЛОЧНАЯ ЖЕЛЕЗА - ФАБРИКА ПО • • • СИНТЕЗУ БЕЛКОВ (ДО 600 КГ/КОРОВА/ПЕРИОД ЛАКТАЦИИ). ГЛАВНЫЕ БЕЛКИ АЛЬФА-S 1 -КАЗЕИН АЛЬФА-S 2 -КАЗЕИН, БЕТА-КАЗЕИН КАППА-КАЗЕИН ЛАКТАЛЬБУМИН

ПРОМОТОРЫ, СПЕЦИФИЧНЫЕ ДЛЯ МОЛОЧНОЙ ЖЕЛЕЗЫ • ГЕНЫ КАЗЕИНОВ И ЛАКТАЛЬБУМИНА ИМЕЮТ ПРОМОТОРЫ, СПЕЦИФИЧНЫЕ ДЛЯ МОЛОЧНОЙ ЖЕЛЕЗЫ • ГЕН, КОНТРОЛИРУЕМЫЙ ТАКИМ ПРОМОТОРОМ, ЭКСПРЕССИРУЕТСЯ ИЗБИРАТЕЛЬНО В МОЛОЧНОЙ ЖЕЛЕЗЕ • ЕГО БЕЛКОВЫЙ ПРОДУКТ ВЫДЕЛЯЕТСЯ В МОЛОКО, ОТКУДА ОН МОЖЕТ БЫТЬ ПОЛУЧЕН В ЧИСТОМ ВИДЕ

• • • ТРАНСГЕННЫЕ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ ЖИВОТНЫЕ КОЗЫ ОВЦЫ СВИНЬИ КОРОВЫ КУРЫ

НЕКОТОРЫЕ БИОЛОГИЧЕСКИ АКТИВНЫЕ БЕЛКИ, ПОЛУЧАЕМЫЕ С ПОМОЩЬЮ ТРАНСГЕННЫХ ЖИВОТНЫХ БЕЛОК • • • ЖИВОТНОЕ ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА - КОЗА УРОКИНАЗА КОЗА ФАКТОР IX СВЕРТЫВАНИЯ КРОВИ ОВЦА ЛАКТОФЕРРИН КОЗА КОРОВ А • ХИМОЗИН ОВЦА

ИЗМЕНЕНИЕ БИОЛОГИЧЕСКИХ СВОЙСТВ ТРАНСГЕННЫХ ЖИВОТНЫХ • УСТОЙЧИВОСТЬ К ИНФЕКЦИЯМ, • УСКОРЕНИЕ РОСТА (ГЕН ГОРМОНА РОСТА) • ДРУГИЕ СВОЙСТВА

НАУЧНОЕ И БИОТЕХНОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ТРАНСГЕННЫХ ЖИВОТНЫХ • • ОПРЕДЕЛЕНИЕ ФУНКЦИИ ТРАНСГЕНА СОЗДАНИЕ МОДЕЛЕЙ НЕКОТОРЫХ БОЛЕЗНЕЙ ЧЕЛОВЕКА ПОЛУЧЕНИЕ БИОЛОГИЧЕСКИ АКТИВНЫХ БЕЛКОВ УЛУЧШЕНИЕ СВОЙСТВ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ

ПЕРСПЕКТИВЫ • СОЗДАНИЕ НОВЫХ ПОРОД СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ С РАЗЛИЧНЫМИ ПОЛЕЗНЫМИ СВОЙСТВАМИ • СУЩЕСТВЕННОЕ РАСШИРЕНИЕ АССОРТИМЕНТА БАВ, ПОЛУЧАЕМЫХ В ТРАНСГЕННЫХ ЖИВОТНЫХ
Молекулярная биотехнология 3.ppt