Ваше (жизненное) время ограничено… Не позволяйте шуму чужих


































6190-lektsia-4-karbonily-soon.ppt
- Количество слайдов: 98
 Ваше (жизненное) время ограничено… Не позволяйте шуму чужих мнений перебить ваш внутренний голос. И самое главное, имейте храбрость следовать вашему сердцу и интуиции. Они каким-то образом уже знают, кем вы действительно хотите стать. Все остальное вторично. Стив Джобс
Ваше (жизненное) время ограничено… Не позволяйте шуму чужих мнений перебить ваш внутренний голос. И самое главное, имейте храбрость следовать вашему сердцу и интуиции. Они каким-то образом уже знают, кем вы действительно хотите стать. Все остальное вторично. Стив Джобс
 Альдегиды и кетоны
Альдегиды и кетоны
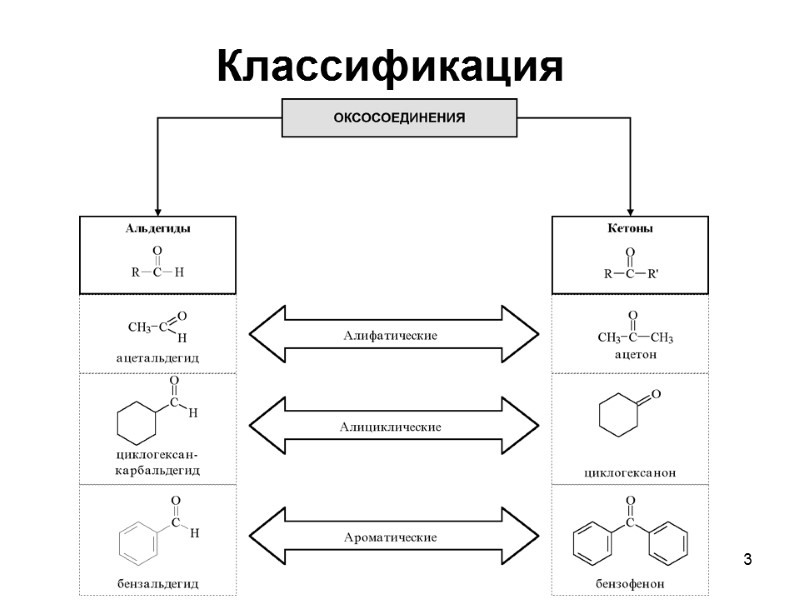
 3 Классификация
3 Классификация
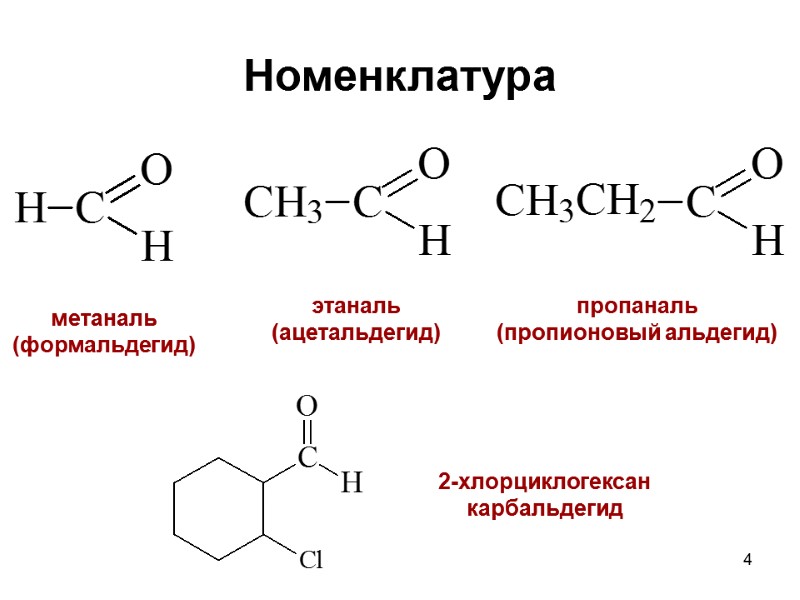
 4 Номенклатура метаналь (формальдегид) этаналь (ацетальдегид) пропаналь (пропионовый альдегид) 2-хлорциклогексан карбальдегид
4 Номенклатура метаналь (формальдегид) этаналь (ацетальдегид) пропаналь (пропионовый альдегид) 2-хлорциклогексан карбальдегид
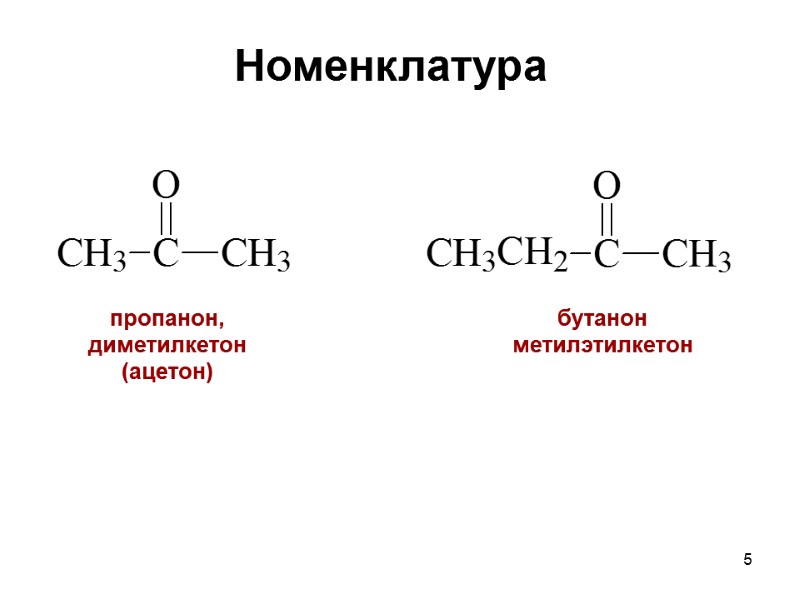
 5 Номенклатура бутанон метилэтилкетон пропанон, диметилкетон (ацетон)
5 Номенклатура бутанон метилэтилкетон пропанон, диметилкетон (ацетон)
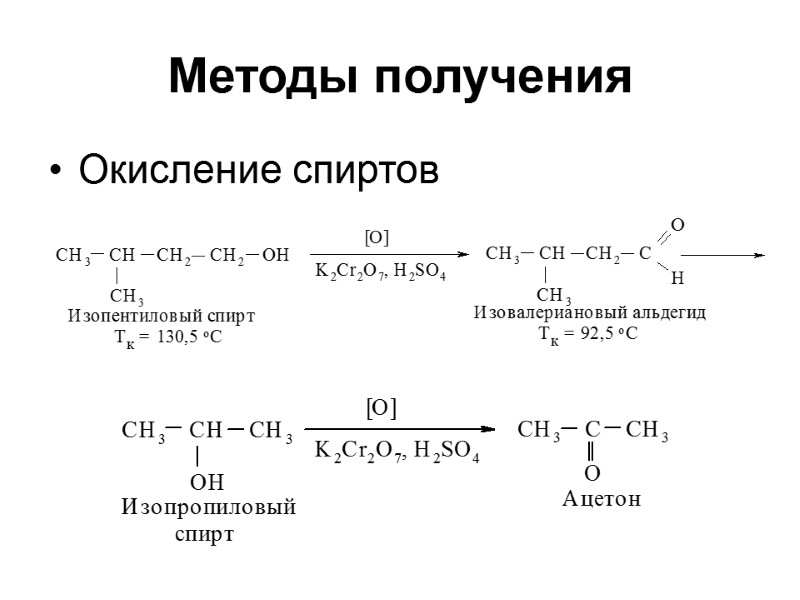
 Методы получения Окисление спиртов
Методы получения Окисление спиртов
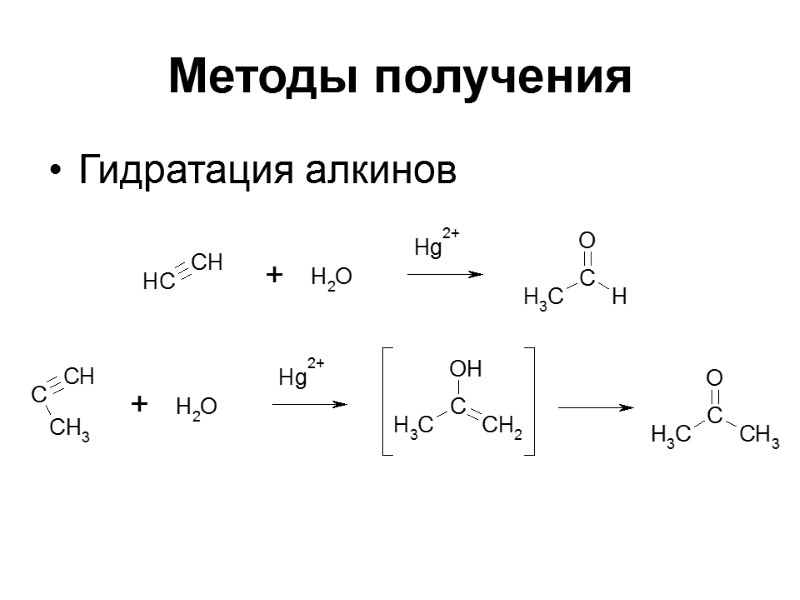
 Методы получения Гидратация алкинов
Методы получения Гидратация алкинов
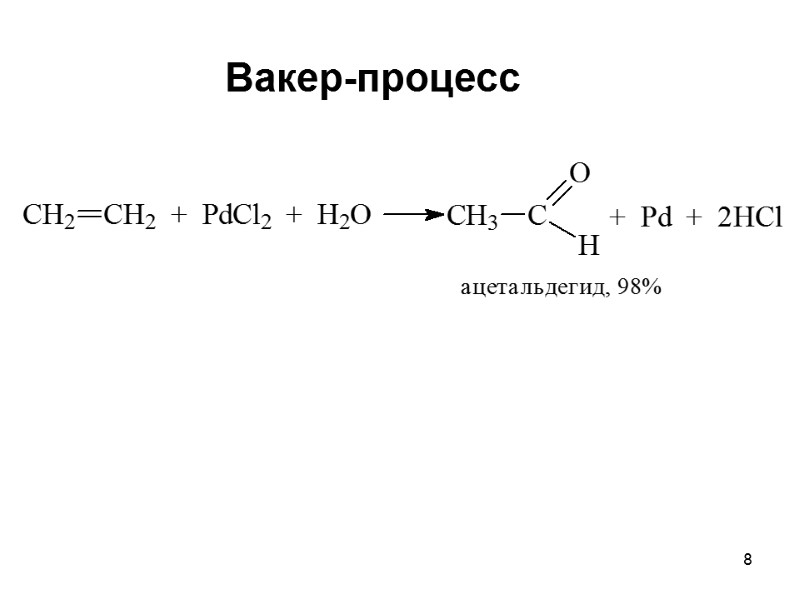
 8 Вакер-процесс
8 Вакер-процесс
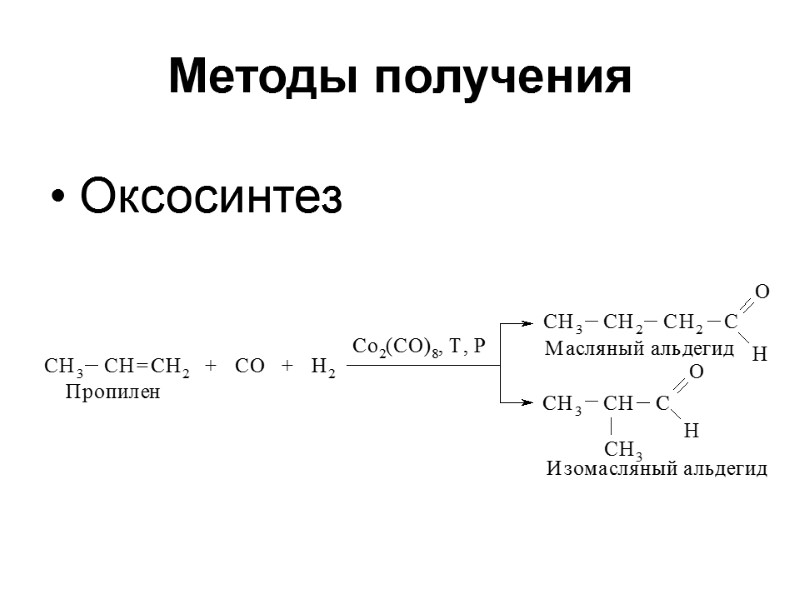
 Методы получения Оксосинтез
Методы получения Оксосинтез
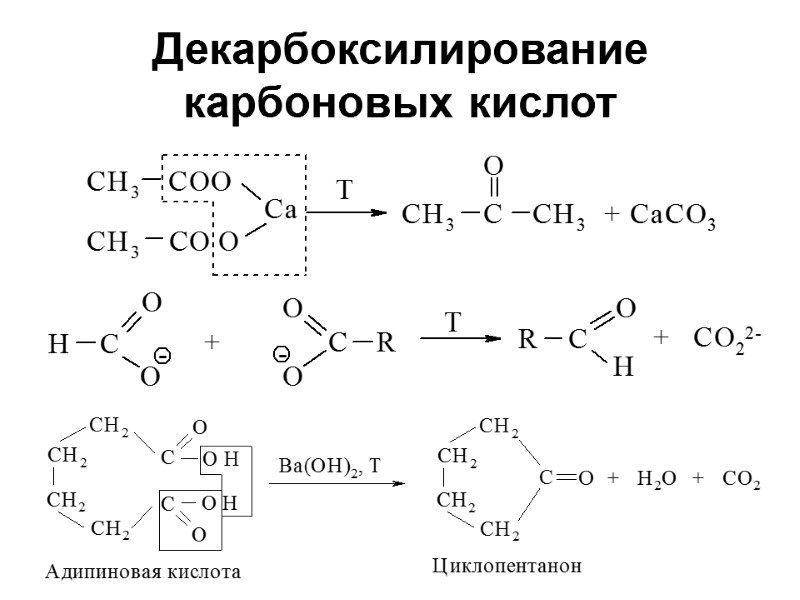
 Декарбоксилирование карбоновых кислот
Декарбоксилирование карбоновых кислот
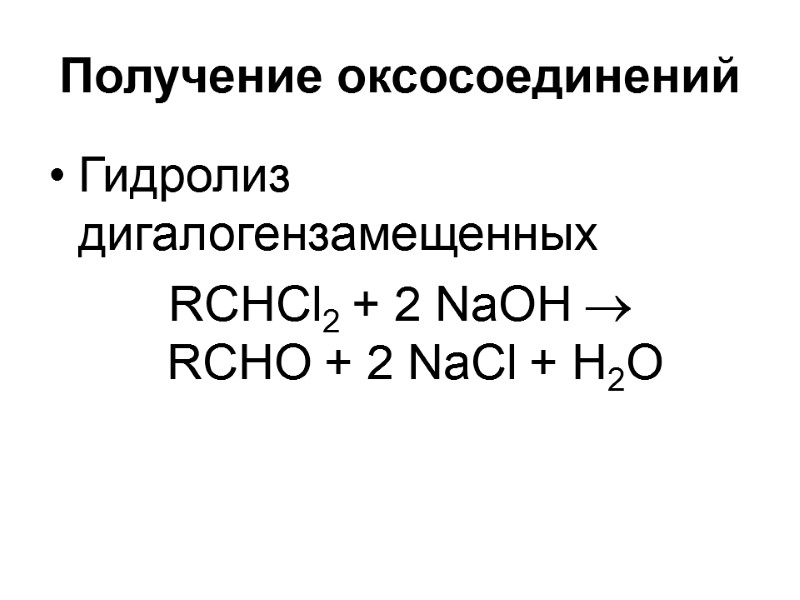
 Получение оксосоединений Гидролиз дигалогензамещенных RCHCl2 + 2 NaOH RCHO + 2 NaCl + H2О
Получение оксосоединений Гидролиз дигалогензамещенных RCHCl2 + 2 NaOH RCHO + 2 NaCl + H2О
 Физические свойства Низшие альдегиды имеют резкий запах Высшие гомологи имеют запах цветов и фруктов Низшие альдегиды и кетоны заметно растворимы в воде Растворимость резко уменьшается, когда число атомов углерода в молекуле равно или более пяти
Физические свойства Низшие альдегиды имеют резкий запах Высшие гомологи имеют запах цветов и фруктов Низшие альдегиды и кетоны заметно растворимы в воде Растворимость резко уменьшается, когда число атомов углерода в молекуле равно или более пяти
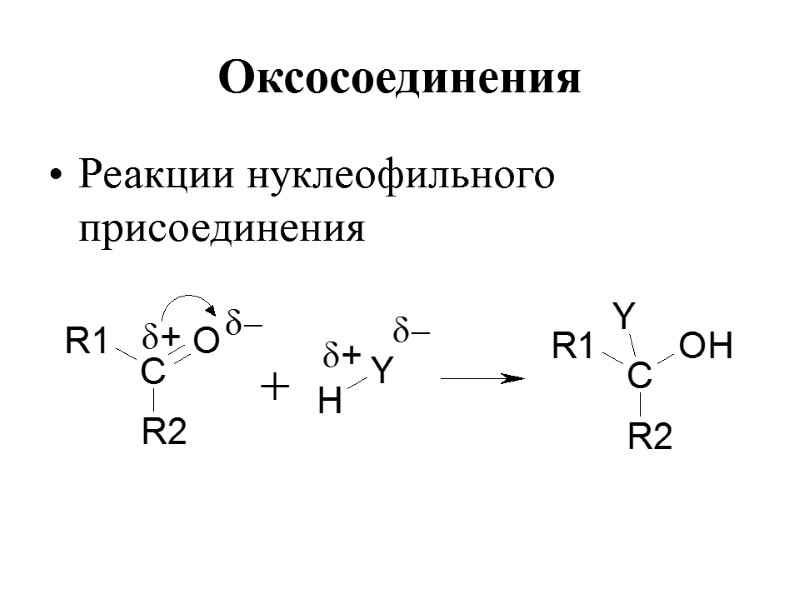
 Оксосоединения Реакции нуклеофильного присоединения
Оксосоединения Реакции нуклеофильного присоединения
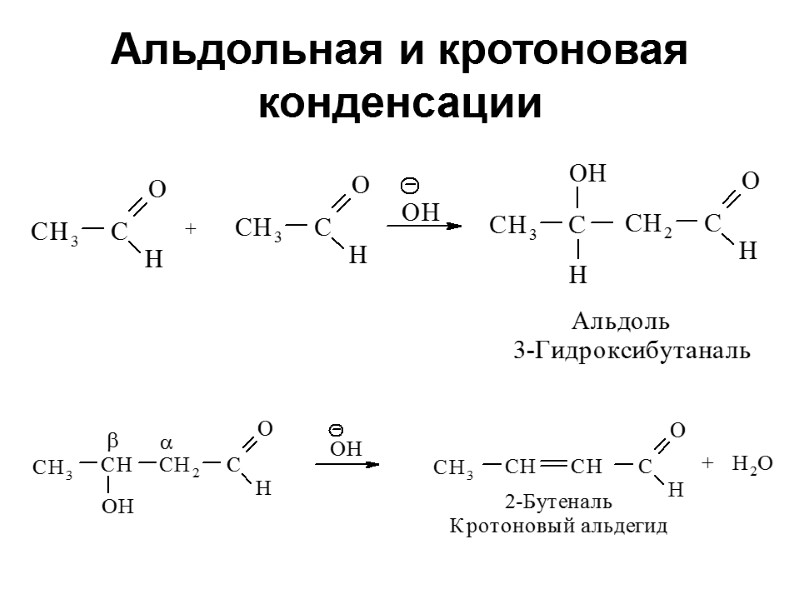
 Альдольная и кротоновая конденсации
Альдольная и кротоновая конденсации
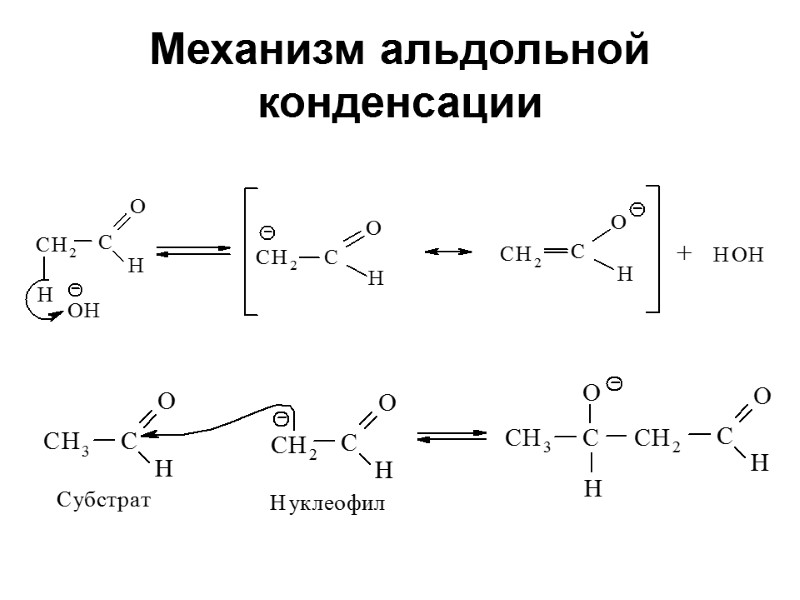
 Механизм альдольной конденсации
Механизм альдольной конденсации
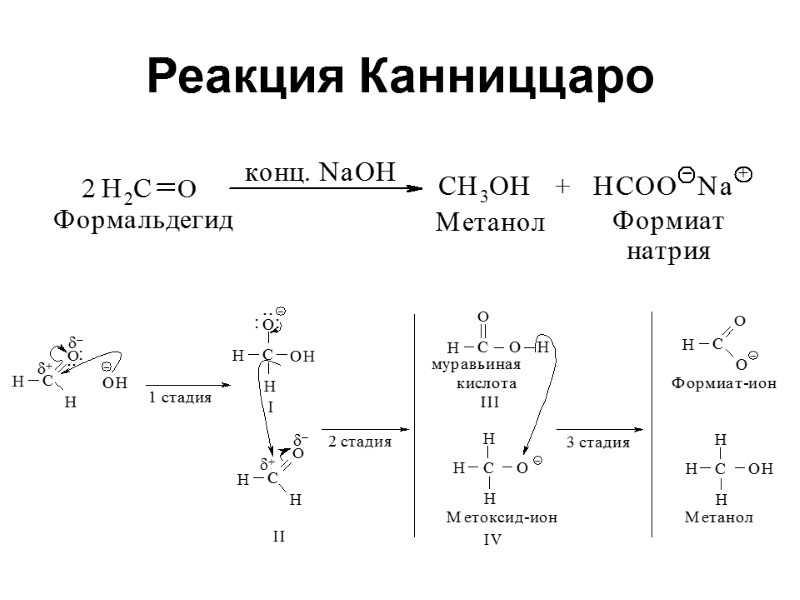
 Реакция Канниццаро
Реакция Канниццаро
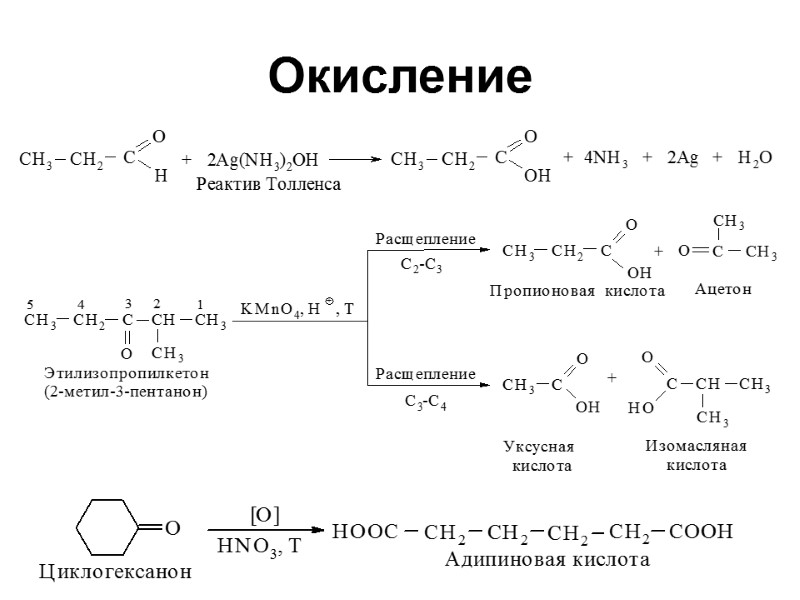
 Окисление
Окисление
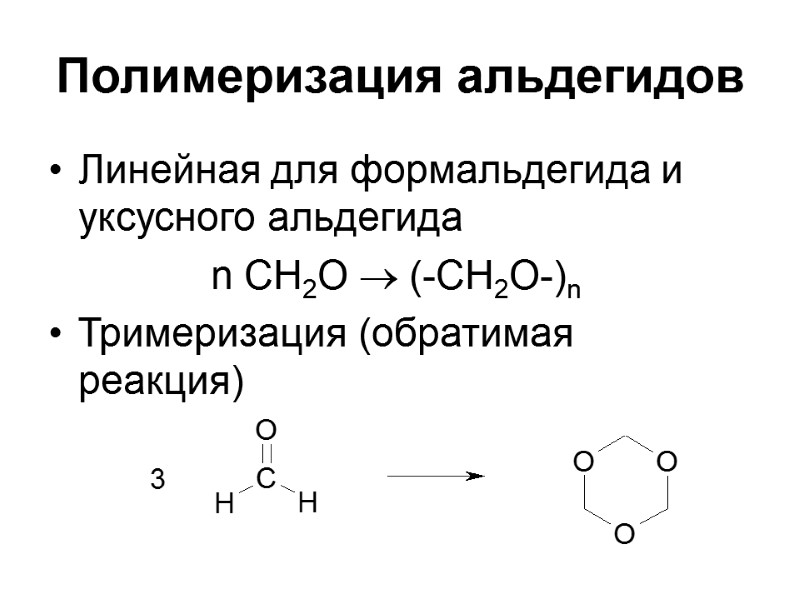
 Полимеризация альдегидов Линейная для формальдегида и уксусного альдегида n CH2O (-CH2O-)n Тримеризация (обратимая реакция)
Полимеризация альдегидов Линейная для формальдегида и уксусного альдегида n CH2O (-CH2O-)n Тримеризация (обратимая реакция)
 Карбоновые кислоты и их производные
Карбоновые кислоты и их производные
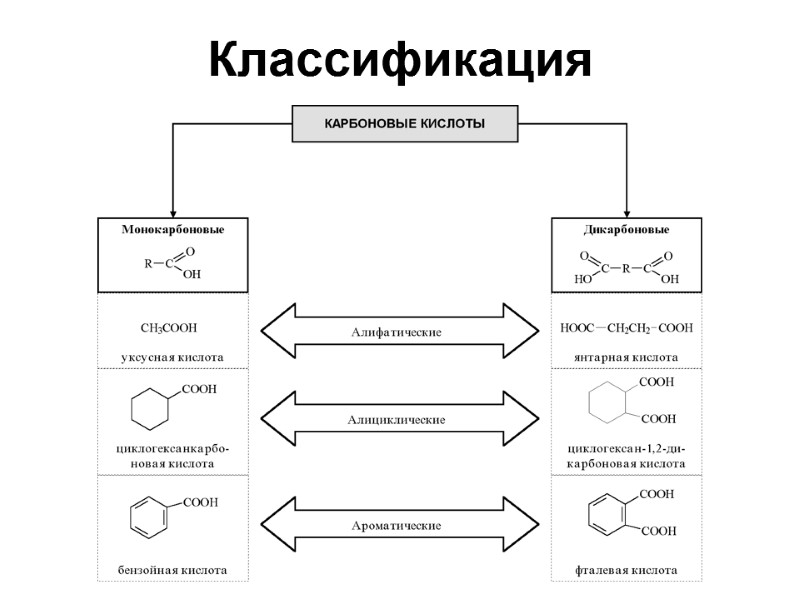
 Классификация
Классификация
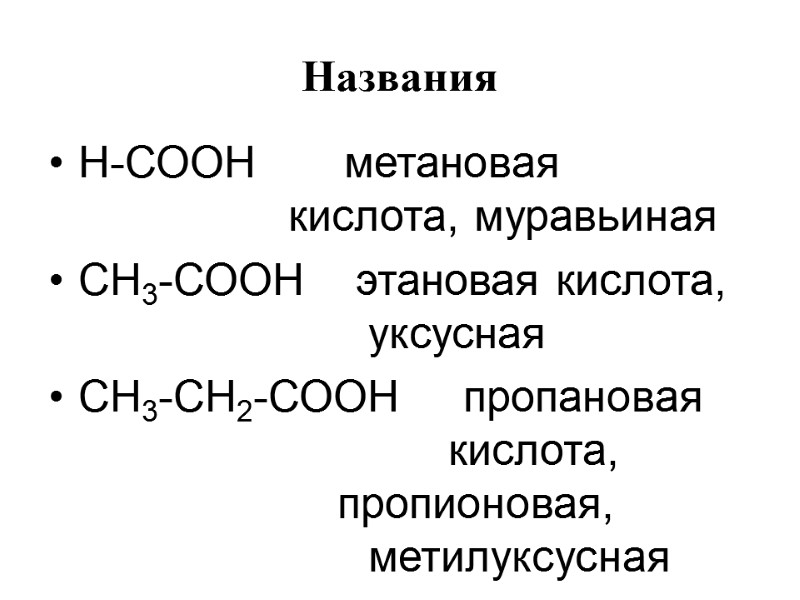
 Названия Н-СООН метановая кислота, муравьиная СН3-СООН этановая кислота, уксусная СН3-СН2-СООН пропановая кислота, пропионовая, метилуксусная
Названия Н-СООН метановая кислота, муравьиная СН3-СООН этановая кислота, уксусная СН3-СН2-СООН пропановая кислота, пропионовая, метилуксусная
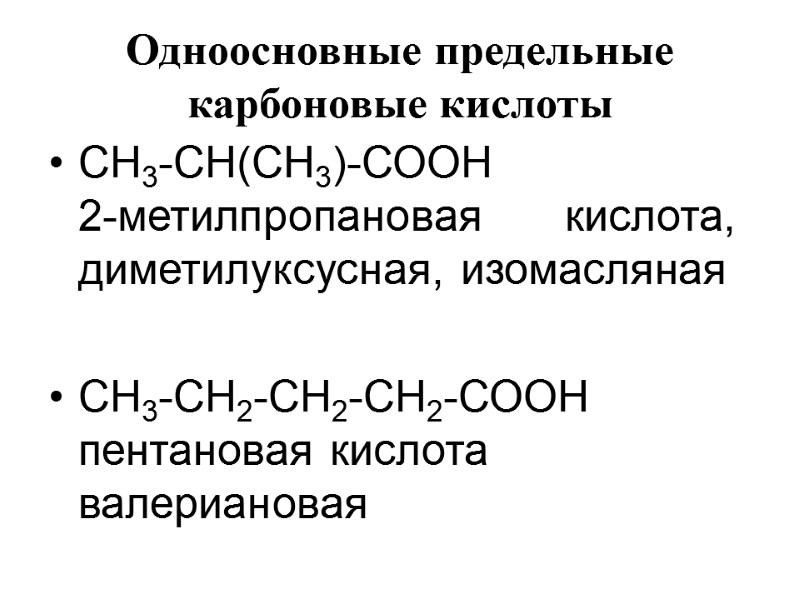
 Одноосновные предельные карбоновые кислоты СН3-СН(СН3)-СООН 2-метилпропановая кислота, диметилуксусная, изомасляная СН3-СН2-СН2-СН2-СООН пентановая кислота валериановая
Одноосновные предельные карбоновые кислоты СН3-СН(СН3)-СООН 2-метилпропановая кислота, диметилуксусная, изомасляная СН3-СН2-СН2-СН2-СООН пентановая кислота валериановая
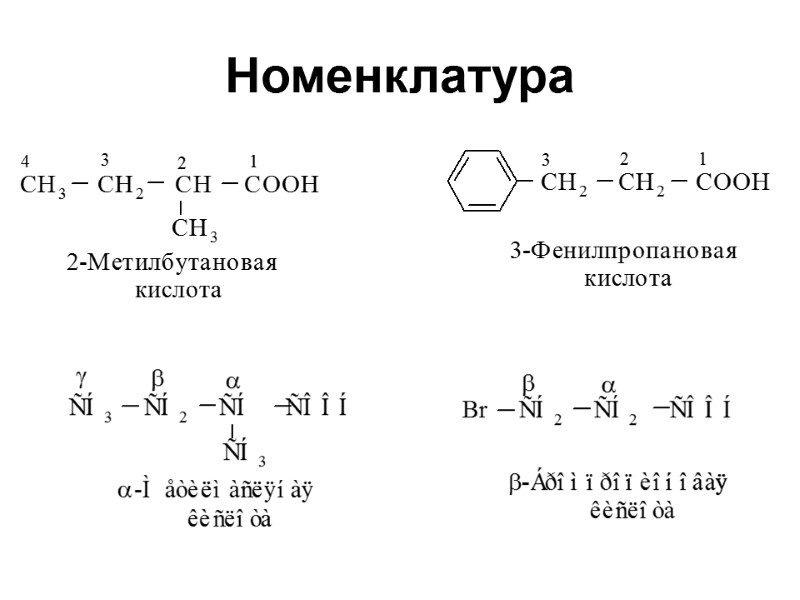
 Номенклатура
Номенклатура
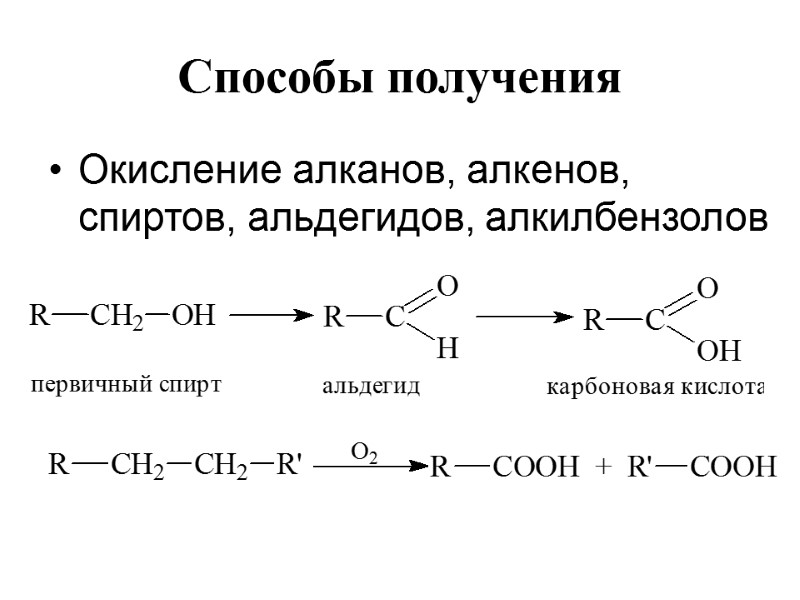
 Способы получения Окисление алканов, алкенов, спиртов, альдегидов, алкилбензолов
Способы получения Окисление алканов, алкенов, спиртов, альдегидов, алкилбензолов
 Способы получения Гидролиз (омыление) нитрилов R-CN + 2 Н2О R-СООН + NH3
Способы получения Гидролиз (омыление) нитрилов R-CN + 2 Н2О R-СООН + NH3
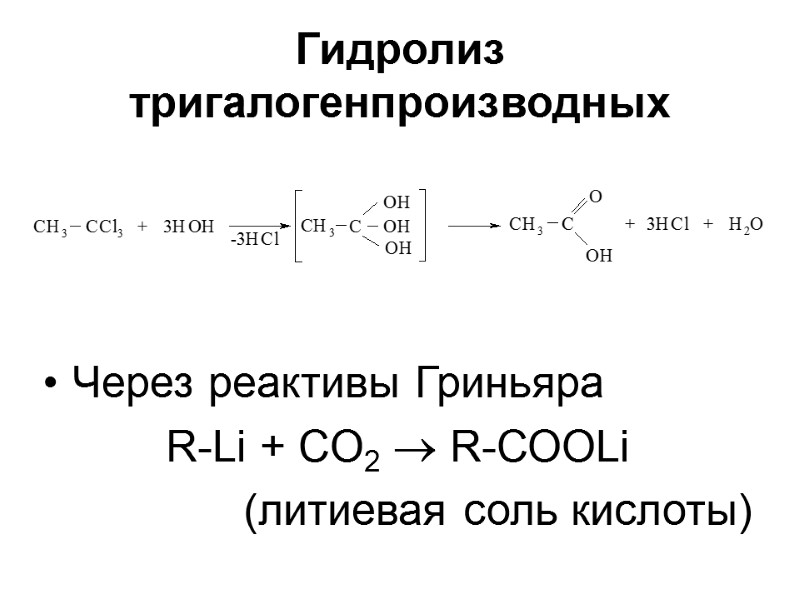
 Гидролиз тригалогенпроизводных Через реактивы Гриньяра R-Li + CO2 R-СООLi (литиевая соль кислоты)
Гидролиз тригалогенпроизводных Через реактивы Гриньяра R-Li + CO2 R-СООLi (литиевая соль кислоты)
 Физические свойства Муравьиная и уксусная кислоты обладают раздражающим запахом Масляная, валериановая и капроновая кислоты имеют неприятный запах Высшие жирные и ароматические кислоты не имеют запаха, поскольку обладают малой летучестью
Физические свойства Муравьиная и уксусная кислоты обладают раздражающим запахом Масляная, валериановая и капроновая кислоты имеют неприятный запах Высшие жирные и ароматические кислоты не имеют запаха, поскольку обладают малой летучестью
 Физические свойства Алифатические кислоты по растворимости похожи на спирты: кислоты С1-С4 смешиваются с водой, растворимость валериановой кислоты незначительна, а высшие кислоты практически не растворимы в воде
Физические свойства Алифатические кислоты по растворимости похожи на спирты: кислоты С1-С4 смешиваются с водой, растворимость валериановой кислоты незначительна, а высшие кислоты практически не растворимы в воде
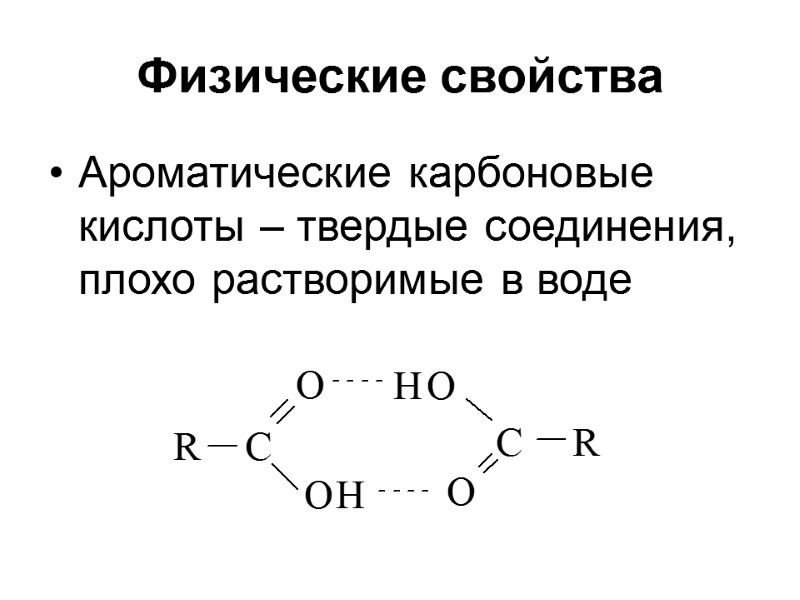
 Физические свойства Ароматические карбоновые кислоты – твердые соединения, плохо растворимые в воде
Физические свойства Ароматические карбоновые кислоты – твердые соединения, плохо растворимые в воде
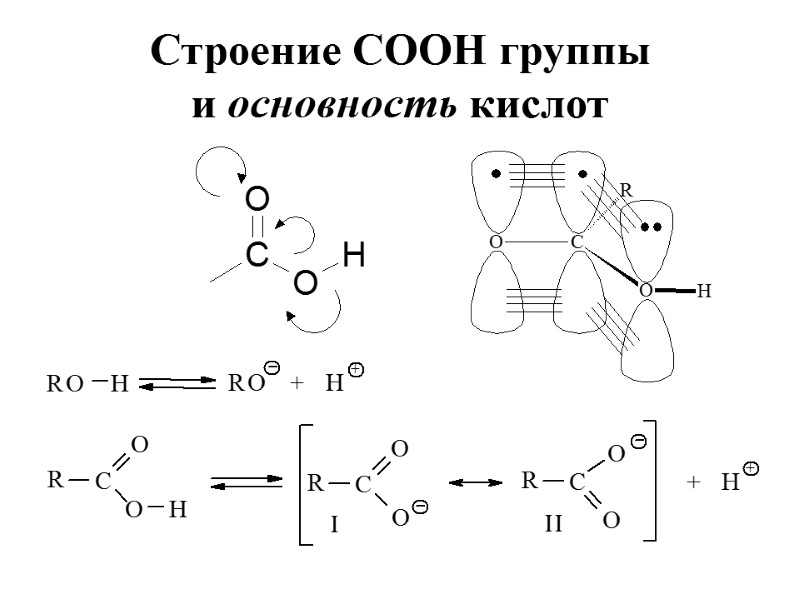
 Строение СООН группы и основность кислот
Строение СООН группы и основность кислот
 Влияние заместителей на кислотность Электронодонорные заместители увеличивают отрицательный заряд и дестабилизируют анион – кислотность уменьшается
Влияние заместителей на кислотность Электронодонорные заместители увеличивают отрицательный заряд и дестабилизируют анион – кислотность уменьшается
 Влияние заместителей на кислотность Электроноакцепторные заместители, способствующие распределению отрицательного заряда в анионе, делают его более устойчивым и тем самым увеличивают кислотность
Влияние заместителей на кислотность Электроноакцепторные заместители, способствующие распределению отрицательного заряда в анионе, делают его более устойчивым и тем самым увеличивают кислотность
 Химические свойства Кислотные свойства уксусная кислота 4,76 монохлоруксусная кислота 2,85 дихлоруксусная кислота 1,25 трихлоруксусная кислота 0,66 pKa
Химические свойства Кислотные свойства уксусная кислота 4,76 монохлоруксусная кислота 2,85 дихлоруксусная кислота 1,25 трихлоруксусная кислота 0,66 pKa
 Химические свойства С основаниями С основными оксидами С активными металлами С солями
Химические свойства С основаниями С основными оксидами С активными металлами С солями
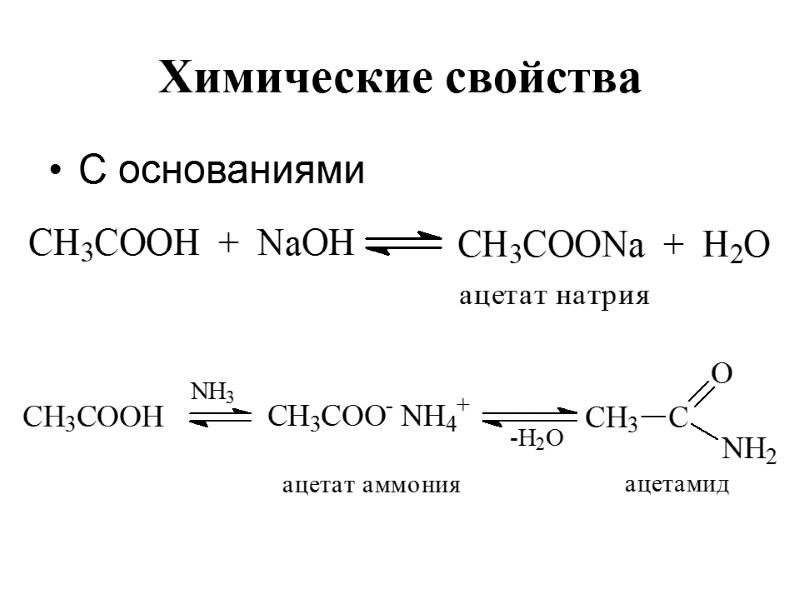
 Химические свойства С основаниями
Химические свойства С основаниями
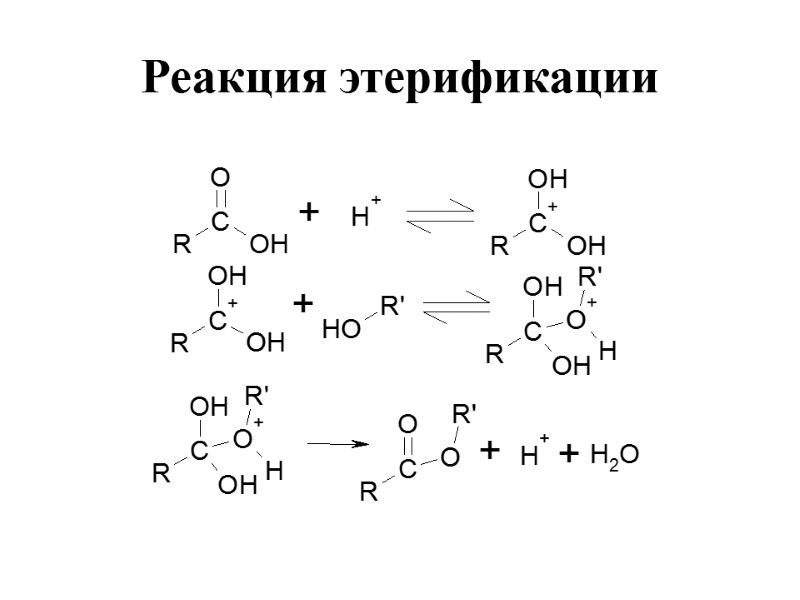
 Реакция этерификации
Реакция этерификации
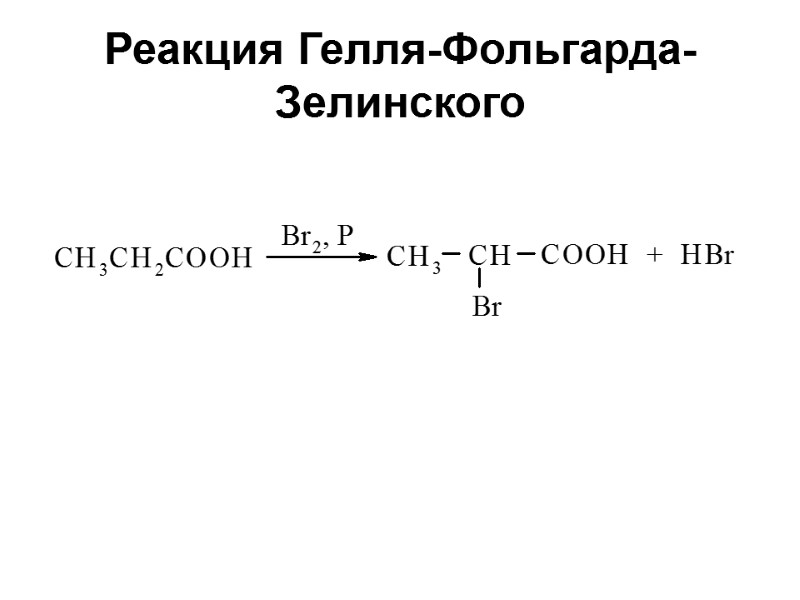
 Реакция Гелля-Фольгарда-Зелинского
Реакция Гелля-Фольгарда-Зелинского
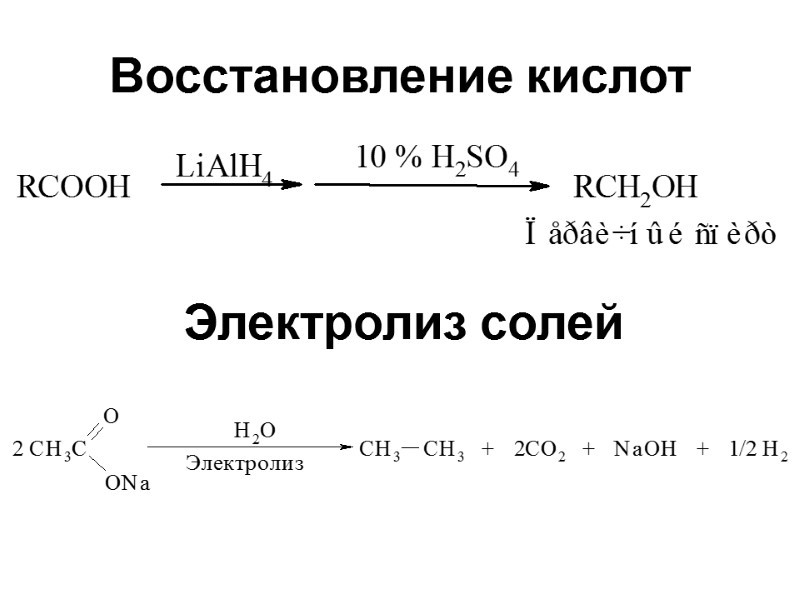
 Восстановление кислот Электролиз солей
Восстановление кислот Электролиз солей
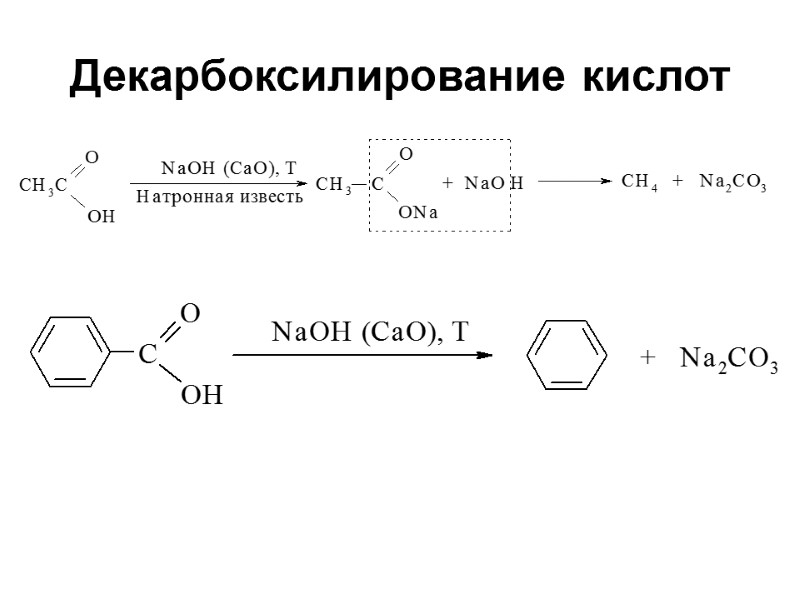
 Декарбоксилирование кислот
Декарбоксилирование кислот
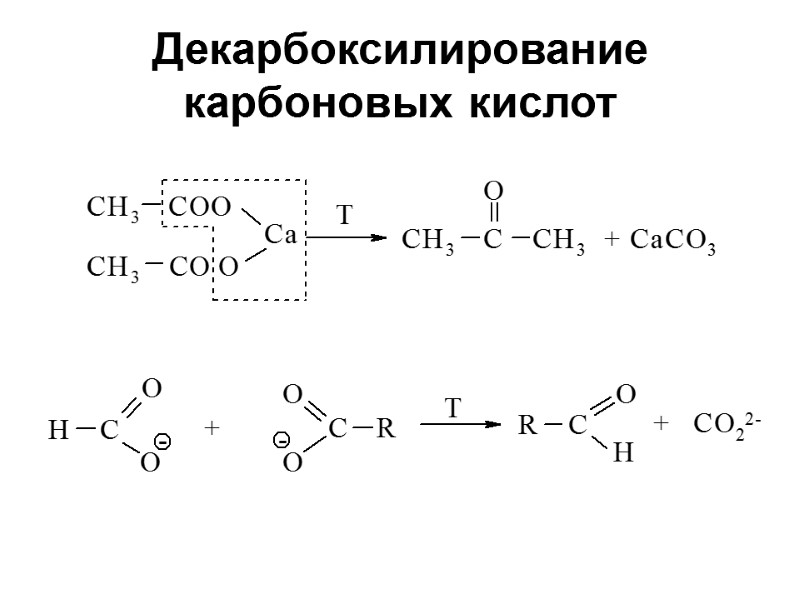
 Декарбоксилирование карбоновых кислот
Декарбоксилирование карбоновых кислот
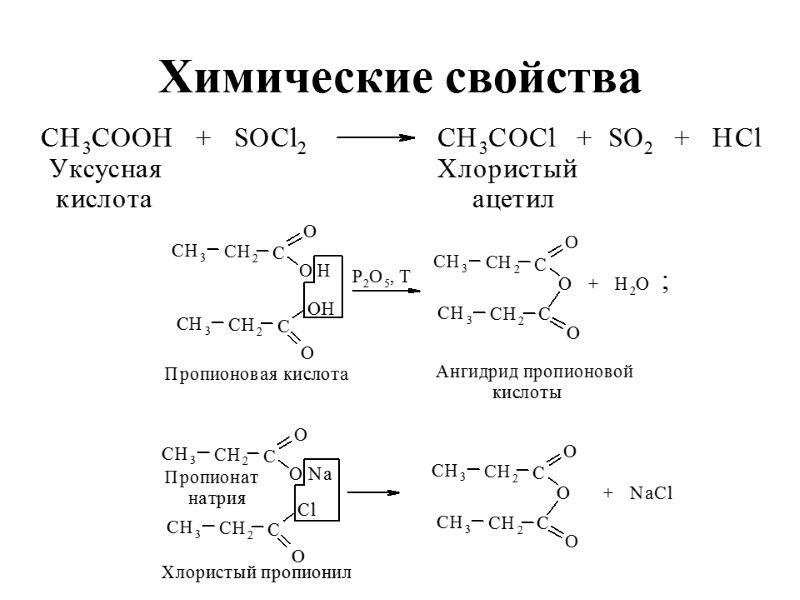
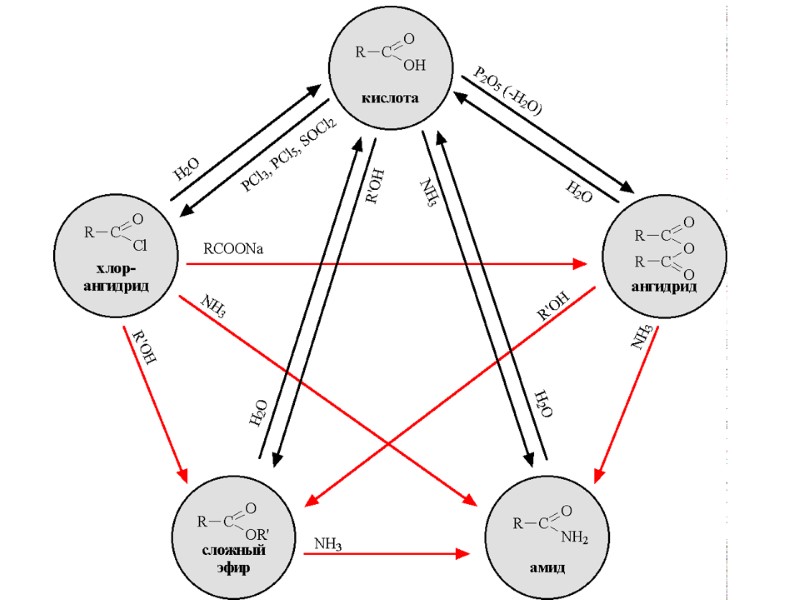
 Химические свойства
Химические свойства
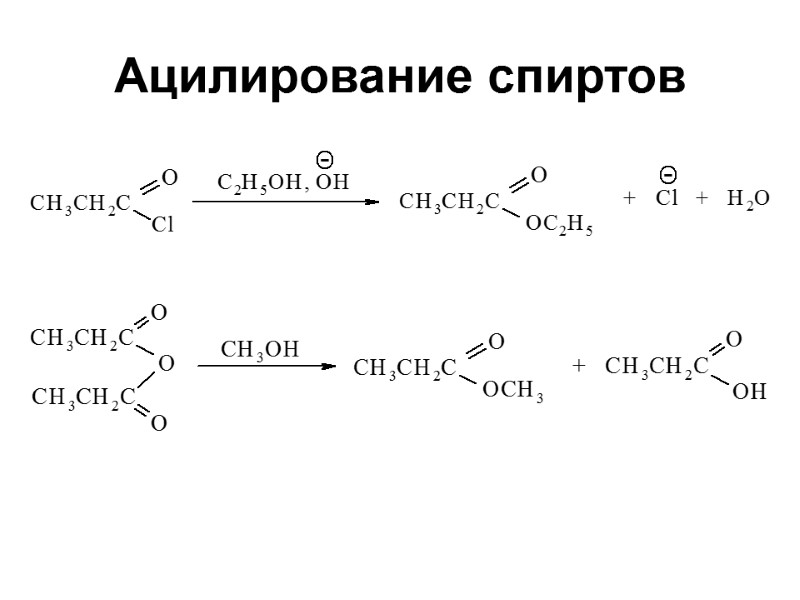
 Ацилирование спиртов
Ацилирование спиртов
 Сложные эфиры HCOOC2H5 - этилформиат, этиловый эфир муравьиной к-ты CH3COOCH3 - метилацетат, метиловый эфир уксусной к-ты CH3COOC4H9 - бутилацетат, уксуснобутиловый эфир CH3CH2COOCH3 - метилпропионат, метиловый эфир пропионовой кислоты
Сложные эфиры HCOOC2H5 - этилформиат, этиловый эфир муравьиной к-ты CH3COOCH3 - метилацетат, метиловый эфир уксусной к-ты CH3COOC4H9 - бутилацетат, уксуснобутиловый эфир CH3CH2COOCH3 - метилпропионат, метиловый эфир пропионовой кислоты
 Сложные эфиры Многие обладают приятным фруктовым запахом Муравьиноамиловый - вишни Муравьиноэтиловый – рома Уксусноамиловый – банана Масляноэтиловый – абрикоса Маслянобутиловый – ананаса Изовалерияноэтиловый – яблока
Сложные эфиры Многие обладают приятным фруктовым запахом Муравьиноамиловый - вишни Муравьиноэтиловый – рома Уксусноамиловый – банана Масляноэтиловый – абрикоса Маслянобутиловый – ананаса Изовалерияноэтиловый – яблока
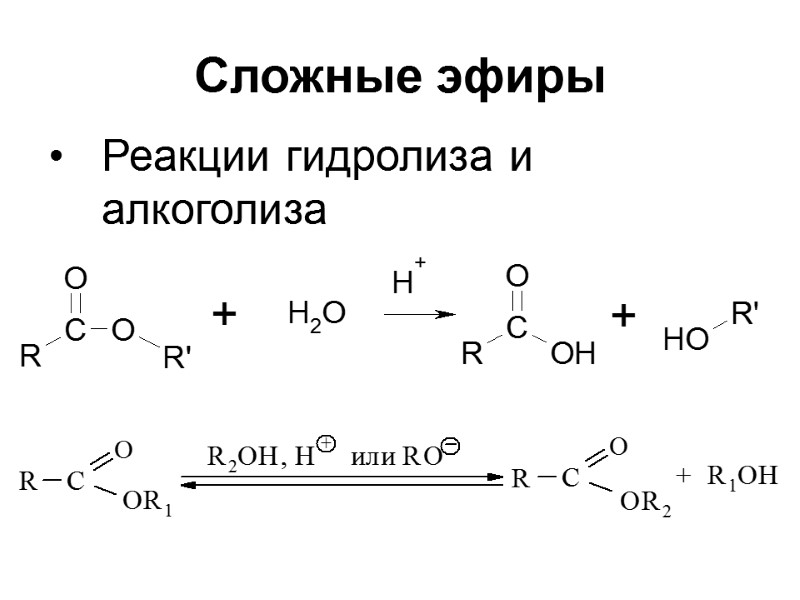
 Сложные эфиры Реакции гидролиза и алкоголиза
Сложные эфиры Реакции гидролиза и алкоголиза
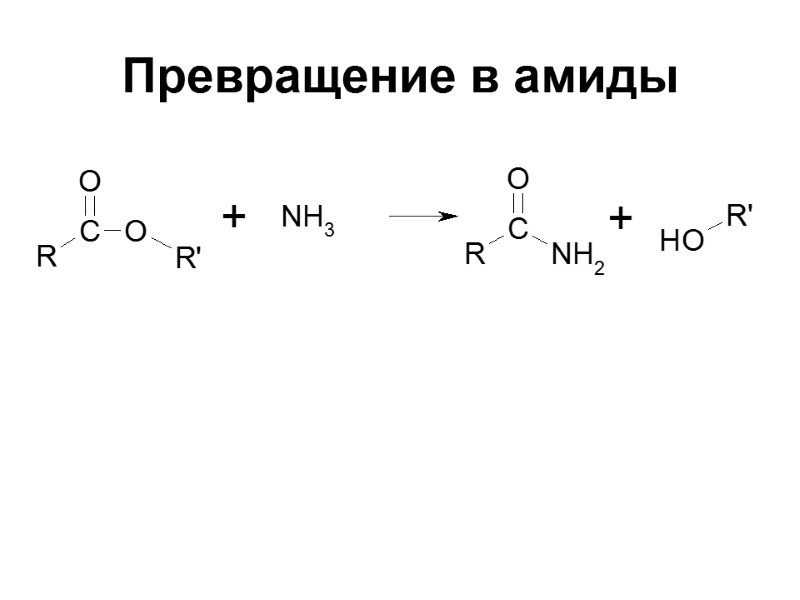
 Превращение в амиды
Превращение в амиды
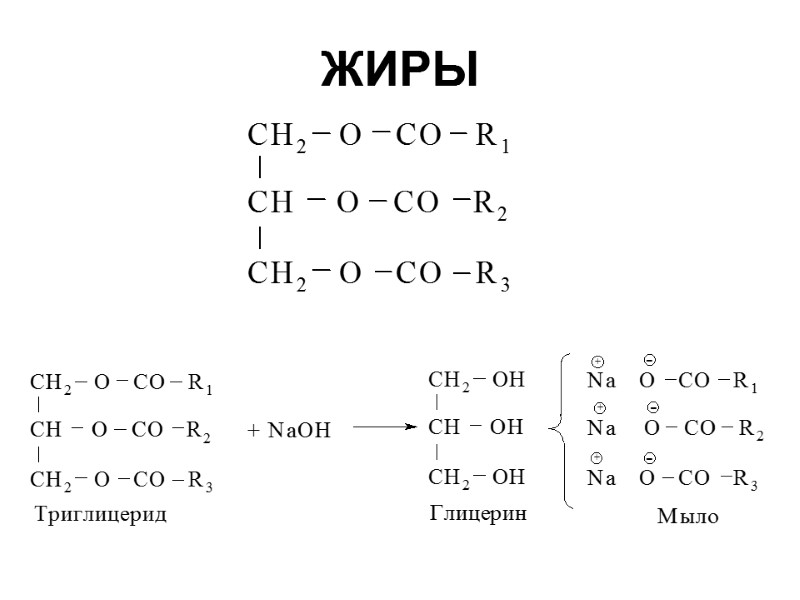
 ЖИРЫ
ЖИРЫ

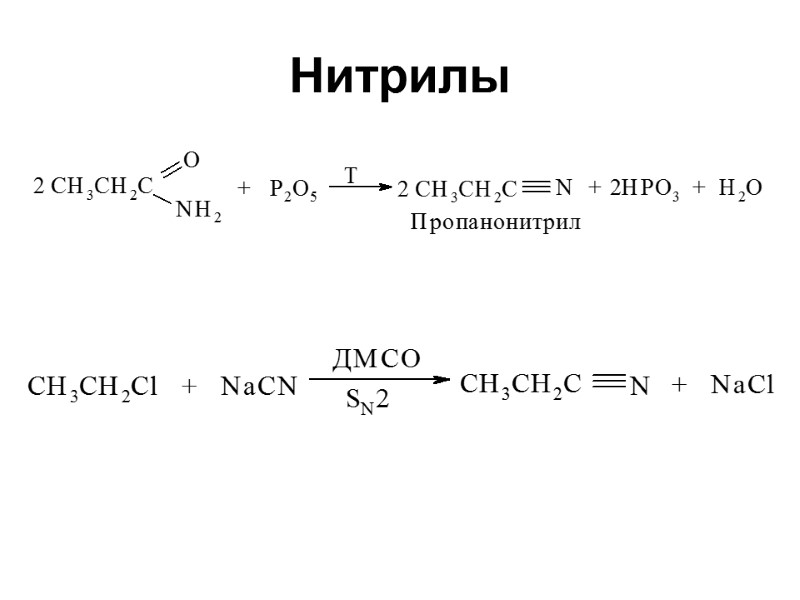
 Нитрилы
Нитрилы
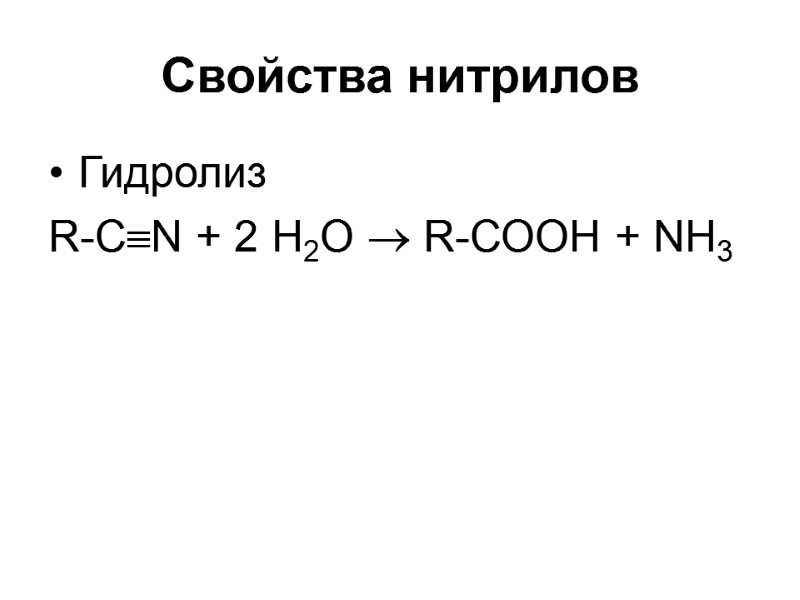
 Свойства нитрилов Гидролиз R-CN + 2 Н2О R-СООН + NH3
Свойства нитрилов Гидролиз R-CN + 2 Н2О R-СООН + NH3
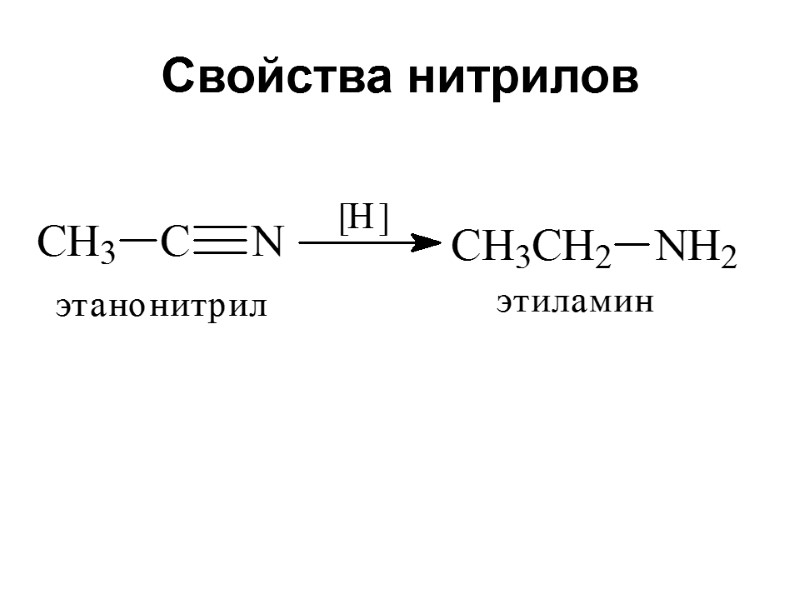
 Свойства нитрилов
Свойства нитрилов
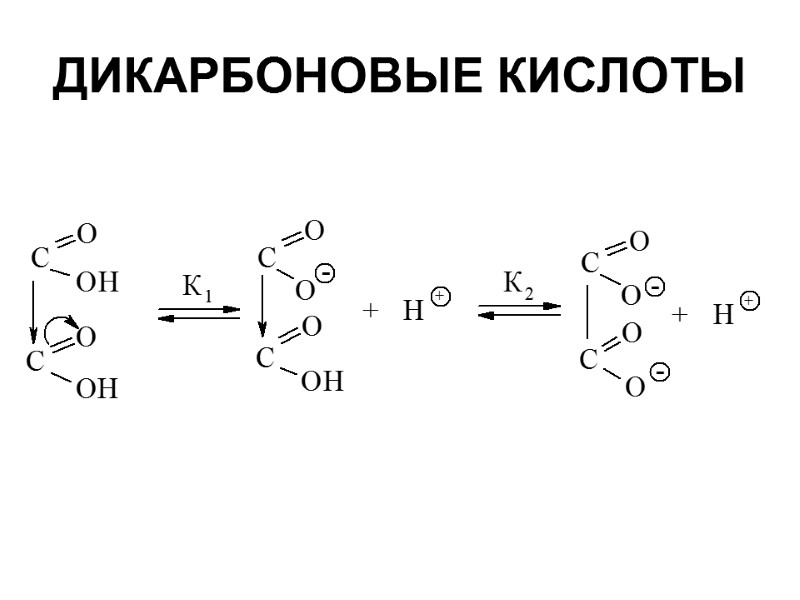
 ДИКАРБОНОВЫЕ КИСЛОТЫ
ДИКАРБОНОВЫЕ КИСЛОТЫ
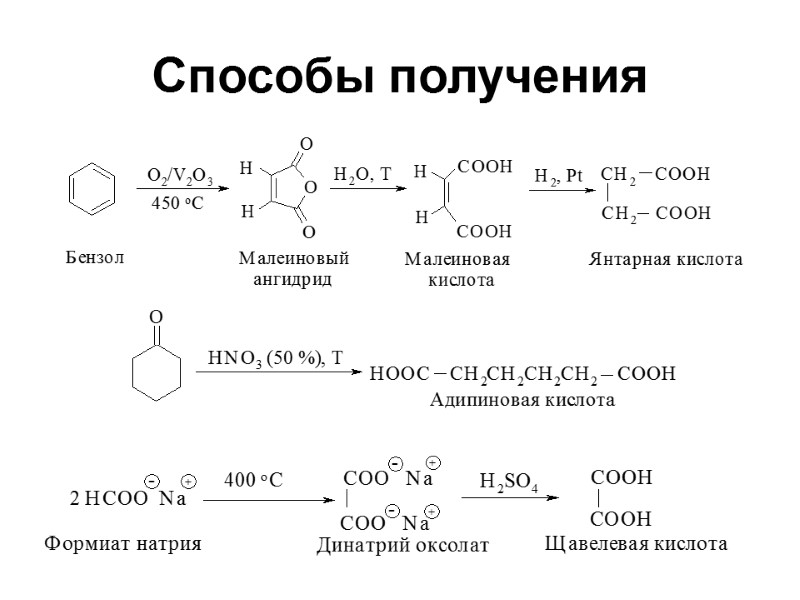
 Способы получения
Способы получения
 Способы получения
Способы получения
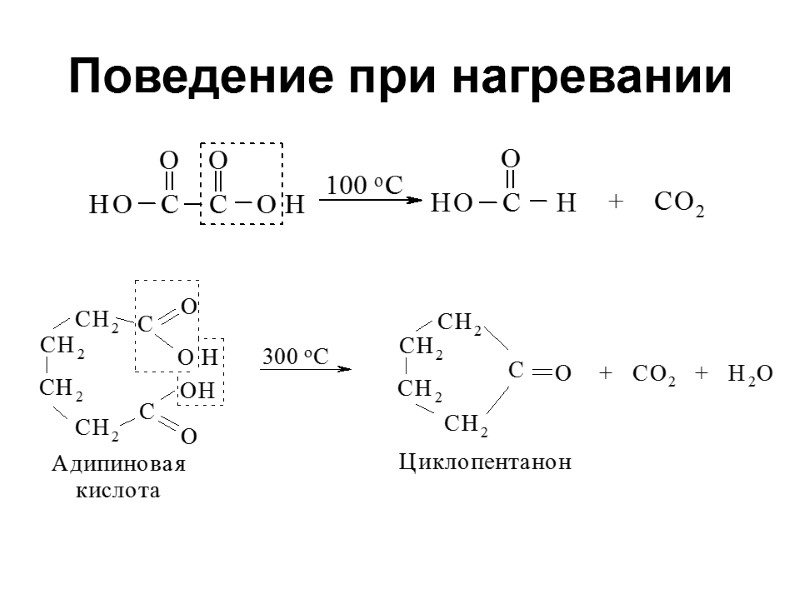
 Поведение при нагревании
Поведение при нагревании
 Поведение при нагревании
Поведение при нагревании
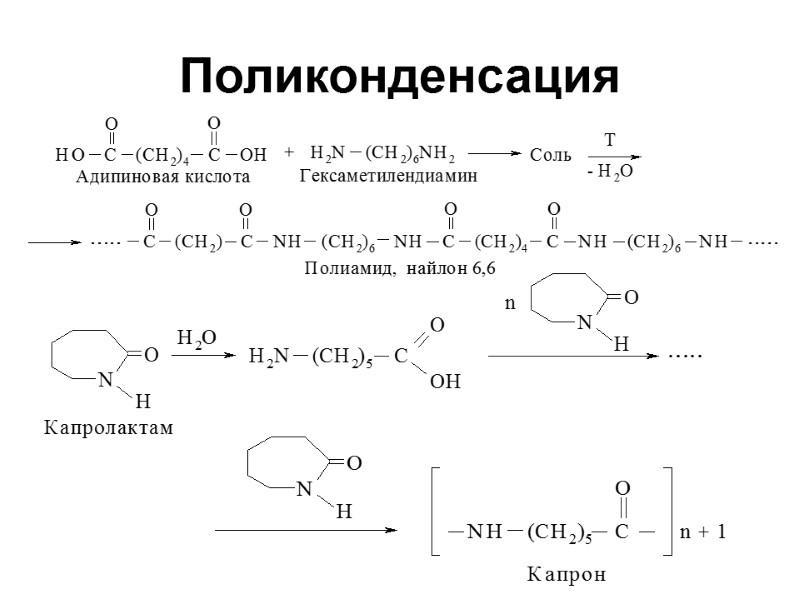
 Поликонденсация
Поликонденсация
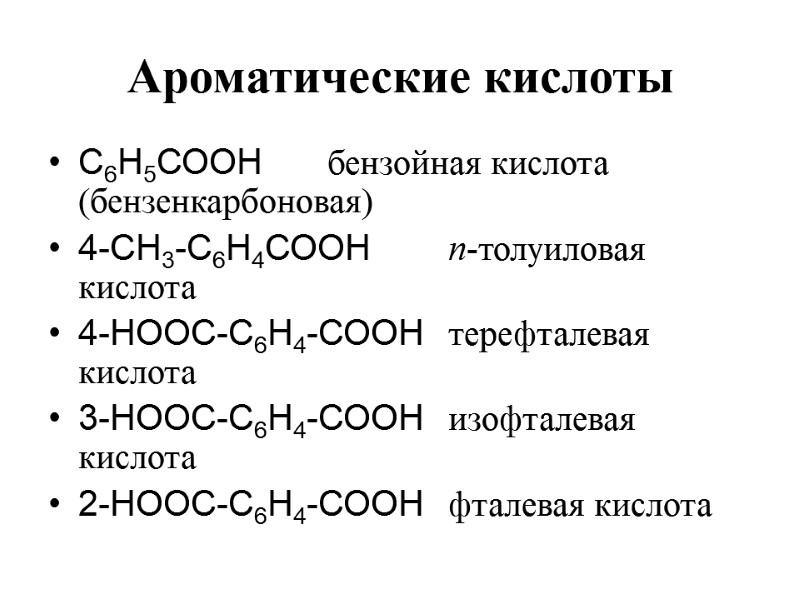
 Ароматические кислоты С6Н5СООН бензойная кислота (бензенкарбоновая) 4-СН3-С6Н4СООН п-толуиловая кислота 4-НООС-С6Н4-СООН терефталевая кислота 3-НООС-С6Н4-СООН изофталевая кислота 2-НООС-С6Н4-СООН фталевая кислота
Ароматические кислоты С6Н5СООН бензойная кислота (бензенкарбоновая) 4-СН3-С6Н4СООН п-толуиловая кислота 4-НООС-С6Н4-СООН терефталевая кислота 3-НООС-С6Н4-СООН изофталевая кислота 2-НООС-С6Н4-СООН фталевая кислота
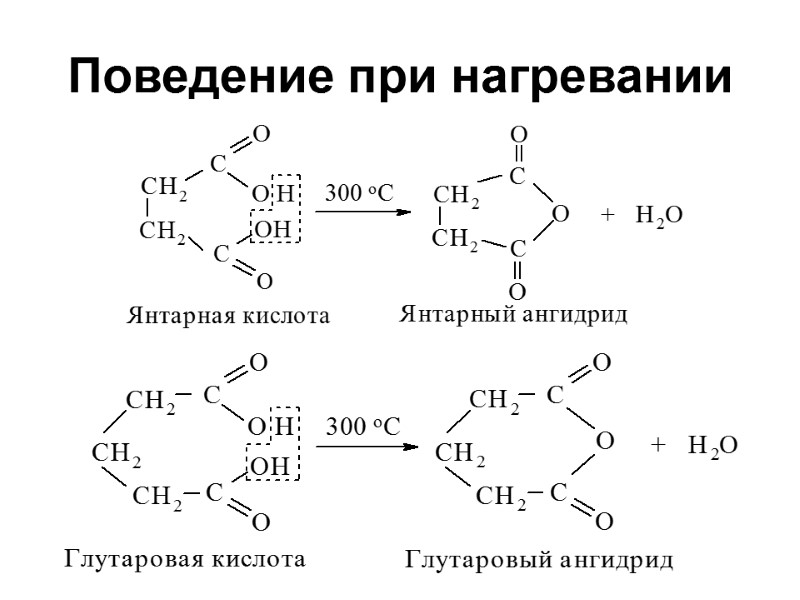
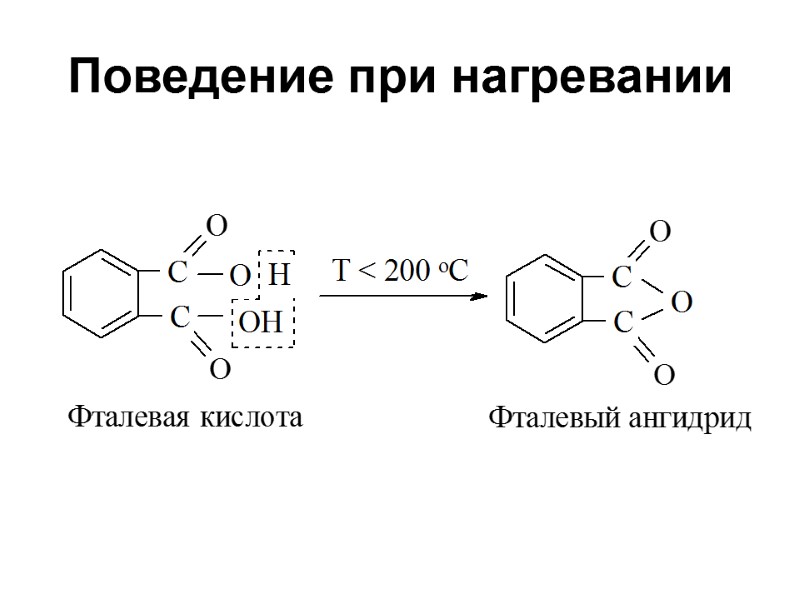
 Поведение при нагревании
Поведение при нагревании
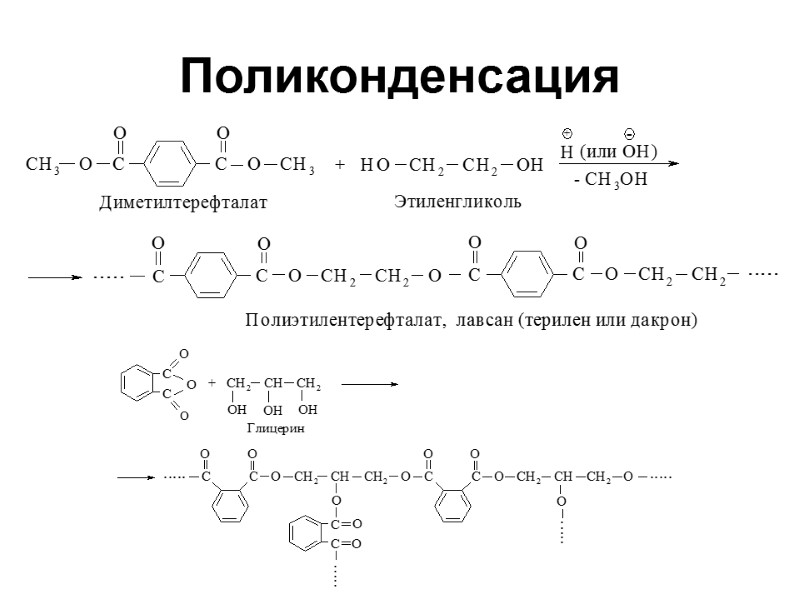
 Поликонденсация
Поликонденсация
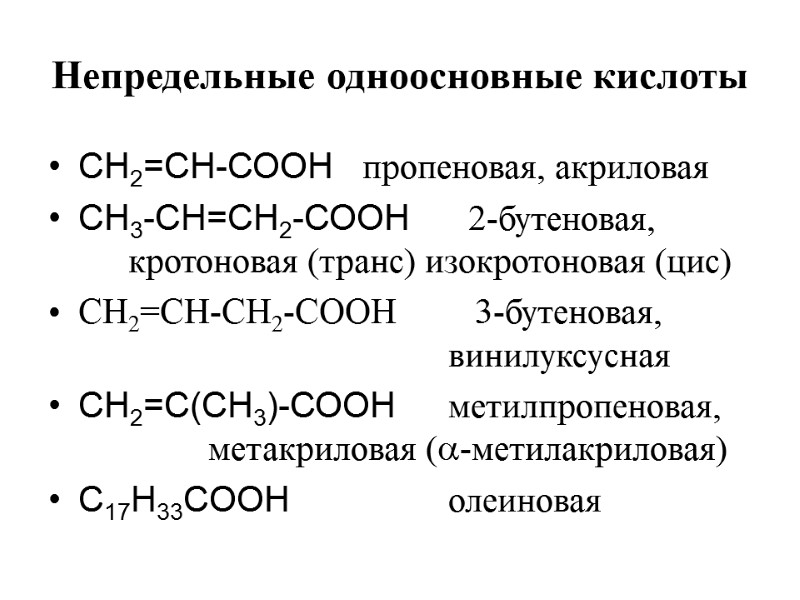
 Непредельные одноосновные кислоты СН2=СН-СООН пропеновая, акриловая CН3-СН=СН2-СООН 2-бутеновая, кротоновая (транс) изокротоновая (цис) CН2=СН-СН2-СООН 3-бутеновая, винилуксусная СН2=С(СН3)-СООН метилпропеновая, метакриловая (-метилакриловая) C17H33COOH олеиновая
Непредельные одноосновные кислоты СН2=СН-СООН пропеновая, акриловая CН3-СН=СН2-СООН 2-бутеновая, кротоновая (транс) изокротоновая (цис) CН2=СН-СН2-СООН 3-бутеновая, винилуксусная СН2=С(СН3)-СООН метилпропеновая, метакриловая (-метилакриловая) C17H33COOH олеиновая
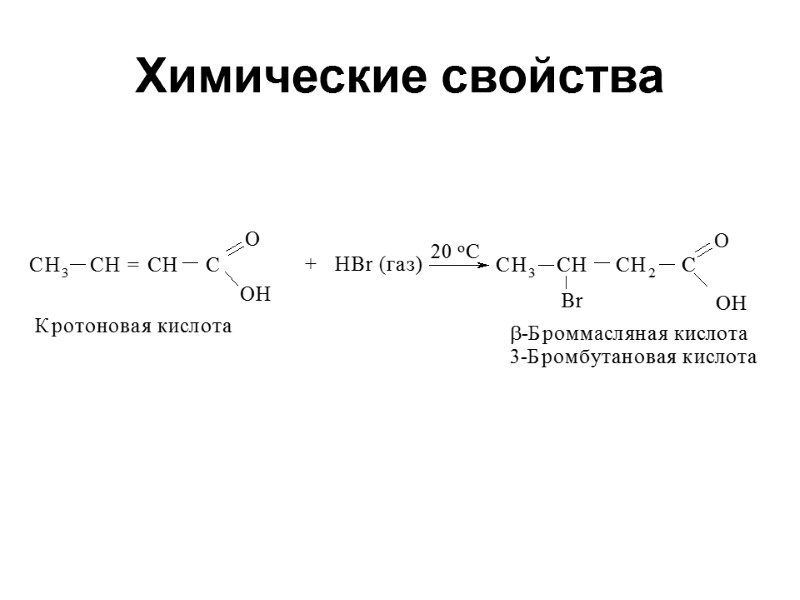
 Химические свойства
Химические свойства
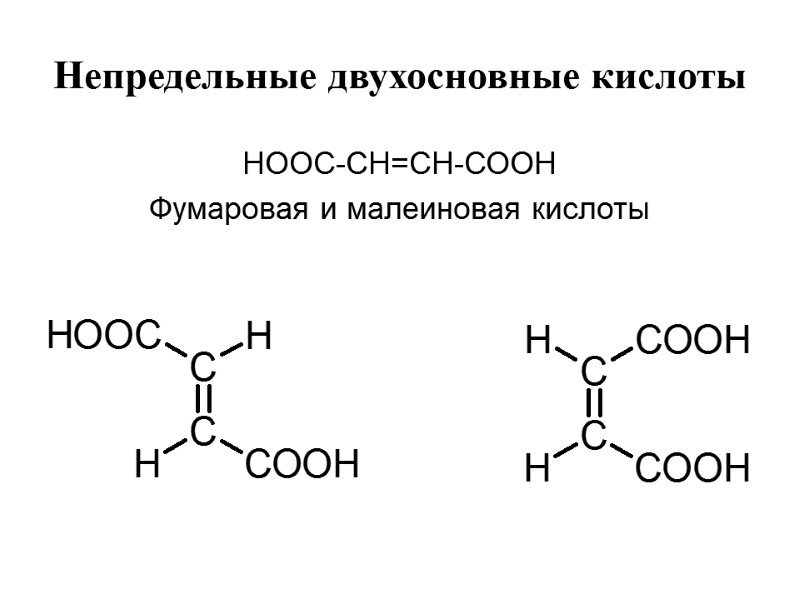
 Непредельные двухосновные кислоты НООС-СН=СН-СООН Фумаровая и малеиновая кислоты
Непредельные двухосновные кислоты НООС-СН=СН-СООН Фумаровая и малеиновая кислоты
 Гидроксикислоты или Оксикислоты
Гидроксикислоты или Оксикислоты
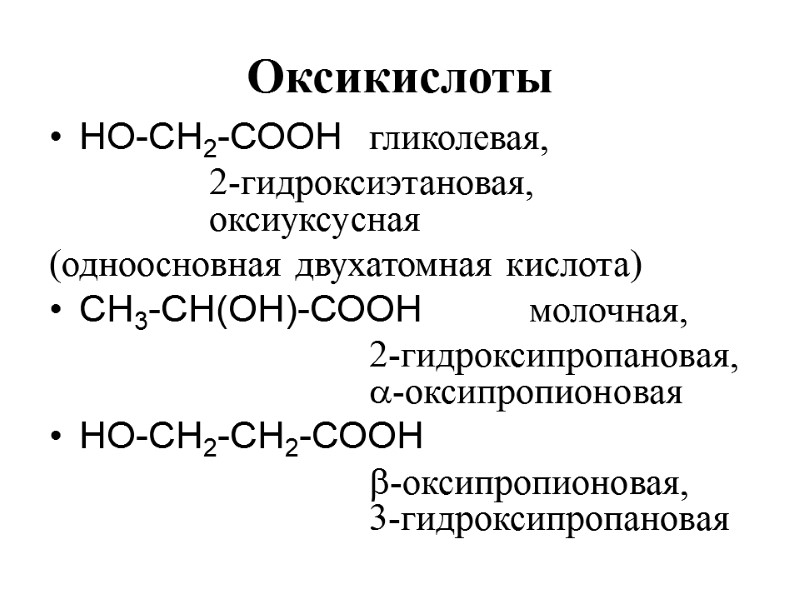
 Оксикислоты НО-СН2-СООН гликолевая, 2-гидроксиэтановая, оксиуксусная (одноосновная двухатомная кислота) СН3-СН(ОН)-СООН молочная, 2-гидроксипропановая, -оксипропионовая НО-СН2-СН2-СООН -оксипропионовая, 3-гидроксипропановая
Оксикислоты НО-СН2-СООН гликолевая, 2-гидроксиэтановая, оксиуксусная (одноосновная двухатомная кислота) СН3-СН(ОН)-СООН молочная, 2-гидроксипропановая, -оксипропионовая НО-СН2-СН2-СООН -оксипропионовая, 3-гидроксипропановая
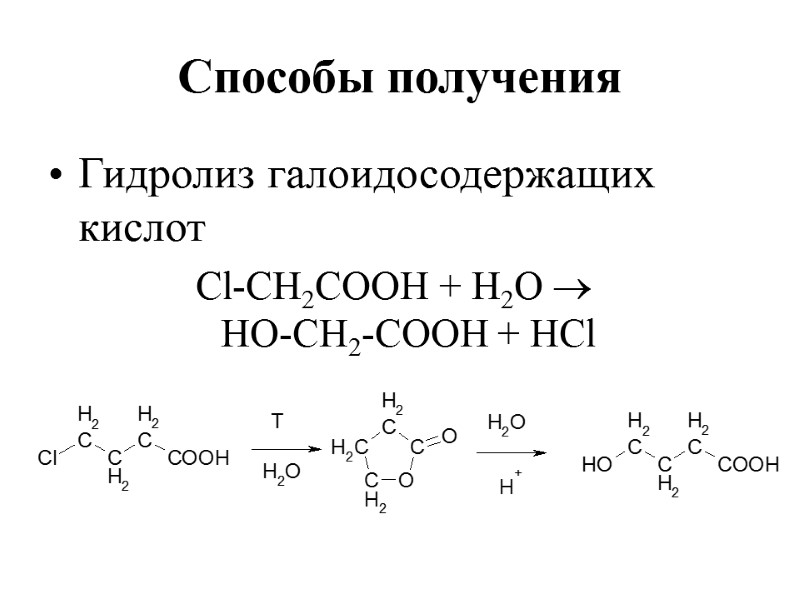
 Способы получения Гидролиз галоидосодержащих кислот Cl-СН2СООН + Н2О НО-СН2-СООН + HCl
Способы получения Гидролиз галоидосодержащих кислот Cl-СН2СООН + Н2О НО-СН2-СООН + HCl
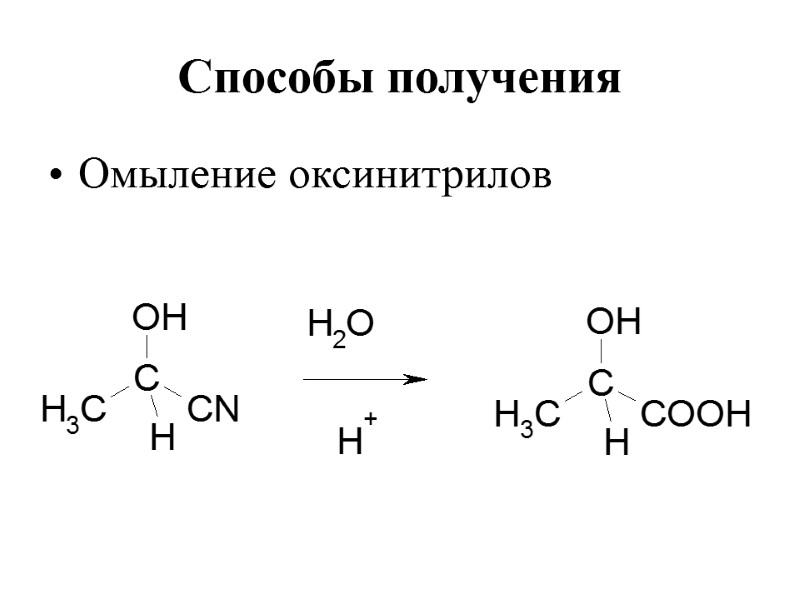
 Способы получения Омыление оксинитрилов
Способы получения Омыление оксинитрилов
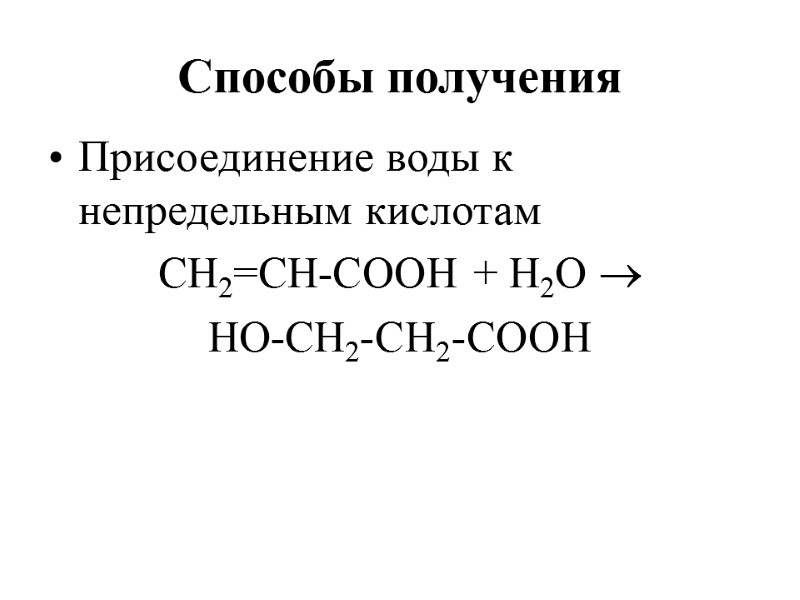
 Способы получения Присоединение воды к непредельным кислотам CН2=СН-СOOH + Н2О HO-СН2-СН2-СООН
Способы получения Присоединение воды к непредельным кислотам CН2=СН-СOOH + Н2О HO-СН2-СН2-СООН
 Химические свойства По карбоксильной группе По гидроксильной группе
Химические свойства По карбоксильной группе По гидроксильной группе
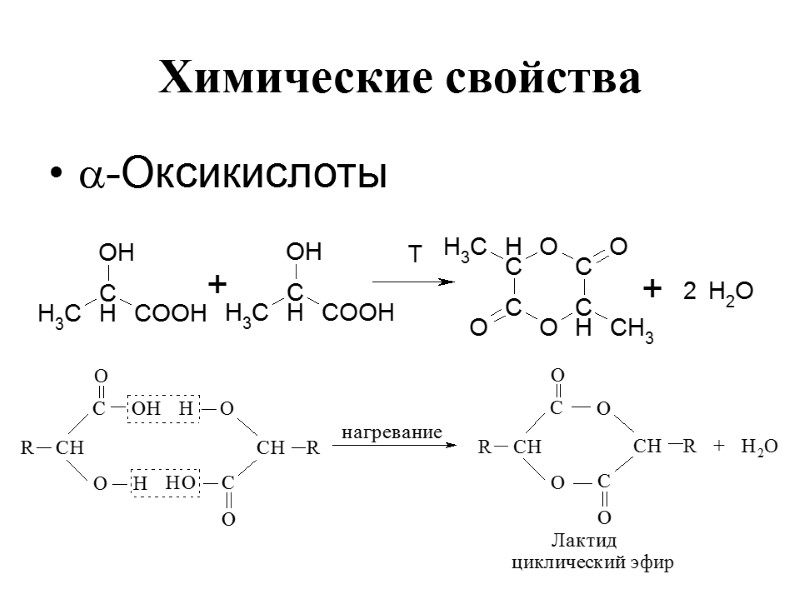
 Химические свойства -Оксикислоты
Химические свойства -Оксикислоты
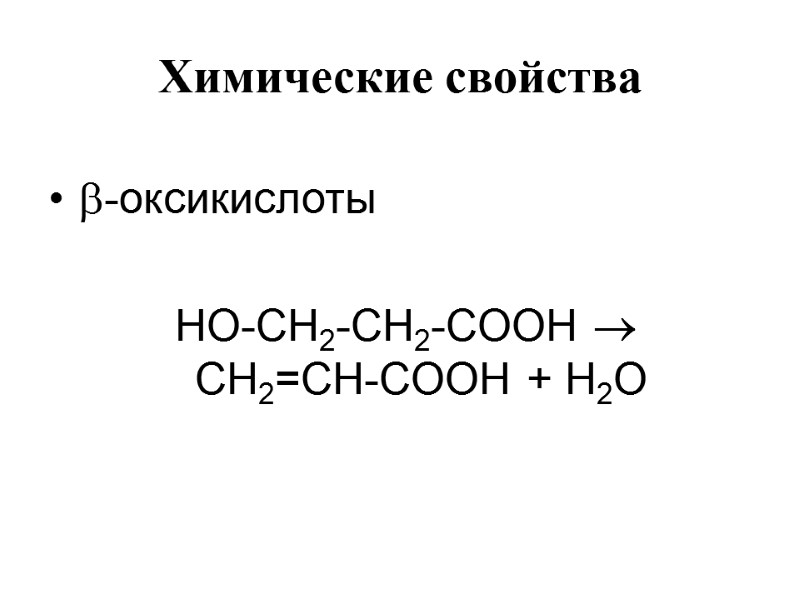
 Химические свойства -оксикислоты HO-СН2-СН2-СOОН СН2=СН-СOОН + H2O
Химические свойства -оксикислоты HO-СН2-СН2-СOОН СН2=СН-СOОН + H2O
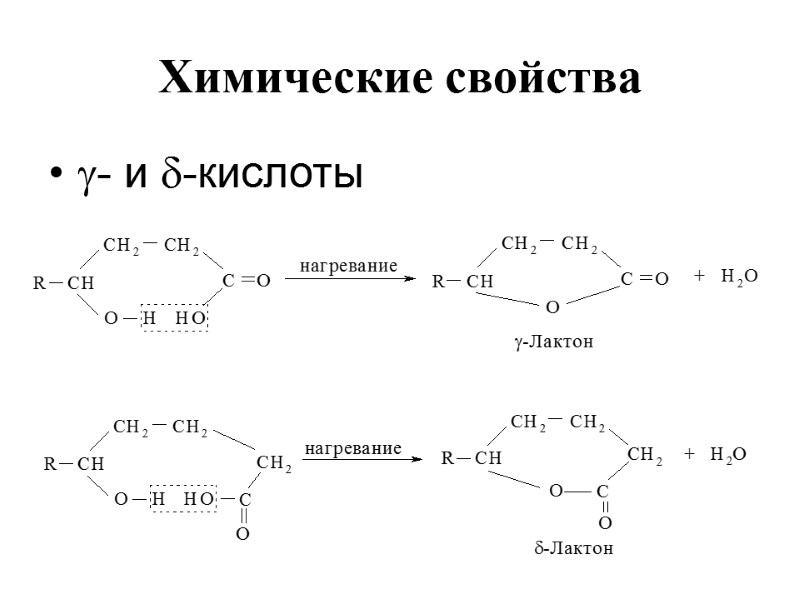
 Химические свойства - и -кислоты
Химические свойства - и -кислоты
 Химические свойства При кипячении с разбавленными кислотами -кислоты расщепляются СН3-СН(ОН)-СООН Н-СООН + СН3-СНО
Химические свойства При кипячении с разбавленными кислотами -кислоты расщепляются СН3-СН(ОН)-СООН Н-СООН + СН3-СНО
 Особый вид изомерии - стереоизомерия Стереоизомеры различаются пространственным расположением атомов или групп вокруг асимметрического центра и являются оптически активными соединениями - способны вращать плоскость поляризованного света
Особый вид изомерии - стереоизомерия Стереоизомеры различаются пространственным расположением атомов или групп вокруг асимметрического центра и являются оптически активными соединениями - способны вращать плоскость поляризованного света
 Конфигурации Конфигурация молекулы определяется расположением атомов в пространстве и не может быть изменена без нарушения связей между ними
Конфигурации Конфигурация молекулы определяется расположением атомов в пространстве и не может быть изменена без нарушения связей между ними
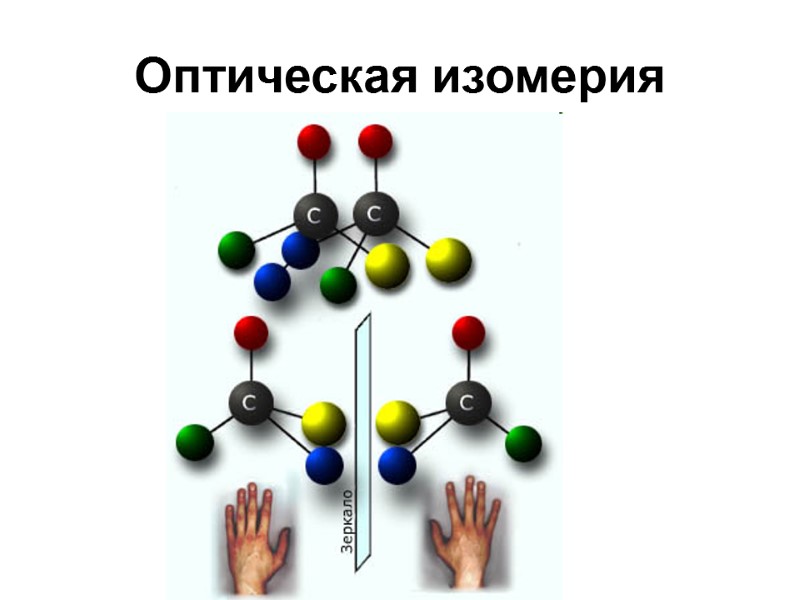
 Оптические изомеры Энантиомеры - соединения, являющиеся зеркальными отображениями друг друга (их называют хиральными) Например, бутанол-2 хирален, а этанол - ахирален, т.к. его молекула имеет плоскость симметрии
Оптические изомеры Энантиомеры - соединения, являющиеся зеркальными отображениями друг друга (их называют хиральными) Например, бутанол-2 хирален, а этанол - ахирален, т.к. его молекула имеет плоскость симметрии
 Оптическая изомерия
Оптическая изомерия
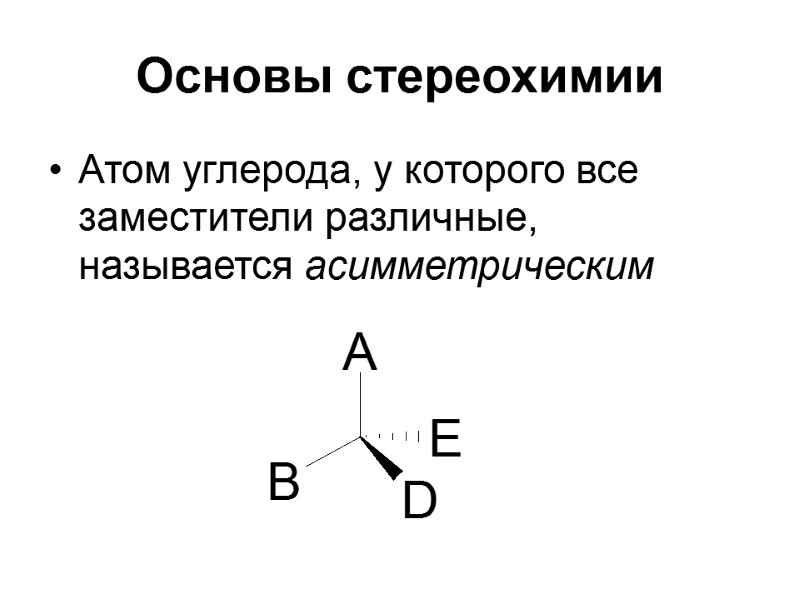
 Основы стереохимии Атом углерода, у которого все заместители различные, называется асимметрическим
Основы стереохимии Атом углерода, у которого все заместители различные, называется асимметрическим
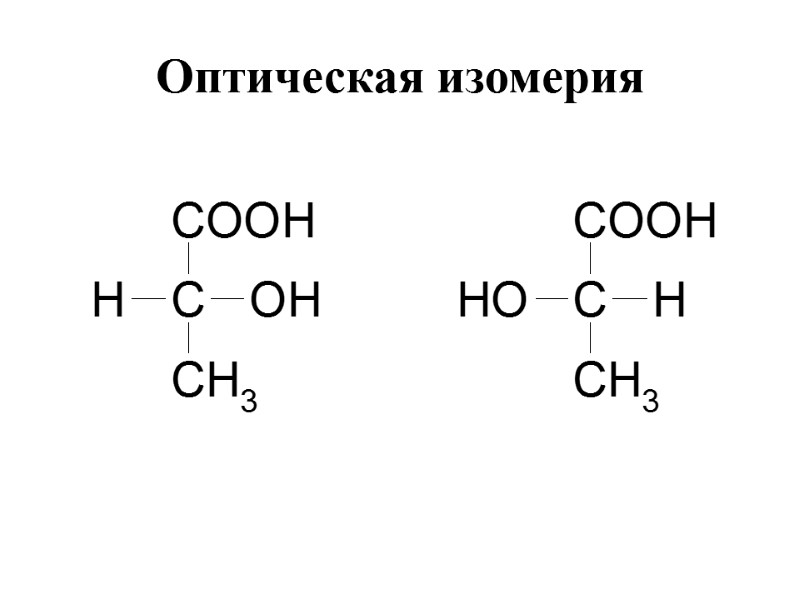
 Оптическая изомерия
Оптическая изомерия
 Оптическая изомерия Антипод - энантиомер Рацемическая смесь
Оптическая изомерия Антипод - энантиомер Рацемическая смесь
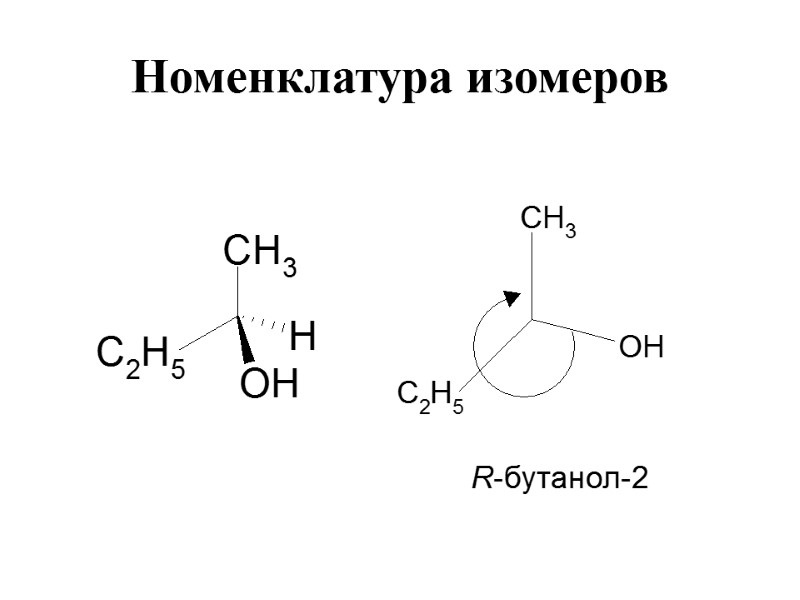
 Номенклатура изомеров Изомеры различают по знаку вращения плоскости поляризованного света: “+” - по часовой стрелке “-“ – против часовой стрелки правило Фишера – L или D-ряд (по глицериновому альдегиду)
Номенклатура изомеров Изомеры различают по знаку вращения плоскости поляризованного света: “+” - по часовой стрелке “-“ – против часовой стрелки правило Фишера – L или D-ряд (по глицериновому альдегиду)

 Номенклатура изомеров Правило последовательности старшинства атомов и групп Кана-Ингольда-Прелога: Старшинство определяется атомными номерами - чем больше, тем старше
Номенклатура изомеров Правило последовательности старшинства атомов и групп Кана-Ингольда-Прелога: Старшинство определяется атомными номерами - чем больше, тем старше
 Номенклатура изомеров
Номенклатура изомеров
 Диастереомеры Если оптические изомеры не являются энантиомерами (зеркальными отображениями друг друга), то они диастереомеры
Диастереомеры Если оптические изомеры не являются энантиомерами (зеркальными отображениями друг друга), то они диастереомеры
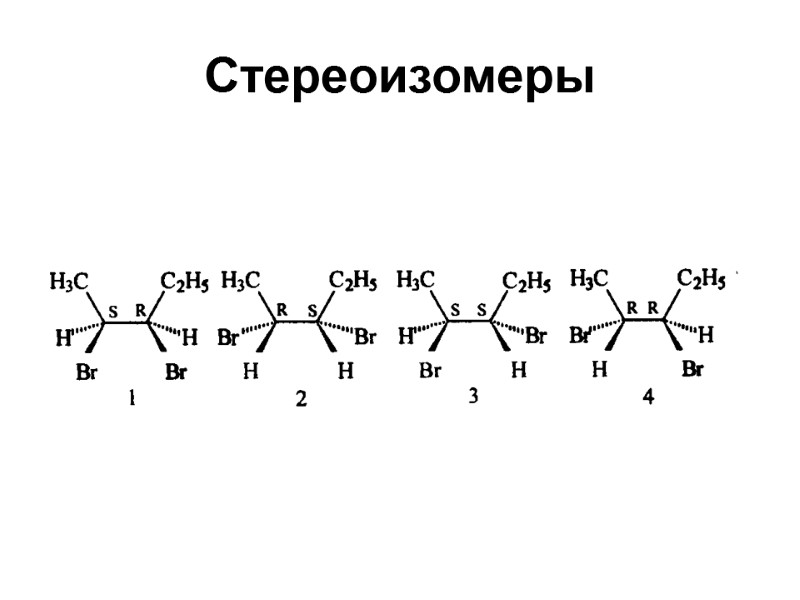
 Стереоизомеры
Стереоизомеры
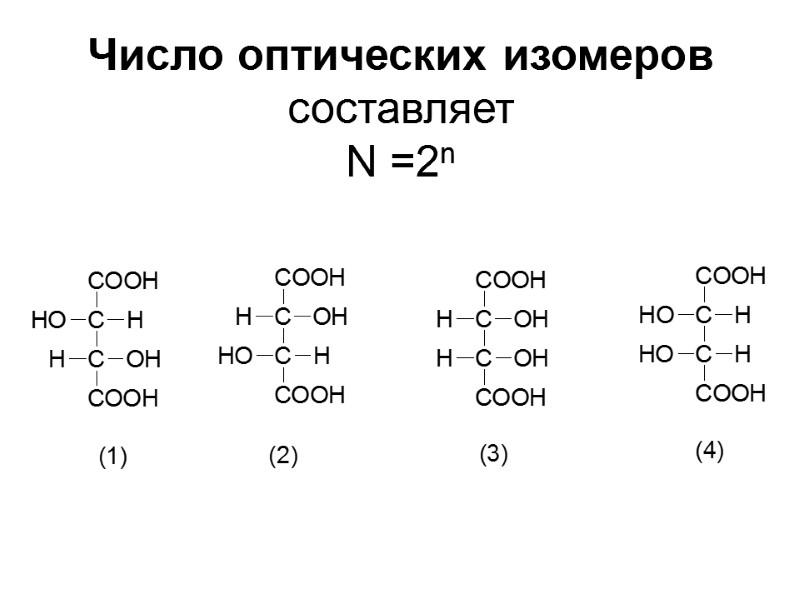
 Число оптических изомеров составляет N =2n
Число оптических изомеров составляет N =2n
 Диастереомеры В отличие от энантиомеров диастереомеры имеют различные физические (Тпл, Тк, n) и химические свойства Оптическое вращение у них может отличаться по направлению и по величине
Диастереомеры В отличие от энантиомеров диастереомеры имеют различные физические (Тпл, Тк, n) и химические свойства Оптическое вращение у них может отличаться по направлению и по величине
 Диастереомеры Различие в свойствах у диастереомеров используют для разделения рацемических смесей
Диастереомеры Различие в свойствах у диастереомеров используют для разделения рацемических смесей
 Разделение рацемических смесей A1* + A2* + B* A1*B* + A2*B* A1*B* A1* + B*
Разделение рацемических смесей A1* + A2* + B* A1*B* + A2*B* A1*B* A1* + B*
 Разделение рацемических смесей Кинетическое расщепление Основано на разной скорости реакции энантиомеров с хиральным агентом A1* + A2* + B* A1*B* + A2*
Разделение рацемических смесей Кинетическое расщепление Основано на разной скорости реакции энантиомеров с хиральным агентом A1* + A2* + B* A1*B* + A2*
 Разделение рацемических смесей Физический способ Разная форма кристаллов у изомеров (Пастер пинцетом разделял соли виноградной кислоты)
Разделение рацемических смесей Физический способ Разная форма кристаллов у изомеров (Пастер пинцетом разделял соли виноградной кислоты)
 Разделение рацемических смесей С помощью бактерий Они поедают один изомер, другой остается
Разделение рацемических смесей С помощью бактерий Они поедают один изомер, другой остается
 Асимметрический синтез Асимметрический синтез - получение оптически активных соединений из оптически недеятельных
Асимметрический синтез Асимметрический синтез - получение оптически активных соединений из оптически недеятельных
 Асимметрический синтез Частичный асимметрический синтез проводят с участием оптически активного реагента Абсолютный асимметрический синтез - без участия оптически активного реагента
Асимметрический синтез Частичный асимметрический синтез проводят с участием оптически активного реагента Абсолютный асимметрический синтез - без участия оптически активного реагента
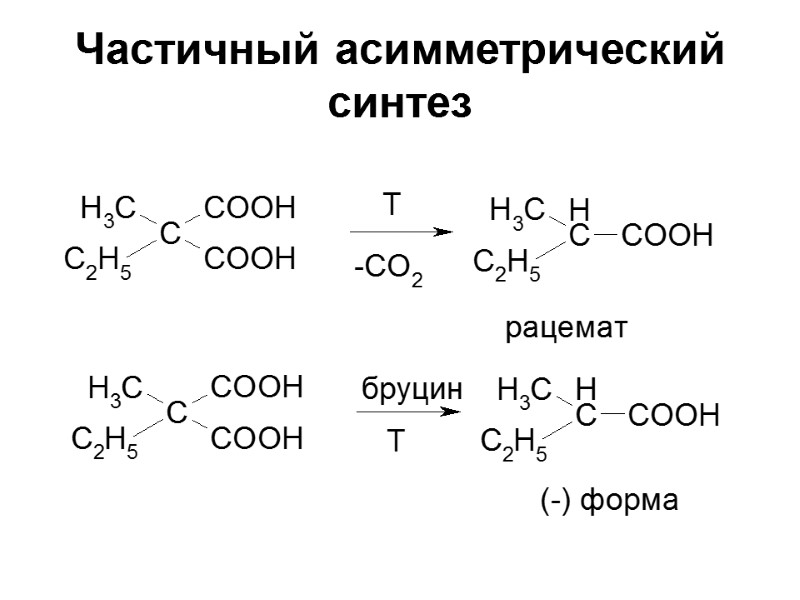
 Частичный асимметрический синтез
Частичный асимметрический синтез
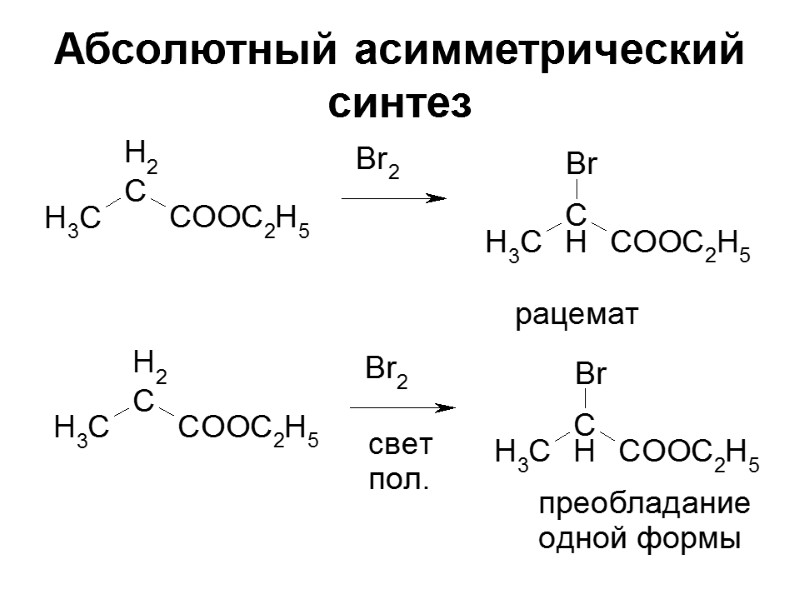
 Абсолютный асимметрический синтез
Абсолютный асимметрический синтез
 Контрольное задание № 4 Напишите схемы реакций: 1) Получения диметилового эфира щавелевой кислоты 2) Декарбоксилирования пропионовой кислоты 3) Получения гетероцепного полимера 4) «Серебряного зеркала» для бензальдегида 5) Хлорирования бутановой кислоты
Контрольное задание № 4 Напишите схемы реакций: 1) Получения диметилового эфира щавелевой кислоты 2) Декарбоксилирования пропионовой кислоты 3) Получения гетероцепного полимера 4) «Серебряного зеркала» для бензальдегида 5) Хлорирования бутановой кислоты

