Валидация аналитических методик ст.ppt
- Количество слайдов: 31
 Валидация аналитических методик
Валидация аналитических методик
 • Валидация – • Валидация -
• Валидация – • Валидация -
 Цель: • 1. минизация и количественная оценка возможности возникновения ошибок • 2. • 3. одним методом можно определять разные вещества • 4.
Цель: • 1. минизация и количественная оценка возможности возникновения ошибок • 2. • 3. одним методом можно определять разные вещества • 4.
 • 5. Один метод на разном оборудовании – различная точность (погрешности) • 6. Методика – метод + пробоподготовка – погрешности • 7. Персонал (случайные ошибки)
• 5. Один метод на разном оборудовании – различная точность (погрешности) • 6. Методика – метод + пробоподготовка – погрешности • 7. Персонал (случайные ошибки)
 Какие аналитические процедуры валидируются
Какие аналитические процедуры валидируются
 Валидация требуется для следующих групп методик • Идентификация веществ _________________ • Количественное определение _________________ • Контроль предельно допустимых значений содержания примесей • Определение количественного содержаний веществ в ЛП
Валидация требуется для следующих групп методик • Идентификация веществ _________________ • Количественное определение _________________ • Контроль предельно допустимых значений содержания примесей • Определение количественного содержаний веществ в ЛП
 Особенности
Особенности
 Основные документы, регламентирующие процесс валидации: • общая фармакопейная статья ОФС в USP, • ОФС РФ «Валидация фармакопейных методов» , • ГОСТ РФ «Точность (правильность и прецизионность) методов и результатов измерений» , • ГОСТ Р ИСО 5725 -1 -2002 (является полным аутентичным текстом международного стандарта ИСО 5725 -1 -1994), • документы IUPAK (Международный союз фундаментальной и прикладной химии) и ICН — международной конференции по гармонизации технических требований к регистрации лекарств для человека в странах ЕС, Японии и США.
Основные документы, регламентирующие процесс валидации: • общая фармакопейная статья ОФС в USP, • ОФС РФ «Валидация фармакопейных методов» , • ГОСТ РФ «Точность (правильность и прецизионность) методов и результатов измерений» , • ГОСТ Р ИСО 5725 -1 -2002 (является полным аутентичным текстом международного стандарта ИСО 5725 -1 -1994), • документы IUPAK (Международный союз фундаментальной и прикладной химии) и ICН — международной конференции по гармонизации технических требований к регистрации лекарств для человека в странах ЕС, Японии и США.
 Документы • ICH – международная организация по гармонизации • Q 2 A руководство по валидации аналитических методик • - термины и определения • Содержит основные этапы и принципы • Q 2 B Процедура проведения валидации аналитических методов • Рекомендации по отдельным этапам
Документы • ICH – международная организация по гармонизации • Q 2 A руководство по валидации аналитических методик • - термины и определения • Содержит основные этапы и принципы • Q 2 B Процедура проведения валидации аналитических методов • Рекомендации по отдельным этапам
 организация процесса валидации методики • 1. Разработать протокол валидации или рабочий процесс для валидации, в котором определить приложение, цель и область метода, эксплуатационные параметры и критерий приемки, валидационные эксперименты; 2. Определить необходимые рабочие характеристики оборудования, квалифицировать материалы, например, стандарты и реактивы; 3. Исполнить эксперименты предвалидации, корректировать параметры метода или критерии приемки в случае необходимости; 4. Исполнить полные внутренние и внешние эксперименты валидации; 5. Разработать СОП (стандартную операционную процедуру) для рутинного выполнения метода, определить критерии для ревалидации; 6. Определить тип и частоту испытаний пригодности метода; 7. Документировать эксперименты и результаты валидации в отчете.
организация процесса валидации методики • 1. Разработать протокол валидации или рабочий процесс для валидации, в котором определить приложение, цель и область метода, эксплуатационные параметры и критерий приемки, валидационные эксперименты; 2. Определить необходимые рабочие характеристики оборудования, квалифицировать материалы, например, стандарты и реактивы; 3. Исполнить эксперименты предвалидации, корректировать параметры метода или критерии приемки в случае необходимости; 4. Исполнить полные внутренние и внешние эксперименты валидации; 5. Разработать СОП (стандартную операционную процедуру) для рутинного выполнения метода, определить критерии для ревалидации; 6. Определить тип и частоту испытаний пригодности метода; 7. Документировать эксперименты и результаты валидации в отчете.
 Валидационные характеристики аналитических методов • • ___________(precision) __________ (accuracy) ; __________ (reproducibility) ; __________ (repeatability) __________ (robustness) ; __________ (linearity); ___________________ (range) _____________________ (specificity) ; • ___________ (limit of detection -LOD ) ; • ______________________ (limit of quantitation LOQ);
Валидационные характеристики аналитических методов • • ___________(precision) __________ (accuracy) ; __________ (reproducibility) ; __________ (repeatability) __________ (robustness) ; __________ (linearity); ___________________ (range) _____________________ (specificity) ; • ___________ (limit of detection -LOD ) ; • ______________________ (limit of quantitation LOQ);
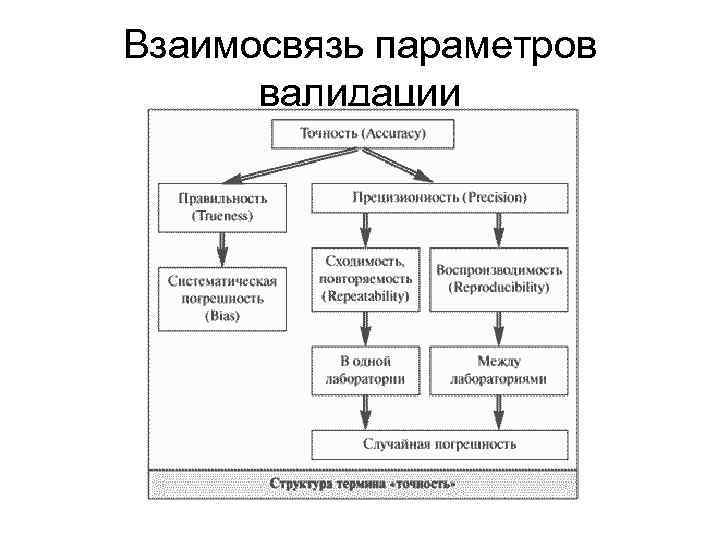 Взаимосвязь параметров валидации
Взаимосвязь параметров валидации
 Точность (рrecision) - Показатель правильности - значение систематической ошибки. Правильность оценивается на основе не менее 9 результатов определений по всему диапазону концентраций (_______________________________________) и не менее 6 определений при 100%
Точность (рrecision) - Показатель правильности - значение систематической ошибки. Правильность оценивается на основе не менее 9 результатов определений по всему диапазону концентраций (_______________________________________) и не менее 6 определений при 100%
 Правильность (аccuracy, тrueness) - • зависит только от случайных факторов • не связана с истинным значением измеряемой величины • выражается величиной стандартного отклонения (коэффициент вариации) • показатели прецизионности - повторяемость (сходимость) и воспроизводимость
Правильность (аccuracy, тrueness) - • зависит только от случайных факторов • не связана с истинным значением измеряемой величины • выражается величиной стандартного отклонения (коэффициент вариации) • показатели прецизионности - повторяемость (сходимость) и воспроизводимость
 повторяемость (repeatability) - степень согласованности результатов измерений (испытаний), полученных одним и тем же методом на идентичных объектах испытаний, в одной и той же лаборатории, одним и тем же испытателем, с использованием одного и того же оборудования, в пределах короткого промежутка времени. Повторяемость оценивается величиной относительного стандартного отклонения Sr , которая не должна превышать 2%.
повторяемость (repeatability) - степень согласованности результатов измерений (испытаний), полученных одним и тем же методом на идентичных объектах испытаний, в одной и той же лаборатории, одним и тем же испытателем, с использованием одного и того же оборудования, в пределах короткого промежутка времени. Повторяемость оценивается величиной относительного стандартного отклонения Sr , которая не должна превышать 2%.
 Воспроизводимость (reproducibility) - мера совпадения результатов измерений, полученных одним и тем же методом, на идентичных образцах, в разных лабораториях, разными испытателями, с использованием различного оборудования. Воспроизводимость: Оценивается величиной относительного стандартного отклонения Sr, которая не должна превышать 3%. Выражает точность результатов испытаний, проведенных в условиях различных лабораторий
Воспроизводимость (reproducibility) - мера совпадения результатов измерений, полученных одним и тем же методом, на идентичных образцах, в разных лабораториях, разными испытателями, с использованием различного оборудования. Воспроизводимость: Оценивается величиной относительного стандартного отклонения Sr, которая не должна превышать 3%. Выражает точность результатов испытаний, проведенных в условиях различных лабораторий
 Устойчивость (robustness) - (изменение состава, скорости потока или р. Н мобильной фазы в методах ВЭЖХ, температуры в ГХ, длины волны в УФВ- методах, р. Н среды и др. ) Изучаются в ходе робастности: • Параметры методики • Стабильность растворов • ВЭЖХ – смена колонки
Устойчивость (robustness) - (изменение состава, скорости потока или р. Н мобильной фазы в методах ВЭЖХ, температуры в ГХ, длины волны в УФВ- методах, р. Н среды и др. ) Изучаются в ходе робастности: • Параметры методики • Стабильность растворов • ВЭЖХ – смена колонки
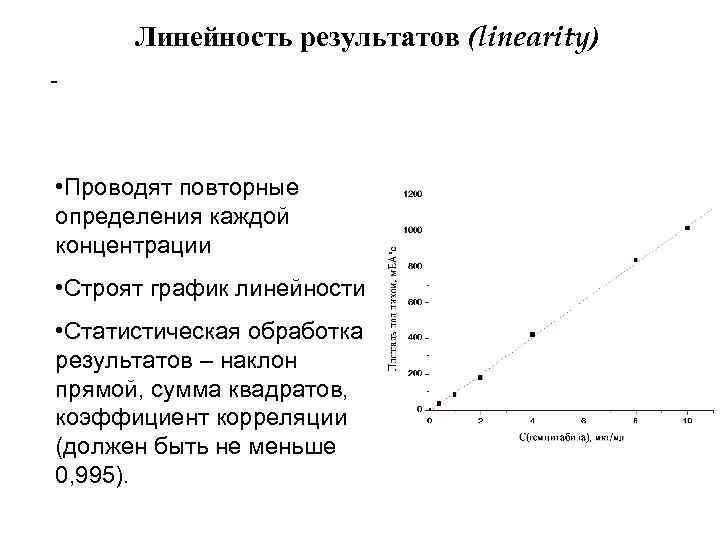 Линейность результатов (linearity) - • Проводят повторные определения каждой концентрации • Строят график линейности • Статистическая обработка результатов – наклон прямой, сумма квадратов, коэффициент корреляции (должен быть не меньше 0, 995).
Линейность результатов (linearity) - • Проводят повторные определения каждой концентрации • Строят график линейности • Статистическая обработка результатов – наклон прямой, сумма квадратов, коэффициент корреляции (должен быть не меньше 0, 995).
 Специфичность, селективность (specifity, selectivity) – Определяется: способностью достоверно определять лекарственное вещество в присутствии примесных соединений, продуктов деградации и вспомогательных веществ.
Специфичность, селективность (specifity, selectivity) – Определяется: способностью достоверно определять лекарственное вещество в присутствии примесных соединений, продуктов деградации и вспомогательных веществ.
 Предел обнаружения (limit of detection) - Предел обнаружения обычно выражается как концентрация анализируемого вещества в образце, например, в % или долях на миллион (ppm), миллиард (ppb). Соотношение сигнал/шум (для методов с базовыми шумами)
Предел обнаружения (limit of detection) - Предел обнаружения обычно выражается как концентрация анализируемого вещества в образце, например, в % или долях на миллион (ppm), миллиард (ppb). Соотношение сигнал/шум (для методов с базовыми шумами)
 Пригодность системы (system suitability) • Параметры пригодности системы обеспечивают соблюдение валидности метода в тех случаях, когда в процессе анализа возможны некоторые внутрилабораторные изменения условий анализа. • Тесты пригодности системы зависят от типа метода, но особенно важны для хроматографических методов.
Пригодность системы (system suitability) • Параметры пригодности системы обеспечивают соблюдение валидности метода в тех случаях, когда в процессе анализа возможны некоторые внутрилабораторные изменения условий анализа. • Тесты пригодности системы зависят от типа метода, но особенно важны для хроматографических методов.
 Аналитические методы • 1. Селективные • 2. Неселективные методы
Аналитические методы • 1. Селективные • 2. Неселективные методы
 Категория / типы методик • Категории: • Трансфер (проверка пригодности в условиях конкретной лаборатории) • Методика, разработанная впервые • …. • Типы: • 1. фармакопейные • 2. нефармакопейные (производидитель) • Испытуемые образцы: • Субстанция • ЛП
Категория / типы методик • Категории: • Трансфер (проверка пригодности в условиях конкретной лаборатории) • Методика, разработанная впервые • …. • Типы: • 1. фармакопейные • 2. нефармакопейные (производидитель) • Испытуемые образцы: • Субстанция • ЛП
 План валидации • • - первый этап Содержание: Лист утверждения Состав валидационной группы Описание аналитического метода Условия эксперимента Порядок проведения валидации и критерии приемлемости • График проведения • Бланки-формы
План валидации • • - первый этап Содержание: Лист утверждения Состав валидационной группы Описание аналитического метода Условия эксперимента Порядок проведения валидации и критерии приемлемости • График проведения • Бланки-формы
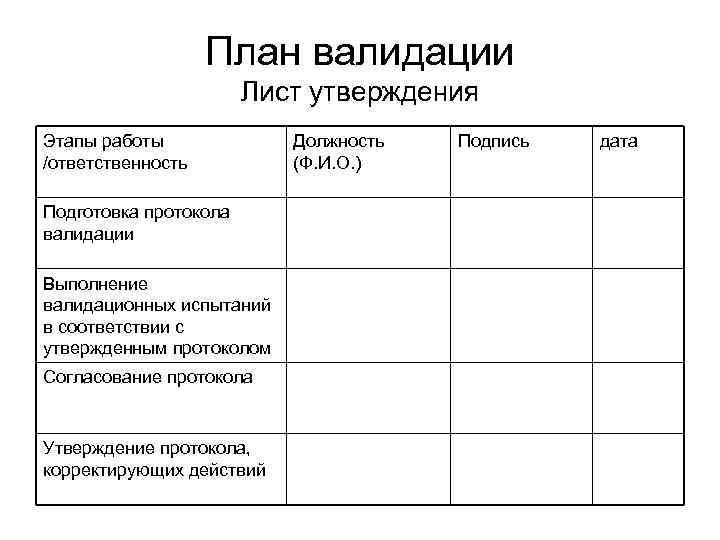 План валидации Лист утверждения Этапы работы /ответственность Подготовка протокола валидации Выполнение валидационных испытаний в соответствии с утвержденным протоколом Согласование протокола Утверждение протокола, корректирующих действий Должность (Ф. И. О. ) Подпись дата
План валидации Лист утверждения Этапы работы /ответственность Подготовка протокола валидации Выполнение валидационных испытаний в соответствии с утвержденным протоколом Согласование протокола Утверждение протокола, корректирующих действий Должность (Ф. И. О. ) Подпись дата
 Порядок тестирования валидационных характеристик • • Специфичность Точность Диапазон Пределы Правильность Линейность Робастность
Порядок тестирования валидационных характеристик • • Специфичность Точность Диапазон Пределы Правильность Линейность Робастность
 Использование параметров валидации для различных типов АМ Параметр валидации идентификация Определение примесей количественно Специфичность + Правильность пределы + + Определение содержания + + + Повторяемость + + Промежуточная точность + + LOD + LOQ + Линейность + + Диапазон + + Точность устойчивость + + +
Использование параметров валидации для различных типов АМ Параметр валидации идентификация Определение примесей количественно Специфичность + Правильность пределы + + Определение содержания + + + Повторяемость + + Промежуточная точность + + LOD + LOQ + Линейность + + Диапазон + + Точность устойчивость + + +
 Валидационные документы
Валидационные документы
 Валидация спектрофотометрических методик • При проведении валидации необходимо доказать, что методика позволяет контролировать качество данного ЛС на оборудовании и в условиях данной лаборатории, а также в любой другой лаборатории на любом другом оборудовании, при условии, что оно отвечает требованиям Фармакопеи и/или дополнительным требованиям. • Особенностью валидации многоволнового СФанализа - прогноз погрешности должен обязательно предшествовать экспериментальной валидации — бессмысленно экспериментально проверять методику, которая заранее дает неприемлемо высокую погрешность.
Валидация спектрофотометрических методик • При проведении валидации необходимо доказать, что методика позволяет контролировать качество данного ЛС на оборудовании и в условиях данной лаборатории, а также в любой другой лаборатории на любом другом оборудовании, при условии, что оно отвечает требованиям Фармакопеи и/или дополнительным требованиям. • Особенностью валидации многоволнового СФанализа - прогноз погрешности должен обязательно предшествовать экспериментальной валидации — бессмысленно экспериментально проверять методику, которая заранее дает неприемлемо высокую погрешность.
 • В отчет о валидации методики обычно рекомендуется включать: • — цель и контекст метода (область применения, процедура); — тип анализируемых веществ и матрицы; — детальную информацию о реактивах, эталонах и приготовлении контрольных (стандартных) образцов; — процедуры для проверок качества стандартов и используемых реактивов; — соображения безопасности; — параметры метода; — критические параметры, установленные при испытании прочности; — перечень оборудования и его функциональных и эксплуатационных характеристик, например (для хроматографии), размеры ячейки, шум базовой линии, диапазон температур колонки;
• В отчет о валидации методики обычно рекомендуется включать: • — цель и контекст метода (область применения, процедура); — тип анализируемых веществ и матрицы; — детальную информацию о реактивах, эталонах и приготовлении контрольных (стандартных) образцов; — процедуры для проверок качества стандартов и используемых реактивов; — соображения безопасности; — параметры метода; — критические параметры, установленные при испытании прочности; — перечень оборудования и его функциональных и эксплуатационных характеристик, например (для хроматографии), размеры ячейки, шум базовой линии, диапазон температур колонки;
 • — детальные условия проведения экспериментов, включая подготовку пробы; — процедуры вычислений и статистической обработки результатов; — процедуры для контроля качества в процессе эксплуатации методики (например, испытания пригодности системы); — графическую информацию, например хроматограммы, спектры и калибровочные кривые; — пределы эксплуатационных данных для принятия метода; — ожидаемую неопределенность результатов измерения; — критерии для ревалидации; — специалистов, которые разрабатывали и первоначально валидировали метод; — резюме и заключения.
• — детальные условия проведения экспериментов, включая подготовку пробы; — процедуры вычислений и статистической обработки результатов; — процедуры для контроля качества в процессе эксплуатации методики (например, испытания пригодности системы); — графическую информацию, например хроматограммы, спектры и калибровочные кривые; — пределы эксплуатационных данных для принятия метода; — ожидаемую неопределенность результатов измерения; — критерии для ревалидации; — специалистов, которые разрабатывали и первоначально валидировали метод; — резюме и заключения.


