 Валентность. Валентные возможности и размеры атомов химических элементов.
Валентность. Валентные возможности и размеры атомов химических элементов.
 Что такое валентность? «Валентность химического элемента – способность его атомов соединяться с другими атомами в определенных соотношениях» . «Валентность – способность атомов одного элемента присоединять определенное количество атомов другого элемента» . «Валентность – свойство атомов, вступая в химические соединения, отдавать или принимать определенное количество электронов (электровалентность) или объединять электроны для образования общих для двух атомов электронных пар (ковалентность)» .
Что такое валентность? «Валентность химического элемента – способность его атомов соединяться с другими атомами в определенных соотношениях» . «Валентность – способность атомов одного элемента присоединять определенное количество атомов другого элемента» . «Валентность – свойство атомов, вступая в химические соединения, отдавать или принимать определенное количество электронов (электровалентность) или объединять электроны для образования общих для двух атомов электронных пар (ковалентность)» .
 Валентность и валентные возможности – важные характеристики химического элемента. Они определяются структурой атомов и периодически изменяются с увеличением зарядов ядер. Что, по-вашему, означает понятие «валентная возможность» ?
Валентность и валентные возможности – важные характеристики химического элемента. Они определяются структурой атомов и периодически изменяются с увеличением зарядов ядер. Что, по-вашему, означает понятие «валентная возможность» ?
 «Возможность – средство, условие, необходимое для осуществления чего -нибудь» ; «возможный – такой, который может произойти, осуществимый, допустимый, дозволительный, мыслимый» . толковый словарь С. И. Ожегова
«Возможность – средство, условие, необходимое для осуществления чего -нибудь» ; «возможный – такой, который может произойти, осуществимый, допустимый, дозволительный, мыслимый» . толковый словарь С. И. Ожегова
 Валентные возможности атомов – это допустимые валентности элемента, весь спектр их значений в различных соединениях.
Валентные возможности атомов – это допустимые валентности элемента, весь спектр их значений в различных соединениях.
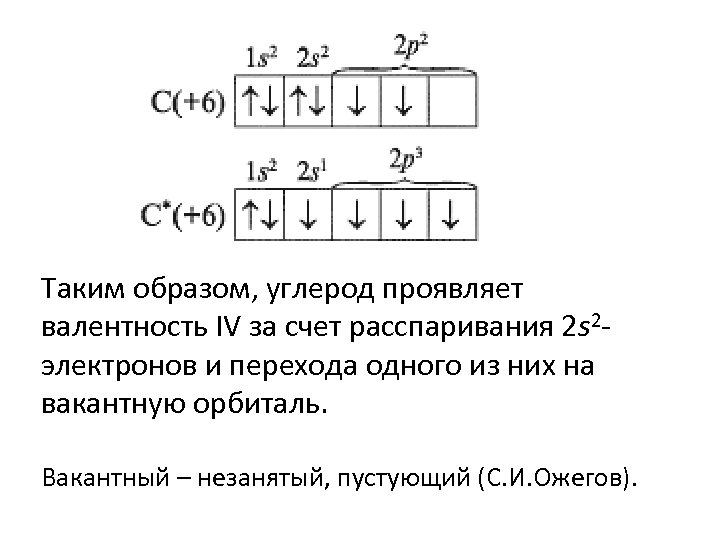 Таким образом, углерод проявляет валентность IV за счет расспаривания 2 s 2 электронов и перехода одного из них на вакантную орбиталь. Вакантный – незанятый, пустующий (С. И. Ожегов).
Таким образом, углерод проявляет валентность IV за счет расспаривания 2 s 2 электронов и перехода одного из них на вакантную орбиталь. Вакантный – незанятый, пустующий (С. И. Ожегов).
 Почему валентность С – II и IV, а Н – I, Нe – 0, Be – II, B – III, P – V? Сопоставьте электронографические формулы элементов и установите причину разной валентности
Почему валентность С – II и IV, а Н – I, Нe – 0, Be – II, B – III, P – V? Сопоставьте электронографические формулы элементов и установите причину разной валентности
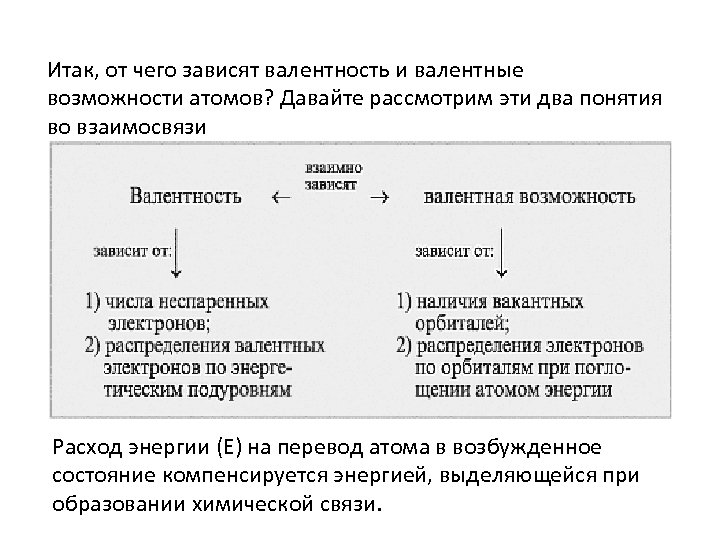 Итак, от чего зависят валентность и валентные возможности атомов? Давайте рассмотрим эти два понятия во взаимосвязи Расход энергии (Е) на перевод атома в возбужденное состояние компенсируется энергией, выделяющейся при образовании химической связи.
Итак, от чего зависят валентность и валентные возможности атомов? Давайте рассмотрим эти два понятия во взаимосвязи Расход энергии (Е) на перевод атома в возбужденное состояние компенсируется энергией, выделяющейся при образовании химической связи.
 В чем отличие атома в основном (стационарном) состоянии от атома в возбужденном состоянии? Вывод Валентные возможности атомов химических элементов определяются: 1) числом неспаренных электронов (одноэлектронных орбиталей); 2) наличием свободных орбиталей; 3) наличием неподеленных пар электронов.
В чем отличие атома в основном (стационарном) состоянии от атома в возбужденном состоянии? Вывод Валентные возможности атомов химических элементов определяются: 1) числом неспаренных электронов (одноэлектронных орбиталей); 2) наличием свободных орбиталей; 3) наличием неподеленных пар электронов.
 Могут ли быть следующие валентности у элементов: Li – III, O – IV, Ne – II? Поясните свой ответ, используя электронные и электронографические формулы этих элементов. Нет, т. к. в этом случае затраты энергии на перемещение электрона (1 s 2 p или 2 p 3 s) настолько велики, что не могут быть компенсированы энергией, выделяющейся при образовании химической связи.
Могут ли быть следующие валентности у элементов: Li – III, O – IV, Ne – II? Поясните свой ответ, используя электронные и электронографические формулы этих элементов. Нет, т. к. в этом случае затраты энергии на перемещение электрона (1 s 2 p или 2 p 3 s) настолько велики, что не могут быть компенсированы энергией, выделяющейся при образовании химической связи.
 Есть еще один вид валентной возможности атомов – это наличие неподеленных электронных пар (образование ковалентной связи по донорноакцепторному механизму): Атом кислорода при образовании иона гидроксония предоставляет общую электронную пару, т. е. является донором, а ион водорода акцептором.
Есть еще один вид валентной возможности атомов – это наличие неподеленных электронных пар (образование ковалентной связи по донорноакцепторному механизму): Атом кислорода при образовании иона гидроксония предоставляет общую электронную пару, т. е. является донором, а ион водорода акцептором.
 Задание на дом Параграф 5 Вопросы 12, 13, 16 (у), 14(п), стр. 22 Задачи 3, 4, стр. 23
Задание на дом Параграф 5 Вопросы 12, 13, 16 (у), 14(п), стр. 22 Задачи 3, 4, стр. 23