 Валентность и степень окисления. Химическая связь 11. 02. 2018
Валентность и степень окисления. Химическая связь 11. 02. 2018
 Важно! • № группы = количеству электронов на внешнем уровне • № периода = количеству электронных уровней от количества электронов на внешнем уровне зависят валентность и степень окисления
Важно! • № группы = количеству электронов на внешнем уровне • № периода = количеству электронных уровней от количества электронов на внешнем уровне зависят валентность и степень окисления
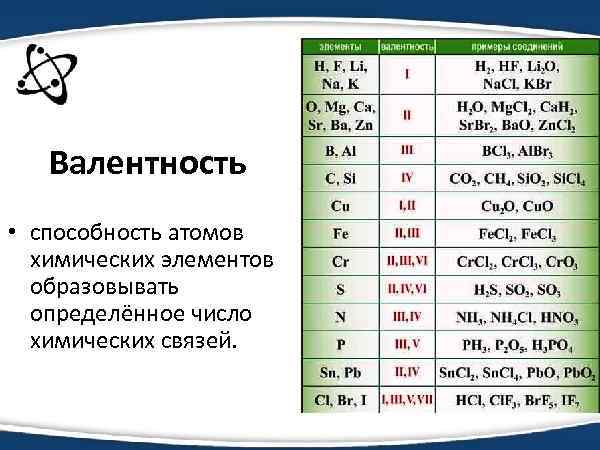 Валентность • способность атомов химических элементов образовывать определённое число химических связей.
Валентность • способность атомов химических элементов образовывать определённое число химических связей.
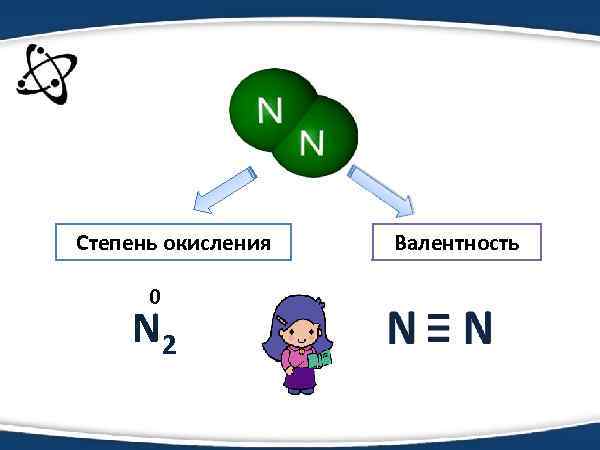 Степень окисления 0 N 2 Валентность
Степень окисления 0 N 2 Валентность
 Электроотрицательность это способность атомов притягивать электроны при связывании с другими атомами. Окислитель – забирает электроны ( «окислитель– грабитель» )
Электроотрицательность это способность атомов притягивать электроны при связывании с другими атомами. Окислитель – забирает электроны ( «окислитель– грабитель» )
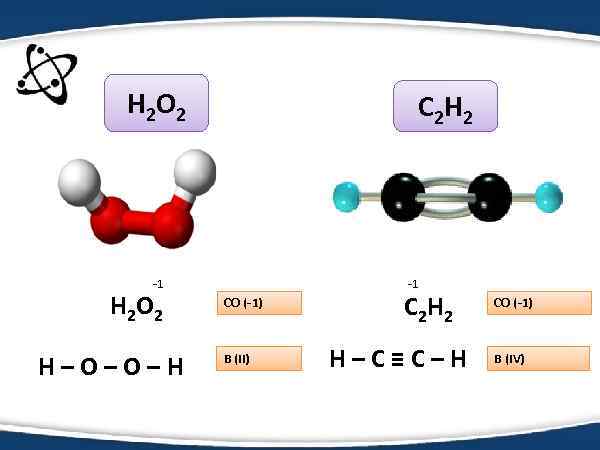 Н 2 О 2 C 2 H 2 -1 Н 2 О 2 Н–О–О–Н -1 СО (-1) В (II) C 2 H 2 Н–С≡С–Н СО (-1) В (IV)
Н 2 О 2 C 2 H 2 -1 Н 2 О 2 Н–О–О–Н -1 СО (-1) В (II) C 2 H 2 Н–С≡С–Н СО (-1) В (IV)
 Степень окисления – это условный заряд атомов химического элемента в соединении, если предположить, что оно состоит только из ионов. Ø Степень окисления может быть положительной, отрицательной, нулевой Ø Степень окисления простых веществ равна 0: N 2, H 2, S 8, Cu, O 3 и др. Ø F всегда имеет степень окисления -1 -1 Na. F → F Ø О всегда имеет степень окисления -2, кроме соединений со фтором Сa. O → (-2), OF 2 → (+2)
Степень окисления – это условный заряд атомов химического элемента в соединении, если предположить, что оно состоит только из ионов. Ø Степень окисления может быть положительной, отрицательной, нулевой Ø Степень окисления простых веществ равна 0: N 2, H 2, S 8, Cu, O 3 и др. Ø F всегда имеет степень окисления -1 -1 Na. F → F Ø О всегда имеет степень окисления -2, кроме соединений со фтором Сa. O → (-2), OF 2 → (+2)
 Ø Степень окисления Н всегда (+1), исключения – соединения с металлами, где степень окисления Н (-1): Ca. H 2, KH, Li. H и др. Ø У металлов степень окисления только положительная. У металлов А групп она совпадает с валентностью Ø Минимальная степень окисления = № группы – 8, у N (3) Ø Максимальная степень окисления равна номеру группы, например у N (+5)
Ø Степень окисления Н всегда (+1), исключения – соединения с металлами, где степень окисления Н (-1): Ca. H 2, KH, Li. H и др. Ø У металлов степень окисления только положительная. У металлов А групп она совпадает с валентностью Ø Минимальная степень окисления = № группы – 8, у N (3) Ø Максимальная степень окисления равна номеру группы, например у N (+5)
 • Образуется между ионами – заряженными частицами; • Образуется между элементами, Электроотрицательность которых сильно отличается друг от друга; • Существует в солях, основаниях и оксидах металлов: Na. Cl, KOH, Na 2 O • Металлы отдают электроны с последнего слоя. Неметаллы принимают недостающие электроны.
• Образуется между ионами – заряженными частицами; • Образуется между элементами, Электроотрицательность которых сильно отличается друг от друга; • Существует в солях, основаниях и оксидах металлов: Na. Cl, KOH, Na 2 O • Металлы отдают электроны с последнего слоя. Неметаллы принимают недостающие электроны.
 Ковалентная неполярная связь • Образуется между элементами неметаллами с одинаковой Электроотрицательность за счет объединения неспаренных электронных пар в общие пары: Н-Н; О=О. Она образуется в простых веществах неметаллах, а также в веществе фосфин РН 3
Ковалентная неполярная связь • Образуется между элементами неметаллами с одинаковой Электроотрицательность за счет объединения неспаренных электронных пар в общие пары: Н-Н; О=О. Она образуется в простых веществах неметаллах, а также в веществе фосфин РН 3
 Ковалентная полярная связь • Образуется между элементами неметаллами, Электроотрицательность которых незначительно отличается друг о друга. Между неметаллами также образуются общие электронные пары. Но они будут смещаться в сторону боле сильного неметалла: Н→: Cl; H→O←H
Ковалентная полярная связь • Образуется между элементами неметаллами, Электроотрицательность которых незначительно отличается друг о друга. Между неметаллами также образуются общие электронные пары. Но они будут смещаться в сторону боле сильного неметалла: Н→: Cl; H→O←H
 • Образуется между атомами и ионами металлов. Существует в простых веществах металлах, а также в их сплавах. Занимает промежуточное положение между ионной и ковалентной связями: Ме 0 – n e- ↔ Ме+n
• Образуется между атомами и ионами металлов. Существует в простых веществах металлах, а также в их сплавах. Занимает промежуточное положение между ионной и ковалентной связями: Ме 0 – n e- ↔ Ме+n
 • Образуется между водородом и более электроотрицательным элементом. Чаще всего это кислород, азот, сера. Связь непрочная, но так как она образуется между многими молекулами, то она как бы «сшивает» их друг с другом: Н-О …. Н-О l l Н Н
• Образуется между водородом и более электроотрицательным элементом. Чаще всего это кислород, азот, сера. Связь непрочная, но так как она образуется между многими молекулами, то она как бы «сшивает» их друг с другом: Н-О …. Н-О l l Н Н
 Домашнее задание • Выучить §
Домашнее задание • Выучить §