Вакуолярная система клетки.ppt
- Количество слайдов: 75

Вакуолярная система клетки. Рибосомы. Аппарат внутриклеточного переваривания. Цитоскелет

Диктиосома– стопка уплощенных цистерн (стек массивы) с отшнуровывющимися везикулами. Для АГ в отличие от других внутриклеточных органелл характерна полярность его структуры. Рассматривается всего 5 функционально различных компартментов АГ: n 1. переходный ЭР (t. ER) exit sites (сайт выхода) n 2. промежуточные везикуло-тубулярные структуры (VTC или ERGIC — ER-Golgi intermediate compartment), цис сеть, n 3. Цис - цистерна n 4. срединные (medial) стопки цистерны, n 5. транс (trans)- тубулярная сеть, везикулотубулярные структуры (VTC)
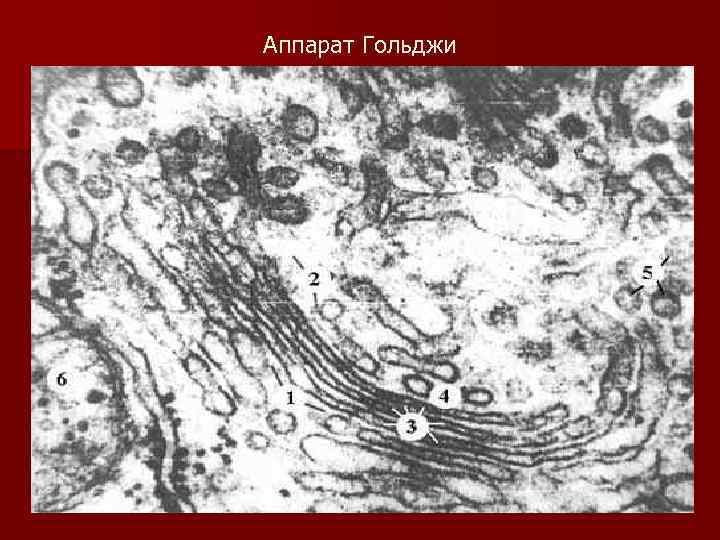
Аппарат Гольджи

В диктиосоме АГ от 3 до 8 цистерн, располагающихся параллельно другу на расстоянии 15— 20 им. 1. переходный ЭР (t. ER) exit sites (сайт выхода) К цис-поверхности АГ прилегает канал ER на мембране которого находятся особые участки, так называемые сайты выхода (exit sites), и многочисленные мелкие почки. 2. промежуточные везикуло-тубулярные компоненты (VTC) цис - стороны VTC является промежуточным элементом между цистернами АГ и ER. Он представлен мелкими пузырьками с окаймлением COPI и СОРII, тубулами, которые, возникают за счет слияния пузырьков, потерявших свое окаймление из белков СОРII и являются мембранными переносчиками карго из ER в

Каждый компартмент АГ обладает своим собственным набором ферментов, являющихся интегральными белками мембран АГ. n Все белки резидентные. n Белков АГ – ферменты процессинга. n Во всех компартментах АГ выявлен ряд рецепторов к резидентным белкам, способствующих их опосредованному рецептором возврату в исходные мембраны. n


К вогнутой транс-поверхности АГ примыкают его производные: n секреторные гладкие пузырьки, n окаймленные кларином пузырьки, n лизосомы, n конденсированные вакуоли (или незрелые секреторные гранулы) n зрелые секреторные гранулы.
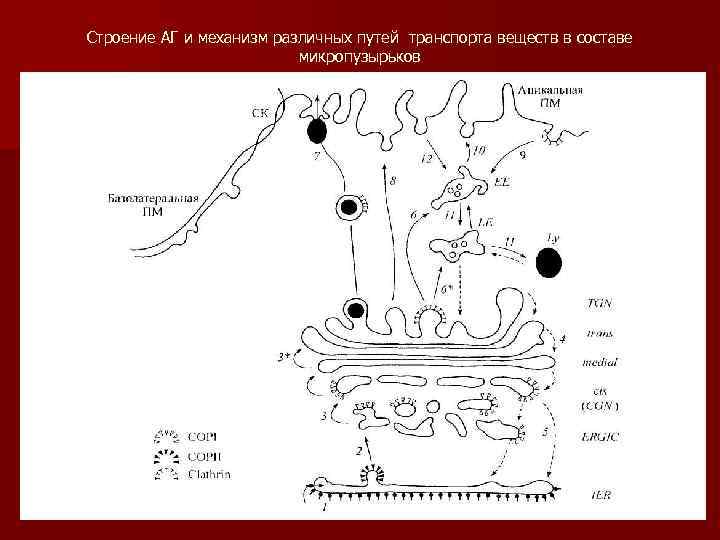
Строение АГ и механизм различных путей транспорта веществ в составе микропузырьков
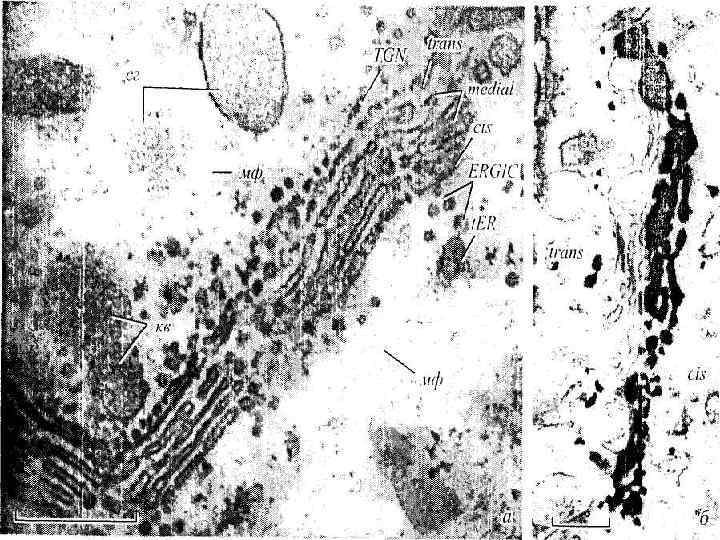

Важную роль в поддержании пространственной организации АГ и экзо-, и эндоцитозного путей в клетке отводят элементам цитоскелета — микротрубочкам и микрофиламентам. АГ удерживается в определенном положении в клетке с помощью микротрубочек, отходящих от центросомы. Имеет место ассоциация плюс-концов микротрубочек с мембранами АГ. Перемещение органеллы к осуществляется с помощью моторных белков: — цитоплазматическим динеином, который тянет органеллу в направлении минус-конца микротрубочек,

- кинезином, двигающим его к плюс-концу. В транспорте мембранных переносчиков от ER к АГ и ретроградном транспорте пузырьков COPI, в транспортировке секреторных пузырьков от транс стороны АГ к плазматической мембране по микротрубочкам участвуют белки из группы кинезинов и актина. Микрофиламенты поддерживают полярность АГ.

Функции АГ: 1. Процессинг углеводов белков и липидов, перемещающихся по секреторному пути. 2. Сортировка и транспорт белков получая мембраны от ER и поставляя их в плазматическую мембрану или др. внутриклеточные мембраны. 3. В мембраннах АГ концентрируются разнообразные сигнальные, сортирующие и цитоскелетные белки, чем обеспечивается способность динамически трансформироваться в ответ на специфические стимулы или др. клеточные изменения.

4. (ER) и (АГ) составляет единую мембранную систему клетки, в пределах которой происходят процессы обмена белками и липидами с помощью направленного и регулируемого внутриклеточного мембранного транспорта. При этом сохраняется уникальность состава мембран органелл. 5. Участие в секреции продуктов, синтезируемых в клетке. 6. Синтез полисахаридов и гликопротеинов (гликокаликса, слизи).

7. Процессинг молекул, который осуществляется в топографически определенном его компоненте : n включение углеводных компонентов в гликопротеины (терминальное гликозилирование), n добавление фосфатных групп (фосфорилирование), n добавление жирных кислот (ацилирование), n добавление сульфатных остатков (сульфатирование), n частичное расщепление белковых молекул (протеолитическая доработка). n конденсация секреторного продукта (в конденсирующих вакуолях) и образование секреторных гранул;

От цис- к транс-поверхности АГ в его мембранах увеличиваются концентрации сфингомиелина и холестерина, продуцирующихся из церамида и фосфатидилхолина ER с помощью фермента АГ сфингомиелинсинтазы. В транс компартментах АГ синтезируются гликосфинголипиды, включающиеся затем в состав плазматической мембраны. Связь холестерина со сфинголипидом приводит к сегрегации ненасыщенных липидов бислоя и образованию специализированных липиднопротеиновых мембранных доменов, так называемых рафтов, которых становится больше в трансцистернах АГ и затем в плазматической мембране.

Они играют существенную роль в процессах эндоцитоза, образовании кавеол, мембранном транспорте и др.

Механизм формирования микропузырьков и их адресная рассылка.

Биогенез АГ сборка АГ de novo. В восстановлении АГ существенную роль играют те интегральные и периферические белки, которые синтезируются в ER. Сборка АГ de novo зависит от регуляторной активности малых ГТФаз, находящихся в ER (SAR 1 и ARF 1). Сначала в области переходного ER формируются экспортные домены, затем дифференцируются элементы ERGIC, и уже после этого возникает стопка цистерн. При восстановлении микротрубочек стопки АГ двигаются по ним в сторону центра, организующего микротрубочки, где они собираются в разветвленную сеть.

Модели структурно-функциональной организации АГ n 1. Матурационная модель (классическая) предложена в 1950 -е годы французским исследователем Грассе (Grasse, 1957). По этой модели цис-цистерны АГ всегда формируются de novo и последовательно и конститутивно созревают к транс-поверхности. Согласно этой модели нет необходимости в везикулярном транспорте, чтобы поддерживать структурную и функциональную целостность АГ. Однако модель не объясняет уникальности каждой цистерны, содержащей свой индивидуальный набор ферментов.

n 2. Везикулярная модель (Palade, 1975) на Паладе открыл векторный транспорт секреторных продуктов, показал существование везикулярного транспорта и продемонстрировал роль АГ в концентрировании и упаковке синтезированных белков в секреторные гранулы В 1986 г. было продемонстрировано, что в транспорте через АГ участвуют не клатриновые пузырьки, а пузырьки с окаймлением COPI.
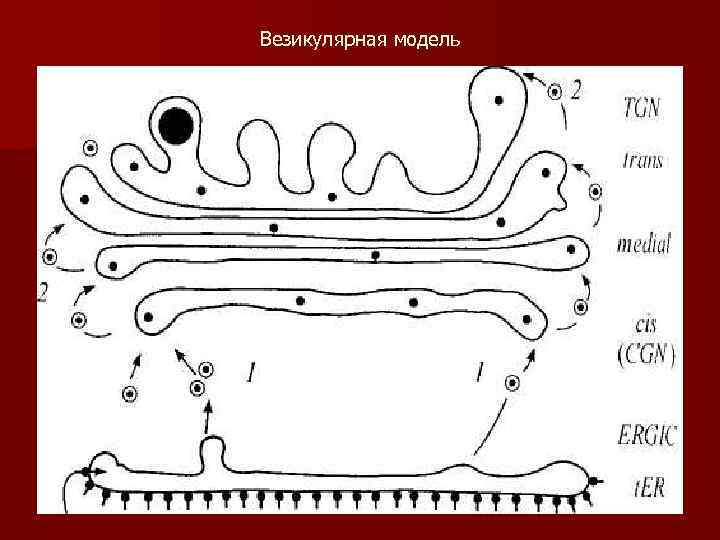
Везикулярная модель

3. Модель созревания цистерн - гибрид между везикулярной и матурационной (везикуломатурационная). n 4. модель латеральной диффузии —модель основана на непрерывности циркуляции ферментов АГ через тубулярные связи между цистернами. n
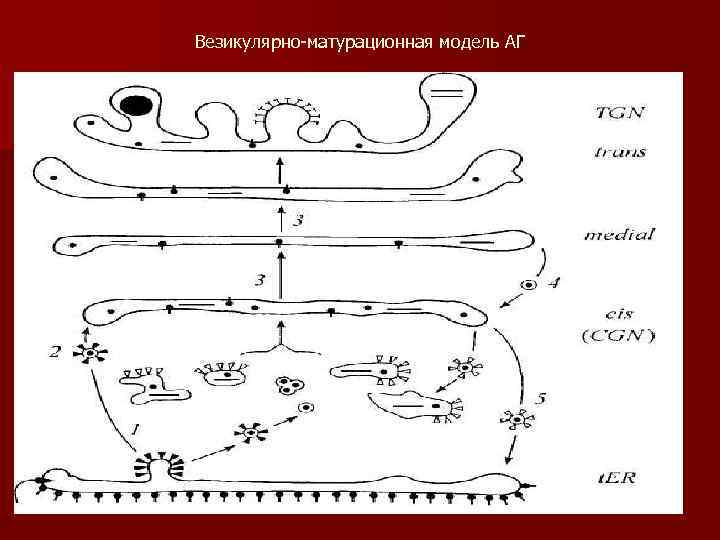
Везикулярно-матурационная модель АГ

Сортировка белков и регуляция процессов их транспорта в АГ 1. Роль окаймленных пузырьков и других типов переносчиков в транспорте белков через АГ. Существует несколько типов окаймления мембран отпочковывающихся пузырьков: n COPI , n СОРИ n клатрин. COPI - цитозольный белковый комплекс, связанный с ГТФ-связывающим белком ARF 1. При обмене ГДФ на ГТФ с помощью обменного фактора GEF происходит почкование пузырька.

Клатрин - через адапторные протеины API, клатрин связывается с мембраной, участвуя в ее деформации. Миронов и соавторы охарактеризовали 4 тина переносчиков карго со следующей динамикой: 1 -й — мешковидные расширения па мембране ER вблизи сайтов выхода; 2 -й — длинные уплощенные мешочки, отходящие от ER, но связанные с ним; 3 -й --— топкие мембранные тубулы, лишенные рибосом; 4 -и —- более сложные структуры состоящие из параллельно уложенных мешочков.

2. Транспорт белков из транс сети АГ. белки, транспортирующиеся через АГ, ковалентно модифицируются ферментами и конденсируются в просвете транс сети АГ, затем они сортируются и направляются к соответствующим мишеням (органеллы, пл. м. ).

Специфичность транспорта и слияния пузырьков.
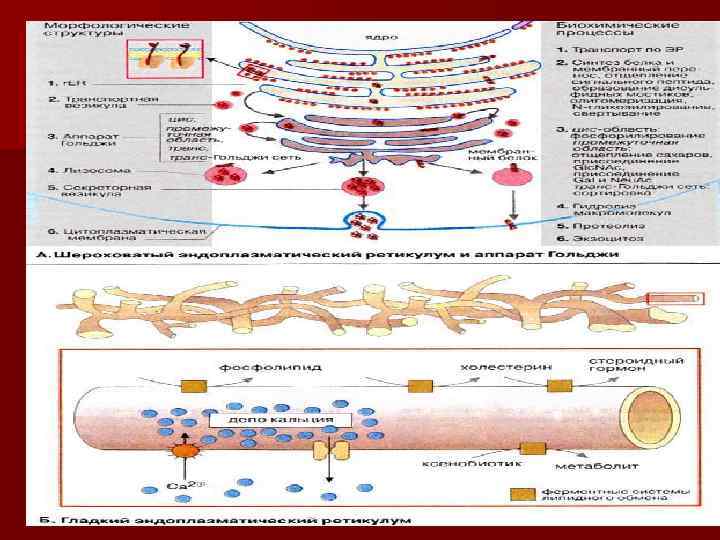

г. ЭР
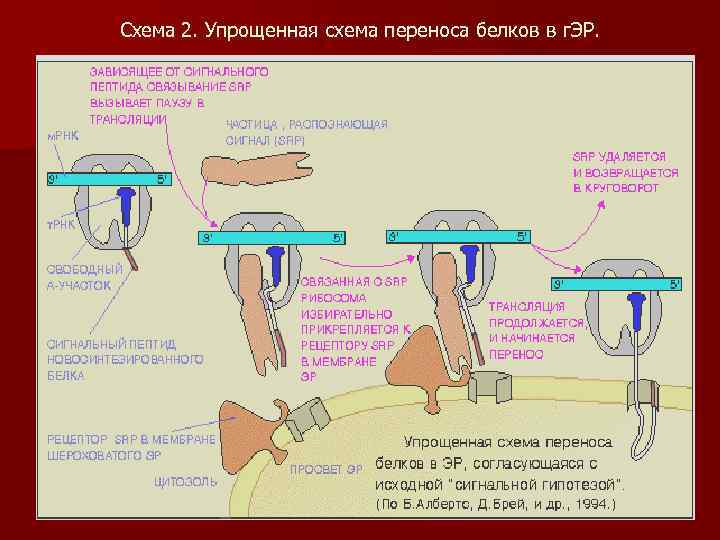
Схема 2. Упрощенная схема переноса белков в г. ЭР.
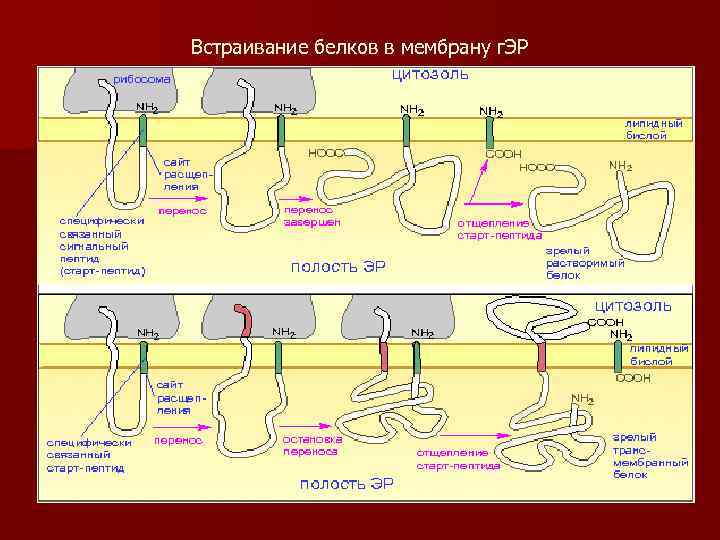
Встраивание белков в мембрану г. ЭР
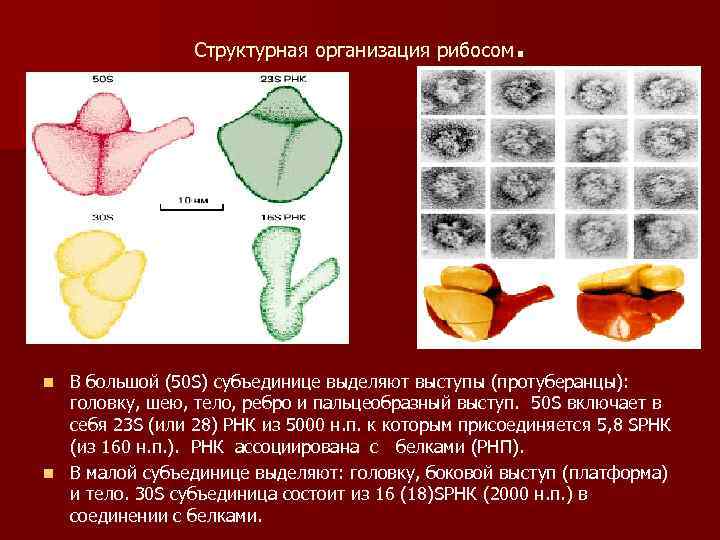
. Структурная организация рибосом В большой (50 S) субъединице выделяют выступы (протуберанцы): головку, шею, тело, ребро и пальцеобразный выступ. 50 S включает в себя 23 S (или 28) РНК из 5000 н. п. к которым присоединяется 5, 8 SРНК (из 160 н. п. ). РНК ассоциирована с белками (РНП). n В малой субъединице выделяют: головку, боковой выступ (платформа) и тело. 30 S субъединица состоит из 16 (18)SРНК (2000 н. п. ) в соединении с белками. n
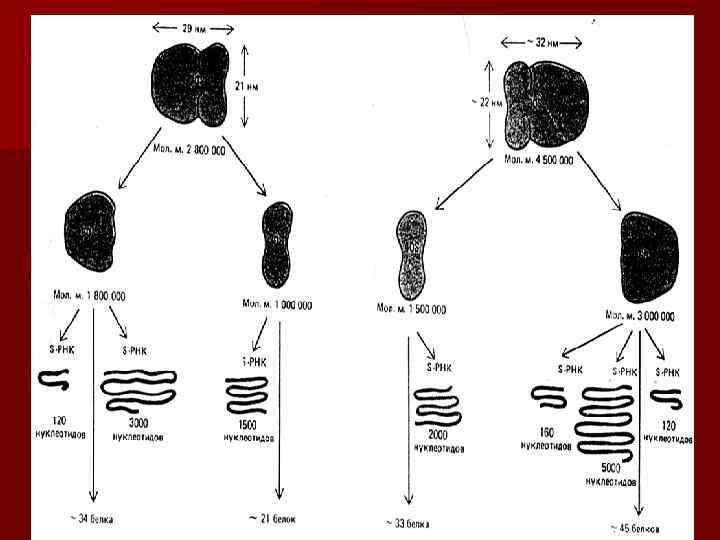
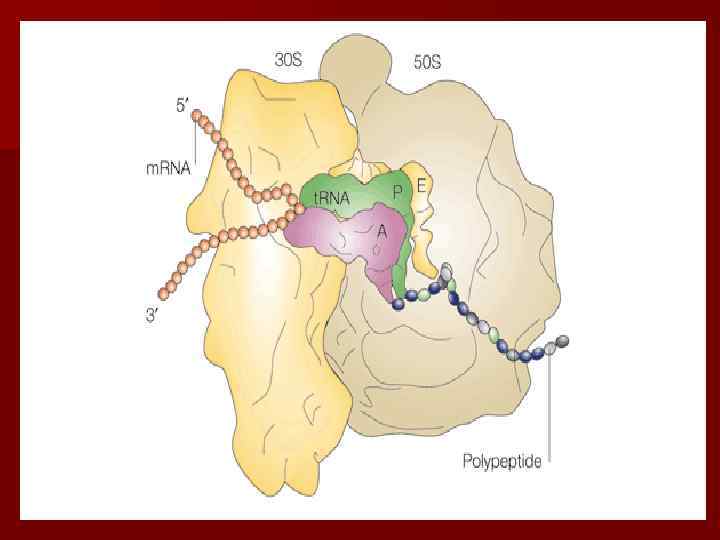

Гетерогенность лизосом.
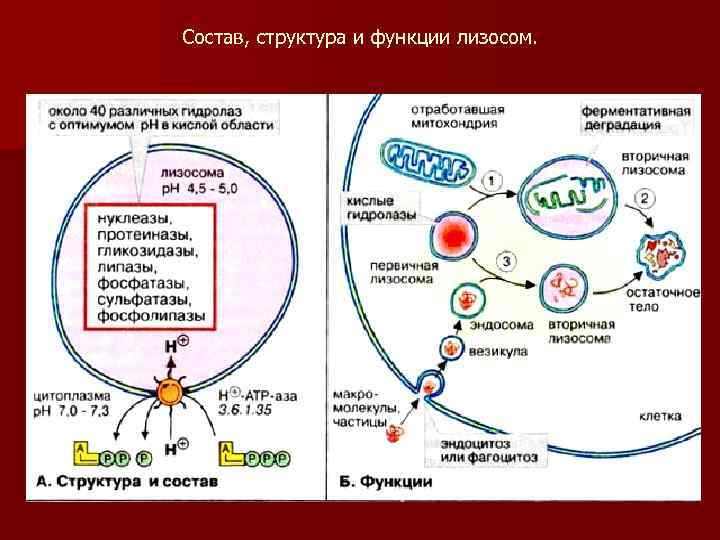
Состав, структура и функции лизосом.
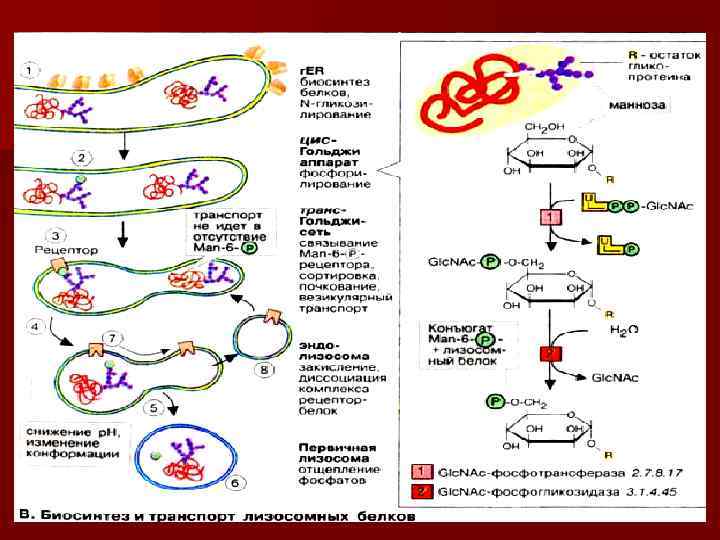
Структурная организация пероксисомы.
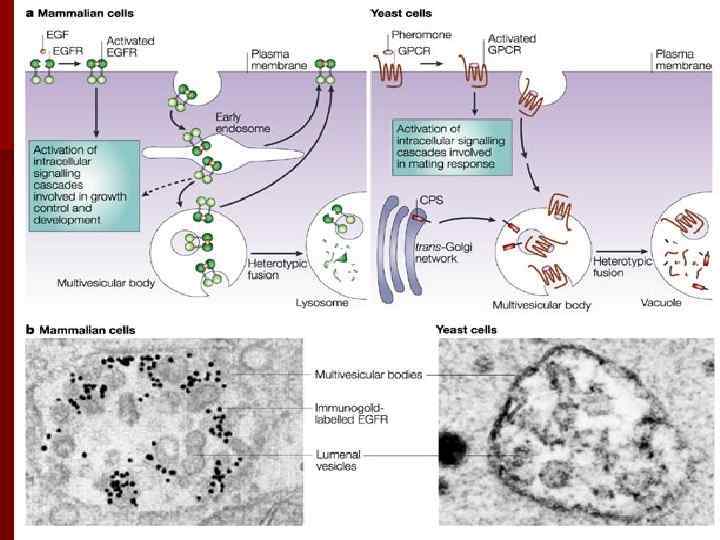
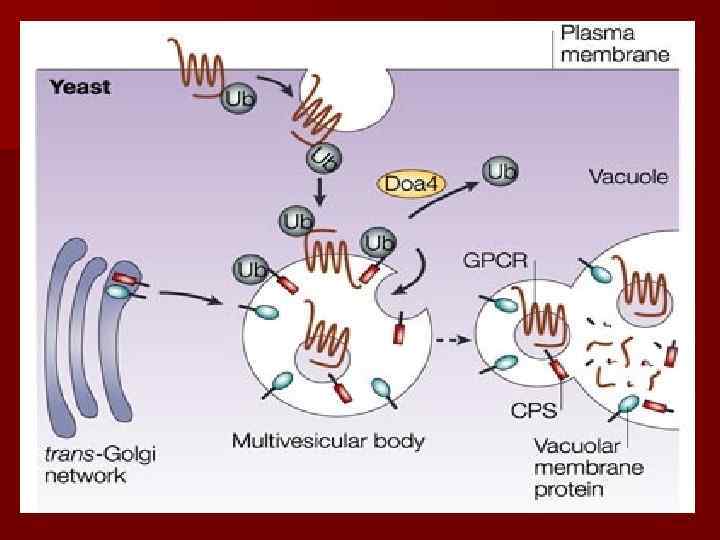
ПРОТЕОСОМЫ
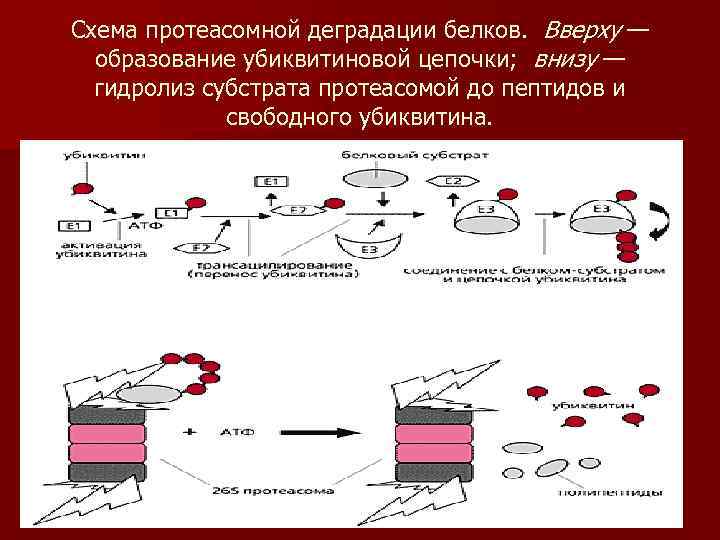
Схема протеасомной деградации белков. Вверху — образование убиквитиновой цепочки; внизу — гидролиз субстрата протеасомой до пептидов и свободного убиквитина.

Цитоскелет- сложная динамичная система микротрубочек, микрофиламентов, промежуточных филаментов и микротрабекул. Функции цитоскелета: 1. Служит клетке механическим каркасом, поддержание и изменение формы клетки; 2. «рельсы» для распределение и перемещение компонентов клетки; 3. транспорт веществ в клетку и из неё (эндо- и экзоцитоз); 4. участие в межклеточных соединениях; 5. «Мотор» для клеточного движения; 6. контроль клеточного цикла. Способен к самоорганизации и к организации цитоплазмы. Самоорганизация – в трехмерные паттерны с участием моторных белков за счет механизмов: 1. мех. сил которые генерируются моторными б. за счет гидролиза АТФ; 2. Обр. филаментов в соответствующем месте; 3. Использование динамических свойств концов филаментов.

Организации цитоплазмы: 1. Поляризованные радиальные лучи ц. микротрубочек (MTs) с «-» концами, собранными в центре клетки и взаимодействуют с микротубулярными моторами, органеллами или хромосомами. 2. В интерфазе, радиальные лучи MTs управляют трафиком мембран и предопределяют локализацию органелл через микротубулярные моторы (кинезины или динеины). 3. Во время митоза фокальные точки MT звезд служат в качестве полюсов митотического веретена. 4. Механические силы, продуцируемые динеинами, используются в транспорте с захватом сайтов на «-» концах МТ. 5. Возможны три механизма нуклеации МТ на нецентросомных сайтах. 1. Цитоплазматический динеи связывается с γ-tubulin кольцевым комплексом, этому способствует перицентрин. 2. цитоплазматический динеин участвует в транспорте различных белков которые индуцируют захват или нуклеацию МТ. 3. Динеин/динактин комплекс кооперируется с центросомами для организации радиального расположения МТ.

Микротрубочки химический состав: димеры из белковых молекул - и -тубулина. Функции: 1. поддержание формы и полярности клеток; 2. обеспечение внутриклеточного транспорта органелл, секреторных и транспортных везикул и вакуолей; 3. обеспечение движения ресничек, хромосом в митозе; 4. образование основы других органелл (реснички, центриоли, жгутики).
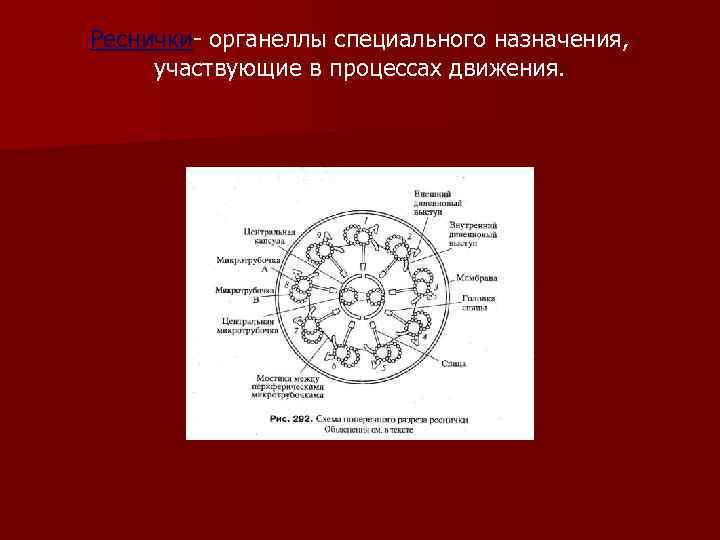
Реснички- органеллы специального назначения, участвующие в процессах движения.

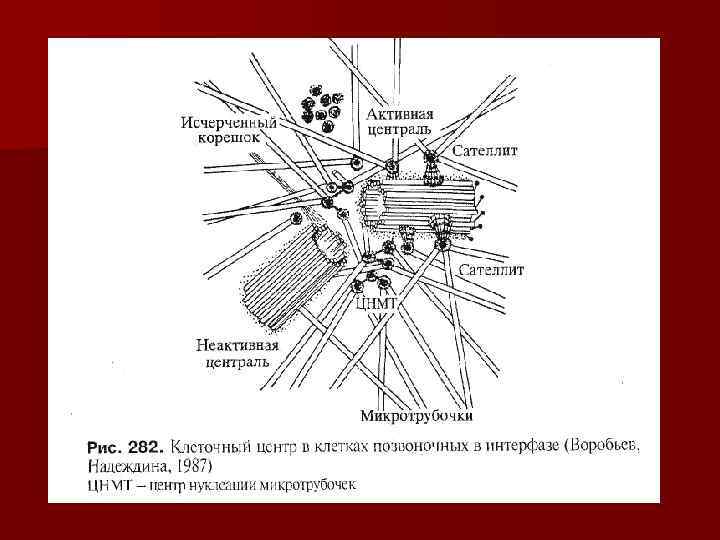
Клеточный центр функции: 1. Организация сети цитоплазматических трубочек ( «кинетическая органелла» ); 2. Определение полюсов делящейся клетки; 3. Центры образования микротрубочек ахроматинового веретена деления.
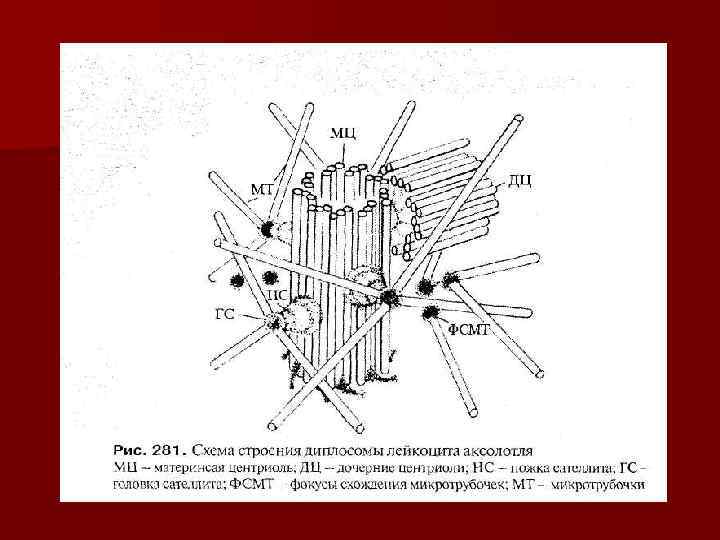
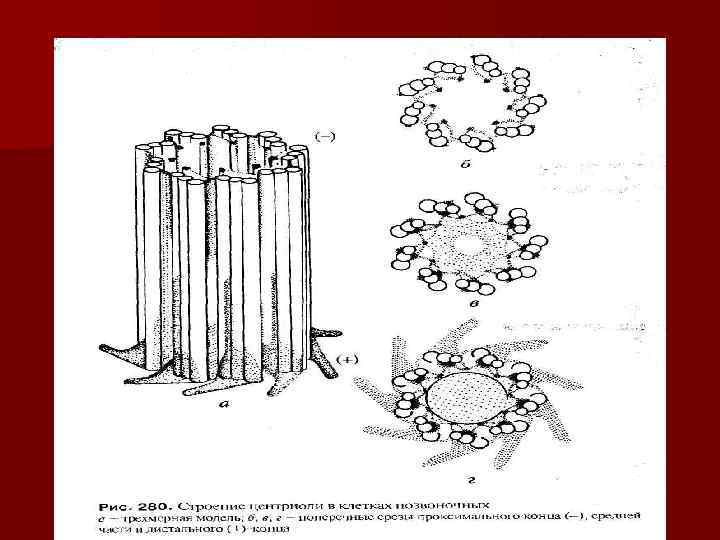

Микрофиламенты-Белковые нити толщиной 5 -7 нм, расположены поодиночке, в виде пучков или сети. АКТИН- основной белок микрофиламентов. Актиновые нити связываются между собой линкерным белком филамином. Актин взаимодействует с миозином. Прикрепление микрофиламентов к плазмолемме происходит через их связи с «якорными» белками интегринами непосредственно или через ряд промежуточных белков - талин, ванкулин, альфа-актинин.

Функции микрофиламентов n n n n Обеспечение сократимости мышечных клеток ( при взаимодействии с миозином); эндо- и экзоцитоз, образование псевдоподий и миграция клеток; перемещение внутри клетки органелл, транспортных пузырьков; обеспечение определенной «жёсткости» клетки за счёт наличия кортикальной сети; формирование сократимой перетяжки при цитотомии; образование основы некоторых органелл (микроворсинки, стереоцилии); участие в образовании опоясывающих десмосом.

микроворсинки - это пальцевидные выросты цитоплазмы клетки диаметром 0, 1 мкм. , основу которых составляют актиновые филаменты. Микроворсинки: - обеспечивают многократное увеличение рабочей поверхности клетки; - на их поверхности происходит расщепление и всасывание веществ. Белки микроворсинок: - актин, - фигибрин и виллин (поперечные «сшивки» ), - минимиозин (прикрепляют актин к плазмолемме), - миозиновые филаменты прикрепляются у основания микроворсинки к актиновым филаментам.
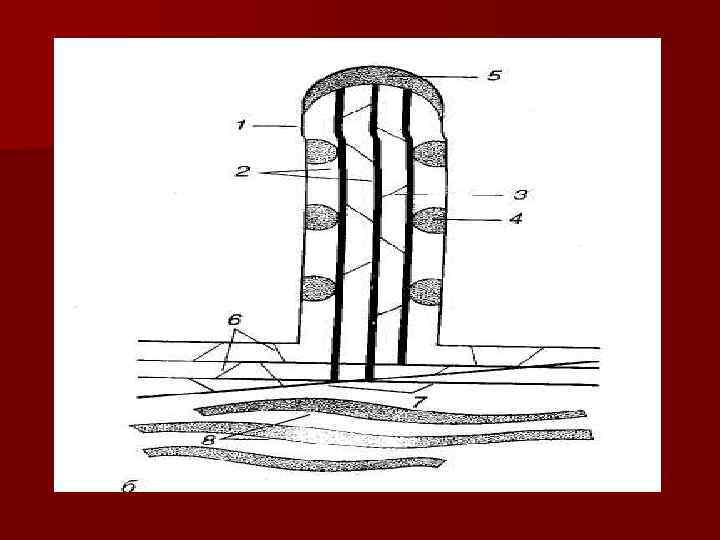

Промежуточные филаменты -белковые нити толщиной 10 нм. Функции: n n n структурная (поддерживающая и опорная); обеспечение равномерного распределения сил деформации между клетками; участие в образовании рогового вещества в эпителии кожи; поддержание формы отростков нервных клеток и фиксация трансмембранных белков; удержание миофибрилл в мышечной ткани; участие в формировании дисмосом и полудисмосом.
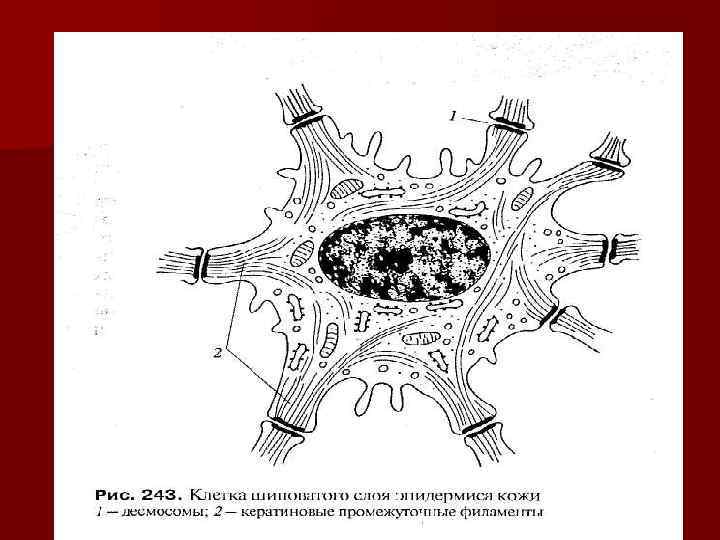

Химическая основа промежуточных филаментов и кислые; 1. в эпителии- кератины нейтральные 2. в нейронах- белки нейрофиламентов; 3. в глиоцитах- глиальный фибриллярный кислый белок; 4. в мышечных клетках- белок дисмин; 5. в клетках мезенхимного происхождения- белок виментин; 6. в ядрах всех клеток- ядерный ламин. Идентификация классов промежуточных филаментов имеет значение в диагностике опухолевого процесса.

микротрабекулы Это IV система цитоскелета, представленная нитями неравнополярной толщины (2 -10 нм), связывающая плазмолемму, различные органеллы и три системы цитоскелета. В «узлах» микротрабекулярной сети располагаются свободные рибосомы и полисомы. Белок МТС не идентифицирован.
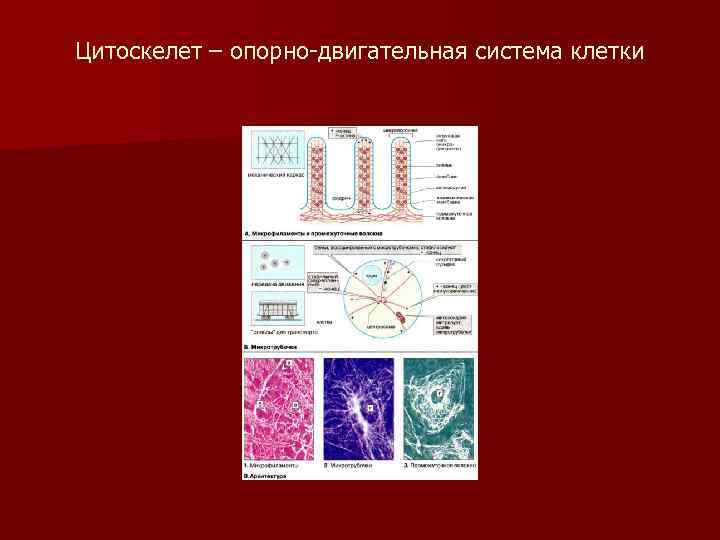
Цитоскелет – опорно-двигательная система клетки
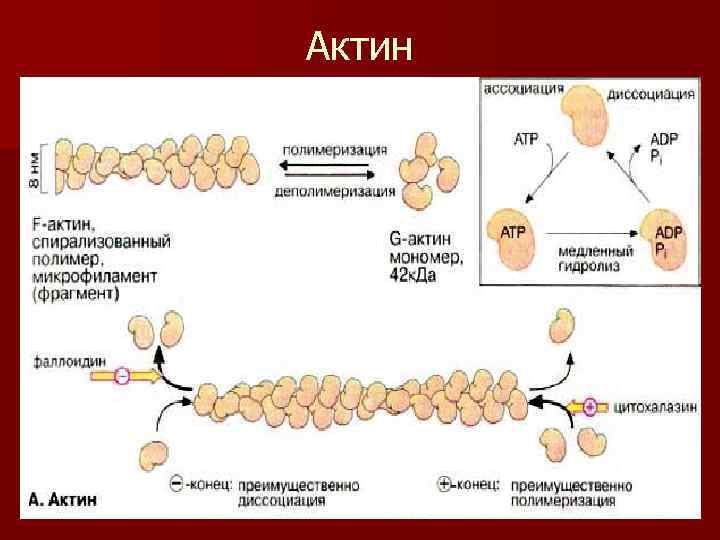
Актин
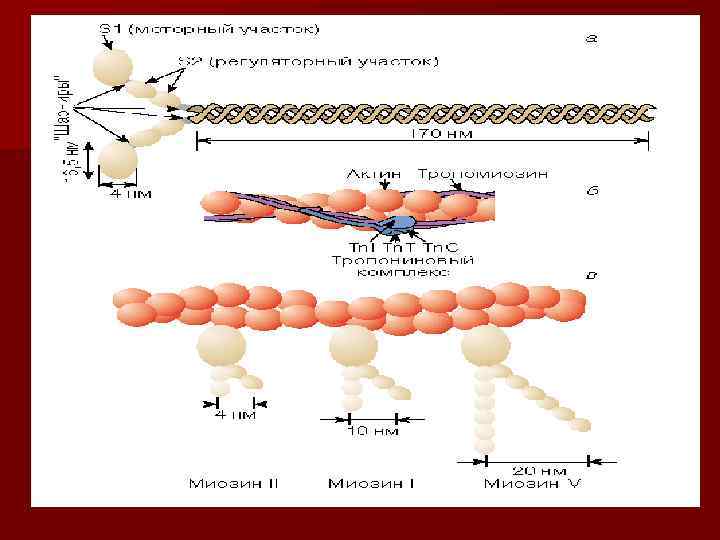
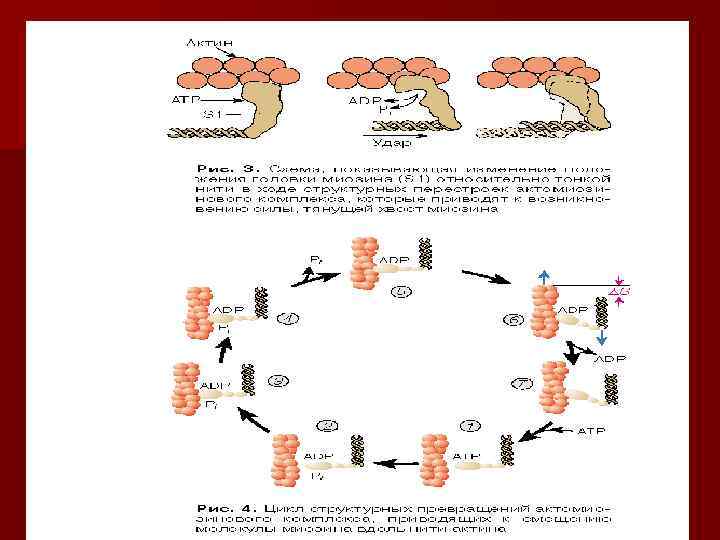

Микрофиламенты (миофибрилы)

Микрофиламенты (миофибрилы)
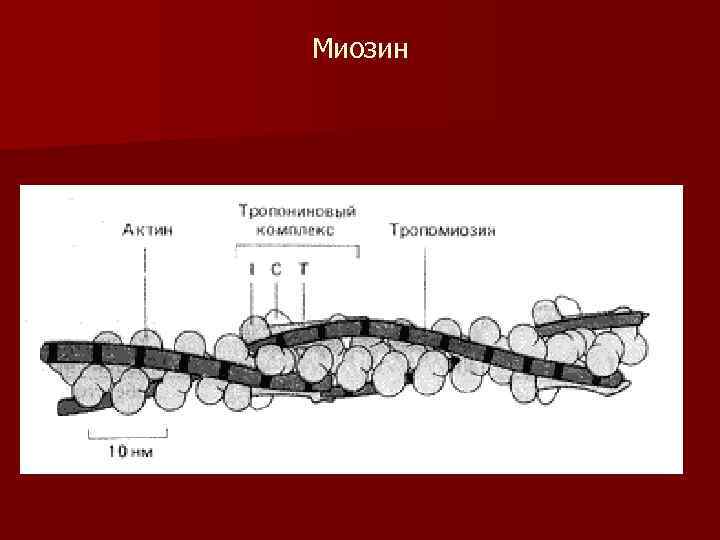
Миозин

клеточный центр, митотический аппарат
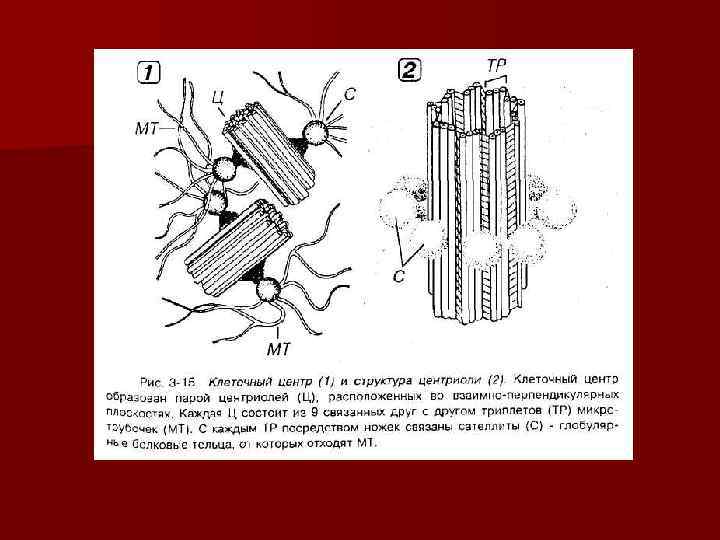
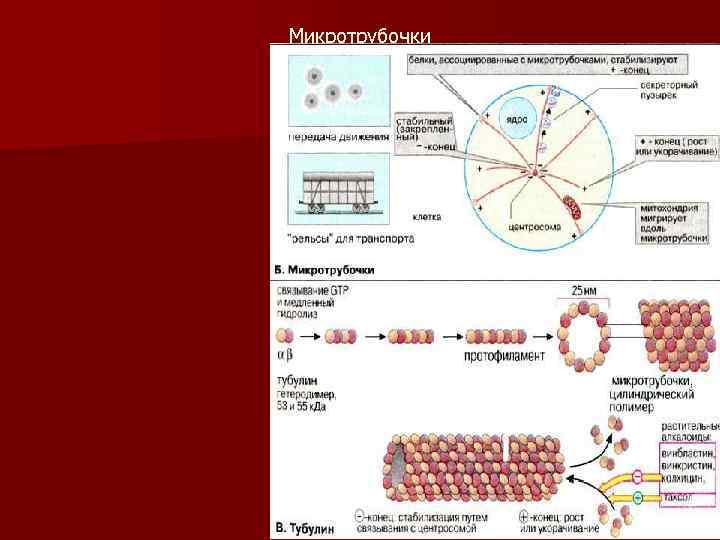
Микротрубочки


n Организация микротрубочки жгутика
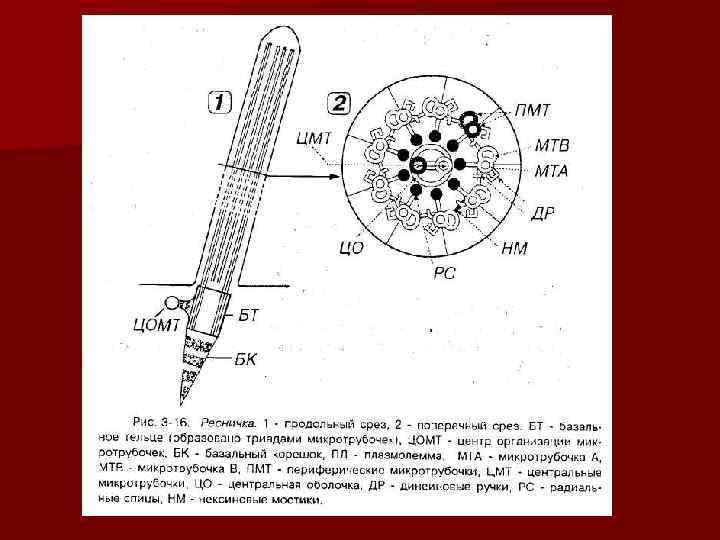
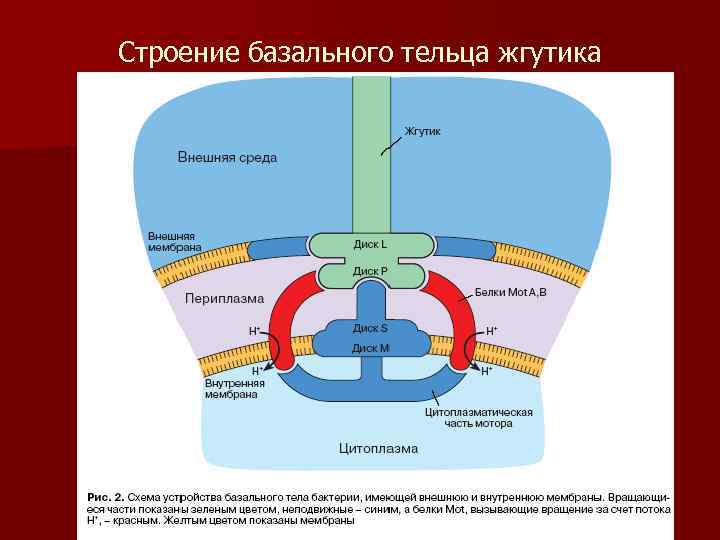
Строение базального тельца жгутика
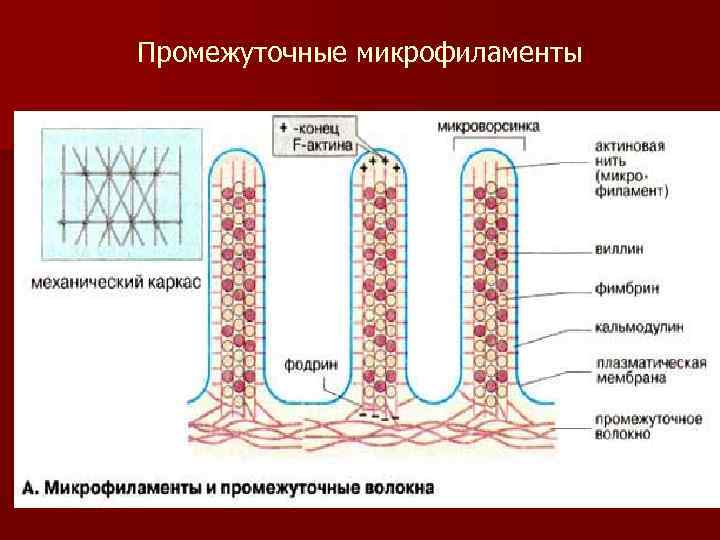
Промежуточные микрофиламенты
Вакуолярная система клетки.ppt