Л4 - Комплексные соед..ppt
- Количество слайдов: 21

В живых организмах присутствуют комплексные соединения биогенных металлов - с белками, - витаминами и др. - комплексные соединения играют роль - -ферментов - - выполняют специфические функции в обмене веществ.
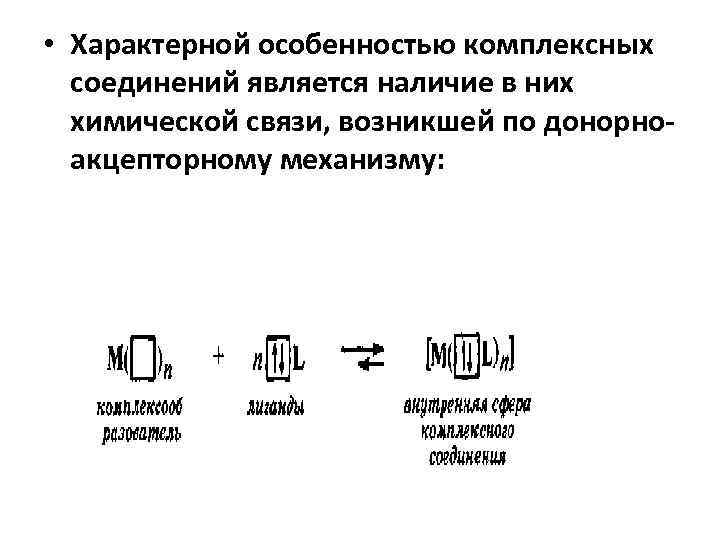
• Характерной особенностью комплексных соединений является наличие в них химической связи, возникшей по донорноакцепторному механизму:

• Комплексные соединения - устойчивые химические соединения сложного состава, в которых обязательно имеется хотя бы одна связь, возникшая по донорно-акцеп-торному механизму. • В каждом комплексном соединении различают внутреннюю и внешнюю сферы: • K 3+ Al(OH)6 -3 Сu(NH 3)4 +2 (NO 3)2

• Комплексообразователь (центральный атом) - атом или ион, который является акцептором электронных пар, предоставляя свободные атомные орбитали, и занимает центральное положение в комплексном соединении. • Роль комплексообразователя выполняют • -----атомы или ионы d- и f-металлов; • -----Атомы неметаллов с различной положительной степенью окисления: В+3, S+6, S+4. • ---- Отрицательно заряженные ионы неметаллов: N 3–, I–, S 2–. • Число свободных атомных орбиталей, предоставляемых комплексообразователем, определяет его координационное число- оно равно удвоенному заряду иона комплексообразователя. • • В комплексных соединениях комплексообразователь связан с лигандами.

• Лиганды - молекулы или ионы, которые являются донорами электронных пар и непосредственно связаны с комплексообразователем. • Лиганды-анионы : •
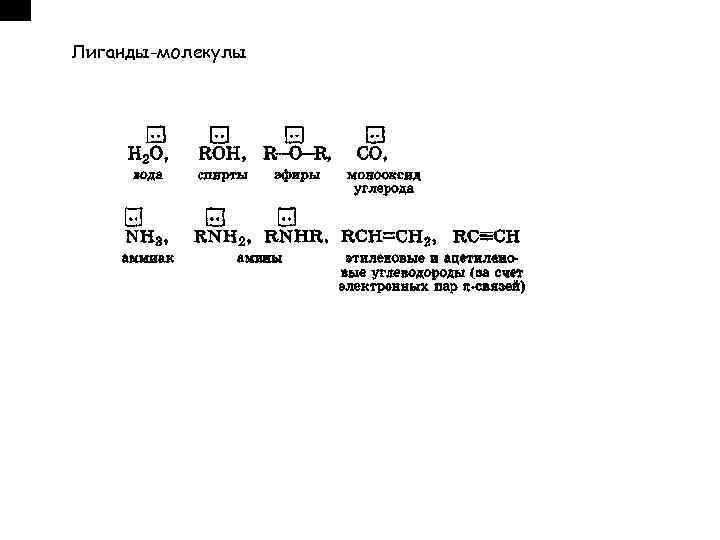
Лиганды-молекулы

• По числу связей, образуемых лигандом с комплексообразо-вателем, лиганды делятся на моно-, би- и полидентатные

• Внешняя сфера комплексного соединения — это положительно или отрицательно заряженные ионы, нейтрализующие заряд комплексного иона и связанные с ним ионной связью

• Теории строения комплексных соединений. • 1. С точки зрения электростатической теории В. Косселя и А. Магнуса образование комплексных соединений обусловлено действием кулоновских сил-притяжением между центральным катионом металла и анионами или полярными молекулами лигандов • ---- не объясняла многие свойства комплексных соединений — магнитные свойства, окраску, реакционноспособность

• 2. В 1891 г. швейцарский учёный Альфред Вернер предложил координационную теорию комплексных соединений, которая легла в основу и современных представлений. • 3. теории кристаллического поля. • - лиганды создают электростатическое поле, под действием которого меняется энергия электронных орбиталей центрального иона. При этом меняется распределение электронов. На орбиталях центрального атома освобождаются места для электронов лиганда. Освободившиеся орбитали используются для образования донорно-акцепторной связи с лиганд

• Метод валентных связей. • --Связь между центральным атомом и лигандами донорноакцепторная. Лиганды предоставляют электронные пары, а ядро — свободные орбитали. • -----Мерой прочности служит степень перекрывания орбиталей. Обобществление электронных пар донора и акцептора сопровождается выделением энергии. • Так как запас энергии уменьшается, связь становится устойчивой. • ----Донорно-акцепторная связь характеризуется направленностью, отсюда конфигурация комплексного иона строго определённая. • -----Строение и прочность комплекса зависят от характера орбиталей, участвующих в гибридизации

• • • • Классификация комплексных соединений. I тип: комплексные соединения с одинаковыми лигандами называются однородными, а с разными лигандами — неоднородными. II тип: за основу берётся химическая природа комплекса [комплексы катионные, анионные, нейтральные]. III тип: наиболее распространена классификация по химической природе лигандов. 1. Аммиакаты —: [Ag(NH 3)2]Cl. 2. Ацидокомплексы: лиганды — анионы кислот: К 3[Fe(CN)6]. 3. Аквакомплексы — лигандами являются молекулы воды: [Со(Н 2 О)6]SО 4. 4. Гидроксокомплексы — лигандами являются гидроксогруппы: К 3[Al(ОН)6]. 5. Сверхкомплексные соединения: число лигандов превышает координационное число: [Cu(H 2 O)4]SO 4 • H 2 O 6. Внутрикомплексные соединения: Комплексообразователь как бы втянут внутрь лиганда [хелат — «клешня рака» ]. лиганды — сложные молекулы, образующие с комплексообразователем помимо донорно-акцепторной связи, ещё ковалентные связи: H 2 C—H 2 N NH 2—CH 2 Cu O=C—O O—C=O

• В живых организмах в полидентных лигандах донорные атомы связаны в единое кольцо-цикл. • - порфирины [железо в гемоглобине, магний в хлорофилле, кобальт в витамине В 12]. • Полидентные лиганды связываются с ионами металла гораздо сильнее, чем монодентные с теми же донорными атомами [прочность комплексов на 8– 10 порядков выше]. • Повышенная прочность комплексных соединений с полидентными лигандами называется хелатным эффектом. • Чем выше заряд ионов-комплексообразователей и выше основность лигандов, тем выше хелатный эффект. • Хелатный эффект снижается, если ион сильно гидратирован и имеет малый радиус. • Так как ионы Н+ конкурируют с ионами металла, повышение кислотности среды снижает хелатный эффект.

• • • • Международная (Женевская) номенклатура КС I. КС разбивается на внешнюю и внутреннюю сферы. вначале дается название аниона, а потом катиона: II. Комплекс называется следующим образом: а) сначала перечисляются лиганды с указанием их числа в комплексе; б) лигнады-анионы называются с добавлением окончания ”о” : OH- гидроксо, F- - фторо и т. д. г) нейтральные лиганды называются так же как молекулы: Cl 2 - хлор, и т. д. (исключения: H 2 O - аква, NH 3 - аммин, CO после перечисления лигандов дается название комплексообразователя с указанием его заряда: . --- Катионный комплекс - по-русски в родит. падеже: [Co+2(H 2 O) 06]SO 4 -2 - сульфат гексааквакобальта (+2); --- анионный комплекс то название комплексообразователя - полатыни с окончанием “ат”: K 3[Fe+3(CN) -1 6] - гексацианоферрат (+3) калия. ---- если комплекс не заряжен, то комплексообразователь называется по-русски в именительном падеже: [Fe 0(CO)0 5] - пентакарбонилжелезо;
![• Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во • Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во](https://present5.com/presentation/3/-30500059_18305197.pdf-img/-30500059_18305197.pdf-15.jpg)
• Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во внутренней и внешней сфере: [Cr(H 2 O)6]Cl 3 [Cr(H 2 O)5 Cl]Cl 2 • H 2 O фиолетовый светло-зелёный 2. Ионизационная изомерия: различное распределение ионов между внешней и внутренней сферами: [Co(NH 3)5 SO 4]Br [Co(NH 3)5 Br]SO 4 красный красно-фиолетовый 3. Геометрическая изомерия обусловлена различным пространственным расположением лигандов неоднородного комплекса в одной и той же внутренней сфере: NH 3 Cl / / Pt Pt / / NH 3 Cl Cl NH 3 оранжевый [цис] светло-зелёный [транс] Различное биологическое действие: цис-изомер используется в онкологической практике. 4. Координационная изомерия [переход лигандов от одного комплексообразователя к другому].
![» » » КС диссоциирует : [Ag(NH 3)2]Cl = [Ag(NH 3)2]+ + Cl– комплексные » » » КС диссоциирует : [Ag(NH 3)2]Cl = [Ag(NH 3)2]+ + Cl– комплексные](https://present5.com/presentation/3/-30500059_18305197.pdf-img/-30500059_18305197.pdf-16.jpg)
» » » КС диссоциирует : [Ag(NH 3)2]Cl = [Ag(NH 3)2]+ + Cl– комплексные ионы обратимо дисоциируют: [Ag(NH 3)2]+ Ag+ + 2 NН 3 закон действующих масс: » » Константа диссоциации — это константа нестойкости, мера неустойчивости комплексного иона. » Чем меньше константа ионизации, тем устойчивее комплекс. » Чем больше константа устойчивости, тем устойчивее комплекс.

• На прочность комплекса, на константу ионизации влияют природа комплексообразователя, т. к. от природы комплексообразователя зависит заряд, радиус, степень гидратации, формы его электронных орбиталей • для прогнозирования связывания иона металла с биолигандами имеет концепция жёстких и мягких кислот и оснований, в соответствии с которой ионы металлов — кислоты и лиганды — основания делятся на жёсткие и мягкие группы.

• Кислоты — жёсткие: H+, Li+, Na+, K+, Mn 2+, Cr 3+, Fe 3+, Co 3+, Mg 2+, Ca 2+; • мягкие: Cu+, Ag+, Au+, Pt 2+, Pt 4+, Hg 2+, Cd 2+. • Основания — жёсткие: H 2 O, OH–, NH 3, RNH 2, Cl–, PO 43–, SO 42–; • мягкие: SCN–, R 1 S–, R 2 S, H–, S 2 O 3 2–, SH. • правило: • Устойчивые комплексы образуются между жёсткой кислотой и жёстким основанием или между мягкой кислотой и мягким основанием.

• Комплексообразователи и лиганды нашего организма. • : • Ca 2+ < Mg 2+ < Mn 2+ < Fe 2+ < Cd 2+ < Co 2+ < Zn 2+ < Ni 2+ < Cu 2+ • - [Na+ и К+] присутствуют в основном в свободном виде, . • - Са 2+, Мg 2+ существуют как в свободном виде, так и в виде комплексов. • - Ионы тяжёлых металлов — Fe 2+, . — легче связываются с атомами азота и серы, например, в порфиринах.

• • Общие понятия об активном центре металлоферментов. ферменты представляют собой комплексные соединения с металлами, ионы которых определяют активный центр фермента и пространственную структуру [конформацию] фермента. Кроме того, в силу хелатного эффекта они придают прочность белкам. В состав ферментов входят микроэлементы: Mn — в состав 12 ферментов; Fe — в состав 70 ферментов; Cu — в состав 30 ферментов; Zn — в состав более 100 ферментов; Мо и Со — в состав нескольких ферментов. .

• Значение комплексов в медицине. • Биохимик Дж. Вуд писал: . Биохимия — это координационная химия живых систем» . • В медицине применяются: • 1. Лекарственные препараты на основе комплексов металлов в онкологии, психиатрии, при воспалительных заболеваниях. • 2. Радиодиагностика — использование комплексов металлов, меченых радиоактивными изотопами для выяснения путей перемещения лекарств. • 3. Радиотерапия — направление радиоактивного изотопа в поражённый участок с целью локального воздействия на него. • 4. Хелатотерапия — при металлотоксикозах и металлоаллергических заболеваниях.
Л4 - Комплексные соед..ppt