лекция 3 Комплексы.ppt
- Количество слайдов: 20

- В живых организмах присутствуют комплексные соединения биогенных металлов - с белками, - витаминами и др. комплексные соединения играют роль ферментов - выполняют специфические функции в обмене веществ.

Комплексные соединения • Комплексные соединения (КС) – устойчивые химические соединения сложного состава, в которых обязательно имеется хотя бы одна связь, возникающая по донорно-акцепторному механизму. • Строение КС: внутренняя сфера внешняя сфера Комплексообразователь [Me Ln ] X (центральный атом) Атом или ион, который предоставляет свободные атомные орбитали и занимает центральное положение в КС. Хорошие комплексообразователи: d- и f- элементы, хуже p-элементы. Координационное число Лиганды Молекулы или ионы, которые являются донорами электронных пар и непосредственно связаны с комплексообразователем. • Примеры КС: [Cu(NH 3)4]SO 4, K 3[Fe(CN)6], [Pt(NH 3)2 Cl 2]
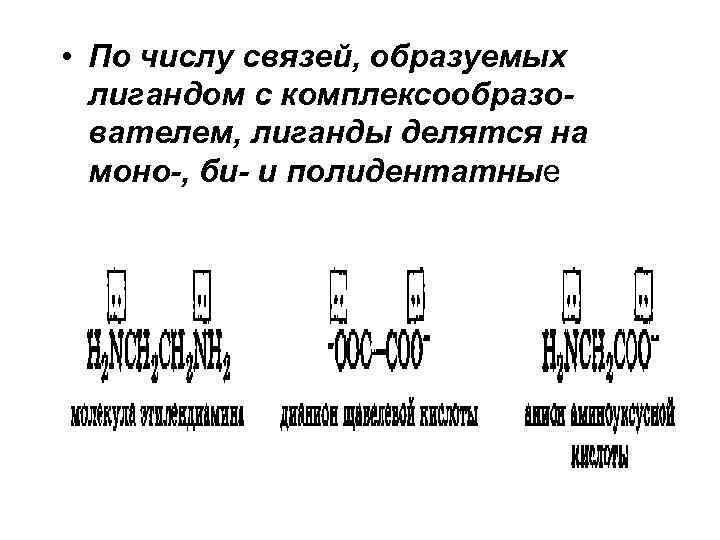
• По числу связей, образуемых лигандом с комплексообразователем, лиганды делятся на моно-, би- и полидентатные

• Внешняя сфера комплексного соединения — это положительно или отрицательно заряженные ионы, нейтрализующие заряд комплексного иона и связанные с ним ионной связью
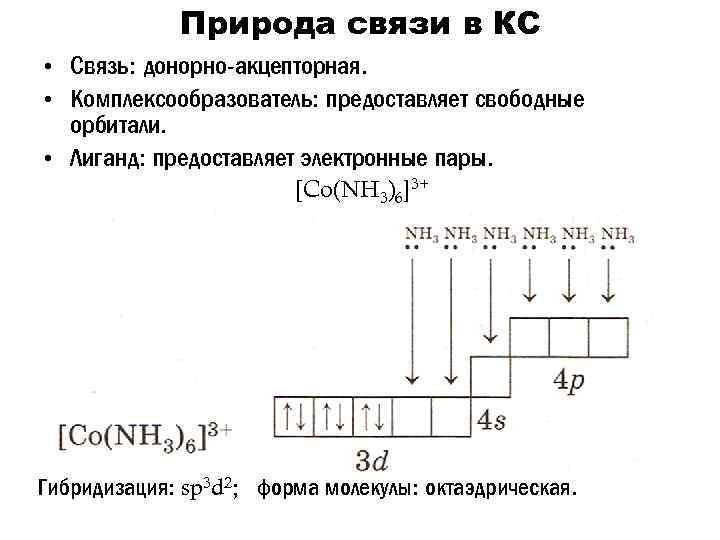
Природа связи в КС • Связь: донорно-акцепторная. • Комплексообразователь: предоставляет свободные орбитали. • Лиганд: предоставляет электронные пары. [Co(NH 3)6]3+ Гибридизация: sp 3 d 2; форма молекулы: октаэдрическая.

• ======В 1891 г. швейцарский учёный Альфред Вернер предложил координационную теорию комплексных соединений, которая легла в основу и современных представлений. • =====теория кристаллического поля. • - лиганды создают электростатическое поле, под действием которого на орбиталях центрального атома освобождаются места для электронов лиганда. • -Освободившиеся орбитали используются для образования донорно-акцепторной связи с лиганд

• Метод валентных связей. • --Связь между центральным атомом и лигандами донорно-акцепторная. Лиганды предоставляют электронные пары, а ядро — свободные орбитали. • -----Мерой прочности служит степень перекрывания орбиталей. • ----Донорно-акцепторная связь характеризуется направленностью, отсюда конфигурация комплексного иона строго определённая. • -----Строение и прочность комплекса зависят от характера орбиталей, участвующих в гибридизации
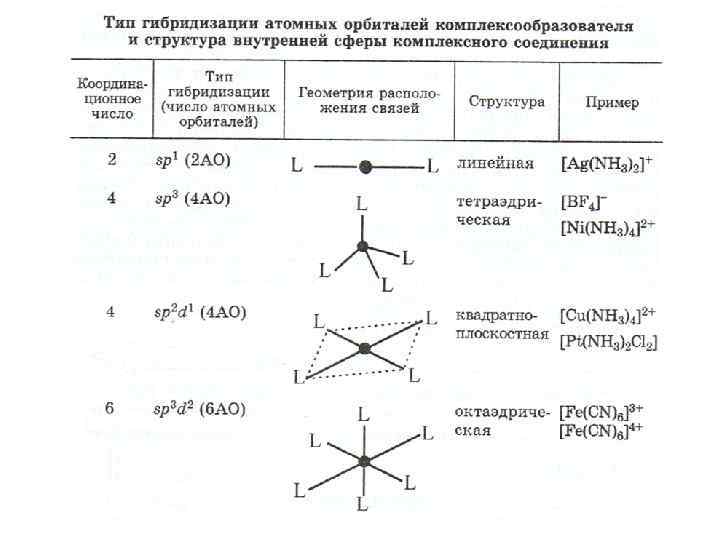

• • • Классификация комплексных соединений. I тип: комплексные соединения с одинаковыми лигандами называются однородными, а с разными лигандами — неоднородными. II тип: за основу берётся химическая природа комплекса [комплексы катионные, анионные, нейтральные]. III тип: наиболее распространена классификация по химической природе лигандов. 1. Аммиакаты —: [Ag(NH 3)2]Cl. 2. Ацидокомплексы: лиганды — анионы кислот: К 3[Fe(CN)6]. 3. Аквакомплексы — лигандами являются молекулы воды: [Со(Н 2 О)6]SО 4. 4. Гидроксокомплексы — лигандами являются гидроксогруппы: К 3[Al(ОН)6]. 6. Внутрикомплексные соединения: Комплексообразователь как бы втянут внутрь лиганда [хелат — «клешня рака» ]. лиганды — сложные молекулы, образующие с комплексообразователем помимо донорно-акцепторной связи, ещё ковалентные связи: H 2 C—H 2 N NH 2—CH 2 Cu O=C—O O—C=O

• В живых организмах в полидентных лигандах донорные атомы связаны в единое кольцо-цикл: • порфирины [железо в гемоглобине, магний в хлорофилле, кобальт в витамине В 12]. • Полидентные лиганды связываются с ионами металла гораздо сильнее, чем монодентные с теми же донорными атомами [прочность комплексов на 8– 10 порядков выше]. • Повышенная прочность комплексных соединений с полидентными лигандами называется хелатным эффектом. • Чем выше заряд ионов-комплексообразователей и выше основность лигандов, тем выше хелатный эффект. • Хелатный эффект снижается, если ион сильно гидратирован и имеет малый радиус. • Так как ионы Н+ конкурируют с ионами металла, повышение кислотности среды снижает хелатный эффект.
![• Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во • Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во](https://present5.com/presentation/3/133036861_33338715.pdf-img/133036861_33338715.pdf-11.jpg)
• Изомерия комплексных соединений. ……. 1. Сольватная [гидратная]: различие в распределении воды во внутренней и внешней сфере: [Cr(H 2 O)6]Cl 3 [Cr(H 2 O)5 Cl]Cl 2 • H 2 O фиолетовый светло-зелёный 2. Ионизационная изомерия: различное распределение ионов между внешней и внутренней сферами: [Co(NH 3)5 SO 4]Br [Co(NH 3)5 Br]SO 4 красный красно-фиолетовый 3. Геометрическая изомерия обусловлена различным пространственным расположением лигандов неоднородного комплекса в одной и той же внутренней сфере: NH 3 Cl / / Pt Pt / / NH 3 Cl Cl NH 3 оранжевый [цис] светло-зелёный [транс] Различное биологическое действие: цис-изомер используется в онкологической практике. 4. Координационная изомерия [переход лигандов от одного комплексообразователя к другому].

• Химические свойства комплексных соединений • 1. Диссоциация. • Первичная диссоциация: [Ag(NH 3)2 ]Cl [Ag(NH 3)2 ]+ + Cl • Вторичная диссоциация: [Ag(NH 3)2 ]+ ↔Ag+ + 2 NH 3 • Чем меньше Кнест, тем стабильнее комплексное соединение. • Кнест многих комплексов имеют малые значения, следовательно, для связывания ионов из раствора эффективно использовать реакцию комплексообразования.

• Это свойство используется в аналитической практике для определения содержания ионов (комплексометрия) и в медицинской практике – для выведения из организма ионов тяжелых металлов в виде растворимых комплексов.

2. Образование КС. • Cu. SO 4 + 4 NH 3 H 2 O [Cu(NH 3)4]SO 4 + 4 H 2 O • Ag. Cl + 2 NH 3 H 2 O [Ag(NH 3)2]Cl + 2 H 2 O 3. Трансформация и разрушение – происходят вследствие образования: • а) более устойчивого комплекса Например, более прочного связывания комплексообразователя с новым лигандом, т. е. реакции обмена лигандами во внутренней сфере: [Pt(NH 3)4]Cl 2 + 4 KCN K 2[Pt(CN)4] + 4 NH 3 + 2 KCl.

На этом свойстве основана хелатотерапия – детоксикация организма от металлов токсикантов при помощи лиганд-препаратов на основе полидентантных лигандов, которые образуют с токсикантами более прочные водорастворимые комплексы, но не выводят ионы биометаллов. В хелатотерапии используются: • Na 2 S 2 O 3 (тиосульфат Na), • ЭДТА и ее соли (тетацин кальций: Ca. Na 2 ЭДТА), •

• для прогнозирования связывания иона металла с биолигандами имеется концепция жёстких и мягких кислот и оснований, в соответствии с которой ионы металлов — кислоты(акцепторы электронных пар по Льюлису) и лиганды (доноры электронных пар по Льюлису ) — основания делятся на жёсткие и мягкие группы.

• Кислоты — • жёсткие: H+, Li+, Na+, K+, Mn 2+, Cr 3+, Fe 3+, Co 3+, Mg 2+, Ca 2+; • мягкие: Cu+, Ag+, Au+, Pt 2+, Pt 4+, Hg 2+, Cd 2+. • Основания — • жёсткие: H 2 O, OH–, NH 3, RNH 2, Cl–, PO 43–, SO 42–; • мягкие: SCN–, R 1 S–, R 2 S, H–, S 2 O 3 2–, SH. • правило: • Устойчивые комплексы образуются между жёсткой кислотой и жёстким основанием или между мягкой кислотой и мягким основанием.

• Комплексообразователи и лиганды нашего организма. • : • Ca 2+ < Mg 2+ < Mn 2+ < Fe 2+ < Cd 2+ < Co 2+ < Zn 2+ < Ni 2+ < Cu 2+ • - [Na+ и К+] присутствуют в основном в свободном виде, . • - Са 2+, Мg 2+ существуют как в свободном виде, так и в виде комплексов.

• • Общие понятия об активном центре металлоферментов. ферменты представляют собой комплексные соединения с металлами, ионы которых определяют активный центр фермента и пространственную структуру [конформацию] фермента. Кроме того, в силу хелатного эффекта они придают прочность белкам. В состав ферментов входят микроэлементы: Mn — в состав 12 ферментов; Fe — в состав 70 ферментов; Cu — в состав 30 ферментов; Zn — в состав более 100 ферментов; Мо и Со — в состав нескольких ферментов. .

• Значение комплексов в медицине. • Биохимик Дж. Вуд писал: . Биохимия — это координационная химия живых систем» . • В медицине применяются: • 1. Лекарственные препараты на основе комплексов металлов в онкологии, психиатрии, при воспалительных заболеваниях. • 2. Радиодиагностика — использование комплексов металлов, меченых радиоактивными изотопами для выяснения путей перемещения лекарств. • 3. Радиотерапия — направление радиоактивного изотопа в поражённый участок с целью локального воздействия на него. • 4. Хелатотерапия — при металлотоксикозах и металлоаллергических заболеваниях.
лекция 3 Комплексы.ppt