геохимия_7.ppt
- Количество слайдов: 30


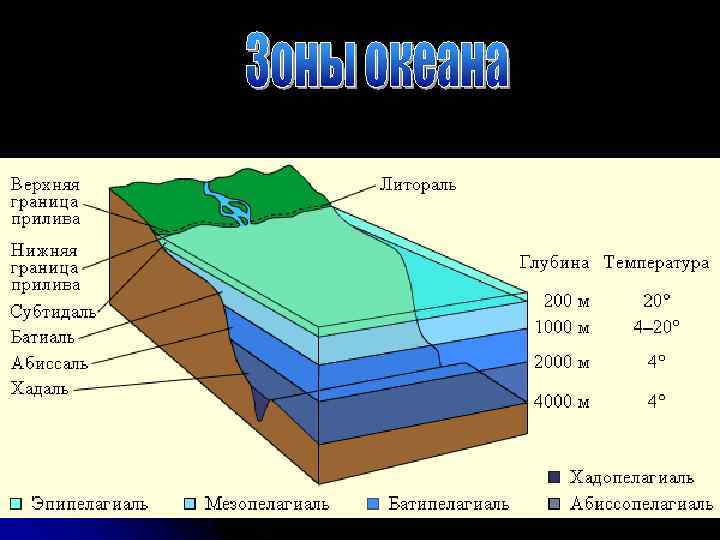
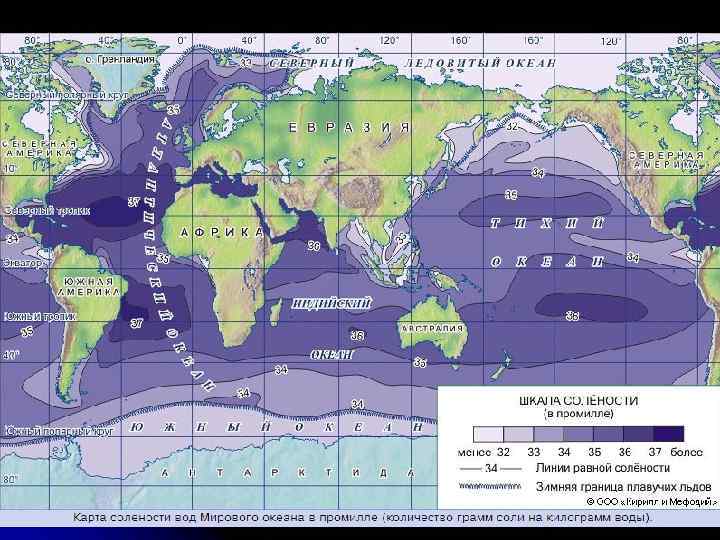
 В воде океанов присутствуют почти все химические элементы, известные на Земле. Однако в количественном отношении в составе морской воды резко преобладают только четыре химических элемента: кислород, водород, хлор и натрий, на долю которых приходится 99, 5% по весу. Содержание растворенных в морской воде химических элементов и соединений, ее соленость определяются или в весовых процентах, или в промиллях (1‰). Средняя соленость морской (океанической) воды равна 35‰. Это значит, что в 1 л (1 кг) воды содержится 35 г солей. Средняя химическая характеристика морской воды Название солей Содержание солей в граммах на 1 л воды Хлориды: Хлористый натрий (Nа. Сl) в вес. % 27, 2 77, 8 3, 8 10, 9 1, 7 4, 7 Сернокислый кальций (Са. SО 4) 1, 2 3, 6 Сернокислый калий (К 2 SО 4) 0, 9 2, 5 Углекислый кальций (Са. СО 3) 0, 1 0, 3 Бромистый магний (Мg. Вr 2) 0, 1 0, 2 Хлористый магний (Мg. Сl 2) Сульфаты: Сернокислый магний (Мg. SО 4) Всего 35, 0 100, 0
В воде океанов присутствуют почти все химические элементы, известные на Земле. Однако в количественном отношении в составе морской воды резко преобладают только четыре химических элемента: кислород, водород, хлор и натрий, на долю которых приходится 99, 5% по весу. Содержание растворенных в морской воде химических элементов и соединений, ее соленость определяются или в весовых процентах, или в промиллях (1‰). Средняя соленость морской (океанической) воды равна 35‰. Это значит, что в 1 л (1 кг) воды содержится 35 г солей. Средняя химическая характеристика морской воды Название солей Содержание солей в граммах на 1 л воды Хлориды: Хлористый натрий (Nа. Сl) в вес. % 27, 2 77, 8 3, 8 10, 9 1, 7 4, 7 Сернокислый кальций (Са. SО 4) 1, 2 3, 6 Сернокислый калий (К 2 SО 4) 0, 9 2, 5 Углекислый кальций (Са. СО 3) 0, 1 0, 3 Бромистый магний (Мg. Вr 2) 0, 1 0, 2 Хлористый магний (Мg. Сl 2) Сульфаты: Сернокислый магний (Мg. SО 4) Всего 35, 0 100, 0
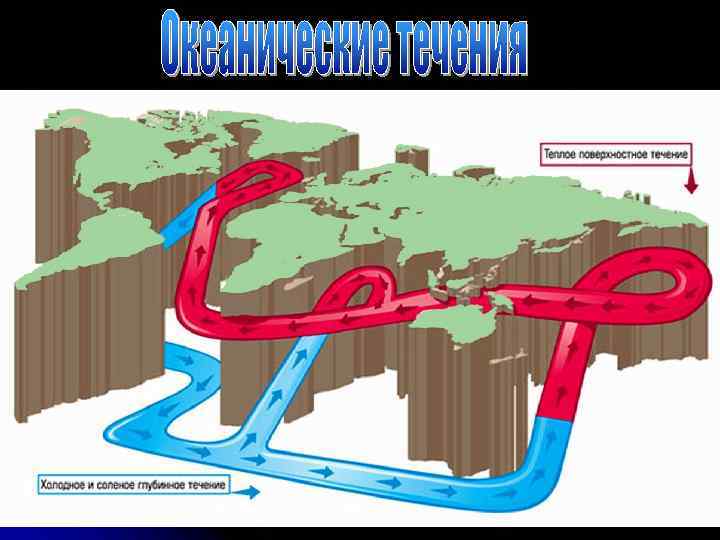
 В морской воде всегда растворены различные газы. Большая часть из них проникает в воду из атмосферы. Это подтверждается химическим родством состава газов, образующих атмосферный воздух и растворенных в морской воде, что видно из следующих данных: Содержание в объемных %: атмосфера гидросфера N 2 – 79 64 O 2 – 21 36 По насыщенности растворенным кислородом выделяются три вертикальные зоны: 1. Верхняя зона, близкая к поверхности, имеет мощность от 100 до 300 м и характеризуется наиболее высоким содержанием растворенного кислорода(8 9 мг/л в высоких широтах и 4, 3 5 мг/л – в низких). Концентрация кислорода в верхней зоне определяется соотношением процессов фотосинтеза, абсорбции, идущих с выделением кислорода и поглощением его животнымии растительными организмами, и процессами окисления. 2. Средняя зона расположена на глубинах 200 400 м и характеризуется значительно более низким содержанием кислорода (0, 4 1, 0 мг/л). 3. Глубинная зона охватывает глубины 1400 600 м, содержание кислорода в среднем составляет 5 мг/л, источником его поступления являются глубинные арктические и антарктические течения.
В морской воде всегда растворены различные газы. Большая часть из них проникает в воду из атмосферы. Это подтверждается химическим родством состава газов, образующих атмосферный воздух и растворенных в морской воде, что видно из следующих данных: Содержание в объемных %: атмосфера гидросфера N 2 – 79 64 O 2 – 21 36 По насыщенности растворенным кислородом выделяются три вертикальные зоны: 1. Верхняя зона, близкая к поверхности, имеет мощность от 100 до 300 м и характеризуется наиболее высоким содержанием растворенного кислорода(8 9 мг/л в высоких широтах и 4, 3 5 мг/л – в низких). Концентрация кислорода в верхней зоне определяется соотношением процессов фотосинтеза, абсорбции, идущих с выделением кислорода и поглощением его животнымии растительными организмами, и процессами окисления. 2. Средняя зона расположена на глубинах 200 400 м и характеризуется значительно более низким содержанием кислорода (0, 4 1, 0 мг/л). 3. Глубинная зона охватывает глубины 1400 600 м, содержание кислорода в среднем составляет 5 мг/л, источником его поступления являются глубинные арктические и антарктические течения.
 Углекислота, как и кислород, попадает в морскую воду в основном из атмосферы, проникая в толщу воды путем диффузии и захвата при волнении. Иногда углекислый газ поступает в толщу морской воды, выделяясь при извержениях вулканов непосредственно на дне моря. Наконец, он образуется в воде в результате процессов дыхания населяющих ее организмов. Количество свободной углекислоты в океане в 15– 30 раз больше, чем в атмосфере. В морской воде углекислота содержится не только в свободном виде, но и в химически связанном – в форме карбонатов и бикарбонатов. Между свободной, карбонатной и бикарбонатной углекислотой в морской воде имеется сложное подвижное равновесие, так количество бикарбонатов зависит от количества свободной СО 2, а при изменении условий часть их может перейти в карбонаты. Например, при нагревании воды может произойти реакция: 2 Nа. НСО 3 = Na 2 СО 3 + Н 2 О + СО 2. И, наоборот, при более низкой температуре карбонат натрия может вновь соединиться со свободной углекислотой, если ее достаточно в растворе, и образовать бикарбонат: Nа 2 СО 3 + СО 2 + Н 2 О = 2 Nа. НСО 3 Бикарбонат кальция Са(НСО 3)2, как соль слабой и непрочной угольной кислоты, также легко разлагается с выделением углекислого газа, воды и образованием карбоната кальция (Са. СО 3), и вновь соединяется с углекислотой.
Углекислота, как и кислород, попадает в морскую воду в основном из атмосферы, проникая в толщу воды путем диффузии и захвата при волнении. Иногда углекислый газ поступает в толщу морской воды, выделяясь при извержениях вулканов непосредственно на дне моря. Наконец, он образуется в воде в результате процессов дыхания населяющих ее организмов. Количество свободной углекислоты в океане в 15– 30 раз больше, чем в атмосфере. В морской воде углекислота содержится не только в свободном виде, но и в химически связанном – в форме карбонатов и бикарбонатов. Между свободной, карбонатной и бикарбонатной углекислотой в морской воде имеется сложное подвижное равновесие, так количество бикарбонатов зависит от количества свободной СО 2, а при изменении условий часть их может перейти в карбонаты. Например, при нагревании воды может произойти реакция: 2 Nа. НСО 3 = Na 2 СО 3 + Н 2 О + СО 2. И, наоборот, при более низкой температуре карбонат натрия может вновь соединиться со свободной углекислотой, если ее достаточно в растворе, и образовать бикарбонат: Nа 2 СО 3 + СО 2 + Н 2 О = 2 Nа. НСО 3 Бикарбонат кальция Са(НСО 3)2, как соль слабой и непрочной угольной кислоты, также легко разлагается с выделением углекислого газа, воды и образованием карбоната кальция (Са. СО 3), и вновь соединяется с углекислотой.
 Сероводорода в большинстве случаев в морской воде нет, но в глубоких слоях некоторых замкнутых морских бассейнов (Черное море) он присутствует в больших количествах. Наличие в морской воде азота и кислорода хорошо объясняется проникновением воздуха в воду, или аэрацией воды. Наличие же сероводорода требует, совершенно иного объяснения. После работ А. Д. Архангельского, установлено, что источниками сероводорода в нижней зоне Черного моря могут быть: 1) процесс восстановления сульфатов до сульфидов с помощью анаэробных бактерий; 2) восхождение этого газа с больших глубин литосферы, где он образуется в магматических очагах (ювенильный сероводород) как продукт дегазации магмы; 3) разложение остатков организмов, главным образом мелких животных и растений, плавающих в верхних слоях воды.
Сероводорода в большинстве случаев в морской воде нет, но в глубоких слоях некоторых замкнутых морских бассейнов (Черное море) он присутствует в больших количествах. Наличие в морской воде азота и кислорода хорошо объясняется проникновением воздуха в воду, или аэрацией воды. Наличие же сероводорода требует, совершенно иного объяснения. После работ А. Д. Архангельского, установлено, что источниками сероводорода в нижней зоне Черного моря могут быть: 1) процесс восстановления сульфатов до сульфидов с помощью анаэробных бактерий; 2) восхождение этого газа с больших глубин литосферы, где он образуется в магматических очагах (ювенильный сероводород) как продукт дегазации магмы; 3) разложение остатков организмов, главным образом мелких животных и растений, плавающих в верхних слоях воды.
 В морской воде присутствуют разнообразные микроэлементы, концентрации которых по абсолютным значениям невелики, однакс общее их содержание весьма значительно. Наибольшие концентрации отмечены для таких элементов, как литий (200 мкг/л), рубидий (120 мкг/л), иод (60 мг/л), барий (30 мкг/л). Концентрация водородных ионов (р. Н) в океанической воде характеризуется незначительным диапазоном колебаний (7, 9 8, 3). Наибольшие ее величины (8, 0 8, 35) характерны для поверхностных слоев океана, что обусловлено интенсивным потреблением СО 2 при фотосинтезе. Установлено, что увеличение количества диатомовых водорослей сопровождается повышением р. Н. С возрастанием глубины р. Н уменьшается
В морской воде присутствуют разнообразные микроэлементы, концентрации которых по абсолютным значениям невелики, однакс общее их содержание весьма значительно. Наибольшие концентрации отмечены для таких элементов, как литий (200 мкг/л), рубидий (120 мкг/л), иод (60 мг/л), барий (30 мкг/л). Концентрация водородных ионов (р. Н) в океанической воде характеризуется незначительным диапазоном колебаний (7, 9 8, 3). Наибольшие ее величины (8, 0 8, 35) характерны для поверхностных слоев океана, что обусловлено интенсивным потреблением СО 2 при фотосинтезе. Установлено, что увеличение количества диатомовых водорослей сопровождается повышением р. Н. С возрастанием глубины р. Н уменьшается

 Реки являются наиболее подвижной частью гидросферы, характеризующейся легкой изменчивостью химического состава вод в зависимости от целого ряда причин: климатические и погодные условия, соотношение между атмосферным и грунтовым питанием, химический состав атмосферных вод, геологическое строение, состав пород водосборной площадки и т. д. Схема баланса растворенных веществ водосбора по О. А. Алёкину Ппочв + Ппор + Патм + Пэол + Порг = Ри + Рэол + Рраст + Х. В данной схеме левая часть равенства представляет собой сумму поступлений растворенных веществ на территорию речного бассейна. Ппочв – почвенные растворы и сухие соли почв; Ппор – вещества, выносимые из пород; Патм – атмосферные осадки; Пэол – вещества, переносимые ветром; Порг – вещества, образующиеся при минерализации или гумификации органических остатков. Одновременно происходит убыль растворенных веществ, представленная в правой части равенства Ри – ионный вынос речными водами; Рэол – вынос веществ с поверхности вод ветром; Рраст – поглощение растворенных веществ растительностью; X – увеличение или убыль растворенных веществ в бассейне.
Реки являются наиболее подвижной частью гидросферы, характеризующейся легкой изменчивостью химического состава вод в зависимости от целого ряда причин: климатические и погодные условия, соотношение между атмосферным и грунтовым питанием, химический состав атмосферных вод, геологическое строение, состав пород водосборной площадки и т. д. Схема баланса растворенных веществ водосбора по О. А. Алёкину Ппочв + Ппор + Патм + Пэол + Порг = Ри + Рэол + Рраст + Х. В данной схеме левая часть равенства представляет собой сумму поступлений растворенных веществ на территорию речного бассейна. Ппочв – почвенные растворы и сухие соли почв; Ппор – вещества, выносимые из пород; Патм – атмосферные осадки; Пэол – вещества, переносимые ветром; Порг – вещества, образующиеся при минерализации или гумификации органических остатков. Одновременно происходит убыль растворенных веществ, представленная в правой части равенства Ри – ионный вынос речными водами; Рэол – вынос веществ с поверхности вод ветром; Рраст – поглощение растворенных веществ растительностью; X – увеличение или убыль растворенных веществ в бассейне.
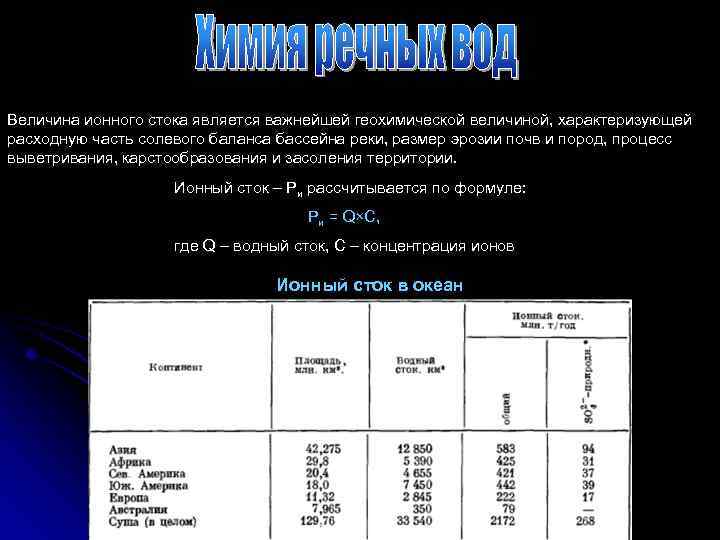 Величина ионного стока является важнейшей геохимической величиной, характеризующей расходную часть солевого баланса бассейна реки, размер эрозии почв и пород, процесс выветривания, карстообразования и засоления территории. Ионный сток – Ри рассчитывается по формуле: Ри = Q×C, где Q – водный сток, С – концентрация ионов Ионный сток в океан
Величина ионного стока является важнейшей геохимической величиной, характеризующей расходную часть солевого баланса бассейна реки, размер эрозии почв и пород, процесс выветривания, карстообразования и засоления территории. Ионный сток – Ри рассчитывается по формуле: Ри = Q×C, где Q – водный сток, С – концентрация ионов Ионный сток в океан
 Все разнообразие речных вод можно представить в виде отдельных групп, характеризующихся водами, близкими по величине общей минерализации и составу основных компонентов. По величине минерализации выделяются следующие группы: 1) малая минерализация (до 200 мг/л); 2) средняя минерализация (200– 500 мг/л); 3) повышенная минерализация (500– 1000 мг/л); 3) высокая минерализация (>1000 мг/л). По составу основных ионов выделяются реки с преобладающими водами одного из трех названных выше классов: 1) гидрокарбонатного, 2) сульфатного, 3) хлоридного, а также реки определенной группы катионного состава – кальциевой, магниевой, натриевой
Все разнообразие речных вод можно представить в виде отдельных групп, характеризующихся водами, близкими по величине общей минерализации и составу основных компонентов. По величине минерализации выделяются следующие группы: 1) малая минерализация (до 200 мг/л); 2) средняя минерализация (200– 500 мг/л); 3) повышенная минерализация (500– 1000 мг/л); 3) высокая минерализация (>1000 мг/л). По составу основных ионов выделяются реки с преобладающими водами одного из трех названных выше классов: 1) гидрокарбонатного, 2) сульфатного, 3) хлоридного, а также реки определенной группы катионного состава – кальциевой, магниевой, натриевой
 Бассейны рек с гидрокарбонатным классом вод занимают около 83% территории России. По катионному составу это преимущественно воды кальциевой группы. В большинстве это воды малой минерализации. Гидрокарбонатные воды средней минерализации имеют меньшее распространение. Наиболее редки гидрокарбонатные воды с минерализацией более 1000 мг/л. Зона развития сульфатных вод на земном шаре имеет гораздо меньшее распространение. Она приурочена к районам слабого и неустойчивого увлажнения. На территории России эта зона расположена на юге европейской части и Западной Сибири и совпадает с районами распространения степей и частично полупустынь. Наиболее характерна для этих рек повышенная, а иногда высокая минерализация. Зона распространения рек с водами хлоридного класса занимает еще меньшую площадь. В России она составляет около 7% площади всех бассейнов – это преимущественно степные районы и полупустыни. Преобладающими катионами в водах хлоридного класса являются ионы натрия. Минерализация этих вод, как правило, высока, обычно выше 1000 мг/л, реже от 500 до 1000 мг/л.
Бассейны рек с гидрокарбонатным классом вод занимают около 83% территории России. По катионному составу это преимущественно воды кальциевой группы. В большинстве это воды малой минерализации. Гидрокарбонатные воды средней минерализации имеют меньшее распространение. Наиболее редки гидрокарбонатные воды с минерализацией более 1000 мг/л. Зона развития сульфатных вод на земном шаре имеет гораздо меньшее распространение. Она приурочена к районам слабого и неустойчивого увлажнения. На территории России эта зона расположена на юге европейской части и Западной Сибири и совпадает с районами распространения степей и частично полупустынь. Наиболее характерна для этих рек повышенная, а иногда высокая минерализация. Зона распространения рек с водами хлоридного класса занимает еще меньшую площадь. В России она составляет около 7% площади всех бассейнов – это преимущественно степные районы и полупустыни. Преобладающими катионами в водах хлоридного класса являются ионы натрия. Минерализация этих вод, как правило, высока, обычно выше 1000 мг/л, реже от 500 до 1000 мг/л.
 Концентрация микроэлементов в водах определяется целым рядом факторов, таких как: 1) низкое содержание микроэлементов в породах литосферы; 2) низкая растворимость природных минералов, содержащих эти элементы; 3) влияние ионного состава воды (особенно величин р. Н и Eh) на устойчивость химических элементов в природных растворах; 4) адсорбция различными сорбентами; 5) извлечение элементов из вод бактериями и живыми организмами. Растворимость природных минералов Pb и Cu в водных растворах различного хим. состава
Концентрация микроэлементов в водах определяется целым рядом факторов, таких как: 1) низкое содержание микроэлементов в породах литосферы; 2) низкая растворимость природных минералов, содержащих эти элементы; 3) влияние ионного состава воды (особенно величин р. Н и Eh) на устойчивость химических элементов в природных растворах; 4) адсорбция различными сорбентами; 5) извлечение элементов из вод бактериями и живыми организмами. Растворимость природных минералов Pb и Cu в водных растворах различного хим. состава

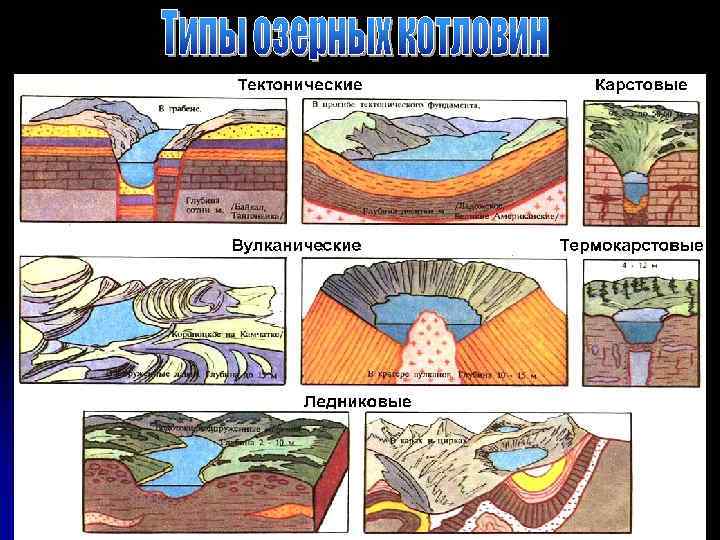
 Озера по сравнению с реками имеют очень замедленный водообмен, поэтому при формировании их химического состава даже в сходных с реками климатических и геохимических условиях между ними наблюдаются значительные различия. По степени минерализации принято различать озера пресные, солоноватые и соленые. Общая минерализация пресных озер составляет <1 г/л. Они формируются в условиях избыточного и достаточного увлажнения и имеют постоянный в течение года сток. Соляные озера характеризуются общей минерализацией воды свыше 25 г/л. Они формируются в районах с засушливым климатом, в условиях высокого испарения с поверхности, весьма незначительного стока или полного его отсутствия. Это приводит к накоплению в воде озера различных солей, поступающих с притоками. Солоноватые озера характерны для районов недостаточного увлажнения. Они имеют сток в отдельные сезоны года, при этом в системе приток – озеро – сток устанавливается некоторое равновесие, определяющее минерализацию воды в озере. Величина минерализации солоноватых озер колеблется в пределах 1 25 г/л.
Озера по сравнению с реками имеют очень замедленный водообмен, поэтому при формировании их химического состава даже в сходных с реками климатических и геохимических условиях между ними наблюдаются значительные различия. По степени минерализации принято различать озера пресные, солоноватые и соленые. Общая минерализация пресных озер составляет <1 г/л. Они формируются в условиях избыточного и достаточного увлажнения и имеют постоянный в течение года сток. Соляные озера характеризуются общей минерализацией воды свыше 25 г/л. Они формируются в районах с засушливым климатом, в условиях высокого испарения с поверхности, весьма незначительного стока или полного его отсутствия. Это приводит к накоплению в воде озера различных солей, поступающих с притоками. Солоноватые озера характерны для районов недостаточного увлажнения. Они имеют сток в отдельные сезоны года, при этом в системе приток – озеро – сток устанавливается некоторое равновесие, определяющее минерализацию воды в озере. Величина минерализации солоноватых озер колеблется в пределах 1 25 г/л.
 Основными ионами, характеризующими химический состав озерной воды, являются как и для всех природных вод, HCO 3+, SO 42 , Cl , Са 2+, Mg 2+, Na+ и К+. Основной состав вод формируется в результате подвижного равновесия между приходными и расходными составляющими солевого баланса: Sпр + Sатм. ос + Sгр = Sст + Sэол + Sфил + Sос, где Snp – соли, вносимые притоками; Sатм. ос – соли, вносимые атмосферными осадками и пылью; Sпр – соли, вносимые грунтовыми водами; Sст – соли, выносимые стоками; Sэол – соли, выносимые ветром; Sфил – соли, теряемые при фильтрации; Sос – соли, выпадающие в осадок. В изменении состава озерных вод наблюдается та же закономерность, что и в речных водах – с ростом минерализации наблюдается относительный рост ионов в следующей последовательности: HCO 3 → SO 42 → Cl ; Ca 2+ → Mg 2+ → Na+
Основными ионами, характеризующими химический состав озерной воды, являются как и для всех природных вод, HCO 3+, SO 42 , Cl , Са 2+, Mg 2+, Na+ и К+. Основной состав вод формируется в результате подвижного равновесия между приходными и расходными составляющими солевого баланса: Sпр + Sатм. ос + Sгр = Sст + Sэол + Sфил + Sос, где Snp – соли, вносимые притоками; Sатм. ос – соли, вносимые атмосферными осадками и пылью; Sпр – соли, вносимые грунтовыми водами; Sст – соли, выносимые стоками; Sэол – соли, выносимые ветром; Sфил – соли, теряемые при фильтрации; Sос – соли, выпадающие в осадок. В изменении состава озерных вод наблюдается та же закономерность, что и в речных водах – с ростом минерализации наблюдается относительный рост ионов в следующей последовательности: HCO 3 → SO 42 → Cl ; Ca 2+ → Mg 2+ → Na+
 В пресных озерах преобладают гидрокарбонатные ионы (4 600 мг/л), второе место занимает сульфат ион (2 40 мг/л), содержание хлор иона колеблется в пределах 1 60 мг/л. Из катионов преобладает Са 2+ (2 140 мг/л), содержание иона магния изменяется от 2 до 60 мг/л. Типы соляных озер
В пресных озерах преобладают гидрокарбонатные ионы (4 600 мг/л), второе место занимает сульфат ион (2 40 мг/л), содержание хлор иона колеблется в пределах 1 60 мг/л. Из катионов преобладает Са 2+ (2 140 мг/л), содержание иона магния изменяется от 2 до 60 мг/л. Типы соляных озер

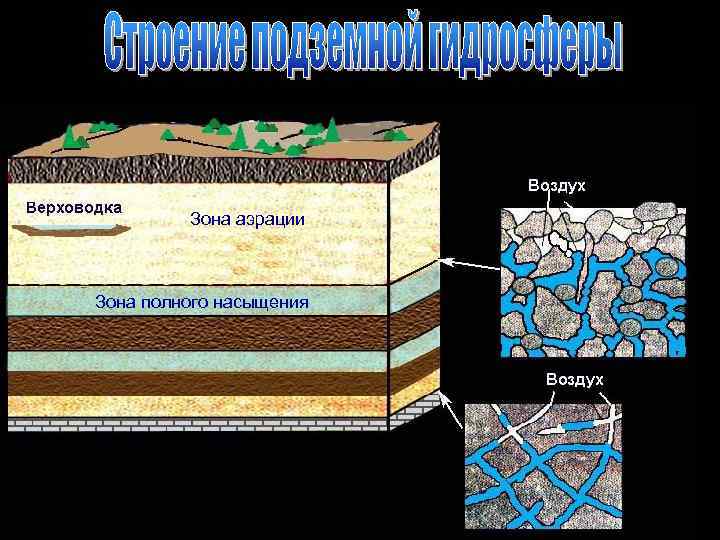 Зона аэрации Зона полного насыщения
Зона аэрации Зона полного насыщения
 Одно и многоатомные ионы высококларковых элементов, обладающие наибольшей растворимостью – анионы: Cl , SО 42 , НСО 3 , СО 32 , катионы: Na+, Mg 2+, Са 2+, К+, а также кремнекислота H 4 Si. О 4, которая присутствует в подземных водах в молекулярной форме относятся к группе макрокомпонентов. В меньших количествах (обычно первые мг/дм 3) присутствуют в химическом составе воды, такие ионы, как NH 4+, Fe 2+, Fe 3+, NO 2 , которые называют мезокомпонентами. Минерализация (г/дм 3, г/кг, ) – суммарная масса растворенных твердых минеральных веществ в единице объема или массы воды. Сумма ионов – то же, но чаще в мольном (эквивалентном) выражении, вычисляется суммированием ммоль/дм 3 (мг экв/л) веществ, определенных химическим анализом. Сухой остаток – масса нелетучих (при 110 или 180°С) минеральных и органических соединений, отнесенная к единице объема – определяется взвешиванием осадка, полученного при выпаривании и последующем высушивании определенного объема воды
Одно и многоатомные ионы высококларковых элементов, обладающие наибольшей растворимостью – анионы: Cl , SО 42 , НСО 3 , СО 32 , катионы: Na+, Mg 2+, Са 2+, К+, а также кремнекислота H 4 Si. О 4, которая присутствует в подземных водах в молекулярной форме относятся к группе макрокомпонентов. В меньших количествах (обычно первые мг/дм 3) присутствуют в химическом составе воды, такие ионы, как NH 4+, Fe 2+, Fe 3+, NO 2 , которые называют мезокомпонентами. Минерализация (г/дм 3, г/кг, ) – суммарная масса растворенных твердых минеральных веществ в единице объема или массы воды. Сумма ионов – то же, но чаще в мольном (эквивалентном) выражении, вычисляется суммированием ммоль/дм 3 (мг экв/л) веществ, определенных химическим анализом. Сухой остаток – масса нелетучих (при 110 или 180°С) минеральных и органических соединений, отнесенная к единице объема – определяется взвешиванием осадка, полученного при выпаривании и последующем высушивании определенного объема воды
 Водородный показатель (р. Н) дает представление об общем щелочно кислотном состоянии воды и является одной из важнейших интегральных характеристик. От щелочно кислотного состояния воды зависят многие гидрохимические процессы: осаждение и растворение, миграционная способность, характер микрофлоры и т. д. Водородный показатель представляет десятичный логарифм концентрации водородных ионов, взятый с обратным знаком: p. H = – lg[H +] Окислительно восстановительный потенциал (Eh) воды характеризует соотношение окисленных и восстановленных форм всех содержащихся в ней элементов переменной валентности и является важнейшей характеристикой состава воды. Из таких элементов для химического состава подземных вод наибольшее значение имеют: S ( 2, +4, +6), Fe (+2, +3), N ( 3, +5), Mn (+2, +3, +4), P (+3, +5) и др. Жесткость воды обусловлена наличием в ней соединений кальция и магния. Различают 5 видов жесткости: общую, карбонатную, некарбонатную, устранимую (временную), неустранимую (постоянную). Количественной мерой общей жесткости является сумма миллиграмм эквивалентов кальция и магния в единице объема.
Водородный показатель (р. Н) дает представление об общем щелочно кислотном состоянии воды и является одной из важнейших интегральных характеристик. От щелочно кислотного состояния воды зависят многие гидрохимические процессы: осаждение и растворение, миграционная способность, характер микрофлоры и т. д. Водородный показатель представляет десятичный логарифм концентрации водородных ионов, взятый с обратным знаком: p. H = – lg[H +] Окислительно восстановительный потенциал (Eh) воды характеризует соотношение окисленных и восстановленных форм всех содержащихся в ней элементов переменной валентности и является важнейшей характеристикой состава воды. Из таких элементов для химического состава подземных вод наибольшее значение имеют: S ( 2, +4, +6), Fe (+2, +3), N ( 3, +5), Mn (+2, +3, +4), P (+3, +5) и др. Жесткость воды обусловлена наличием в ней соединений кальция и магния. Различают 5 видов жесткости: общую, карбонатную, некарбонатную, устранимую (временную), неустранимую (постоянную). Количественной мерой общей жесткости является сумма миллиграмм эквивалентов кальция и магния в единице объема.
 Основными ингредиентами химического состава подземных водявляются: 1) растворенные минеральные вещества; 2) органические вещества; 3) газы; 4) изотопы; 5) антропогенные компоненты загрязнители. Растворенные минеральные вещества в первую очередь представлены макрокомпонентами: хлор ионом, сульфат ионом, натрий ионом, калий ионом, магний ионом и кремнекислотой. Хлор ион участвует в процессах седиментации и галогенеза, является основным анионом седиментационных вод артезианских бассейнов и вод, формирующихся в результате растворения соляных толщ и засоленных пород. Огромные количества хлора поступают в подземную гидросферу с бытовыми и промышленными стоками. Содержание хлора в подземных водах характеризуется максимальным разбросом – от тысячных долей г/дм 3 до 340 360 г/дм 3 в рассолах.
Основными ингредиентами химического состава подземных водявляются: 1) растворенные минеральные вещества; 2) органические вещества; 3) газы; 4) изотопы; 5) антропогенные компоненты загрязнители. Растворенные минеральные вещества в первую очередь представлены макрокомпонентами: хлор ионом, сульфат ионом, натрий ионом, калий ионом, магний ионом и кремнекислотой. Хлор ион участвует в процессах седиментации и галогенеза, является основным анионом седиментационных вод артезианских бассейнов и вод, формирующихся в результате растворения соляных толщ и засоленных пород. Огромные количества хлора поступают в подземную гидросферу с бытовыми и промышленными стоками. Содержание хлора в подземных водах характеризуется максимальным разбросом – от тысячных долей г/дм 3 до 340 360 г/дм 3 в рассолах.
 Сульфат ион поступает в подземные воды при растворении сульфатсодержащих минералов гипса (Ca. SO 4 2 H 2 O), ангидрита (Ca. SO 4) и др. Содержание сульфат иона в подземных водах изменяется от первых мг/дм 3 до нескольких десятков г/дм 3. Гидрокарбонат ионы, свободная углекислота представляет так называемую систему компонентов карбонатного равновесия: СО 3 (газ) + Н 2 О Н 2 СО 3 Н+ + НСО 3 2 Н+ + CO 32 Компоненты карбонатной системы поступают в подземные воды при растворении с участием углекислоты атмосферного, биохимического, термометаморфического генезиса слаборастворимых карбонатных минералов – кальцита (Са. СО 3) и доломита (Са. Мg(СО 3)2). Натрий ион, как и хлор прекрасно мигрирует и накапливается в подземных водах, в том числе в рассолах. Содержание натрия в питьевых водах не должно превышать 0, 2 г/дм 3. Калий ион, в отличие от натрия, активно участвует в биохимических процессах, легко сорбируется, быстро связывается в труднорастворимые соединения в коре выветривания, захватываясь кристаллической решеткой глинистых минералов. Поэтому, его содержание в верхней части гидрогеологического разреза, незначительно.
Сульфат ион поступает в подземные воды при растворении сульфатсодержащих минералов гипса (Ca. SO 4 2 H 2 O), ангидрита (Ca. SO 4) и др. Содержание сульфат иона в подземных водах изменяется от первых мг/дм 3 до нескольких десятков г/дм 3. Гидрокарбонат ионы, свободная углекислота представляет так называемую систему компонентов карбонатного равновесия: СО 3 (газ) + Н 2 О Н 2 СО 3 Н+ + НСО 3 2 Н+ + CO 32 Компоненты карбонатной системы поступают в подземные воды при растворении с участием углекислоты атмосферного, биохимического, термометаморфического генезиса слаборастворимых карбонатных минералов – кальцита (Са. СО 3) и доломита (Са. Мg(СО 3)2). Натрий ион, как и хлор прекрасно мигрирует и накапливается в подземных водах, в том числе в рассолах. Содержание натрия в питьевых водах не должно превышать 0, 2 г/дм 3. Калий ион, в отличие от натрия, активно участвует в биохимических процессах, легко сорбируется, быстро связывается в труднорастворимые соединения в коре выветривания, захватываясь кристаллической решеткой глинистых минералов. Поэтому, его содержание в верхней части гидрогеологического разреза, незначительно.
 Кальций ион поступает в воды при растворении кальцита, доломита, гипса, разрушении плагиоклазов. Он участвует в биохимических процессах и хорошо сорбируется. В связи с этим он может преобладать в катионном составе гидрокарбонатных подземных грунтовых вод при содержании до 0, 4 г/дм 3. Магний ион в подземных водах очень редко является преобладающим, он характеризуется слабой миграционной способностью. Природные карбонаты магния (доломит, магнезит) малораствори мы, в связи с чем магний, наряду с кальцием, может являться одним из основных компонентов состава слабоминерализованных грунтовых вод гидрокарбонатного состава. В рассолах содержание магния не превышает нескольких десятков г/дм 3. Наиболее распространенными газами в подземных водах являются кислород (О 2), углекислота (СО 2), сероводород (Н 2 S), водород (Н 2), метан (СН 4), тяжелые углеводороды, азот (N 2) и благородные газы. Газы в подземных водах находятся как в растворенном состоянии, так и в свободном виде. При уменьшении давления растворенные газы могут переходить в свободные.
Кальций ион поступает в воды при растворении кальцита, доломита, гипса, разрушении плагиоклазов. Он участвует в биохимических процессах и хорошо сорбируется. В связи с этим он может преобладать в катионном составе гидрокарбонатных подземных грунтовых вод при содержании до 0, 4 г/дм 3. Магний ион в подземных водах очень редко является преобладающим, он характеризуется слабой миграционной способностью. Природные карбонаты магния (доломит, магнезит) малораствори мы, в связи с чем магний, наряду с кальцием, может являться одним из основных компонентов состава слабоминерализованных грунтовых вод гидрокарбонатного состава. В рассолах содержание магния не превышает нескольких десятков г/дм 3. Наиболее распространенными газами в подземных водах являются кислород (О 2), углекислота (СО 2), сероводород (Н 2 S), водород (Н 2), метан (СН 4), тяжелые углеводороды, азот (N 2) и благородные газы. Газы в подземных водах находятся как в растворенном состоянии, так и в свободном виде. При уменьшении давления растворенные газы могут переходить в свободные.
 Для установления генезиса и условий формирования подземных вод важное значение придается коэффициентам пропорциональности: r. Nа/r. Сl, Сl/Вr, Са/Sr, Вr/I и некоторым другим. Причем, при вычислении отношения Na/Cl, натрий и хлор берутся в мг экв, на что указывает индекс r; для определения остальных коэффициентов пропорциональности элементы берутся в мг/л. : При сопоставлении коэффициентов пропорциональности, за исходные берутся отношения, свойственные для вод океана. Для океанической воды отношения равны:
Для установления генезиса и условий формирования подземных вод важное значение придается коэффициентам пропорциональности: r. Nа/r. Сl, Сl/Вr, Са/Sr, Вr/I и некоторым другим. Причем, при вычислении отношения Na/Cl, натрий и хлор берутся в мг экв, на что указывает индекс r; для определения остальных коэффициентов пропорциональности элементы берутся в мг/л. : При сопоставлении коэффициентов пропорциональности, за исходные берутся отношения, свойственные для вод океана. Для океанической воды отношения равны:
 В водах выщелачивания атмосферного генезиса обычно r. Na/r. Cl изменяется в пределах от 1 до 2; Сl/Br > 300, в том числе и при разрушении залежей каменной соли, а также и для вод внутриконтинентальных морей (для вод Аральского моря отношение Сl/Br изменяется от 2071 до 2187); Са/Sr 200. В седиментационных водах морского генезиса отношение r. Nа/r. Сl < 0, 85; Сl/Br < 300; Са/Sr 33.
В водах выщелачивания атмосферного генезиса обычно r. Na/r. Cl изменяется в пределах от 1 до 2; Сl/Br > 300, в том числе и при разрушении залежей каменной соли, а также и для вод внутриконтинентальных морей (для вод Аральского моря отношение Сl/Br изменяется от 2071 до 2187); Са/Sr 200. В седиментационных водах морского генезиса отношение r. Nа/r. Сl < 0, 85; Сl/Br < 300; Са/Sr 33.


