карбоновые кислоты.ppt
- Количество слайдов: 12


v v Карбоновыми кислотами называются производные углеводородов, в молекуле которых содержится одна или несколько карбоксильных групп –COOH. Общая формула карбоновых кислот: В зависимости от природы радикала, связанного с карбоксильной группой, кислоты подразделяются на предельные, непредельные и ароматические. Число карбоксильных групп определяет основность кислот. Общая формула предельных одноосновных кислот: Сn. H 2 n+1 COOH (или Сn. H 2 n. O 2).

Модели молекул Уксусная кислота Муравьиная кислота

Номенклатура v v v v v Распространены тривиальные названия. По правилам IUPAC к названию углеводорода добавляют "- овая кислота". HCOOH – муравьиная кислота CH 3 COOH – уксусная кислота CH 3 CH 2 COOH – пропионовая кислота CH 3(CH 2)2 COOH – масляная кислота CH 3(CH 2)3 COOH – валериановая кислота CH 3(CH 2)4 COOH – капроновая кислота C 6 H 5 COOH – бензойная кислота CH 3(CH 2)14 COOH – пальмитиновая кислота CH 3(CH 2)16 COOH – стеариновая кислота

Изомерия. v v v Для алифатических кислот - изомеризация углеводородного радикала. Для ароматических - изомерия положения заместителя при бензольном кольце. Межклассовая изомерия со сложными эфирами (например, CH 3 -COOH и HCOO-CH 3).

Физические свойства v С 1 - С 3 жидкости с характерным резким запахом v v С 4 - С 9 вязкие маслянистые жидкости с неприятным запахом С С 10 твердые нерастворимые вещества Карбоновые кислоты имеют аномально высокие температуры кипения из-за наличия межмолекулярных водородных связей и существуют в основном в виде димеров. С ростом относительной молекулярной массы температура кипения предельных одноосновных кислот увеличивается

Получение v v v v Окисление первичных спиртов и альдегидов (кислородом на катализаторе; KMn. O 4; K 2 Cr 2 O 7): R-CH 2 OH → RCOOH каталитическое окисление метана: 2 CH 4 + 3 O 2 → 2 H–COOH + 2 H 2 O каталитическое окисление бутана: 2 CH 3–CH 2–CH 3 + 5 O 2 → 4 CH 3 COOH + 2 H 2 O Ароматические кислоты синтезируют окислением гомологов бензола: в качестве окислителя можно использовать растворы KMn. O 4 или K 2 Cr 2 O 7 в кислой среде: 5 C 6 H 5 CH 3 + 6 KMn. O 4 + 9 H 2 SO 4 → 5 C 6 H 5 COOH + 3 K 2 SO 4 + 6 Mn. SO 4 + 14 H 2 O

Химические свойства v v Карбоновые кислоты- слабые электролиты, в водном растворе диссоциируют: R–COOH R–COO- + H+ Карбоновые кислоты обладают свойствами, характерными для минеральных кислот. Они реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот. Взаимодействие с металлами: 2 СH 3 COOH + Mg → (CH 3 COO)2 Mg + H 2 v Взаимодействие с основными оксидами: 2 СH 3 COOH + Сa. O → (CH 3 COO)2 Ca + H 2 O v Взаимодействие с основаниями: H–COOH + Na. OH → H–COONa + H 2 O

v Взаимодействие с солями более слабых и летучих кислот: v 2 СH 3 CH 2 COOH + Na 2 CO 3 → 2 CH 3 CH 2 COONa + H 2 O + CO 2 Взаимодействие со спиртами: CH 3 COOH+ C 2 H 5 OH CH 3 COOC 2 H 5 + H 2 O Взаимодействие с галогенами: v CH 3 COOH + Cl 2 → Cl. CH 2 COOH + HCl v v v Раствор муравьиной кислоты, в отличие от других карбоновых кислот дает реакцию «серебряного зеркала» HCOOH + Ag 2 O → CO 2+ H 2 O

Применение v Муравьиная кислота – в медицине, в пчеловодстве, в v Уксусная кислота – в пищевой и химической промышленности v Масляная кислота – для получения ароматизирующих добавок, v v органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя. (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). пластификаторов и флотореагентов. Щавелевая кислота – в металлургической промышленности (удаление окалины). Стеариновая C 17 H 35 COOH и пальмитиновая кислота C 15 H 31 COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.

Какие вещества образуются, если в реакцию вступят вещества, модели молекул которых изображены на рисунке? составьте уравнение химической реакции.
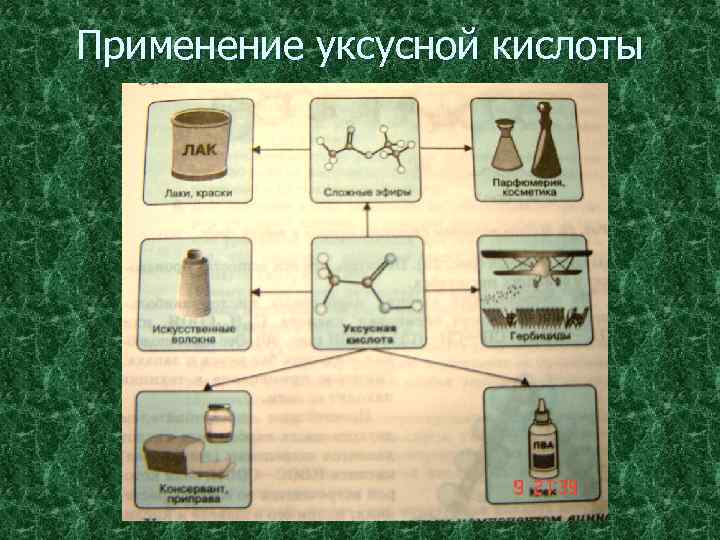
Применение уксусной кислоты
карбоновые кислоты.ppt