В-клеточный иммунный ответ Габибов А.Г. Лекция 3 Динамика

В-клеточный иммунный ответ Габибов А.Г. Лекция 3
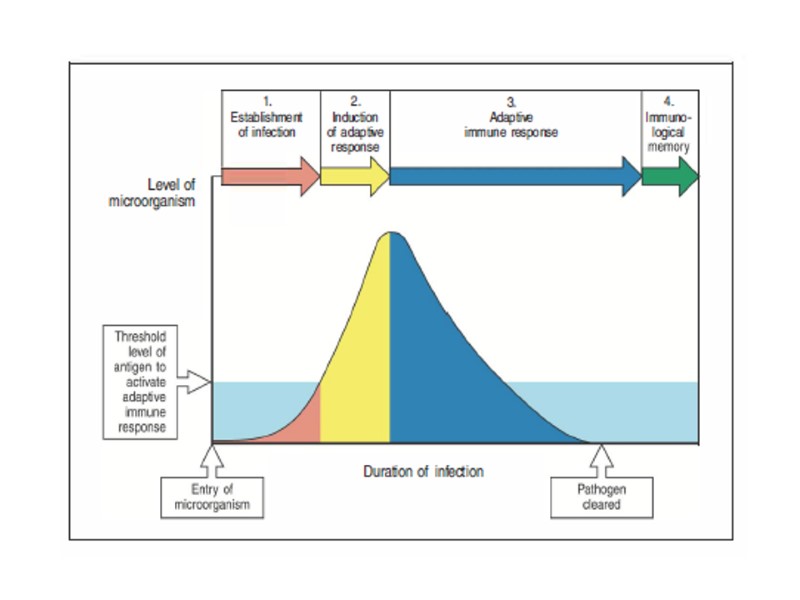
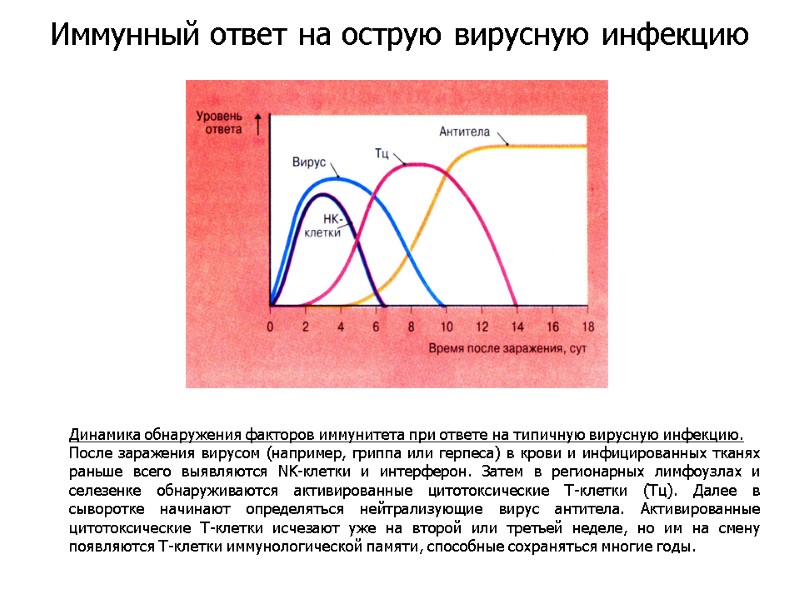
Динамика обнаружения факторов иммунитета при ответе на типичную вирусную инфекцию. После заражения вирусом (например, гриппа или герпеса) в крови и инфицированных тканях раньше всего выявляются NK-клетки и интерферон. Затем в регионарных лимфоузлах и селезенке обнаруживаются активированные цитотоксические Т-клетки (Тц). Далее в сыворотке начинают определяться нейтрализующие вирус антитела. Активированные цитотоксические Т-клетки исчезают уже на второй или третьей неделе, но им на смену появляются Т-клетки иммунологической памяти, способные сохраняться многие годы. Иммунный ответ на острую вирусную инфекцию
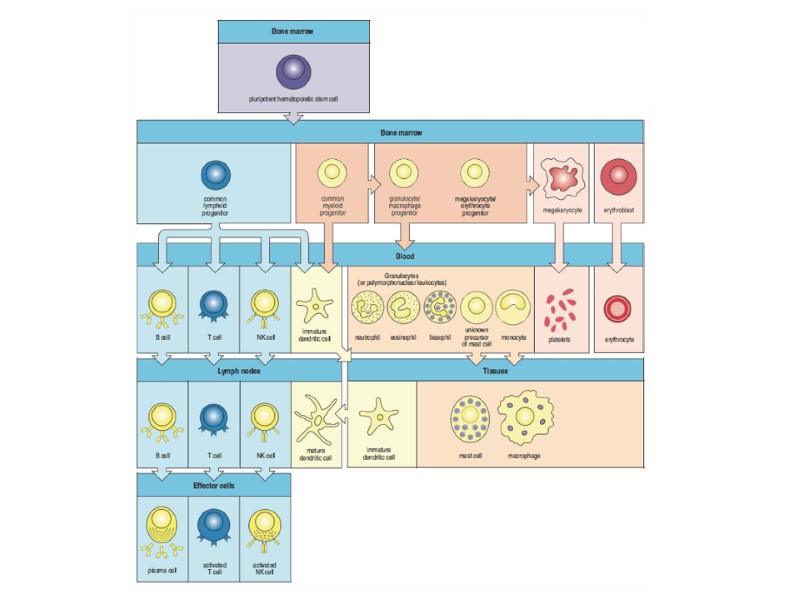
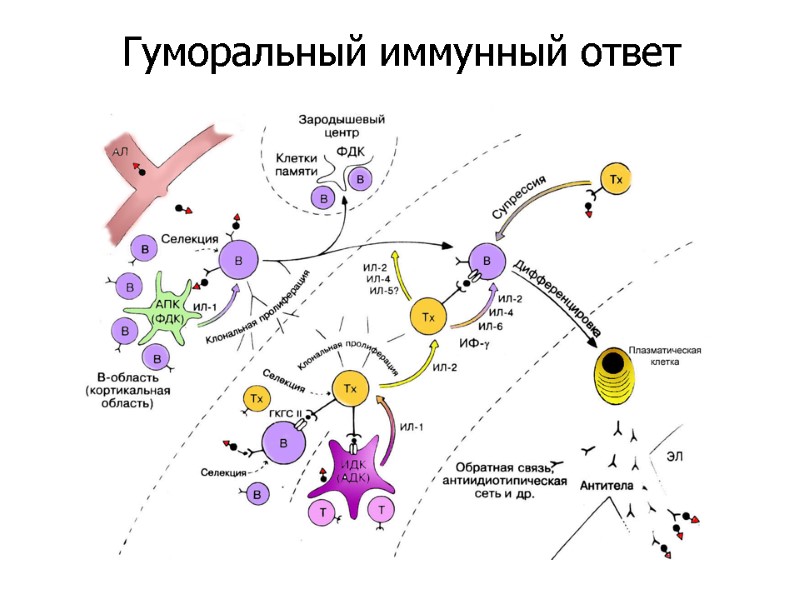
Гуморальный иммунный ответ

Гуморальный иммунный ответ, вызванный первичной антигенной стимуляцией, протекает в 4 фазы. Лаг-фаза, в течение которой антитела в сыворотке крови не обнаруживаются. Лог-фаза, в течение которой титр антител нарастает логарифмически. Фаза плато – стадия стабилизации титра антител. Фаза затухания ответа, во время которой происходит выведение или атаболизирование иммуноглобулинов. Временные соотношения между фазами и уровень продуцируемых антител зависят от природы антигенного стимула и особенностей организма. Четыре фазы первичного гуморального ответа
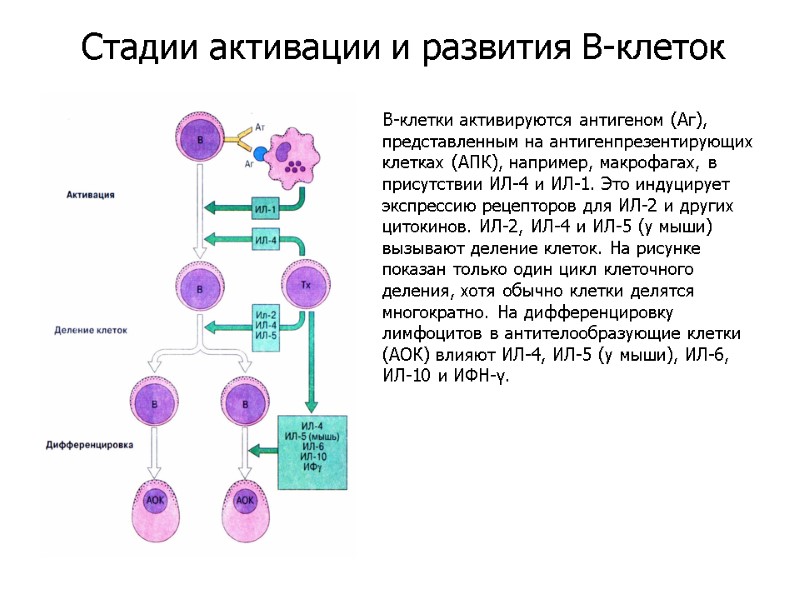
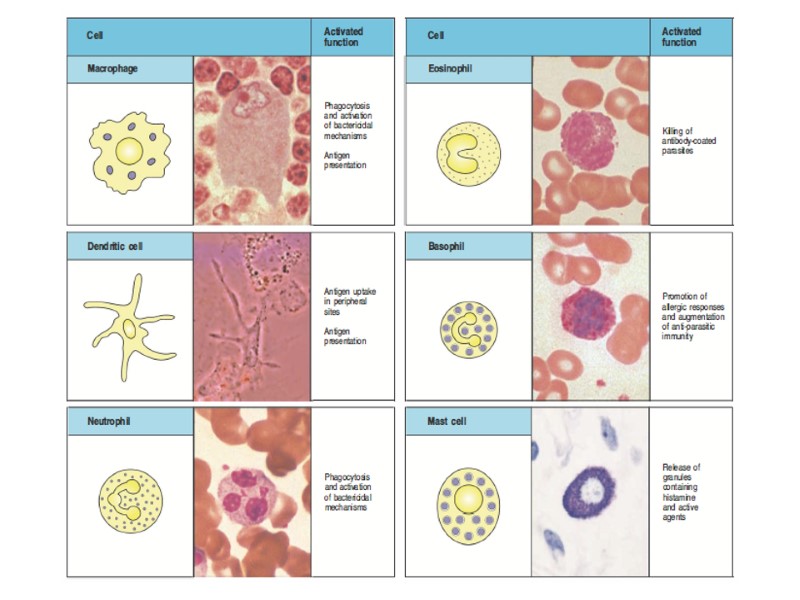
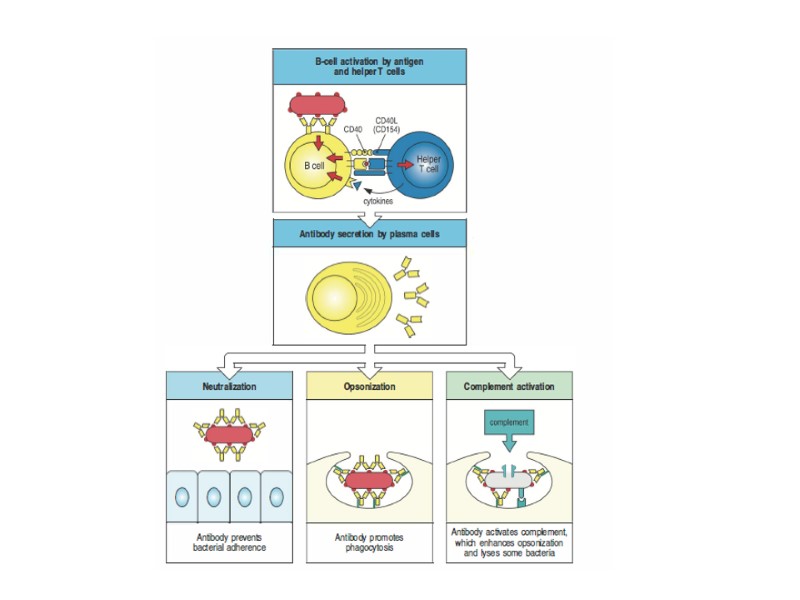
В-клетки активируются антигеном (Аг), представленным на антигенпрезентирующих клетках (АПК), например, макрофагах, в присутствии ИЛ-4 и ИЛ-1. Это индуцирует экспрессию рецепторов для ИЛ-2 и других цитокинов. ИЛ-2, ИЛ-4 и ИЛ-5 (у мыши) вызывают деление клеток. На рисунке показан только один цикл клеточного деления, хотя обычно клетки делятся многократно. На дифференцировку лимфоцитов в антителообразующие клетки (АОК) влияют ИЛ-4, ИЛ-5 (у мыши), ИЛ-6, ИЛ-10 и ИФН-γ. Стадии активации и развития В-клеток

Антиген-презентирующие клетки (АПК), например дендритные клетки, презентируют антиген непримированным Т-лимфоцитам. В-лимфоциты также связывают антиген и презентируют его Т-клеткам, получая от них сигнал к делению и дифференцировке в антителообразующие клетки (АОК) и В-клетки иммунологической памяти (Вп). Кооперация клеток при образовании антител
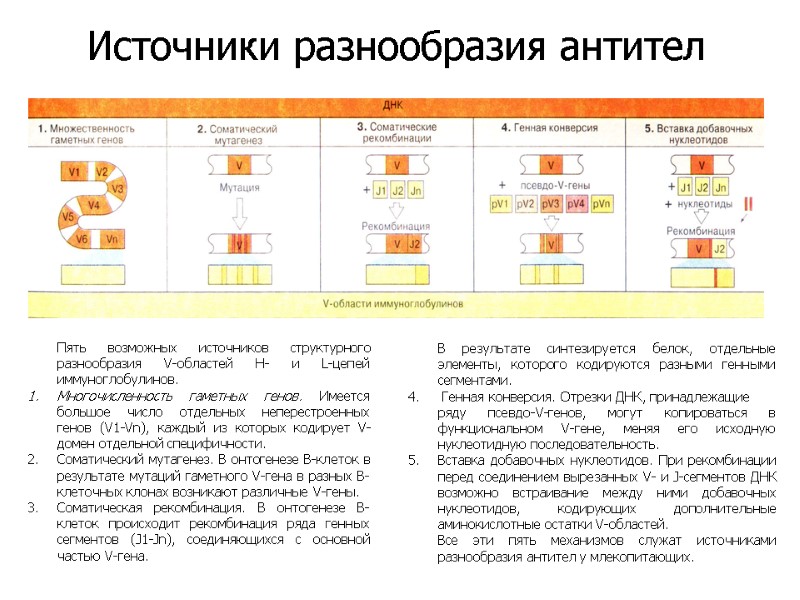
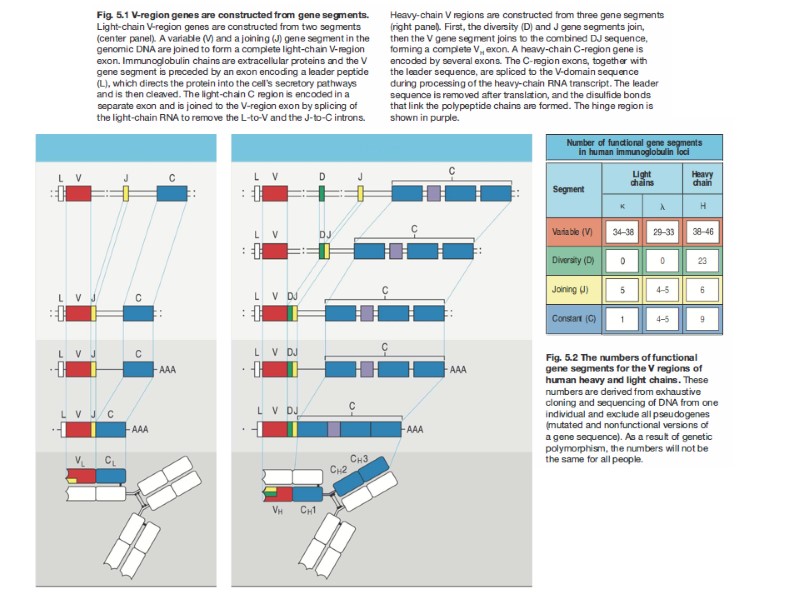
Пять возможных источников структурного разнообразия V-областей Н- и L-цепей иммуноглобулинов. Многочисленность гаметных генов. Имеется большое число отдельных неперестроенных генов (V1-Vn), каждый из которых кодирует V-домен отдельной специфичности. Соматический мутагенез. В онтогенезе В-клеток в результате мутаций гаметного V-гена в разных В-клеточных клонах возникают различные V-гены. Соматическая рекомбинация. В онтогенезе В-клеток происходит рекомбинация ряда генных сегментов (J1-Jn), соединяющихся с основной частью V-гена. В результате синтезируется белок, отдельные элементы, которого кодируются разными генными сегментами. Генная конверсия. Отрезки ДНК, принадлежащие ряду псевдо-V-генов, могут копироваться в функциональном V-гене, меняя его исходную нуклеотидную последовательность. Вставка добавочных нуклеотидов. При рекомбинации перед соединением вырезанных V- и J-сегментов ДНК возможно встраивание между ними добавочных нуклеотидов, кодирующих дополнительные аминокислотные остатки V-областей. Все эти пять механизмов служат источниками разнообразия антител у млекопитающих. Источники разнообразия антител
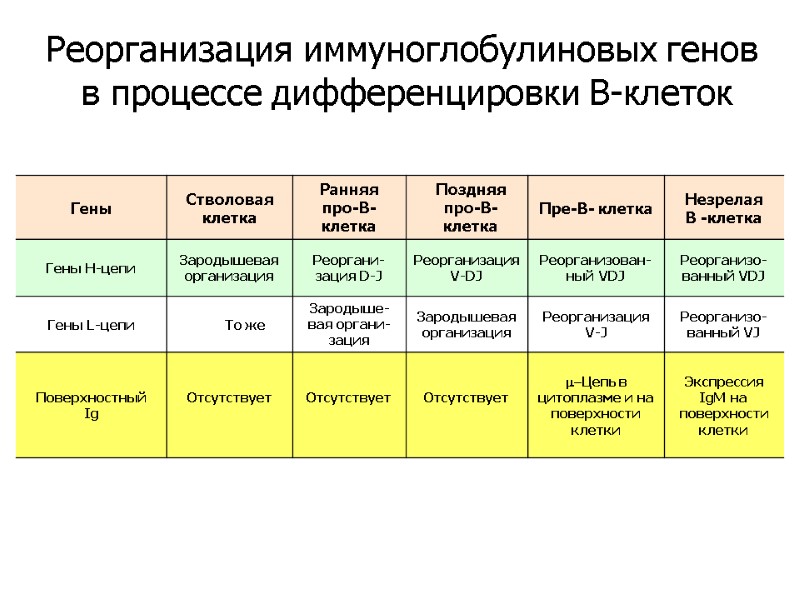
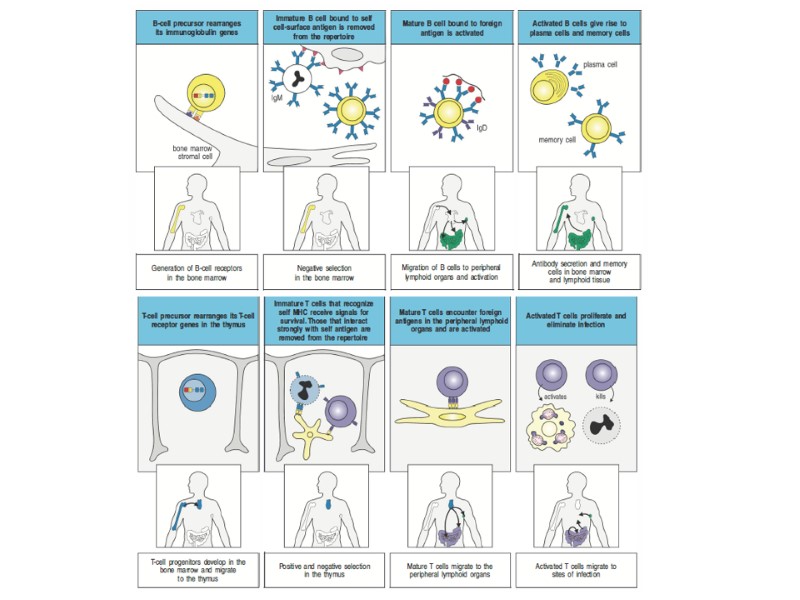
Реорганизация иммуноглобулиновых генов в процессе дифференцировки В-клеток
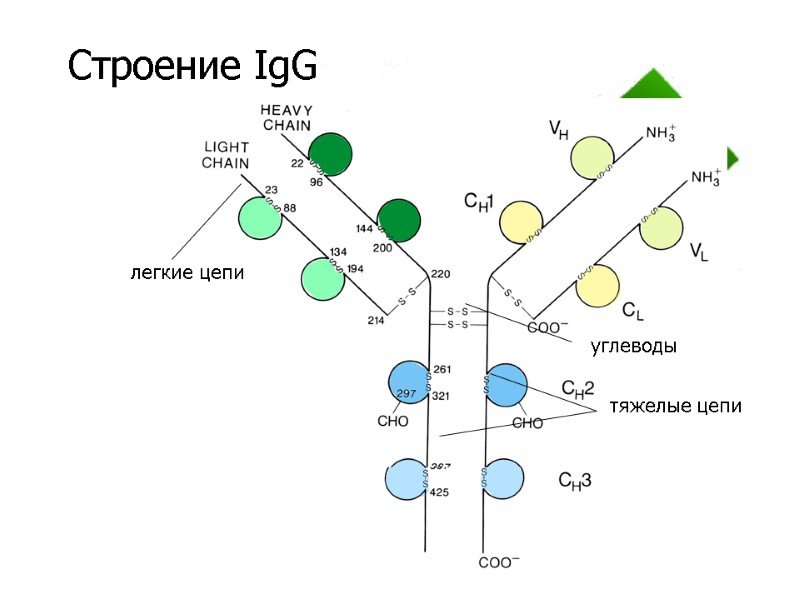
Строение IgG легкие цепи тяжелые цепи углеводы

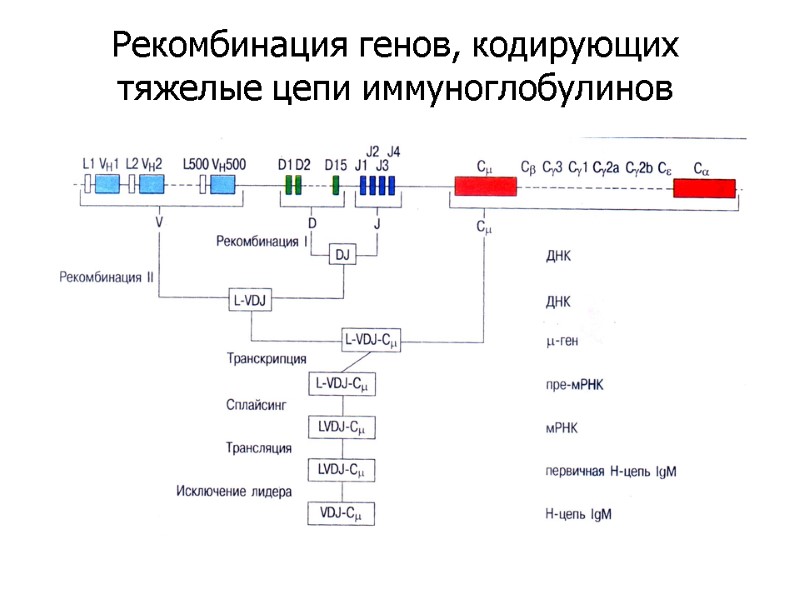
Рекомбинация генов, кодирующих тяжелые цепи иммуноглобулинов

Рекомбинация генов, кодирующих k-цепи иммуноглобулинов В некоммитированной В-клетке гены, кодирующие k-цепь иммуноглобу-линов, отделены в ДНК значительным расстоянием. Процесс рекомбинации начинается с объединения одного из Vk-генов (Vk2) с одним из J-мини-генов (J4). В результате формируется k-локус, контролирующий незрелую пре-мРНК ядра. При созревании такой РНК происходит слияние (сплайсинг) VJ с Сk-геном за счет делеции некодируемой последовательности нуклеотидов. Зрелая мРНК представляет собой единый информационный участок (LVk2J4Ck), транслирующий первичную к-цепь. При созревании k-цепи лидерная последовательность аминокислотных остатков (L) удаляется, что и приводит, наконец, к формированию полноценной k-цепи
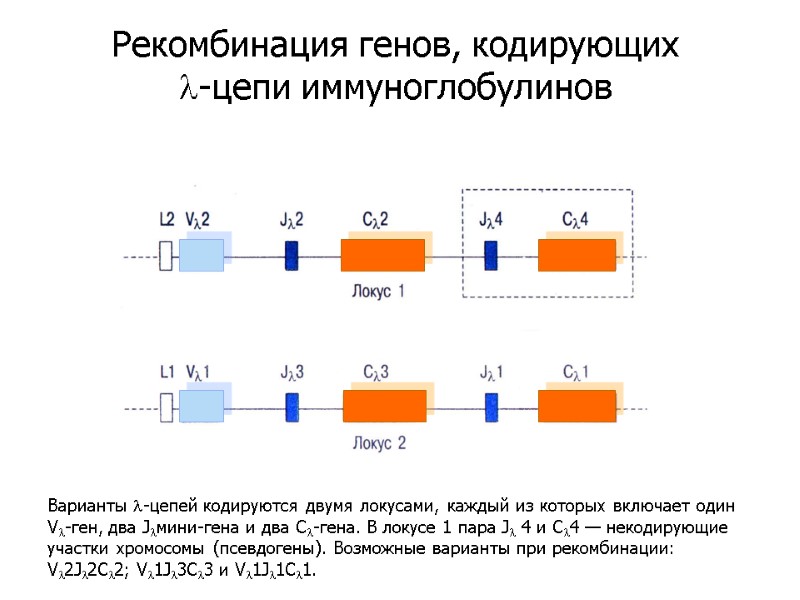
Варианты l-цепей кодируются двумя локусами, каждый из которых включает один Vl-ген, два Jlмини-гена и два Сl-гена. В локусе 1 пара Jl 4 и Сl4 — некодирующие участки хромосомы (псевдогены). Возможные варианты при рекомбинации: Vl2Jl2Cl2; Vl1Jl3Cl3 и Vl1Jl1Cl1. Рекомбинация генов, кодирующих l-цепи иммуноглобулинов

Классы и подклассы иммуноглобулинов у человека.

Биологическое значение синтеза иммуноглобулинов разных классов IgD Первичное распознавание свободного АГ, участие в активации В-лимфоцитов, участие в презентации АГ Т-лимфоцитам mIgМ Первичное распознавание свободного АГ, участие в регуляции пула зрелых В-клеток, модулирующая роль в активации В-лим- фоцитов, участие в презентации АГ Т-лимфоцитам IgМ Нейтрализация инфекционных свойств патогенов; элиминация антигена в корпускулярной форме из кровотока с участием комплемента; элиминация антигена путем его присоединения к поверхности эритроцитов с последующим фагоцитозом; регу- ляция процессов дифференцировки Т-лимфоцитов и ЕК IgG1-3 Элиминация антигена из кровотока, ЦНС: в молекулярной фор- форме – с участием фагоцитов, в корпускулярной форме - с участием комплемента; нейтрализация инфекционных свойств патогенов, включая вирусы; обеспечение плацентарного имму- нитета; реализация антителозависимой цитотоксичности IgА Формирование барьера на поверхности слизистых оболочек для проникновения антигенов во внутренние среды организма, нейтрализация инфекционных свойств патогенов, в т.ч.вирусов IgE,G4 Формирование тканевого барьера для распространения антиге- нов по организму, нейтрализация инфекционных свойств пато- генов, в т.ч.гельминтов и вирусов; развитие воспаления и шока

Классы и подклассы иммуноглобулинов у человека.

Пространственное объединение гипервариабельных участков V-домена тяжелой цепи IgG человека (миеломного белка New)

Антигенная детерминанта VL-домен легкой цепи VH-домен тяжелой цепи Связывание и узнавание антигена

Часть идиотип-антиидиотипической сети Возмущение сети под влиянием антигена Идиотипы, антиидиотипы и их сети
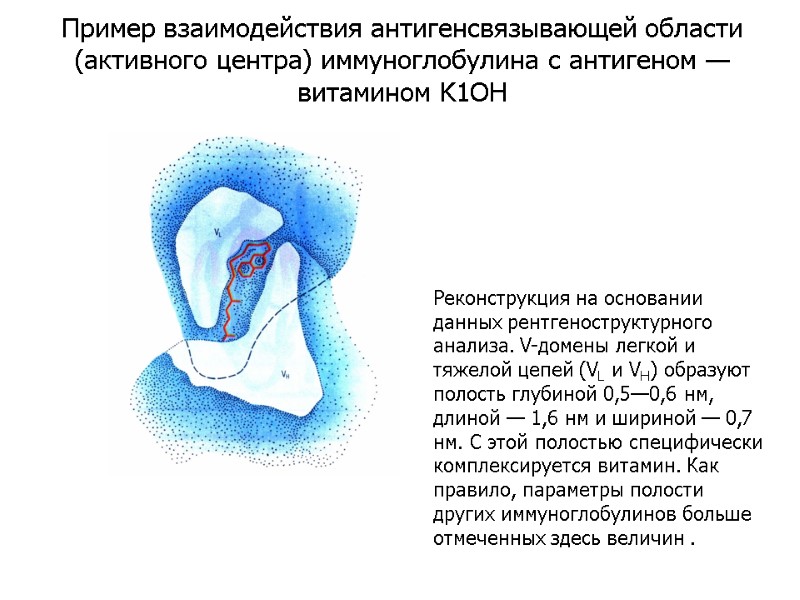
Реконструкция на основании данных рентгеноструктурного анализа. V-домены легкой и тяжелой цепей (VL и VH) образуют полость глубиной 0,5—0,6 нм, длиной — 1,6 нм и шириной — 0,7 нм. С этой полостью специфически комплексируется витамин. Как правило, параметры полости других иммуноглобулинов больше отмеченных здесь величин . Пример взаимодействия антигенсвязывающей области (активного центра) иммуноглобулина с антигеном — витамином K1OH
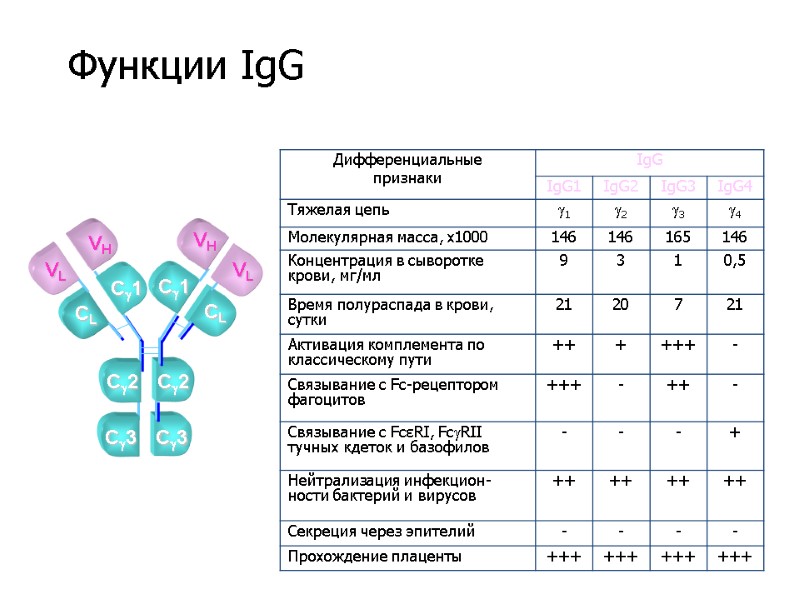
VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 Функции IgG

АГ Активация системы комплемента, лизис мик- робных и других клеток, несущих АГ C2 C2 IgG1, IgG3, IgG2 КЛЕТКА ОРГАНИЗМА IgG3, IgG1 CD16 (FcRIII) ЕСТЕСТВЕННЫЙ КИЛЛЕР Перфорин Обеспечение механизмов антителозависимой цитотоксичности по отношению к клеткам, несущим АГ ФАГОЦИТИРУЮЩИЕ КЛЕТКИ CD64 (FcRI) CD32 (FcRII) Присоединение иммунных комплексов (ИК) к фагоцитам через рецепторы к Fc- фрагментам IgG1 и IgG3 I типа (СD64 на активированных фагоцитах), II и III типа (СD32 и СD16 на любых фагоцитирую- щих клетках) с последующей элимина- цией ИК путем фагоцитоза Дегрануляция Функции IgG
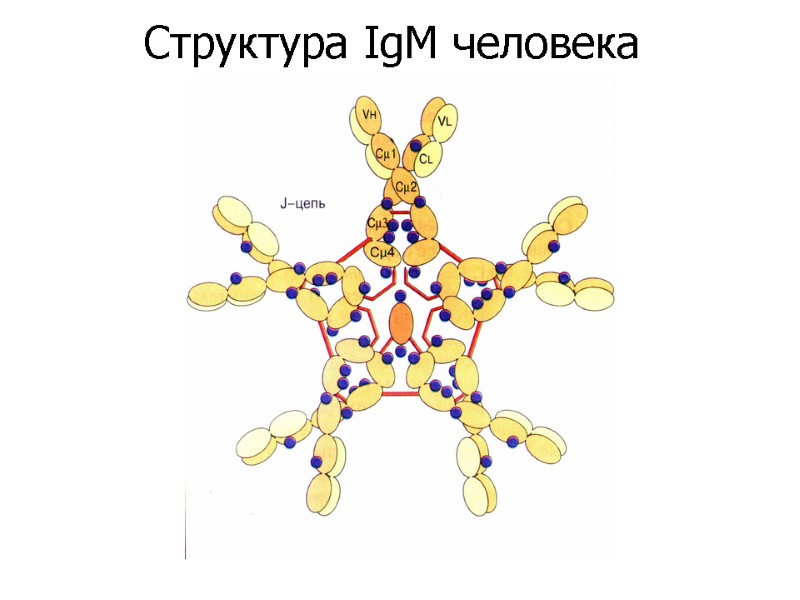
Структура IgM человека
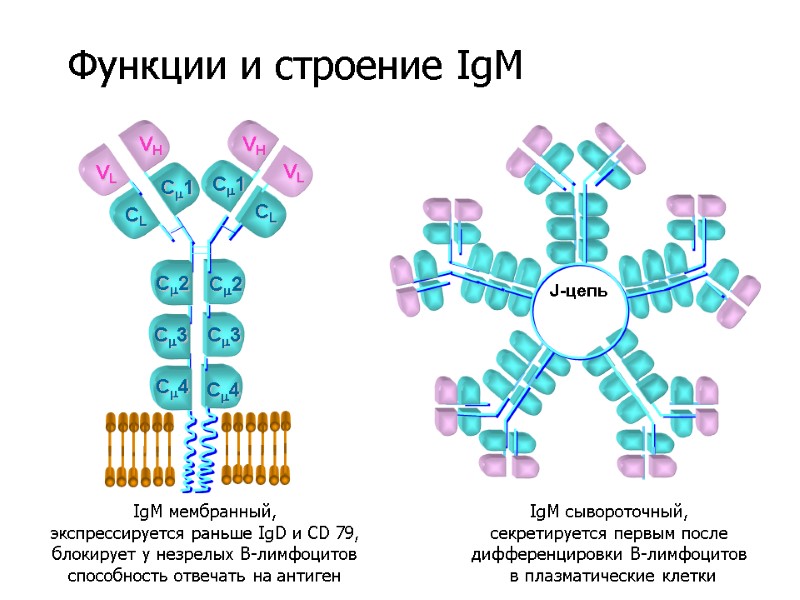
VL VH VH VL C3 C2 CL C1 IgM мембранный, экспрессируется раньше IgD и CD 79, блокирует у незрелых В-лимфоцитов способность отвечать на антиген IgM сывороточный, секретируется первым после дифференцировки В-лимфоцитов в плазматические клетки CL C1 C2 C3 C4 C4 J-цепь Функции и строение IgM
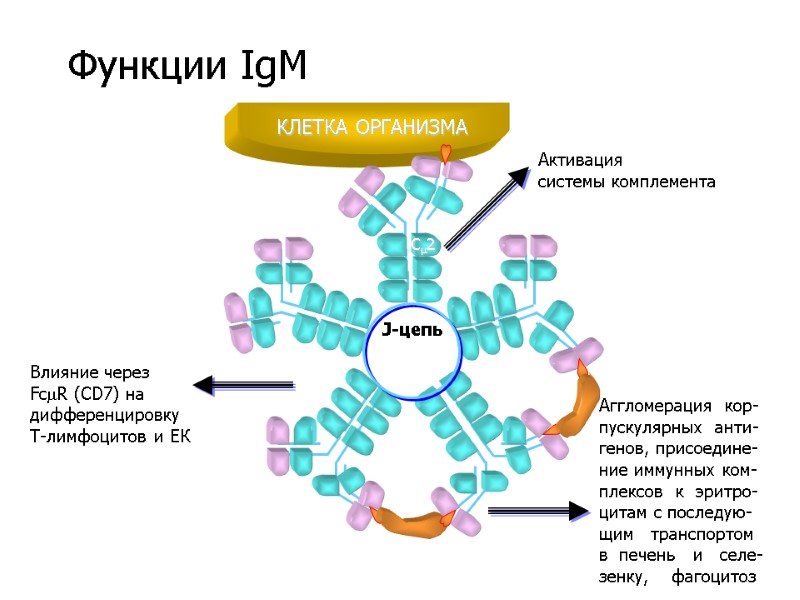
J-цепь Активация системы комплемента C2 Аггломерация кор- пускулярных анти- генов, присоедине- ние иммунных ком- плексов к эритро- цитам с последую- щим транспортом в печень и селе- зенку, фагоцитоз Влияние через FcR (CD7) на дифференцировку Т-лимфоцитов и ЕК КЛЕТКА ОРГАНИЗМА Функции IgM

Первичная иммунизация вызывает образование антител преимущественно IgM- изотипа; повторное введение антигена стимулирует образование антител в основном IgG-изотипа. Механизм переключения (switch-over) изотипа схематично представлен справа. При первичном ответе рекомбинировавший участок V-D-J считывается одновременно с Сμ-сегментом гена. После удаления интронов при процессинге первичного РНК-транскрипта образуется мРНК для секретируемой формы IgM. В процессе «созревания» иммунного ответа происходит переключающая изотип рекомбинация между участком γ3 и расположенным ниже С-геном (в данном случае - Сγ3). Разделяющий их участок ДНК образует петлю, а затем вырезается. В результате происходит утрата генов Сμ и Сδ, а два участка переключения соединяются. «Созревание» (maturation) иммунного ответа и переключение (switch-over) изотипа
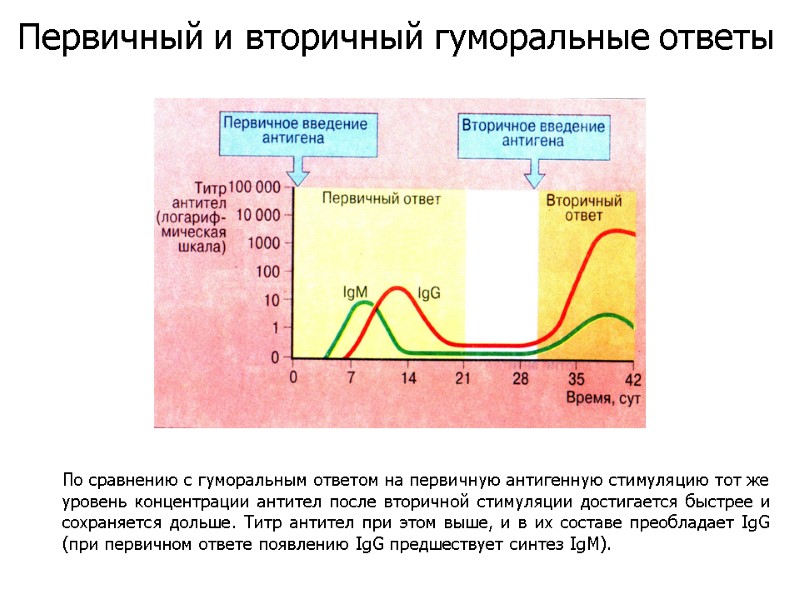
По сравнению с гуморальным ответом на первичную антигенную стимуляцию тот же уровень концентрации антител после вторичной стимуляции достигается быстрее и сохраняется дольше. Титр антител при этом выше, и в их составе преобладает IgG (при первичном ответе появлению IgG предшествует синтез IgM). Первичный и вторичный гуморальные ответы
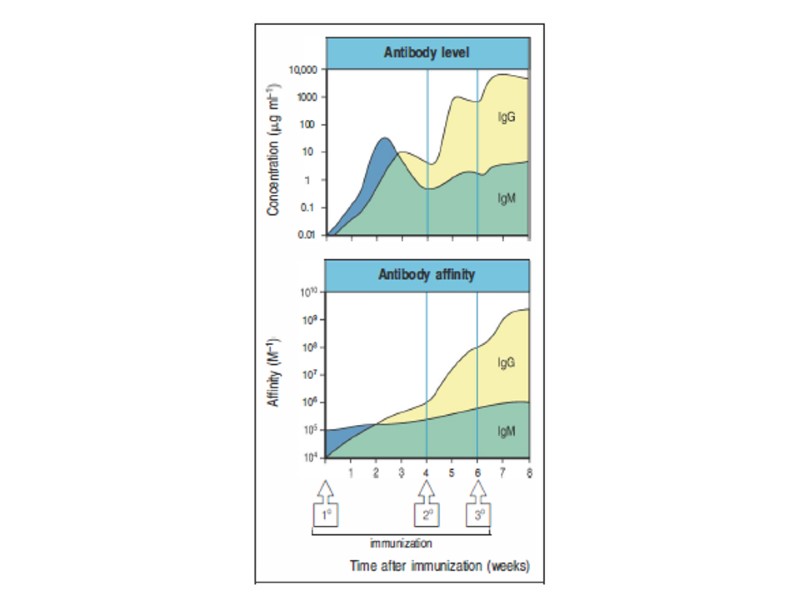
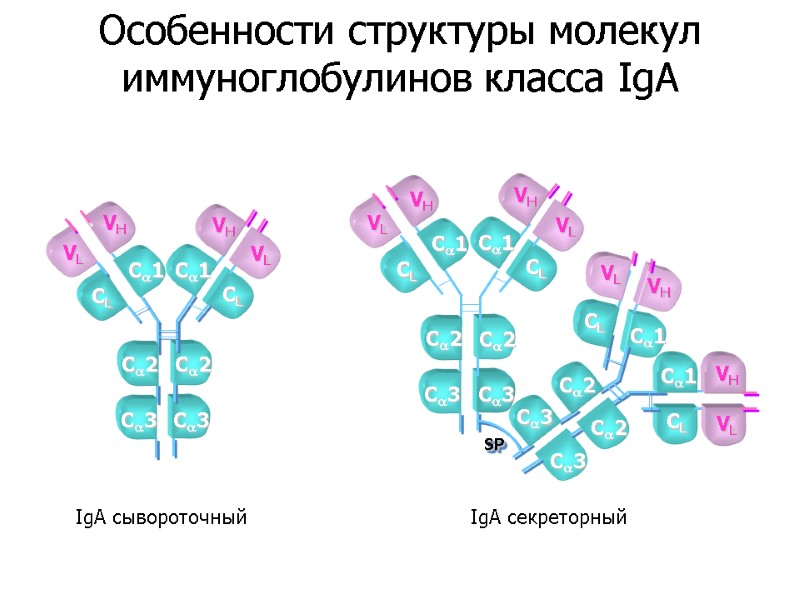
VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 IgA сывороточный VL VH VH VL C3 C2 CL C1 CL C1 C2 C3 C2 C2 VL VH CL C1 C3 C3 SP VH VL CL C1 IgA секреторный Особенности структуры молекул иммуноглобулинов класса IgA
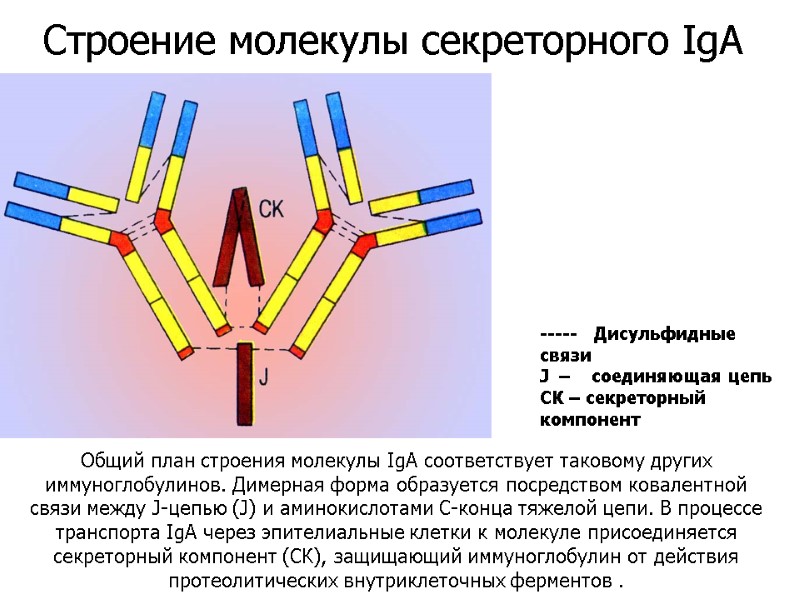
Общий план строения молекулы IgA соответствует таковому других иммуноглобулинов. Димерная форма образуется посредством ковалентной связи между J-цепью (J) и аминокислотами С-конца тяжелой цепи. В процессе транспорта IgA через эпителиальные клетки к молекуле присоединяется секреторный компонент (СК), защищающий иммуноглобулин от действия протеолитических внутриклеточных ферментов . ----- Дисульфидные связи J – соединяющая цепь СК – секреторный компонент Строение молекулы секреторного IgA
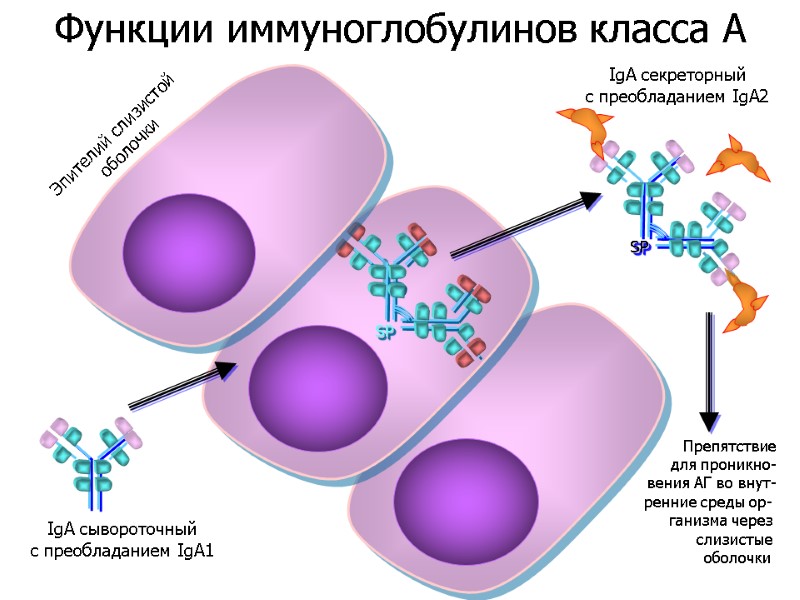
IgA сывороточный c преобладанием IgA1 SP SP SP IgA секреторный c преобладанием IgA2 Эпителий слизистой оболочки Препятствие для проникно- вения АГ во внут- ренние среды ор- ганизма через слизистые оболочки Функции иммуноглобулинов класса A
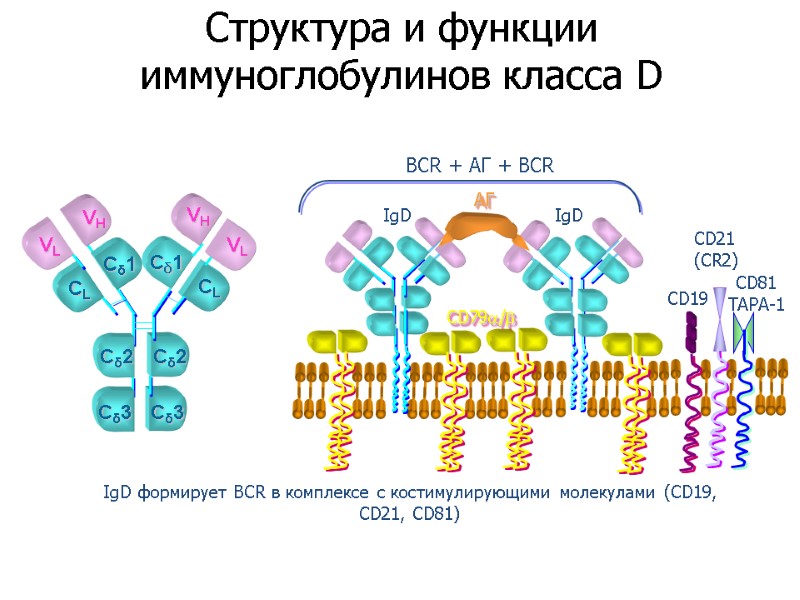
Структура и функции иммуноглобулинов класса D АГ IgD IgD CD79/ CD19 CD21 (CR2) IgD формирует ВСR в комплексе с костимулирующими молекулами (CD19, CD21, CD81) BCR + АГ + BCR CD81 TAPA-1 VL VH VH VL Cδ3 Cδ2 CL Cδ1 CL Cδ1 Cδ2 Cδ3
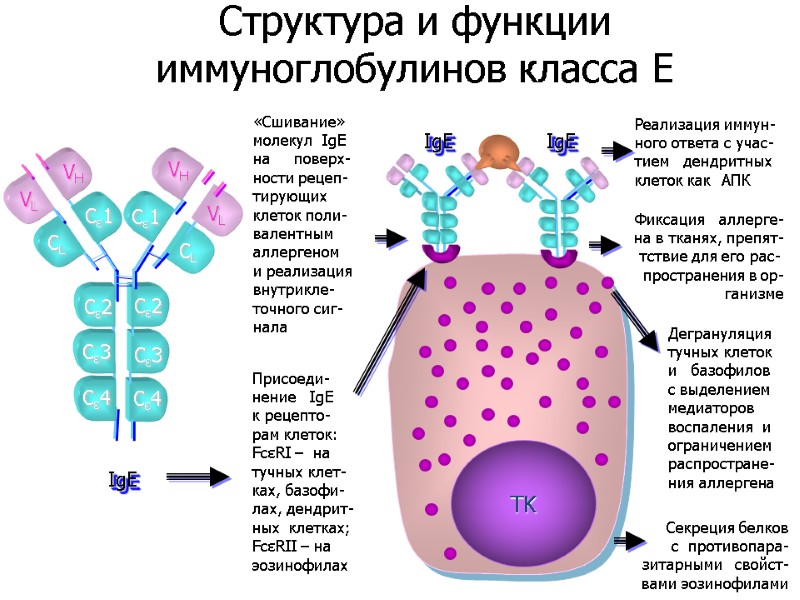
Секреция белков с противопара- зитарными свойст- вами эозинофилами VL VH VH VL Cε3 Cε2 CL Cε1 CL Cε1 Cε2 Cε3 IgE Cε4 Cε4 Структура и функции иммуноглобулинов класса E TK IgE IgE Реализация иммун- ного ответа с учас- тием дендритных клеток как АПК Фиксация аллерге- на в тканях, препят- тствие для его рас- пространения в ор- ганизме Дегрануляция тучных клеток и базофилов с выделением медиаторов воспаления и ограничением распростране- ния аллергена «Сшивание» молекул IgE на поверх- ности рецеп- тирующих клеток поли- валентным аллергеном и реализация внутрикле- точного сиг- нала Присоеди- нение IgE к рецепто- рам клеток: FcεRI – на тучных клет- ках, базофи- лах, дендрит- ных клетках; FcεRII – на эозинофилах
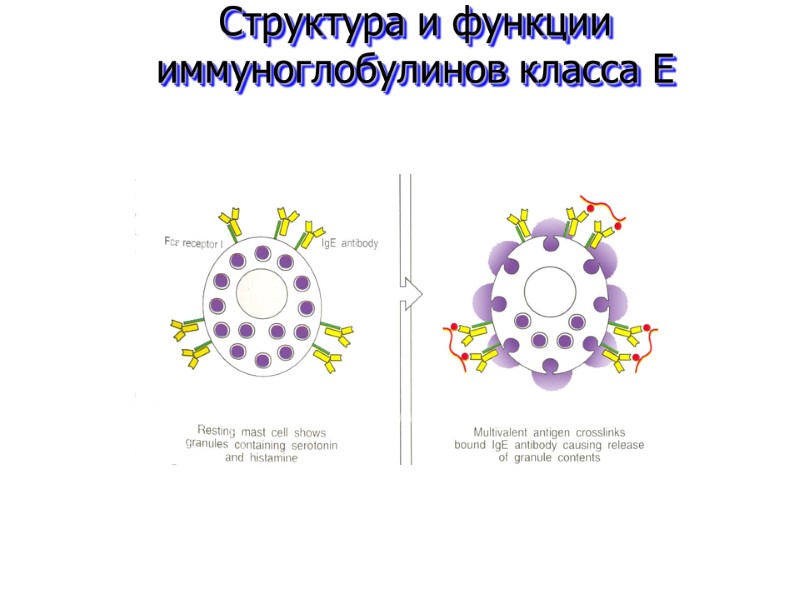
Структура и функции иммуноглобулинов класса E
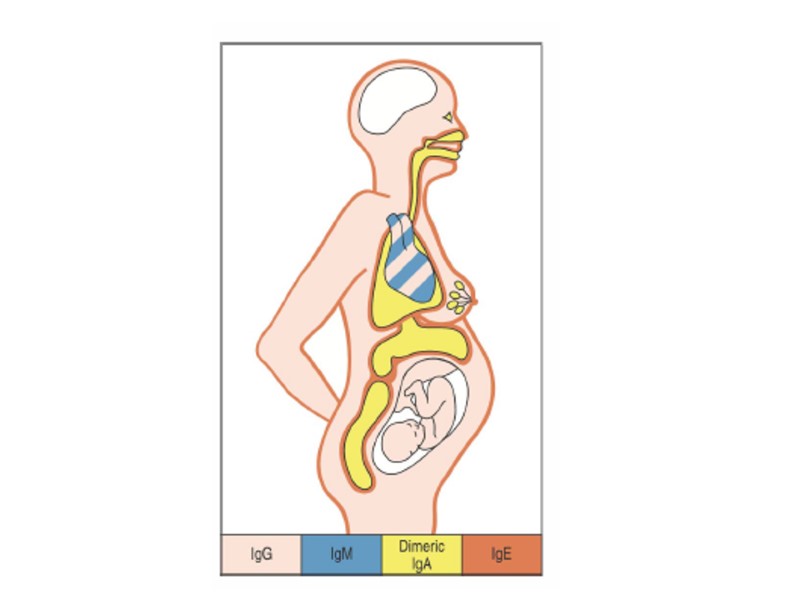
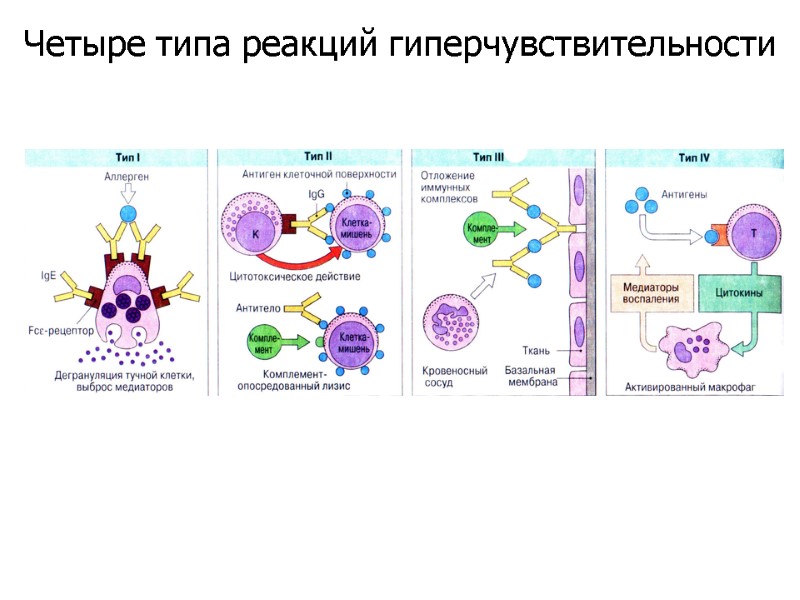
Четыре типа реакций гиперчувствительности
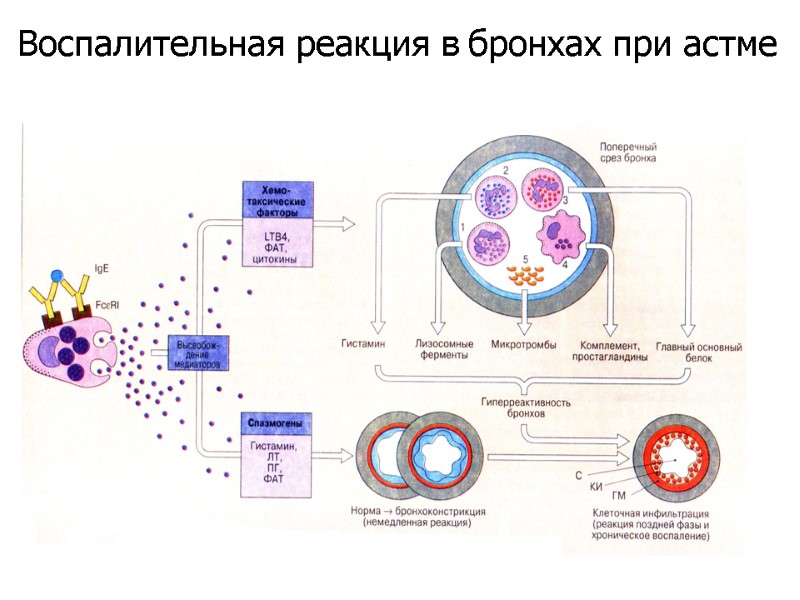
Воспалительная реакция в бронхах при астме
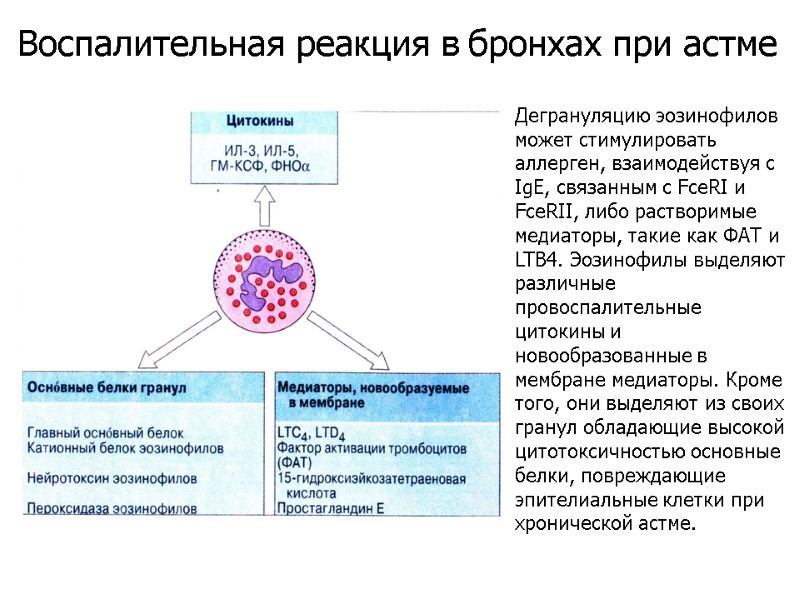
Дегрануляцию эозинофилов может стимулировать аллерген, взаимодействуя с IgE, связанным с FceRI и FceRII, либо растворимые медиаторы, такие как ФАТ и LTB4. Эозинофилы выделяют различные провоспалительные цитокины и новообразованные в мембране медиаторы. Кроме того, они выделяют из своих гранул обладающие высокой цитотоксичностью основные белки, повреждающие эпителиальные клетки при хронической астме. Воспалительная реакция в бронхах при астме
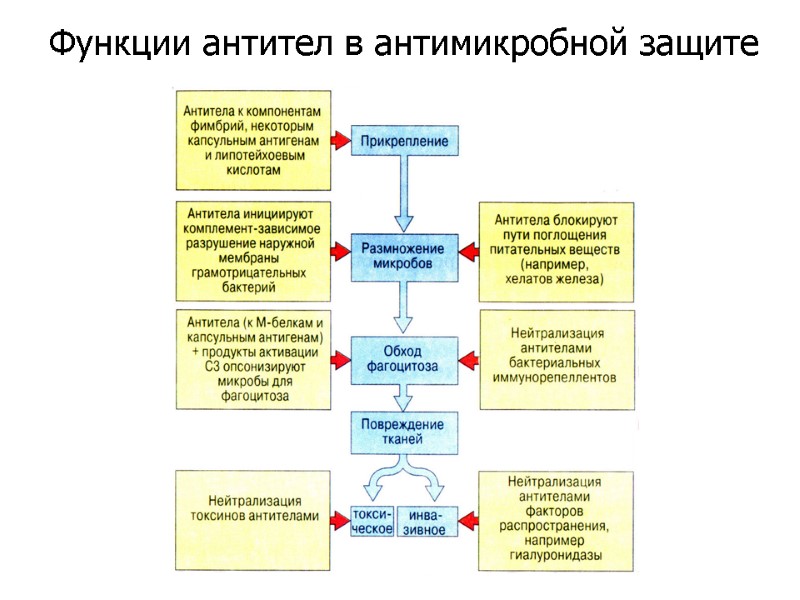
Функции антител в антимикробной защите

Антитела и НК
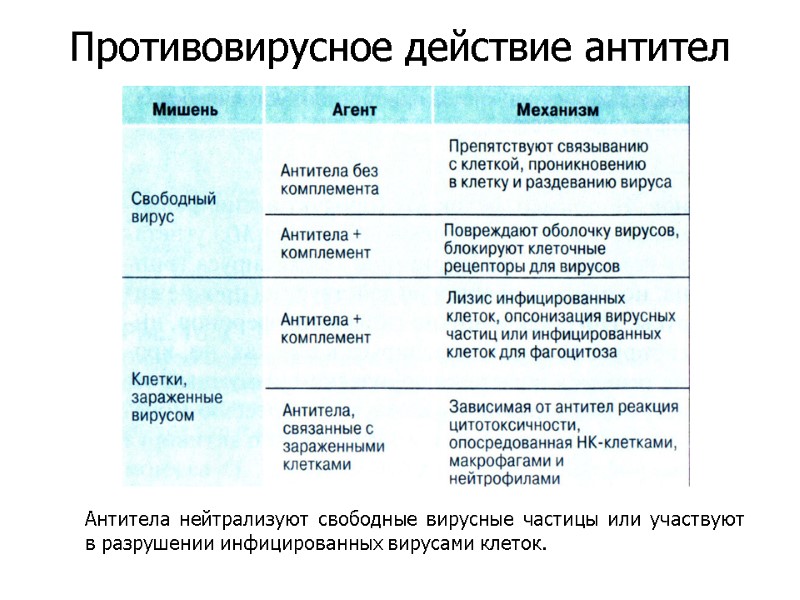
Антитела нейтрализуют свободные вирусные частицы или участвуют в разрушении инфицированных вирусами клеток. Противовирусное действие антител
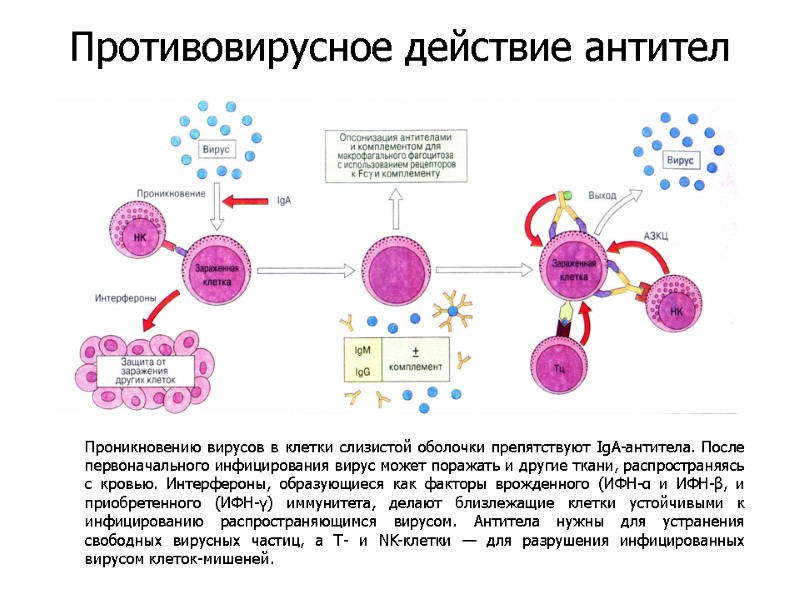
Проникновению вирусов в клетки слизистой оболочки препятствуют IgA-антитела. После первоначального инфицирования вирус может поражать и другие ткани, распространяясь с кровью. Интерфероны, образующиеся как факторы врожденного (ИФН-α и ИФН-β, и приобретенного (ИФН-γ) иммунитета, делают близлежащие клетки устойчивыми к инфицированию распространяющимся вирусом. Антитела нужны для устранения свободных вирусных частиц, а Т- и NK-клетки — для разрушения инфицированных вирусом клеток-мишеней. Противовирусное действие антител
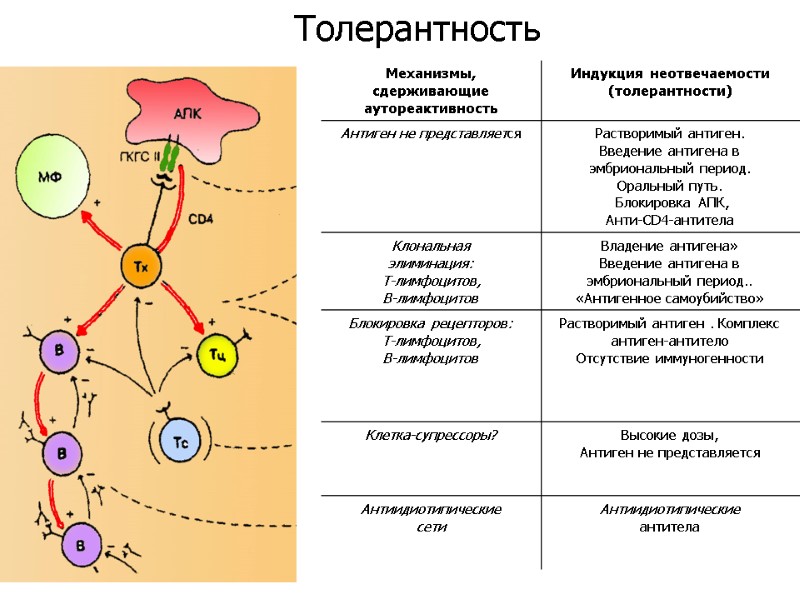
Толерантность
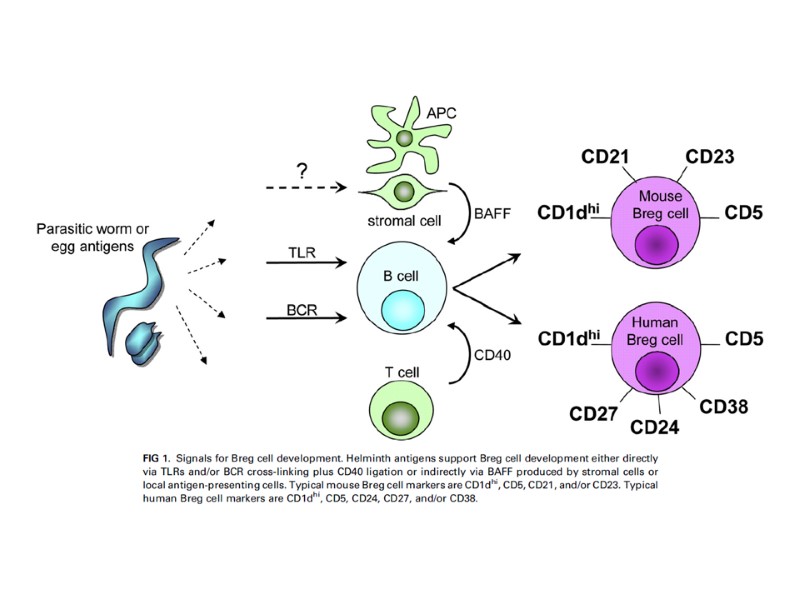
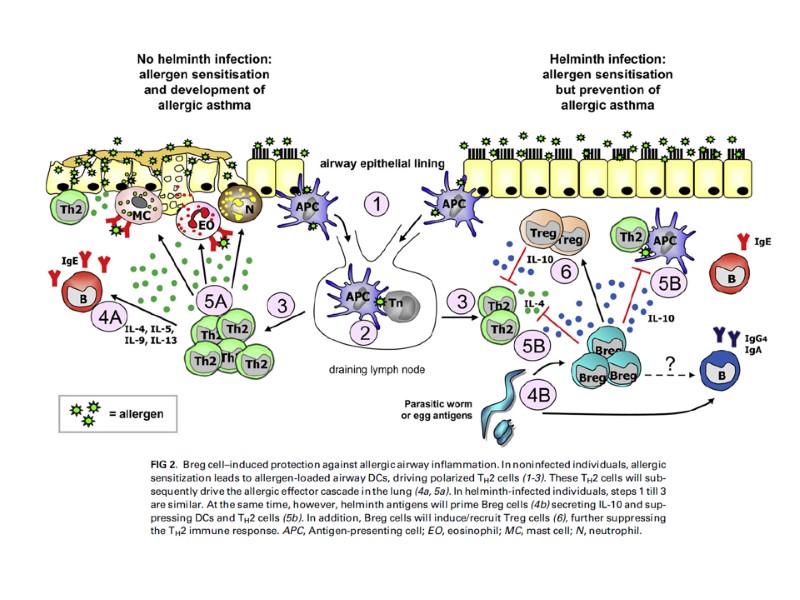
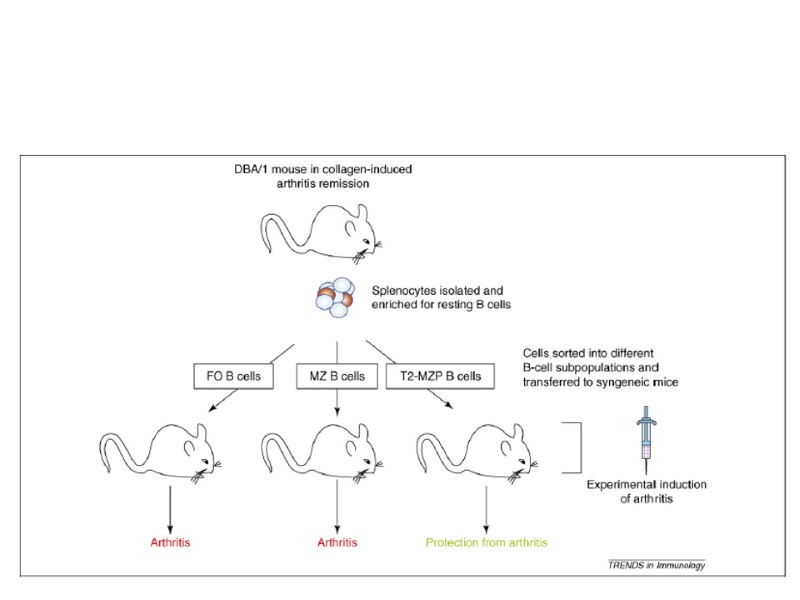

Paul Ehrlich 1854-1915



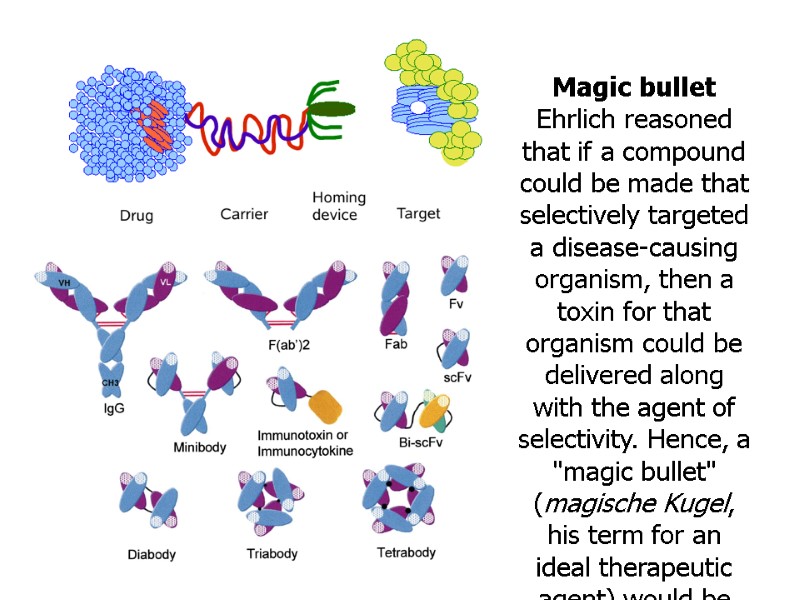
Magic bullet Ehrlich reasoned that if a compound could be made that selectively targeted a disease-causing organism, then a toxin for that organism could be delivered along with the agent of selectivity. Hence, a "magic bullet" (magische Kugel, his term for an ideal therapeutic agent) would be created that killed only the organism targeted. The concept of a "magic bullet" was to some extent realized by the invention of monoclonal antibodies as they provide a very specific binding affinity.
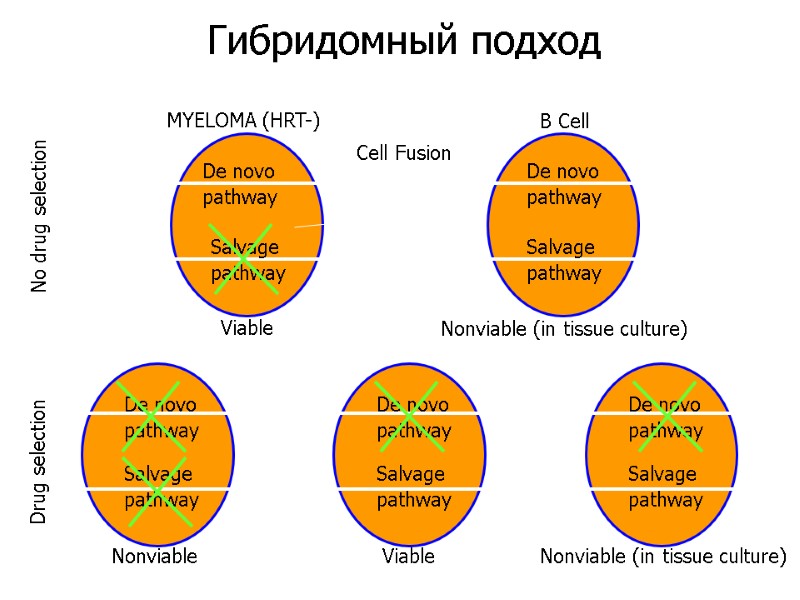
MYELOMA (HRT-) B Cell No drug selection Drug selection De novo pathway De novo pathway Salvage pathway De novo pathway De novo pathway De novo pathway Salvage pathway Salvage pathway Salvage pathway Salvage pathway Viable Nonviable (in tissue culture) Nonviable (in tissue culture) Nonviable Viable Cell Fusion Гибридомный подход
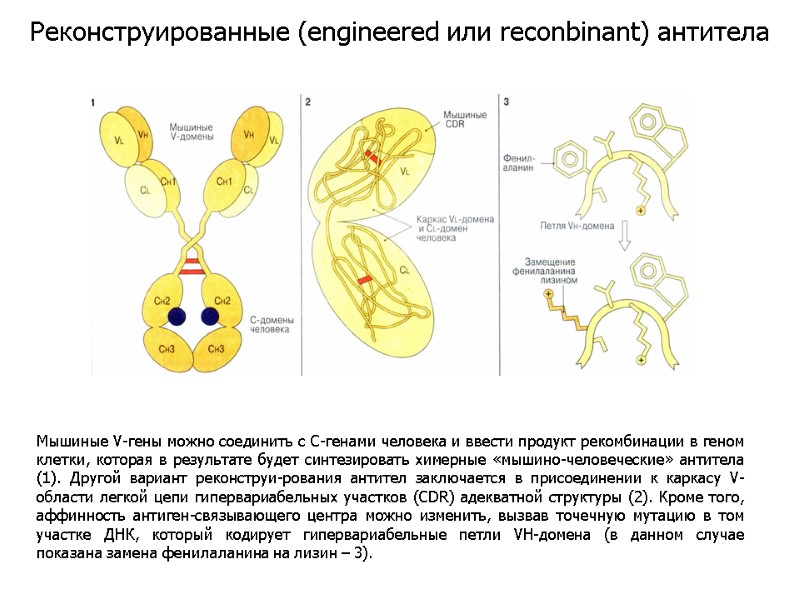
Мышиные V-гены можно соединить с С-генами человека и ввести продукт рекомбинации в геном клетки, которая в результате будет синтезировать химерные «мышино-человеческие» антитела (1). Другой вариант реконструи-рования антител заключается в присоединении к каркасу V-области легкой цепи гипервариабельных участков (CDR) адекватной структуры (2). Кроме того, аффинность антиген-связывающего центра можно изменить, вызвав точечную мутацию в том участке ДНК, который кодирует гипервариабельные петли VH-домена (в данном случае показана замена фенилаланина на лизин – 3). Реконструированные (engineered или reconbinant) антитела

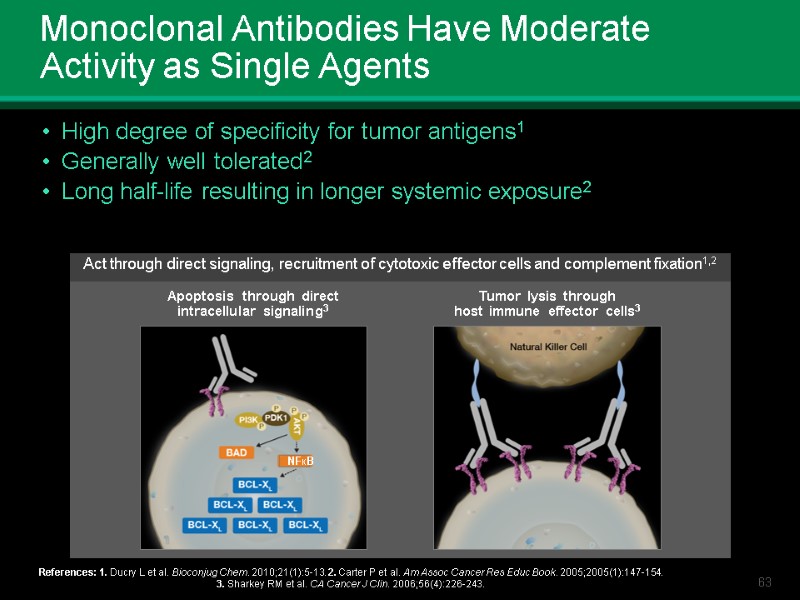
Monoclonal Antibodies Have Moderate Activity as Single Agents High degree of specificity for tumor antigens1 Generally well tolerated2 Long half-life resulting in longer systemic exposure2 References: 1. Ducry L et al. Bioconjug Chem. 2010;21(1):5-13. 2. Carter P et al. Am Assoc Cancer Res Educ Book. 2005;2005(1):147-154. 3. Sharkey RM et al. CA Cancer J Clin. 2006;56(4):226-243. Apoptosis through direct intracellular signaling3 Tumor lysis through host immune effector cells3 Act through direct signaling, recruitment of cytotoxic effector cells and complement fixation1,2 NFКB

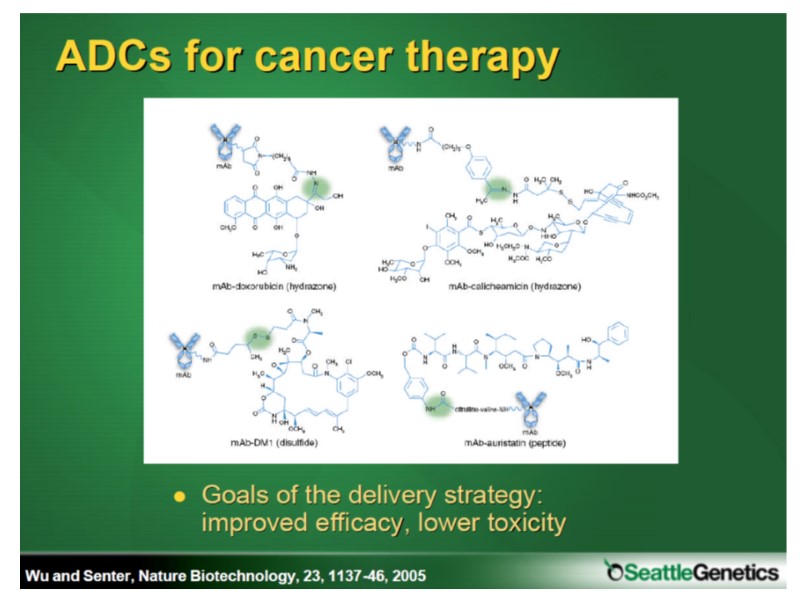
Elements of an Antibody-Drug Conjugate (ADC) References: 1. Carter PJ et al. Cancer J. 2008;14(3):154-169. 2. Senter PD. Curr Opin Chem Biol. 2009;13(3):235-244. 3. Polson AG et al. Cancer Res. 2009;69(6):2358-2364. Antibody Specific for a tumor-associated antigen that has restricted expression on normal cells.1,2 Cytotoxic agent Designed to kill target cells when internalized and released.1,2
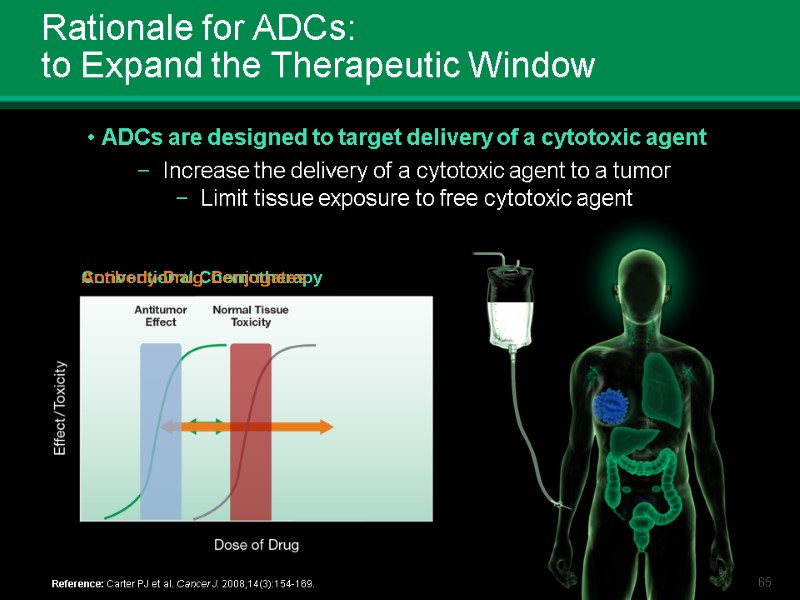
Rationale for ADCs: to Expand the Therapeutic Window Conventional Chemotherapy Antibody-Drug Conjugates ADCs are designed to target delivery of a cytotoxic agent Increase the delivery of a cytotoxic agent to a tumor Limit tissue exposure to free cytotoxic agent Reference: Carter PJ et al. Cancer J. 2008;14(3):154-169.
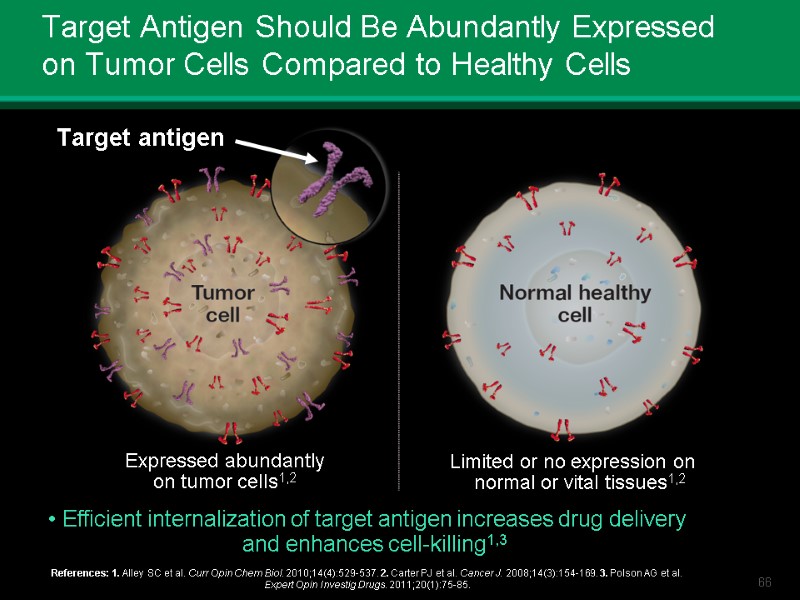
Target Antigen Should Be Abundantly Expressed on Tumor Cells Compared to Healthy Cells Target antigen Efficient internalization of target antigen increases drug delivery and enhances cell-killing1,3 Expressed abundantly on tumor cells1,2 Limited or no expression on normal or vital tissues1,2 References: 1. Alley SC et al. Curr Opin Chem Biol. 2010;14(4):529-537. 2. Carter PJ et al. Cancer J. 2008;14(3):154-169. 3. Polson AG et al. Expert Opin Investig Drugs. 2011;20(1):75-85.
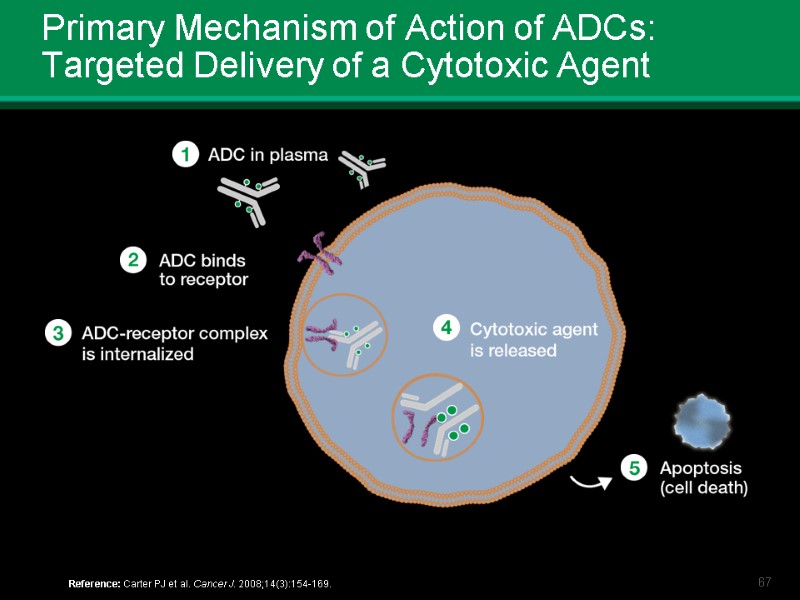
Primary Mechanism of Action of ADCs: Targeted Delivery of a Cytotoxic Agent Reference: Carter PJ et al. Cancer J. 2008;14(3):154-169.
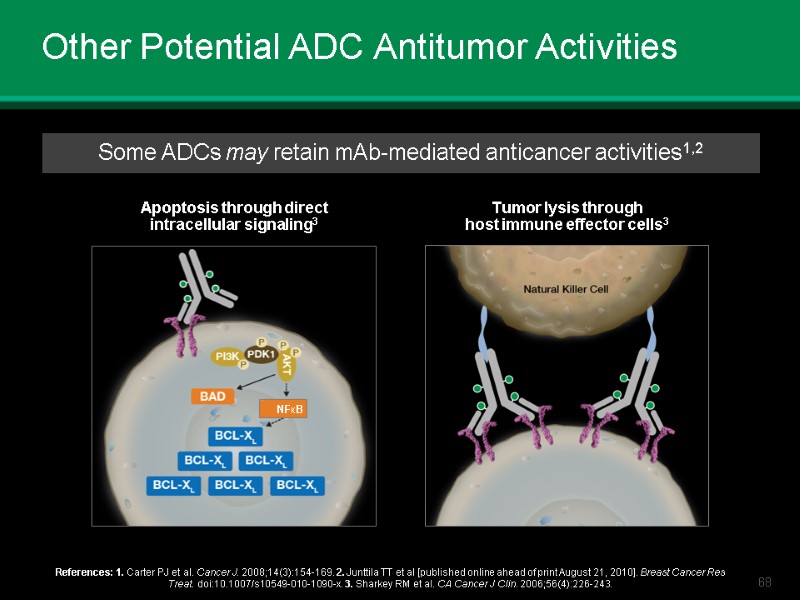
Other Potential ADC Antitumor Activities References: 1. Carter PJ et al. Cancer J. 2008;14(3):154-169. 2. Junttila TT et al [published online ahead of print August 21, 2010]. Breast Cancer Res Treat. doi:10.1007/s10549-010-1090-x. 3. Sharkey RM et al. CA Cancer J Clin. 2006;56(4):226-243. Some ADCs may retain mAb-mediated anticancer activities1,2 Apoptosis through direct intracellular signaling3 Tumor lysis through host immune effector cells3 NFКB
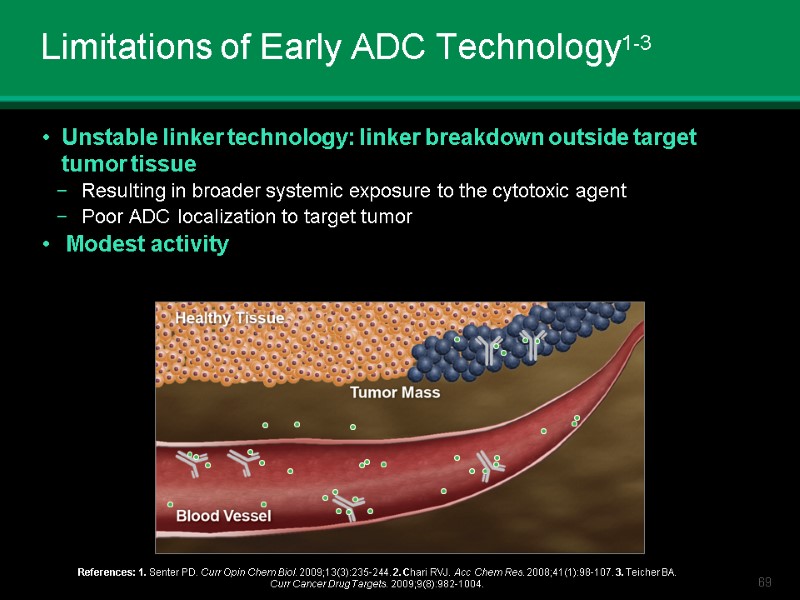
Limitations of Early ADC Technology1-3 Unstable linker technology: linker breakdown outside target tumor tissue Resulting in broader systemic exposure to the cytotoxic agent Poor ADC localization to target tumor Modest activity References: 1. Senter PD. Curr Opin Chem Biol. 2009;13(3):235-244. 2. Chari RVJ. Acc Chem Res. 2008;41(1):98-107. 3. Teicher BA. Curr Cancer Drug Targets. 2009;9(8):982-1004.

Next-Generation ADCs: Engineered & Optimized Improved by incorporation of:1,2 A more potent cytotoxic agent* A more stable linker Improved conjugation technology Optimized ratio of cytotoxic agents per antibody References: 1. Alley SC et al. Curr Opin Chem Biol. 2010;14(4):529-537. 2. Hamblett KJ et al. Clin Cancer Res. 2004;10(20):7063-7070. * As demonstrated in preclinical models.
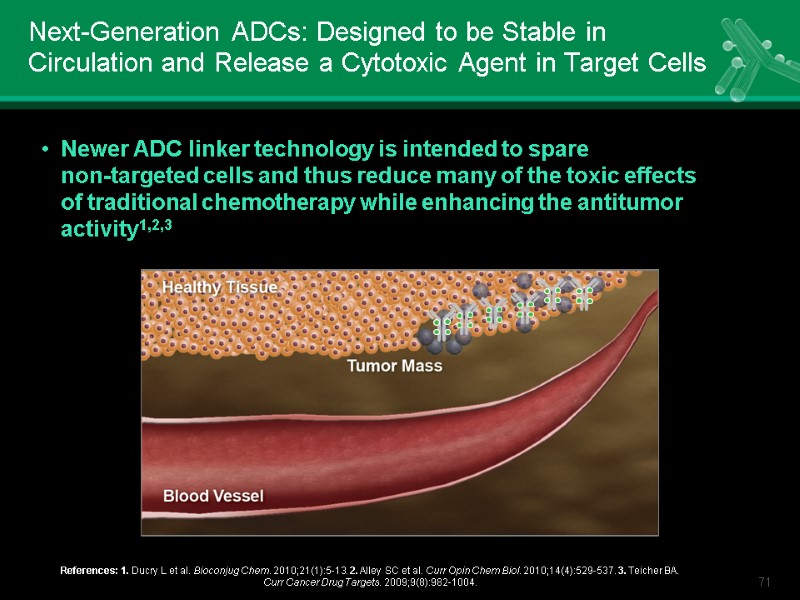
Next-Generation ADCs: Designed to be Stable in Circulation and Release a Cytotoxic Agent in Target Cells Newer ADC linker technology is intended to spare non-targeted cells and thus reduce many of the toxic effects of traditional chemotherapy while enhancing the antitumor activity1,2,3 References: 1. Ducry L et al. Bioconjug Chem. 2010;21(1):5-13. 2. Alley SC et al. Curr Opin Chem Biol. 2010;14(4):529-537. 3. Teicher BA. Curr Cancer Drug Targets. 2009;9(8):982-1004.
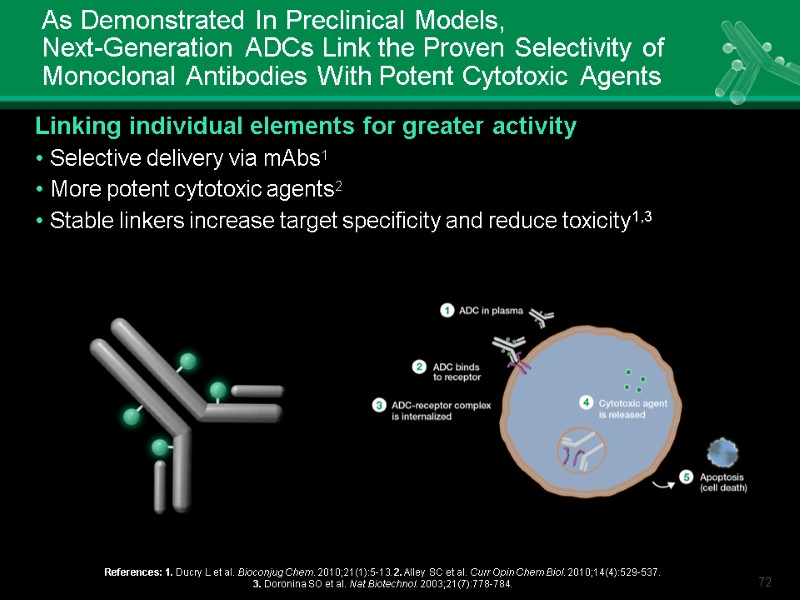
As Demonstrated In Preclinical Models, Next-Generation ADCs Link the Proven Selectivity of Monoclonal Antibodies With Potent Cytotoxic Agents Linking individual elements for greater activity Selective delivery via mAbs1 More potent cytotoxic agents2 Stable linkers increase target specificity and reduce toxicity1,3 References: 1. Ducry L et al. Bioconjug Chem. 2010;21(1):5-13. 2. Alley SC et al. Curr Opin Chem Biol. 2010;14(4):529-537. 3. Doronina SO et al. Nat Biotechnol. 2003;21(7):778-784.

ADC Components Targeting AB Choice of target (tumor/normal tissue ratio) Internalization (must have feature) Intracellular trafficking (presumed as important but not clearly spelled) Payload Highly potent (mostly tubulin active) Linker Cleavable vs non-cleavable Stable in circulation
Т-клеточный иммунный ответ Габибов А.Г. Лекция 4
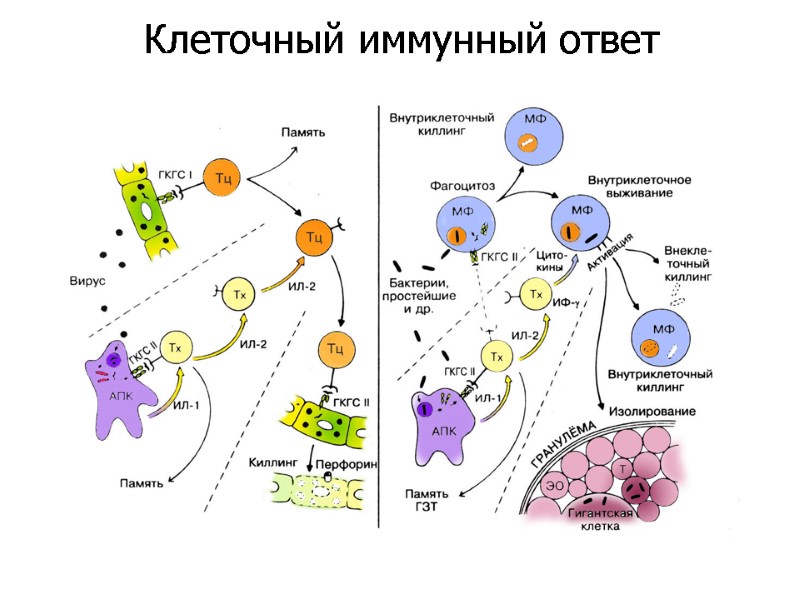
Клеточный иммунный ответ
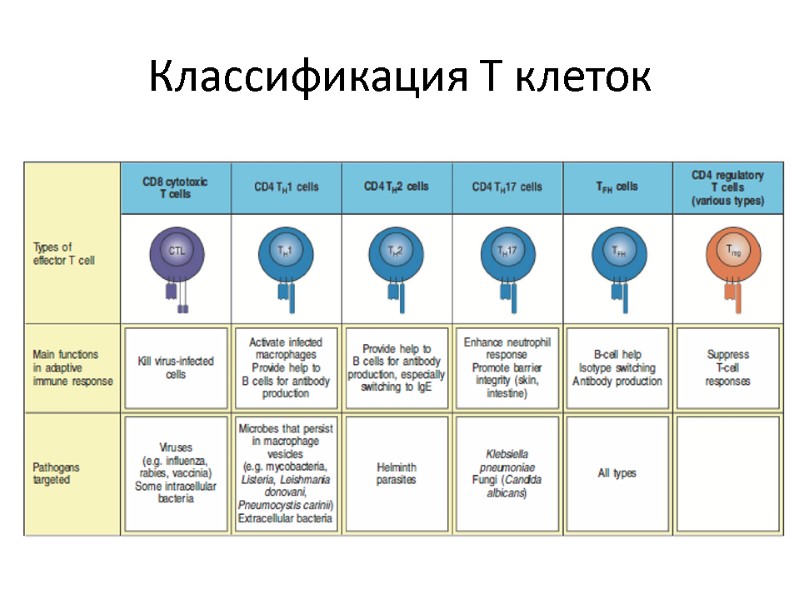
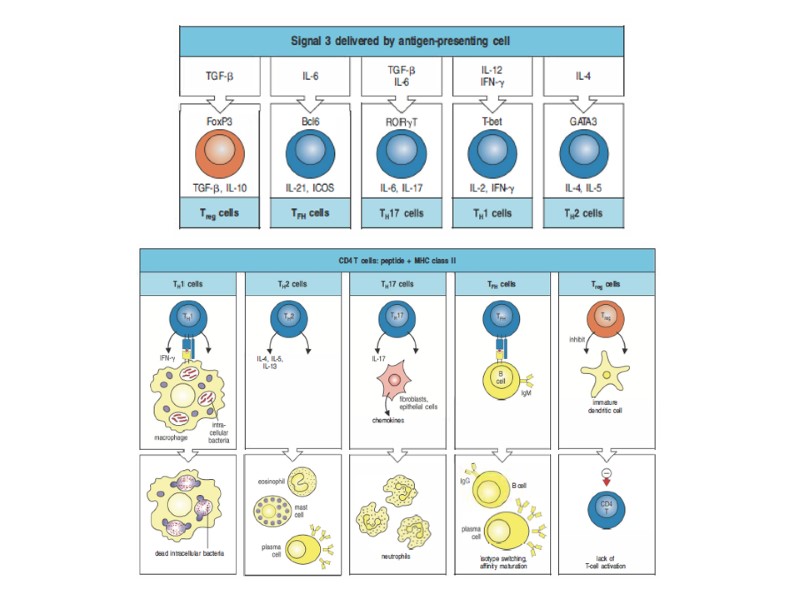
Классификация Т клеток
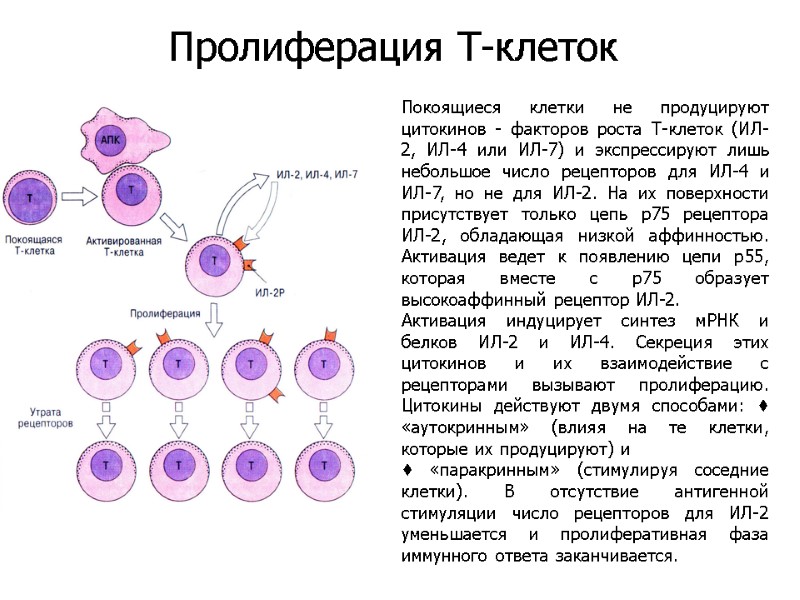
Покоящиеся клетки не продуцируют цитокинов - факторов роста Т-клеток (ИЛ-2, ИЛ-4 или ИЛ-7) и экспрессируют лишь небольшое число рецепторов для ИЛ-4 и ИЛ-7, но не для ИЛ-2. На их поверхности присутствует только цепь р75 рецептора ИЛ-2, обладающая низкой аффинностью. Активация ведет к появлению цепи р55, которая вместе с р75 образует высокоаффинный рецептор ИЛ-2. Активация индуцирует синтез мРНК и белков ИЛ-2 и ИЛ-4. Секреция этих цитокинов и их взаимодействие с рецепторами вызывают пролиферацию. Цитокины действуют двумя способами: ♦ «аутокринным» (влияя на те клетки, которые их продуцируют) и ♦ «паракринным» (стимулируя соседние клетки). В отсутствие антигенной стимуляции число рецепторов для ИЛ-2 уменьшается и пролиферативная фаза иммунного ответа заканчивается. Пролиферация Т-клеток
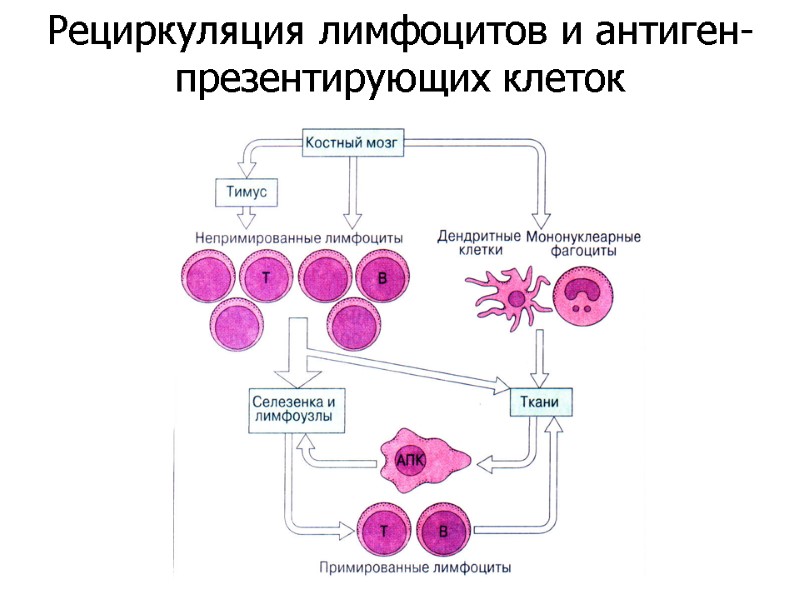
Рециркуляция лимфоцитов и антиген-презентирующих клеток
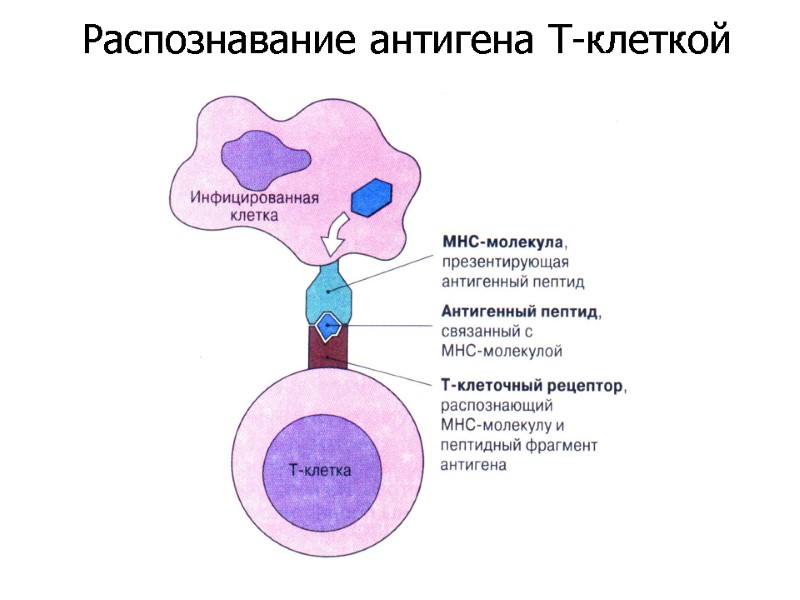
Распознавание антигена Т-клеткой
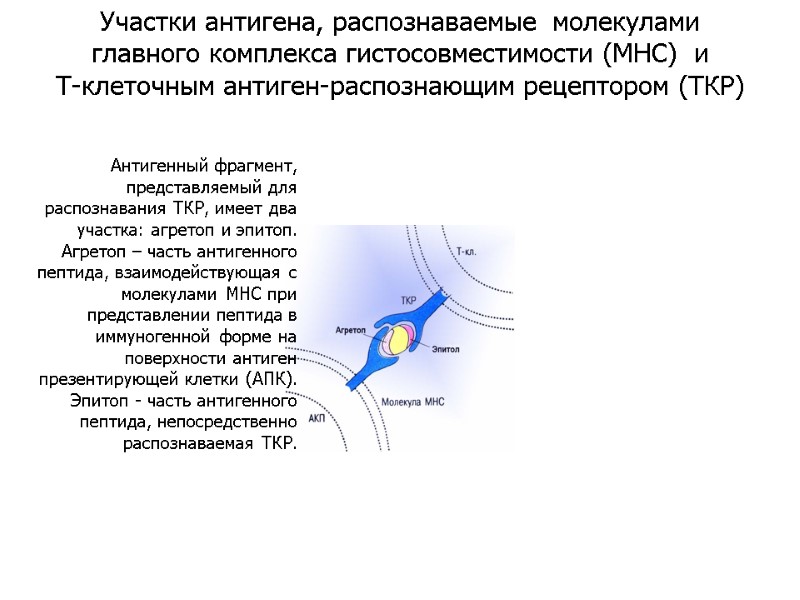
Антигенный фрагмент, представляемый для распознавания ТКР, имеет два участка: агретоп и эпитоп. Агретоп – часть антигенного пептида, взаимодействующая с молекулами МНС при представлении пептида в иммуногенной форме на поверхности антиген презентирующей клетки (АПК). Эпитоп - часть антигенного пептида, непосредственно распознаваемая ТКР. Участки антигена, распознаваемые молекулами главного комплекса гистосовместимости (МНС) и Т-клеточным антиген-распознающим рецептором (ТКР)
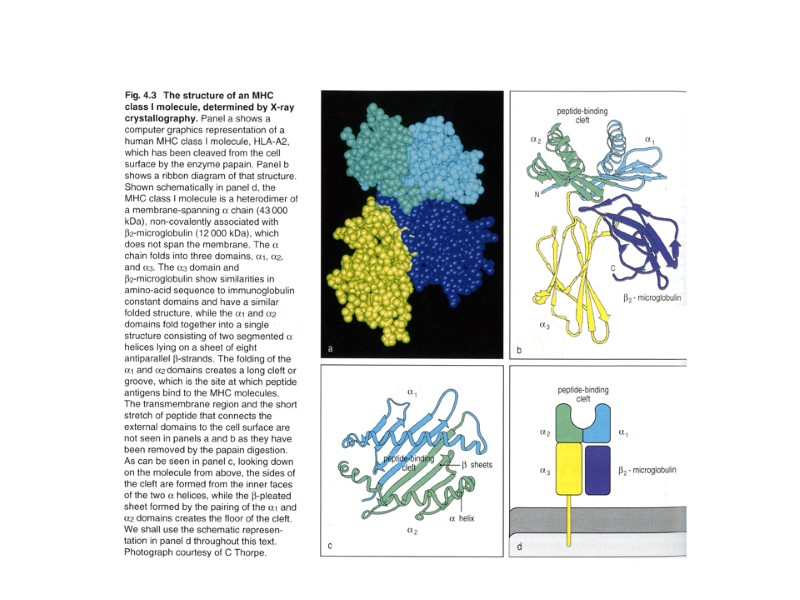
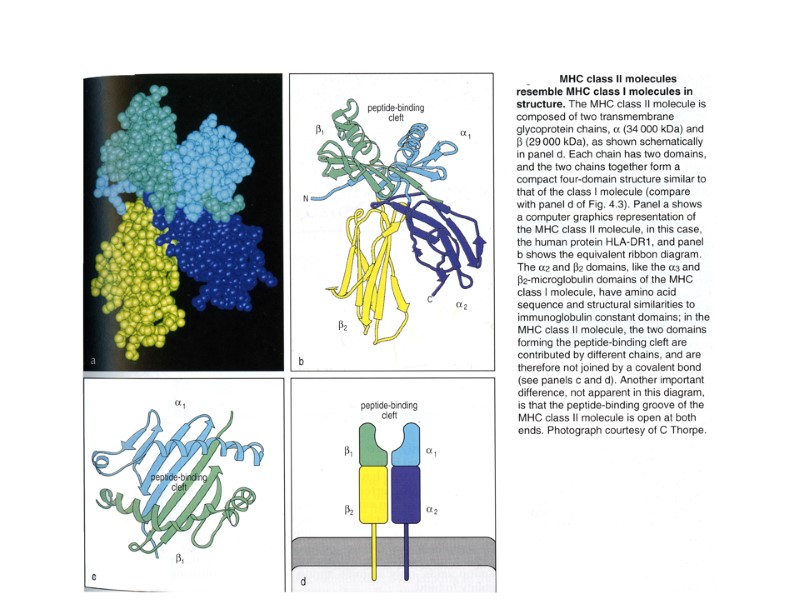
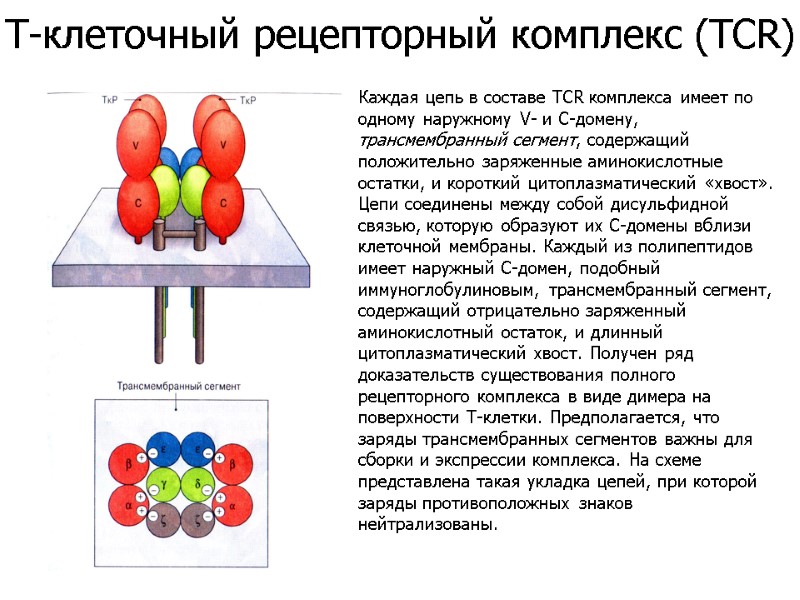
Каждая цепь в составе TCR комплекса имеет по одному наружному V- и С-домену, трансмембранный сегмент, содержащий положительно заряженные аминокислотные остатки, и короткий цитоплазматический «хвост». Цепи соединены между собой дисульфидной связью, которую образуют их С-домены вблизи клеточной мембраны. Каждый из полипептидов имеет наружный С-домен, подобный иммуноглобулиновым, трансмембранный сегмент, содержащий отрицательно заряженный аминокислотный остаток, и длинный цитоплазматический хвост. Получен ряд доказательств существования полного рецепторного комплекса в виде димера на поверхности Т-клетки. Предполагается, что заряды трансмембранных сегментов важны для сборки и экспрессии комплекса. На схеме представлена такая укладка цепей, при которой заряды противоположных знаков нейтрализованы. Т-клеточный рецепторный комплекс (TCR)
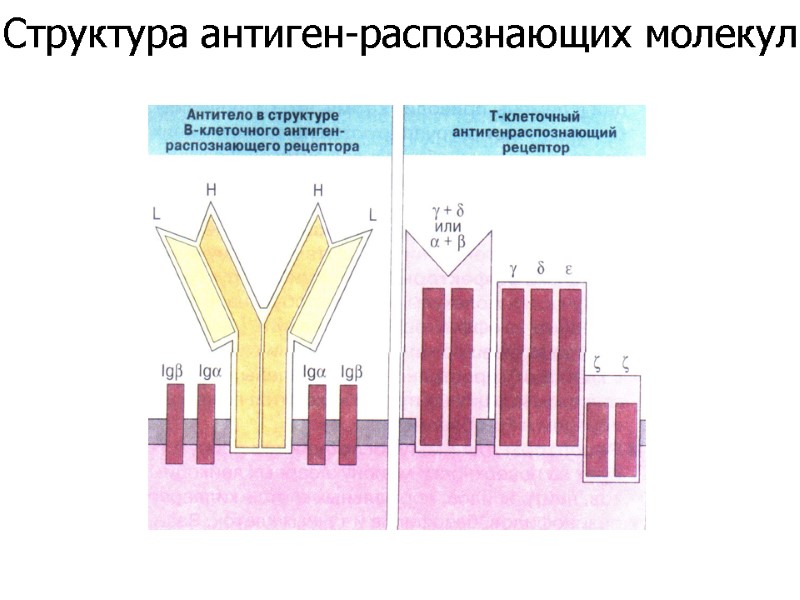
Структура антиген-распознающих молекул
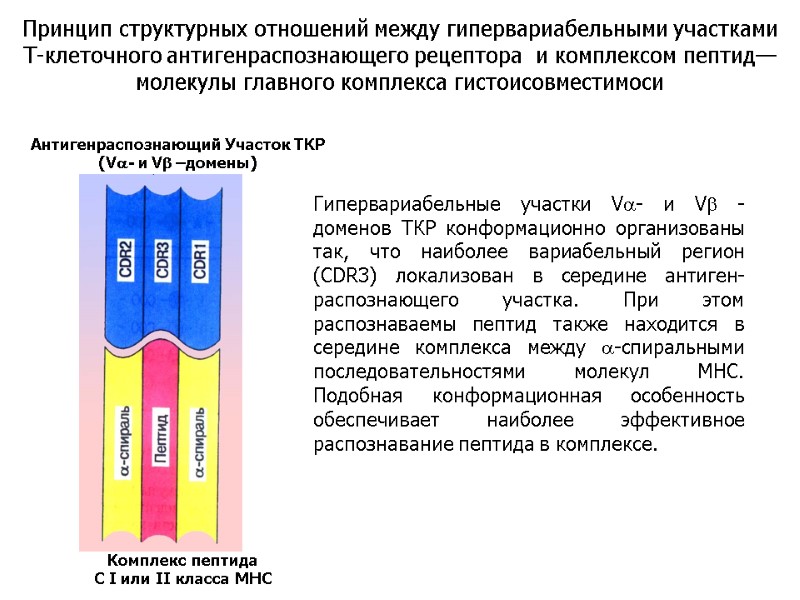
Гипервариабельные участки Va- и Vb -доменов ТКР конформационно организованы так, что наиболее вариабельный регион (CDR3) локализован в середине антиген-распознающего участка. При этом распознаваемы пептид также находится в середине комплекса между a-спиральными последовательностями молекул МНС. Подобная конформационная особенность обеспечивает наиболее эффективное распознавание пептида в комплексе. Антигенраспознающий Участок ТКР (Va- и Vb –домены) Комплекс пептида С I или II класса МНС Принцип структурных отношений между гипервариабельными участками Т-клеточного антигенраспознающего рецептора и комплексом пептид—молекулы главного комплекса гистоисовместимоси
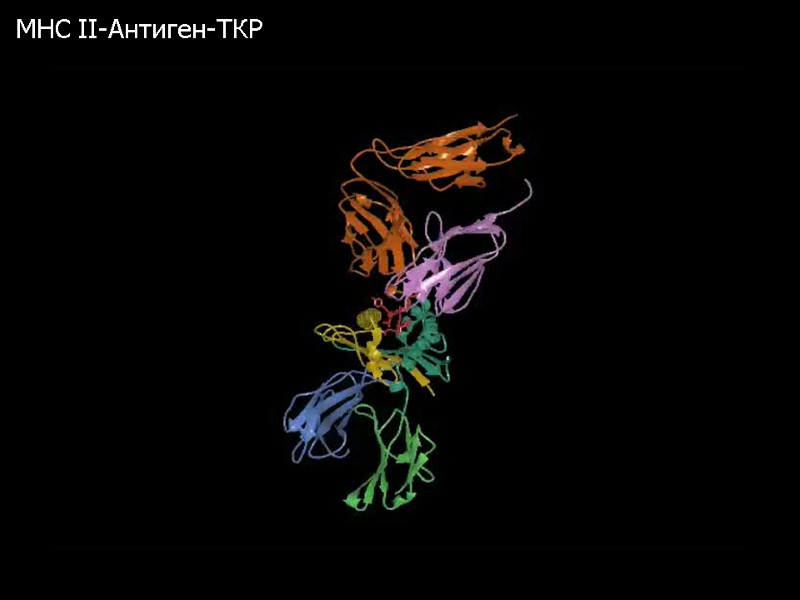
MHC II-Антиген-ТКР
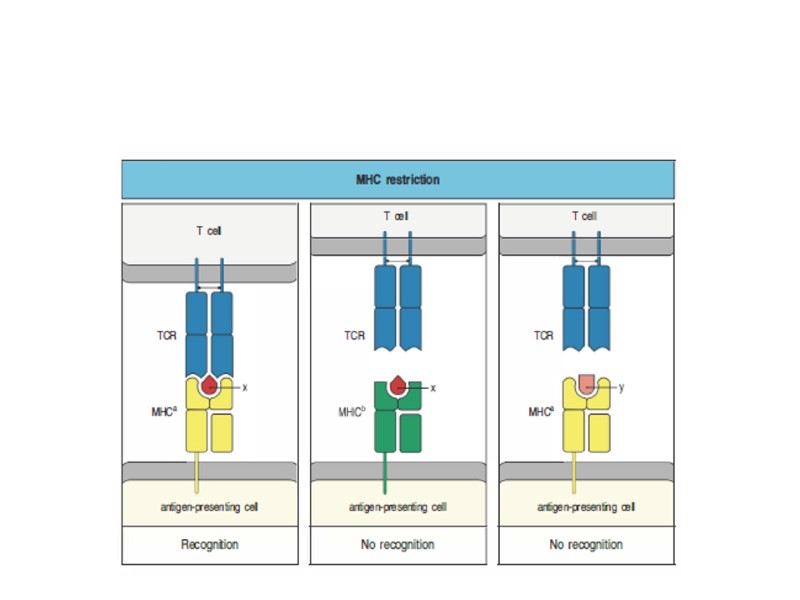
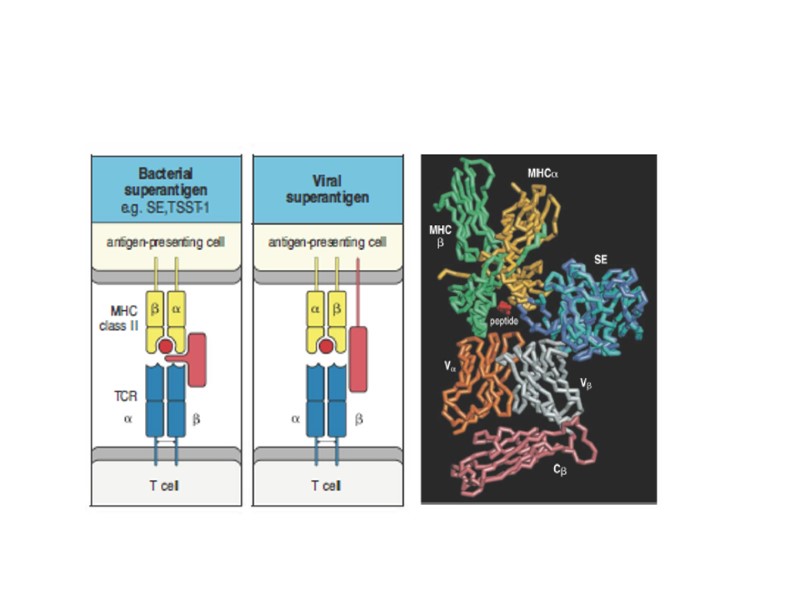

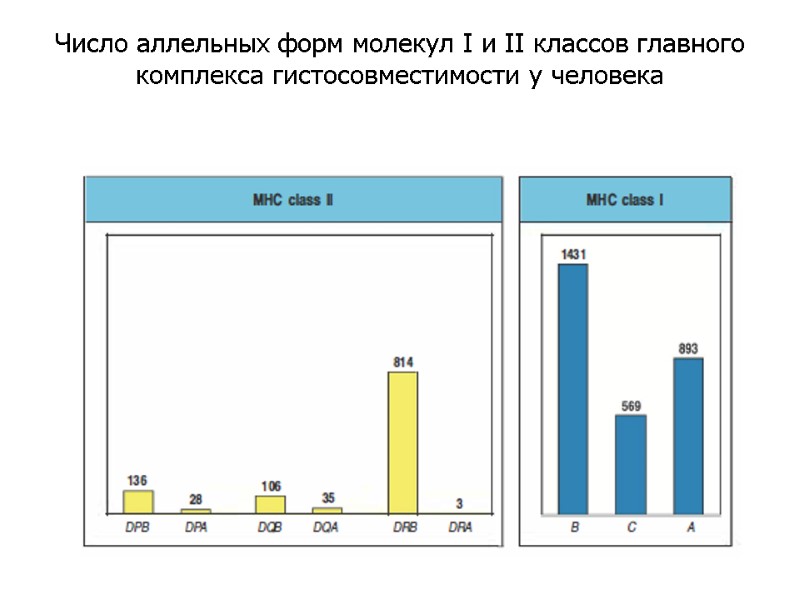
Число аллельных форм молекул I и II классов главного комплекса гистосовместимости у человека
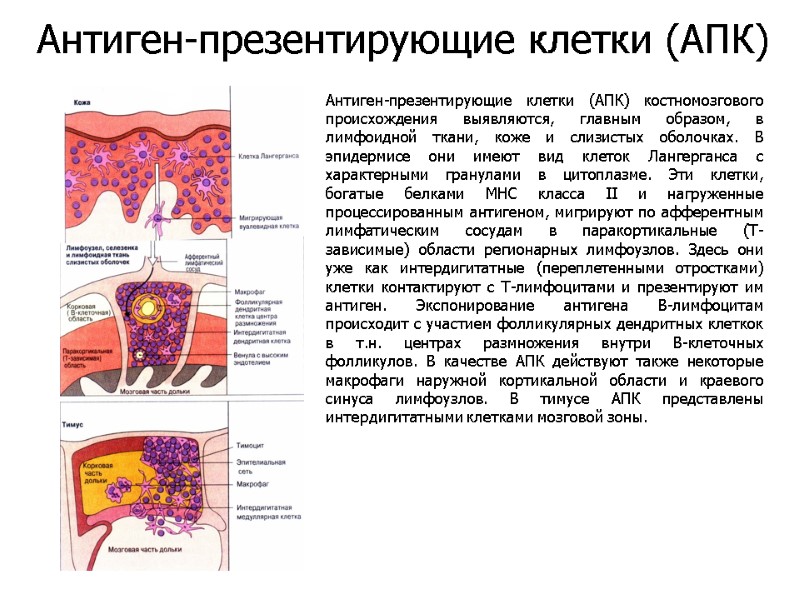
Антиген-презентирующие клетки (АПК) костномозгового происхождения выявляются, главным образом, в лимфоидной ткани, коже и слизистых оболочках. В эпидермисе они имеют вид клеток Лангерганса с характерными гранулами в цитоплазме. Эти клетки, богатые белками МНС класса II и нагруженные процессированным антигеном, мигрируют по афферентным лимфатическим сосудам в паракортикальные (Т-зависимые) области регионарных лимфоузлов. Здесь они уже как интердигитатные (переплетенными отростками) клетки контактируют с Т-лимфоцитами и презентируют им антиген. Экспонирование антигена В-лимфоцитам происходит с участием фолликулярных дендритных клеткок в т.н. центрах размножения внутри В-клеточных фолликулов. В качестве АПК действуют также некоторые макрофаги наружной кортикальной области и краевого синуса лимфоузлов. В тимусе АПК представлены интердигитатными клетками мозговой зоны. Антиген-презентирующие клетки (АПК)
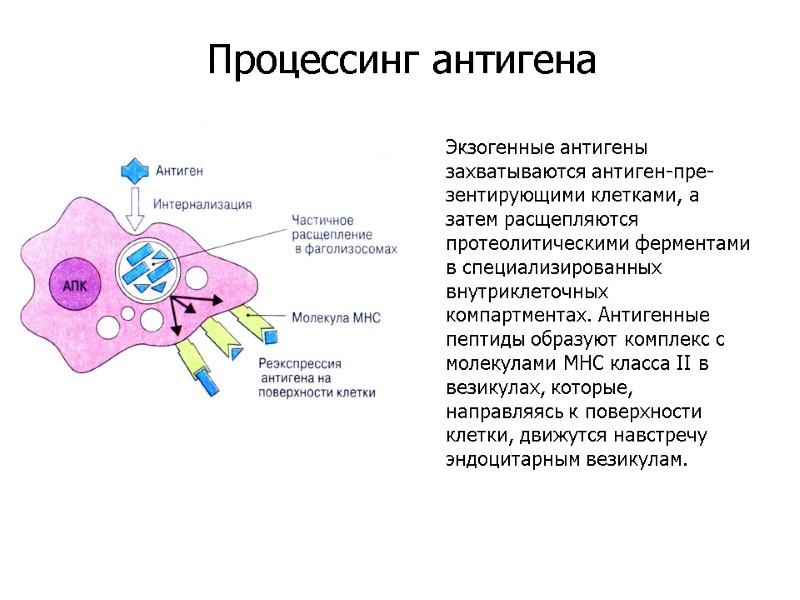
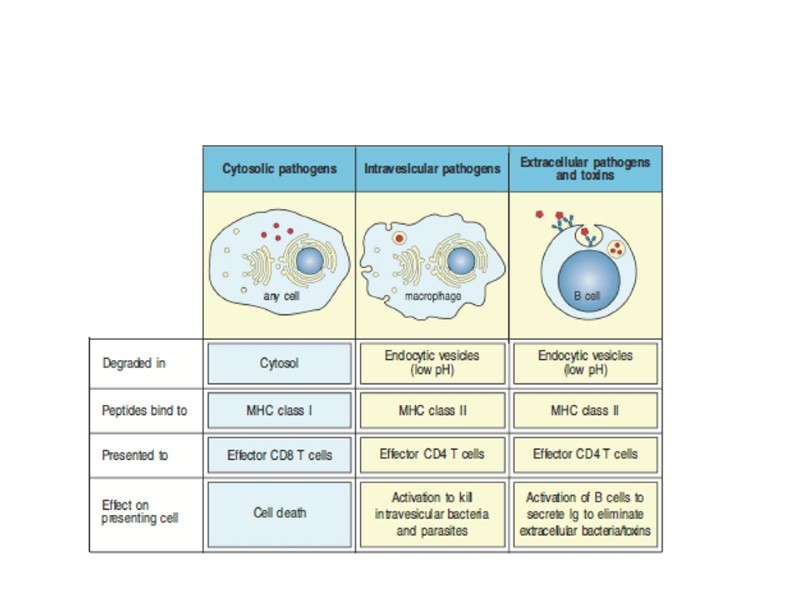
Экзогенные антигены захватываются антиген-пре-зентирующими клетками, а затем расщепляются протеолитическими ферментами в специализированных внутриклеточных компартментах. Антигенные пептиды образуют комплекс с молекулами МНС класса II в везикулах, которые, направляясь к поверхности клетки, движутся навстречу эндоцитарным везикулам. Процессинг антигена
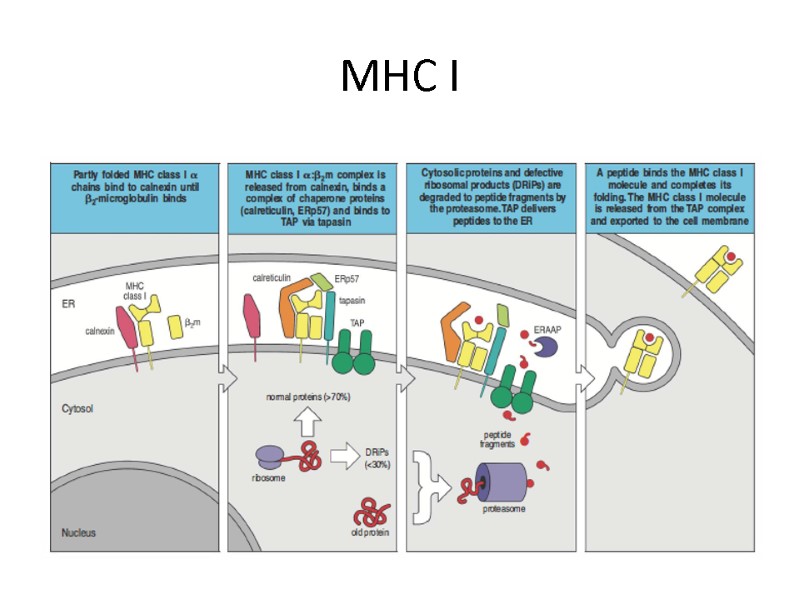
MHC I
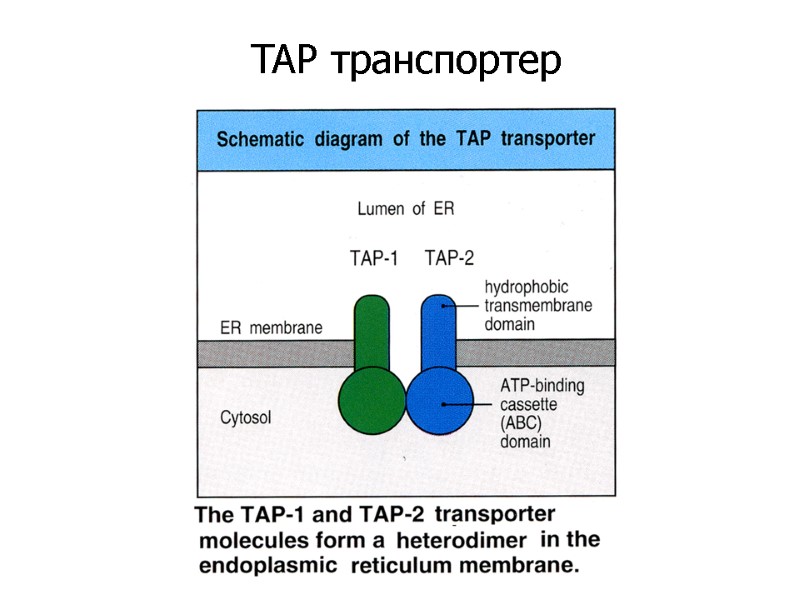
TAP транспортер
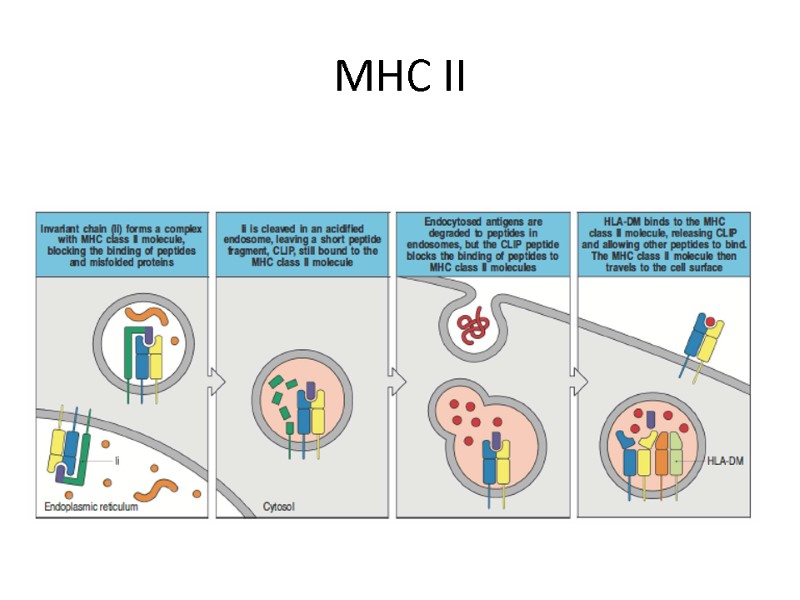
MHC II

BiaCore T-200 высочайшая чувствительность отсутствие метки количественная характеристика взаимодействия возможность определить механизм взаимодействия

MHC класса II M. Hahn et al Nature Immunology 2005
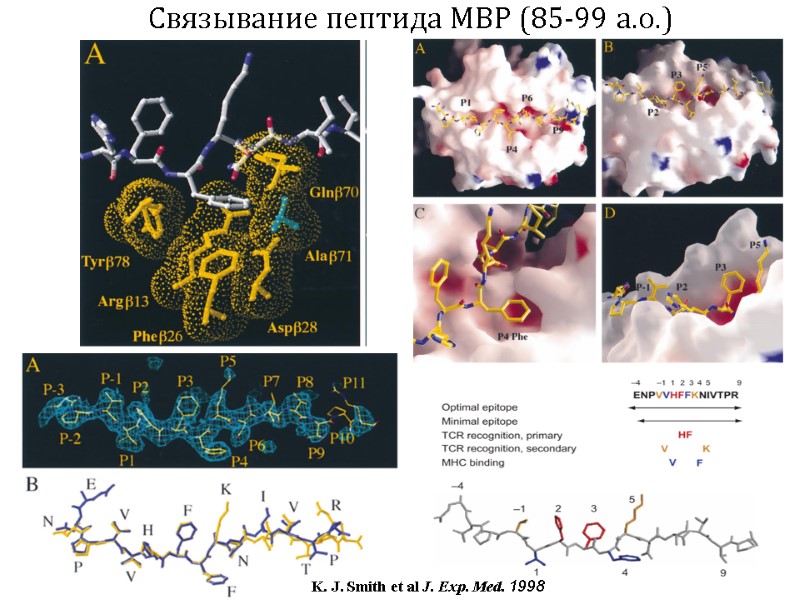
Связывание пептида MBP (85-99 а.о.) K. J. Smith et al J. Exp. Med. 1998
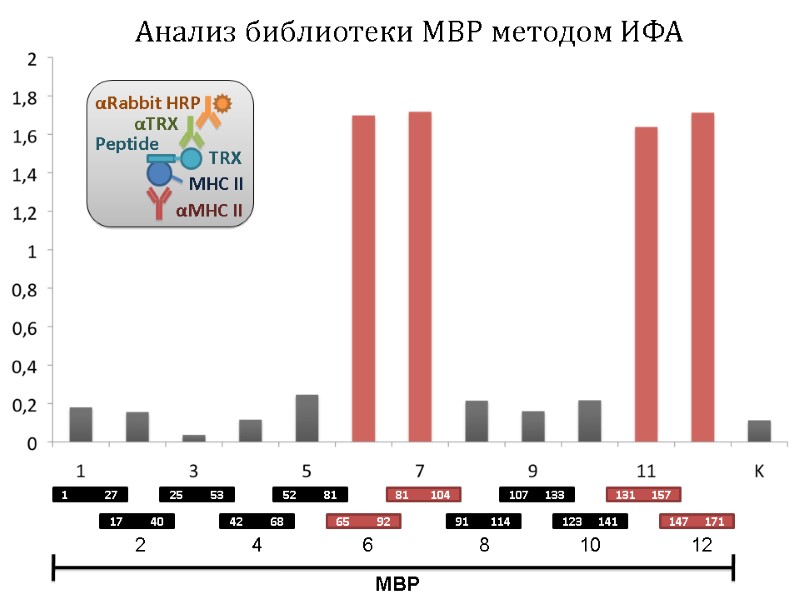
1 27 17 40 25 53 42 68 52 81 65 92 81 104 91 114 107 133 123 141 131 157 147 171 2 4 6 8 10 12 MBP Анализ библиотеки MBP методом ИФА
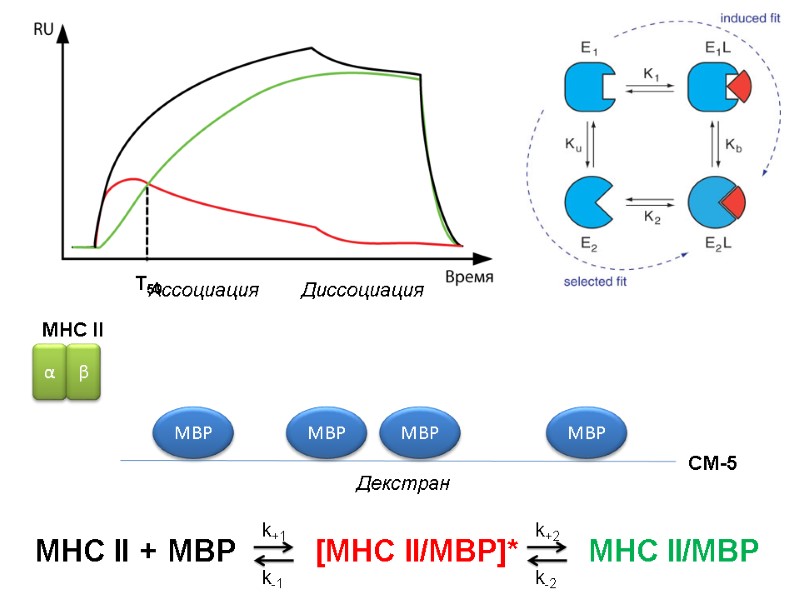
MBP Декстран CM-5 MBP MBP MBP Ассоциация Диссоциация T50
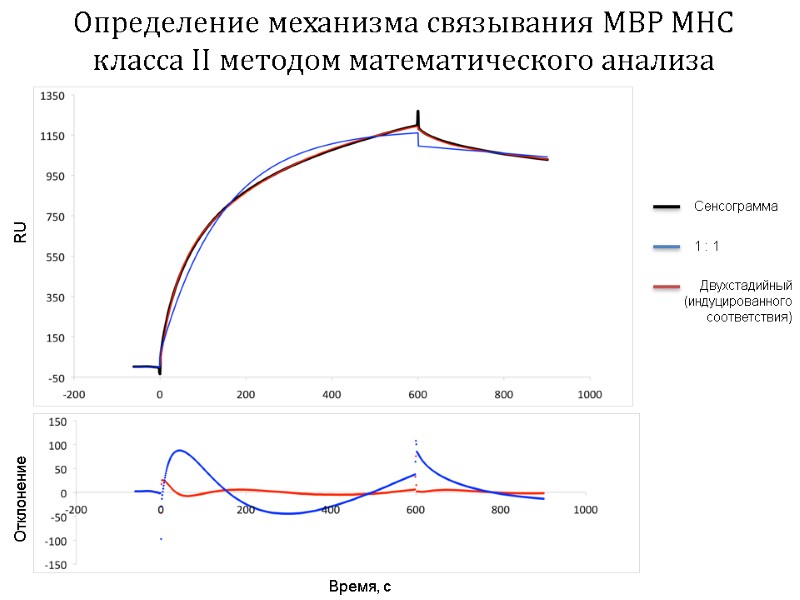
Определение механизма связывания MBP MHC класса II методом математического анализа Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Время, с RU Отклонение
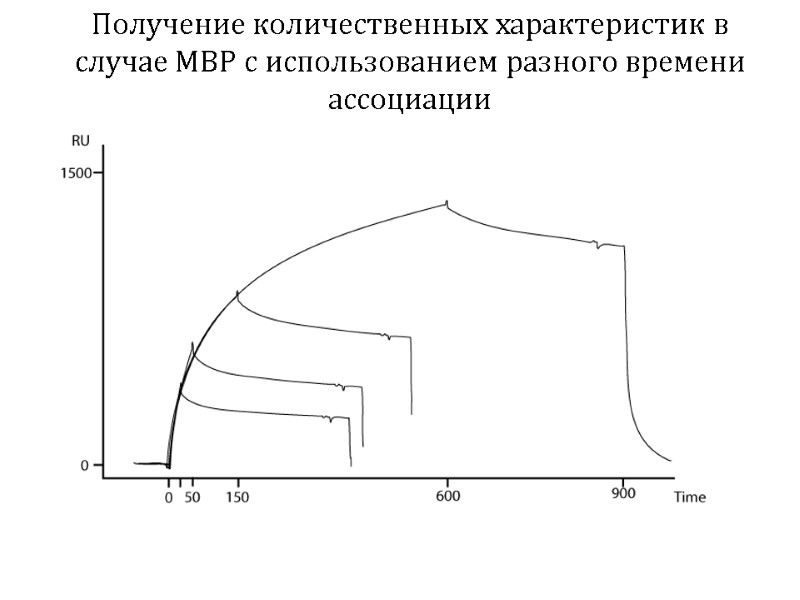
Получение количественных характеристик в случае MBP с использованием разного времени ассоциации
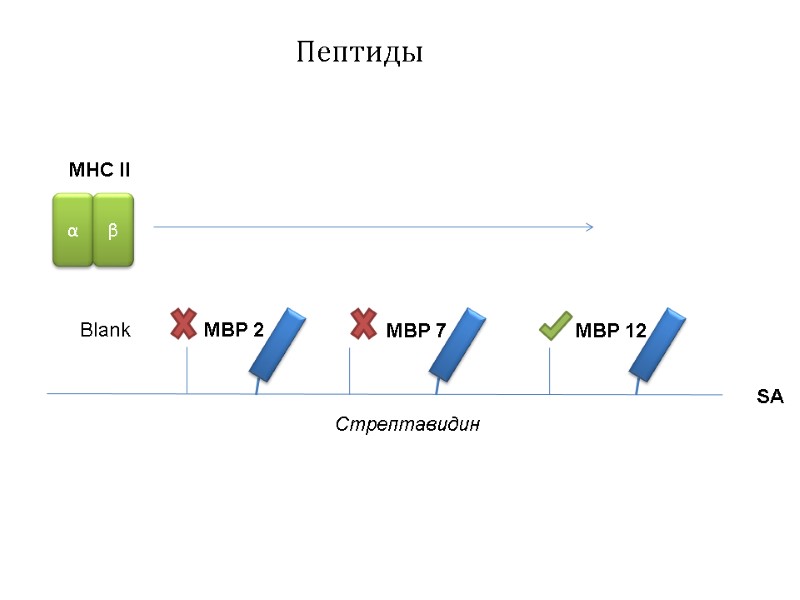
Пептиды Стрептавидин MBP 2 MBP 7 MBP 12 SA Blank
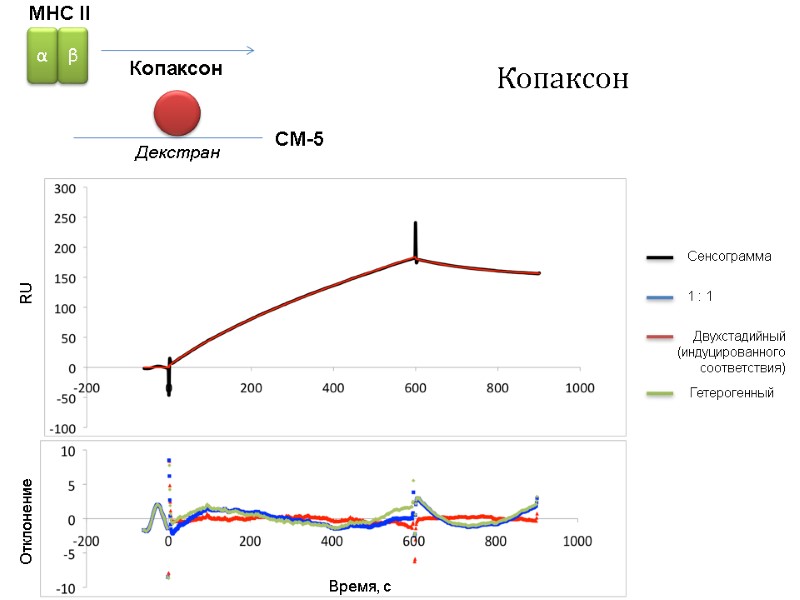
Копаксон Сенсограмма 1 : 1 Двухстадийный (индуцированного соответствия) Гетерогенный Время, с RU Отклонение
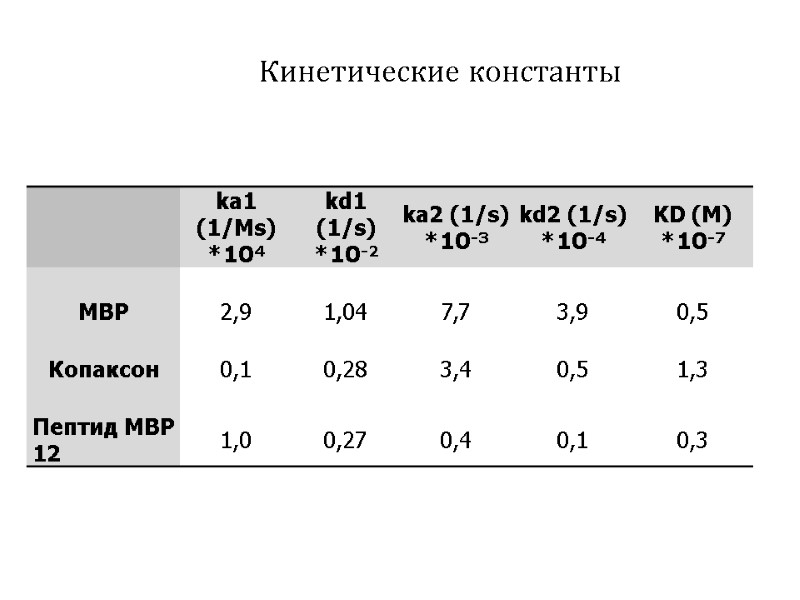
Кинетические константы
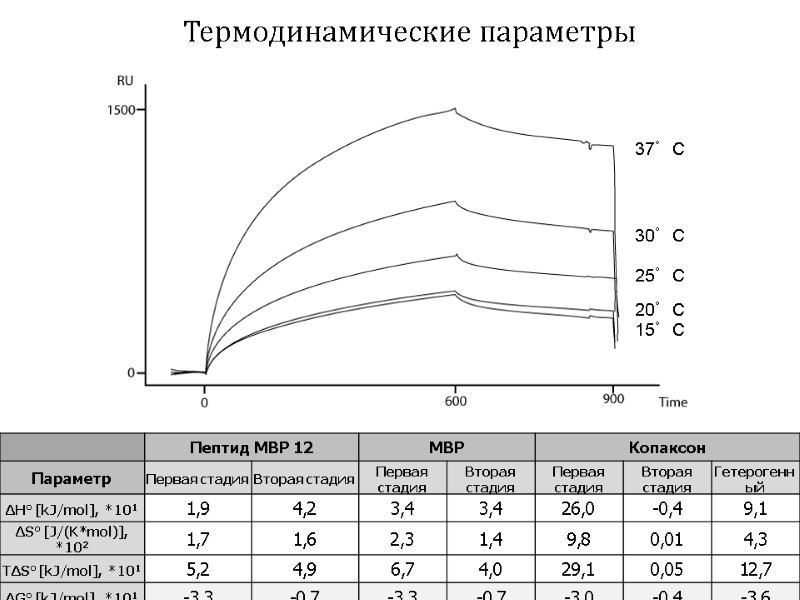
Термодинамические параметры 37°С 30°С 25°С 20°С 15°С
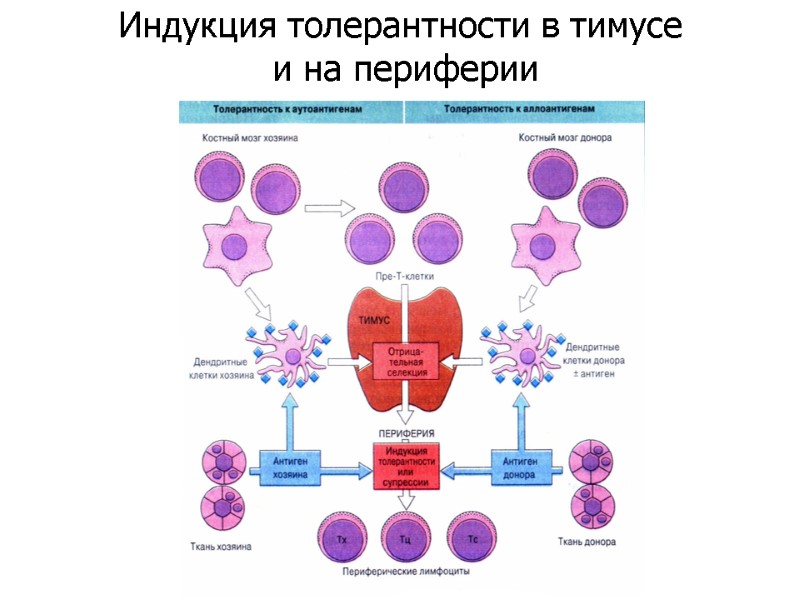
Индукция толерантности в тимусе и на периферии
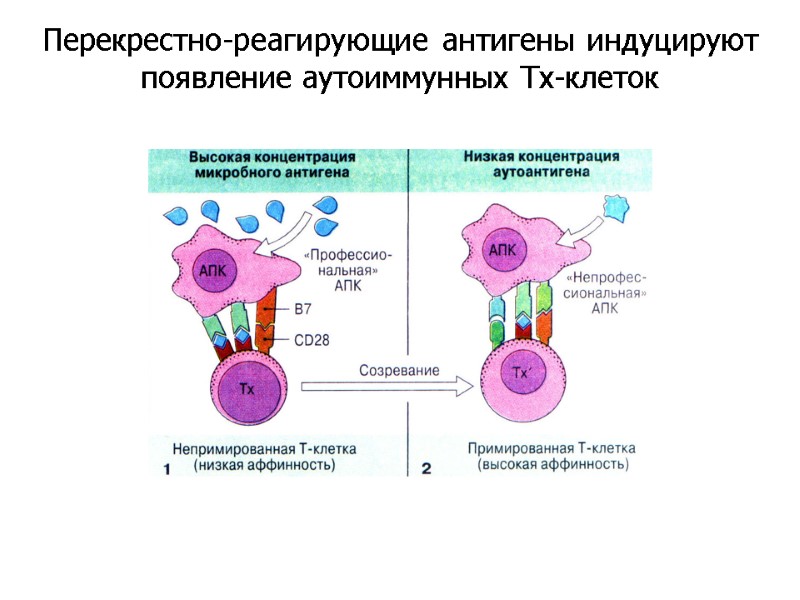
Перекрестно-реагирующие антигены индуцируют появление аутоиммунных Тх-клеток

b Molecular Mimicry (viral or bacterlial infection) Dendritic Cell/B Cell Release of sequestered antigen Breakdown of T-cell supression Abnormalily in the thymic selection process Macrophage Activated TH cell Target tissue epithelium Antiself antibodies Help Inflammation and local DTH TISSUE DAMAGE Аутореактивные Т-клетки
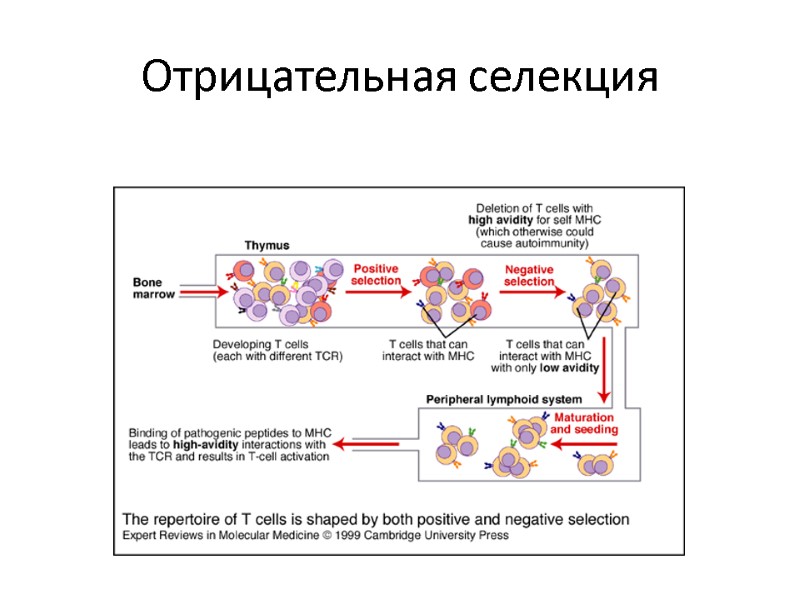
Отрицательная селекция
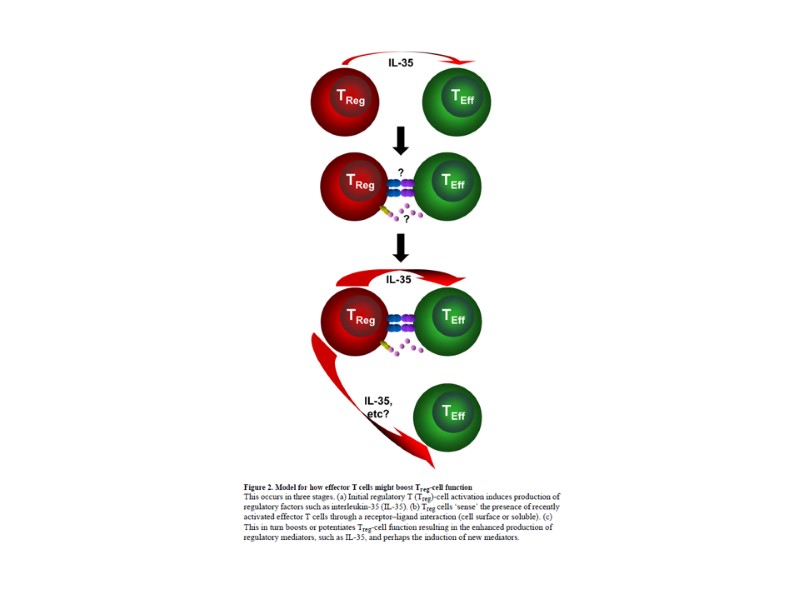
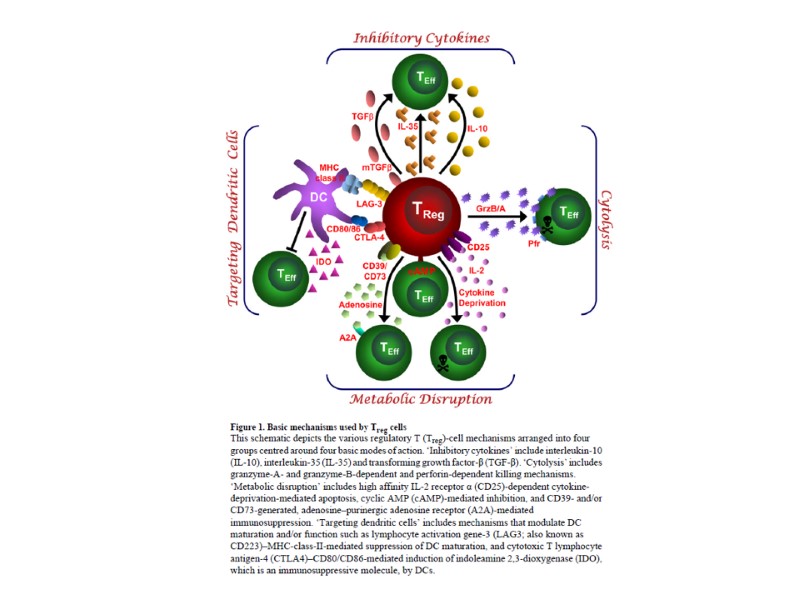
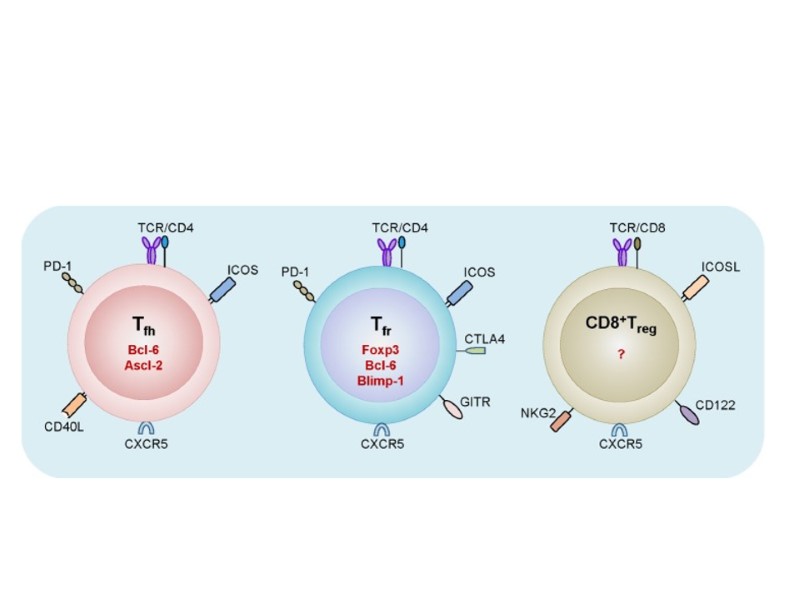
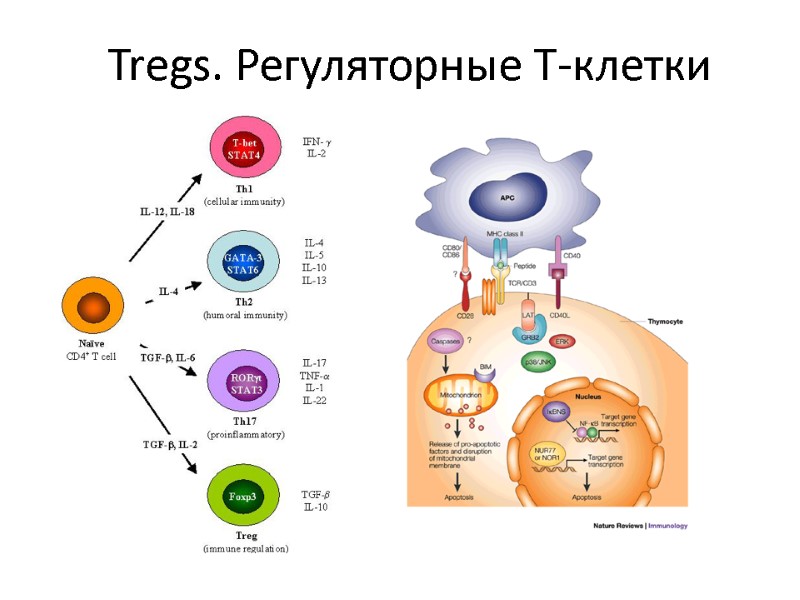
Tregs. Регуляторные Т-клетки
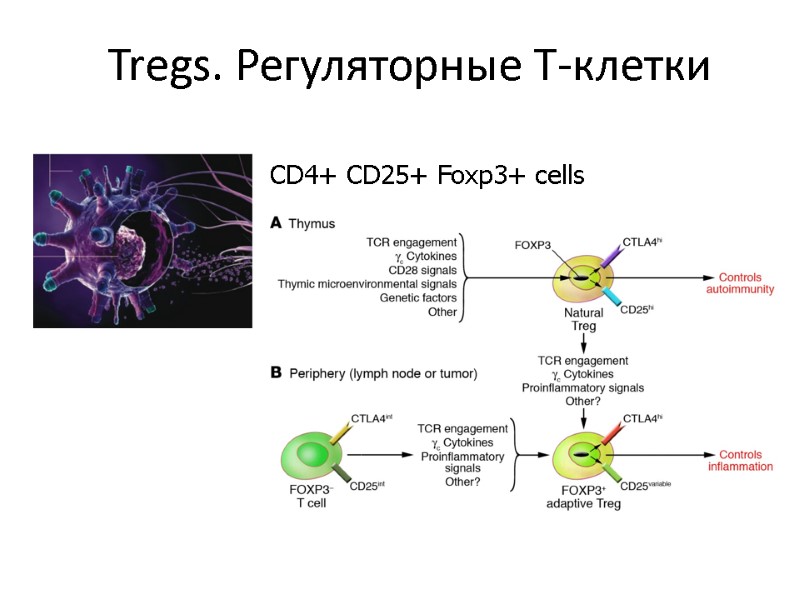
Tregs. Регуляторные Т-клетки CD4+ CD25+ Foxp3+ cells
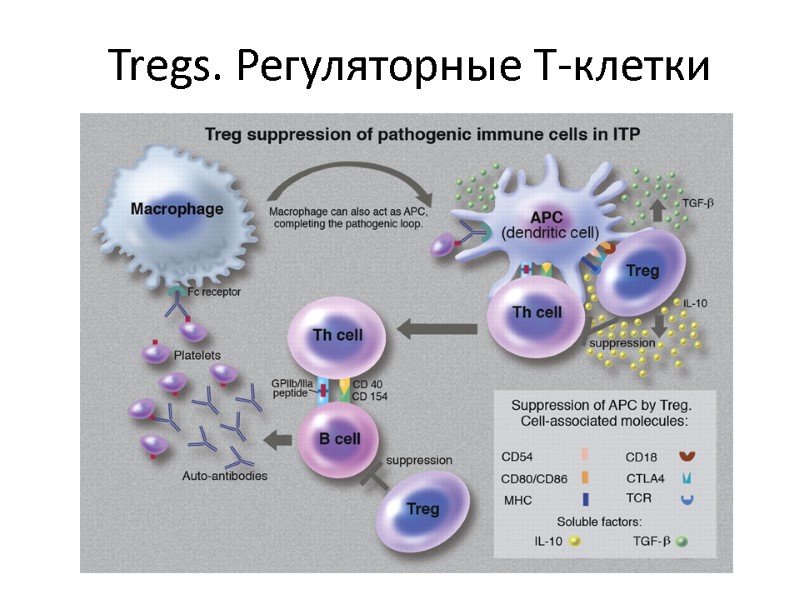
Tregs. Регуляторные Т-клетки
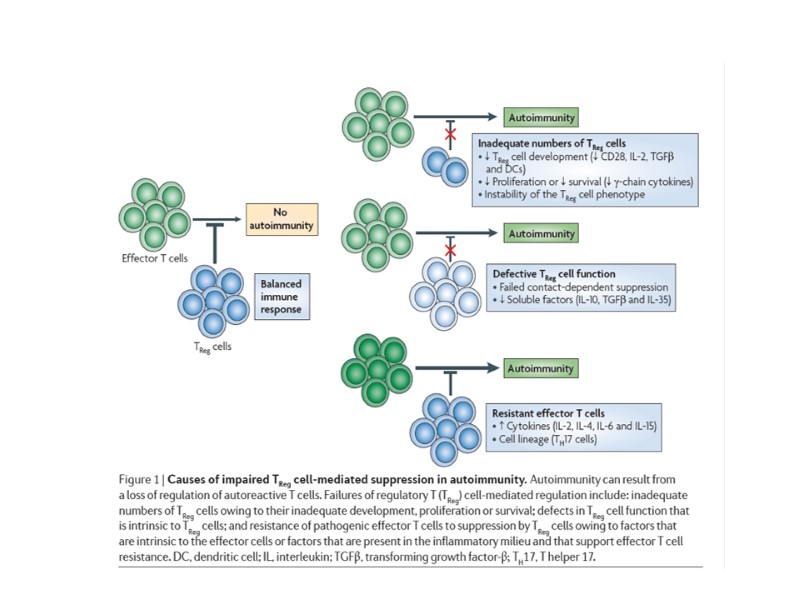
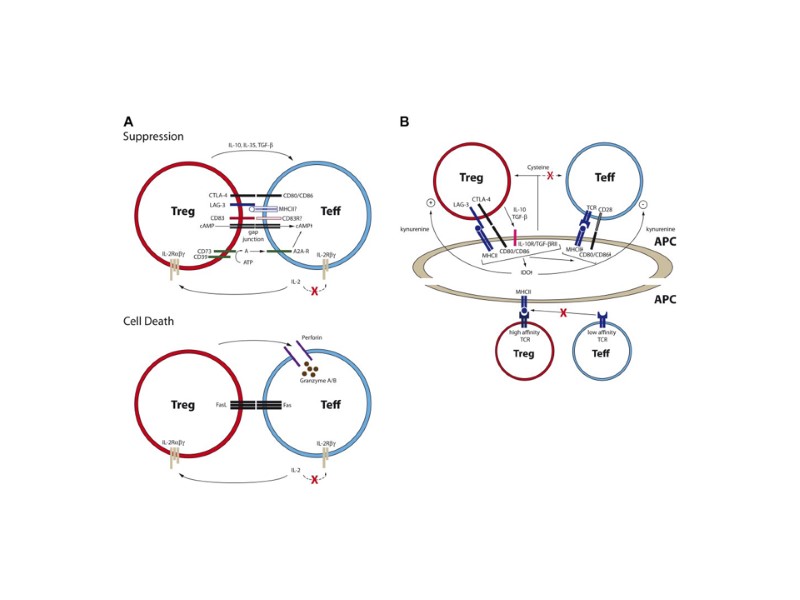
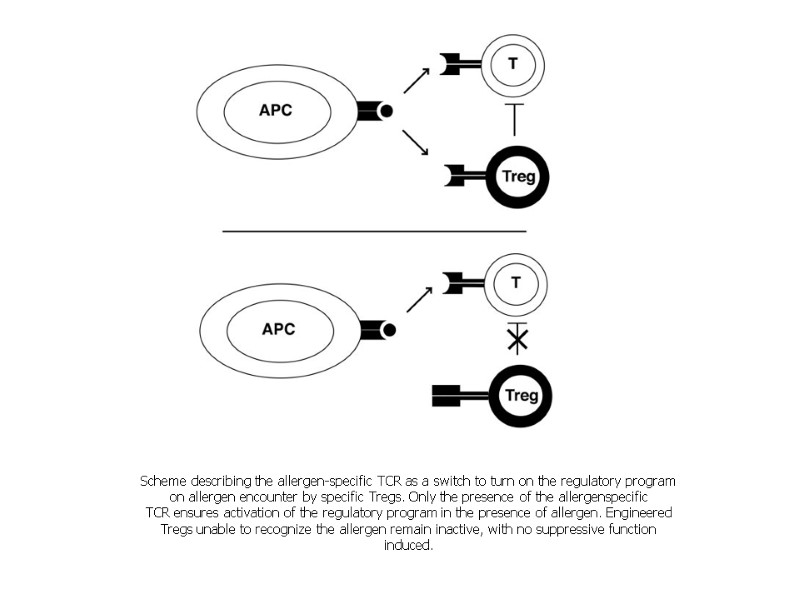
Scheme describing the allergen-specific TCR as a switch to turn on the regulatory program on allergen encounter by specific Tregs. Only the presence of the allergenspecific TCR ensures activation of the regulatory program in the presence of allergen. Engineered Tregs unable to recognize the allergen remain inactive, with no suppressive function induced.
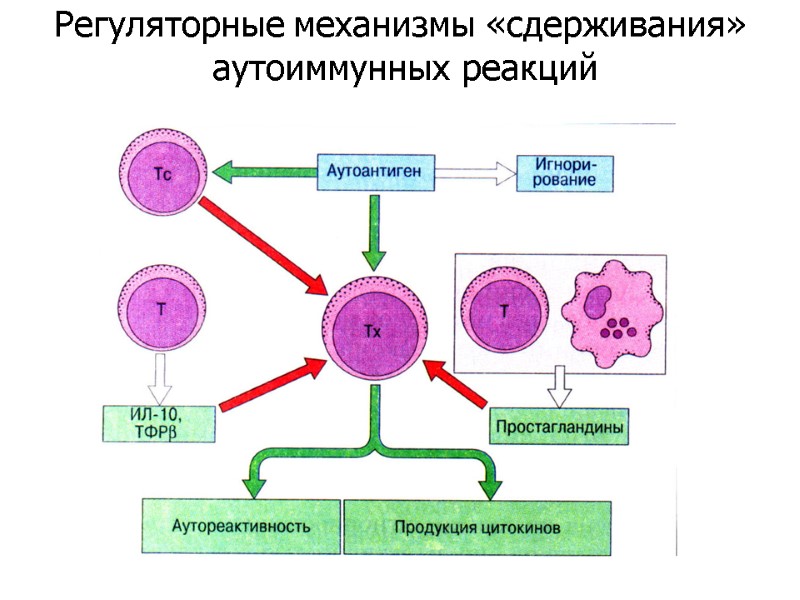
Регуляторные механизмы «сдерживания» аутоиммунных реакций
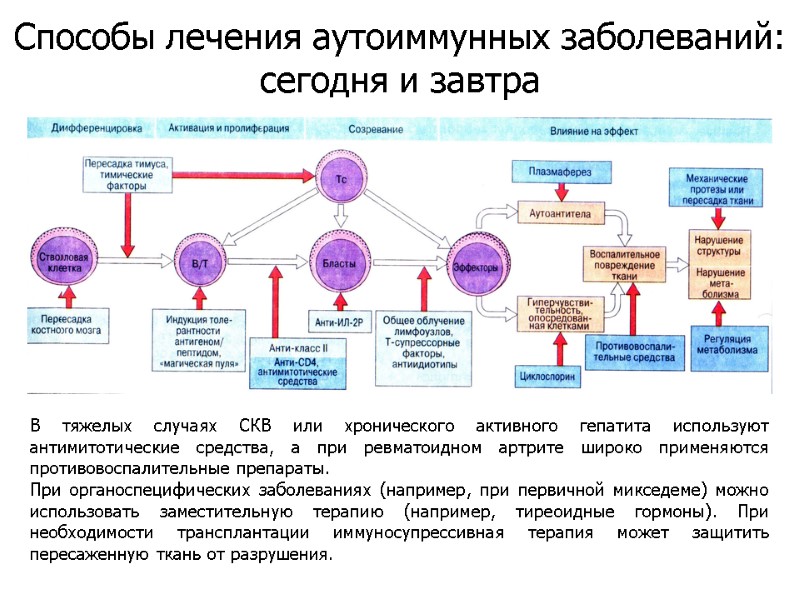
В тяжелых случаях СКВ или хронического активного гепатита используют антимитотические средства, а при ревматоидном артрите широко применяются противовоспалительные препараты. При органоспецифических заболеваниях (например, при первичной микседеме) можно использовать заместительную терапию (например, тиреоидные гормоны). При необходимости трансплантации иммуносупрессивная терапия может защитить пересаженную ткань от разрушения. Способы лечения аутоиммунных заболеваний: сегодня и завтра
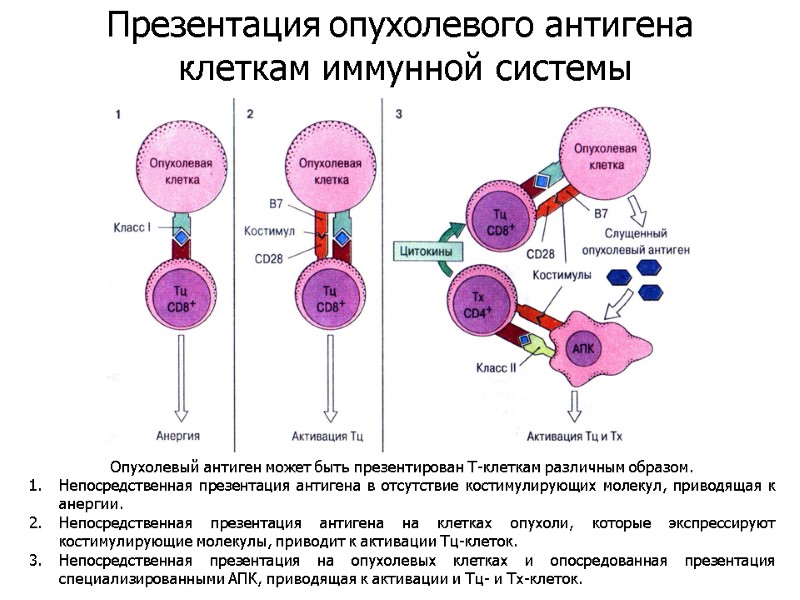
Опухолевый антиген может быть презентирован Т-клеткам различным образом. Непосредственная презентация антигена в отсутствие костимулирующих молекул, приводящая к анергии. Непосредственная презентация антигена на клетках опухоли, которые экспрессируют костимулирующие молекулы, приводит к активации Тц-клеток. Непосредственная презентация на опухолевых клетках и опосредованная презентация специализированными АПК, приводящая к активации и Тц- и Тх-клеток. Презентация опухолевого антигена клеткам иммунной системы
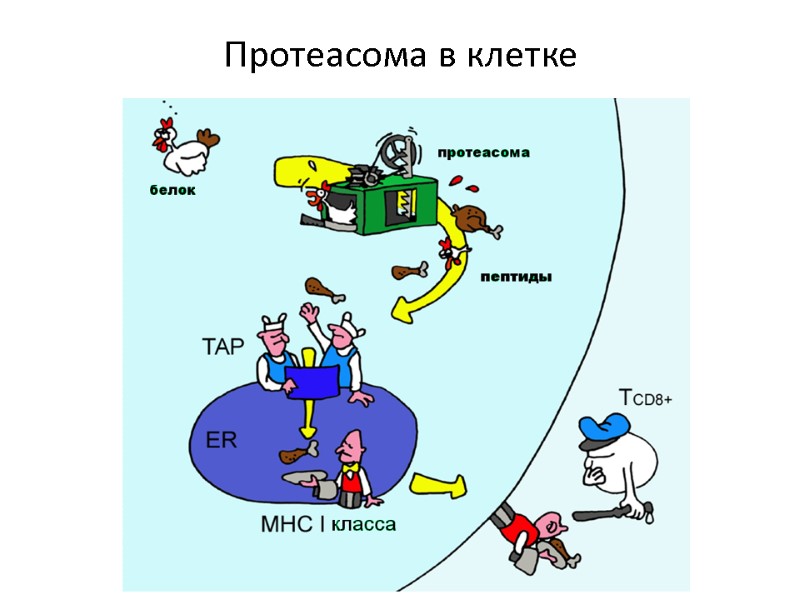
Протеасома в клетке
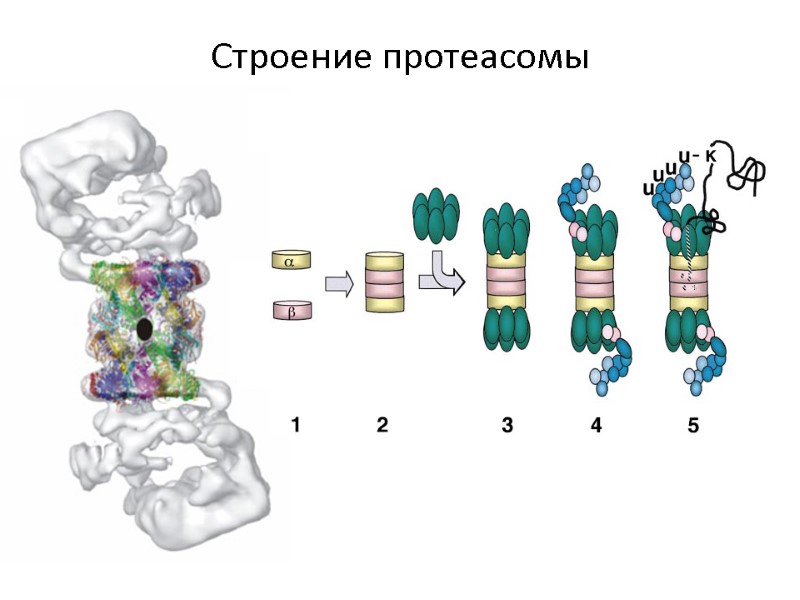
Строение протеасомы
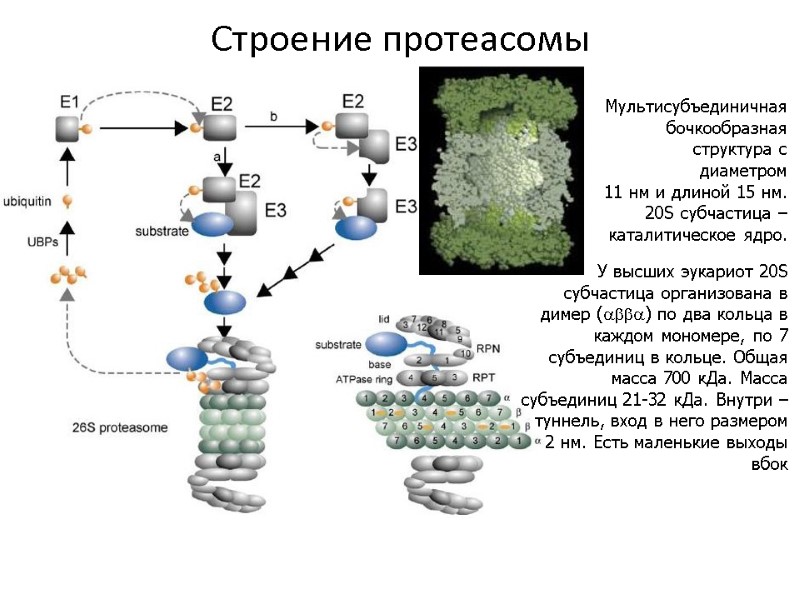
Мультисубъединичная бочкообразная структура с диаметром 11 нм и длиной 15 нм. 20S субчастица – каталитическое ядро. У высших эукариот 20S субчастица организована в димер () по два кольца в каждом мономере, по 7 субъединиц в кольце. Общая масса 700 кДа. Масса субъединиц 21-32 кДа. Внутри – туннель, вход в него размером 2 нм. Есть маленькие выходы вбок Строение протеасомы

Строение активных центров β1 (Y) субъединица проявляет каспазоподобную (пептидилглутамил-пептидгидролазную PGPH) активность, β2 (Z)– активность трипсинового типа (T-L)и β5 (X) обладает химотрипсиноподобной активностью (ChT-L).
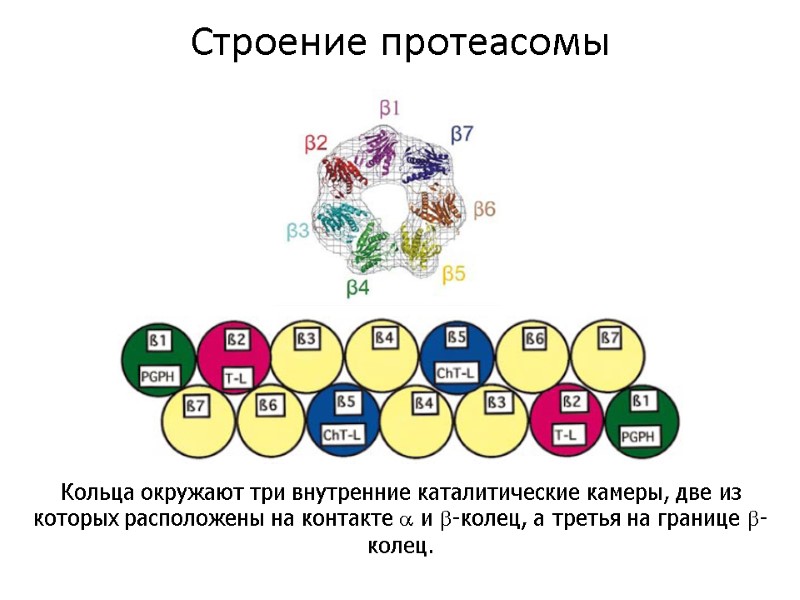
Строение протеасомы Кольца окружают три внутренние каталитические камеры, две из которых расположены на контакте и -колец, а третья на границе -колец.
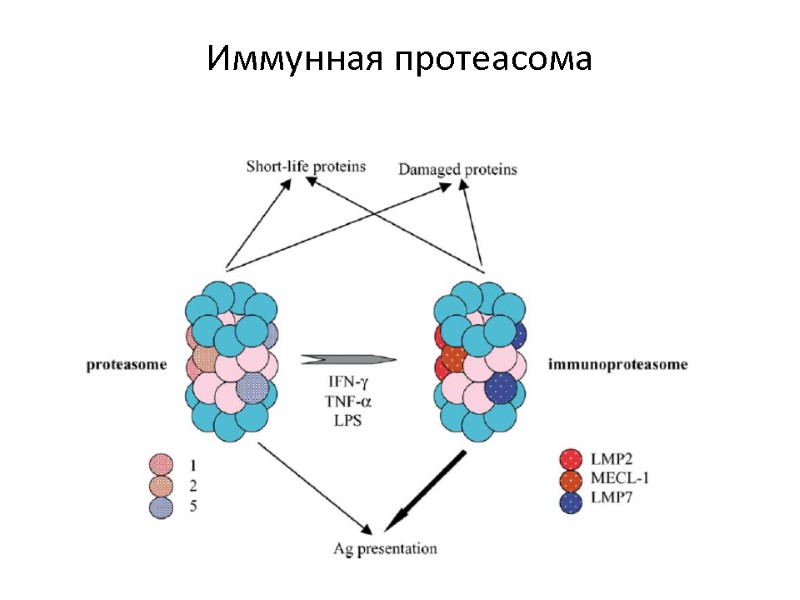
Иммунная протеасома
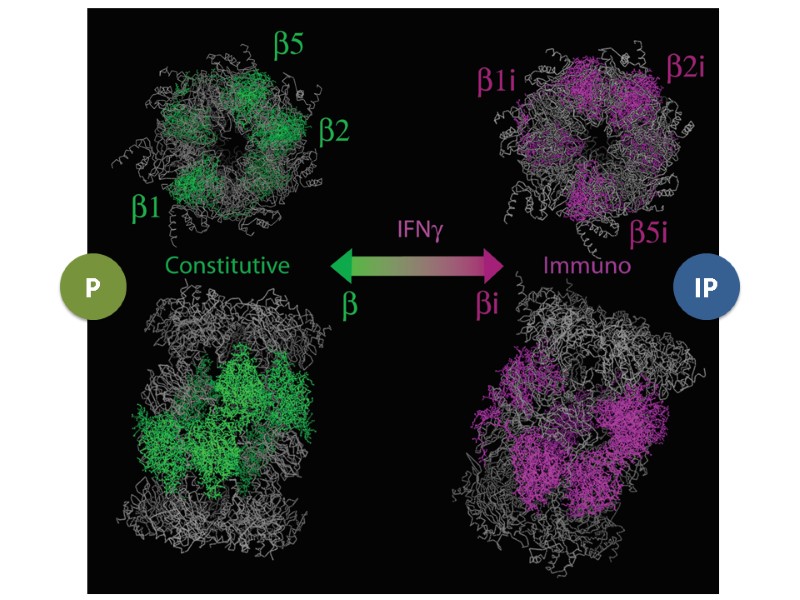
P IP
Brain: near to 100% const proteasome Spleen: 90% immuno proteasome
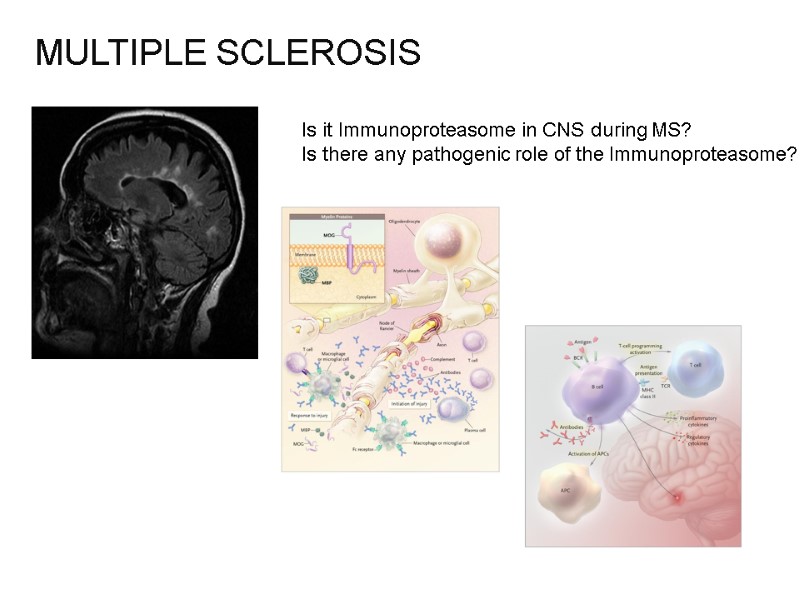
MULTIPLE SCLEROSIS Is it Immunoproteasome in CNS during MS? Is there any pathogenic role of the Immunoproteasome?
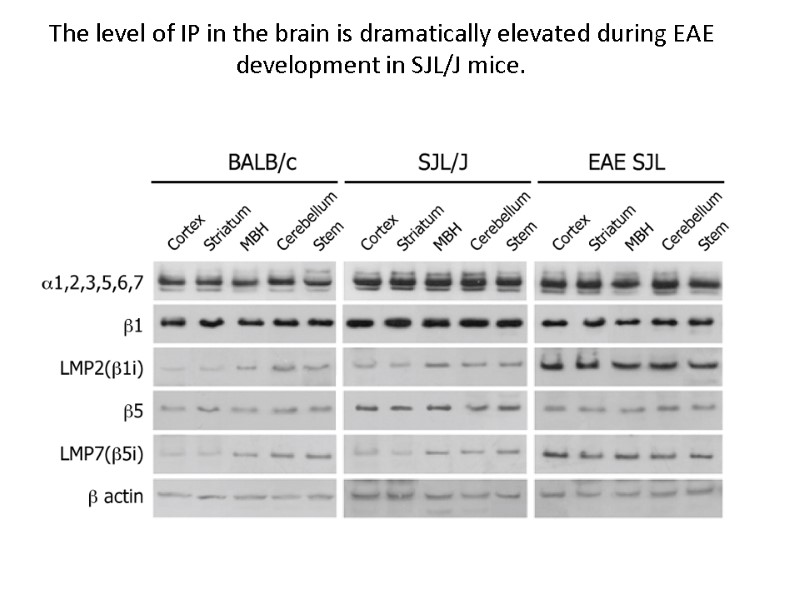
The level of IP in the brain is dramatically elevated during EAE development in SJL/J mice.
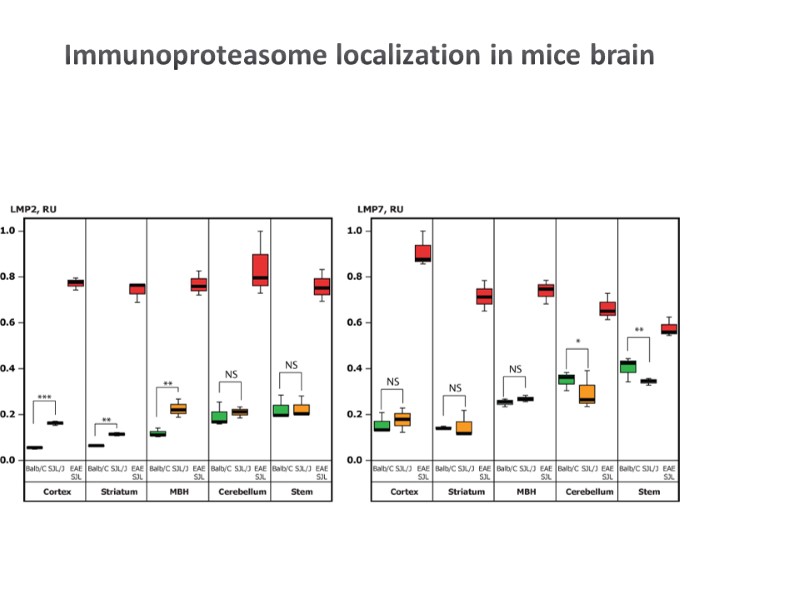
Immunoproteasome localization in mice brain
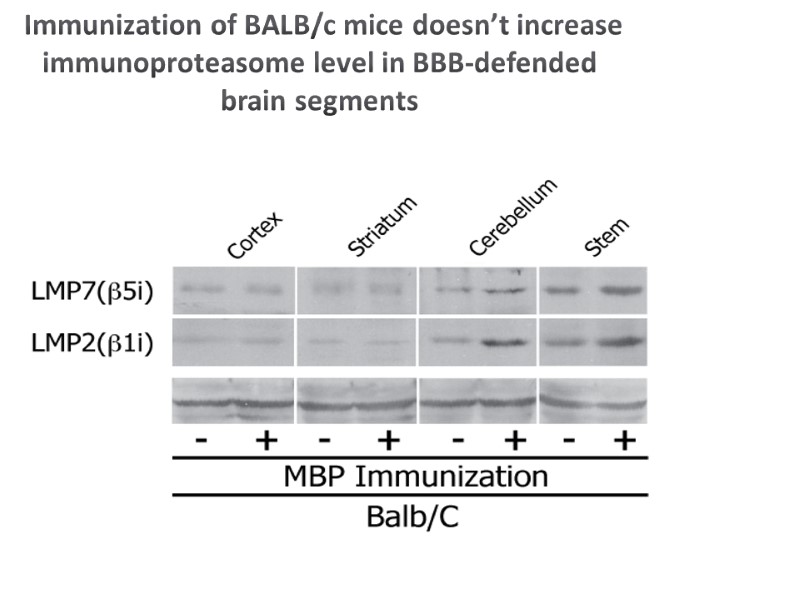
Immunization of BALB/c mice doesn’t increase immunoproteasome level in BBB-defended brain segments
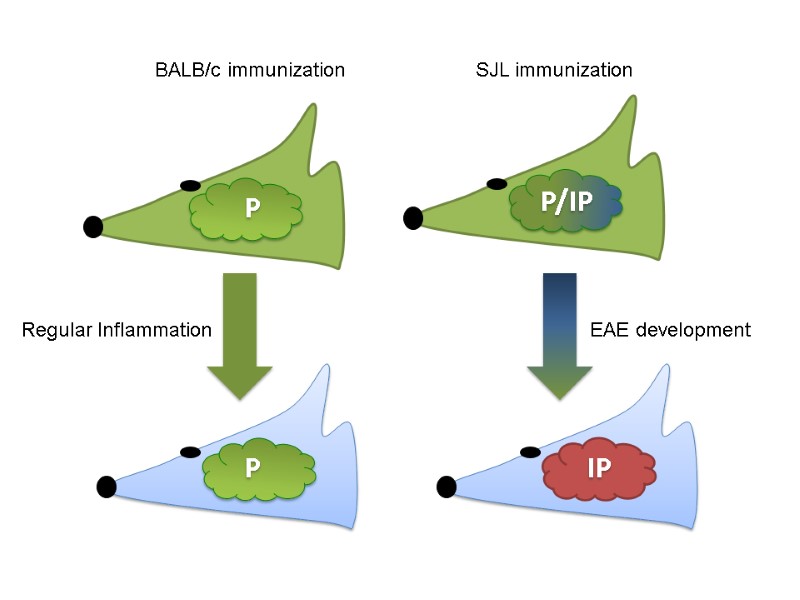
BALB/c immunization SJL immunization Regular Inflammation EAE development P IP P P/IP
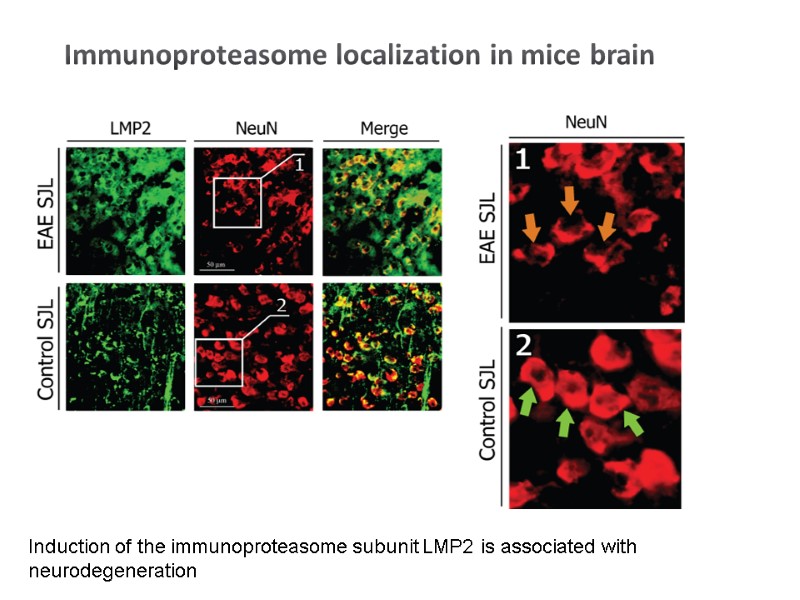
Immunoproteasome localization in mice brain Induction of the immunoproteasome subunit LMP2 is associated with neurodegeneration
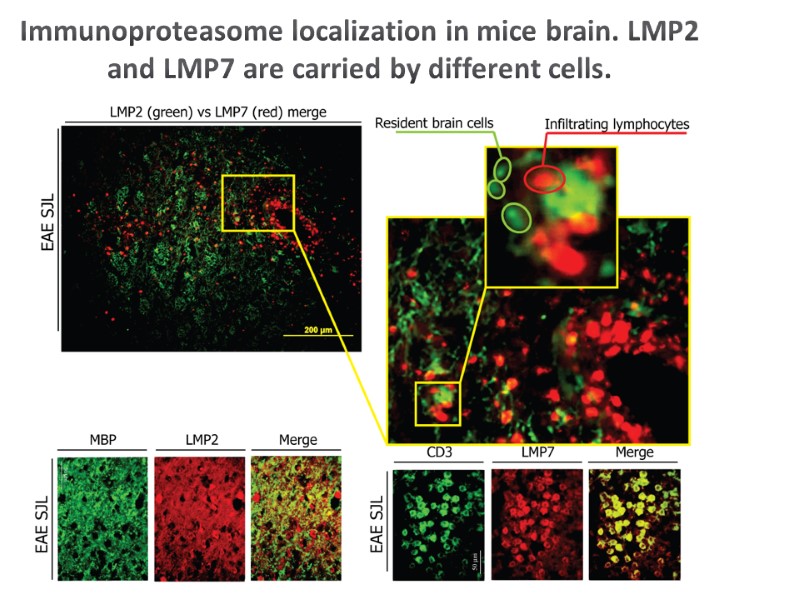
Immunoproteasome localization in mice brain. LMP2 and LMP7 are carried by different cells.
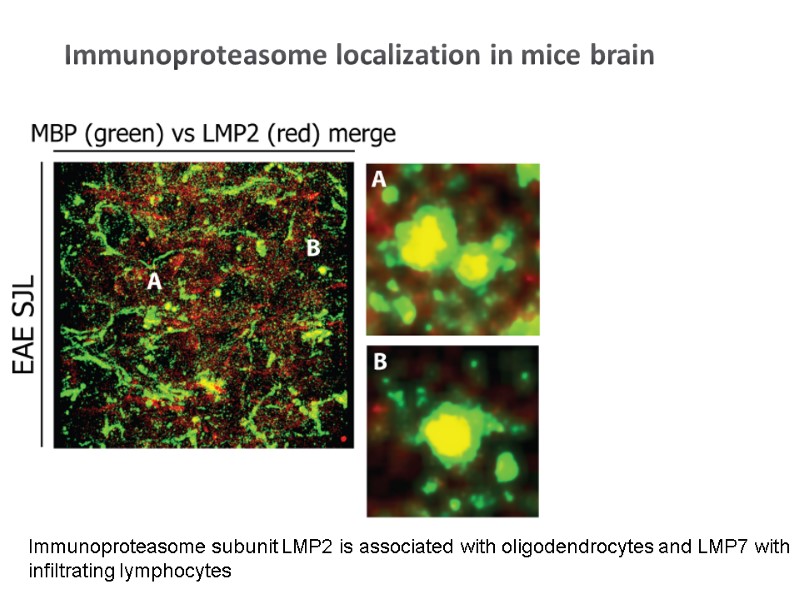
Immunoproteasome localization in mice brain Immunoproteasome subunit LMP2 is associated with oligodendrocytes and LMP7 with infiltrating lymphocytes
The source of immune proteasome is SJL/J EAE mice
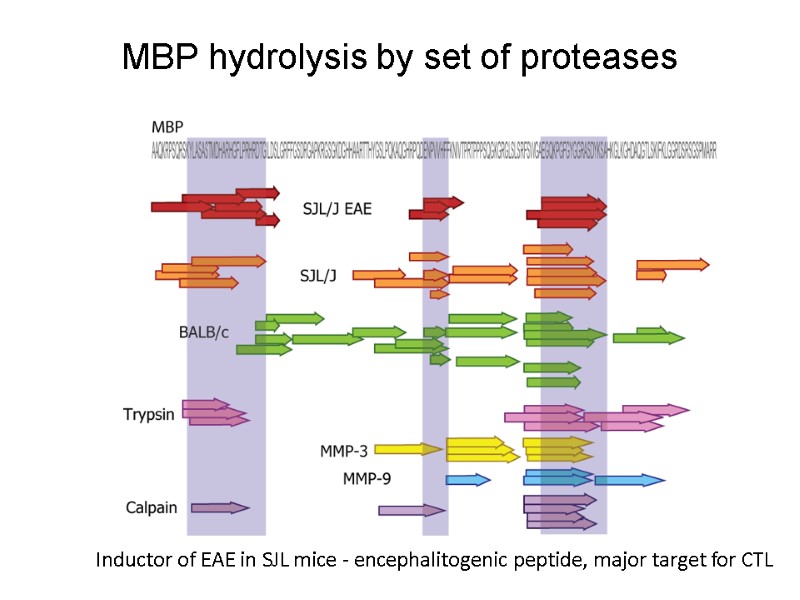
Inductor of EAE in SJL mice - encephalitogenic peptide, major target for CTL MBP hydrolysis by set of proteases
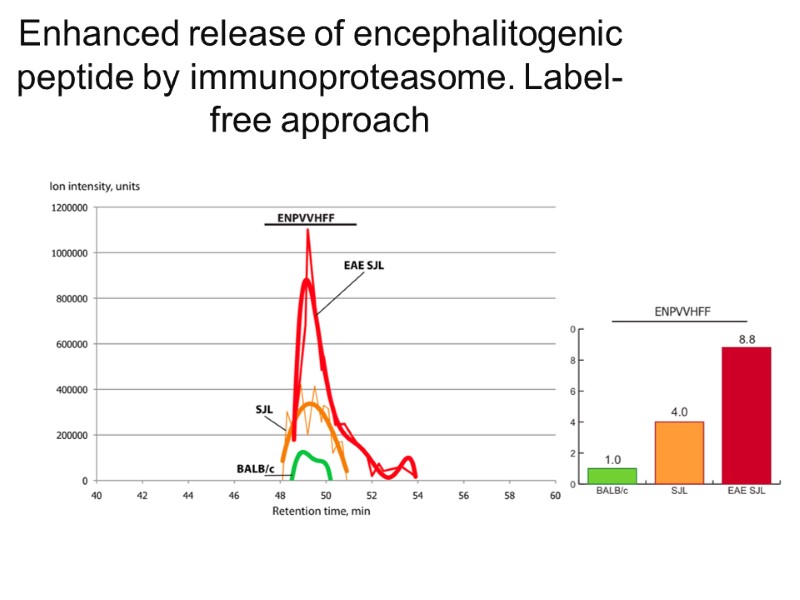
Enhanced release of encephalitogenic peptide by immunoproteasome. Label-free approach

Enhanced release of encephalitogenic peptide by immunoproteasome. LC-ESI approach with Isotope labeled peptide. SJL EAE SJL ENPVVHFF ENPVVHFF* ENPVVHFF ENPVVHFF*
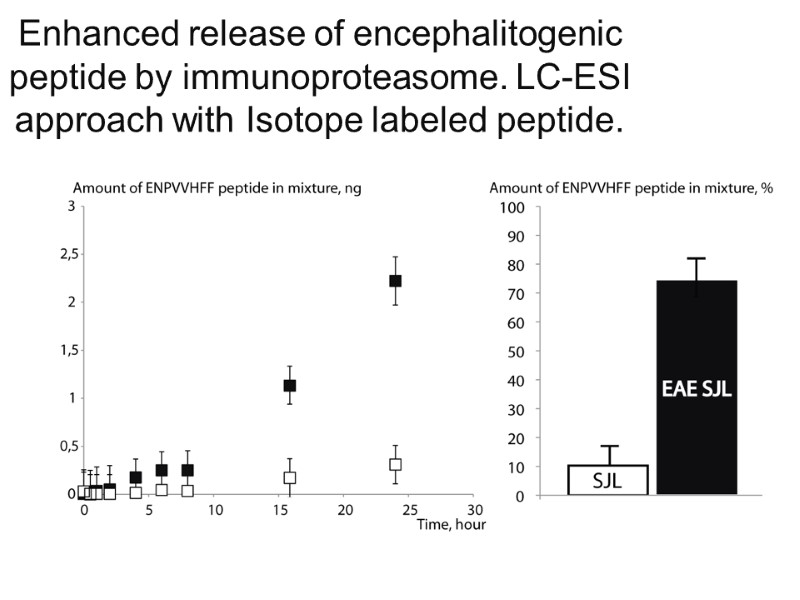
Enhanced release of encephalitogenic peptide by immunoproteasome. LC-ESI approach with Isotope labeled peptide.
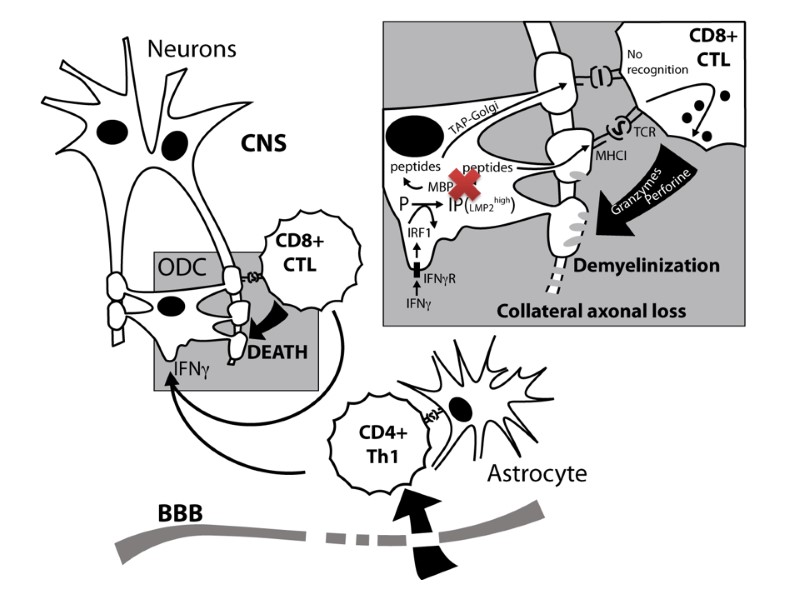

Immunoproteasome marks oligodendrocytes for CTL (immune system) Some kind of target designation

Oligodendrocyte CD4+ Th1 IFNg IFNg CTLs ?

How can we prevent this process? The answer is: Inhibitors or siRNA
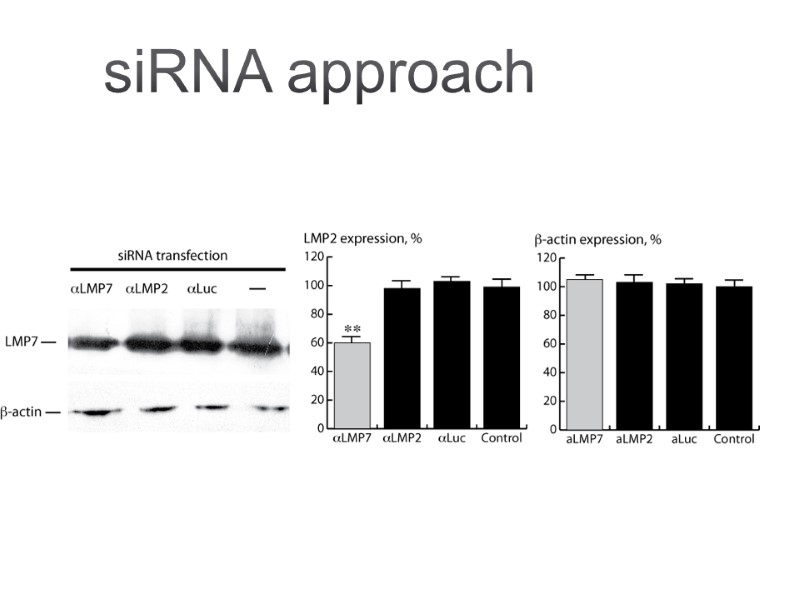
siRNA approach
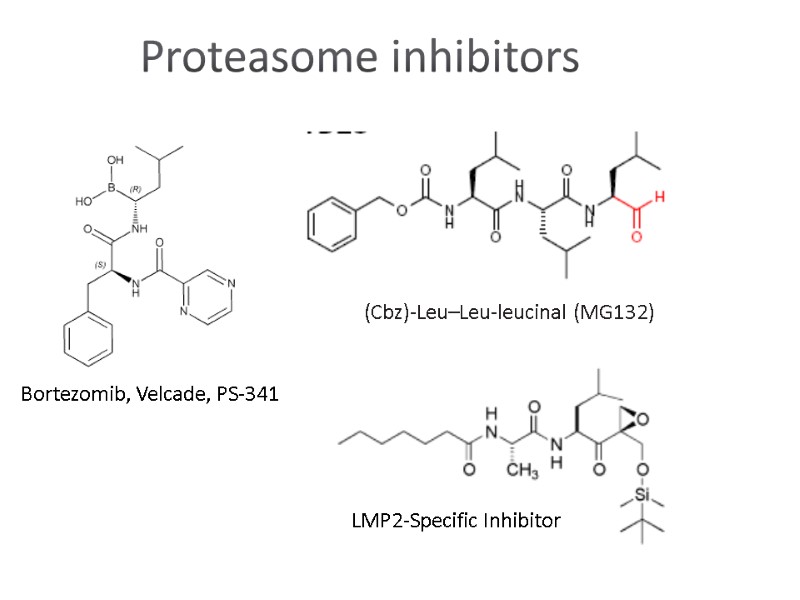
Bortezomib, Velcade, PS-341 (Cbz)-Leu–Leu-leucinal (MG132) LMP2-Specific Inhibitor Proteasome inhibitors
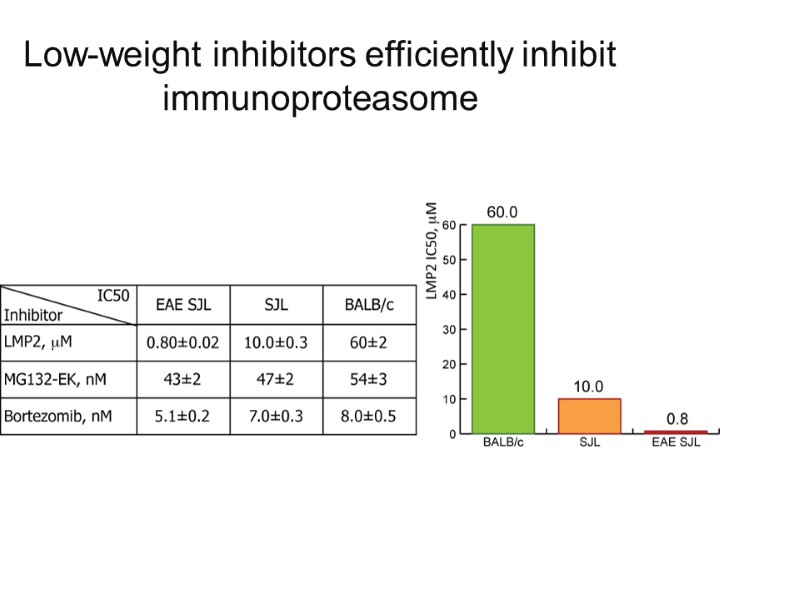
Low-weight inhibitors efficiently inhibit immunoproteasome

Ability of proteasomes from brain tissues of EAE SJL mice to processed MBP peptide epitopes is significantly impeded by LMP-2 specific inhibitor (LMP2), Bortezomib (BZ) and MG132 epoxy ketone (MG132EK)

Autoreactive Cytotoxic Lymphocyte Oligodendrocyte IFNg Proteasome Immunoproteasome Immunoproteasome as a target for MS treatment MHCI TCR Cytotoxicity

Conclusions We have shown that 26S proteasome purified from brain tissues of EAE SJL mice efficiently generates MBP immunodominant fragments, MHC class I restricted peptide ENPVVHFF in particular, due to the dramatically shifted balance between constitutive- versus immuno- proteasomes in CNS. We proposed for how immunoproteasome is mechanistically involved in pathogenesis of autoimmune demyelination; a mechanism providing a link between altered MBP prosessing in oligodendrocytes which marks them to autoreactive CD8+ cytotoxic T-lymphocytes and collateral axonal loss. We also showed that specific inhibitors selectively blocked SJL EAE brain-derived immunoproteosome activity suggesting a novel immunotherapeutic modality for treatment autoimmune neurological diseases.
16604-university_2_2014.ppt
- Количество слайдов: 156

