VA группа.ppt
- Количество слайдов: 57

V группа периодической системы VA-группа

Особенности • Азот, фосфор и в значительной степени мышьяк, стремятся обобщить свои электроны атома-партнёра по связи с образованием ковалентного соединения. Сурьма и висмут – элементы -неметаллы, склонные к образованию ионных гетероатомных соединений. • В степени окисления +5 понижают свою устойчивость в ряду N - Bi. V проявляет свойства сильнейшего окислителя (инертность 6 s 2 -электронной пары) 2

Особенности • Степень окисления азота в его соединениях изменяется в широких пределах – от -3 до +5. • В большинстве соединений азота между атомами азота и других элементов осуществляется ковалентная связь. В соединениях типа Mg 3 N 2 существует в достаточной степени ионная связь азота. • Фосфор отличается от азота наличием 3 dорбитали. Размеры атома фосфора значительно больше, а электроотрицательность в 1, 5 раза меньше, чем у азота. 3

Особенности • Азот склонен к созданию молекулярных структур с очень прочными кратными ковалентными связями (за счёт pπорбиталей азота). Фосфор обычно образует одинарные σ-связи. Большая прочность одинарных связей Р-Р объясняется уменьшением у атома фосфора межэлектронного отталкивания валентных электронов. • Фосфор образует полимеры с одинаковыми связями, а азот – мономолекулярные соединения с кратными связями 4

Особенности • Лёгкая поляризуемость атомов As, Sb и Bi, обусловленная строением электронной оболочки, является причиной быстрого нарастания металлических свойств в ряду P – Bi. 5

Нахождение в природе Азот – основная часть воздуха. В литосфере – в форме различных минералов (селитры). Образование нейтрального азота при взаимодействии в почве: KNO 2 + NH 4 Cl = N 2↑ + KCl + 2 H 2 O Фосфор. Основные минералы: • фосфорит - ЗСа 3(РО 4)2·Са. СО 3·Са(ОН, F)2 • апатит - общая формула Са 5[РО 4]3 Х 2, где Х - обычно F (фторапатит), иногда Сl (хлорапатит). 6

Нахождение в природе Элементы подгруппы мышьяка Принадлежат к числу халькофильных, представлены в основном в виде сульфидов. Мышьяк: реальгар As. S, аурипигмент As 2 S 3, арсенопирит (мышьяковый колчедан) Fe. As. S или Fe. S 2 • Fe. As 2 (промышленное значение), лёллингит Fe. As 2. 7

Нахождение в природе Реальгар As. S Аурипигмент As 2 S 3 8

Нахождение в природе • Сурьма - встречается в самородном виде, минералы - антимонит Sb 2 S 3, сервантит Sb 2 O 4, кермезит Sb 2 S 2 O. Также существуют сурьмяно-ртутные, медносурьмяные, золото-сурьмяные, сурьмяновольфрамовые руды. • Висмут - редкий рассеянный элемент, собственные минералы очень редки. Важнейшие минералы: висмутин, или висмутовый блеск Bi 2 S 3, бисмит Bi 2 O 3. 9

Азот • Относится к т. н. постоянным газам. Имеет очень низкие Тпл и Ткип. Простым сжатием при обычной температуре азот нельзя превратить в жидкость. • Энергия тройной связи равна 945, 4 к. Дж/моль. Необычно прочная (~523 к. Дж/моль) первая из разрываемых в молекуле N 2 связей. Это препятствует разрушению тройной связи. • Азот плохо растворяется в воде: в 100 объёмах воды растворяется всего 2, 35 объёма N 2. 10

Азот 3 Mg + N 2 = Mg 3 N 2 6 Li + N 2 = Li 3 N C кислородом, водородом и галогенами азот реагирует при высоких температурах и в присутствии катализаторов. Проблема связывания молекулярного азота различными комплексными соединениями – комплексы рутения, родия, палладия, иногда железа, титана, кобальта с различными сложными лигандами. 11

Азот • Комплексы молекулярного азота (комплексы диазота, нитрогенильные комплексные соединения): [Ru(NH 3)5 H 2 O]2+ + N 2 = [Ru(NH 3)5 N 2]2+ + + H 2 O [Fe(CN)5 NO]2 - + NН 3 = [Fe(CN)5 N 2]3 - + + H 3 O + 12

Фосфор Белый фосфор Рбел – прозрачное, мягкое, легкоплавкое, химически очень активное вещество. Хранят под слоем воды. Молекула имеет состав Р 4. На воздухе загорается уже при незначительном нагревании, при ударе или трении. Мелкодисперсный белый фосфор самовоспламеняется на воздухе. Белый фосфор светится. P 4 + 3 O 2 = 2 P 2 O 3 + O 2 = P 2 O 5 Активно реагирует с галогенами, серой. 13

Фосфор С металлами Рбел даёт фосфиды: 6 Mg + P 4 = 2 Mg 3 P 2 P 4 + 3 KOH + 3 H 2 O = 3 KH 2 PO 2 + PH 3↑ Получение: 2 Сa 3(PO 4)2 + 6 Si. O 2 + 10 C 6 Ca. Si. O 3 + 10 CO↑ + P 4↑ 14

Фосфор • Красный фосфор Ркр – аморфное вещество красно-фиолетового цвета. Имеет полимерное строение: группы P 4, соединенные в бесконечные цепи, которые образованы за счёт разрыва одной связи Р – Р в каждом тетраэдре P 4. Химически инертен, температура воспламенения на воздухе – 210 о. С. При ударе или трении: 6 P + 5 KCl. O 3 = 3 P 2 O 5 + 5 KCl 15

Фосфор 16 P + 5 HNO 3 = H 3 PO 4 + 5 NO 2↑ + H 2 O Красный фосфор получают из белого: Рбел Ркр Фиолетовый фосфор Рфиол или фосфор Гитторфа – образуется при медленном охлаждении Рбел. Рфиол – это клеточные фрагменты Р 9 и Р 8, связанные между собой в очень сложную трёхмерную структуру. Пурпурный, рубиновый, светлокрасный фосфор – образуются из Рбел в результате полимеризации, протекающей в различных растворителях.

Фосфор • Чёрный фосфор Рчерн – получают нагреванием Рбел до 200 о. С под давлением 12 000 атм. Рчерн – полупроводник, имеет слоистую структуру. Является самой устойчивой формой существования фосфора. 17

Кислородные соединения 18 • Увеличение ионного вклада в химическую связь Э–О – причина роста термодинамической стабильности оксидов Э 2 О 3 и Э 2 О 5 при переходе от азота к фосфору и от мышьяка к сурьме. Резкое возрастание окислительной способности соответствующих соединений. Падение устойчивости этих оксидов от Р к As и от Sb к Bi обусловлено ростом деформируемости атомов. • Для оксидов характерно нерегулярное изменение свойств однотипных соединений в ряду N-Bi – вторичная периодичность.
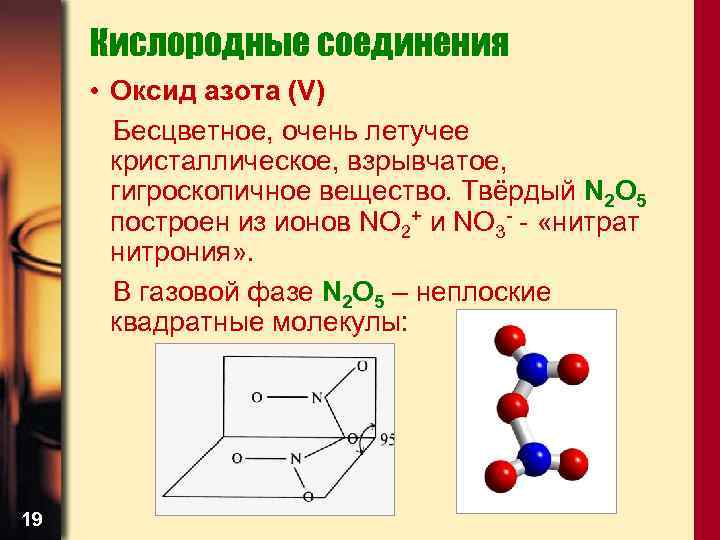
Кислородные соединения • Оксид азота (V) Бесцветное, очень летучее кристаллическое, взрывчатое, гигроскопичное вещество. Твёрдый N 2 O 5 построен из ионов NO 2+ и NO 3 - - «нитрат нитрония» . В газовой фазе N 2 O 5 – неплоские квадратные молекулы: 19

Кислородные соединения 2 N 2 O 5 = 4 NO 2↑ + O 2↑ Активный окислитель: N 2 O 5 + Na = Na. NO 3 + NO 2↑ N 2 O 5 + I 2 = I 2 O 5 + N 2↑ Соли нитрония: N 2 O 5 + HCl. O 4 = NO 2+Cl. O 4 - + HNO 3 перхлорат нитрония Получение N 2 O 5: 2 HNO 3 + P 2 O 5 = N 2 O 5 + 2 HPO 3 2 NO 2 + O 3 = N 2 O 5 + O 2↑ 20
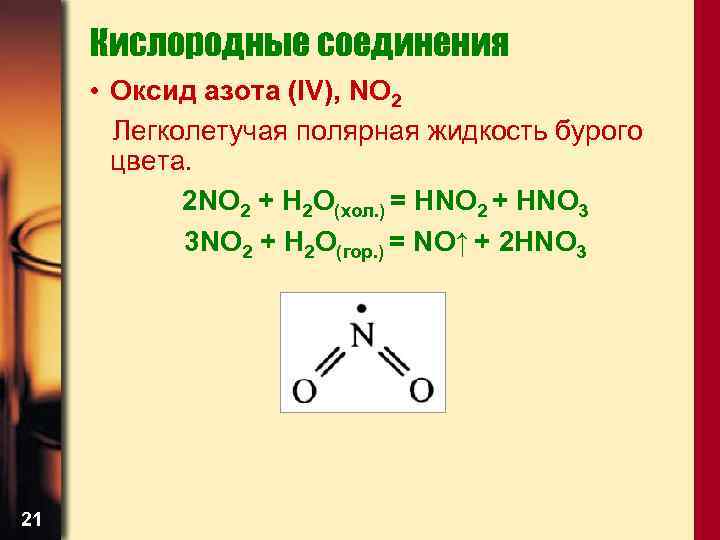
Кислородные соединения • Оксид азота (IV), NO 2 Легколетучая полярная жидкость бурого цвета. 2 NO 2 + Н 2 O(хол. ) = HNO 2 + HNO 3 3 NO 2 + Н 2 O(гор. ) = NO↑ + 2 HNO 3 21

Кислородные соединения • «Нечётная» парамагнитная молекула (17 валентных электронов), легко димеризуется. 2 NO 2 N 2 O 4 Диоксид азота обладает окислительными свойствами: 8 Р + 10 NO 2 = 2 P 2 O 5↑ + N 2↑ 2 C + 2 NO 2 = 2 CO 2↑ + N 2↑ 2 NO 2 + 2 Na. OH = Na. NO 3 + Na. NO 2 + H 2 O Получение: 2 Pb(NO 3)2 = 2 Pb. O + 4 NO 2↑ + O 2↑ 22
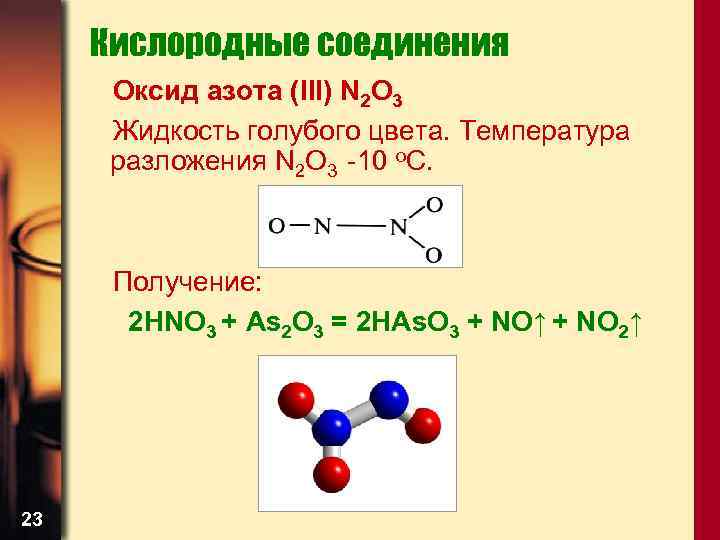
Кислородные соединения Оксид азота (III) N 2 O 3 Жидкость голубого цвета. Температура разложения N 2 O 3 -10 о. С. Получение: 2 HNO 3 + As 2 O 3 = 2 HAs. O 3 + NO↑ + NO 2↑ 23

Кислородные соединения Оксид азота (II) NO Бесцветный газ. Ковалентное соединение с малой полярностью связи. NO диспропорционирует уже при 30 -50 о. С: 3 NO = N 2 O + NO 2 Ион нитрозила NO+ более устойчив, чем NO. N 2 O 3 + 3 H 2 SO 4 = 2 NO+ + 3 HSO 4 - + H 2 O + H+ NO+HSO 4 - - нитрозилсерная кислота – ионный характер связи катион-анион. 24

Кислородные соединения NO – парамагнитное, но неокрашенное вещество. Сравнительно термически устойчив и мало реакционноспособен. Химические свойства NO: 3 NO + O 2 = 2 NO 2 Нитрозилгалогениды NOX, где X = F, Cl, Br: 2 NO + Х 2 = 2 NOХ NO + 2 HNO 3, конц. = 3 NO 2 ↑ + H 2 O 2 NO + K 2 Cr 2 O 7 + 4 H 2 SO 4 = 2 HNO 3 + Cr 2(SO 4)3 + K 2 SO 4 + 3 H 2 O 25

Кислородные соединения • Получение NO: 3 Cu + 8 HNO 3 = 3 Cu(NO 3)2 + 2 NO↑ + 4 H 2 O 2 KNO 2 + 2 KI + 4 H 2 SO 4 = 4 KHSO 4 + I 2 + 2 NO↑ + 2 H 2 O Оксид азота (I) N 2 O ( «веселящий газ» ) Бесцветный газ, сладковатый на вкус 26

Кислородные соединения Разлагается при нагревании: 2 N 2 O = 2 N 2↑ + O 2↑ N 2 O - cильный окислитель: 5 N 2 O + 2 Р = P 2 O 5 + 5 N 2↑ 2 N 2 O + C = CO 2↑ + 2 N 2↑ Получение: NH 4 NO 3 N 2 O↑ + 2 H 2 O↑ 27
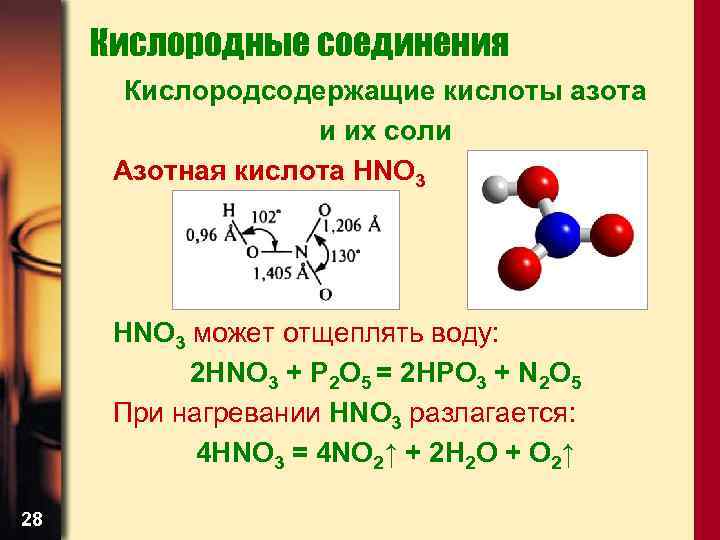
Кислородные соединения Кислородсодержащие кислоты азота и их соли Азотная кислота HNO 3 может отщеплять воду: 2 HNO 3 + P 2 O 5 = 2 HPO 3 + N 2 O 5 При нагревании HNO 3 разлагается: 4 HNO 3 = 4 NO 2↑ + 2 H 2 O + O 2↑ 28

Кислородные соединения Самоионизация (100%-я азотная кислота): 2 HNO 3 NO 2+ + NO 3 - + H 2 O [NO 2+][NO 3 -]·H 2 O – гидрат нитрата нитрония. HNO 3, проявляя окислительные свойства, восстанавливается с образованием различных продуктов: NO 2, N 2 O 3, NO, N 2, NH 3. Ход процесса зависит от природы восстановителя, концентрации реагента и температуры. Если используется концентрированная HNO 3, окончательным продуктом её восстановления всегда является NO 2. 29

Кислородные соединения 2 HNO 3 + NO = 3 NO 2↑ + H 2 O В промышленности HNO 3 синтезируют только растворением NO 2 в горячей воде в присутствии О 2, получается 68%-ный азеотроп: 4 NO 2 + 2 H 2 O + O 2 = 4 HNO 3 Продукт нитрования клетчатки (С 6 H 10 O 5)n – нитроцеллюлоза [C 6 H 7 O 5(NO 2)3]n – основная часть динамита. Взрыв динамита: [C 6 H 7 O 5(NO 2)3]n = 3 n. N 2↑ + 9 n. CO↑ + 3 n. CO 2↑ + + 7 n. H 2 O 30

Кислородные соединения Нитраты Хорошо растворимы в воде. Расплавы нитратов – сильные окислители. Вспышка чёрного пороха обусловлена именно окисляющим действием селитры: 2 KNO 3 + S + 3 C = K 2 S + N 2↑ + 3 CO 2↑ Термическое разложение нитратов: 2 Pb(NO 3)2 = 2 Pb. O + 4 NO 2↑ + O 2↑ 2 Ag. NO 3 = 2 Ag + 2 NO 2↑ + O 2↑ 2 Na. NO 3 = 2 Na. NO 2 + O 2↑ 31 NH 4 NO 3 = N 2 O↑ + 2 H 2 O↑

Кислородные соединения Ортонитраты натрия и калия Э 3 NO 4 – получаются взаимодействием нитрата и оксида щелочного элемента (серебряный тигель, 300 о. С): Na. NO 3 + Na 2 O = Na 3 NO 4 32

Кислородные соединения Азотистая кислота HNO 2 Существует только в растворе, неустойчива: 3 HNO 2 = HNO 3 + H 2 O + NO 2↑ Причина «слабости» кислотных свойств: 1) Меньший размер аниона NO 22) В азотной кислоте больше атомов кислорода, оттягивающих электронную плотность от атома азота. 33
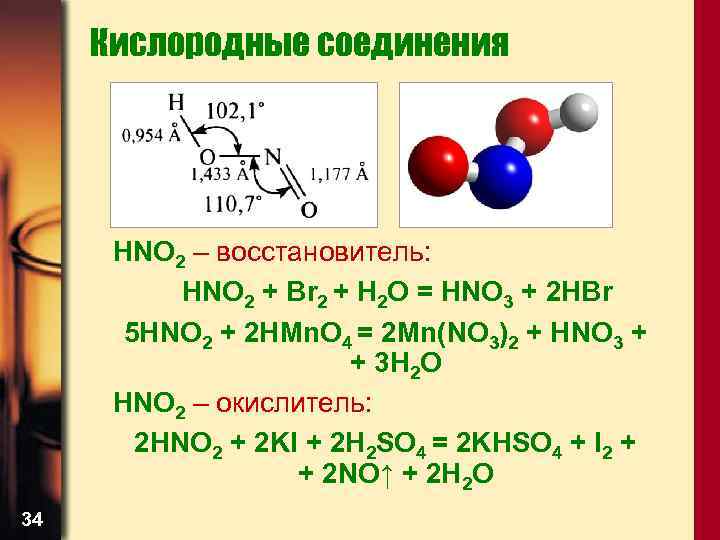
Кислородные соединения HNO 2 – восстановитель: HNO 2 + Br 2 + H 2 O = HNO 3 + 2 HBr 5 HNO 2 + 2 HMn. O 4 = 2 Mn(NO 3)2 + HNO 3 + + 3 H 2 O HNO 2 – окислитель: 2 HNO 2 + 2 KI + 2 H 2 SO 4 = 2 KHSO 4 + I 2 + + 2 NO↑ + 2 H 2 O 34

Кислородные соединения Несмотря на более низкую степень окисления азота в HNO 2, азотистая кислота – более сильный окислитель, чем HNO 3, если их сравнивать в одинаковых условиях. Получение: 2 KNO 2 + H 2 SO 4 = HNO 2 + KHSO 4 35

Кислородные соединения Азотноватистая кислота H 2 N 2 O 2 Бесцветные взрывчатые кристаллы. При хранении постепенно разлагается: H 2 N 2 O 2 = H 2 O + N 2 O↑ (обратная реакция не идёт!) Соли H 2 N 2 O 2 – гипонитриты Э 2 N 2 O 2. Получение: 2 Na. NO 2 + 4[H] = Na 2 N 2 O 2 + 2 H 2 O 36

Кислородные соединения • Динитразовая кислота HN 3 O 4 Бесцветная подвижная жидкость, недавно полученная В. А. Тартаковским с сотр. (ИОХ им. Н. Д. Зелинского РАН). Разлагается: HN 3 O 4 = HNO 3 + N 2 O Является одной из сильнейших кислот. 37
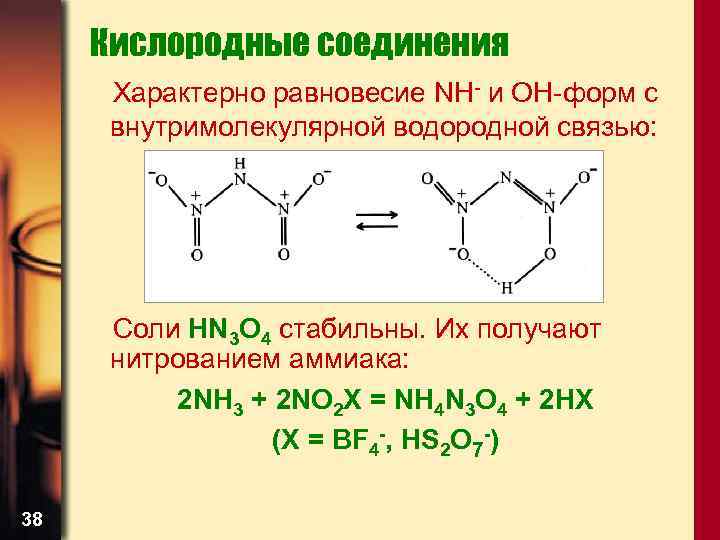
Кислородные соединения Характерно равновесие NH- и OH-форм с внутримолекулярной водородной связью: Соли HN 3 O 4 стабильны. Их получают нитрованием аммиака: 2 NH 3 + 2 NO 2 X = NH 4 N 3 O 4 + 2 HX (X = BF 4 -, HS 2 O 7 -) 38

Кислородные соединения • Оксид фосфора (V) P 2 O 5 α-модификация – P 4 O 10 – твёрдое вещество белого цвета. Получают при взаимодействии фосфора с избытком кислорода: P 4 + 5 O 2 = P 4 O 10↑ P 4 O 10 широко используется как сильнейшее водоотнимающее средство. 39

Кислородные соединения • Оксид фосфора (III) P 2 O 3 Белое кристаллическое вещество. Димер P 4 O 6. Легко окисляется на воздухе: P 4 O 6 + 2 O 2 = P 4 O 10 C горячей водой: P 4 O 6 + 6 H 2 O = PH 3↑ + 3 H 3 PO 4 C холодной водой: P 4 O 6 + 6 H 2 O = 4 H 3 PO 3 P 4 O 6 + 6 HСl = 2 H 3 PO 3 + 2 PCl 3 40

Кислородные соединения Получают при медленном окислении Р 4 кислородом воздуха: P 4 + 3 O 2 = P 4 O 6 41

Кислородные соединения • Кислоты фосфора Обще свойство кислородсодержащих кислот фосфора (V) - отсутствие окислительных свойств. - Ортофосфорная кислота H 3 PO 4 – бесцветные кристаллы, очень гигроскопичные. - Метафосфорная кислота (HPO 3)4 – прозрачная стекловидная масса. - Пирофосфорная кислота H 4 P 2 O 7 – бесцветное стеклообразное или кристаллическое вещество. 42
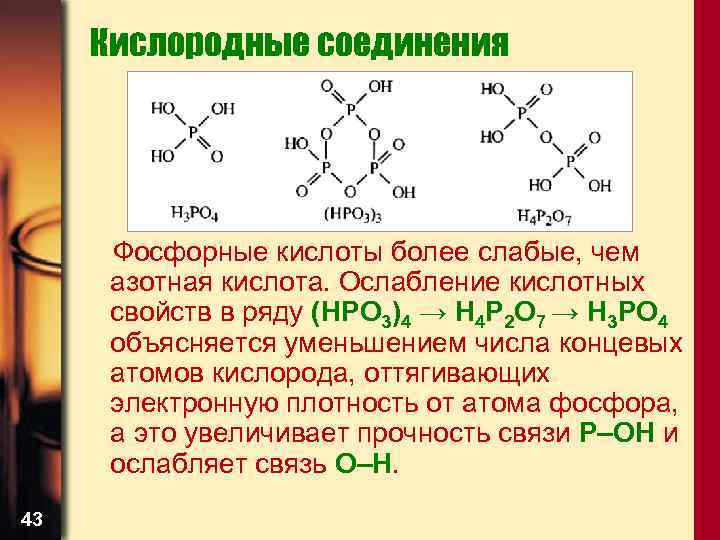
Кислородные соединения Фосфорные кислоты более слабые, чем азотная кислота. Ослабление кислотных свойств в ряду (HPO 3)4 → H 4 P 2 O 7 → H 3 PO 4 объясняется уменьшением числа концевых атомов кислорода, оттягивающих электронную плотность от атома фосфора, а это увеличивает прочность связи Р–ОН и ослабляет связь О–Н. 43

Кислородные соединения • Фосфаты Средние ортофосфаты сильно гидролизуются: Na 3 PO 4 + H 2 O Na. OH + Na 2 HPO 4 Растворимые гидрофосфаты подвергаются гидролизу в меньшей степени: Na 2 HPO 4 + H 2 O Na. OH + Na. H 2 PO 4 + H 2 O Na. OH + H 3 PO 4 Гидролиз дигидрофосфатов ЩЭ практически не идёт. 44

Кислородные соединения При нагревании дигидрофосфаты и гидрофосфаты отщепляют воду: Na. H 2 PO 4 = Na. PO 3 + H 2 O 2 Na 2 HPO 4 = Na 4 P 2 O 7 + H 2 O Метафосфаты имеют полимерное строение. Растворимы только соли ЩЭ. Пирофосфаты могут быть только кислыми и средними. Из средних – (ЩЭ)4 P 2 O 7 – растворимы только соли Na и K. Гидролизуются: Na 4 P 2 O 7 + 2 H 2 O Na 2 Н 2 Р 2 O 7 + 2 Na. OН 45

Кислородные соединения При прокаливании пирофосфаты М 2 P 2 O 7 (M = Mg, ЩЗЭ и Zn): 3 М 2 P 2 O 7 = 2 М 3(PO 4)2 + P 2 O 5↑ Пирофосфаты ядовиты. 46

Кислородные соединения • Фосфористая кислота H 3 PO 3 – твёрдое вещество белого цвета, при нагревании разлагается: 4 Н 3 PO 3 = 3 Н 3 PO 4 + PН 3↑ Обесцвечивает раствор перманганата калия: 2 KMn. O 4 + 5 Н 3 PO 3 = 2 Mn(H 2 PO 4)2 + K 2 HPO 4 + 3 Н 2 O Обладает восстановительными свойствами 47
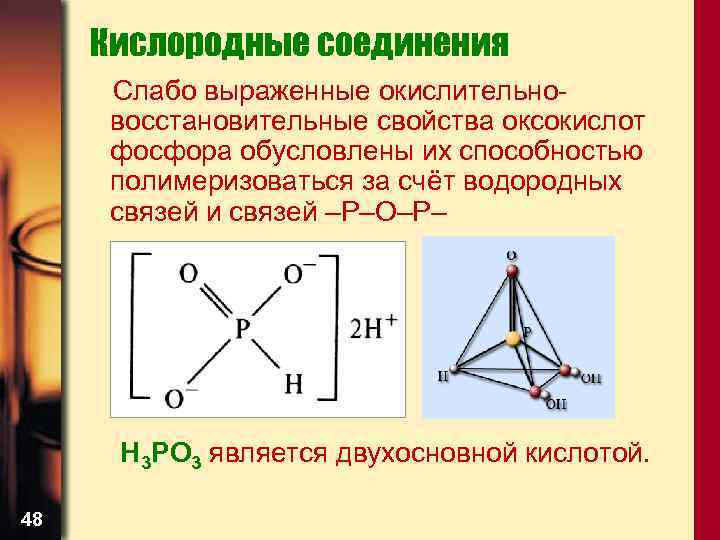
Кислородные соединения Слабо выраженные окислительновосстановительные свойства оксокислот фосфора обусловлены их способностью полимеризоваться за счёт водородных связей и связей –Р–О–Р– Н 3 PO 3 является двухосновной кислотой. 48
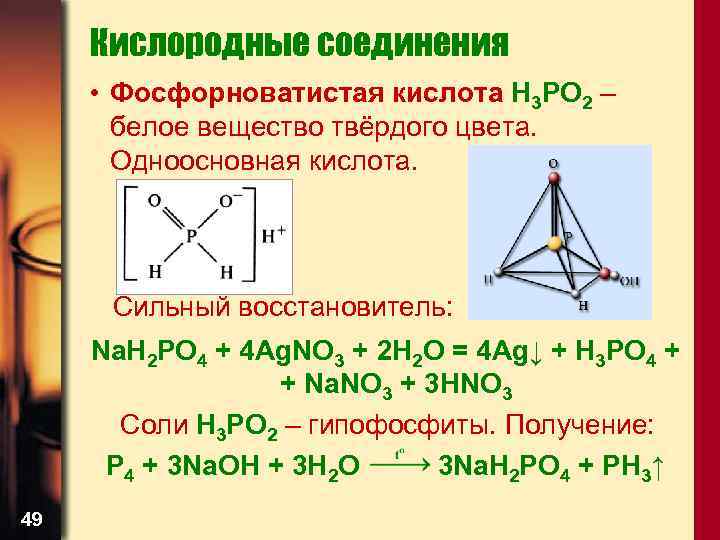
Кислородные соединения • Фосфорноватистая кислота H 3 PO 2 – белое вещество твёрдого цвета. Одноосновная кислота. Сильный восстановитель: Na. H 2 PO 4 + 4 Ag. NO 3 + 2 Н 2 O = 4 Ag↓ + H 3 PO 4 + + Na. NO 3 + 3 НNO 3 Соли H 3 PO 2 – гипофосфиты. Получение: P 4 + 3 Na. OH + 3 Н 2 O 3 Na. H 2 PO 4 + PH 3↑ 49
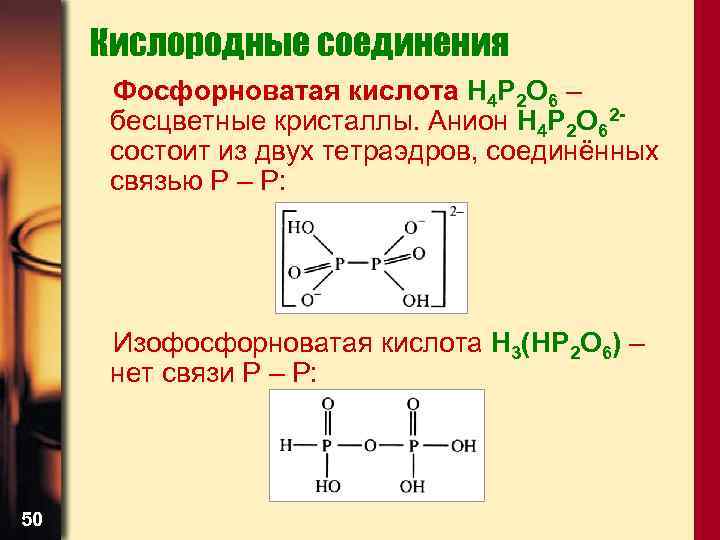
Кислородные соединения Фосфорноватая кислота H 4 P 2 O 6 – бесцветные кристаллы. Анион H 4 P 2 O 62 состоит из двух тетраэдров, соединённых связью Р – Р: Изофосфорноватая кислота H 3(НP 2 O 6) – нет связи Р – Р: 50

Кислородные соединения Оксиды мышьяка Оксид мышьяка (V) As 2 O 5 Получают нагреванием мышьяковой кислоты до 200 о. С: 2 H 3 As. O 4 = As 2 O 5 + 3 Н 2 O При температуре >250 о. С происходит переход оксида As. V в оксид As. III: As 2 O 5 = As 2 O 3 + О 2 ↑ As 2 O 3 чрезвычайно ядовит. 51

Кислородные соединения Мышьяковая кислота H 3 As. O 4 – бесцветное кристаллическое вещество. При нагревании: 2 H 3 As. O 4 As 2 O 5 + 3 Н 2 O Кислотные свойства H 3 As. O 4 выражены достаточно сильно, но мышьяковая кислота проявляет амфотерность. 3 H+ + As. O 43 H 3 As. O 4 As(ОН)5 As 5+·aq + 5 OHВ кислой среде проявляет свойства окислителя: H 3 As. O 4 + 2 HI = I 2 + HAs. O 2 + 2 Н 2 O 52

Кислородные соединения • В щелочной среде является восстановителем: I 2 + Na. As. O 2 + 4 Na. OH = 2 Na. I + Na 3 As. O 4 + + 2 Н 2 O Мышьяковистая кислота H 3 As. O 3 Более слабая, менее устойчивая, чем мышьяковая. Основной формой является оксид состава As 2 O 3· 3 Н 2 O. Мышьяковистая кислота амфотерна: Н 2 O + H+ + As. O 2 H 3 As. O 3 As(ОН)3 As 3+ + 3 OH 53

Кислородные соединения Выделить в твёрдом виде индивидуальную мышьяковистую кислоту не удаётся. 54

Кислородные соединения 55

Кислородные соединения 56

Кислородные соединения 57
VA группа.ppt