
В 1923 г. И. Бренстед и Т. Лоури предложили общую протолитическую теорию кислот и оснований. Кислота - молекула или ион, способные отдавать катион водорода (протон). Кислота - донор протонов. СН 3 СООH H+ + СН 3 СОО– слабая сопряж. к-та сопряж. основание Основание — молекула или ион, способные присоединять катион водорода (протон). Основание - акцептор протонов. ОН- + Н+ = Н 2 О NH 3 +Н+= = NH 4+ отдавая протон, кислота превращается в основание, которое называют сопряженным этой кислоте А мфолиты — молекулы или ионы, способные как отдавать, так и присоединять протон, а следовательно, вступать в реакции, характерные как для кислот, так и для оснований. Н 2 О + НС 1 = Н 3 О+ + СГ основание кислота Н 2 О + NH 3 = NH 4+ + ОНкислота основание Амфолитами являются =====гидроксиды некоторых металлов (Zn, Al, Pb, Sn, Cr): ====гидроанионы многоосновных кислот, например НСОз-, НРО 4 2 -. ====соединения, молекулы которых содержат две различные кислотно-основные группы, H 2 N—CHR—СООН основание кислота

n n n n ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ И ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ Н 2 О Н+ + ОН– Константа диссоциации воды при 25 С равна: В 1 литре воды содержится 1000/18=55, 6 молей [Н+] [ОН–] = = К [Н 2 О] = 1, 8 10– 16 55, 6 = 10– 14 моль/л = KW, где KW — ионное произведение воды. Если концентрации [Н+] и [ОН–] равны, что соответствует нейтральному раствору, то [Н+] = [ОН –] = 10– 7 моль/л.
![Водородным показателем называют величину, численно равную отрицательному десятичному логарифму активности [или концентрации] водородных ионов Водородным показателем называют величину, численно равную отрицательному десятичному логарифму активности [или концентрации] водородных ионов](https://present5.com/presentation/3/79489300_134748135.pdf-img/79489300_134748135.pdf-3.jpg)
Водородным показателем называют величину, численно равную отрицательному десятичному логарифму активности [или концентрации] водородных ионов и выраженную в грамм-ионах на литр или в молях на литр. • lg KW = lg[Н+] + lg[ОН–] = lg 10– 14 • Беря логарифмы с обратным знаком, получим: • р. Н + р. ОН = 14 • Следовательно, р. Н и р. ОН являются сопряжёнными величинами: если р. Н = 3, то р. ОН = 14 – 3 = 11. • р. Н крови = 7, 3 -7, 4 • р. Н желудочного сока = 0, 9 -1, 5 [взр. ], • =======новорожденных — 7, 0; • ====у детей 4 -7 лет — 2, 5; • ==== у детей 14 лет — 2, 0 • • р. Н слюны = 7, 3 -7, 9

n Методы определения р. Н растворов. n Для определения р. Н растворов используют n индикаторный применяется в том случае, когда необходимо быстро и приблизительно оценить р. Н исследуемого раствора. n нельзя определить р. Н мутных и окрашенных растворов. Ионометрический метод позволяет определить этот показатель с. большей точностью (0, 01 ед. р. Н). n можно определить р. Н мутных, окра шенных и любых других водных растворов

n n n n Индикаторы — это органические соединения, слабые кислоты или основания, анионы которых имеют одну окраску, а недиссоциированные молекулы — другую. HInd H+ + Ind– При [HInd] = [Ind–] [Н+] = Кинд, тогда р. К = р. Кинд является точкой перехода индикатора, она равна тому значению р. Н, при котором индикатор диссоциирован наполовину: [HInd] = [Ind–]. Зоной перехода индикатора называется область между двумя значениями р. Н, в которой происходит заметное изменение окраски индикатора. Чем меньше зона перехода индикатора, тем чувствительнее индикатор. Универсальный индикатор — это смесь индикаторов со смежными зонами перехода.
![Для количественной характеристики кислотных свойств растворов пользуются величинами общей, активной и потенциальной кислотности, [Н+]общ, Для количественной характеристики кислотных свойств растворов пользуются величинами общей, активной и потенциальной кислотности, [Н+]общ,](https://present5.com/presentation/3/79489300_134748135.pdf-img/79489300_134748135.pdf-6.jpg)
Для количественной характеристики кислотных свойств растворов пользуются величинами общей, активной и потенциальной кислотности, [Н+]общ, [Н+]акт, [Н+]пот в моль/л. Общая кислотность - это концентрация всех катионов Н+ (свободных и связанных), имеющихся в растворе равна сумме молярных концентраций эквивалентов всех кислот (сильных и слабых), находящихся в растворе: n [Н+]общ = сумме C I (1/z к-ты) Активная кислотность — это концентрация свободных катионов Н+, p. Н = -lg [H+] = -lg [Н+]акт Потенциальная кислотность - это концентрация катионов Н+, связанных в молекулы или ионы слабых кислот, имеющихся в растворе. n n [Н+]пот = [Н+]общ - [Н+]акт [Н+]пот = сумме Ci(1/z слабой к-ты)

n n n n Активную кислотность можно определить четырьмя способами: 1. Кондуктометрический. 2. Титриметрический - с индикатором диметиламидоазобензолом ограничен, т. к. применим только к растворам сильных кислот, где концентрация ионов водорода достаточно высока, например, в желудочном соке. 3. Потенциометрический — наиболее современный, точный и универсальный метод определения активной кислотности 4. Колориметрический [colour — цветной]. == позволяют определить р. Н с точностью до 0, 1. ==только для бесцветных, прозрачных, слабомутных и слабоокрашенных жидкостей, .

n n n Все колориметрические методы определения концентрации водородных ионов основаны на законе Ламберта-Бера, : для двух растворов, одинаково поглощающих свет, произведение толщины слоя раствора [d] на концентрацию раствора [С] при прочих равных условиях есть величина постоянная: d C = d 1 C 1 Из этого закона вытекает принцип, лежащий в основе всей колориметрии: «Если при одинаковой толщине слоёв растворы одного и того же вещества имеют одинаковую окраску, то они имеют и одинаковую концентрацию» .

• Буферными системами называются растворы, способные стойко сохранять постоянство концентрации ионов водорода как при добавлении кислот или щелочей, • так и при разведении. • Состав буферных систем. • а/ из слабой кислоты и её соли, образованной сильным основанием; • б/ из слабого основания и его соли, образованной сильной кислотой. • Буферная система а) типа содержит слабую кислоту и избыток сопряжённого основания: • СН 3 СООH H+ + СН 3 СОО– • слабая сопряж. к-тасопряж. основание • Буферная система б) типа слабое основание и избыток сопряжённой с ним кислоты: • NH 3 + H+ NH 4+ • слабое сопряж. основание сопряж. кислота

• • • р. Н буферных смесей. Кислый буфер СН 3 СООH H+ + СН 3 СОО– • Прологарифмируем и получим уравнение Гендерсона. Гассельбальха: • р. Н = р. Ка + lg [акцептор протона] [донор протона] • р. Н = р. Ка + lg [соль] [кислота
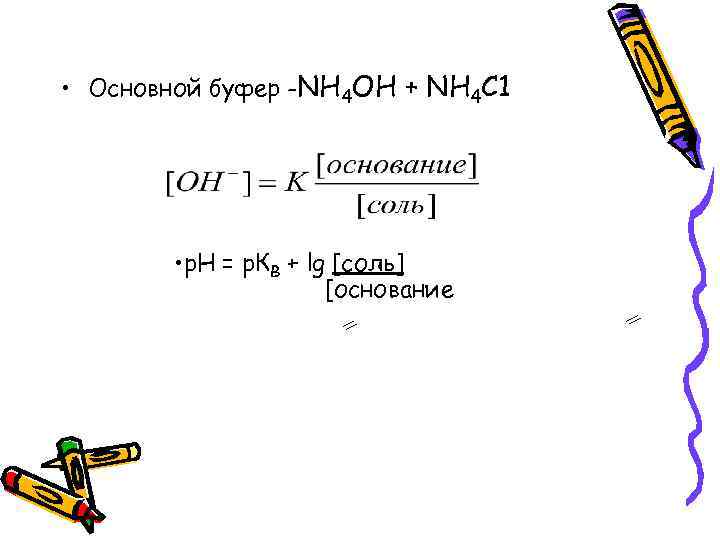
• Основной буфер -NH 4 ОН + NH 4 C 1 • р. Н = р. КВ + lg [соль] [основание

• Общий механизм действия буферных растворов • НА Н+ + А– • а/ А– + Н+ НА [при добавлении сильной кислоты] • б/ НА + ОН– Н 2 О + А– [при добавлении щелочи] • Рассмотрим этот механизм на примере ацетатного буфера. • а/ При добавлении HCl происходит взаимодействие с СН 3 СООNa: • СН 3 СООNa СН 3 СОО– + Na+ • СН 3 СОО– + Na+ + H+ + Cl– Na+ + Cl– + СН 3 СООН • б/ При добавлении щелочи : • СН 3 СООН + Na+ + OH– СН 3 СОО– + Na+ + Н 2 О

• При разбавлении буферных растворов • концентрации всех компонентов уменьшаются. • Но так как они изменяются одинаково, то их отношение остается неизменным. • Величина константы диссоциации слабого электролита также не изменяется при разведении.

• Буферной емкостью (В) называется число мольэквивалентов сильной кислоты или щелочи, которые нужно добавить к 1 литру буферного раствора, чтобы изме нить величинур. Н на единицу .

• Какие факторы определяют буферную ёмкость? • 1. Наибольшей буферной ёмкостью обладают концентрированные буферные растворы, . • 2. Из двух буферных растворов с одинаковой концентрацией буферная ёмкость будет больше у того раствора, у которого соотношение компонентов равно единице или близко к единице • 3. при разбавлении р. Н раствора не меняется, но его буферная ёмкость падает.

• • • • Кинетика сложных реакций. Сложные реакции подразделяются на параллельные, последовательные, сопряжённые и цепные. А. Параллельные реакции — связанная система реакций, имеющих одни и те же исходные реагенты, но различные продукты реакции. Скорость системы параллельных реакций равна сумме скоростей отдельных реакций: v 1 4 KCl + 6 O 2 4 KCl. O 3 vобщ = v 1 + v 2 3 KCl. O 4 + KCl Б. Последовательные реакции — связанная система реакций, в которой продукты предыдущих стадий расходуются в последующих реакциях. Скорость реакции= скорости самой медленной (лимитирующей) стадии. 2 NO + O 2 = N 2 O 4 v 1 1/ 2 NO ↔ [NO]2 v 2 2/ [NO]2 + O 2 ↔ N 2 O 4

• В. Сопряжённые реакции —реакции, каждая из которых происходит только при условии протекания другой реакции, причем обе реакции имеют общий промежуточный продукт • 1/ 6 Fe. O + 2 H 2 Cr. O 4 = 3 Fe 2 O 3[катализатор!] + Cr 2 O 3 + 2 H 2 O • 2/ 6 HI + 2 H 2 Cr. O 4 = 3 I 2 + Cr 2 O 3 + 5 H 2 O • Г. Цепные реакции — связанная система сложных реакций, протекающих последовательно, параллельно и сопряжённо с участием свободных радикалов [горение, взрывы, фотохимические реакции]. • Основные стадии реакции: • а/ зарождение цепи; • б/ разветвление цепи; • в/ продолжение цепи; • г/ обрыв цепи.

• Цепные реакции можно подразделить на неразветвлённые и разветвлённые. неразветвлённая реакция: • Cl 2 + hν = Cl • + Cl • • H 2 + Cl • = HCl + H • • H • + Cl 2 = HCl + Cl • • К разветвленным реакциям полимеризации, крекинг, сгорание топлива в двигателях, окисление и др. , например, ядерные цепные реакции

n n n n n фотохимические реакции — реакции, происходящие под действием лучей света [видимых, инфракрасных, ультрафиолетовых]. Эффективность фотохимической реакции определяется так называемым квантовым выходом γ: γ = число молекул продукта реакции число поглощённых квантов Фотохимические реакции бывают различных типов: а/ синтез вещества [фотосинтез] и б/ разложение веществ под действием света [фотолиз : hν 2 HCl → H 2 + Cl 2 Фотосинтез, происходящий в растениях — сложный окислительно-восстановительный процесс, сочетающий фотохимические реакции с ферментативными. | CO 2 + 2 H 2 O → [H—C—OH]n + O 2 |
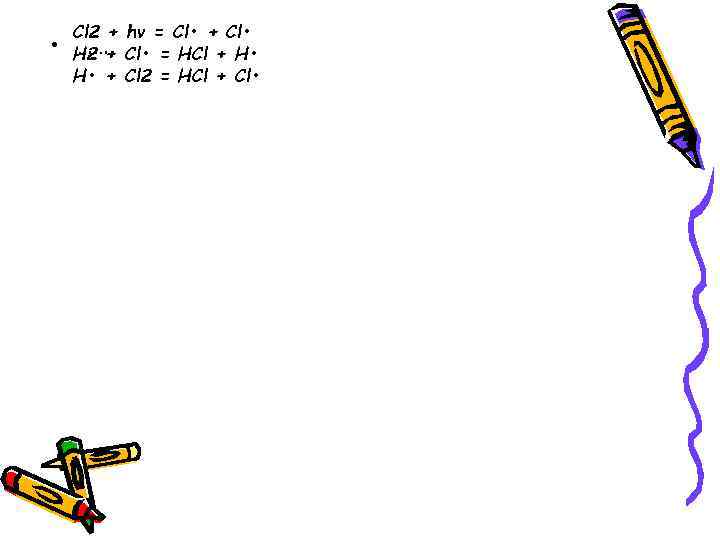
• Cl 2 + hν = Cl • + Cl • ……. H 2 + Cl • = HCl + H • + Cl 2 = HCl + Cl •


n n n Кислоты — жёсткие: H+, Li+, Na+, K+, Mn 2+, Cr 3+, Fe 3+, Co 3+, Mg 2+, Ca 2+; мягкие: Cu+, Ag+, Au+, Pt 2+, Pt 4+, Hg 2+, Cd 2+. Основания — жёсткие: H 2 O, OH–, NH 3, RNH 2, Cl–, PO 43–, SO 42–; мягкие: SCN–, R 1 S–, R 2 S, H–, S 2 O 3 2–, SH. правило: Устойчивые комплексы образуются между жёсткой кислотой и жёстким основанием или между мягкой кислотой и мягким основанием.

n n n Комплексообразователи и лиганды нашего организма. : Ca 2+ < Mg 2+ < Mn 2+ < Fe 2+ < Cd 2+ < Co 2+ < Zn 2+ < Ni 2+ < Cu 2+ - [Na+ и К+] присутствуют в основном в свободном виде, . - Са 2+, Мg 2+ существуют как в свободном виде, так и в виде комплексов. - Ионы тяжёлых металлов — Fe 2+, . — легче связываются с атомами азота и серы, например, в порфиринах.

n n n n Общие понятия об активном центре металлоферментов. ферменты представляют собой комплексные соединения с металлами, ионы которых определяют активный центр фермента и пространственную структуру [конформацию] фермента. Кроме того, в силу хелатного эффекта они придают прочность белкам. В состав ферментов входят микроэлементы: Mn — в состав 12 ферментов; Fe — в состав 70 ферментов; Cu — в состав 30 ферментов; Zn — в состав более 100 ферментов; Мо и Со — в состав нескольких ферментов. .

n n n n Значение комплексов в медицине. Биохимик Дж. Вуд писал: . Биохимия — это координационная химия живых систем» . В медицине применяются: 1. Лекарственные препараты на основе комплексов металлов в онкологии, психиатрии, при воспалительных заболеваниях. 2. Радиодиагностика — использование комплексов металлов, меченых радиоактивными изотопами для выяснения путей перемещения лекарств. 3. Радиотерапия — направление радиоактивного изотопа в поражённый участок с целью локального воздействия на него. 4. Хелатотерапия — при металлотоксикозах и металлоаллергических заболеваниях.