Лекция 6 Ферменты.ppt
- Количество слайдов: 45

 В 1878 гг. Кюне предложил термин энзим (от греч. en – внутри, zyme – закваска). Оба названия свидетельствуют о том, что первые сведения об этих веществах были получены при изучении процес сов брожения. Роль ферментов в жизнедеятельности всех живых организмов огромна. И. П. Павлов писал: «Ферменты есть, так сказать, первый акт жизненной деятельности. Все химические процессы направля ются в теле именно этими веществами, они есть возбудители всех химических превращений. Все эти вещества играют огромную роль, они обусловливают собою те процессы, благодаря которым проявляется жизнь, они и есть в полном смысле возбудители жизни» .
В 1878 гг. Кюне предложил термин энзим (от греч. en – внутри, zyme – закваска). Оба названия свидетельствуют о том, что первые сведения об этих веществах были получены при изучении процес сов брожения. Роль ферментов в жизнедеятельности всех живых организмов огромна. И. П. Павлов писал: «Ферменты есть, так сказать, первый акт жизненной деятельности. Все химические процессы направля ются в теле именно этими веществами, они есть возбудители всех химических превращений. Все эти вещества играют огромную роль, они обусловливают собою те процессы, благодаря которым проявляется жизнь, они и есть в полном смысле возбудители жизни» .
 Раздел биохимии, изучающий биологические катализаторы белковой природы, называется энзимологией. Круг вопросов, изучаемых энзимологией, весьма разнообразен. Он включает выделение и очистку ферментов с целью установления их состава и молекулярной структуры; изучение условий и скорости действия ферментов, а также влияния на них разнообразных физических и химических факторов.
Раздел биохимии, изучающий биологические катализаторы белковой природы, называется энзимологией. Круг вопросов, изучаемых энзимологией, весьма разнообразен. Он включает выделение и очистку ферментов с целью установления их состава и молекулярной структуры; изучение условий и скорости действия ферментов, а также влияния на них разнообразных физических и химических факторов.
 Ферменты и катализаторы неорганической природы, подчиняясь общим законам катализа, имеют сходные признаки: • катализируют только энергетически возможные реакции; • не изменяют направление реакции; • не расходуются в процессе реакции; • не участвуют в образовании продуктов реакции. Однако ферменты по ряду признаков отличаются от катализаторов неорганической природы: • ферменты – белки; • ферменты «работают» в «мягких» условиях: при атмосферном давлении, при температуре 30 – 40°С, р. Н среды близко к нейтральному; • скорость ферментного катализа выше, чем небиологического; • обладают высокой специфичностью по отношению к субстрату, каждый фермент катализирует единственную реакцию либо группу реакций одного типа; • ферменты – катализаторы с регулируемой активностью; • ферментативный процесс можно представить в виде цепи простых химических превращений вещества, четко запрограммированных во времени и в пространстве.
Ферменты и катализаторы неорганической природы, подчиняясь общим законам катализа, имеют сходные признаки: • катализируют только энергетически возможные реакции; • не изменяют направление реакции; • не расходуются в процессе реакции; • не участвуют в образовании продуктов реакции. Однако ферменты по ряду признаков отличаются от катализаторов неорганической природы: • ферменты – белки; • ферменты «работают» в «мягких» условиях: при атмосферном давлении, при температуре 30 – 40°С, р. Н среды близко к нейтральному; • скорость ферментного катализа выше, чем небиологического; • обладают высокой специфичностью по отношению к субстрату, каждый фермент катализирует единственную реакцию либо группу реакций одного типа; • ферменты – катализаторы с регулируемой активностью; • ферментативный процесс можно представить в виде цепи простых химических превращений вещества, четко запрограммированных во времени и в пространстве.
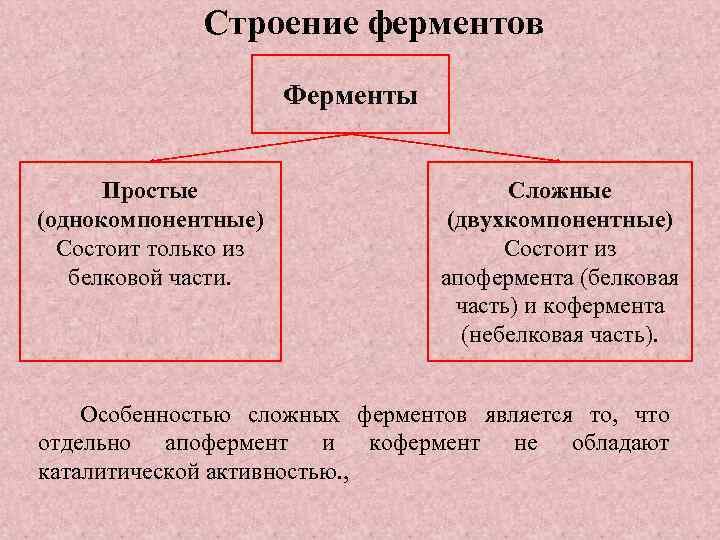 Строение ферментов Ферменты Простые (однокомпонентные) Состоит только из белковой части. Сложные (двухкомпонентные) Состоит из апофермента (белковая часть) и кофермента (небелковая часть). Особенностью сложных ферментов является то, что отдельно апофермент и кофермент не обладают каталитической активностью. ,
Строение ферментов Ферменты Простые (однокомпонентные) Состоит только из белковой части. Сложные (двухкомпонентные) Состоит из апофермента (белковая часть) и кофермента (небелковая часть). Особенностью сложных ферментов является то, что отдельно апофермент и кофермент не обладают каталитической активностью. ,
 Кофакторы ферментов – вещества, необходимые некоторым ферментам для проявления активности. Известны две группы кофакторов: неорганические – ионы металлов и некоторые анионы. органические – соединения нуклеотидной природы, производные витаминов. Ионы металлов, выполняющих роль кофакторов в ферментативных реакциях, это ионы калия, магния, кальция, цинка, меди, железа, молибдена. Ферменты, активируемые катионами металлов Название фермента Катионы металлов Аконитаза Альдолаза Аминоацил т. РНК синтетаза Аргиназа Гексокиназа Карбоксипептидаза Креатинкиназа Фосфатаза Фосфоглюкомутаза Fe 2+ Zn 2+, Co 2+ Mg 2+, Zn 2+ Mg 2+, Co 2+ Mg 2+, Mn 2+ Zn 2+ Ca 2+ Co 2+ Mn 2+, Co 2+
Кофакторы ферментов – вещества, необходимые некоторым ферментам для проявления активности. Известны две группы кофакторов: неорганические – ионы металлов и некоторые анионы. органические – соединения нуклеотидной природы, производные витаминов. Ионы металлов, выполняющих роль кофакторов в ферментативных реакциях, это ионы калия, магния, кальция, цинка, меди, железа, молибдена. Ферменты, активируемые катионами металлов Название фермента Катионы металлов Аконитаза Альдолаза Аминоацил т. РНК синтетаза Аргиназа Гексокиназа Карбоксипептидаза Креатинкиназа Фосфатаза Фосфоглюкомутаза Fe 2+ Zn 2+, Co 2+ Mg 2+, Zn 2+ Mg 2+, Co 2+ Mg 2+, Mn 2+ Zn 2+ Ca 2+ Co 2+ Mn 2+, Co 2+
 Витамины и их производные – коферменты Витамин В 1 (тиамин) В 2 (рибофлавин) В 3 (пантотеновая кислота) В 5 (РР или никотиновая кислота) В 6 (пиридоксин) Коферментная форма Тиаминдифосфат (ТДФ) ФМН и ФАД Коэнзим А (Ко. А) Катализируемая форма Декарбоксилирование Дегидрирование Перенос ацильных групп НАД и НАДФ Дегидрирование Пиридоксальфосфат В 12 (цианкобаламин) Вс (фолиевая кислота) Н (биотин) Кобамиды (Метил В 12, Кофермент В 12) Тетрагидрофолевая кислота Биотин Перенос аминогрупп, декарбоксилирование аминокислот, изомеризация Перенос метильных групп N (липоевая кислота) Липоевая кислота Перенос формила Перенос карбоксильных групп Окислительное декарбоксилирование ФАД – флавинадениндинуклеотид; НАД – никотинаминадениндинуклеотид; ФМН – флавомононуклеотид; НАДФ – никотинаминадениндинуклеотидфосфат;
Витамины и их производные – коферменты Витамин В 1 (тиамин) В 2 (рибофлавин) В 3 (пантотеновая кислота) В 5 (РР или никотиновая кислота) В 6 (пиридоксин) Коферментная форма Тиаминдифосфат (ТДФ) ФМН и ФАД Коэнзим А (Ко. А) Катализируемая форма Декарбоксилирование Дегидрирование Перенос ацильных групп НАД и НАДФ Дегидрирование Пиридоксальфосфат В 12 (цианкобаламин) Вс (фолиевая кислота) Н (биотин) Кобамиды (Метил В 12, Кофермент В 12) Тетрагидрофолевая кислота Биотин Перенос аминогрупп, декарбоксилирование аминокислот, изомеризация Перенос метильных групп N (липоевая кислота) Липоевая кислота Перенос формила Перенос карбоксильных групп Окислительное декарбоксилирование ФАД – флавинадениндинуклеотид; НАД – никотинаминадениндинуклеотид; ФМН – флавомононуклеотид; НАДФ – никотинаминадениндинуклеотидфосфат;
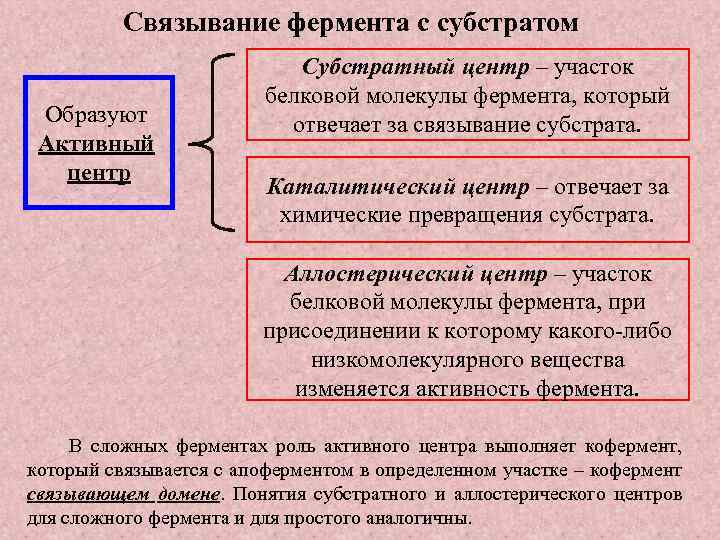 Связывание фермента с субстратом Образуют Активный центр Субстратный центр – участок белковой молекулы фермента, который отвечает за связывание субстрата. Каталитический центр – отвечает за химические превращения субстрата. Аллостерический центр – участок белковой молекулы фермента, присоединении к которому какого либо низкомолекулярного вещества изменяется активность фермента. В сложных ферментах роль активного центра выполняет кофермент, который связывается с апоферментом в определенном участке – кофермент связывающем домене. Понятия субстратного и аллостерического центров для сложного фермента и для простого аналогичны.
Связывание фермента с субстратом Образуют Активный центр Субстратный центр – участок белковой молекулы фермента, который отвечает за связывание субстрата. Каталитический центр – отвечает за химические превращения субстрата. Аллостерический центр – участок белковой молекулы фермента, присоединении к которому какого либо низкомолекулярного вещества изменяется активность фермента. В сложных ферментах роль активного центра выполняет кофермент, который связывается с апоферментом в определенном участке – кофермент связывающем домене. Понятия субстратного и аллостерического центров для сложного фермента и для простого аналогичны.
 Субстратный центр простого фермента это участок белковой молекулы фермента, который отвечает за связывание субстрата. Субстратный центр образно называют «якорной площадкой» , где субстрат прикрепляется к ферменту за счет различных взаимодействий между определенными боковыми радикалами аминокислотных остатков и соответствующими группами молекулы субстрата. Субстрат с ферментом связывается посредством ионных взаимодействий, водородных связей; иногда субстрат и фермент связываются ковалентно.
Субстратный центр простого фермента это участок белковой молекулы фермента, который отвечает за связывание субстрата. Субстратный центр образно называют «якорной площадкой» , где субстрат прикрепляется к ферменту за счет различных взаимодействий между определенными боковыми радикалами аминокислотных остатков и соответствующими группами молекулы субстрата. Субстрат с ферментом связывается посредством ионных взаимодействий, водородных связей; иногда субстрат и фермент связываются ковалентно.
 Каталитический центр простого фермента представляет собой уникальное сочетание нескольких аминокислотных остатков, расположенных на разных участках полипептидной цепи. Образование каталитического центра происходит одновременно с формированием третичной структуры белковой молекулы фермента. Чаще всего в состав каталитического центра входят остатки серина, цистеина, тирозина, гистидина, аргинина, аспарагиновой и глутаминовой кислот.
Каталитический центр простого фермента представляет собой уникальное сочетание нескольких аминокислотных остатков, расположенных на разных участках полипептидной цепи. Образование каталитического центра происходит одновременно с формированием третичной структуры белковой молекулы фермента. Чаще всего в состав каталитического центра входят остатки серина, цистеина, тирозина, гистидина, аргинина, аспарагиновой и глутаминовой кислот.
 Аллостерический центр представляет собой участок молекулы фермента, в результате присоединения к которому какого то низкомолекулярного вещества изменяется третичная структура белковой молекулы фермента, что влечет за собой изменение его активности. Аллостерический центр является регуляторным центром фермента.
Аллостерический центр представляет собой участок молекулы фермента, в результате присоединения к которому какого то низкомолекулярного вещества изменяется третичная структура белковой молекулы фермента, что влечет за собой изменение его активности. Аллостерический центр является регуляторным центром фермента.
 Механизм действия ферментов Основы механизма действия ферментов были изучены в начале XX века. В 1902 году английский химик А. Браун высказал предположение о том, что фермент, воздействуя на субстрат, должен образовать с ним промежуточный фермент – субстратный комплекс. Одновременно и независимо от А. Брауна это же предположение высказал французский ученый В. Анри. В 1913 году Л. Михелис и М. Ментэн подтвердили и развили представления о механизме действия ферментов, который можно представить в виде схемы: E+S [E*S]` [EP] E+P где E – фермент; S – субстрат; P – продукт.
Механизм действия ферментов Основы механизма действия ферментов были изучены в начале XX века. В 1902 году английский химик А. Браун высказал предположение о том, что фермент, воздействуя на субстрат, должен образовать с ним промежуточный фермент – субстратный комплекс. Одновременно и независимо от А. Брауна это же предположение высказал французский ученый В. Анри. В 1913 году Л. Михелис и М. Ментэн подтвердили и развили представления о механизме действия ферментов, который можно представить в виде схемы: E+S [E*S]` [EP] E+P где E – фермент; S – субстрат; P – продукт.
 На первой стадии ферментативного катализа происходит образование фермент субстратного комплекса, где фермент и субстрат могут быть связаны ионной, ковалентной или иной связью. Образование комплекса E*S происходит практически мгновенно. На второй стадии субстрат под воздействием связанного с ним фермента видоизменяется и становится более доступным для соответствующей химической реакции. Эта стадия определяет скорость всего процесса. На третьей стадии происходит химическая реакция, в результате которой образуется комплекс продукта реакции с ферментом. Заключительным процессом является высвобождение продукта реакции из комплекса.
На первой стадии ферментативного катализа происходит образование фермент субстратного комплекса, где фермент и субстрат могут быть связаны ионной, ковалентной или иной связью. Образование комплекса E*S происходит практически мгновенно. На второй стадии субстрат под воздействием связанного с ним фермента видоизменяется и становится более доступным для соответствующей химической реакции. Эта стадия определяет скорость всего процесса. На третьей стадии происходит химическая реакция, в результате которой образуется комплекс продукта реакции с ферментом. Заключительным процессом является высвобождение продукта реакции из комплекса.
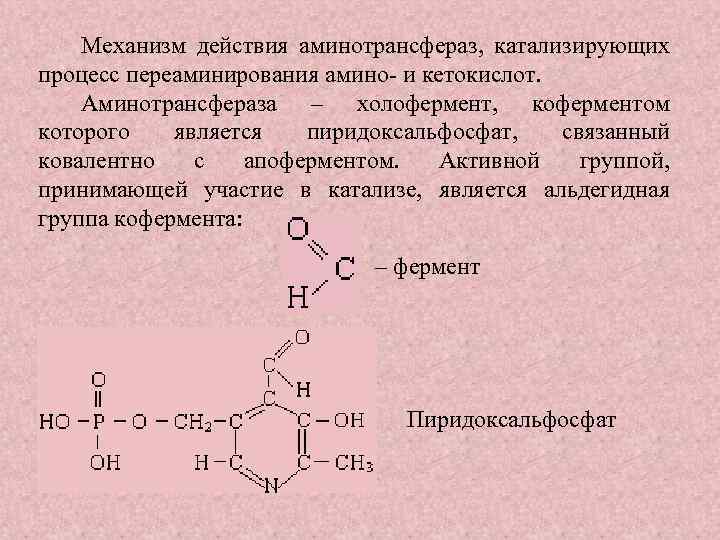 Механизм действия аминотрансфераз, катализирующих процесс переаминирования амино и кетокислот. Аминотрансфераза – холофермент, коферментом которого является пиридоксальфосфат, связанный ковалентно с апоферментом. Активной группой, принимающей участие в катализе, является альдегидная группа кофермента: – фермент Пиридоксальфосфат
Механизм действия аминотрансфераз, катализирующих процесс переаминирования амино и кетокислот. Аминотрансфераза – холофермент, коферментом которого является пиридоксальфосфат, связанный ковалентно с апоферментом. Активной группой, принимающей участие в катализе, является альдегидная группа кофермента: – фермент Пиридоксальфосфат
![На первой стадии ферментативного катализа происходит образование ферментсубстратного комплекса [E*S], в котором фермент и На первой стадии ферментативного катализа происходит образование ферментсубстратного комплекса [E*S], в котором фермент и](https://present5.com/presentation/-31160604_33693297/image-15.jpg) На первой стадии ферментативного катализа происходит образование ферментсубстратного комплекса [E*S], в котором фермент и субстрат связаны ковалентной связью:
На первой стадии ферментативного катализа происходит образование ферментсубстратного комплекса [E*S], в котором фермент и субстрат связаны ковалентной связью:
 На второй стадии происходит преобразование субстрата, выражающееся в таутомерной перегруппировке, что приводит к образованию комплекса [E*S]`:
На второй стадии происходит преобразование субстрата, выражающееся в таутомерной перегруппировке, что приводит к образованию комплекса [E*S]`:
 Третья стадия В результате химической реакции образуется кетокислота, а фермент высвобождается из комплекса в виде пиридоксаминфермента. Чтобы не нарушался один из основных принципов катализа, в данном процессе принимает участие кетокислота.
Третья стадия В результате химической реакции образуется кетокислота, а фермент высвобождается из комплекса в виде пиридоксаминфермента. Чтобы не нарушался один из основных принципов катализа, в данном процессе принимает участие кетокислота.
 Свойства ферментов Ферменты обладают всеми свойствами белков. Однако по сравнению с белками, выполняющими другие функции в клетке, ферменты имеют ряд специфических, присущих только им свойств. 1. Зависимость активности фермента от температуры; 2. Зависимость активности фермента от p. H среды; 3. Специфичность; 4. Влияние на активность ферментов активаторов и ингибиторов.
Свойства ферментов Ферменты обладают всеми свойствами белков. Однако по сравнению с белками, выполняющими другие функции в клетке, ферменты имеют ряд специфических, присущих только им свойств. 1. Зависимость активности фермента от температуры; 2. Зависимость активности фермента от p. H среды; 3. Специфичность; 4. Влияние на активность ферментов активаторов и ингибиторов.
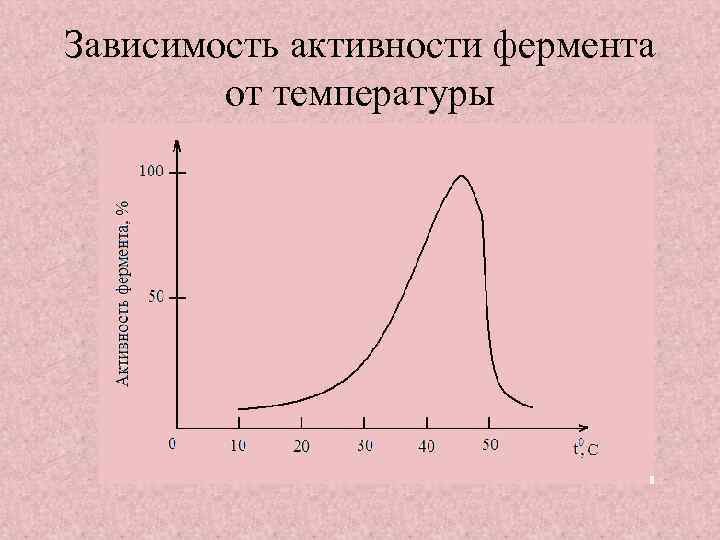 Зависимость активности фермента от температуры
Зависимость активности фермента от температуры
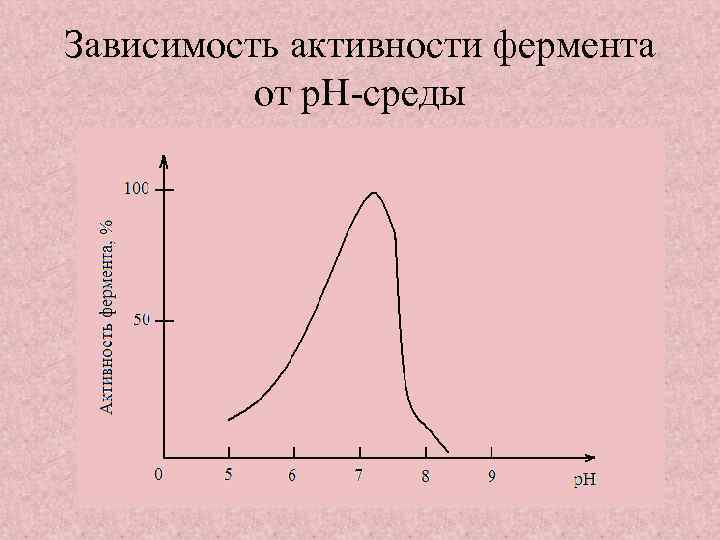 Зависимость активности фермента от p. H среды
Зависимость активности фермента от p. H среды
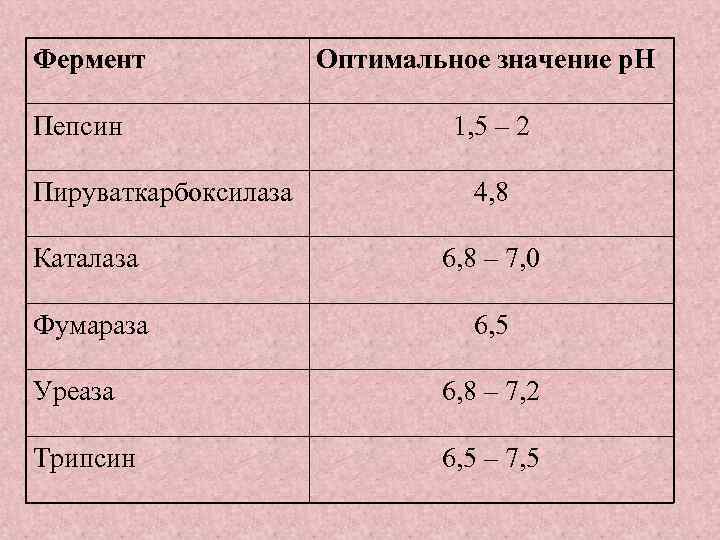 Фермент Пепсин Пируваткарбоксилаза Оптимальное значение р. Н 1, 5 – 2 4, 8 Каталаза 6, 8 – 7, 0 Фумараза 6, 5 Уреаза 6, 8 – 7, 2 Трипсин 6, 5 – 7, 5
Фермент Пепсин Пируваткарбоксилаза Оптимальное значение р. Н 1, 5 – 2 4, 8 Каталаза 6, 8 – 7, 0 Фумараза 6, 5 Уреаза 6, 8 – 7, 2 Трипсин 6, 5 – 7, 5
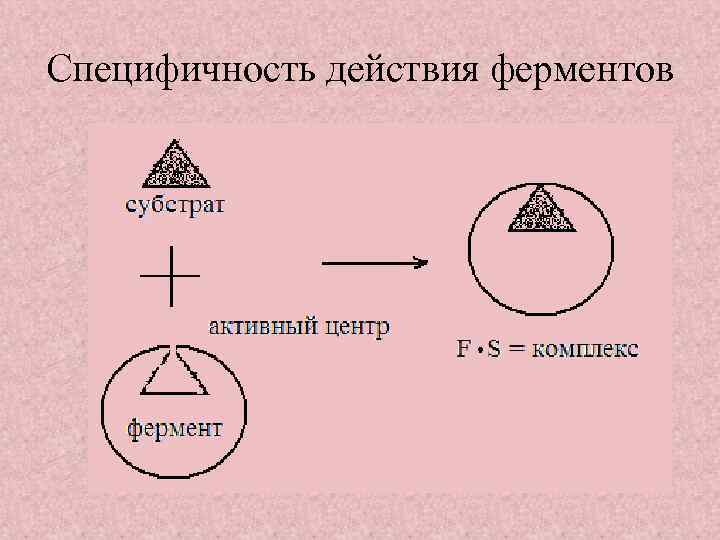 Специфичность действия ферментов
Специфичность действия ферментов
 Специфичность – избирательность фермента по отношению к субстрату Стереохимическая субстратная специфичность фермент катализирует превращение только одного стереоизомера субстрата Абсолютная субстратная специфичность Групповая субстратная специфичность фермент катализирует превращение только одного субстрата фермент катализирует превращение группы субстратов сходной химической структуры
Специфичность – избирательность фермента по отношению к субстрату Стереохимическая субстратная специфичность фермент катализирует превращение только одного стереоизомера субстрата Абсолютная субстратная специфичность Групповая субстратная специфичность фермент катализирует превращение только одного субстрата фермент катализирует превращение группы субстратов сходной химической структуры
 Влияние на активность ферментов активаторов и ингибиторов АКТИВАТОРЫ Повышают активность ферментов Mg 2+ Mn 2+ Zn 2+ K+ Co+ Cl ИНГИБИТОРЫ Понижают активность ферментов Эндогенные вещества Экзогенные вещества
Влияние на активность ферментов активаторов и ингибиторов АКТИВАТОРЫ Повышают активность ферментов Mg 2+ Mn 2+ Zn 2+ K+ Co+ Cl ИНГИБИТОРЫ Понижают активность ферментов Эндогенные вещества Экзогенные вещества
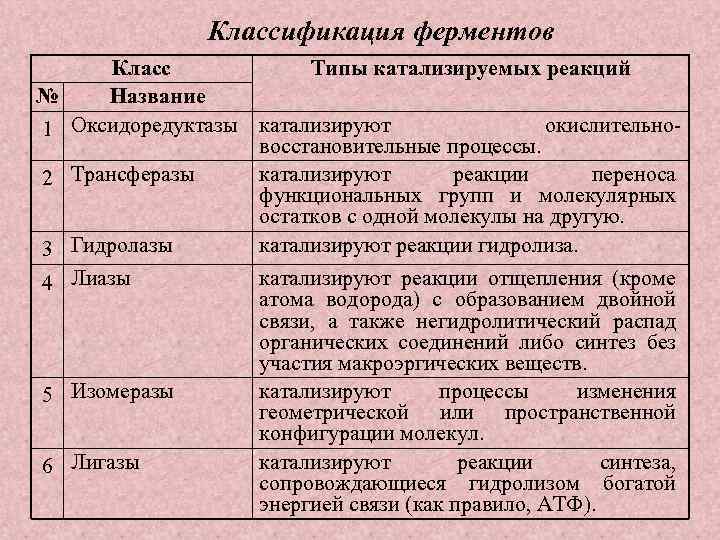 Классификация ферментов Класс № Название 1 Оксидоредуктазы 2 Трансферазы 3 Гидролазы 4 Лиазы 5 Изомеразы 6 Лигазы Типы катализируемых реакций катализируют окислительно восстановительные процессы. катализируют реакции переноса функциональных групп и молекулярных остатков с одной молекулы на другую. катализируют реакции гидролиза. катализируют реакции отщепления (кроме атома водорода) с образованием двойной связи, а также негидролитический распад органических соединений либо синтез без участия макроэргических веществ. катализируют процессы изменения геометрической или пространственной конфигурации молекул. катализируют реакции синтеза, сопровождающиеся гидролизом богатой энергией связи (как правило, АТФ).
Классификация ферментов Класс № Название 1 Оксидоредуктазы 2 Трансферазы 3 Гидролазы 4 Лиазы 5 Изомеразы 6 Лигазы Типы катализируемых реакций катализируют окислительно восстановительные процессы. катализируют реакции переноса функциональных групп и молекулярных остатков с одной молекулы на другую. катализируют реакции гидролиза. катализируют реакции отщепления (кроме атома водорода) с образованием двойной связи, а также негидролитический распад органических соединений либо синтез без участия макроэргических веществ. катализируют процессы изменения геометрической или пространственной конфигурации молекул. катализируют реакции синтеза, сопровождающиеся гидролизом богатой энергией связи (как правило, АТФ).
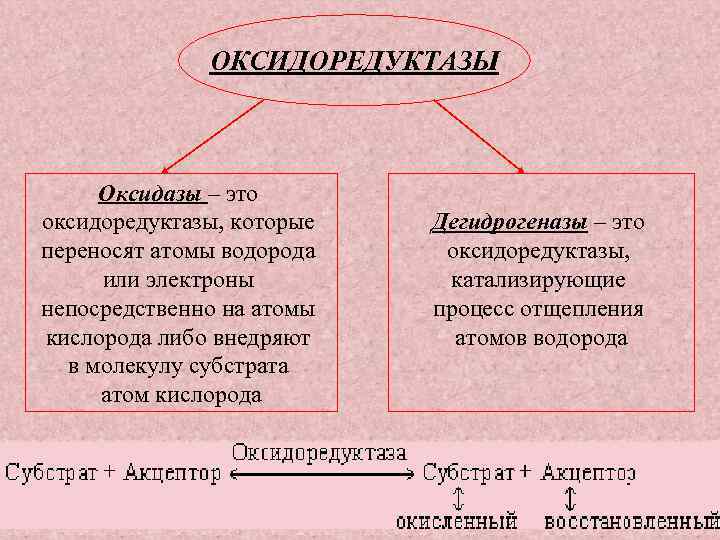 ОКСИДОРЕДУКТАЗЫ Оксидазы – это оксидоредуктазы, которые переносят атомы водорода или электроны непосредственно на атомы кислорода либо внедряют в молекулу субстрата атом кислорода Дегидрогеназы – это оксидоредуктазы, катализирующие процесс отщепления атомов водорода
ОКСИДОРЕДУКТАЗЫ Оксидазы – это оксидоредуктазы, которые переносят атомы водорода или электроны непосредственно на атомы кислорода либо внедряют в молекулу субстрата атом кислорода Дегидрогеназы – это оксидоредуктазы, катализирующие процесс отщепления атомов водорода
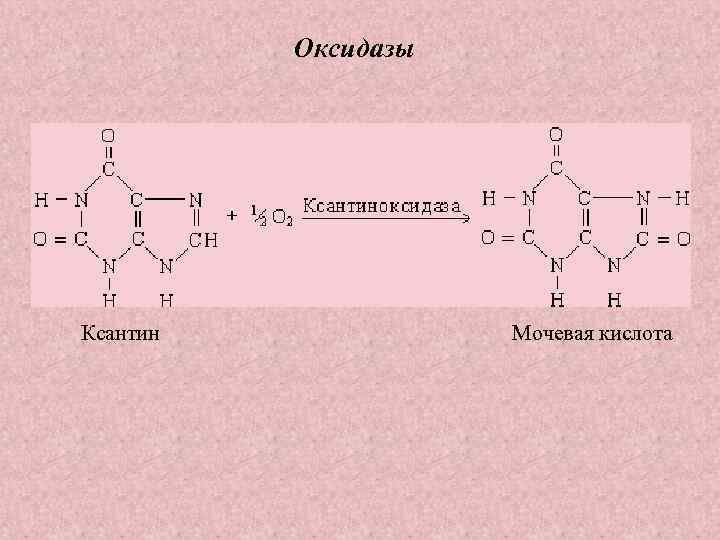 Оксидазы Ксантин Мочевая кислота
Оксидазы Ксантин Мочевая кислота
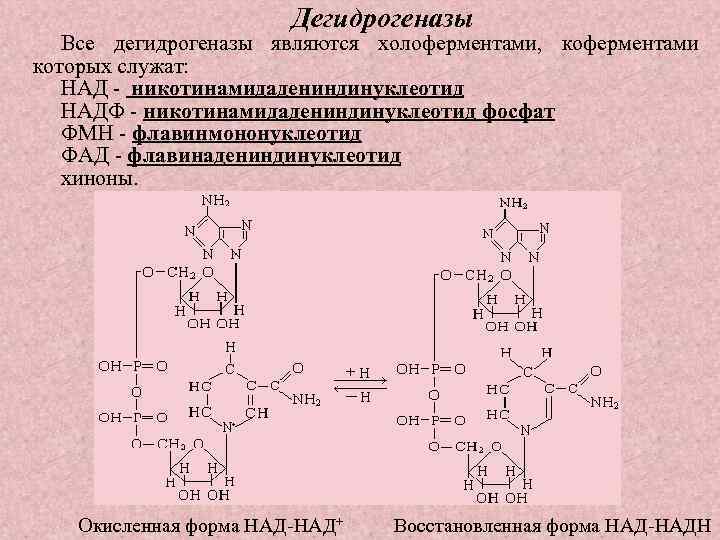 Дегидрогеназы Все дегидрогеназы являются холоферментами, коферментами которых служат: НАД никотинамидадениндинуклеотид НАДФ никотинамидадениндинуклеотид фосфат ФМН флавинмононуклеотид ФАД флавинадениндинуклеотид хиноны. Окисленная форма НАД+ Восстановленная форма НАДН
Дегидрогеназы Все дегидрогеназы являются холоферментами, коферментами которых служат: НАД никотинамидадениндинуклеотид НАДФ никотинамидадениндинуклеотид фосфат ФМН флавинмононуклеотид ФАД флавинадениндинуклеотид хиноны. Окисленная форма НАД+ Восстановленная форма НАДН
 Примером процесса, катализируемого НАД зависимой дегидрогеназой, может служить окисление молочной кислоты (лактата) до пировиноградной кислоты (пирувата): Молочная кислота Пировиноградная кислота
Примером процесса, катализируемого НАД зависимой дегидрогеназой, может служить окисление молочной кислоты (лактата) до пировиноградной кислоты (пирувата): Молочная кислота Пировиноградная кислота
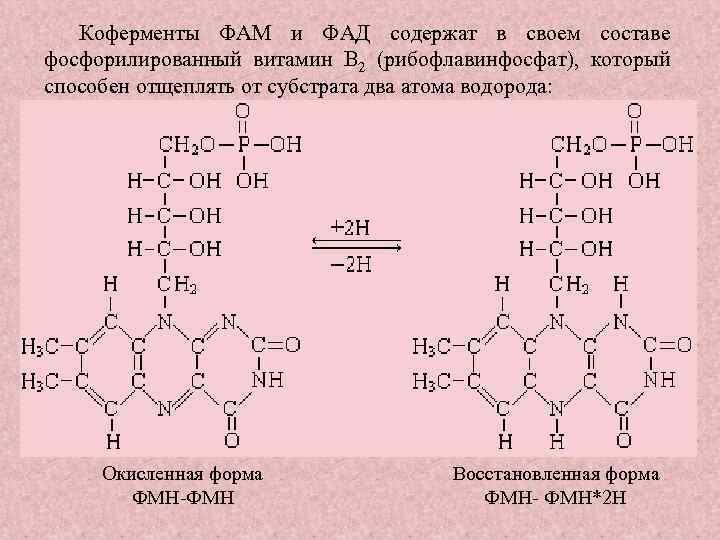 Коферменты ФАМ и ФАД содержат в своем составе фосфорилированный витамин В 2 (рибофлавинфосфат), который способен отщеплять от субстрата два атома водорода: Окисленная форма ФМН Восстановленная форма ФМН*2 Н
Коферменты ФАМ и ФАД содержат в своем составе фосфорилированный витамин В 2 (рибофлавинфосфат), который способен отщеплять от субстрата два атома водорода: Окисленная форма ФМН Восстановленная форма ФМН*2 Н
 Пример реакции, катализируемой ФАД зависимой дегидрогеназой: Янтарная кислота Фумаровая кислота
Пример реакции, катализируемой ФАД зависимой дегидрогеназой: Янтарная кислота Фумаровая кислота
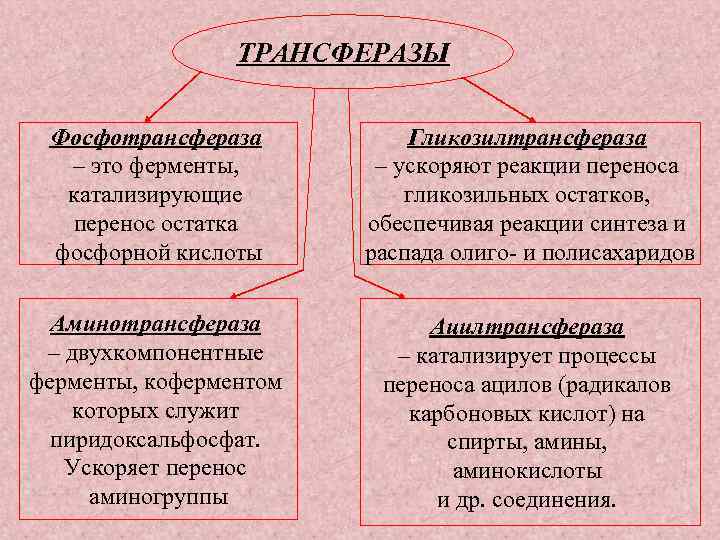 ТРАНСФЕРАЗЫ Фосфотрансфераза – это ферменты, катализирующие перенос остатка фосфорной кислоты Гликозилтрансфераза – ускоряют реакции переноса гликозильных остатков, обеспечивая реакции синтеза и распада олиго и полисахаридов Аминотрансфераза – двухкомпонентные ферменты, коферментом которых служит пиридоксальфосфат. Ускоряет перенос аминогруппы Ацилтрансфераза – катализирует процессы переноса ацилов (радикалов карбоновых кислот) на спирты, аминокислоты и др. соединения.
ТРАНСФЕРАЗЫ Фосфотрансфераза – это ферменты, катализирующие перенос остатка фосфорной кислоты Гликозилтрансфераза – ускоряют реакции переноса гликозильных остатков, обеспечивая реакции синтеза и распада олиго и полисахаридов Аминотрансфераза – двухкомпонентные ферменты, коферментом которых служит пиридоксальфосфат. Ускоряет перенос аминогруппы Ацилтрансфераза – катализирует процессы переноса ацилов (радикалов карбоновых кислот) на спирты, аминокислоты и др. соединения.
 Фосфотрансферазы, использующие в качестве донора фосфатной группы молекулу АТФ, называются киназами. Глицерин Фосфоглицерин
Фосфотрансферазы, использующие в качестве донора фосфатной группы молекулу АТФ, называются киназами. Глицерин Фосфоглицерин
 Гликозилтрансферазы Если гликозильный остаток переносится на молекулу фосфорной кислоты, то процесс называется фосфоролизом, а ферменты, обеспечивающие этот процесс, называются фосфорилазами.
Гликозилтрансферазы Если гликозильный остаток переносится на молекулу фосфорной кислоты, то процесс называется фосфоролизом, а ферменты, обеспечивающие этот процесс, называются фосфорилазами.
 Ацилтрансферазы Источником ацилов является ацил-Ко. А, который можно рассматривать в качестве кофактора в реакциях переноса ацильных групп. Фосфоглицерин Пальмитил Ко. А Фосфатидная кислота
Ацилтрансферазы Источником ацилов является ацил-Ко. А, который можно рассматривать в качестве кофактора в реакциях переноса ацильных групп. Фосфоглицерин Пальмитил Ко. А Фосфатидная кислота
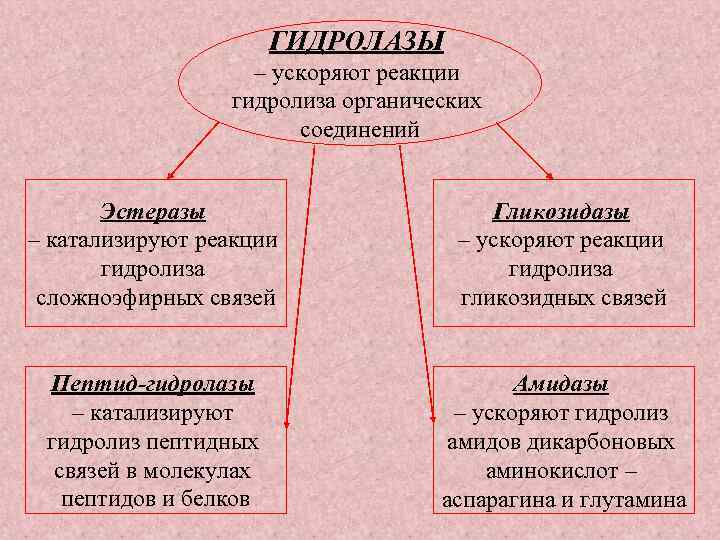 ГИДРОЛАЗЫ – ускоряют реакции гидролиза органических соединений Эстеразы – катализируют реакции гидролиза сложноэфирных связей Гликозидазы – ускоряют реакции гидролиза гликозидных связей Пептид-гидролазы – катализируют гидролиз пептидных связей в молекулах пептидов и белков Амидазы – ускоряют гидролиз амидов дикарбоновых аминокислот – аспарагина и глутамина
ГИДРОЛАЗЫ – ускоряют реакции гидролиза органических соединений Эстеразы – катализируют реакции гидролиза сложноэфирных связей Гликозидазы – ускоряют реакции гидролиза гликозидных связей Пептид-гидролазы – катализируют гидролиз пептидных связей в молекулах пептидов и белков Амидазы – ускоряют гидролиз амидов дикарбоновых аминокислот – аспарагина и глутамина
 Эстеразы Трипальмитин β Пальмитилглицерин Пальмитиновая кислота Липаза ускоряет гидролиз внешних сложноэфирных связей в молекуле триглицерида. Особенно широко распространены эстеразы, катализирующие гидролиз сложных эфиров фосфорной кислоты и углеводов. Эти ферменты называются фосфатазами:
Эстеразы Трипальмитин β Пальмитилглицерин Пальмитиновая кислота Липаза ускоряет гидролиз внешних сложноэфирных связей в молекуле триглицерида. Особенно широко распространены эстеразы, катализирующие гидролиз сложных эфиров фосфорной кислоты и углеводов. Эти ферменты называются фосфатазами:
 Гликозидазы Из гликозидаз, действующих на полисахариды, наиболее распространены амилазы.
Гликозидазы Из гликозидаз, действующих на полисахариды, наиболее распространены амилазы.
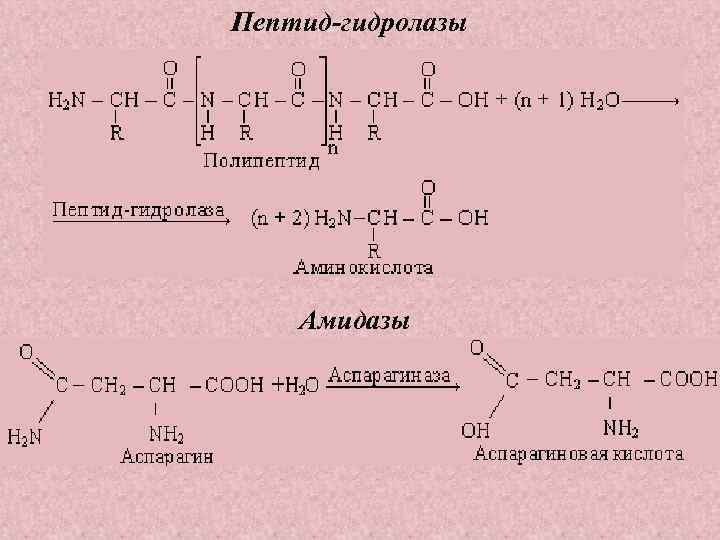 Пептид-гидролазы Амидазы
Пептид-гидролазы Амидазы
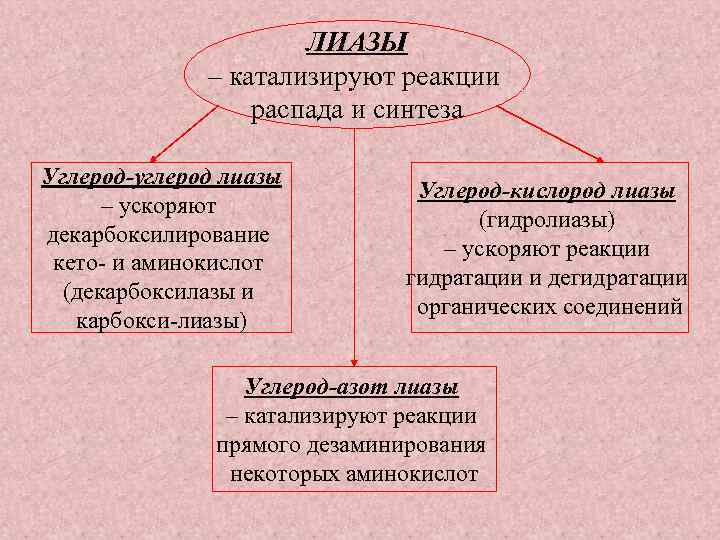 ЛИАЗЫ – катализируют реакции распада и синтеза Углерод-углерод лиазы – ускоряют декарбоксилирование кето и аминокислот (декарбоксилазы и карбокси лиазы) Углерод-кислород лиазы (гидролиазы) – ускоряют реакции гидратации и дегидратации органических соединений Углерод-азот лиазы – катализируют реакции прямого дезаминирования некоторых аминокислот
ЛИАЗЫ – катализируют реакции распада и синтеза Углерод-углерод лиазы – ускоряют декарбоксилирование кето и аминокислот (декарбоксилазы и карбокси лиазы) Углерод-кислород лиазы (гидролиазы) – ускоряют реакции гидратации и дегидратации органических соединений Углерод-азот лиазы – катализируют реакции прямого дезаминирования некоторых аминокислот
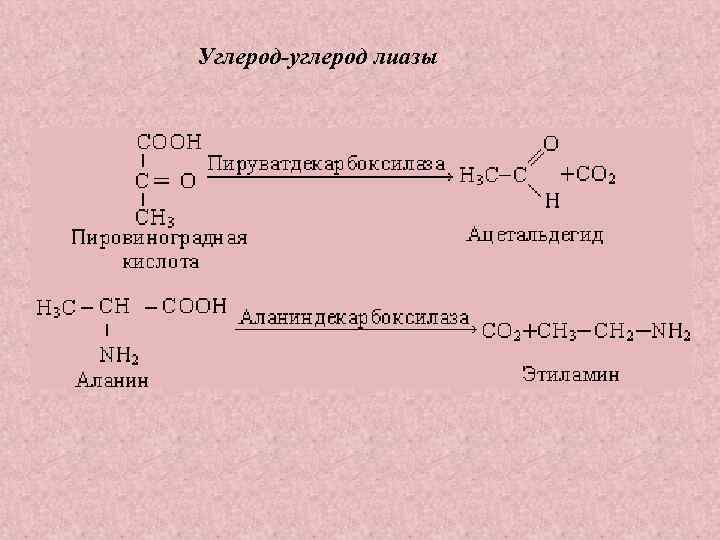 Углерод-углерод лиазы
Углерод-углерод лиазы
 Углерод-кислород лиазы (гидролиазы) Углерод-азот лиазы
Углерод-кислород лиазы (гидролиазы) Углерод-азот лиазы
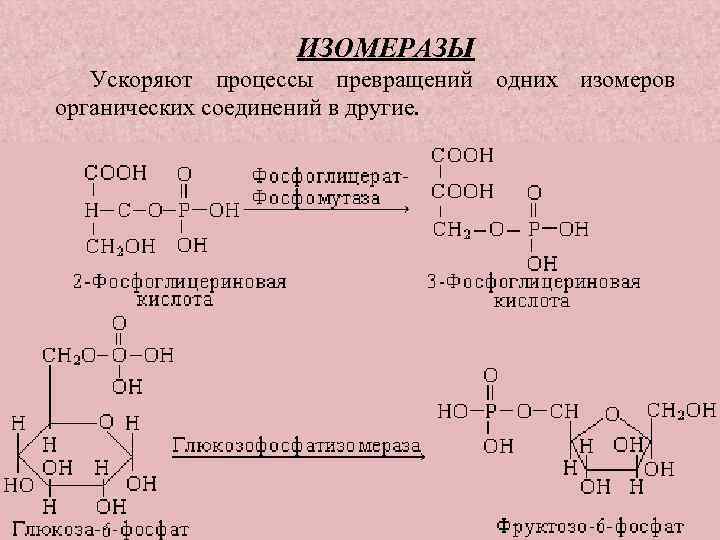 ИЗОМЕРАЗЫ Ускоряют процессы превращений одних изомеров органических соединений в другие.
ИЗОМЕРАЗЫ Ускоряют процессы превращений одних изомеров органических соединений в другие.
 ЛИГАЗЫ (синтетазы) Обеспечивают синтез различных органических соединений Важной реакцией является образование ацил коэнзима А (Ко. А), которая тоже ускоряется ферментом, относящимся к рассматриваемому классу:
ЛИГАЗЫ (синтетазы) Обеспечивают синтез различных органических соединений Важной реакцией является образование ацил коэнзима А (Ко. А), которая тоже ускоряется ферментом, относящимся к рассматриваемому классу:
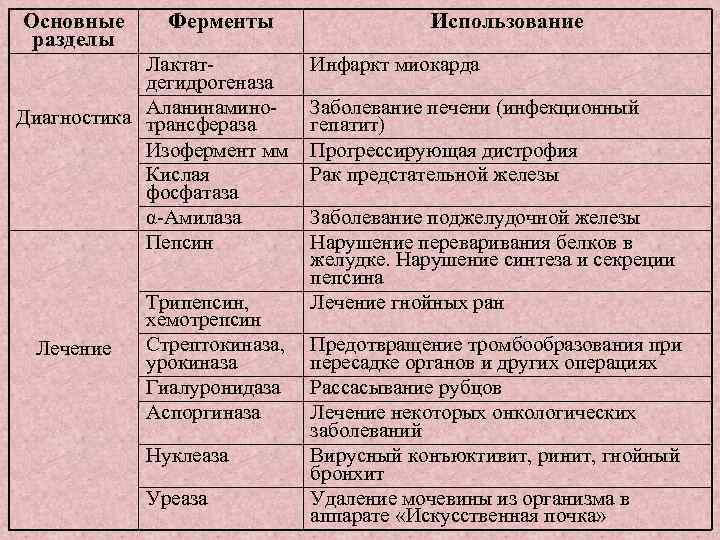 Основные разделы Ферменты Лактат дегидрогеназа Диагностика Аланинамино трансфераза Изофермент мм Кислая фосфатаза α Амилаза Пепсин Лечение Трипепсин, хемотрепсин Стрептокиназа, урокиназа Гиалуронидаза Аспоргиназа Нуклеаза Уреаза Использование Инфаркт миокарда Заболевание печени (инфекционный гепатит) Прогрессирующая дистрофия Рак предстательной железы Заболевание поджелудочной железы Нарушение переваривания белков в желудке. Нарушение синтеза и секреции пепсина Лечение гнойных ран Предотвращение тромбообразования при пересадке органов и других операциях Рассасывание рубцов Лечение некоторых онкологических заболеваний Вирусный конъюктивит, ринит, гнойный бронхит Удаление мочевины из организма в аппарате «Искусственная почка»
Основные разделы Ферменты Лактат дегидрогеназа Диагностика Аланинамино трансфераза Изофермент мм Кислая фосфатаза α Амилаза Пепсин Лечение Трипепсин, хемотрепсин Стрептокиназа, урокиназа Гиалуронидаза Аспоргиназа Нуклеаза Уреаза Использование Инфаркт миокарда Заболевание печени (инфекционный гепатит) Прогрессирующая дистрофия Рак предстательной железы Заболевание поджелудочной железы Нарушение переваривания белков в желудке. Нарушение синтеза и секреции пепсина Лечение гнойных ран Предотвращение тромбообразования при пересадке органов и других операциях Рассасывание рубцов Лечение некоторых онкологических заболеваний Вирусный конъюктивит, ринит, гнойный бронхит Удаление мочевины из организма в аппарате «Искусственная почка»


