6_Med_genetika_Epigenetika.ppt
- Количество слайдов: 38
 Уважаемые студенты! Ответьте письменно на следующие вопросы: 1) Что такое эпигенетика? 2) Какие биохимические механизмы лежат в основе эпигенетических явлений? 3) Когда происходят наиболее интенсивные изменения метилирования ДНК, затрагивающие весь геном? Для чего они нужны? 4) Может ли организм существовать при «выключенной» системе метилирования ДНК? Ответ обоснуйте. 5) Чем отличаются функции ДНК-метилтрансфераз разных типов? 6) Почему во время беременности рекомендуют принимать фолиевую кислоту? Почему рекомендуют отказываться от вегетарианства? Время на ответы – 1 час (до 15. 00). Учитывая то, что на лекции многих не было, предоставляю вам возможность полистать слайды (в этой презентации). Соблюдайте тишину!!!
Уважаемые студенты! Ответьте письменно на следующие вопросы: 1) Что такое эпигенетика? 2) Какие биохимические механизмы лежат в основе эпигенетических явлений? 3) Когда происходят наиболее интенсивные изменения метилирования ДНК, затрагивающие весь геном? Для чего они нужны? 4) Может ли организм существовать при «выключенной» системе метилирования ДНК? Ответ обоснуйте. 5) Чем отличаются функции ДНК-метилтрансфераз разных типов? 6) Почему во время беременности рекомендуют принимать фолиевую кислоту? Почему рекомендуют отказываться от вегетарианства? Время на ответы – 1 час (до 15. 00). Учитывая то, что на лекции многих не было, предоставляю вам возможность полистать слайды (в этой презентации). Соблюдайте тишину!!!
 Лекция № 6 Эпигенетика «Генетика предполагает, а эпигенетика располагает» . P. Medawar & J. Medawar
Лекция № 6 Эпигенетика «Генетика предполагает, а эпигенетика располагает» . P. Medawar & J. Medawar
 Центральная догма молекулярной биологии: ДНК ------ РНК ------- БЕЛОК Генотип--------фенотип ДНК ответственна за хранение, передачу и реализацию наследственной информации
Центральная догма молекулярной биологии: ДНК ------ РНК ------- БЕЛОК Генотип--------фенотип ДНК ответственна за хранение, передачу и реализацию наследственной информации
 Доимплантационное развитие человека День 1. Стадия зиготы День 2. Эмбрион в стадии дробления 4 бластомера День 3. Эмбрион на стадии дробления 8 клеток. День 4. Морула. 4 День 5. Бластоциста
Доимплантационное развитие человека День 1. Стадия зиготы День 2. Эмбрион в стадии дробления 4 бластомера День 3. Эмбрион на стадии дробления 8 клеток. День 4. Морула. 4 День 5. Бластоциста
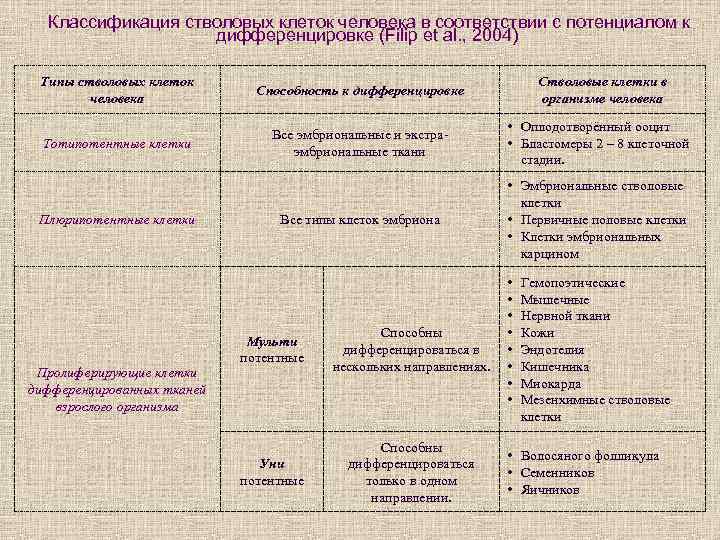 Классификация стволовых клеток человека в соответствии с потенциалом к дифференцировке (Filip et al. , 2004) Типы стволовых клеток человека Способность к дифференцировке Тотипотентные клетки Все эмбриональные и экстраэмбриональные ткани • Оплодотворённый ооцит • Бластомеры 2 – 8 клеточной стадии. Все типы клеток эмбриона • Эмбриональные стволовые клетки • Первичные половые клетки • Клетки эмбриональных карцином Плюрипотентные клетки Пролиферирующие клетки дифференцированных тканей взрослого организма Мульти потентные Способны дифференцироваться в нескольких направлениях. Уни потентные Способны дифференцироваться только в одном направлении. Стволовые клетки в организме человека • • Гемопоэтические Мышечные Нервной ткани Кожи Эндотелия Кишечника Миокарда Мезенхимные стволовые клетки • Волосяного фолликула • Семенников • Яичников
Классификация стволовых клеток человека в соответствии с потенциалом к дифференцировке (Filip et al. , 2004) Типы стволовых клеток человека Способность к дифференцировке Тотипотентные клетки Все эмбриональные и экстраэмбриональные ткани • Оплодотворённый ооцит • Бластомеры 2 – 8 клеточной стадии. Все типы клеток эмбриона • Эмбриональные стволовые клетки • Первичные половые клетки • Клетки эмбриональных карцином Плюрипотентные клетки Пролиферирующие клетки дифференцированных тканей взрослого организма Мульти потентные Способны дифференцироваться в нескольких направлениях. Уни потентные Способны дифференцироваться только в одном направлении. Стволовые клетки в организме человека • • Гемопоэтические Мышечные Нервной ткани Кожи Эндотелия Кишечника Миокарда Мезенхимные стволовые клетки • Волосяного фолликула • Семенников • Яичников
 Разные судьбы, функции, морфология, «способности» клеток при одинаковом генотипе
Разные судьбы, функции, морфология, «способности» клеток при одинаковом генотипе
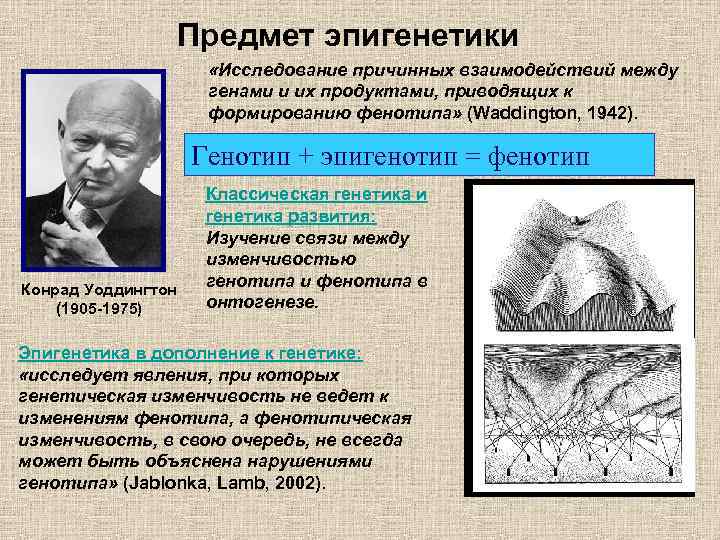 Предмет эпигенетики «Исследование причинных взаимодействий между генами и их продуктами, приводящих к формированию фенотипа» (Waddington, 1942). Генотип + эпигенотип = фенотип Конрад Уоддингтон (1905 -1975) Классическая генетика и генетика развития: Изучение связи между изменчивостью генотипа и фенотипа в онтогенезе. Эпигенетика в дополнение к генетике: «исследует явления, при которых генетическая изменчивость не ведет к изменениям фенотипа, а фенотипическая изменчивость, в свою очередь, не всегда может быть объяснена нарушениями генотипа» (Jablonka, Lamb, 2002).
Предмет эпигенетики «Исследование причинных взаимодействий между генами и их продуктами, приводящих к формированию фенотипа» (Waddington, 1942). Генотип + эпигенотип = фенотип Конрад Уоддингтон (1905 -1975) Классическая генетика и генетика развития: Изучение связи между изменчивостью генотипа и фенотипа в онтогенезе. Эпигенетика в дополнение к генетике: «исследует явления, при которых генетическая изменчивость не ведет к изменениям фенотипа, а фенотипическая изменчивость, в свою очередь, не всегда может быть объяснена нарушениями генотипа» (Jablonka, Lamb, 2002).
 Эпигенетическое наследование В более общем смысле, предметом эпигенетики являются явления, связанные с развитием различных фенотипов клеток или организмов на основе одного генотипа. В более узком смысле эпигенетика – раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток. Эпигенетическое наследование – наследование паттерна экспрессии генов.
Эпигенетическое наследование В более общем смысле, предметом эпигенетики являются явления, связанные с развитием различных фенотипов клеток или организмов на основе одного генотипа. В более узком смысле эпигенетика – раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток. Эпигенетическое наследование – наследование паттерна экспрессии генов.
 Эпигенетическая регуляция - наследственные и ненаследственные изменения в экспрессии конкретного гена без каких-либо соответствующих структурных изменений в его нуклеотидной последовательности. Эпигенетические явления: импринтинг, эффект положения, особенности структурно-функциональной организации хроматина определенных хромосомных локусов, влияющие на экспрессию генов, интерференция РНК.
Эпигенетическая регуляция - наследственные и ненаследственные изменения в экспрессии конкретного гена без каких-либо соответствующих структурных изменений в его нуклеотидной последовательности. Эпигенетические явления: импринтинг, эффект положения, особенности структурно-функциональной организации хроматина определенных хромосомных локусов, влияющие на экспрессию генов, интерференция РНК.
 ДВА ВИДА ИНФОРМАЦИИ В ГЕНОМЕ Генетическая – закодированная в ДНК программа создания живого организма Эпигенетическая (динамическая) – как, где и когда должна быть реализована генетическая информация. Каждый вид информации обеспечен своими системами: Кодирования Хранения Передачи
ДВА ВИДА ИНФОРМАЦИИ В ГЕНОМЕ Генетическая – закодированная в ДНК программа создания живого организма Эпигенетическая (динамическая) – как, где и когда должна быть реализована генетическая информация. Каждый вид информации обеспечен своими системами: Кодирования Хранения Передачи
 Изменения генетические • Необратимы (мутации) • Изменения первичной структуры ДНК • Стабильно наследуемые эпигенетические • Обратимы • Не затрагивают изменений первичной структуры ДНК • Бывают долговременные и кратковременные
Изменения генетические • Необратимы (мутации) • Изменения первичной структуры ДНК • Стабильно наследуемые эпигенетические • Обратимы • Не затрагивают изменений первичной структуры ДНК • Бывают долговременные и кратковременные
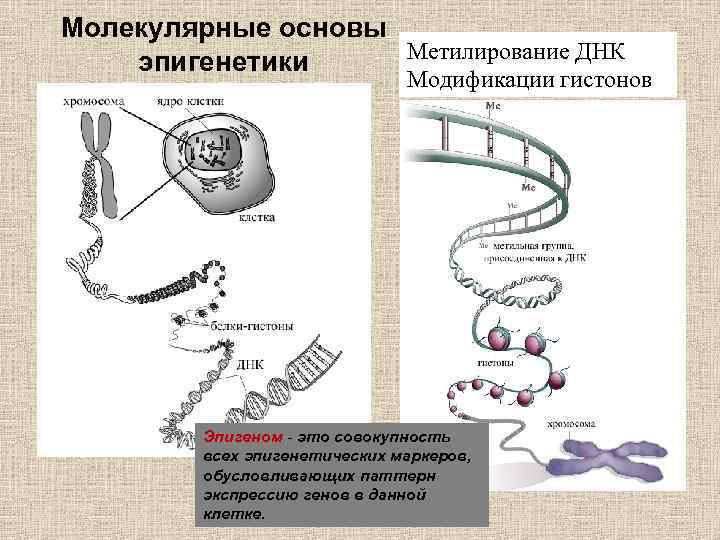 Молекулярные основы Метилирование ДНК эпигенетики Модификации гистонов Эпигеном - это совокупность всех эпигенетических маркеров, обусловливающих паттерн экспрессию генов в данной клетке.
Молекулярные основы Метилирование ДНК эпигенетики Модификации гистонов Эпигеном - это совокупность всех эпигенетических маркеров, обусловливающих паттерн экспрессию генов в данной клетке.
 Посттрансляционные модификации гистонов
Посттрансляционные модификации гистонов
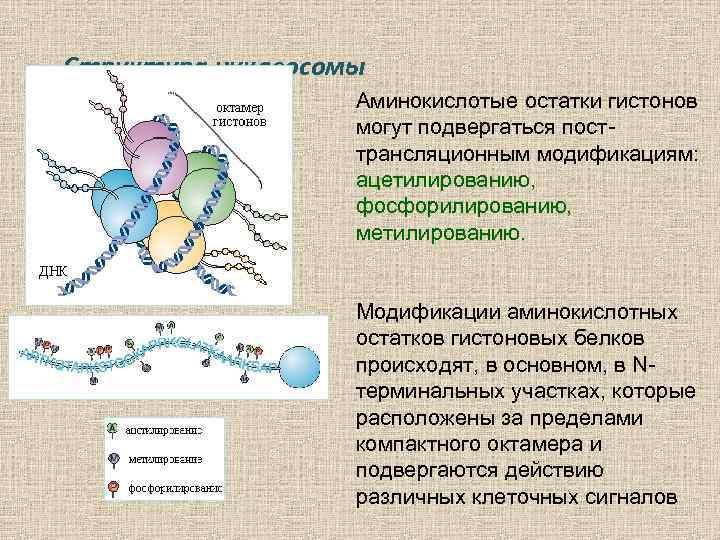 Структура нуклеосомы Аминокислотые остатки гистонов могут подвергаться посттрансляционным модификациям: ацетилированию, фосфорилированию, метилированию. Модификации аминокислотных остатков гистоновых белков происходят, в основном, в Nтерминальных участках, которые расположены за пределами компактного октамера и подвергаются действию различных клеточных сигналов
Структура нуклеосомы Аминокислотые остатки гистонов могут подвергаться посттрансляционным модификациям: ацетилированию, фосфорилированию, метилированию. Модификации аминокислотных остатков гистоновых белков происходят, в основном, в Nтерминальных участках, которые расположены за пределами компактного октамера и подвергаются действию различных клеточных сигналов
 В зависимости от типа и сайта модификаций аминокислотных остатков, каждая нуклеосома имеет свой «гистоновый код» , регулирующий активность транскрипции
В зависимости от типа и сайта модификаций аминокислотных остатков, каждая нуклеосома имеет свой «гистоновый код» , регулирующий активность транскрипции
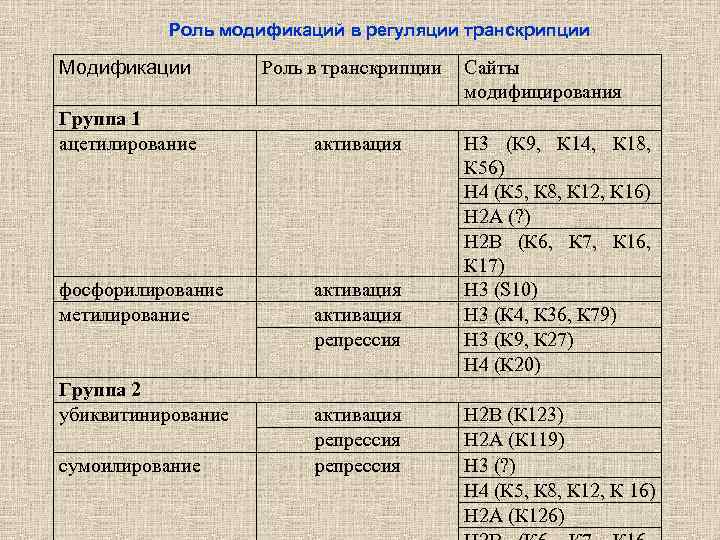 Роль модификаций в регуляции транскрипции Модификации Роль в транскрипции Группа 1 ацетилирование активация фосфорилирование метилирование Группа 2 убиквитинирование сумоилирование активация репрессия Сайты модифицирования Н 3 (К 9, К 14, К 18, К 56) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (? ) Н 2 В (К 6, К 7, К 16, К 17) Н 3 (S 10) Н 3 (К 4, К 36, К 79) Н 3 (К 9, К 27) Н 4 (К 20) Н 2 В (К 123) Н 2 А (К 119) Н 3 (? ) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (К 126)
Роль модификаций в регуляции транскрипции Модификации Роль в транскрипции Группа 1 ацетилирование активация фосфорилирование метилирование Группа 2 убиквитинирование сумоилирование активация репрессия Сайты модифицирования Н 3 (К 9, К 14, К 18, К 56) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (? ) Н 2 В (К 6, К 7, К 16, К 17) Н 3 (S 10) Н 3 (К 4, К 36, К 79) Н 3 (К 9, К 27) Н 4 (К 20) Н 2 В (К 123) Н 2 А (К 119) Н 3 (? ) Н 4 (К 5, К 8, К 12, К 16) Н 2 А (К 126)
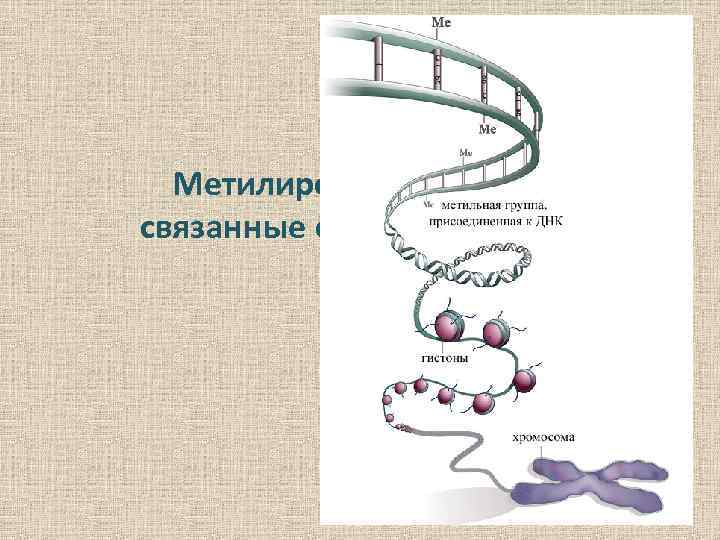 Метилирование ДНК и связанные с ним процессы
Метилирование ДНК и связанные с ним процессы
 Молекулярные основы эпигенетики H H N CH 3 4 3 5 6 N 1 Б. Ф. Ванюшин Впервые определил природу метилируемых последовательностей ДНК у разных видов организмов (1959 г. ) N 2 O Robin Holliday Обосновал роль метилирования ДНК в регуляции работы гена. Предложил термин «эпимутация» (1987 г. )
Молекулярные основы эпигенетики H H N CH 3 4 3 5 6 N 1 Б. Ф. Ванюшин Впервые определил природу метилируемых последовательностей ДНК у разных видов организмов (1959 г. ) N 2 O Robin Holliday Обосновал роль метилирования ДНК в регуляции работы гена. Предложил термин «эпимутация» (1987 г. )
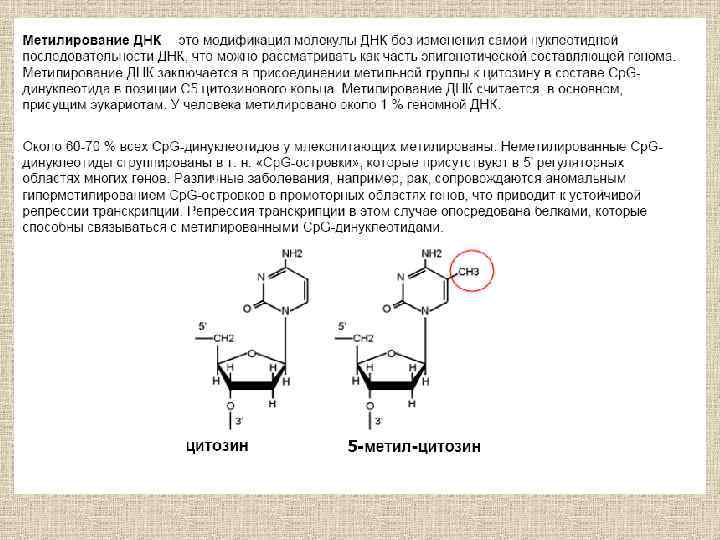
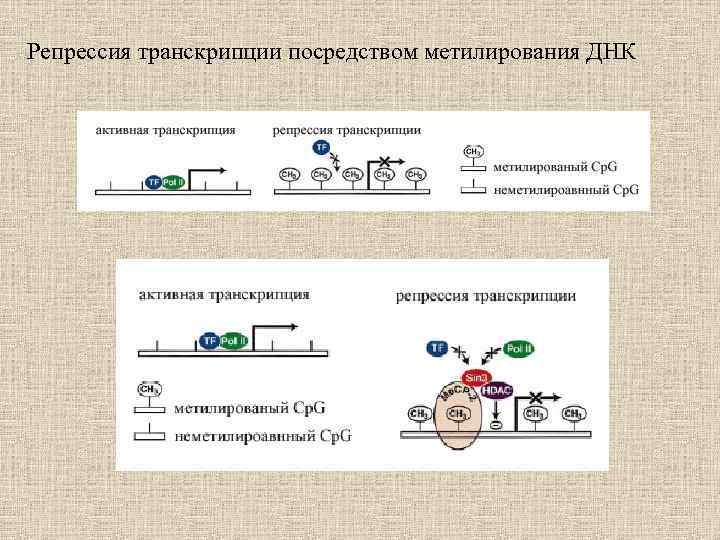 Репрессия транскрипции посредством метилирования ДНК
Репрессия транскрипции посредством метилирования ДНК
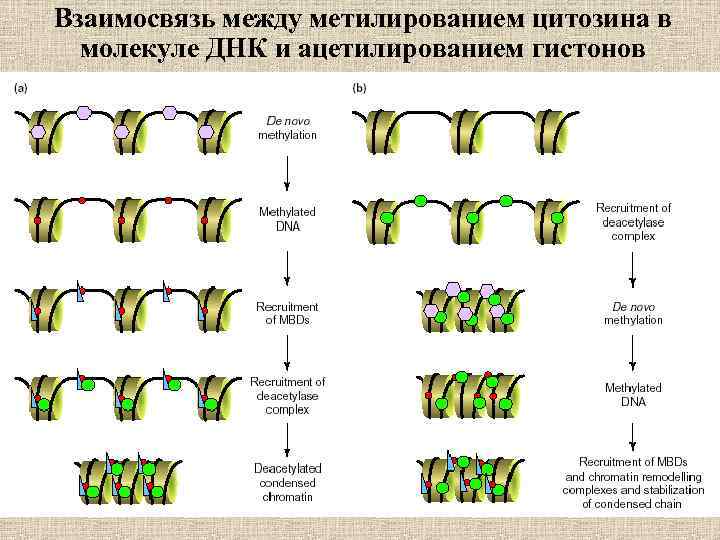 Взаимосвязь между метилированием цитозина в молекуле ДНК и ацетилированием гистонов
Взаимосвязь между метилированием цитозина в молекуле ДНК и ацетилированием гистонов
 Механизмы инактивации гена в результате метилирования промоторной области 1. Метильные группы нарушают ДНК-белковые взаимодействия, выступая в большую бороздку ДНК и препятствуя связыванию специфических транскрипционных факторов. 2. Метилированные районы ДНК специфически связывают транскрипционные репрессоры. 3. Метилирование ДНК влияет на структуру хроматина.
Механизмы инактивации гена в результате метилирования промоторной области 1. Метильные группы нарушают ДНК-белковые взаимодействия, выступая в большую бороздку ДНК и препятствуя связыванию специфических транскрипционных факторов. 2. Метилированные районы ДНК специфически связывают транскрипционные репрессоры. 3. Метилирование ДНК влияет на структуру хроматина.
 Метилирование ДНК в клетке контролирует все (!) генетические процессы, в том числе такие как : Транскрипция (клеточная дифференцировка) Репликация Рекомбинация Репарация Транспозиция генов Инактивация Х-хромосомы
Метилирование ДНК в клетке контролирует все (!) генетические процессы, в том числе такие как : Транскрипция (клеточная дифференцировка) Репликация Рекомбинация Репарация Транспозиция генов Инактивация Х-хромосомы
 Биологическая специфичность метилирования ДНК: • • • Видовая (штаммовая) Тканевая (клеточная) Органоидная (ядро, митохондрии, пластиды) Внутримолекулярная (островки метилирования, повторы) Возрастная Резкое искажение метилирования ДНК: • отсутствие метильных доноров (рак, гепатома) • суперметилирование ДНК РАК • полное выключение (knockout) ДНК-метилазного гена остановка развития, апоптоз, смерть (без метилирования ДНК жизни нет!)
Биологическая специфичность метилирования ДНК: • • • Видовая (штаммовая) Тканевая (клеточная) Органоидная (ядро, митохондрии, пластиды) Внутримолекулярная (островки метилирования, повторы) Возрастная Резкое искажение метилирования ДНК: • отсутствие метильных доноров (рак, гепатома) • суперметилирование ДНК РАК • полное выключение (knockout) ДНК-метилазного гена остановка развития, апоптоз, смерть (без метилирования ДНК жизни нет!)
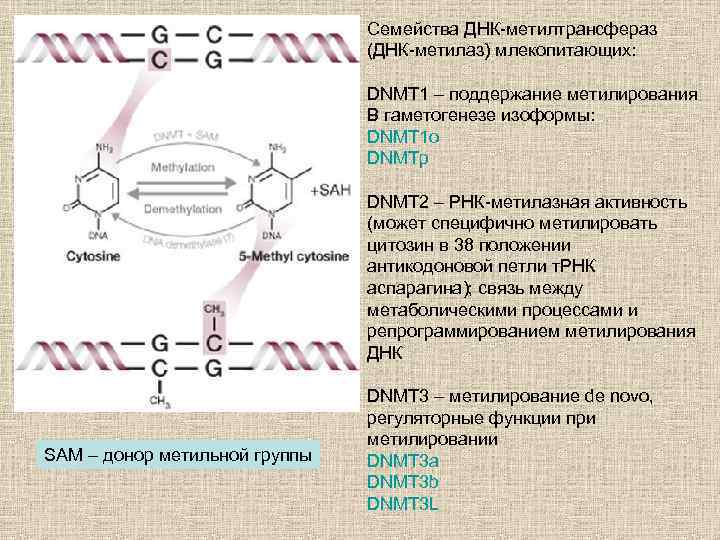 Семейства ДНК-метилтрансфераз (ДНК-метилаз) млекопитающих: DNMT 1 – поддержание метилирования В гаметогенезе изоформы: DNMT 1 o DNMTp DNMT 2 – РНК-метилазная активность (может специфично метилировать цитозин в 38 положении антикодоновой петли т. РНК аспарагина); связь между метаболическими процессами и репрограммированием метилирования ДНК SAM – донор метильной группы DNMT 3 – метилирование de novo, регуляторные функции при метилировании DNMT 3 a DNMT 3 b DNMT 3 L
Семейства ДНК-метилтрансфераз (ДНК-метилаз) млекопитающих: DNMT 1 – поддержание метилирования В гаметогенезе изоформы: DNMT 1 o DNMTp DNMT 2 – РНК-метилазная активность (может специфично метилировать цитозин в 38 положении антикодоновой петли т. РНК аспарагина); связь между метаболическими процессами и репрограммированием метилирования ДНК SAM – донор метильной группы DNMT 3 – метилирование de novo, регуляторные функции при метилировании DNMT 3 a DNMT 3 b DNMT 3 L
 De novo метилирование ДНК и сохранение характера метилирования ДНК Высокометилированые последовательности: • Сателлитная ДНК • Повторяющиеся элементы (в т. ч. транспозоны и их инертные формы) • Уникальная межгенная ДНК • Экзоны генов
De novo метилирование ДНК и сохранение характера метилирования ДНК Высокометилированые последовательности: • Сателлитная ДНК • Повторяющиеся элементы (в т. ч. транспозоны и их инертные формы) • Уникальная межгенная ДНК • Экзоны генов
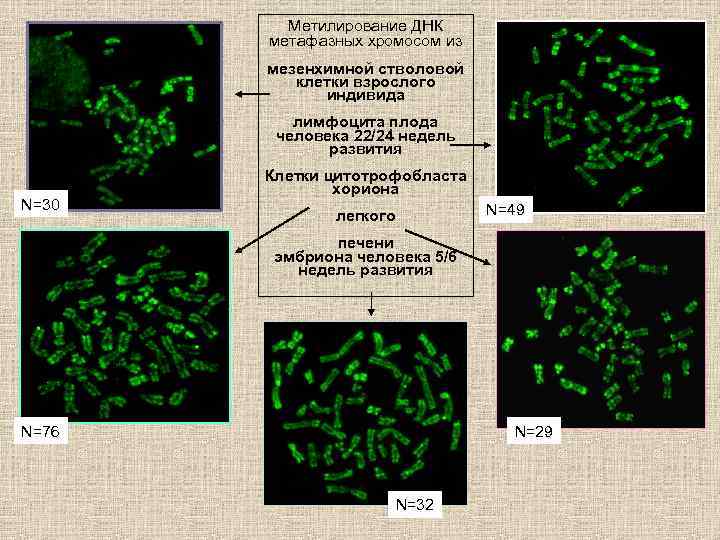 Метилирование ДНК метафазных хромосом из мезенхимной стволовой клетки взрослого индивида лимфоцита плода человека 22/24 недель развития N=30 Клетки цитотрофобласта хориона легкого N=49 печени эмбриона человека 5/6 недель развития N=76 N=29 N=32
Метилирование ДНК метафазных хромосом из мезенхимной стволовой клетки взрослого индивида лимфоцита плода человека 22/24 недель развития N=30 Клетки цитотрофобласта хориона легкого N=49 печени эмбриона человека 5/6 недель развития N=76 N=29 N=32
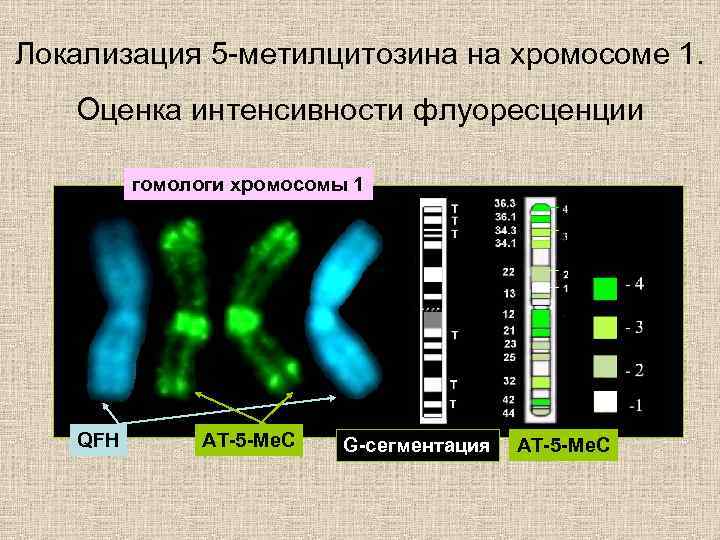 Локализация 5 -метилцитозина на хромосоме 1. Оценка интенсивности флуоресценции гомологи хромосомы 1 QFH АТ-5 -Ме. С G-сегментация АТ-5 -Ме. С
Локализация 5 -метилцитозина на хромосоме 1. Оценка интенсивности флуоресценции гомологи хромосомы 1 QFH АТ-5 -Ме. С G-сегментация АТ-5 -Ме. С
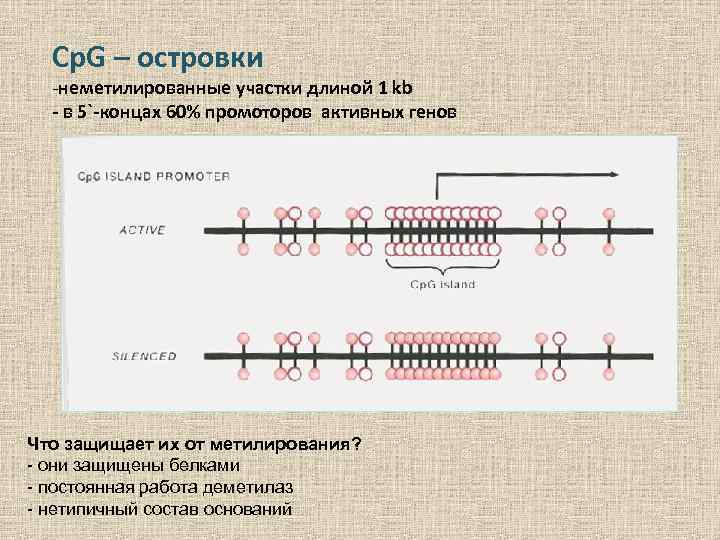 Cp. G – островки -неметилированные участки длиной 1 kb - в 5`-концах 60% промоторов активных генов Что защищает их от метилирования? - они защищены белками - постоянная работа деметилаз - нетипичный состав оснований
Cp. G – островки -неметилированные участки длиной 1 kb - в 5`-концах 60% промоторов активных генов Что защищает их от метилирования? - они защищены белками - постоянная работа деметилаз - нетипичный состав оснований
 Деметилирование – удаление метильных групп из ДНК Пассивное деметилирование – реализуется после репликации ДНК, за счет отсутствия метилазной активности. Новосинтезированная нить ДНК не метилируется по образцу старой, и образуется полуметилированная (гемиметилированная) ДНК. Активное деметилирование – задействована ферментативная система, превращающая 5 -метилцитозин в цитозин независимо от репликации Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК оставались неизвестными!
Деметилирование – удаление метильных групп из ДНК Пассивное деметилирование – реализуется после репликации ДНК, за счет отсутствия метилазной активности. Новосинтезированная нить ДНК не метилируется по образцу старой, и образуется полуметилированная (гемиметилированная) ДНК. Активное деметилирование – задействована ферментативная система, превращающая 5 -метилцитозин в цитозин независимо от репликации Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК оставались неизвестными!
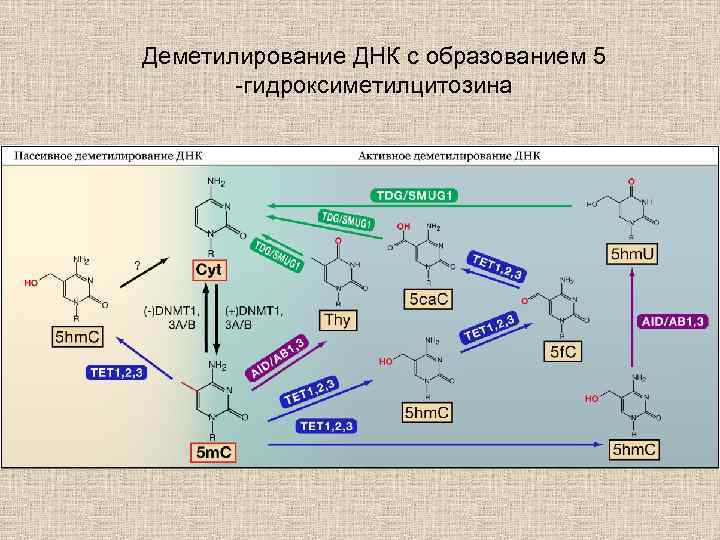 Деметилирование ДНК с образованием 5 -гидроксиметилцитозина
Деметилирование ДНК с образованием 5 -гидроксиметилцитозина
 Методы анализа метилирования 1. Метилчувствительная ПЦР (Not 1, Eag 1, Sac. II, Hpa. II, Hha. I) 2. Метилспецифическая ПЦР Трансформация цитозина в урацил бисульфитом Na 3. Methyl. Light – метилспецифическая ПЦР в реальном времени 4. Биологические микрочипы 5. Специфические антиметилцитозиновые антитела
Методы анализа метилирования 1. Метилчувствительная ПЦР (Not 1, Eag 1, Sac. II, Hpa. II, Hha. I) 2. Метилспецифическая ПЦР Трансформация цитозина в урацил бисульфитом Na 3. Methyl. Light – метилспецифическая ПЦР в реальном времени 4. Биологические микрочипы 5. Специфические антиметилцитозиновые антитела
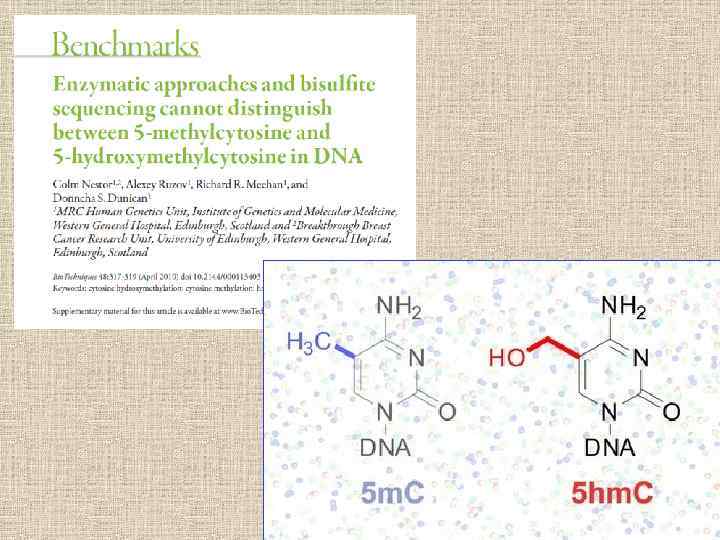
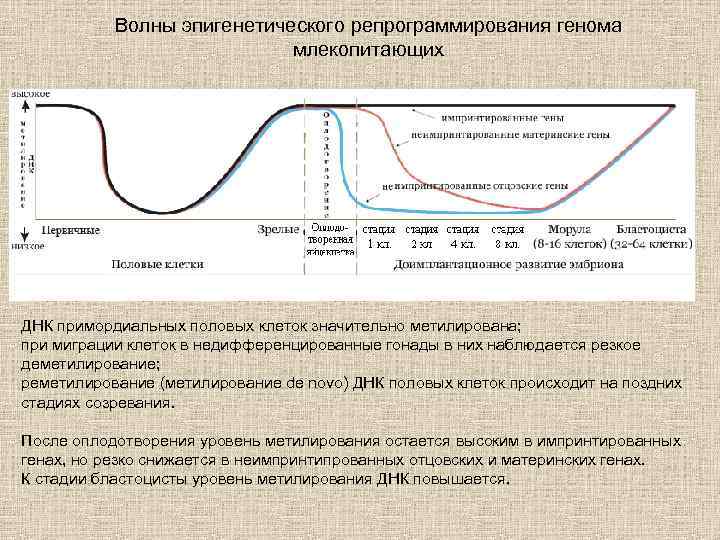 Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается.
Волны эпигенетического репрограммирования генома млекопитающих ДНК примордиальных половых клеток значительно метилирована; при миграции клеток в недифференцированные гонады в них наблюдается резкое деметилирование; реметилирование (метилирование de novo) ДНК половых клеток происходит на поздних стадиях созревания. После оплодотворения уровень метилирования остается высоким в импринтированных генах, но резко снижается в неимпринтипрованных отцовских и материнских генах. К стадии бластоцисты уровень метилирования ДНК повышается.
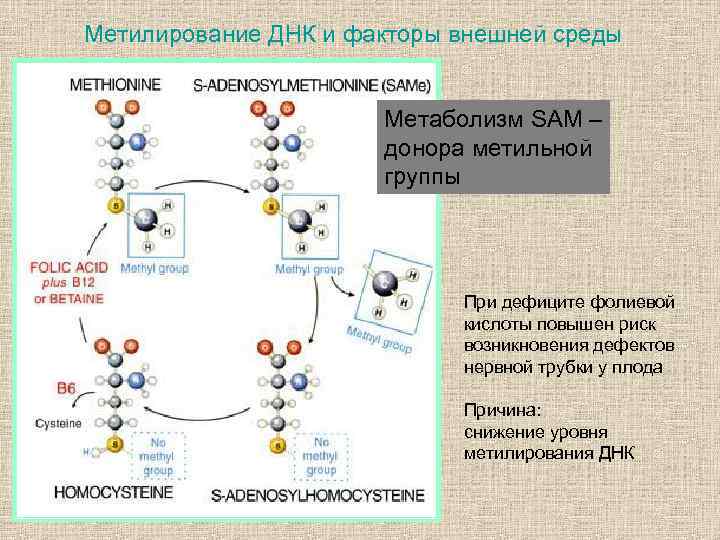 Метилирование ДНК и факторы внешней среды Метаболизм SAM – донора метильной группы При дефиците фолиевой кислоты повышен риск возникновения дефектов нервной трубки у плода Причина: снижение уровня метилирования ДНК
Метилирование ДНК и факторы внешней среды Метаболизм SAM – донора метильной группы При дефиците фолиевой кислоты повышен риск возникновения дефектов нервной трубки у плода Причина: снижение уровня метилирования ДНК
 Метилирование ДНК и факторы внешней среды Доказано влияние на метилирование ДНК металлов – никеля, кадмия, мышьяка, а также хрома, ртути, трихлорэтилена, дихлоруксусной и трихлоруксусной кислоты, бензола, бисфенола. Металлы способствуют образованию в клетке активных форм кислорода, вызывающих повреждения ДНК, которые затрудняют или делают невозможной работу ДНК метилтрансфераз. В 1992 году Баркером была выдвинута гипотеза FEBAD (fetal basis of adult disease). В пользу гипотезы свидетельствует обнаруженная взаимосвязь между воздействием на плод экзогенных и эндогенных факторов и риском последующего развития сердечно-сосудистых заболеваний, сахарного диабета второго типа, остеопороза и некоторых видов рака.
Метилирование ДНК и факторы внешней среды Доказано влияние на метилирование ДНК металлов – никеля, кадмия, мышьяка, а также хрома, ртути, трихлорэтилена, дихлоруксусной и трихлоруксусной кислоты, бензола, бисфенола. Металлы способствуют образованию в клетке активных форм кислорода, вызывающих повреждения ДНК, которые затрудняют или делают невозможной работу ДНК метилтрансфераз. В 1992 году Баркером была выдвинута гипотеза FEBAD (fetal basis of adult disease). В пользу гипотезы свидетельствует обнаруженная взаимосвязь между воздействием на плод экзогенных и эндогенных факторов и риском последующего развития сердечно-сосудистых заболеваний, сахарного диабета второго типа, остеопороза и некоторых видов рака.
 Внешние факторы, действующие на женщину в период беременности, могут изменять характер метилирования ДНК в ее клетках, модифицировать формирующиеся эпигенетические паттерны плода, а также влиять на процесс репрограммирования в формирующихся половых клетках плода!
Внешние факторы, действующие на женщину в период беременности, могут изменять характер метилирования ДНК в ее клетках, модифицировать формирующиеся эпигенетические паттерны плода, а также влиять на процесс репрограммирования в формирующихся половых клетках плода!
 Метилирование ДНК является обратимой реакцией и в значительной степени подвержено воздействию эндогенных и экзогенных факторов. Эти особенности, с одной стороны, увеличивают риск возникновения ошибок из-за влияния негативных факторов, но с другой – дают возможность проводить коррекцию эпигенетической регуляции генома за счет определенных внешних воздействий, в том числе лекарственных средств, гормонов и диеты.
Метилирование ДНК является обратимой реакцией и в значительной степени подвержено воздействию эндогенных и экзогенных факторов. Эти особенности, с одной стороны, увеличивают риск возникновения ошибок из-за влияния негативных факторов, но с другой – дают возможность проводить коррекцию эпигенетической регуляции генома за счет определенных внешних воздействий, в том числе лекарственных средств, гормонов и диеты.


