комплекс.ppt
- Количество слайдов: 75
 Увага! Папка Supplementary повинна знаходитись тут: C: Documents and Settings1Мои документыКурс лекційБудова речовини
Увага! Папка Supplementary повинна знаходитись тут: C: Documents and Settings1Мои документыКурс лекційБудова речовини
 Комплексні сполуки
Комплексні сполуки
 Дуже великий і надзвичайно важливий клас серед неорганічних сполук становлять комплексні або координаційні сполуки атоми структурні складові молекули будь-яких речовин іони Cu 2+ 2 SO 4 Cu. SO 4 → + + NH 3 → [Cu(NH 3)4]SO 4 Hg 2+ + 2 NO 3 Hg(NO 3)2 → + KJ → Hg. J 2↓ + KJ → K 2 Hg. J 4
Дуже великий і надзвичайно важливий клас серед неорганічних сполук становлять комплексні або координаційні сполуки атоми структурні складові молекули будь-яких речовин іони Cu 2+ 2 SO 4 Cu. SO 4 → + + NH 3 → [Cu(NH 3)4]SO 4 Hg 2+ + 2 NO 3 Hg(NO 3)2 → + KJ → Hg. J 2↓ + KJ → K 2 Hg. J 4
![Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Ni. SO 4 Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Ni. SO 4](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-4.jpg) Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Ni. SO 4 + NH 3 → [Ni(NH 3)6]SO 4 Cr 2(SO 4)3 + 12 Na. OH → 2 Na 3[Cr(OH)6] + 3 Na 2 SO 4 Al 2(SO 4)3 + 12 Na. OH → 2 Na 3[Al(OH)6] + 3 Na 2 SO 4
Cu. SO 4 + 4 NH 3 → [Cu(NH 3)4]SO 4 Ni. SO 4 + NH 3 → [Ni(NH 3)6]SO 4 Cr 2(SO 4)3 + 12 Na. OH → 2 Na 3[Cr(OH)6] + 3 Na 2 SO 4 Al 2(SO 4)3 + 12 Na. OH → 2 Na 3[Al(OH)6] + 3 Na 2 SO 4
![Cu. SO 4 + 4 Na. Clкрист. → Na 2[Cu. Сl 4]SO 4 + Cu. SO 4 + 4 Na. Clкрист. → Na 2[Cu. Сl 4]SO 4 +](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-5.jpg) Cu. SO 4 + 4 Na. Clкрист. → Na 2[Cu. Сl 4]SO 4 + Na 2 SO 4 Fe. Cl 3 + 6 KCNS → K 3[Fe(CNS)6] +3 KCl Hg(NO 3)2 + 4 KJ → K 2[Hg. J 4] + 2 KNO 3
Cu. SO 4 + 4 Na. Clкрист. → Na 2[Cu. Сl 4]SO 4 + Na 2 SO 4 Fe. Cl 3 + 6 KCNS → K 3[Fe(CNS)6] +3 KCl Hg(NO 3)2 + 4 KJ → K 2[Hg. J 4] + 2 KNO 3
 Точного визначення, що таке комплексна сполука не існує. SO 42 Hg. J 42+1 +6 -2 H 2 SO 4 +1 +2 -1 K 2 Hg. J 4 H+ + S 6+ + O 2 - H 2 SO 4 2 K+ + Hg 2+ + 4 J- → K 2[Hg. J 4]
Точного визначення, що таке комплексна сполука не існує. SO 42 Hg. J 42+1 +6 -2 H 2 SO 4 +1 +2 -1 K 2 Hg. J 4 H+ + S 6+ + O 2 - H 2 SO 4 2 K+ + Hg 2+ + 4 J- → K 2[Hg. J 4]
 Комплексні сполуки – це сполуки які виникають внаслідок насичення валентних можливостей атомів, або іонів K[Cu. Cl 2] Na 3[Al. F 6] Ni(CO)4 [Cu(NH 3)4]SO 4 K 3[Fe(CN)6] K 2[Si. F 6] K[BF 4]
Комплексні сполуки – це сполуки які виникають внаслідок насичення валентних можливостей атомів, або іонів K[Cu. Cl 2] Na 3[Al. F 6] Ni(CO)4 [Cu(NH 3)4]SO 4 K 3[Fe(CN)6] K 2[Si. F 6] K[BF 4]
 Теорія комплексоутворення 1893 р. – швейцарський вчений Альфред Вернер (1866) запропонував координаційну теорію (теорію утворення комплексних сполук) 1913 р. – Нобелівська премія
Теорія комплексоутворення 1893 р. – швейцарський вчений Альфред Вернер (1866) запропонував координаційну теорію (теорію утворення комплексних сполук) 1913 р. – Нобелівська премія
 Будова комплексних сполук Комплексоутворювач – атом або іон, до якого приєднуються нейтральні молекули або аніони. Комплексоутворювачі повинні відігравати роль акцепторів електронів і мати вільні орбіталі. Комплексоутворювачами можуть бути атоми металів (Co, Fe), іони металів (Cu 2+, Fe 3+, Al 3+), рідше - іони неметалів (бору, силіцію).
Будова комплексних сполук Комплексоутворювач – атом або іон, до якого приєднуються нейтральні молекули або аніони. Комплексоутворювачі повинні відігравати роль акцепторів електронів і мати вільні орбіталі. Комплексоутворювачами можуть бути атоми металів (Co, Fe), іони металів (Cu 2+, Fe 3+, Al 3+), рідше - іони неметалів (бору, силіцію).
 Ліганди (приєднані) – це молекули або іони, які координуються навколо комплексоутворювача. Ліганди повинні бути донорами електронів. Лігандами можуть бути нейтральні молекули ( Н 2 О, NH 3, аміни, спирти, R – NH 2, R – OH, кислоти, ефіри і т. ін. ), або аніони (F-, Cl-, CNS-, C 2 O 42 -, тощо)
Ліганди (приєднані) – це молекули або іони, які координуються навколо комплексоутворювача. Ліганди повинні бути донорами електронів. Лігандами можуть бути нейтральні молекули ( Н 2 О, NH 3, аміни, спирти, R – NH 2, R – OH, кислоти, ефіри і т. ін. ), або аніони (F-, Cl-, CNS-, C 2 O 42 -, тощо)
 Комплексоутворювач разом з лігандами утворює внутрішню координаційну сферу. Ліганди приєднуються до комплексоутворювача у відповідності до його координаційного числа. Координаційне число - кількість місць у просторі (орбіталей), які надає комплексоутворювач для приєднання лігандів. Координаційне число залежить від природи комплексоутворювача і розмірів лігандів.
Комплексоутворювач разом з лігандами утворює внутрішню координаційну сферу. Ліганди приєднуються до комплексоутворювача у відповідності до його координаційного числа. Координаційне число - кількість місць у просторі (орбіталей), які надає комплексоутворювач для приєднання лігандів. Координаційне число залежить від природи комплексоутворювача і розмірів лігандів.
![[Al. F 6]3 - к. ч. = 6 [Al. Cl 4]- к. ч. = [Al. F 6]3 - к. ч. = 6 [Al. Cl 4]- к. ч. =](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-12.jpg) [Al. F 6]3 - к. ч. = 6 [Al. Cl 4]- к. ч. = 4 95% комплексних сполук мають координаційне число 4 або 6 У переважній більшості випадків к. ч. = валентності комплексоутворювача * 2
[Al. F 6]3 - к. ч. = 6 [Al. Cl 4]- к. ч. = 4 95% комплексних сполук мають координаційне число 4 або 6 У переважній більшості випадків к. ч. = валентності комплексоутворювача * 2
![K[Cu. Cl 2] Валентність Координаційне число l 2 [Ag(NH 3)2]Cl 2 K 2[Hg. J K[Cu. Cl 2] Валентність Координаційне число l 2 [Ag(NH 3)2]Cl 2 K 2[Hg. J](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-13.jpg) K[Cu. Cl 2] Валентність Координаційне число l 2 [Ag(NH 3)2]Cl 2 K 2[Hg. J 4] ll 4 [Cu(NH 3)4]SO 4 ll 4 K 3[Co. F 6] lll 6 K 3[Fe(CN)6] lll 6 [Cr(NH 3)6]Cl 3 lll 6
K[Cu. Cl 2] Валентність Координаційне число l 2 [Ag(NH 3)2]Cl 2 K 2[Hg. J 4] ll 4 [Cu(NH 3)4]SO 4 ll 4 K 3[Co. F 6] lll 6 K 3[Fe(CN)6] lll 6 [Cr(NH 3)6]Cl 3 lll 6
![Але Валентність +2 K 4[Fe(CN)6] +2 [Co(NH 3)6]Cl 2 +4 H 2[Pt. Cl 6] Але Валентність +2 K 4[Fe(CN)6] +2 [Co(NH 3)6]Cl 2 +4 H 2[Pt. Cl 6]](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-14.jpg) Але Валентність +2 K 4[Fe(CN)6] +2 [Co(NH 3)6]Cl 2 +4 H 2[Pt. Cl 6] к. ч. ll 6 l. V 6
Але Валентність +2 K 4[Fe(CN)6] +2 [Co(NH 3)6]Cl 2 +4 H 2[Pt. Cl 6] к. ч. ll 6 l. V 6
 Дентатність лігандів визначається кількістю місць, які може займати ліганд (кількість “зубів”) Дентатність = 1 NH 3 R – NH 2 [Co(NH 3)6]Cl 3 Дентатність = 2 CH 2 – CH 2 NH 2 етилендиамін [Co(NH 2 CH 2 NH 2)3]Cl 3
Дентатність лігандів визначається кількістю місць, які може займати ліганд (кількість “зубів”) Дентатність = 1 NH 3 R – NH 2 [Co(NH 3)6]Cl 3 Дентатність = 2 CH 2 – CH 2 NH 2 етилендиамін [Co(NH 2 CH 2 NH 2)3]Cl 3
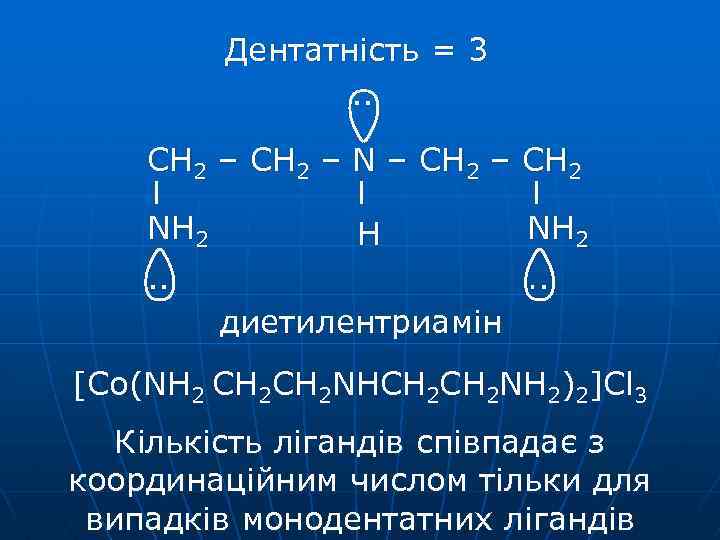 Дентатність = 3 CH 2 – N – CH 2 NH 2 H NH 2 диетилентриамін [Co(NH 2 CH 2 CH 2 NH 2)2]Cl 3 Кількість лігандів співпадає з координаційним числом тільки для випадків монодентатних лігандів
Дентатність = 3 CH 2 – N – CH 2 NH 2 H NH 2 диетилентриамін [Co(NH 2 CH 2 CH 2 NH 2)2]Cl 3 Кількість лігандів співпадає з координаційним числом тільки для випадків монодентатних лігандів
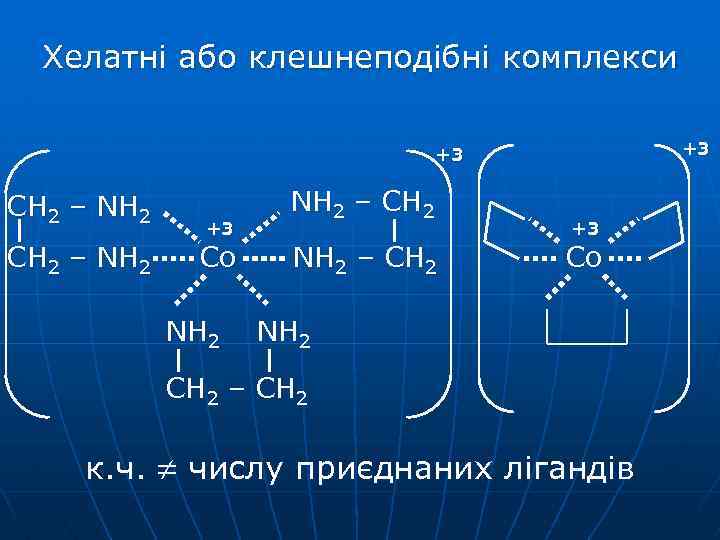 Хелатні або клешнеподібні комплекси +3 +3 CH 2 – NH 2 +3 Co NH 2 – CH 2 +3 Co NH 2 CH 2 – CH 2 к. ч. числу приєднаних лігандів
Хелатні або клешнеподібні комплекси +3 +3 CH 2 – NH 2 +3 Co NH 2 – CH 2 +3 Co NH 2 CH 2 – CH 2 к. ч. числу приєднаних лігандів
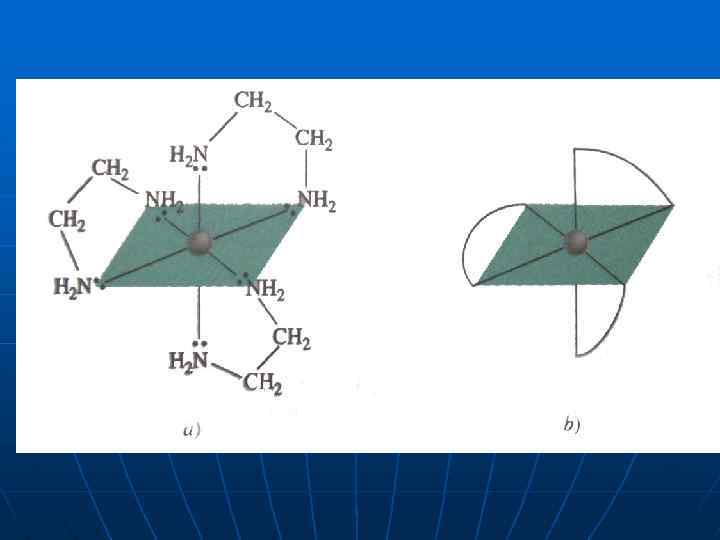
 Деякі ліганди можуть координуватися різними способами і називаються амбідентатними, наприклад NCSУ багатодентатних лігандів водночас можуть бути присутніми і нейтральні і аніоні координаційні групи H H N – CH 2 – C O - O
Деякі ліганди можуть координуватися різними способами і називаються амбідентатними, наприклад NCSУ багатодентатних лігандів водночас можуть бути присутніми і нейтральні і аніоні координаційні групи H H N – CH 2 – C O - O
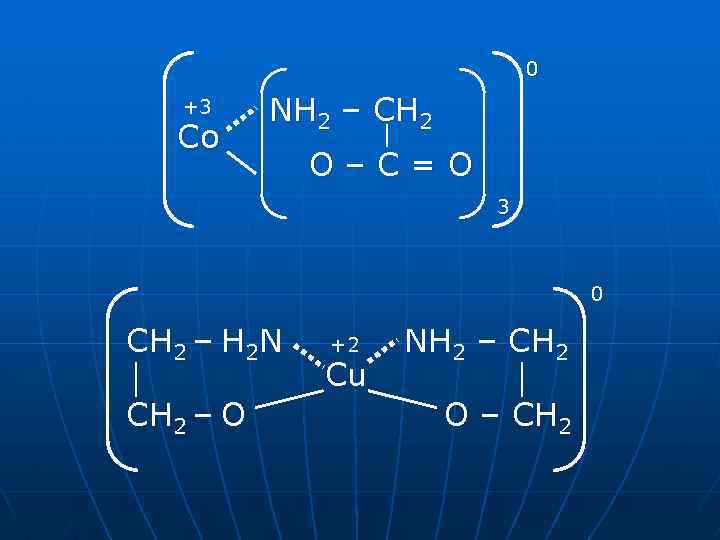 0 +3 Co NH 2 – CH 2 O–C=O 3 0 CH 2 – H 2 N CH 2 – O +2 Cu NH 2 – CH 2 O – CH 2
0 +3 Co NH 2 – CH 2 O–C=O 3 0 CH 2 – H 2 N CH 2 – O +2 Cu NH 2 – CH 2 O – CH 2
![Систематизація комплексних сполук 1) за типом лігандів [Al. F 6]3 -, [Fe(CN)6]3 - - Систематизація комплексних сполук 1) за типом лігандів [Al. F 6]3 -, [Fe(CN)6]3 - -](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-21.jpg) Систематизація комплексних сполук 1) за типом лігандів [Al. F 6]3 -, [Fe(CN)6]3 - - ацидокомплекси [Co(H 2 O)6]2+ - аквакомплекси [Zn(OH)4]2 -, [Cr(OH)6]3 - гідроксокомплекси [Cu(NH 3)4]2+ - амінокомплекси [Cr(H O) Cl ]+ - різнолігандні комплекси
Систематизація комплексних сполук 1) за типом лігандів [Al. F 6]3 -, [Fe(CN)6]3 - - ацидокомплекси [Co(H 2 O)6]2+ - аквакомплекси [Zn(OH)4]2 -, [Cr(OH)6]3 - гідроксокомплекси [Cu(NH 3)4]2+ - амінокомплекси [Cr(H O) Cl ]+ - різнолігандні комплекси
 2) за типом комплексоутворювача Комплексні сполуки Cu(ll), Cu(l), . . . Номенклатура комплексних сполук Аніон називають у називному відмінку, катіон - у родовому відмінку K[Cu. Cl 2] – дихлорокупрат(l) калію K 2[Hg. J 4] - тетрайодомеркурат(ll) калію K 3[Fe(CN)6] – гексаціаноферрат(lll) калію
2) за типом комплексоутворювача Комплексні сполуки Cu(ll), Cu(l), . . . Номенклатура комплексних сполук Аніон називають у називному відмінку, катіон - у родовому відмінку K[Cu. Cl 2] – дихлорокупрат(l) калію K 2[Hg. J 4] - тетрайодомеркурат(ll) калію K 3[Fe(CN)6] – гексаціаноферрат(lll) калію
![[Ag(NH 3)2]Cl – хлорид диаміносрібла [Cu(NH 3)4]SO 4 – сульфат тетраамінокупруму(ll) [Cr(H 2 O)6]Cl [Ag(NH 3)2]Cl – хлорид диаміносрібла [Cu(NH 3)4]SO 4 – сульфат тетраамінокупруму(ll) [Cr(H 2 O)6]Cl](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-23.jpg) [Ag(NH 3)2]Cl – хлорид диаміносрібла [Cu(NH 3)4]SO 4 – сульфат тетраамінокупруму(ll) [Cr(H 2 O)6]Cl 3 - хлорид гексааквахрому(lll) K 3[Cr(OH)6] - гексагідроксохромат(lll) калію [Co(NH 3)4(H 2 O)Cl]Cl 2 – хлорид хлороакватетраамінокобальту(lll)
[Ag(NH 3)2]Cl – хлорид диаміносрібла [Cu(NH 3)4]SO 4 – сульфат тетраамінокупруму(ll) [Cr(H 2 O)6]Cl 3 - хлорид гексааквахрому(lll) K 3[Cr(OH)6] - гексагідроксохромат(lll) калію [Co(NH 3)4(H 2 O)Cl]Cl 2 – хлорид хлороакватетраамінокобальту(lll)
 Просторова будова комплексних сполук Якщо координаційне число = 2, то частинки внутрішньої координаційної сфери розміщені лінійно K[Cl – Cu – Cl]
Просторова будова комплексних сполук Якщо координаційне число = 2, то частинки внутрішньої координаційної сфери розміщені лінійно K[Cl – Cu – Cl]
![Якщо к. ч. = 4 [Hg. J 4]2 - [Pt(NH 3)4]2+ J- H 3 Якщо к. ч. = 4 [Hg. J 4]2 - [Pt(NH 3)4]2+ J- H 3](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-25.jpg) Якщо к. ч. = 4 [Hg. J 4]2 - [Pt(NH 3)4]2+ J- H 3 N Pt Hg 2+ J- +2 NH 3 J- J- тетраедричний H 3 N NH 3 квадратноплощинний
Якщо к. ч. = 4 [Hg. J 4]2 - [Pt(NH 3)4]2+ J- H 3 N Pt Hg 2+ J- +2 NH 3 J- J- тетраедричний H 3 N NH 3 квадратноплощинний
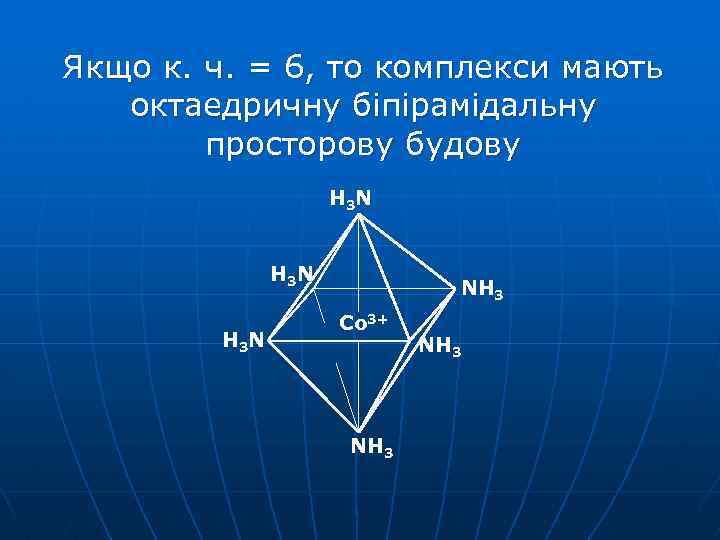 Якщо к. ч. = 6, то комплекси мають октаедричну біпірамідальну просторову будову H 3 N NH 3 Со 3+ NH 3
Якщо к. ч. = 6, то комплекси мають октаедричну біпірамідальну просторову будову H 3 N NH 3 Со 3+ NH 3
![Ізомерія комплексних сполук гідратна ізомерія [Cr(H 2 O)6]Cl 3 ⇆ [Cr(H 2 O)5 Cl]Cl Ізомерія комплексних сполук гідратна ізомерія [Cr(H 2 O)6]Cl 3 ⇆ [Cr(H 2 O)5 Cl]Cl](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-27.jpg) Ізомерія комплексних сполук гідратна ізомерія [Cr(H 2 O)6]Cl 3 ⇆ [Cr(H 2 O)5 Cl]Cl 2 H 2 O ⇆ Фіолетовий Зелений ⇆ [Cr(H 2 O)4 Cl 2]Cl· 2 H 2 O Темнозелений
Ізомерія комплексних сполук гідратна ізомерія [Cr(H 2 O)6]Cl 3 ⇆ [Cr(H 2 O)5 Cl]Cl 2 H 2 O ⇆ Фіолетовий Зелений ⇆ [Cr(H 2 O)4 Cl 2]Cl· 2 H 2 O Темнозелений
![Іонізаційна ізомерія +3 +3 [Co(NH 3)5 Br]SO 4 [Co(NH 3)5 SO 4]Br Координаційна ізомерія Іонізаційна ізомерія +3 +3 [Co(NH 3)5 Br]SO 4 [Co(NH 3)5 SO 4]Br Координаційна ізомерія](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-28.jpg) Іонізаційна ізомерія +3 +3 [Co(NH 3)5 Br]SO 4 [Co(NH 3)5 SO 4]Br Координаційна ізомерія 3+ 3 - [Co(NH 3)6] [Cr(CN)6] катіон аніон 3 - 3+ [Co(CN)6] [Cr(NH 3)6] катіон аніон
Іонізаційна ізомерія +3 +3 [Co(NH 3)5 Br]SO 4 [Co(NH 3)5 SO 4]Br Координаційна ізомерія 3+ 3 - [Co(NH 3)6] [Cr(CN)6] катіон аніон 3 - 3+ [Co(CN)6] [Cr(NH 3)6] катіон аніон
 Стереоізомерія (просторова ізомерія) Стереоізомерія – вид ізомерії сполук, які відрізняються між собою лише просторовим розташуванням атомів
Стереоізомерія (просторова ізомерія) Стереоізомерія – вид ізомерії сполук, які відрізняються між собою лише просторовим розташуванням атомів
![Геометрична (цис-транс-) ізомерія [Pt(NH 3)2 Cl 2] Cl- Pt Clцис- NH 3 +2 Cl. Геометрична (цис-транс-) ізомерія [Pt(NH 3)2 Cl 2] Cl- Pt Clцис- NH 3 +2 Cl.](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-31.jpg) Геометрична (цис-транс-) ізомерія [Pt(NH 3)2 Cl 2] Cl- Pt Clцис- NH 3 +2 Cl. NH 3 +2 Pt транс- NH 3 Cl-
Геометрична (цис-транс-) ізомерія [Pt(NH 3)2 Cl 2] Cl- Pt Clцис- NH 3 +2 Cl. NH 3 +2 Pt транс- NH 3 Cl-
![[Co(NH 3)4 Cl 2] Cl Cl Cl цис- Cl транс- [Co(NH 3)4 Cl 2] Cl Cl Cl цис- Cl транс-](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-32.jpg) [Co(NH 3)4 Cl 2] Cl Cl Cl цис- Cl транс-
[Co(NH 3)4 Cl 2] Cl Cl Cl цис- Cl транс-
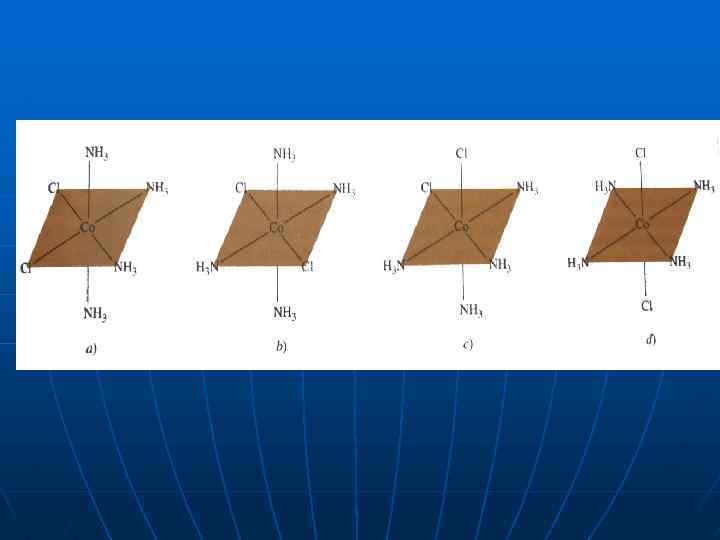
 Дзеркальна (оптична) ізомерія Дзеркальна ізомерія – вид ізомерії сполук, дзеркальні відображення яких не співпадають
Дзеркальна (оптична) ізомерія Дзеркальна ізомерія – вид ізомерії сполук, дзеркальні відображення яких не співпадають
![[Pt(NH 3)2 Br. Cl] NH 3 Pt Br Br Cl Cl Pt NH 3 [Pt(NH 3)2 Br. Cl] NH 3 Pt Br Br Cl Cl Pt NH 3](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-35.jpg) [Pt(NH 3)2 Br. Cl] NH 3 Pt Br Br Cl Cl Pt NH 3
[Pt(NH 3)2 Br. Cl] NH 3 Pt Br Br Cl Cl Pt NH 3
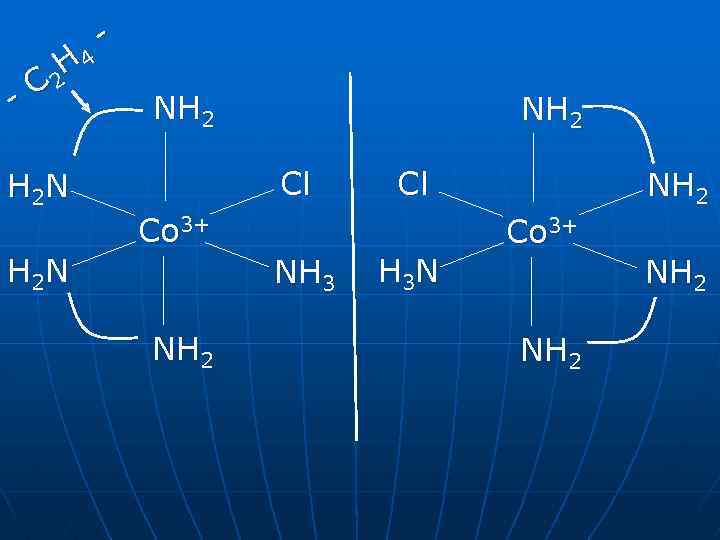 -C H 4 2 H 2 N - NH 2 Cl Cl Co 3+ NH 3 NH 2 H 3 N NH 2 Co 3+ NH 2
-C H 4 2 H 2 N - NH 2 Cl Cl Co 3+ NH 3 NH 2 H 3 N NH 2 Co 3+ NH 2
![Дзеркальні ізомери комплексного катіону [Cr(en)3]3+ Дзеркальні ізомери комплексного катіону [Cr(en)3]3+](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-37.jpg) Дзеркальні ізомери комплексного катіону [Cr(en)3]3+
Дзеркальні ізомери комплексного катіону [Cr(en)3]3+
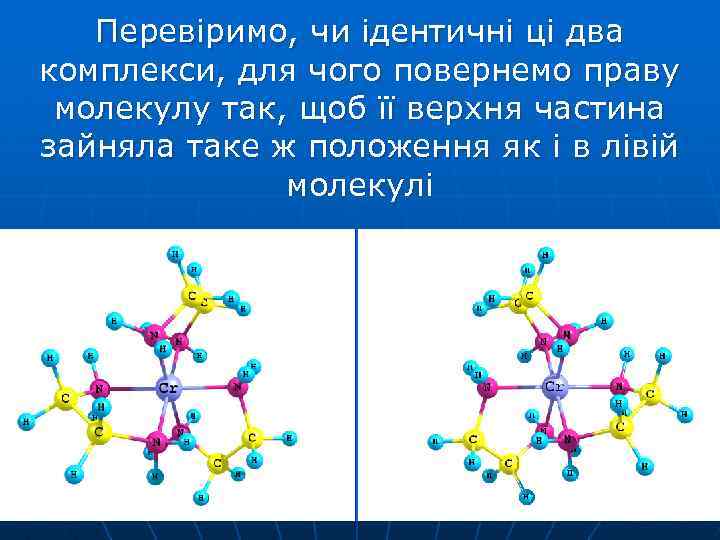 Перевіримо, чи ідентичні ці два комплекси, для чого повернемо праву молекулу так, щоб її верхня частина зайняла таке ж положення як і в лівій молекулі
Перевіримо, чи ідентичні ці два комплекси, для чого повернемо праву молекулу так, щоб її верхня частина зайняла таке ж положення як і в лівій молекулі

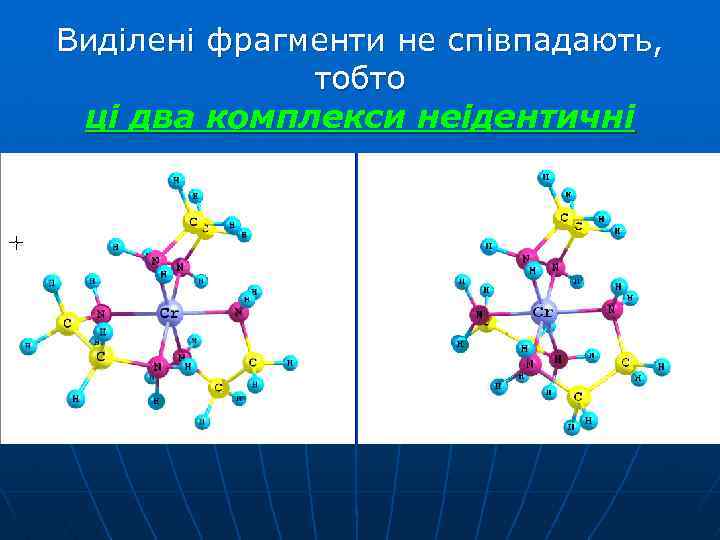 Виділені фрагменти не співпадають, тобто ці два комплекси неідентичні
Виділені фрагменти не співпадають, тобто ці два комплекси неідентичні
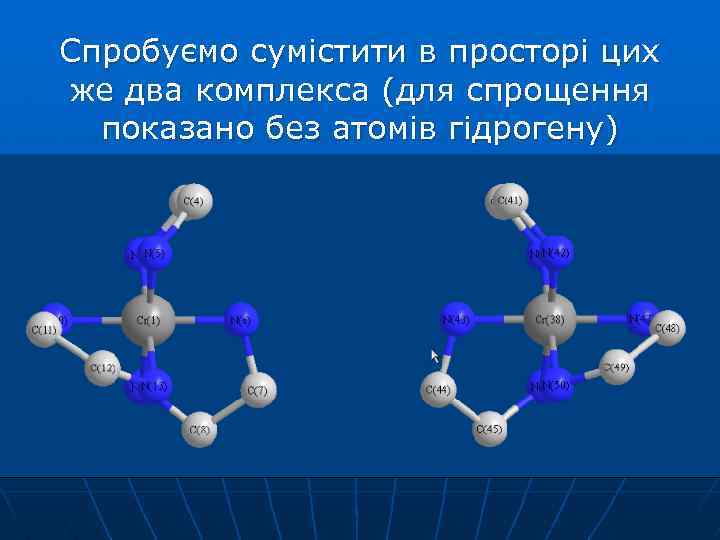 Спробуємо сумістити в просторі цих же два комплекса (для спрощення показано без атомів гідрогену)
Спробуємо сумістити в просторі цих же два комплекса (для спрощення показано без атомів гідрогену)
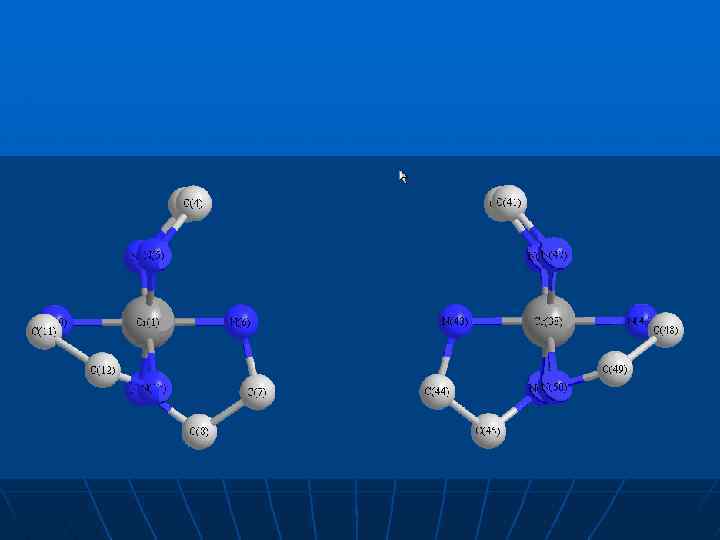
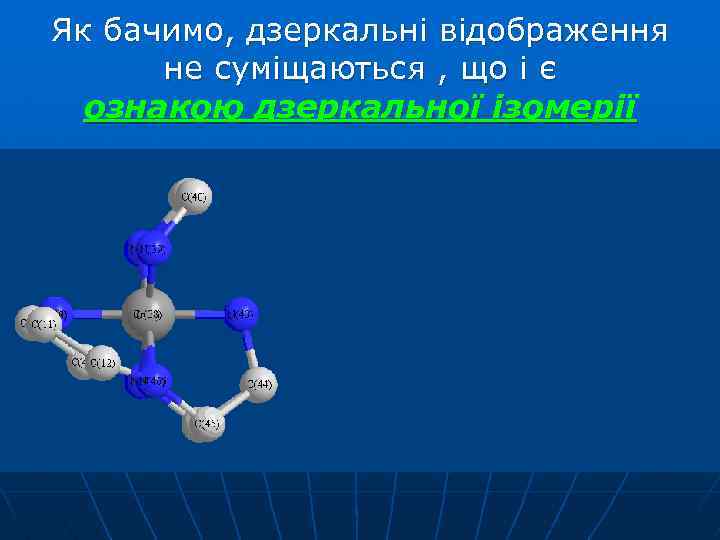 Як бачимо, дзеркальні відображення не суміщаються , що і є ознакою дзеркальної ізомерії
Як бачимо, дзеркальні відображення не суміщаються , що і є ознакою дзеркальної ізомерії
![+3 [Co(NH 3)6]Cl 3 – діамагнітний +3 +3 K 3[Co. F 6], [Cr(NH 3)6]Cl +3 [Co(NH 3)6]Cl 3 – діамагнітний +3 +3 K 3[Co. F 6], [Cr(NH 3)6]Cl](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-44.jpg) +3 [Co(NH 3)6]Cl 3 – діамагнітний +3 +3 K 3[Co. F 6], [Cr(NH 3)6]Cl 3 – парамагнітні K 3[Al(OH)6], [Zn(NH 3)4]Cl 2, [Cu(NH 3)2]J – безбарвні [Cu(NH 3)4]SO 4, K 3[Fe(CNS)6] - забарвлені Властивості комплексних сполук можна пояснити, вивчаючи хімічний зв'язок в комплексних сполуках
+3 [Co(NH 3)6]Cl 3 – діамагнітний +3 +3 K 3[Co. F 6], [Cr(NH 3)6]Cl 3 – парамагнітні K 3[Al(OH)6], [Zn(NH 3)4]Cl 2, [Cu(NH 3)2]J – безбарвні [Cu(NH 3)4]SO 4, K 3[Fe(CNS)6] - забарвлені Властивості комплексних сполук можна пояснити, вивчаючи хімічний зв'язок в комплексних сполуках
 Метод валентних зв'язків За методом валентних зв'язків хімічний зв'язок в комплексних сполуках розглядається як такий, що утворюється за донорно-акцепторним механізмом. Комплексоутворювач – акцептор електронів, орбіталі комплексоутворювача – гібридні 1. к. ч. = 2 sp – гібридизація 2. к. ч. = 4 sp 3 (тетраедр), sp 2 d (квадратноплощинний) 3. к. ч. = 6 sp 3 d 2 або d 2 sp 3
Метод валентних зв'язків За методом валентних зв'язків хімічний зв'язок в комплексних сполуках розглядається як такий, що утворюється за донорно-акцепторним механізмом. Комплексоутворювач – акцептор електронів, орбіталі комплексоутворювача – гібридні 1. к. ч. = 2 sp – гібридизація 2. к. ч. = 4 sp 3 (тетраедр), sp 2 d (квадратноплощинний) 3. к. ч. = 6 sp 3 d 2 або d 2 sp 3
 Ліганди – донори електронів Здатність лігандів утворювати міцніший або слабший зв'язок залежить від сили поля лігандів. Найбільшу силу поля мають ліганди , у складі яких є невеликі за розмірами атоми з порівняно невеликою електронегативністю
Ліганди – донори електронів Здатність лігандів утворювати міцніший або слабший зв'язок залежить від сили поля лігандів. Найбільшу силу поля мають ліганди , у складі яких є невеликі за розмірами атоми з порівняно невеликою електронегативністю
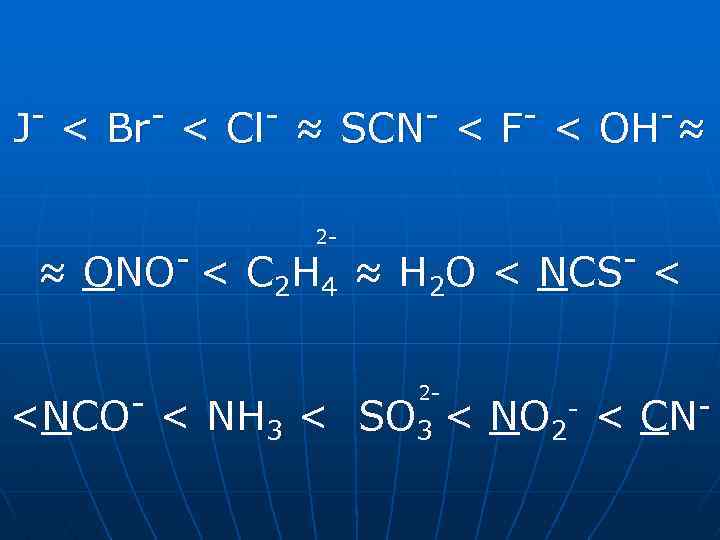 J < ≈ Br < Cl -< ONO
J < ≈ Br < Cl -< ONO
![Розглянемо за МВЗ хімічний зв’язок в комплексах [Co(NH 3)6]3+ та [Co. F 6]3 - Розглянемо за МВЗ хімічний зв’язок в комплексах [Co(NH 3)6]3+ та [Co. F 6]3 -](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-48.jpg) Розглянемо за МВЗ хімічний зв’язок в комплексах [Co(NH 3)6]3+ та [Co. F 6]3 - Co 3 d 74 s 2 Co 3+ 3 d 64 s 0 Co 3+ 3 d 4 s 4 p
Розглянемо за МВЗ хімічний зв’язок в комплексах [Co(NH 3)6]3+ та [Co. F 6]3 - Co 3 d 74 s 2 Co 3+ 3 d 64 s 0 Co 3+ 3 d 4 s 4 p
![[Co(NH 3)6]3+ Так як NH 3 є лігандом сильного поля, то під впливом сильного [Co(NH 3)6]3+ Так як NH 3 є лігандом сильного поля, то під впливом сильного](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-49.jpg) [Co(NH 3)6]3+ Так як NH 3 є лігандом сильного поля, то під впливом сильного поля ліганду в комплексі відбувається спарювання електронів на d-підрівні комплексоутворювача 3 d 4 s 4 p d 2 sp 3 – гібридизація (внутрішня) 6 NH 3 Комплекс [Сo(NH 3)6]3+ - діамагнітний
[Co(NH 3)6]3+ Так як NH 3 є лігандом сильного поля, то під впливом сильного поля ліганду в комплексі відбувається спарювання електронів на d-підрівні комплексоутворювача 3 d 4 s 4 p d 2 sp 3 – гібридизація (внутрішня) 6 NH 3 Комплекс [Сo(NH 3)6]3+ - діамагнітний
![[Co. F 6]3 F- - ліганд слабкого поля, тому електрони в комплексі на d-підрівні [Co. F 6]3 F- - ліганд слабкого поля, тому електрони в комплексі на d-підрівні](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-50.jpg) [Co. F 6]3 F- - ліганд слабкого поля, тому електрони в комплексі на d-підрівні розміщуються так, як і в іоні Co 3+ 6 F- sp 3 d 2 – гібридизація (зовнішня) [Co. F 6]3 - - парамагнітний, тому що є неспарені електрони
[Co. F 6]3 F- - ліганд слабкого поля, тому електрони в комплексі на d-підрівні розміщуються так, як і в іоні Co 3+ 6 F- sp 3 d 2 – гібридизація (зовнішня) [Co. F 6]3 - - парамагнітний, тому що є неспарені електрони
 Кількісно магнітні властивості характаризують магнітним моментом = √n(n+2) n – число неспарених електронів [Co(NH 3)6]3+ = √ 0(0+2) = 0 м. Б. [Co. F 6]3 - = √ 4(4 -2) = √ 24 = 4, 9 м. Б.
Кількісно магнітні властивості характаризують магнітним моментом = √n(n+2) n – число неспарених електронів [Co(NH 3)6]3+ = √ 0(0+2) = 0 м. Б. [Co. F 6]3 - = √ 4(4 -2) = √ 24 = 4, 9 м. Б.
![[Cr(NH 3)6]Cl 3 Cr 3 d 54 s 1 Cr 3+ 3 d 34 [Cr(NH 3)6]Cl 3 Cr 3 d 54 s 1 Cr 3+ 3 d 34](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-52.jpg) [Cr(NH 3)6]Cl 3 Cr 3 d 54 s 1 Cr 3+ 3 d 34 s 0 3 d 4 s 4 p 4 d d 2 sp 3 6 NH 3 комплекс парамагнітний = √ 3(3+2)= √ 15 = 3, 87 м. Б. Для хрому всі комплекси парамагнітні
[Cr(NH 3)6]Cl 3 Cr 3 d 54 s 1 Cr 3+ 3 d 34 s 0 3 d 4 s 4 p 4 d d 2 sp 3 6 NH 3 комплекс парамагнітний = √ 3(3+2)= √ 15 = 3, 87 м. Б. Для хрому всі комплекси парамагнітні
![+3 K 3[Fe(CN)6] +2 K 4[Fe(CN)6] Fe 3 d 64 s 2 Fe+2 3 +3 K 3[Fe(CN)6] +2 K 4[Fe(CN)6] Fe 3 d 64 s 2 Fe+2 3](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-53.jpg) +3 K 3[Fe(CN)6] +2 K 4[Fe(CN)6] Fe 3 d 64 s 2 Fe+2 3 d 64 s 0 3 d 4 s 4 p 6 CN- 4 d d 2 sp 3 гібридизація комплекс діамагнітний
+3 K 3[Fe(CN)6] +2 K 4[Fe(CN)6] Fe 3 d 64 s 2 Fe+2 3 d 64 s 0 3 d 4 s 4 p 6 CN- 4 d d 2 sp 3 гібридизація комплекс діамагнітний
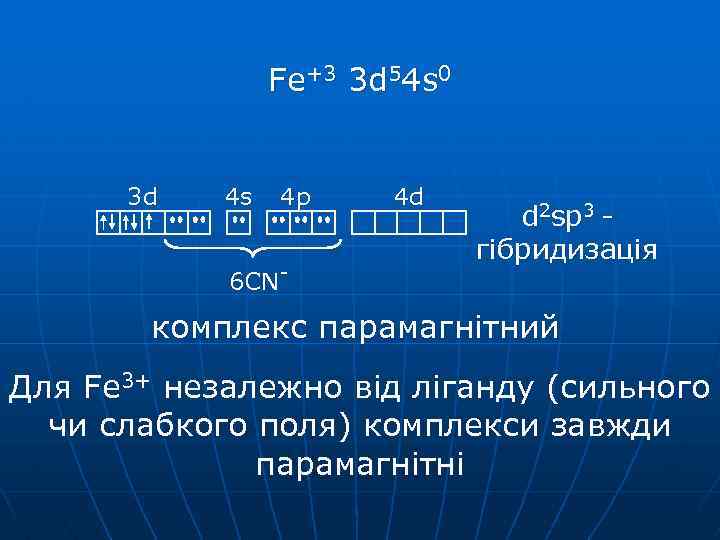 Fe+3 3 d 54 s 0 3 d 4 s 4 p 6 CN- 4 d d 2 sp 3 гібридизація комплекс парамагнітний Для Fe 3+ незалежно від ліганду (сильного чи слабкого поля) комплекси завжди парамагнітні
Fe+3 3 d 54 s 0 3 d 4 s 4 p 6 CN- 4 d d 2 sp 3 гібридизація комплекс парамагнітний Для Fe 3+ незалежно від ліганду (сильного чи слабкого поля) комплекси завжди парамагнітні
![[Zn(NH 3)4]2+ Zn 3 d 104 s 2 Zn 2+ 3 d 10 3 [Zn(NH 3)4]2+ Zn 3 d 104 s 2 Zn 2+ 3 d 10 3](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-55.jpg) [Zn(NH 3)4]2+ Zn 3 d 104 s 2 Zn 2+ 3 d 10 3 d 4 s 4 p 4 NH 3 4 d sp 3 гібридизація комплекс діамагнітний
[Zn(NH 3)4]2+ Zn 3 d 104 s 2 Zn 2+ 3 d 10 3 d 4 s 4 p 4 NH 3 4 d sp 3 гібридизація комплекс діамагнітний
 Теорія кристалічного поля За теорією кристалічного поля (ТКП) внутрішня координаційна сфера комплексів розглядається як така, що складається з позитивно зарядженого іона-комплексрутворювача, що розміщується в центрі, і негативнозаряджених лігандів, які його отчують відповідно до к. ч. Це взаємне розміщення нагадує будову іоних кристалів.
Теорія кристалічного поля За теорією кристалічного поля (ТКП) внутрішня координаційна сфера комплексів розглядається як така, що складається з позитивно зарядженого іона-комплексрутворювача, що розміщується в центрі, і негативнозаряджених лігандів, які його отчують відповідно до к. ч. Це взаємне розміщення нагадує будову іоних кристалів.
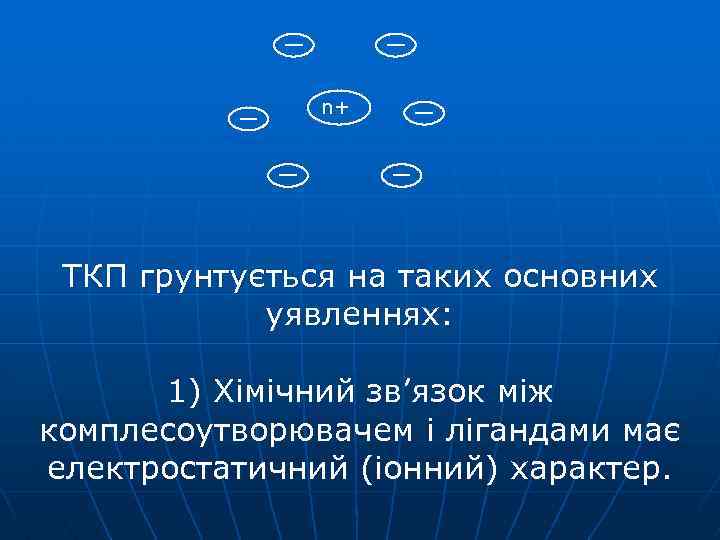 n+ ТКП грунтується на таких основних уявленнях: 1) Хімічний зв’язок між комплесоутворювачем і лігандами має електростатичний (іонний) характер.
n+ ТКП грунтується на таких основних уявленнях: 1) Хімічний зв’язок між комплесоутворювачем і лігандами має електростатичний (іонний) характер.
 2) ліганди розглядаються безструктурно, як носії певного негативного заряду; ліганди створюють навколо комплексоутворювача ефективне електричне (кристалічне) поле. 3) поле лігандів впливає на стан і поведінку всіх електронів на енергетичних рівнях комплексоутворювача, але детально розглядають стан і поведінку найближчих до лігандів d-електронів.
2) ліганди розглядаються безструктурно, як носії певного негативного заряду; ліганди створюють навколо комплексоутворювача ефективне електричне (кристалічне) поле. 3) поле лігандів впливає на стан і поведінку всіх електронів на енергетичних рівнях комплексоутворювача, але детально розглядають стан і поведінку найближчих до лігандів d-електронів.
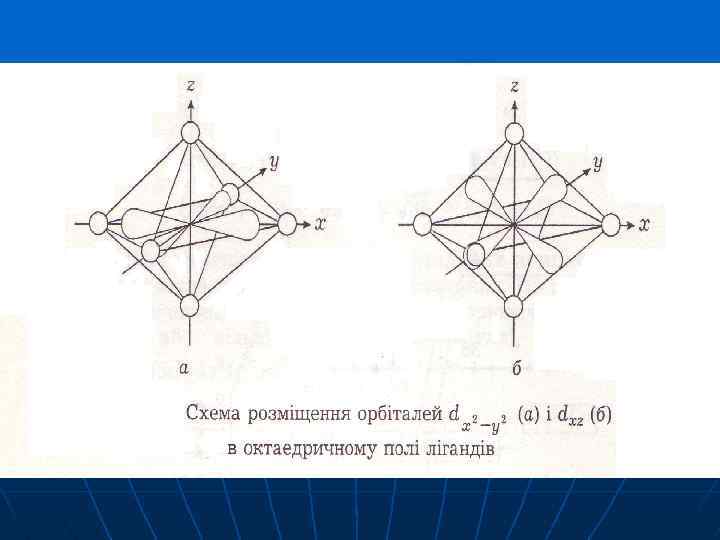
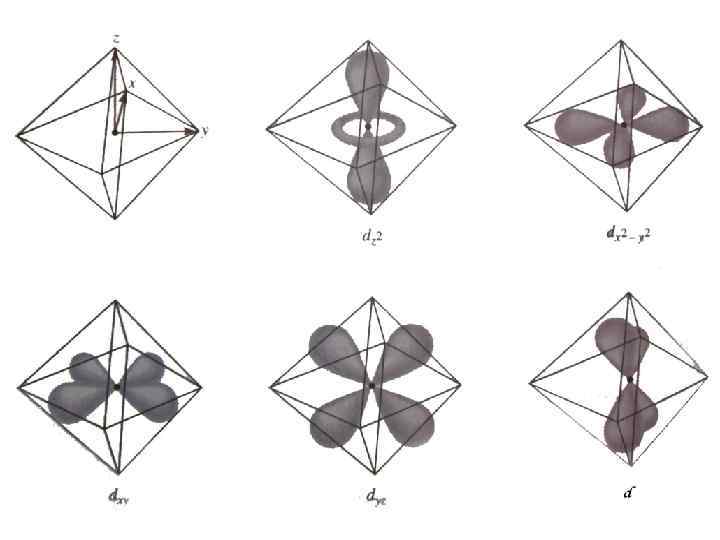
 d-орбіталі dxy dyz dx 2 - y 2 dz 2 Ефетивне кристалічне поле сильніше впливає на ті електрони іонакомплексоутворювача, які розміщені на d -орбіталях, просторово напрямлених у бік ліганду, або близьких до нього.
d-орбіталі dxy dyz dx 2 - y 2 dz 2 Ефетивне кристалічне поле сильніше впливає на ті електрони іонакомплексоутворювача, які розміщені на d -орбіталях, просторово напрямлених у бік ліганду, або близьких до нього.
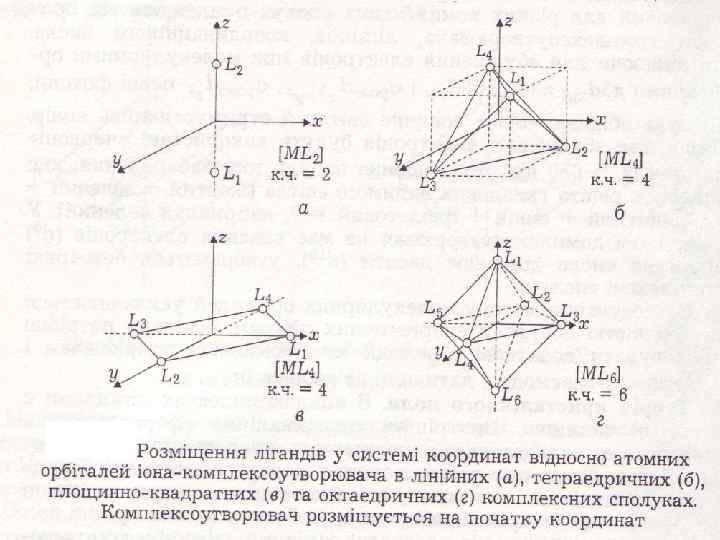
 к. ч. = 2 Найбільше ліганди впливають на електрони, що розташовані на dz 2 орбіталі комплексоуторювача к. ч. = 4 dxy dyz dxz к. ч. = 6 dx 2 - y 2 d z 2 В оточенні лігандів, під дією створюваного ними електричного поля, d -орбіталі комплексоутворювача стають нееквівалентними
к. ч. = 2 Найбільше ліганди впливають на електрони, що розташовані на dz 2 орбіталі комплексоуторювача к. ч. = 4 dxy dyz dxz к. ч. = 6 dx 2 - y 2 d z 2 В оточенні лігандів, під дією створюваного ними електричного поля, d -орбіталі комплексоутворювача стають нееквівалентними
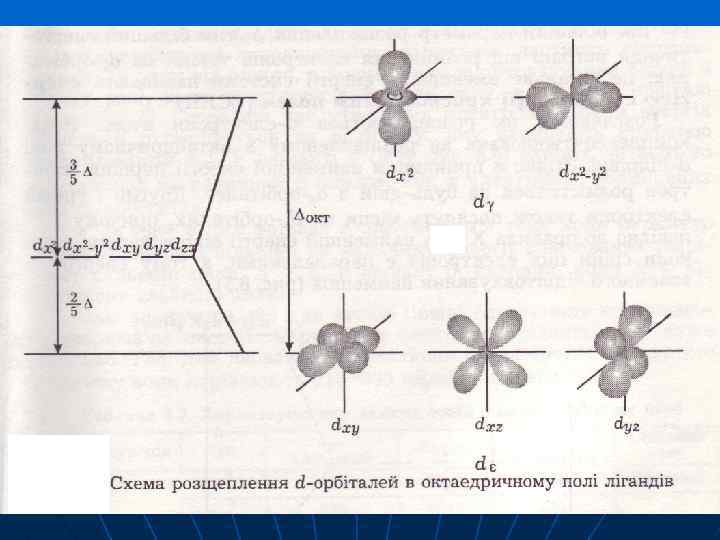
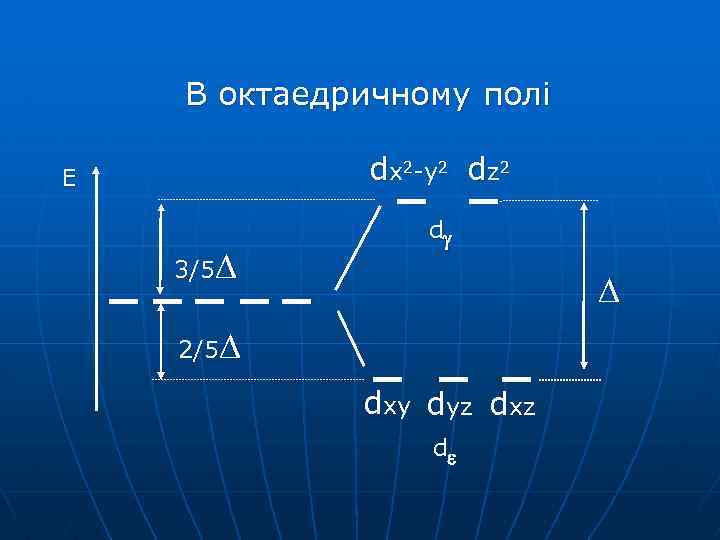 В октаедричному полі dx 2 -y 2 dz 2 Е 3/5 d 2/5 dxy dyz dxz d
В октаедричному полі dx 2 -y 2 dz 2 Е 3/5 d 2/5 dxy dyz dxz d
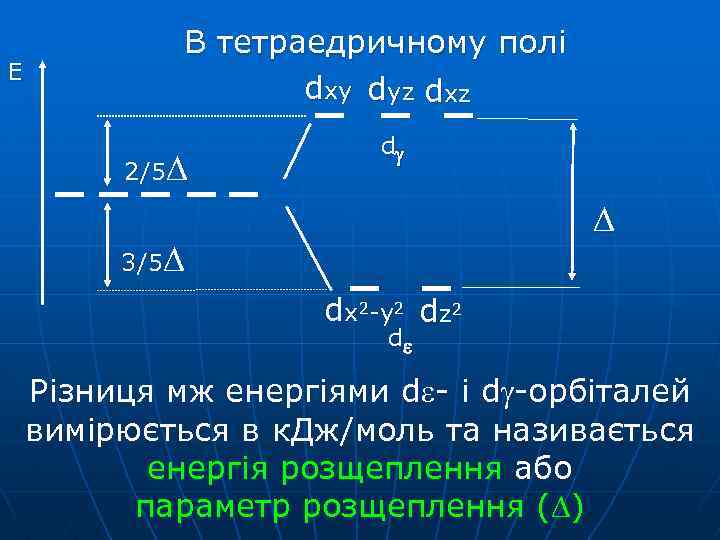 Е В тетраедричному полі dxy dyz dxz 2/5 d 3/5 dx 2 -y 2 dz 2 d Різниця мж енергіями d - і d -орбіталей вимірюється в к. Дж/моль та називається енергія розщеплення або параметр розщеплення ( )
Е В тетраедричному полі dxy dyz dxz 2/5 d 3/5 dx 2 -y 2 dz 2 d Різниця мж енергіями d - і d -орбіталей вимірюється в к. Дж/моль та називається енергія розщеплення або параметр розщеплення ( )
 залежить від: - координаційного числа; - заряду іона комплексоутворювача; А 2+ А 3+ ≈ 120 к. Дж/моль ≈ 240 к. Дж/моль - сили поля лігандів. Чим більша сила поля лігандів, тим розщеплення більше.
залежить від: - координаційного числа; - заряду іона комплексоутворювача; А 2+ А 3+ ≈ 120 к. Дж/моль ≈ 240 к. Дж/моль - сили поля лігандів. Чим більша сила поля лігандів, тим розщеплення більше.
 Чим більший параметр розщеплення Δ, тим більший енергетичний виграш від розміщення електронів тільки на d -орбіталях; це загальне зменшення енергії системи називають енергією стабілізації кристалічним полем (ЕСКП)
Чим більший параметр розщеплення Δ, тим більший енергетичний виграш від розміщення електронів тільки на d -орбіталях; це загальне зменшення енергії системи називають енергією стабілізації кристалічним полем (ЕСКП)
![[Co(NH 3)6]Cl 3 діамагнітний, забарвлений Сo 3 s 23 p 63 d 74 s [Co(NH 3)6]Cl 3 діамагнітний, забарвлений Сo 3 s 23 p 63 d 74 s](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-69.jpg) [Co(NH 3)6]Cl 3 діамагнітний, забарвлений Сo 3 s 23 p 63 d 74 s 24 p 0 Сo 3+ 3 s 23 p 63 d 64 s 04 p 0 Е dx 2 -y 2 dz 2 d dxy dyz dxz d
[Co(NH 3)6]Cl 3 діамагнітний, забарвлений Сo 3 s 23 p 63 d 74 s 24 p 0 Сo 3+ 3 s 23 p 63 d 64 s 04 p 0 Е dx 2 -y 2 dz 2 d dxy dyz dxz d
![[Co. F 6]3 парамагнітний, забарвлений Сo 3+ 3 s 23 p 63 d 64 [Co. F 6]3 парамагнітний, забарвлений Сo 3+ 3 s 23 p 63 d 64](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-70.jpg) [Co. F 6]3 парамагнітний, забарвлений Сo 3+ 3 s 23 p 63 d 64 s 04 p 0 Е dx 2 -y 2 dz 2 d dxy dyz dxz d
[Co. F 6]3 парамагнітний, забарвлений Сo 3+ 3 s 23 p 63 d 64 s 04 p 0 Е dx 2 -y 2 dz 2 d dxy dyz dxz d
 ТКП дає змогу оцінити стійкість комплексних сполук (достовірніше, ніж МВЗ) Дійсно, діамагнітні комплексні сполуки Со(lll) дуже стійкі
ТКП дає змогу оцінити стійкість комплексних сполук (достовірніше, ніж МВЗ) Дійсно, діамагнітні комплексні сполуки Со(lll) дуже стійкі
 Експерементально параметр розщеплення Δ визначають за спектрами поглинання розчинів комплексних сполук Δ = h Забарвлення комплексних сполук Електрони комплексу на розщеплених d-орбіталях розташовуються у відповідності до принципу найменшої енергії та принципу Паулі.
Експерементально параметр розщеплення Δ визначають за спектрами поглинання розчинів комплексних сполук Δ = h Забарвлення комплексних сполук Електрони комплексу на розщеплених d-орбіталях розташовуються у відповідності до принципу найменшої енергії та принципу Паулі.
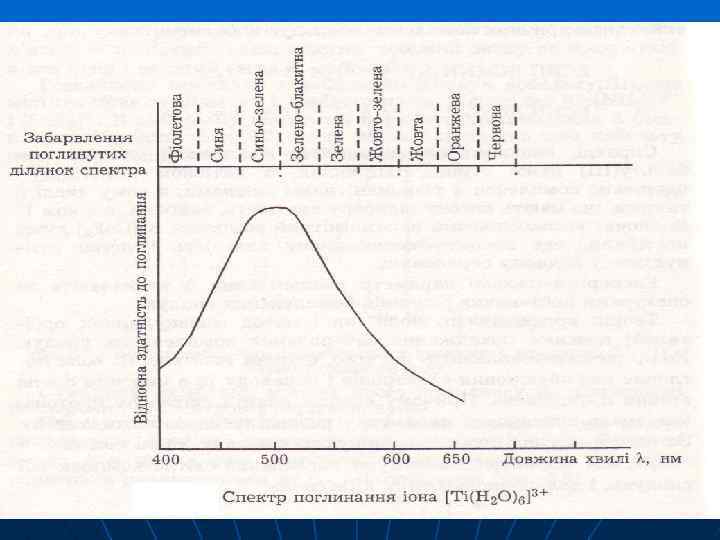
![Для [Ti(H 2 O)6]Cl 3 максимум поглинання відповідає = 20 000 см-1 ( = Для [Ti(H 2 O)6]Cl 3 максимум поглинання відповідає = 20 000 см-1 ( =](https://present5.com/presentation/3/54272390_134597491.pdf-img/54272390_134597491.pdf-74.jpg) Для [Ti(H 2 O)6]Cl 3 максимум поглинання відповідає = 20 000 см-1 ( = 500 нм) Колір цієї сполуки фіолетовий
Для [Ti(H 2 O)6]Cl 3 максимум поглинання відповідає = 20 000 см-1 ( = 500 нм) Колір цієї сполуки фіолетовий
 Якщо на d-орбіталях жодного електрона або 10, то комплексні сполуки будуть безбарвними (d 0, d 10). Якщо є хоча б один електрон або хоча б одного електрона не вистачає, то комплексні сполуки забарвлені (d 1 ÷ d 9)
Якщо на d-орбіталях жодного електрона або 10, то комплексні сполуки будуть безбарвними (d 0, d 10). Якщо є хоча б один електрон або хоча б одного електрона не вистачає, то комплексні сполуки забарвлені (d 1 ÷ d 9)


