кислород.ppt
- Количество слайдов: 24

 Установить различия между понятиями «простое вещество» , «химический элемент» ; Рассмотреть различные способы получения кислорода; Установить оптимальные способы получения кислорода; Изучить химические свойства кислорода.
Установить различия между понятиями «простое вещество» , «химический элемент» ; Рассмотреть различные способы получения кислорода; Установить оптимальные способы получения кислорода; Изучить химические свойства кислорода.
 Dum spiro – spero - пока дышу, надеюсь.
Dum spiro – spero - пока дышу, надеюсь.
 Что Вы можете рассказать о дыхании живых организмов, населяющих Землю?
Что Вы можете рассказать о дыхании живых организмов, населяющих Землю?
 Можете ли Вы вспомнить, когда и в связи с чем Вы впервые узнали о существовании кислорода?
Можете ли Вы вспомнить, когда и в связи с чем Вы впервые узнали о существовании кислорода?
 Самый распространенный элемент – Воздух состоит на 1/5 из – Самый жизненно важный элемент – Я коварный поджигатель Вы огня хотите – нате! Я всесильный окислитель (если только дров дадите)
Самый распространенный элемент – Воздух состоит на 1/5 из – Самый жизненно важный элемент – Я коварный поджигатель Вы огня хотите – нате! Я всесильный окислитель (если только дров дадите)

 Джозеф Пристли В 70 -х г. г. XVIII столетия описал свойства «дефлогистированного воздуха» (кислорода), нагревая оксид ртути, собирая солнечные лучи при помощи увеличительного стекла
Джозеф Пристли В 70 -х г. г. XVIII столетия описал свойства «дефлогистированного воздуха» (кислорода), нагревая оксид ртути, собирая солнечные лучи при помощи увеличительного стекла
 Карл Шееле В 1771 исследовал и доказал сложный состав воздуха; l l. В 1772 г. впервые в истории сумел получить в лаборатории чистый «огневой воздух"
Карл Шееле В 1771 исследовал и доказал сложный состав воздуха; l l. В 1772 г. впервые в истории сумел получить в лаборатории чистый «огневой воздух"
 Антуан Лавуазье • Включил новый элемент в список простых веществ и дал ему название Oxygenium – «рождающий кислоты» ; • Выяснил роль кислорода в процессах горения, обжига металлов и дыхания.
Антуан Лавуазье • Включил новый элемент в список простых веществ и дал ему название Oxygenium – «рождающий кислоты» ; • Выяснил роль кислорода в процессах горения, обжига металлов и дыхания.
 Дмитрий Иванович Менделеев • Автор периодического закона и универсальной системы химических элементов; • «…Очень многие тела горят в кислороде, и от его присутствия и в воздухе. Для начала горения необходимо обыкновенно накалить горючее вещество или только некоторую часть его. Для продолжения горения нет нужды в новом накаливании. » Д. И. Менделеев «Основы химии»
Дмитрий Иванович Менделеев • Автор периодического закона и универсальной системы химических элементов; • «…Очень многие тела горят в кислороде, и от его присутствия и в воздухе. Для начала горения необходимо обыкновенно накалить горючее вещество или только некоторую часть его. Для продолжения горения нет нужды в новом накаливании. » Д. И. Менделеев «Основы химии»
 Китайцы описали кислород еще в VIII веке до нашей эры; В Европе изобретатель подводной лодки Корнелиус Дреббель еще в начале XVII века выделил кислород, выяснил его роль в дыхании и использовал это открытие в своей подводной лодке.
Китайцы описали кислород еще в VIII веке до нашей эры; В Европе изобретатель подводной лодки Корнелиус Дреббель еще в начале XVII века выделил кислород, выяснил его роль в дыхании и использовал это открытие в своей подводной лодке.
 Химический знак Место в периодической системе Неметалл или металл Аr (О) = Валентность Формы распространения в природе
Химический знак Место в периодической системе Неметалл или металл Аr (О) = Валентность Формы распространения в природе
 О; II – период, VI А группа; Неметалл; II В виде простых веществ: О 2, О 3 (озон), в составе сложных веществ: Н 2 О, СО 2 и т. д.
О; II – период, VI А группа; Неметалл; II В виде простых веществ: О 2, О 3 (озон), в составе сложных веществ: Н 2 О, СО 2 и т. д.
 Химическая формула Модель молекулы Мr? M Строение Физические свойства -
Химическая формула Модель молекулы Мr? M Строение Физические свойства -
 О 2; О=О; М (О 2) = 32 г/моль; Молекулярное; - 187○С → -218, 7 ○С → ↑; без цвета, жидкость кристаллы синего вкуса и запаха бледно-синего цвета
О 2; О=О; М (О 2) = 32 г/моль; Молекулярное; - 187○С → -218, 7 ○С → ↑; без цвета, жидкость кристаллы синего вкуса и запаха бледно-синего цвета
 Получение кислорода KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 ↑
Получение кислорода KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 ↑
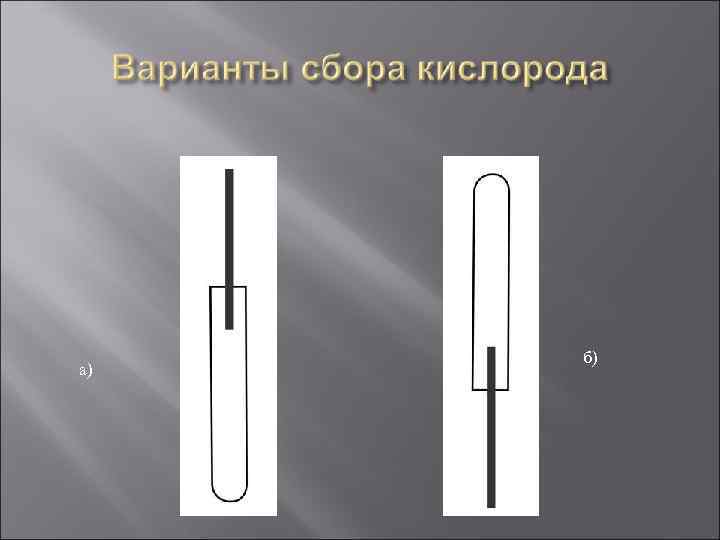 а) б)
а) б)
 Слово «оксид» + Название элемента + Указание валентности (в скобках) для тех случаев, когда элемент имеет переменную валентность Например: Н 2 О – оксид водорода, Са. О – оксид кальция, Hg. О – оксид ртути (II)
Слово «оксид» + Название элемента + Указание валентности (в скобках) для тех случаев, когда элемент имеет переменную валентность Например: Н 2 О – оксид водорода, Са. О – оксид кальция, Hg. О – оксид ртути (II)


 УПРАЖНЕНИЯ ДЛЯ САМОКОНТРОЛЯ • В ряду формул веществ выберите оксиды, дайте им название: CS 2, Mg. O, PH 3, SO 3, CO 2, Al 2 O 3, Mg 3 N 2, Zn. O. • Составьте формулы оксидов: а) оксид марганца (III); б) оксид марганца (VII); в) оксид хрома (VI); г) оксид железа (II).
УПРАЖНЕНИЯ ДЛЯ САМОКОНТРОЛЯ • В ряду формул веществ выберите оксиды, дайте им название: CS 2, Mg. O, PH 3, SO 3, CO 2, Al 2 O 3, Mg 3 N 2, Zn. O. • Составьте формулы оксидов: а) оксид марганца (III); б) оксид марганца (VII); в) оксид хрома (VI); г) оксид железа (II).
 • Продолжите уравнения химических реакций а) Zn + O 2 = б) Al + O 2 = в) CH 4 + O 2 = г) Ca + O 2 = д) Cl 2 + O 2 =
• Продолжите уравнения химических реакций а) Zn + O 2 = б) Al + O 2 = в) CH 4 + O 2 = г) Ca + O 2 = д) Cl 2 + O 2 =
 1. Mg. O – оксид магния; CO 2 - оксид углерода (IV); SO 2 - оксид серы (VI); Al 2 O 3 - оксид алюминия; Zn. O – оксид цинка. 2. а) оксид марганца (III) – Mn 2 O 3; б) оксид марганца (VII) – Mn 2 O 7; в) оксид хрома (VI) – Cr. O 3; 3. а) 2 Zn + O 2 = 2 Zn. O; б) 4 Al + 3 O 2 = 2 Al 2 O 3; в) CH 4 + 2 O 2 = CO 2 + 2 H 2 O г) 2 Ca + O 2 = 2 Ca. O д) 2 Cl 2 + 7 O 2 = 2 Cl 2 O 7 г) оксид железа (II) - Fe. O.
1. Mg. O – оксид магния; CO 2 - оксид углерода (IV); SO 2 - оксид серы (VI); Al 2 O 3 - оксид алюминия; Zn. O – оксид цинка. 2. а) оксид марганца (III) – Mn 2 O 3; б) оксид марганца (VII) – Mn 2 O 7; в) оксид хрома (VI) – Cr. O 3; 3. а) 2 Zn + O 2 = 2 Zn. O; б) 4 Al + 3 O 2 = 2 Al 2 O 3; в) CH 4 + 2 O 2 = CO 2 + 2 H 2 O г) 2 Ca + O 2 = 2 Ca. O д) 2 Cl 2 + 7 O 2 = 2 Cl 2 O 7 г) оксид железа (II) - Fe. O.


