4. Уровни структ.организации белк.молекул1.ppt
- Количество слайдов: 73

УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКОВЫХ МОЛЕКУЛ. ОСОБЕННОСТИ СТРОЕНИЯ Основные вопросы: • 1. Первичная структура белков • 2. Вторичная структура белков • 3. Третичная структура белков • 4. Четвертичная структура белков • 5. Фолдинг белков • 6. Белки шапероны

История изучения структуры белка • Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру белков. • Позднее Уолтер Каузман внёс весомый вклад в понимание законов образования третичной структуры белков и роли в этом процессе гидрофобных взаимодействий. • В 1949 году Фред Сенгер определил аминокислотную последовательность инсулина, продемонстрировав таким способом, что белки — это линейные полимеры аминокислот, а не их разветвлённые (как у некоторых сахаров) цепи. • Первые структуры белков, основанные на дифракции рентгеновских лучей на уровне отдельных атомов были получены в 1960 -х годах и с помощью ЯМР в 1980 -х годах. • В 2006 году Банк данных о белках (Protein Data Bank) содержал около 40 000 структур белков.

Современное изучение структуры белка • В XXI веке исследование белков перешло на качественно новый уровень, когда исследуются не только индивидуальные белки, но и одновременное изменение количества и посттрансляционные модификации большого числа белков отдельных клеток, тканей или организмов. Эта область биохимии называется протеомикой. • С помощью методов биоинформатики стало возможно не только обработать данные рентгенно-структурного анализа, но и предсказать структуру белка, основываясь на его аминокислотной последовательности. • В настоящее время электронная микроскопия больших белковых комплексов и предсказание малых белков и доменов больших белков с помощью компьютерных программ по точности приближаются к разрешению структур на атомном уровне.

• Постулаты (принципы формирования пептидной связи), сформулированные Л. Поллингом и Р. Кори: 1) атомы, образующие пептидную связь, копланарны; вращение атомов или групп атомов вокруг пептидной связи невозможно; 2) принцип эквивалентности вклада АК остатков в образование пептидной связи и, тем самым, в образование полипептидной цепи (исключение пролин); 3) принцип максимума водородных связей.

• Каждый белок характеризуется специфической аминокислотной последовательностью и индивидуальной пространственной структурой (конформацией). • В нативном состоянии белковые макромолекулы обладают специфической конформацией. • Характерная для данного белка конформация определяется последовательностью аминокислотных остатков и стабилизируется водородными связями между пептидными и боковыми группами аминокислотных остатков, а также электростатическим и гидрофобными взаимодействиями.
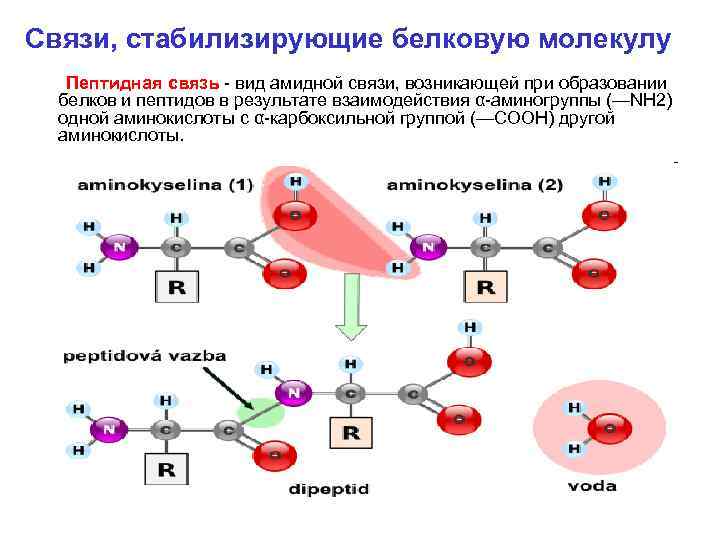
Связи, стабилизирующие белковую молекулу Пептидная связь вид амидной связи, возникающей при образовании белков и пептидов в результате взаимодействия α аминогруппы (—NH 2) одной аминокислоты с α карбоксильной группой (—СООН) другой аминокислоты.
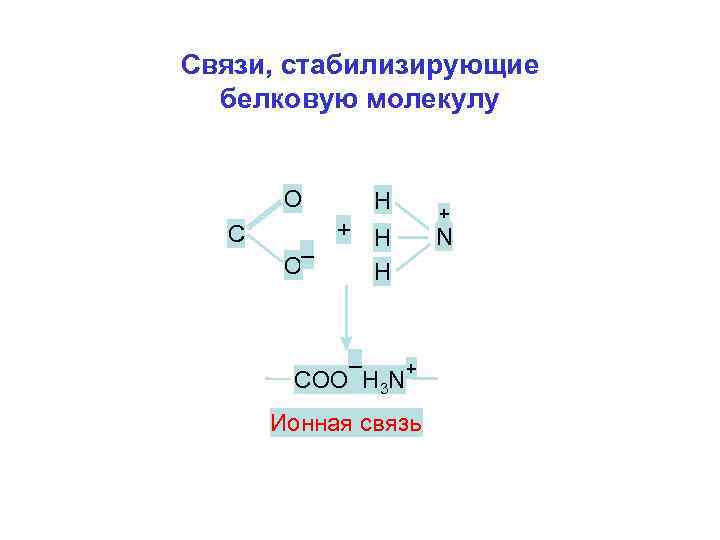
Связи, стабилизирующие белковую молекулу О С Н + Н О– Н – + СОО Н 3 N Ионная связь + N
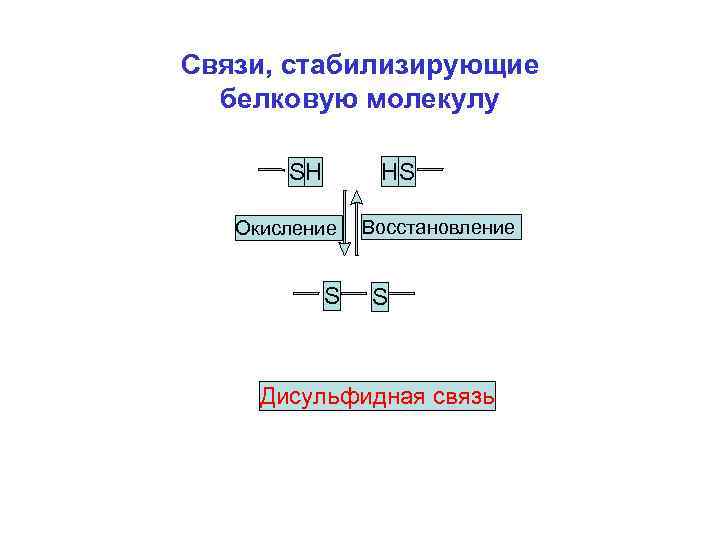
Связи, стабилизирующие белковую молекулу НS SН Окисление Восстановление S S Дисульфидная связь
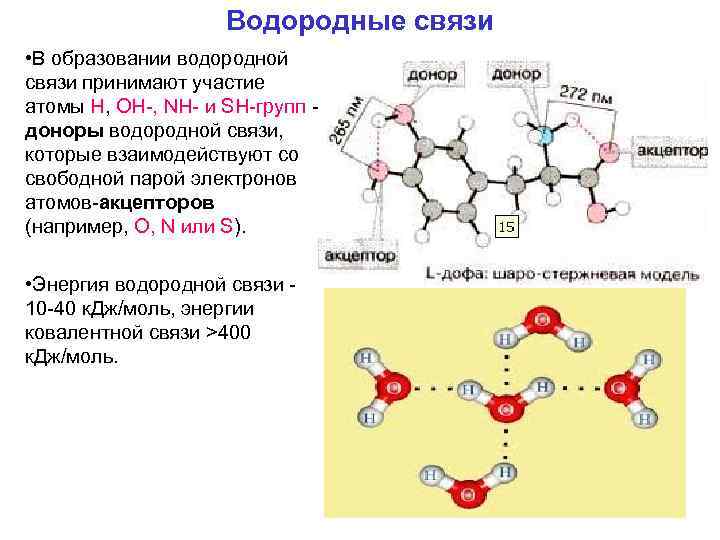
Водородные связи • В образовании водородной связи принимают участие атомы Н, ОН , NH и SH гpупп доноры водородной связи, которые взаимодействуют со свободной парой электронов атомов акцепторов (например, О, N или S). • Энергия водородной связи 10 40 к. Дж/моль, энергии ковалентной связи >400 к. Дж/моль.
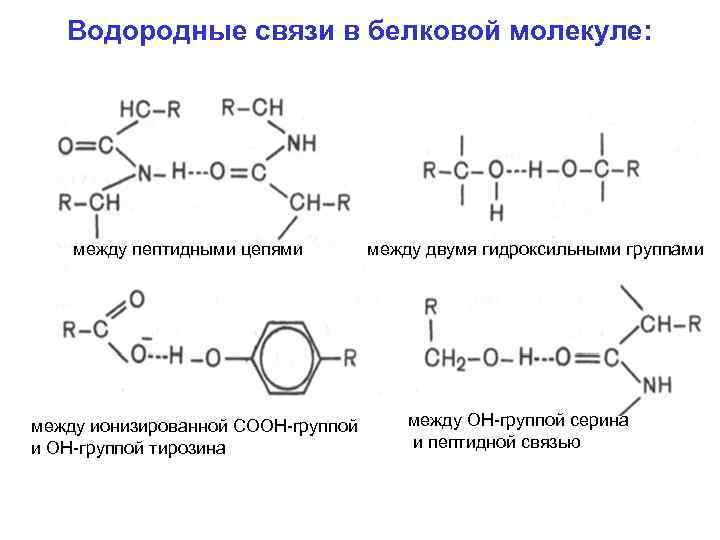
Водородные связи в белковой молекуле: между пептидными цепями между ионизированной СООН группой и ОН группой тирозина между двумя гидроксильными группами между ОН группой серина и пептидной связью
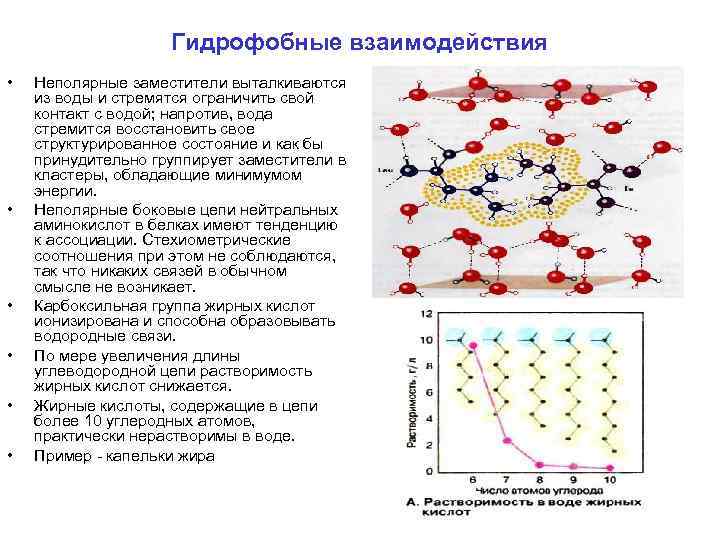
Гидрофобные взаимодействия • • • Неполярные заместители выталкиваются из воды и стремятся ограничить свой контакт с водой; напротив, вода стремится восстановить свое структурированное состояние и как бы принудительно группирует заместители в кластеры, обладающие минимумом энергии. Неполярные боковые цепи нейтральных аминокислот в белках имеют тенденцию к ассоциации. Стехиометрические соотношения при этом не соблюдаются, так что никаких связей в обычном смысле не возникает. Карбоксильная группа жирных кислот ионизирована и способна образовывать водородные связи. По мере увеличения длины углеводородной цепи растворимость жирных кислот снижается. Жирные кислоты, содержащие в цепи более 10 углеродных атомов, практически нерастворимы в воде. Пример капельки жира

R группы некоторых ак т, н р тирозина и валина, неполярны и потому гидрофобны. Если в полипептидной цепи содержится много таких групп, то в водной среде эта цепь стремится свернуться т. о, чтобы гидрофобные группы сблизились возможно теснее, вытолкнув воду. Так свертываются многие глобулярные белки. Их гидрофобные группы ак т бывают обращены при этом внутрь, к центру молекулы, имеющей почти шарообразную форму, а гидрофильные группы — наружу, к водной среде, что делает белок растворимым.

Электростатические связи • Электростатические связи обусловлены взаимным притяжением частиц с разноименными зарядами; например, заряженные положительно ионы натрия могут соединяться с отрицательно заряженными ионами хлора, образуя кристаллический хлористый натрий (поваренную соль). • Эти солевые связи возникают между разноименнно заряженными группами, входящими в состав боковых цепей аминокислот. • Например, аминогруппа лизина при физиологических р. Н несет заряд +1, а карбоксильная группа аспартата или глутамата в составе боковой цепи несет заряд 1. • Следовательно, эти группы могут электростатически взаимодействовать, стабилизируя структуру белка.
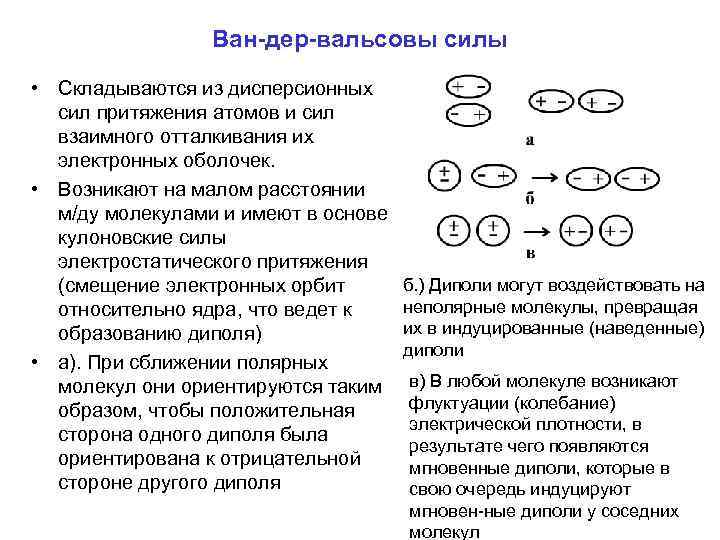
Ван-дер-вальсовы силы • Складываются из дисперсионных сил притяжения атомов и сил взаимного отталкивания их электронных оболочек. • Возникают на малом расстоянии м/ду молекулами и имеют в основе кулоновские силы электростатического притяжения (смещение электронных орбит относительно ядра, что ведет к образованию диполя) • а). При сближении полярных молекул они ориентируются таким образом, чтобы положительная сторона одного диполя была ориентирована к отрицательной стороне другого диполя б. ) Диполи могут воздействовать на неполярные молекулы, превращая их в индуцированные (наведенные) диполи в) В любой молекуле возникают флуктуации (колебание) электрической плотности, в результате чего появляются мгновенные диполи, которые в свою очередь индуцируют мгновен ные диполи у соседних молекул

Ионные связи • • Ионные, или электростатические, взаимодействия представляют собой взаимодействия заряженных групп. При этом, как известно, одноименно заряженные группы отталкиваются, а разноименно заряженные притягиваются. К ним относятся, в частности, взаимодействия ионогенных групп, образующих солевые связи. Если разница электроотрицательности велика (2, 0 и выше), то обр ся ионная связь, а меньше 1, 0 – ковалентная. Фермент—кофермент Фермент—субстрат Антиген—антитело

• • Олигопептиды (ди , три , тетра )– до 20 АК Полипептиды – от 20 до 50 АК Белки – более 50 АК М. м – свыше 6000. Каждому белку свойственна своя геометрическая форма или конформация. • 4 уровня организации белков • Аминокислотная последовательность определяет пространственную структуру белка, а структура эта уже определяет его функцию
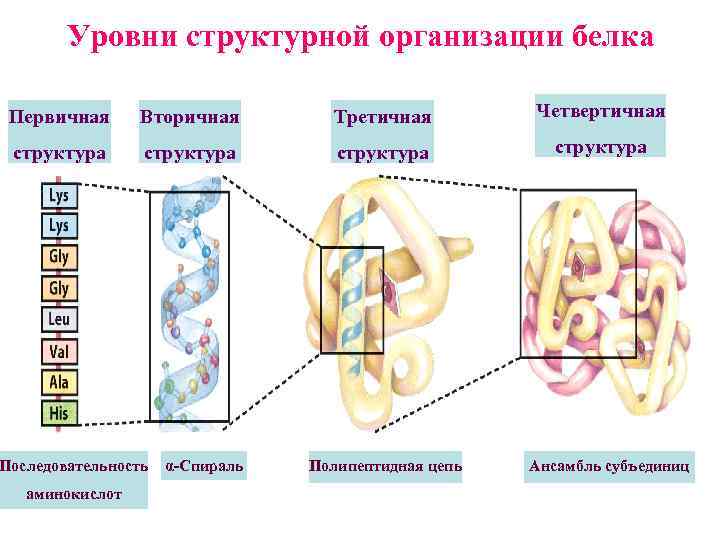
Уровни структурной организации белка Первичная Вторичная Третичная Четвертичная структура Последовательность аминокислот α-Спираль Полипептидная цепь Ансамбль субъединиц


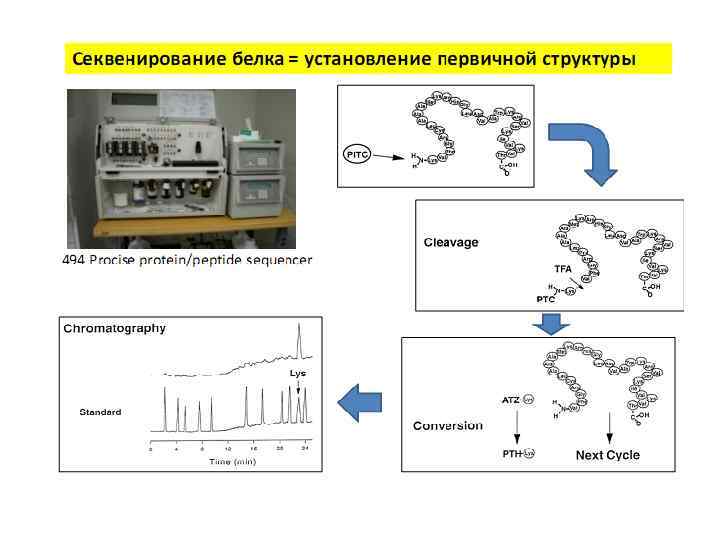
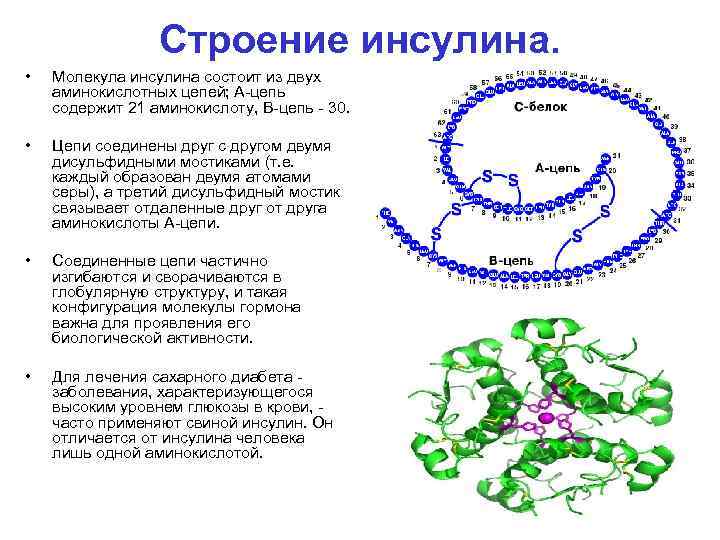
Строение инсулина. • Молекула инсулина состоит из двух аминокислотных цепей; А цепь содержит 21 аминокислоту, В цепь 30. • Цепи соединены друг с другом двумя дисульфидными мостиками (т. е. каждый образован двумя атомами серы), а третий дисульфидный мостик связывает отдаленные друг от друга аминокислоты А цепи. • Соединенные цепи частично изгибаются и сворачиваются в глобулярную структуру, и такая конфигурация молекулы гормона важна для проявления его биологической активности. • Для лечения сахарного диабета заболевания, характеризующегося высоким уровнем глюкозы в крови, часто применяют свиной инсулин. Он отличается от инсулина человека лишь одной аминокислотой.

• Гормон синтезируется в бета клетках, которые входят в отдельные гормон секретирующие группы клеток поджелудочной железы, называемые островками Лангерганса. • Слово "инсулин" (от лат. insula остров) указывает на "островковое" происхождение гормона. • Инсулин был впервые выделен из поджелудочной железы в Канаде в 1921 Ф. Бантингом и Ч. Бестом, сотрудниками Дж. Маклеода. • Признанием их работы явилась Нобелевская премия по физиологии и медицине, присужденная Бантингу и Маклеоду в 1923.
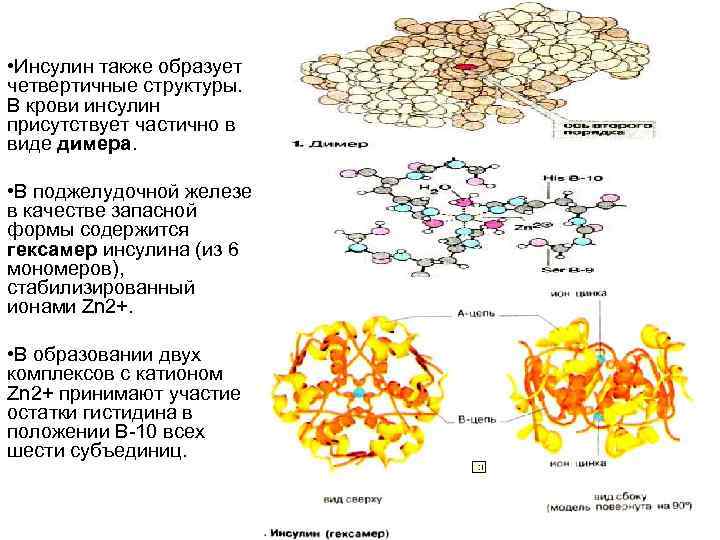
• Инсулин также образует четвертичные структуры. В крови инсулин присутствует частично в виде димера. • В поджелудочной железе в качестве запасной формы содержится гексамер инсулина (из 6 мономеров), стабилизированный ионами Zn 2+. • В образовании двух комплексов с катионом Zn 2+ принимают участие остатки гистидина в положении B 10 всех шести субъединиц.

Функция инсулина. • Инсулин важнейший регулятор промежуточного обмена веществ. • Главное его действие заключается в снижении уровня сахара в крови: он облегчает поглощение и использование глюкозы мышечными и жировыми клетками и тормозит образование новых молекул глюкозы в печени. • Кроме того, он способствует запасанию глюкозы в клетках в форме гликогена, а также накоплению других веществ потенциальных источников энергии (жира, белка), тормозят их распад и утилизацию организмом.

Конформация белков • Линейные полипептидные цепи белков за счет взаимодействия функциональных групп аминокислот приобретают определенную пространственную структуру, называемую «конформация» . • Все молекулы белков, имеющих одинаковую первичную структуру имеют одинаковую конформацию. • В белках различают 2 основных типа конформации полипептидных цепей: вторичную и третичную структуры.
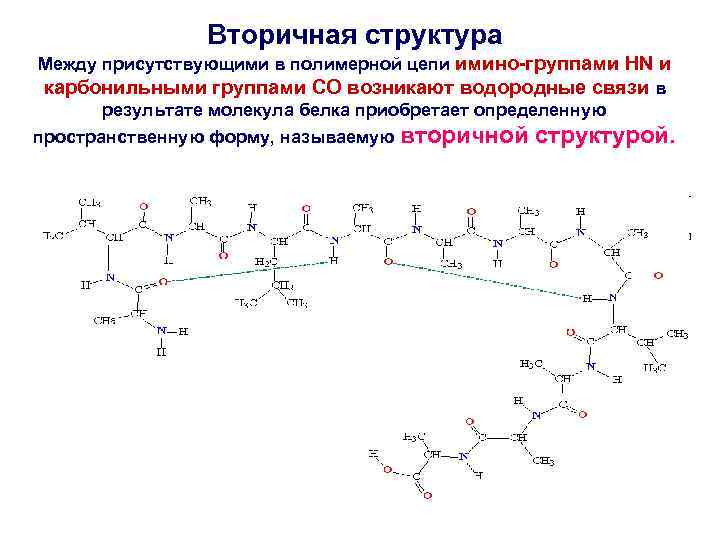
Вторичная структура Между присутствующими в полимерной цепи имино-группами HN и карбонильными группами CO возникают водородные связи в результате молекула белка приобретает определенную пространственную форму, называемую вторичной структурой.
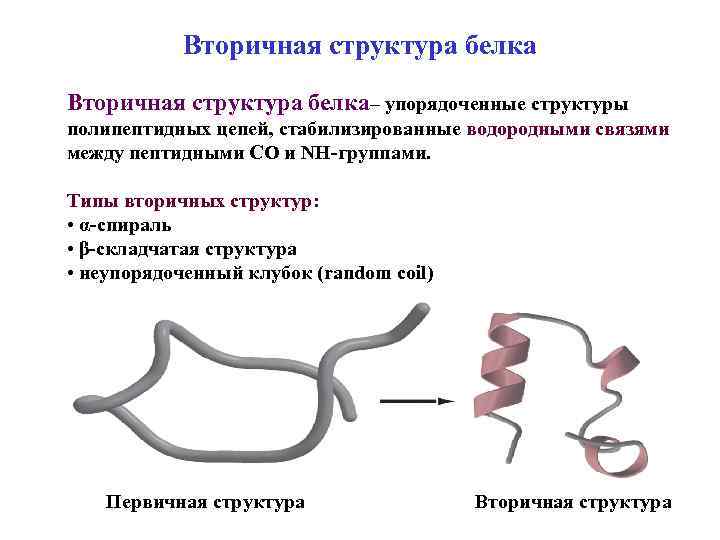
Вторичная структура белка– упорядоченные структуры полипептидных цепей, стабилизированные водородными связями между пептидными СО и NH-группами. Типы вторичных структур: • α-спираль • β-складчатая структура • неупорядоченный клубок (random coil) Первичная структура Вторичная структура
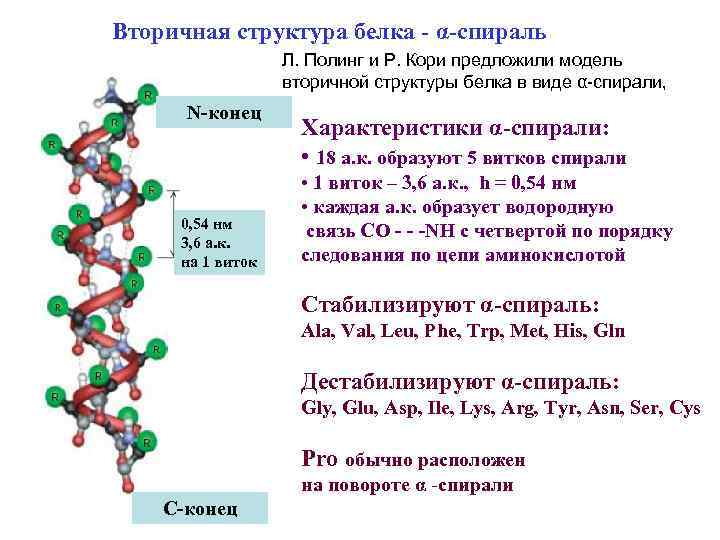
Вторичная структура белка - α-спираль Л. Полинг и Р. Кори предложили модель вторичной структуры белка в виде α спирали, N-конец 0, 54 нм 3, 6 а. к. на 1 виток Характеристики α-спирали: • 18 а. к. образуют 5 витков спирали • 1 виток – 3, 6 а. к. , h = 0, 54 нм • каждая а. к. образует водородную связь СО - - -NH c четвертой по порядку следования по цепи аминокислотой Стабилизируют α-спираль: Ala, Val, Leu, Phe, Trp, Met, His, Gln Дестабилизируют α-спираль: Gly, Glu, Asp, Ile, Lys, Arg, Tyr, Asn, Ser, Cys Pro обычно расположен на повороте α -спирали C-конец
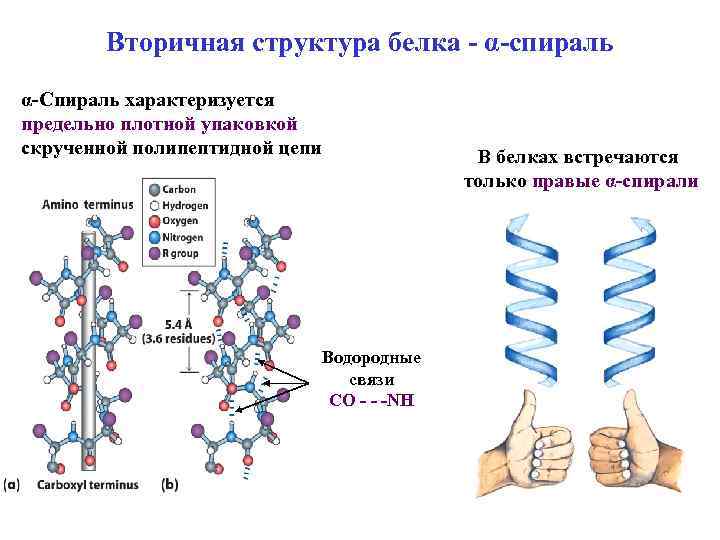
Вторичная структура белка - α-спираль α-Спираль характеризуется предельно плотной упаковкой скрученной полипептидной цепи В белках встречаются только правые α-спирали Водородные связи СО - - -NH
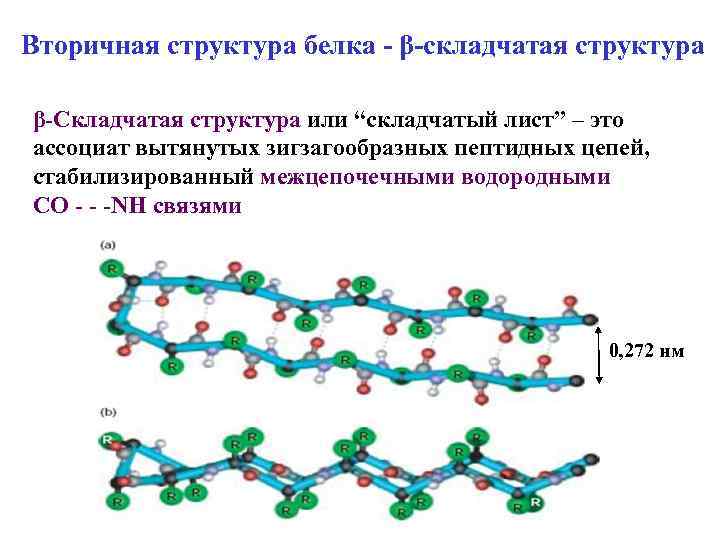
Вторичная структура белка - β-складчатая структура β-Складчатая структура или “складчатый лист” – это ассоциат вытянутых зигзагообразных пептидных цепей, стабилизированный межцепочечными водородными СО - - -NH связями 0, 272 нм
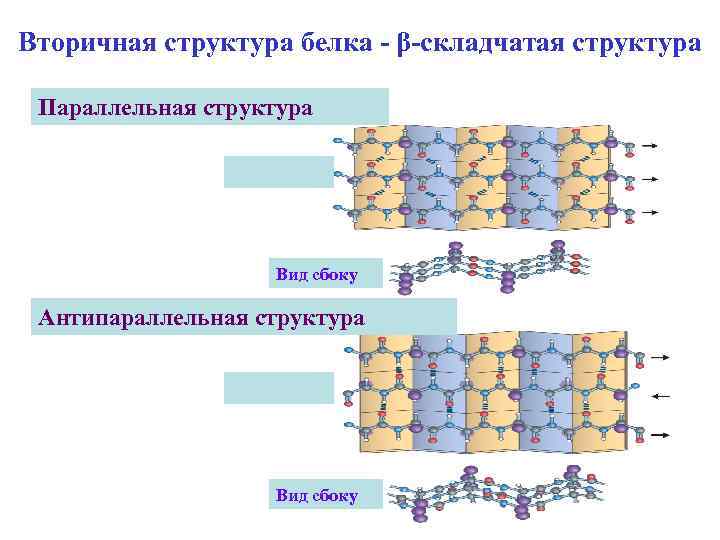
Вторичная структура белка - β-складчатая структура Параллельная структура Вид сбоку Антипараллельная структура Вид сбоку
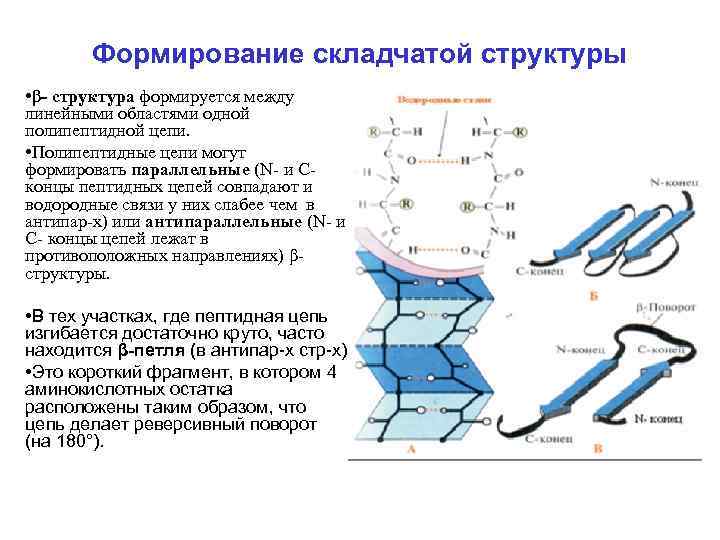
Формирование складчатой структуры • β- структура формируется между линейными областями одной полипептидной цепи. • Полипептидные цепи могут формировать параллельные (N- и Cконцы пептидных цепей совпадают и водородные связи у них слабее чем в антипар-х) или антипараллельные (N- и C- концы цепей лежат в противоположных направлениях) βструктуры. • В тех участках, где пептидная цепь изгибается достаточно круто, часто находится β-петля (в антипар х стр х). • Это короткий фрагмент, в котором 4 аминокислотных остатка расположены таким образом, что цепь делает реверсивный поворот (на 180°).
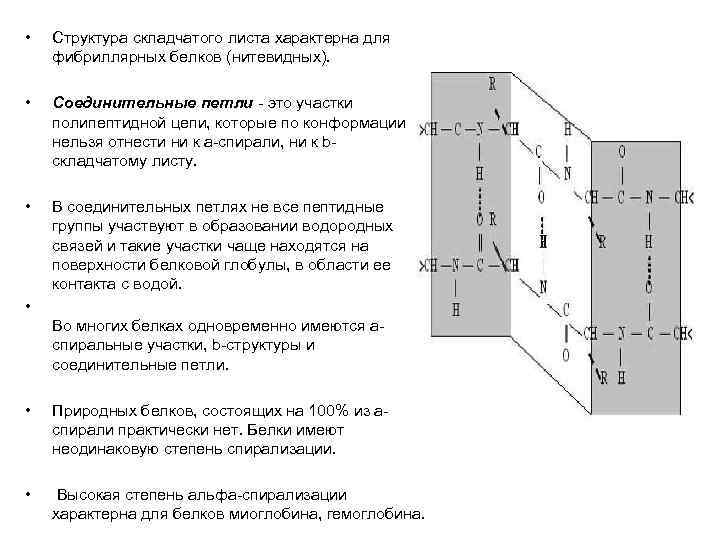
• Структура складчатого листа характерна для фибриллярных белков (нитевидных). • Соединительные петли это участки полипептидной цепи, которые по конформации нельзя отнести ни к a спирали, ни к b складчатому листу. • В соединительных петлях не все пептидные группы участвуют в образовании водородных связей и такие участки чаще находятся на поверхности белковой глобулы, в области ее контакта с водой. Во многих белках одновременно имеются a спиральные участки, b структуры и соединительные петли. • • Природных белков, состоящих на 100% из a спирали практически нет. Белки имеют неодинаковую степень спирализации. • Высокая степень альфа спирализации характерна для белков миоглобина, гемоглобина.
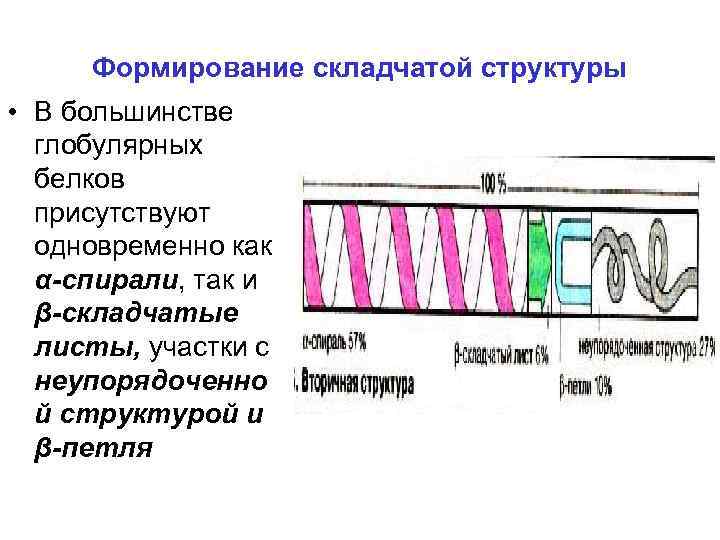
Формирование складчатой структуры • В большинстве глобулярных белков присутствуют одновременно как α-спирали, так и β-складчатые листы, участки с неупорядоченно й структурой и β-петля
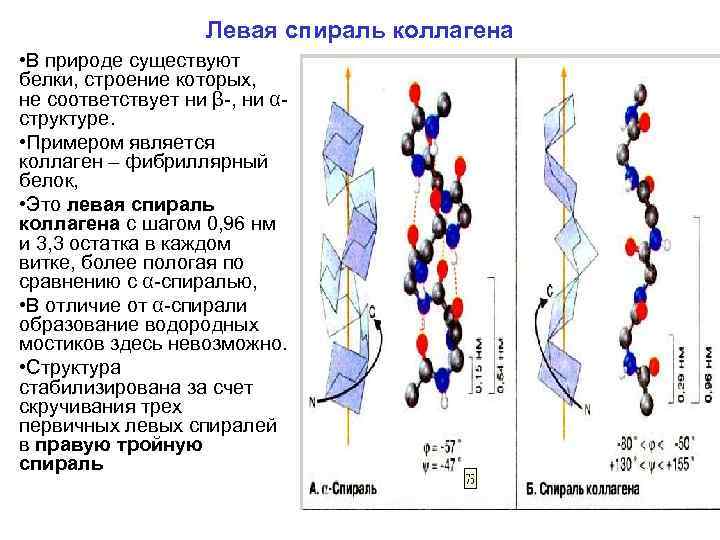
Левая спираль коллагена • В природе существуют белки, строение которых, не соответствует ни β , ни α структуре. • Примером является коллаген – фибриллярный белок, • Это левая спираль коллагена с шагом 0, 96 нм и 3, 3 остатка в каждом витке, более пологая по сравнению с α спиралью, • В отличие от α спирали образование водородных мостиков здесь невозможно. • Структура стабилизирована за счет скручивания трех первичных левых спиралей в правую тройную спираль
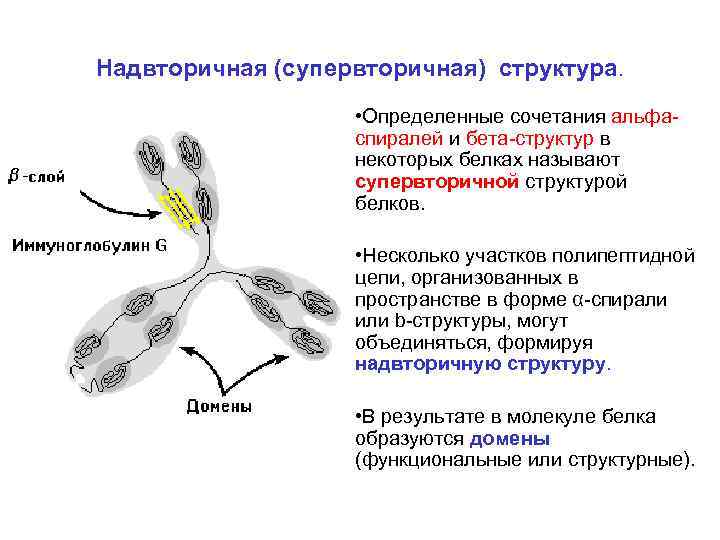
Надвторичная (супервторичная) структура. • Определенные сочетания альфа спиралей и бета структур в некоторых белках называют супервторичной структурой белков. • Несколько участков полипептидной цепи, организованных в пространстве в форме α спирали или b структуры, могут объединяться, формируя надвторичную структуру. • В результате в молекуле белка образуются домены (функциональные или структурные).
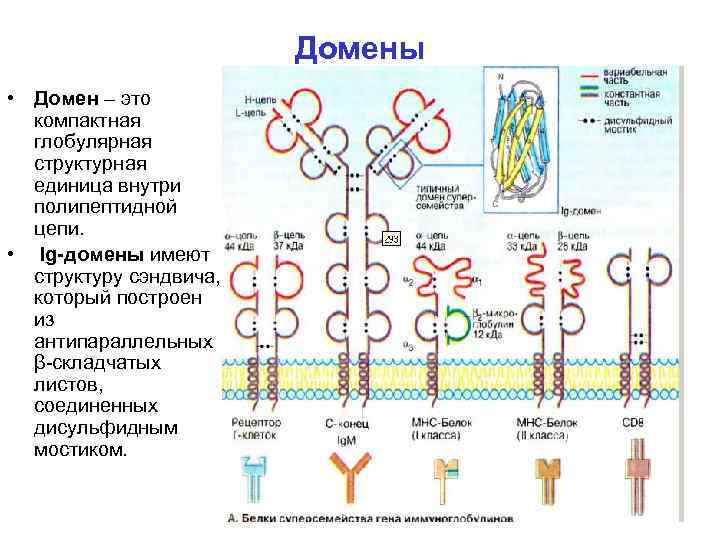
Домены • Домен – это компактная глобулярная структурная единица внутри полипептидной цепи. • Ig-домены имеют структуру сэндвича, который построен из антипараллельных β складчатых листов, соединенных дисульфидным мостиком.
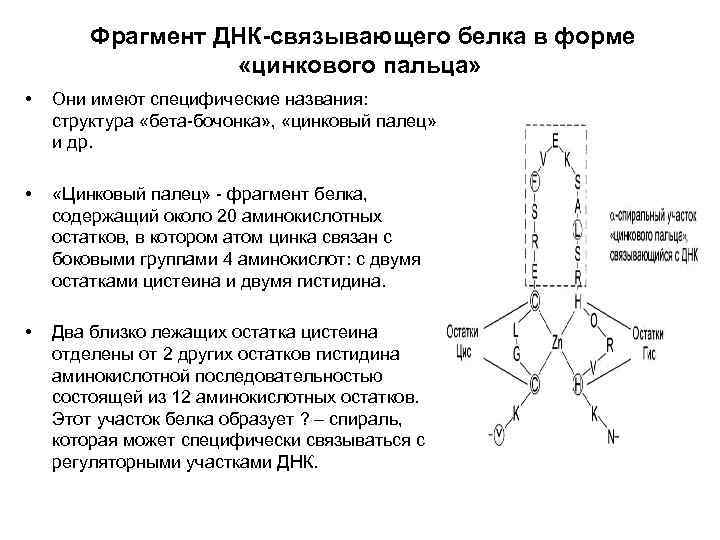
Фрагмент ДНК-связывающего белка в форме «цинкового пальца» • Они имеют специфические названия: структура «бета бочонка» , «цинковый палец» и др. • «Цинковый палец» фрагмент белка, содержащий около 20 аминокислотных остатков, в котором атом цинка связан с боковыми группами 4 аминокислот: с двумя остатками цистеина и двумя гистидина. • Два близко лежащих остатка цистеина отделены от 2 других остатков гистидина аминокислотной последовательностью состоящей из 12 аминокислотных остатков. Этот участок белка образует ? – спираль, которая может специфически связываться с регуляторными участками ДНК.

Супервторичные структуры По наличию α спиралей и β– структур глобулярные белки делятся на 4 группы: 1. Белки, в которых имеются только α– спирали , н р миоглобин, гемоглобин. 2. Белки – и α-спирали и β-структуры.
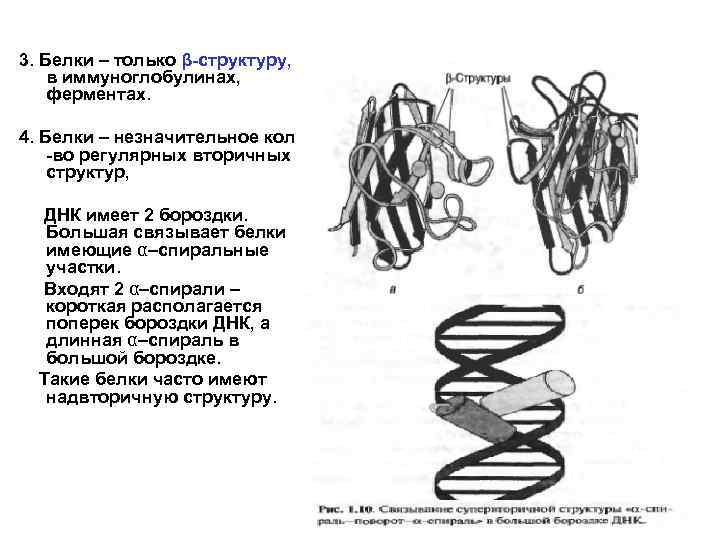
3. Белки – только β-структуру, в иммуноглобулинах, ферментах. 4. Белки – незначительное кол -во регулярных вторичных структур, ДНК имеет 2 бороздки. Большая связывает белки имеющие α–спиральные участки. Входят 2 α–спирали – короткая располагается поперек бороздки ДНК, а длинная α–спираль в большой бороздке. Такие белки часто имеют надвторичную структуру.
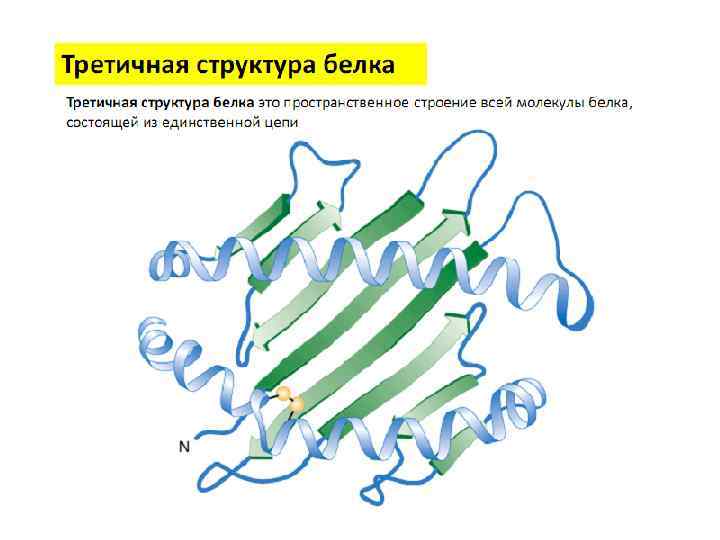


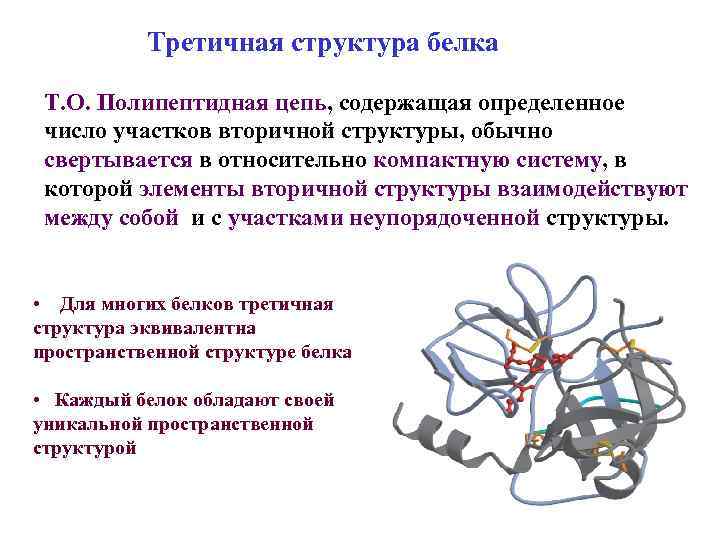
Третичная структура белка Т. О. Полипептидная цепь, содержащая определенное число участков вторичной структуры, обычно свертывается в относительно компактную систему, в которой элементы вторичной структуры взаимодействуют между собой и с участками неупорядоченной структуры. • Для многих белков третичная структура эквивалентна пространственной структуре белка • Каждый белок обладают своей уникальной пространственной структурой
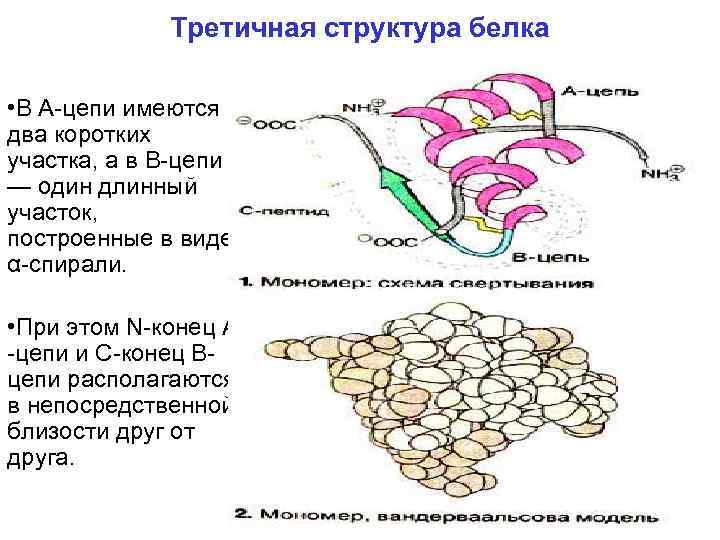
Третичная структура белка • В Α цепи имеются два коротких участка, а в В цепи — один длинный участок, построенные в виде α спирали. • При этом N конец А цепи и С конец В цепи располагаются в непосредственной близости друг от друга.
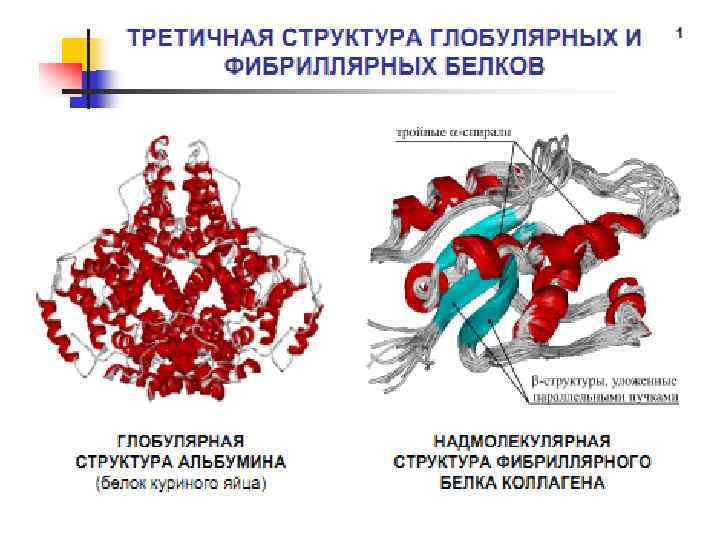
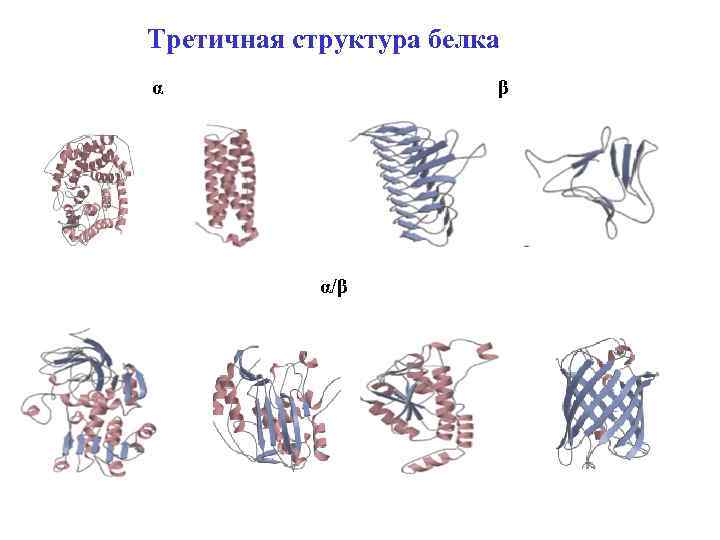
Третичная структура белка α β α/β

• Поддержанию третичной структуры белка способствуют гидрофобные связи, которые образуются внутри молекулы. В образовании этих связей принимают участие неполярные радикалы аминокислот. • У белка, имеющего третичную структуру, на поверхности молекулы формируется участок, который может присоединять к себе другие молекулы, называемые лигандами. (низкомолекулярные орг. и неорганич. молекулы, макромолекулы – ДНК, РНК, полисахариды, белки. Белок узнает определенный участок лиганда, комплементарный центру связывания). • Этот участок называется активный центр и формируется из радикалов аминокислот, которые сближаются друг с другом при формировании третичной структуры. • Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра структуре лиганда.
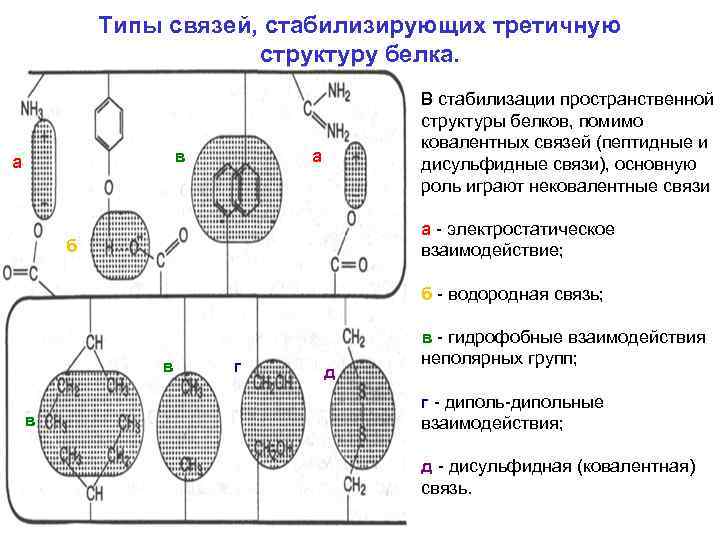
Типы связей, стабилизирующих третичную структуру белка. в а В стабилизации пространственной структуры белков, помимо ковалентных связей (пептидные и дисульфидные связи), основную роль играют нековалентные связи а электростатическое взаимодействие; а б б водородная связь; в в г д в гидрофобные взаимодействия неполярных групп; г дипольные взаимодействия; д дисульфидная (ковалентная) связь.
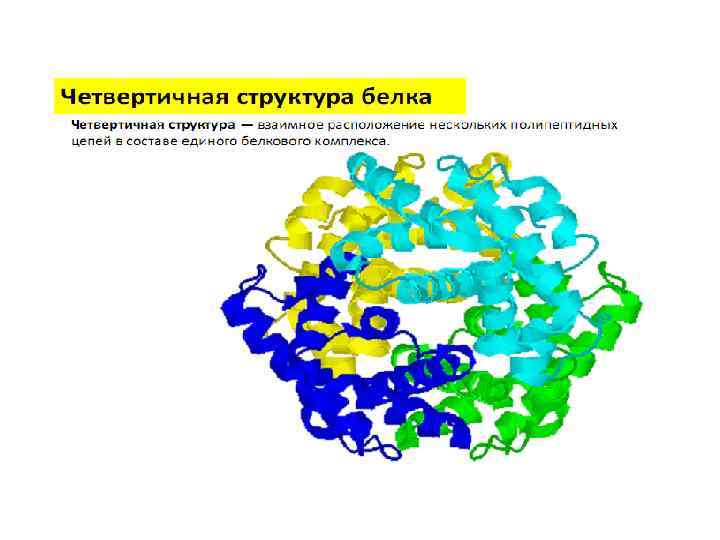
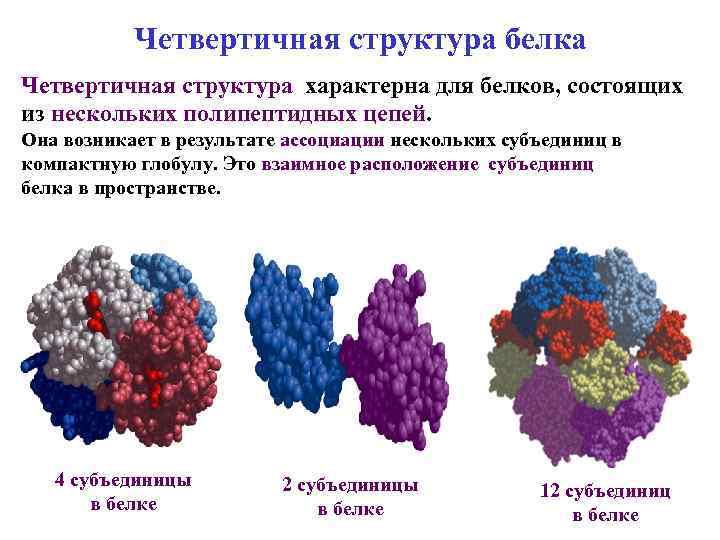
Четвертичная структура белка Четвертичная структура характерна для белков, состоящих из нескольких полипептидных цепей. Она возникает в результате ассоциации нескольких субъединиц в компактную глобулу. Это взаимное расположение субъединиц белка в пространстве. 4 субъединицы в белке 2 субъединицы в белке 12 субъединиц в белке

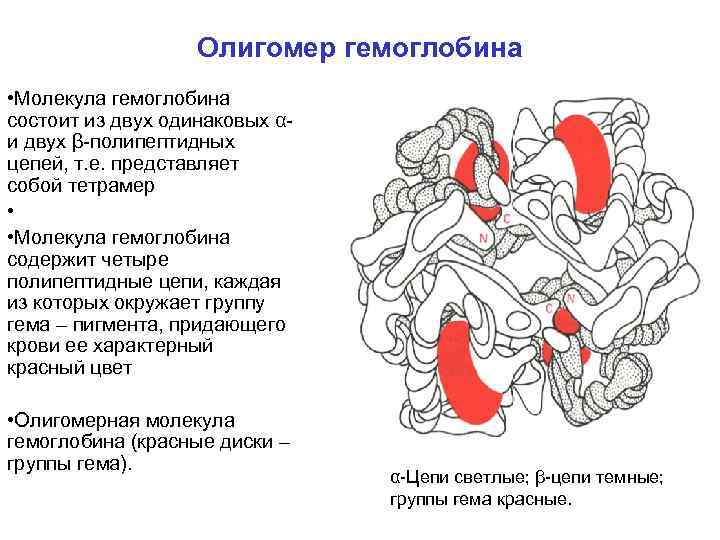
Олигомер гемоглобина • Молекула гемоглобина состоит из двух одинаковых α и двух β полипептидных цепей, т. е. представляет собой тетрамер • • Молекула гемоглобина содержит четыре полипептидные цепи, каждая из которых окружает группу гема – пигмента, придающего крови ее характерный красный цвет • Олигомерная молекула гемоглобина (красные диски – группы гема). α Цепи светлые; β цепи темные; группы гема красные.

• Белки с четвертичной структурой называются олигомерными, а составляющие их индивидуальные полипептидные цепи — субъединицами протомерами или мономерами. • Такие соединения стабилизируются водородными связями и электростатическими взаимодействиями между АК остатками, расположенными на поверхности протомеров. • Преимущества белков с четвертичной структурой: • 1) экономия генетического материала; • 2) уменьшение числа ошибок при синтезе белка; • 3) качественное разнообразие белков — появление у белков новых функций.

Образование четвертичной структуры глобулярного белка

Folding белков. Белки синтезируются в рибосомах в виде длинной полипептидной нити, но затем быстро сворачиваются в свою естественную ( «нативную» ) пространственную структуру. Этот процесс называется фолдинг белка
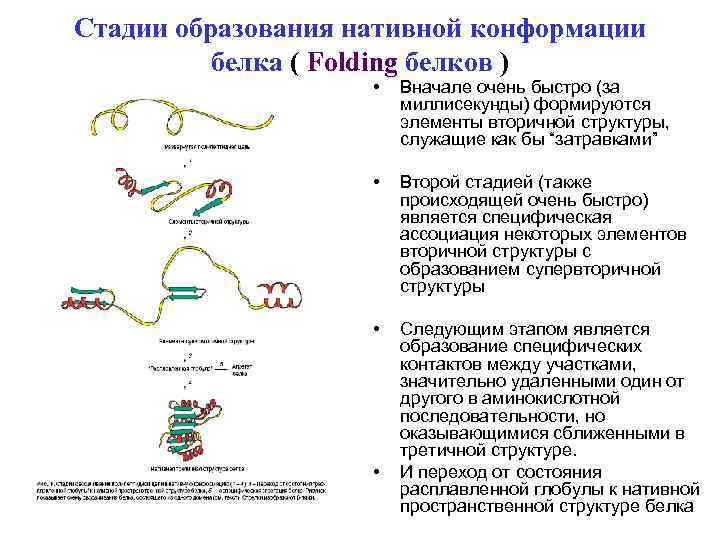
Стадии образования нативной конформации белка ( Folding белков ) • Вначале очень быстро (за миллисекунды) формируются элементы вторичной структуры, служащие как бы “затравками” • Второй стадией (также происходящей очень быстро) является специфическая ассоциация некоторых элементов вторичной структуры с образованием супервторичной структуры • Следующим этапом является образование специфических контактов между участками, значительно удаленными один от другого в аминокислотной последовательности, но оказывающимися сближенными в третичной структуре. И переход от состояния расплавленной глобулы к нативной пространственной структуре белка •

• В фолдинге участвуют белки - шапероны. И хотя большинство только что синтезированных белков могут сворачиваться и при отсутствии шаперонов, некоторому меньшинству обязательно требуется их присутствие

Шапероны.

Шаперо ны, функции • Шаперо ны — класс белков, главная функция которых состоит в восстановлении правильной третичной структуры повреждённых белков, а также образование и диссоциация белковых комплексов. • Многие шапероны являются белками теплового шока, то есть белками, экспрессия которых начинается в ответ на рост температуры или другие клеточные стрессы. • Тепло сильно влияет на фолдинг белка, а некоторые шапероны участвуют в исправлении потенциального вреда, который возникает из за неправильного сворачивания белков. • Другие продолжают обнаруживаться новые функции шаперонов, например, участие в разрушении белка, и в реакциях на заболевания, связанные с агрегацией белков (например, прион).
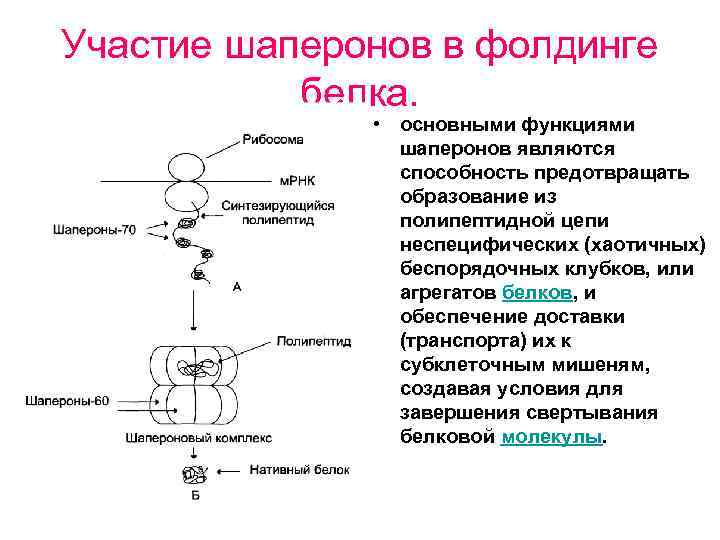
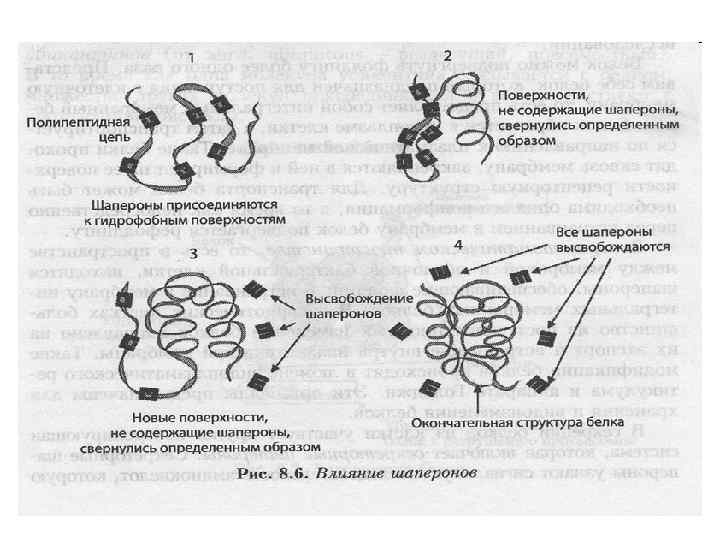
Участие шаперонов в фолдинге белка. • основными функциями шаперонов являются способность предотвращать образование из полипептидной цепи неспецифических (хаотичных) беспорядочных клубков, или агрегатов белков, и обеспечение доставки (транспорта) их к субклеточным мишеням, создавая условия для завершения свертывания белковой молекулы.
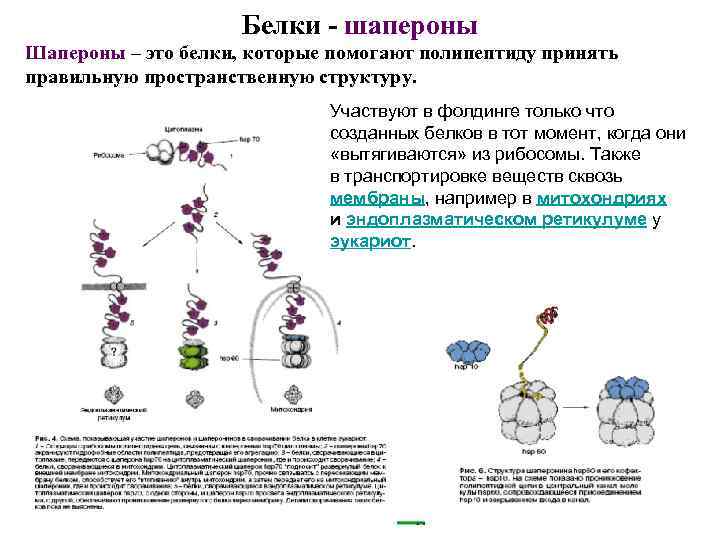
Белки - шапероны Шапероны – это белки, которые помогают полипептиду принять правильную пространственную структуру. Участвуют в фолдинге только что созданных белков в тот момент, когда они «вытягиваются» из рибосомы. Также в транспортировке веществ сквозь мембраны, например в митохондриях и эндоплазматическом ретикулуме у эукариот.

Фолдинг белка. Шапероны. • Аминокислотная последовательность не является единственным фактором, определяющим форму белковой молекулы. • В клетке существуют специальные молекулы, которые активно участвуют в фолдинге белков. • В совокупности молекулы, участвующие в фолдинге белков, называют регуляторами фолдинга, среди которых выделяют несколько типов. • Молекулы, ускоряющие фолдинг, называются катализаторами фолдинга. • Молекулы, служащие для изменения формы белка, — шаперонами фолдинга.

Фолдинг белка. Шапероны. • Существует четыре типа молекул, которые играют роль таких шаперонов. • 1. Молекулы, обеспечивающие правильный фолдинг белков (фолдинг-шапероны — folding chaperones). • 2. Молекулы, созданные для удержания частично свернутой молекулы белка в определенном положении. Это необходимо, чтобы система имела возможность закончить фолдинг (удерживающие шапероны — holding chaperones). • 3. Шапероны, разворачивающие белки с неправильной формой (дезагрегирующие шапероны — disaggregating chaperones). • 4. Шапероны, сопровождающие белки, транспортируемые через клеточную мембрану (секреторные шапероны — secretory chaperons).

Фолдинг шапероны. • • Внутри клетки содержится большое количество воды. Молекулы, находящиеся в ней, обычно заряжены, то есть являются гидрофильными. Незаряженные молекулы гидрофобны. В длинной, линейной последовательности белка имеются гидрофильные участки, а также гидрофобные области. В водной среде клетки гидрофобные поверхности белка стремятся оказаться внутри белковой молекулы, выставляя гидрофильные участки наружу, где они могут взаимодействовать с молекулами воды. Функция небольших молекул фолдинг шаперонов заключается во взаимодействии с гидрофобными поверхностями белка, заряжая их или, напротив, прикрывая заряженные области, что позволяет белку принять правильную форму. Путем добавления и удаления этих молекул клетка определяет, когда и каким образом гидрофобный участок белка окажется внутри белковой молекулы. Тем самым определяется форма белка.

Удерживающие шапероны • Удерживающие шапероны связываются с белками, играя роль своеобразного резервуара этих белков до тех пор, пока фолдинг шапероны не освобождаются и не начинают работу с этими белками. • Удерживающие шапероны поддерживают белки в условиях химического и теплового напряжения до тех пор, пока условия внутри клетки не станут более благоприятными для правильного фолдинга белка. • Это один из механизмов, который использует клетка для предотвращения неправильного фолдинга.

Дезагрегирующие шапероны • Дезагрегирующие шапероны осуществляют рефолдинг белков, фолдинг которых был выполнен неправильно. • Они осуществляют в клетке важную контролирующую функцию по сбору и утилизации вторичного сырья. • Несмотря на существование этих механизмов, определенный процент клеточных белков все же попадает в мусорную кучу, то есть образует нерастворимые включения.

Секреторные шапероны. • В секреции белков из клетки участвует другая контролирующая система, которая включает секреторные шапероны. • Секреторные шапероны узнают сигнальную последовательность аминокислот, которую соответственно называют секреторной последовательностью. • Эта последовательность связывается с секреторным шапероном, шаперон поступает внутрь мембраны, обеспечивая экспорт белка вместе с собой.

Пострансляционная модификация белков Вновь синтезированный белок или полипептид не всегда функционально активны и требуют дополнительных преобразований, включающих: • Фолдинг молекул. • Образование дисульфидных мостиков между остатками цистеина. • Частичный протеолиз. • Присоединение простетической группы. Сборка протомеров в олигомерный белок. • Модификацию аминокислотных остатков: фосфорилирование, гидроксилирование и другие реакции.

Деградация белков – убиквитиновый сигнальный путь Белок выполняет закреплённую за ним функцию, а затем, в определённый момент, клетке необходимо от него избавиться. Последнее обусловлено рядом причин: во - первых, дальнейшая активность белка может навредить клетке, во - вторых, нужно синтезировать новые белки, а перегрузка цитоплазмы полипептидами является источником апоптоза. Внутриклеточную деградацию белков долгое время считали неспецифическим случайным процессом. Настоящим прорывом в данной области послужило открытие убиквитинового сигнального пути. В рамках этого пути деградации белка, которая осуществляется крупным белковым комплексом протеосомой, предшествует присоединение к белку «цепочки» молекул небольшого пептида убиквитина.

Полиубиквитиновая цепочка навешивается в строго определённый момент и является сигналом, свидетельствующим о том, что данный белок подлежит деградации. Аминокислота, по остатку которой убиквитин связывается с белками – лизин. Теперь ясно, что процесс внутриклеточного протеолиза жестко регулируется и чрезвычайно важен для множества базальных клеточных функций. Среди субстратов специфического протеолиза : регуляторы клеточного цикла, компоненты различных сигнальных путей, а также мутантные белки и белки, поврежденные посттрансляционно.

Прионы (от англ. proteinaceous infectious particles — белковые заразные частицы) • Белковые заразные частицы — особый класс инфекционных агентов, чисто белковых, не содержащих нуклеиновых кислот, вызывающих тяжёлые заболевания центральной нервной системы у человека и ряда высших животных (т. н. «медленные инфекции» ). • Прионный белок, обладающий аномальной трёхмерной структурой, способен прямо катализировать структурное превращение гомологичного ему нормального клеточного белка в себе подобный (прионный), присоединяясь к белкумишени и изменяя его конформацию. Как правило, прионное состояние белка характеризуется переходом α-спиралей белка в β-слои. • Прионы — единственные инфекционные агенты, размножение которых происходит без участия нуклеиновых кислот.
4. Уровни структ.организации белк.молекул1.ppt