7e455551f2bbd503c4a02876ec211f37.ppt
- Количество слайдов: 24
 Урок химии в 8 классе Учитель Серова И. А. МОУ лицей № 6
Урок химии в 8 классе Учитель Серова И. А. МОУ лицей № 6
 ТЕМА УРОКА: Упражнения в вычислениях с использованием физических величин «количество вещества» и «молярная масса»
ТЕМА УРОКА: Упражнения в вычислениях с использованием физических величин «количество вещества» и «молярная масса»
 Цель урока: Научиться решать задачи данного типа по алгоритму.
Цель урока: Научиться решать задачи данного типа по алгоритму.
 План урока 1. Актуализация знаний о количестве вещества, молярной массе, молярном объеме 2. Разбор алгоритма решения типовых задач с помощью учебного электронного издания «Виртуальная лаборатория» 3. Самостоятельное решение задач 4. Проверка результатов
План урока 1. Актуализация знаний о количестве вещества, молярной массе, молярном объеме 2. Разбор алгоритма решения типовых задач с помощью учебного электронного издания «Виртуальная лаборатория» 3. Самостоятельное решение задач 4. Проверка результатов
 Количество вещества - число молекул, атомов, ионов и других специфических структурных элементов, из которых состоит вещество. ٧ =m/M= N/NA
Количество вещества - число молекул, атомов, ионов и других специфических структурных элементов, из которых состоит вещество. ٧ =m/M= N/NA
 Моль - единица количества вещества, в 1 моле содержится 6. 02× 1023 (атомов, молекул, ионов и других частиц или их специфических групп). частиц
Моль - единица количества вещества, в 1 моле содержится 6. 02× 1023 (атомов, молекул, ионов и других частиц или их специфических групп). частиц
 Молярная масса вещества — масса одного моль вещества. Она равна отношению массы вещества к соответствующему количеству вещества
Молярная масса вещества — масса одного моль вещества. Она равна отношению массы вещества к соответствующему количеству вещества
 Число Авогадро, 6. 0 константа Авогадро — физическая константа, численно равная количеству специфицированных структурных единиц (атомов, молекул, ионов, электронов или любых других частиц) в 1 моле вещества. 2× 1 0 23
Число Авогадро, 6. 0 константа Авогадро — физическая константа, численно равная количеству специфицированных структурных единиц (атомов, молекул, ионов, электронов или любых других частиц) в 1 моле вещества. 2× 1 0 23
 Молярный объём — объём одного моля вещества, величина, получающаяся от деления молярной массы на плотность. Характеризует плотность упаковки молекул.
Молярный объём — объём одного моля вещества, величина, получающаяся от деления молярной массы на плотность. Характеризует плотность упаковки молекул.
 «Химия (8 -11 класс). Виртуальная лаборатория»
«Химия (8 -11 класс). Виртуальная лаборатория»
 Алгоритм вычисления объема вещества по известной массе Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите объем, занимаемый при н. у. углекислым газом массой 22 г 2. Запишите условие с помощью общепринятых обозначений ДАНО: m(СО 2)=22 г н. у. V(СО 2) - ? 3. Определите молярную массу вещества M(СО 2) = 44 г/моль 4. Определите количество вещества ٧ (СО 2) = 22/44 = 0, 5 моль 5. Определите объем вещества V(CО 2) = 22, 4 л/моль*0, 5 моль = 44, 8 л 6. Запишите ответ Ответ: 11, 2 л
Алгоритм вычисления объема вещества по известной массе Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите объем, занимаемый при н. у. углекислым газом массой 22 г 2. Запишите условие с помощью общепринятых обозначений ДАНО: m(СО 2)=22 г н. у. V(СО 2) - ? 3. Определите молярную массу вещества M(СО 2) = 44 г/моль 4. Определите количество вещества ٧ (СО 2) = 22/44 = 0, 5 моль 5. Определите объем вещества V(CО 2) = 22, 4 л/моль*0, 5 моль = 44, 8 л 6. Запишите ответ Ответ: 11, 2 л
 Алгоритм вычисления массы вещества по известному объему Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите массу 5, 6 л аммиака ( н. у. ) и число атомов водорода в нем ДАНО: V(NH 3) = 5, 6 л m (NH 3) - ? N(H)-? 2. Запишите условие с помощью общепринятых обозначений 3. Определите молярную массу вещества M(NH 3) = 17 г/моль 4. Определите количество вещества ٧ (NH 3) = 5, 6 л/22, 4 л/моль = 0, 25 моль m(NH 3) = 17 г/моль*0, 25 моль = 4, 25 г N(H)=3 N (NH 3) =3 NA * ٧ (NH 3) =3*6, 02*1023 5. Определите массу вещества 6. Рассчитайте число водорода в данном количестве вещества 7. Запишите ответ *0, 25=4, 5*1023 Ответ: m(NH 3) =4, 25 г; N(H)=4, 5*1023
Алгоритм вычисления массы вещества по известному объему Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите массу 5, 6 л аммиака ( н. у. ) и число атомов водорода в нем ДАНО: V(NH 3) = 5, 6 л m (NH 3) - ? N(H)-? 2. Запишите условие с помощью общепринятых обозначений 3. Определите молярную массу вещества M(NH 3) = 17 г/моль 4. Определите количество вещества ٧ (NH 3) = 5, 6 л/22, 4 л/моль = 0, 25 моль m(NH 3) = 17 г/моль*0, 25 моль = 4, 25 г N(H)=3 N (NH 3) =3 NA * ٧ (NH 3) =3*6, 02*1023 5. Определите массу вещества 6. Рассчитайте число водорода в данном количестве вещества 7. Запишите ответ *0, 25=4, 5*1023 Ответ: m(NH 3) =4, 25 г; N(H)=4, 5*1023
 Алгоритм вычисления массы вещества по известному числу частиц ( молекул) Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите массу одной молекулы школьного мела ДАНО: N(Ca. CO 3) =1. m(Ca. CO 3 ) - ? 2. Запишите условие с помощью общепринятых обозначений 3. Определите молярную массу вещества M(Ca. CO 3 )= 100 г/моль 4. Определите количество вещества ٧ = N/NA= 1 / 6, 02*1023 5. Определите массу 1 молекулы 6. Рассчитайте число водорода в данном количестве вещества 7. Запишите ответ m = M/NA = 1 / 6, 02*1023 = 16, 6*10 -23 Ответ: m 1 молекулы - 16, 6*10 -23
Алгоритм вычисления массы вещества по известному числу частиц ( молекул) Последовательность действий Примеры выполнения 1. Прочитайте текст задачи Определите массу одной молекулы школьного мела ДАНО: N(Ca. CO 3) =1. m(Ca. CO 3 ) - ? 2. Запишите условие с помощью общепринятых обозначений 3. Определите молярную массу вещества M(Ca. CO 3 )= 100 г/моль 4. Определите количество вещества ٧ = N/NA= 1 / 6, 02*1023 5. Определите массу 1 молекулы 6. Рассчитайте число водорода в данном количестве вещества 7. Запишите ответ m = M/NA = 1 / 6, 02*1023 = 16, 6*10 -23 Ответ: m 1 молекулы - 16, 6*10 -23
 Проверь ответ! Задача № 1. Ответ: 18 г Задача № 2. Ответ: N(H)=6, 02*1023 , N(O) =3, 01*1023 Задача № 3. Ответ: 7, 1 г Задача № 4. Ответ: 4, 48 л Задача № 5. Ответ: 44, 8 л Задача № 6. Ответ: 11, 2 л
Проверь ответ! Задача № 1. Ответ: 18 г Задача № 2. Ответ: N(H)=6, 02*1023 , N(O) =3, 01*1023 Задача № 3. Ответ: 7, 1 г Задача № 4. Ответ: 4, 48 л Задача № 5. Ответ: 44, 8 л Задача № 6. Ответ: 11, 2 л
 Всё верно? Отличный результат !
Всё верно? Отличный результат !
 Допустил ошибку? Проверь решение.
Допустил ошибку? Проверь решение.
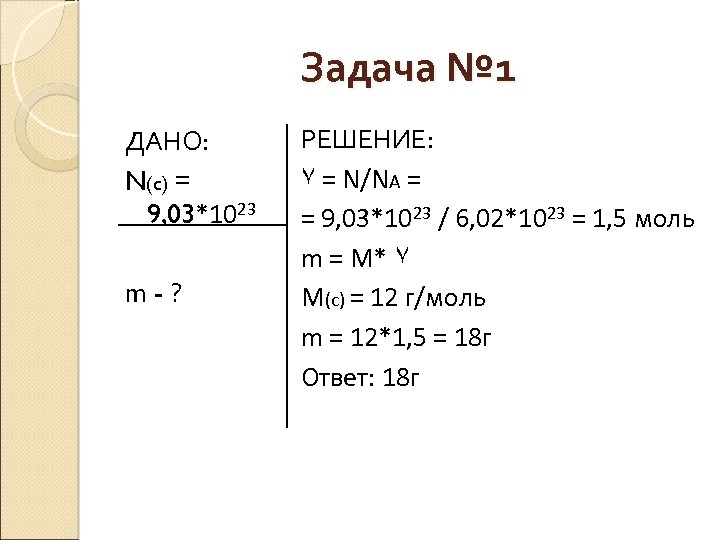 Задача № 1 ДАНО: N(c) = 9, 03*1023 m-? РЕШЕНИЕ: ٧ = N/NA = = 9, 03*1023 / 6, 02*1023 = 1, 5 моль m = M* ٧ M(c) = 12 г/моль m = 12*1, 5 = 18 г Ответ: 18 г
Задача № 1 ДАНО: N(c) = 9, 03*1023 m-? РЕШЕНИЕ: ٧ = N/NA = = 9, 03*1023 / 6, 02*1023 = 1, 5 моль m = M* ٧ M(c) = 12 г/моль m = 12*1, 5 = 18 г Ответ: 18 г
 Задача № 2 ДАНО: m(H 2 O) = 9 г РЕШЕНИЕ: ٧ (H 2 O) = m/M M(H 2 O) = 18 г/моль N(H) - ? ٧ = 9/18 = 0, 5 моль N(O) - ? в одной молекуле H 2 O – 1 атом O. N(O) = 6, 2*1023 * 0, 5 моль = 3, 01*1023 в одной молекуле H 2 O – 2 атома H. N(H) = 6, 02*1023*0, 5*2 = 6, 02*1023 Ответ: N(O) = 3, 01*1023 N(H) = 6, 02*1023
Задача № 2 ДАНО: m(H 2 O) = 9 г РЕШЕНИЕ: ٧ (H 2 O) = m/M M(H 2 O) = 18 г/моль N(H) - ? ٧ = 9/18 = 0, 5 моль N(O) - ? в одной молекуле H 2 O – 1 атом O. N(O) = 6, 2*1023 * 0, 5 моль = 3, 01*1023 в одной молекуле H 2 O – 2 атома H. N(H) = 6, 02*1023*0, 5*2 = 6, 02*1023 Ответ: N(O) = 3, 01*1023 N(H) = 6, 02*1023
 Задача № 3 ДАНО: V(CH 4) = 10 л m(CH 4) - ? РЕШЕНИЕ: ٧=V/VM ٧(CH 4) = 10/22, 4 = 0, 446 моль m = ٧ *M M(CH 4) = 16 г/моль m = 16*0, 446 =7, 1 г Ответ: 7, 1 г
Задача № 3 ДАНО: V(CH 4) = 10 л m(CH 4) - ? РЕШЕНИЕ: ٧=V/VM ٧(CH 4) = 10/22, 4 = 0, 446 моль m = ٧ *M M(CH 4) = 16 г/моль m = 16*0, 446 =7, 1 г Ответ: 7, 1 г
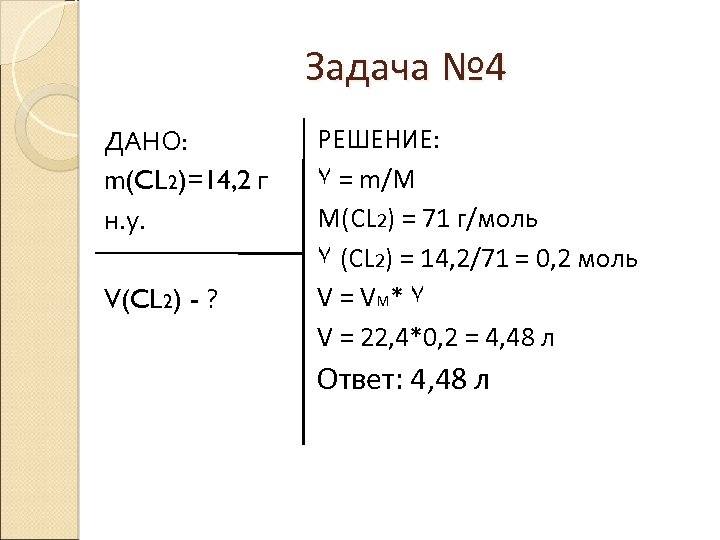 Задача № 4 ДАНО: m(CL 2)=14, 2 г н. у. V(CL 2) - ? РЕШЕНИЕ: ٧ = m/M M(CL 2) = 71 г/моль ٧ (CL 2) = 14, 2/71 = 0, 2 моль V = V M* ٧ V = 22, 4*0, 2 = 4, 48 л Ответ: 4, 48 л
Задача № 4 ДАНО: m(CL 2)=14, 2 г н. у. V(CL 2) - ? РЕШЕНИЕ: ٧ = m/M M(CL 2) = 71 г/моль ٧ (CL 2) = 14, 2/71 = 0, 2 моль V = V M* ٧ V = 22, 4*0, 2 = 4, 48 л Ответ: 4, 48 л
 Задача № 5 ДАНО: N(CL 2) =12, 04*1023 н. у. V(CL 2) - ? РЕШЕНИЕ: ٧ = N/NA ٧ (CL 2) = 12, 04*1023 /6, 02* 1023 = = 2 моль V = V M* ٧ V(CL 2) = 22, 4*2 = 44, 8 л Ответ: 44, 8 л
Задача № 5 ДАНО: N(CL 2) =12, 04*1023 н. у. V(CL 2) - ? РЕШЕНИЕ: ٧ = N/NA ٧ (CL 2) = 12, 04*1023 /6, 02* 1023 = = 2 моль V = V M* ٧ V(CL 2) = 22, 4*2 = 44, 8 л Ответ: 44, 8 л
 Задача № 6 ДАНО: m(HCL)=18, 25 г н. у. V(HCL) -? РЕШЕНИЕ: V = VM * ٧ ٧ = m/M ٧ (HCL) = 18, 25/36, 5 = 0, 5 моль V = 22, 4*0, 5 = 11, 2 л Ответ: 11, 2 л
Задача № 6 ДАНО: m(HCL)=18, 25 г н. у. V(HCL) -? РЕШЕНИЕ: V = VM * ٧ ٧ = m/M ٧ (HCL) = 18, 25/36, 5 = 0, 5 моль V = 22, 4*0, 5 = 11, 2 л Ответ: 11, 2 л

 Сайт для учителя «Я иду на урок химии» (URL: http: //him. 1 september. ru); Основы химии: образовательный сайт: (URL: http: //www. hemi. nsu. ru); Мир химии (URL: http: //chem. km. ru); Chem Net: портал фундаментального химического образования (URL: http: //www. chemnet. ru); Коллекция «Естественно-научные эксперименты» (URL: http: //experiment. edu. ru); Химия для всех: иллюстрированные материалы по общей, органической и неорганической химии (URL: http: //school-sector. relarn. ru/nsm); Химия для школьников (URL: http: //chemistry. r 2. ru); Школьная химия (URL: http: //schoolchemistry. by. ru); Электронная библиотека по химии и технике (URL: http: //rushim. ru/books. htm); Органическая химия: электронный учебник для средней школы (URL: http: //www. chemistry. ssu. samara. ru
Сайт для учителя «Я иду на урок химии» (URL: http: //him. 1 september. ru); Основы химии: образовательный сайт: (URL: http: //www. hemi. nsu. ru); Мир химии (URL: http: //chem. km. ru); Chem Net: портал фундаментального химического образования (URL: http: //www. chemnet. ru); Коллекция «Естественно-научные эксперименты» (URL: http: //experiment. edu. ru); Химия для всех: иллюстрированные материалы по общей, органической и неорганической химии (URL: http: //school-sector. relarn. ru/nsm); Химия для школьников (URL: http: //chemistry. r 2. ru); Школьная химия (URL: http: //schoolchemistry. by. ru); Электронная библиотека по химии и технике (URL: http: //rushim. ru/books. htm); Органическая химия: электронный учебник для средней школы (URL: http: //www. chemistry. ssu. samara. ru


