15386_СЕРА[1]..ppt
- Количество слайдов: 19

Урок СЕРА 2/17/2018 Аблямитова Татьяна Алексеевна Учитель первой кв. категории Гимназия № 139, г. Казань, Республика Татарстан педагогический стаж 19 лет 1

План урока Cера - химический элемент n ИСТОРИЯ СЕРЫ n Сера – простое вещество n ФИЗИЧЕСКИЕ СВОЙСТВА n Химические свойства n получение серы n Проверь себя n 2/17/2018 2
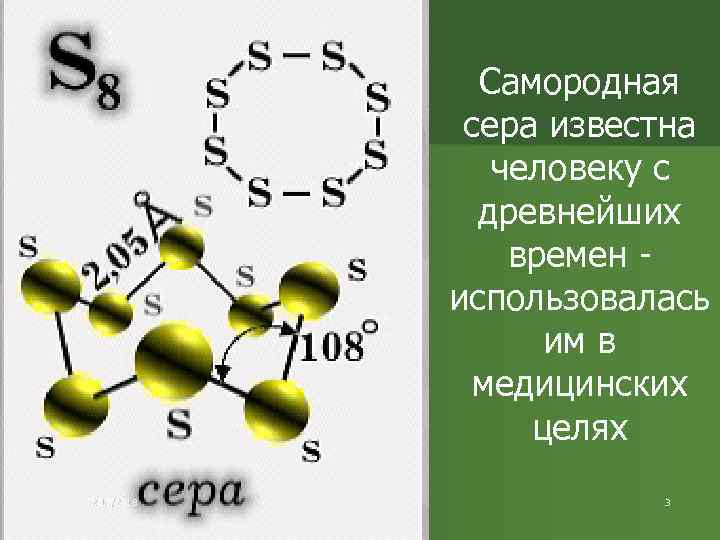
Самородная сера известна человеку с древнейших времен использовалась им в медицинских целях 2/17/2018 3

Cера - химический элемент Положение в ПСХЭ: порядковый номер 16, символ - S, период 3, ряд 3, VI группа, подгруппа главная n Электронная формула: 1 s 22 p 63 s 23 p 6 n Валентные возможности: II, IV, VI n Возможные степени окисления: -2, 0, +2, +4, +6. n 2/17/2018 4

ИСТОРИЯ СЕРЫ n n n 2/17/2018 Элементарную природу серы установил француз Антуан Лоран Лавуазье (по образованию юрист, а по призванию химик) в своих опытах по сжиганию. Древнерусское название "сера" употребляется очень давно. Оно происходит от санскритского слова "сира", что означает светло-желтый. Но есть и другое древнерусское название серы - "жупел" (сера горючая). 5

ИСТОРИЯ СЕРЫ n n Горючесть серы, легкость, с которой она соединяется с металлами, объясняют причину, почему ее считали "принципом горючести" и обязательной составной частью металлических руд. Наивное верование алхимиков о сере выражено в небольшом стихотворении Н. А. Михайловым: Семь металлов создал свет Медь, железо, серебро, По числу семи планет: Злато, олово, свинец. . . Дал нам Космос на добро Сын мой! сера им отец!. . 2/17/2018 6

ИСТОРИЯ СЕРЫ – Жрецы использовали ее в составе "священных курений" при некоторых религиозных обрядах. – Разные горючие смеси для военных целей также содержали серу. Еще у Гомера упоминаются "сернистые испарения" и смертельное действие продуктов горения серы. – Она входила в состав "греческого огня", наводившего ужас на противников. В 941 г. под стенами Царьграда был уничтожен флот киевского князя Игоря. – В летописном своде событий "Повесть временных лет", составленном в Киеве, так описан поход Игоря: "Словно молнию, которая на небе, греки имеют у себя и пускали ее, сжигая нас, поэтому мы и не одолели их". Дружинники князя защищались от "греческого огня" щитами, воловьими шкурами, но потерпели поражение. – Греки выбрасывали горящую смесь через медные трубы, установленные на бортах византийских кораблей. Состав этой смеси был неизвестен. Греки держали его в секрете. Предполагают, что в нее входили нефть, различные горючие масла, смола, селитра, клен, сера и вещества, которые 2/17/2018 7 окрашивали пламя.
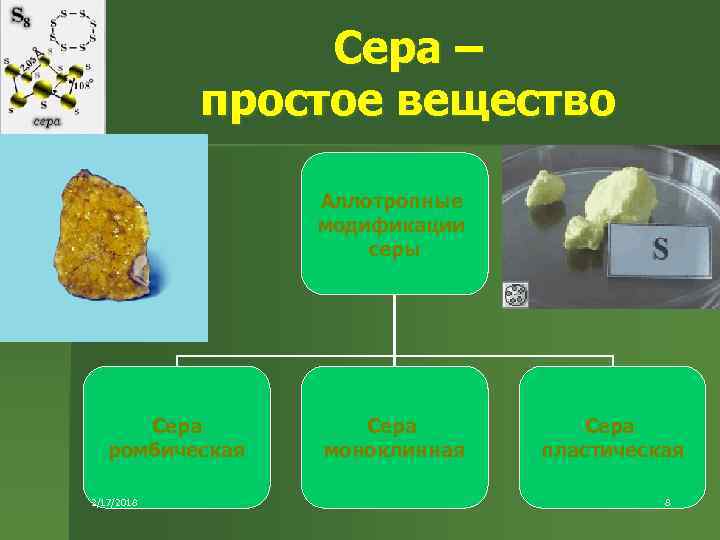
Сера – простое вещество Аллотропные модификации серы Сера ромбическая 2/17/2018 Сера моноклинная Сера пластическая 8

ФИЗИЧЕСКИЕ СВОЙСТВА n n n Сера совершенно не проводит тока и при трении заряжается отрицательным электричеством, поэтому из нее делают круги электрических машин, в которых электрический заряд возбуждается посредством трения. Сера очень плохо проводит тепло. Если в ней содержится менее 0, 1% примесей, то при согревании куска серы в руке слышится своеобразный треск, и случается, что кусок распадается на части. Это происходит из-за напряжений, возникающих в куске вследствие его неравномерного расширения в связи с малой теплопроводностью серы. 2/17/2018 9

ФИЗИЧЕСКИЕ СВОЙСТВА n n n Изменение состава молекул вызывает изменение окраски паров серы от оранжево-желтого до соломенно-желтого. Сера в обычных условиях имеет различный цвет Окраска этих веществ обусловлена способностью поглощать какую-то часть спектра белого света. В результате этого они окрашены в какой-нибудь дополнительный (к цвету поглощения лучей) цвет. Дополнительными, до белого цвета являются следующие пары цветовых сочетаний: красный - голубой, желтый - синий, зеленый - пурпурный и т. д. "Вычитание" какого-либо цвета из белого дает дополнительную окраску вещества. Так, ромбическая сера поглощает синий цвет, поэтому она окрашена в желтый, кристаллический моноклинный селен красного цвета, так как поглощает голубой. 2/17/2018 10

ФИЗИЧЕСКИЕ СВОЙСТВА n n Плавление серы происходит в интервале температур 112 -119, 3°С При этом с увеличением температуры до 155°С вязкость расплава уменьшается и возрастает в тысячи раз в интервале температур 155 -187°С. Затем снова наступает спад. С возрастанием температуры от 155 до 187°С, кольцевые молекулы Ss разрушаются и образуются другие - в виде длинных цепей из нескольких тысяч атомов. Вязкость расплава увеличивается. При t=300°С сера переходит в текучее состояние, а при t= 444, 6°С закипает. В зависимости от температуры в ее парах обнаруживают молекулы S 8, S 6, S 4, S 2. При 1760°С пары серы одноатомны. 2/17/2018 11

Химические свойства n n 1. С металлами При обычных условиях реагирует c щелочными металлами (со всеми): 2 Na + S Na 2 Sопыт щелочноземельными металлами (со всеми), медью, серебром, ртутью образуя сульфиды: Me + S Mex. Sy n При нагревании сера реагирует с другими металлами (Zn, Al, Fe) n и только золото (Au) не взаимодействует с ней ни при каких условиях

Химические свойства 2. С неметаллами § Взаимодействие с водородом при нагревании с образованием сероводорода: H 2 + S H 2 S Взаимодействие с кислородом: S + O 2 SO 2 сернистый газ, при его дальнейшем окислении: SO 2 + O 2 SO 3 серный газ § § из неметаллов с серой не реагируют только азот (N), йод (I)и благородные газы 2/17/2018 13

Химические свойства 2. С неметаллами n n n Взаимодействие с галогенами Известны галогениды серы, селена и теллура Например, хлорид или бромид серы получают при нагревании серы с галогенами в запаянной трубке: 2 S + Br 2 = S 2 Br 2 2 S+Cl 2 = S 2 Cl 2 Хлорид серы S 2 Cl 2 является хорошим растворителем многих химических соединений серы. В химической промышленности его используют в качестве растворителя серы при вулканизации каучука. Сера с водой и разбавленными кислотами не взаимодействует, в то время как теллур окисляется водой при температуре 100 -160°С: 2/17/2018 14 Те + 2 Н 2 О==Те. O 2 + 2 Н 2

Химические свойства 3. Со щелочами n Со щелочами сера взаимодействуют с образованием сульфидов и сульфитов (реакция обратимая): 3 S + 6 КОН = 2 К 2 S + К 2 SО 4 + ЗH 2 O 4. Демеркуризация Со ртутью сера вступает в реакцию в обычных условиях при простом соприкосновении веществ. Если в лаборатории разлили ртуть, ее сначала собирают, а те участки, где ртутные капли нельзя извлечь, засыпают порошкообразной серой. Происходит реакция с образованием безвредного сульфида ртути (II), или киновари: Hg+S=Hg. S 2/17/2018 15

Получение сульфидов из серы n n В школьных условиях можно легко получить сульфиды некоторых металлов, например Cu 2 S. Для этого в пробирку, закрепленную в штативе, вносят немного серы и нагревают ее до кипения. Затем щипцами вводят в пары серы предварительно подогретую полоску медной фольги. Медь энергично взаимодействует с серой: 2 Сu + S = Cu S 2/17/2018 16

Получение серы В промышленных условиях серу получают без подъема руды на поверхность: • путем выплавления из руды водяным паром • окислением сероводорода • восстановлением сернистого газа: 2 H 2 S + O 2 = 2 S + 2 H 2 O SO 2 + C = S + CO 2 SO 2 + 2 CО = S + 2 CO 2 2/17/2018 17

Проверим себя 1. Максимальная валентная возможность серы: а) II б) IV в) VI г) VIII 2. У атома серы число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно: А) 4 и +16 Б) 6 и +32 В) 6 и +16 Г) 4 и +32 3. С каким из А) Б) В) Г) 2/17/2018 металлов сера легче всего вступит в химическое взаимодействие? Cu Al Zn Na 18

литература http: //school-collection. edu. ru/ n http: //ru. wikipedia. org/wiki/%D 0%A 1 %D 0%B 5%D 1%80%D 0%B 0 n n Химия. 9 класс; учеб. для общеобразоват. учреждений/ О. С. Габриелян, -11 -е изд. , испр. - М. : Дрофа, 2006. – 267, с. : ил. 2/17/2018 19
15386_СЕРА[1]..ppt