Prezentatsia_nov.pptx
- Количество слайдов: 19

Урок обобщение знаний по теме: «Теория электролитической диссоциации» Устер Юлия Витальевна учитель химии I кв. категории МАОУ Лицей № 88 г. Екатеринбург

Цель урока: закрепить и углубить знания учащихся об основных понятиях теории электролитической диссоциации.

Задачи урока: 1. Рассмотреть различия между веществамиэлектролитами и неэлектролитами; 2. Дать определение понятию «электролитическая диссоциация» ; 3. Повторить основные понятия ТЭД; 4. Рассмотреть механизм процесса электролитической диссоциации; 5. Отработать запись уравнений диссоциации солей, кислот и оснований;

1. Положительнозаряженный электрод -- Гемфри Деви Майкл Фарадей …(анод). … 2. Отрицательнозаряженный электрод …(катод). … 3. Направленное движение заряженных частиц - …(электрический ток). частиц - … 4. Положительнозаряженные частицы -… …(катионы). . 5. Отрицательнозаряженные частицы -… …(анионы). 6. Вещества, водные растворы или расплавы которых проводят электрический ток -…(электролиты). электрический ток -… 7. Вещества, водные растворы или расплавы которых не не проводят расплавы которых проводят электрический ток -…(неэлектролиты). электрический ток -…. 8. Процесс распада электролита на ионы при растворении или расплавлении вещества -…(диссоциация). вещества -…
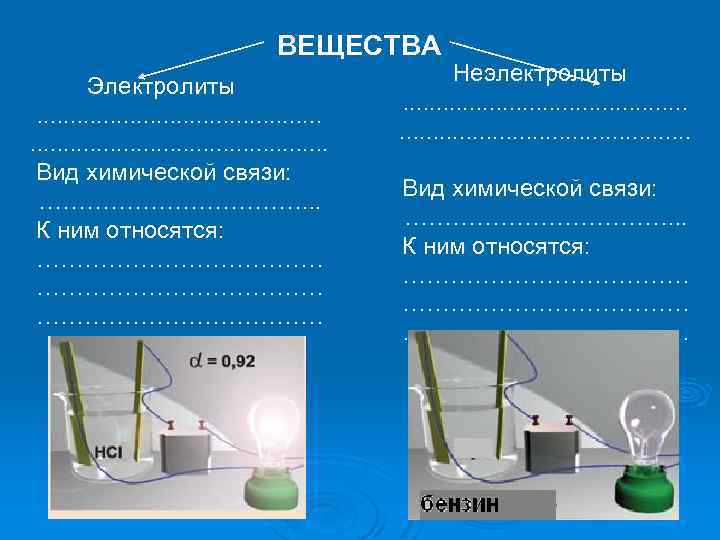
ВЕЩЕСТВА Электролиты. . . . . . Вид химической связи: ………………. . . К ним относятся: ……………………………… Неэлектролиты. . . . . . Вид химической связи: ………………. . . К ним относятся: ………………………………

ВЕЩЕСТВА Электролиты Неэлектролиты водные растворы и расплавы проводят эл. ток) водные растворы и расплавы не проводят эл. ток) Вид химической связи: ионная и ковалентная полярная связь К ним относятся: Кислоты, Основания, Соли Вид химической связи: ковалентная неполярная связь и слабополярная связь К ним относятся: Органические вещества, простые вещества, оксиды…

«Механизм электролитической диссоциации»
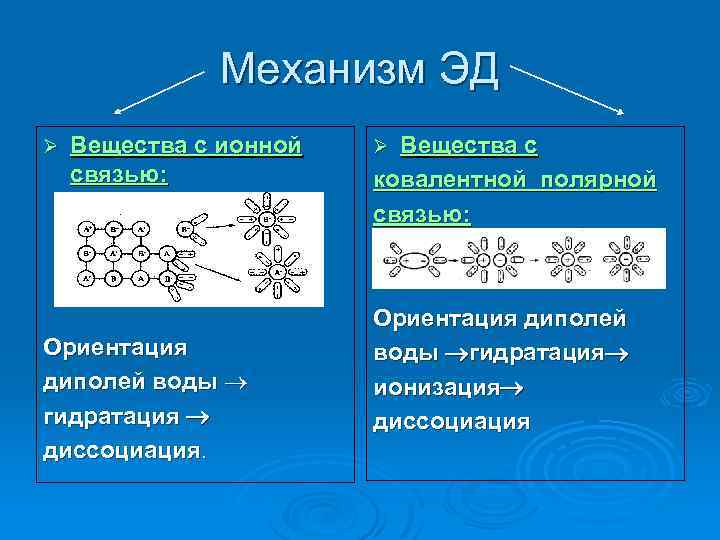
Механизм ЭД Ø Вещества с ионной связью: Ориентация диполей воды гидратация диссоциация. Вещества с ковалентной полярной связью: Ø Ориентация диполей воды гидратация ионизация диссоциация

Сванте Аррениус КОБЛУКОВ Иван Алексеевич Дмитрий Иванович Менделеев КИСТЯКОВСКИЙ Владимир Александрович

Основные положения ТЭД Вещества по их способности проводить ток в растворах делят на ? ? ? и ? ? ? ? . электролиты и неэлектролиты 2. В растворах электролиты диссоциируют (распадаются) на ? ? ? ? ? ? ? ? ? ? положительные и отрицательные ? ? ионы. 1.

Типы ионов 1) 2) 3) катионы По заряду: ? ? ? ? (положительные) и ? ? ? анионы (отрицательные); По отношению к воде: Гидратированные и негидратированные ( в безводных средах) По составу: простые ии ? ? ? ? сложные

Основные положения ТЭД Причиной диссоциации ? ? ? электролитов в водных растворах является его взаимодействие с молекулами воды , т. е. его ? ? ? ? гидратация 4. Под действием электрического тока положительные ионы (? ? ? ? катионы) движутся к катоду, а отрицательные (анионы- к аноду. ? ? ? ) 3.

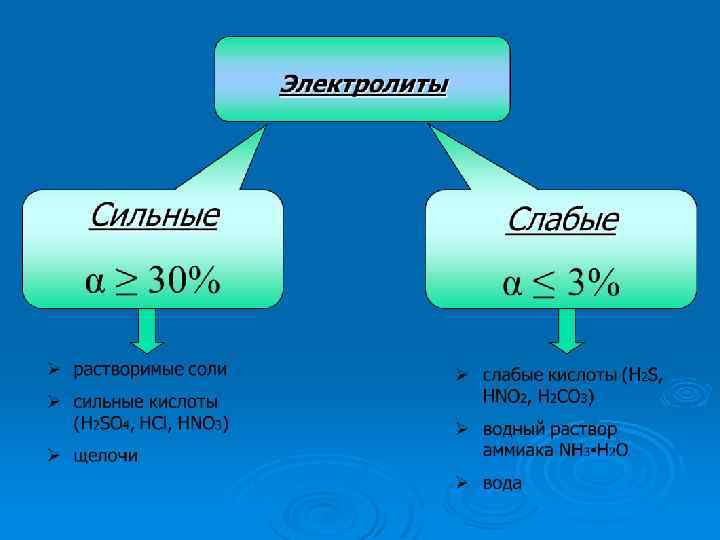
Основные положения ТЭД электролиты 5. Не все ? ? ? в одинаковой ионы мере диссоциируют на ? ? . ? = n / N, где n – число диссоциированных молекул, N – общее число молекул в растворе. Сильные 1 1. Соли ( растворимые). 1. ___________ 2. Основания, образованными 2. ___________ щелочными (Li-Fг) и щелочноземельными(Са-Rа) 3. ___________ металлами. 3. Неорганические кислоты (НNО 3, Диссоциация Н 2 SО 4, НСl, НВг, НI) обратима / необратима ? Диссоциация сильных электролитов необратима (=) =/ Слабые 0 1. ___________ 1. Гидроксиды металлов нерастворимые (Аl(ОН)3, Сr(ОН)3, Zn(ОН)2……. , 2. ___________ гидроксид аммония. 2. Вода. 3. ___________ 3. Органические кислоты и некоторые Диссоциация кислоты: НF, Н 2 S, неорганические Н 2 СО 3, НNО 2, Н 2 SО 3, НСN и др. обратима слабых электролитов Диссоциация / необратима ? является обратимой. ( ) =/

Основные положения ТЭД 6. Свойства растворов электролитов ионов определяются свойствами тех ? ? ? , которые они образуют при ? ? ? диссоциации. Электрол Характерные свойства иты ые общие Значение р. Н среды ионы Кислоты H+ р. Н < 7, изменяют цвет индикаторов Основани я Соли ОНОбщих ионов нет р. Н > 7 , изменяют цвет индикаторов Отсутствуют общие свойства обусловленные наличием общих ионов

Найдите ошибочные утверждения электролиты проводят электрический ток если вещество находится в сухом виде, оно ток не проводит 3. источником тока в растворе электролита являются электроны 4. катионы заряжены отрицательно, анионы положительно 5. растворы проводят ток из-за наличия в них положительных и отрицательных ионов 6. процесс взаимодействия воды с частицами вещества называется гидратацией 7. дистиллированная вода проводит ток 8. причиной диссоциации веществ в воде является особое строение молекулы воды. 9. все растворимые кислоты - сильные электролиты 10. все растворимые основания и соли - сильные электролиты 1. 2.

Мозговой штурм 1. Все металлы проводят электрический ток, следовательно, все металлы – электролиты? Ø 2. Если встать в лужу, в которой лежит оголенный провод, находящийся под напряжением, можно получить смертельный удар током. Следовательно, вода проводит электрический ток. Ø 3. В дистиллированной воде приготовили настой лечебных плодов (шиповника, черники, калины). Настой стал проводить электрический ток. Почему? Ø 4. При рентгеноскопии желудка пациенту дают выпить взвесь Ba. SO 4. Объясните, почему чистый Ba. SO 4 не вызывает отравлений, в то время как зафиксированы случаи со смертельным исходом применении Ba. SO 4 с примесями Ва. Сl 2. Ø

Домашнее задание - задание по карточкам

Спасибо за внимание! Урок окончен!
Prezentatsia_nov.pptx