54f04ebfd65c59cff573030662a6fcdc.ppt
- Количество слайдов: 18

Урок на тему «Галогены» 8 класс МБОУ СОШ № 141 углубленным изучением математики Учитель химии: Рахманина И. А.

"О сколько нам открытий чудных готовит просвещенья дух !“ А. С. Пушкин.

l. Мы изучим непременно, Элементы галогены (А по-русски – солероды), Все от фтора и до йода. Даже новенький астат Быть в семействе этом рад.

l Фамилия - химический знак элемента. l Адрес – местоположение в ПС (группа, подгруппа, период, порядковый номер). l Особенности внутреннего мира – строение его атома (заряд ядра, количество электронов, число энергетических уровней, возможные степени окисления и т. д. ).
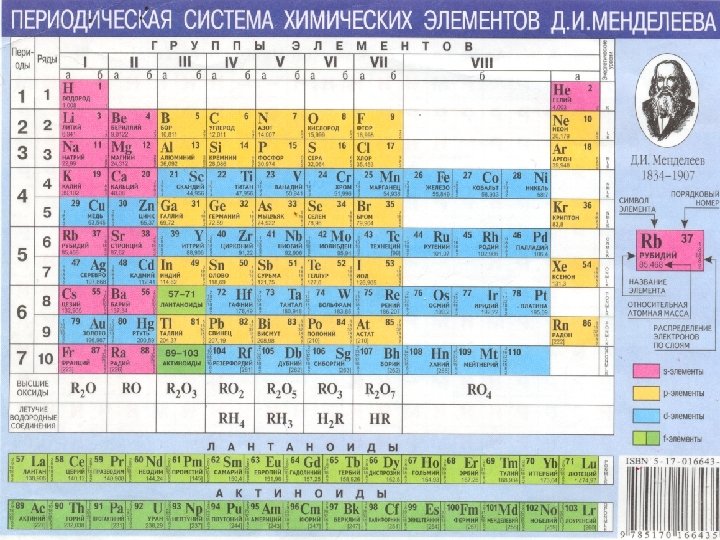

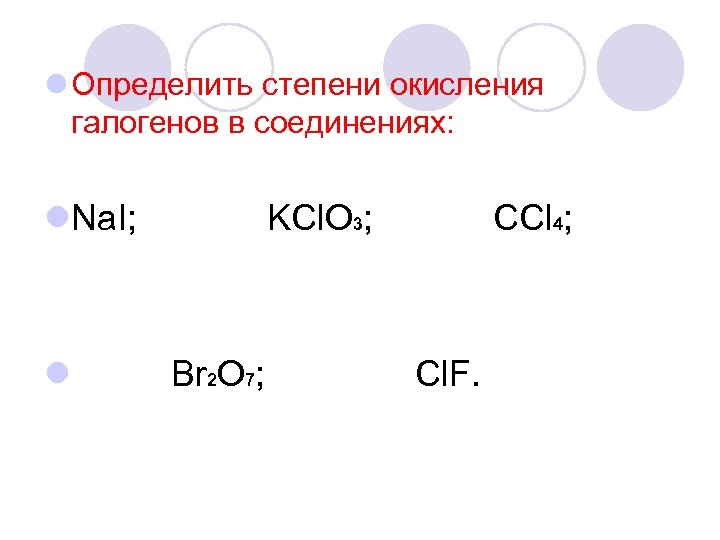
l Определить степени окисления галогенов в соединениях: l. Na. I; l KCl. O 3; Br 2 O 7; CCl 4; Cl. F.
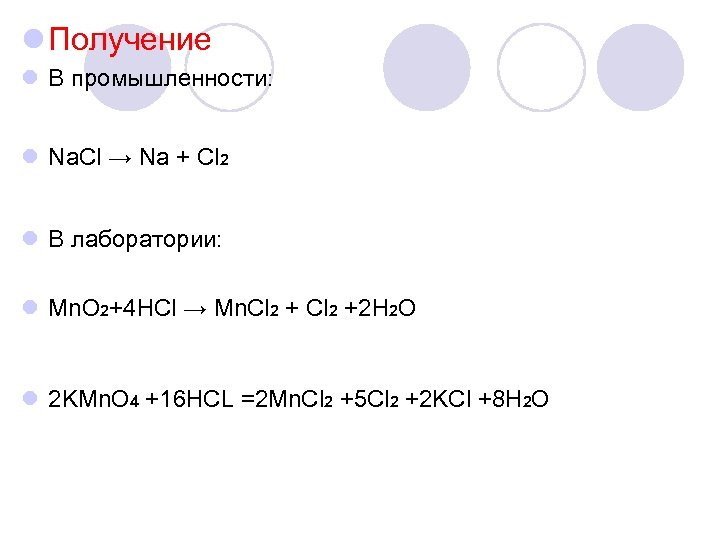
l Получение l В промышленности: l Na. Cl → Na + Cl 2 l В лаборатории: l Mn. O 2+4 HCl → Mn. Cl 2 +2 H 2 O l 2 KMn. O 4 +16 HCL =2 Mn. Cl 2 +5 Cl 2 +2 KCl +8 H 2 O

l Химические свойства l 1. С металлами: l Al + I 2 → Al. I 3
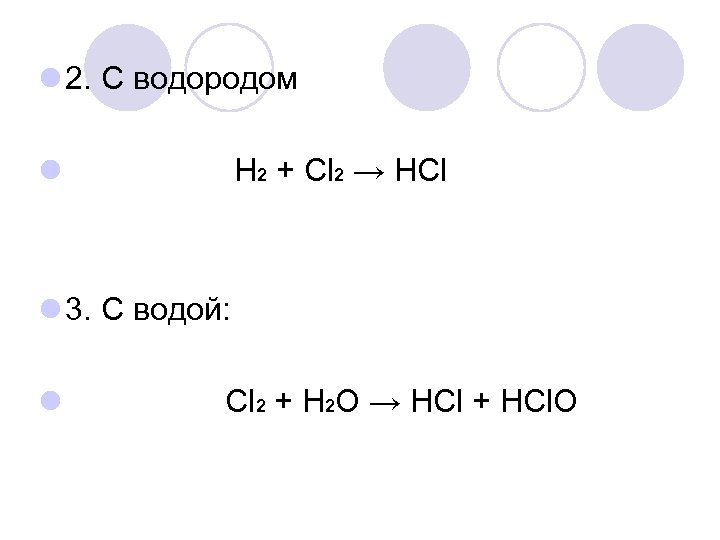
l 2. С водородом l Н 2 + Cl 2 → НСl l 3. С водой: l Cl 2 + H 2 O → HCl + HCl. O
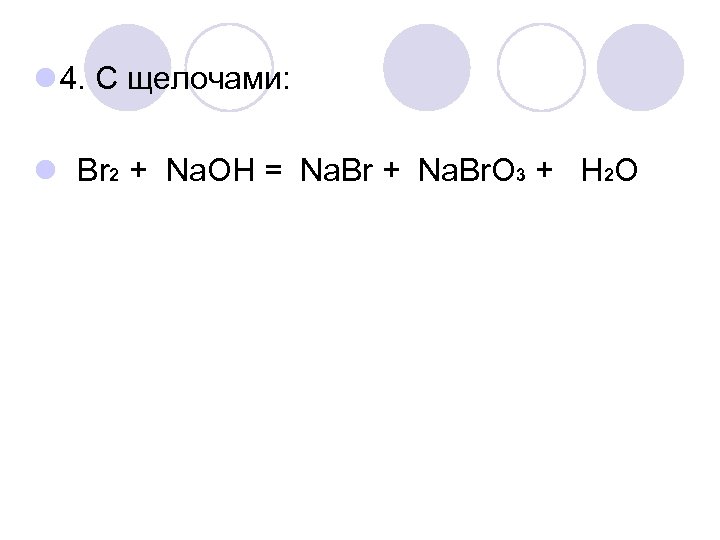
l 4. С щелочами: l Br 2 + Na. OH = Na. Br + Na. Br. O 3 + H 2 O

Хлор хвалился: “Нет мне равных!”, Галоген я самый главный. Зря болтать я не люблю: Все на свете отбелю!” Йод своей красой гордился, Твердым был, но испарился. Фиолетовый, как ночь, Далеко умчался прочь.

Бром разлился океаном, хоть зловонным, но - румяным, Бил себя он грозно в грудь: “Я ведь бром! Не кто-нибудь…”. Фтор молчал и думал: “Эх!. . Ведь приду – окислю всех …. ”
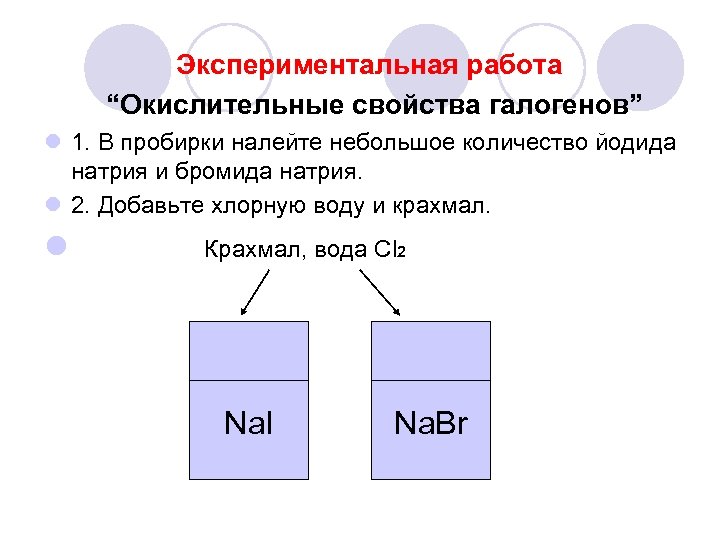
Экспериментальная работа “Окислительные свойства галогенов” l 1. В пробирки налейте небольшое количество йодида натрия и бромида натрия. l 2. Добавьте хлорную воду и крахмал. l Крахмал, вода Сl 2 ____________ Na. I Na. Br

l 3. Опишите наблюдаемые явления. l 4. Запишите уравнения реакции и составьте СЭБ. l Na. I + Cl 2 —> ……. l Na. Br + Cl 2 —> …… l 5. Сделайте вывод.
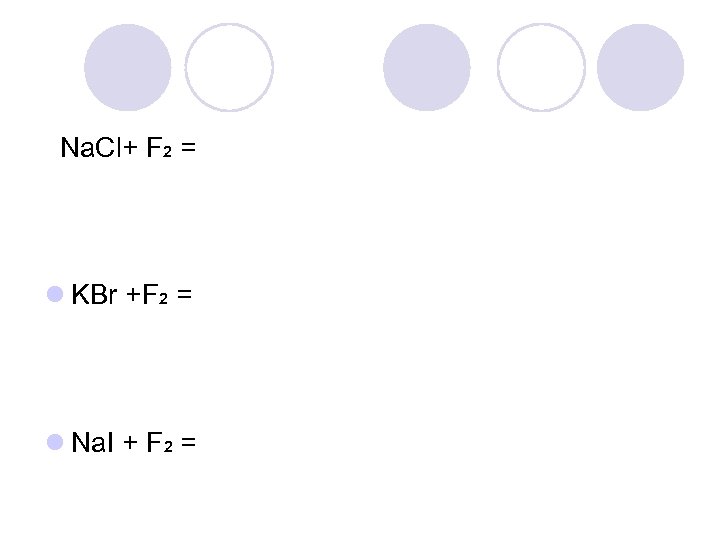
Na. Cl+ F 2 = l KBr +F 2 = l Na. I + F 2 =
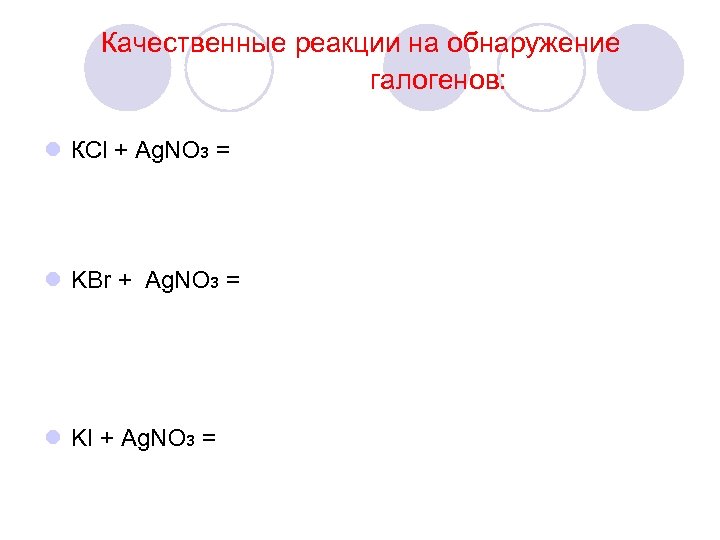
Качественные реакции на обнаружение галогенов: l КCl + Ag. NO 3 = l KBr + Ag. NO 3 = l KI + Ag. NO 3 =

Задание на дом l Составьте уравнения химических реакций, при помощи которых можно осуществить следующие превращения: Cl 2 → Cu. Cl 2→ Cu(OH)2→Cu. O→Cu. Cl 2 → Cu l Решить задачу: Хлороводород, который получили при взаимодействии избытка концентрированной серной кислоты с 58, 5 г хлорида натрия, растворили в 146 г воды. Определите массовую долю хлороводорода в процентах в полученном растворе.
54f04ebfd65c59cff573030662a6fcdc.ppt