 Урок 9 класса Углерод Металлы
Урок 9 класса Углерод Металлы
 Подготовка к ОГЭ: По четвергам в 410 в 17: 00 до 18: 30
Подготовка к ОГЭ: По четвергам в 410 в 17: 00 до 18: 30
 Металлы СО 2 – ангидрид угольной кислоты Н 2 СО 3. При растворении СО 2 в воде частично образуется угольная кислота: Равновесие наблюдается, поскольку угольная кислота очень слабая и в свободном виде неизвестна.
Металлы СО 2 – ангидрид угольной кислоты Н 2 СО 3. При растворении СО 2 в воде частично образуется угольная кислота: Равновесие наблюдается, поскольку угольная кислота очень слабая и в свободном виде неизвестна.
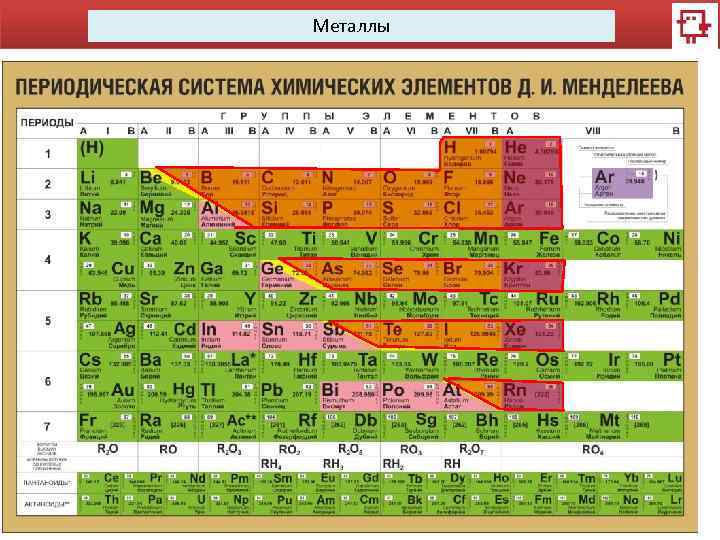
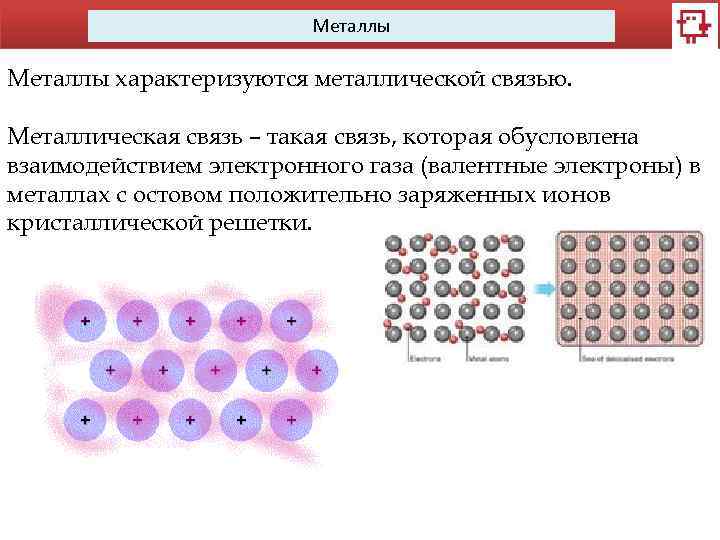 Металлы характеризуются металлической связью. Металлическая связь – такая связь, которая обусловлена взаимодействием электронного газа (валентные электроны) в металлах с остовом положительно заряженных ионов кристаллической решетки.
Металлы характеризуются металлической связью. Металлическая связь – такая связь, которая обусловлена взаимодействием электронного газа (валентные электроны) в металлах с остовом положительно заряженных ионов кристаллической решетки.
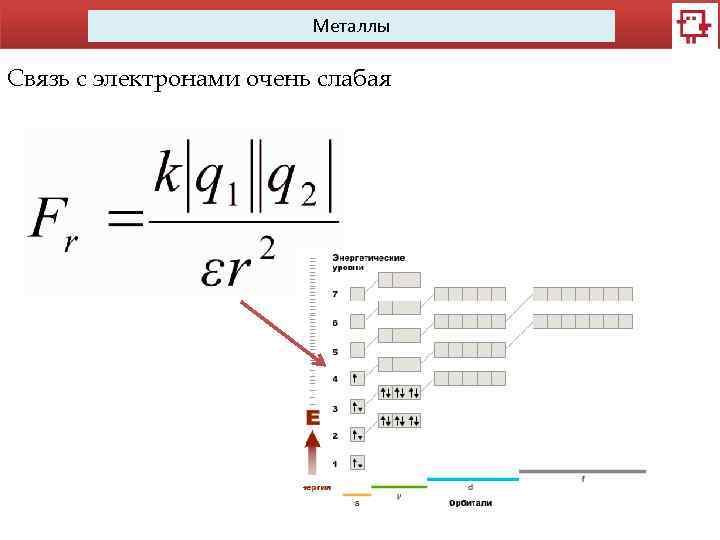 Металлы Связь с электронами очень слабая
Металлы Связь с электронами очень слабая
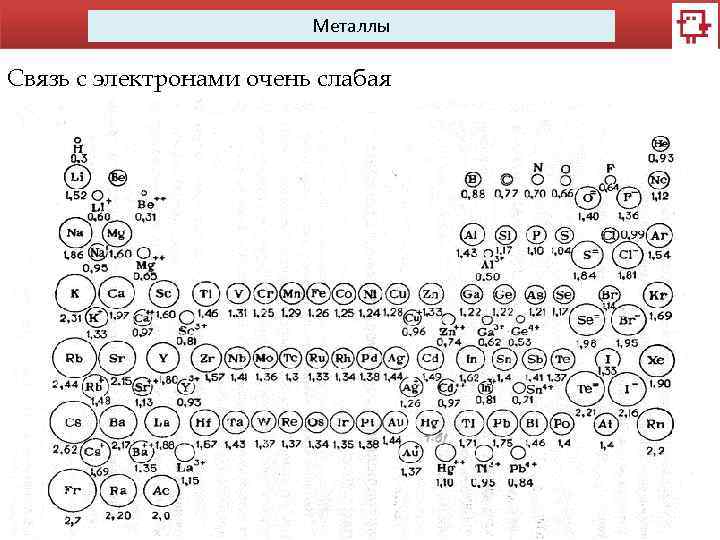 Металлы Связь с электронами очень слабая
Металлы Связь с электронами очень слабая
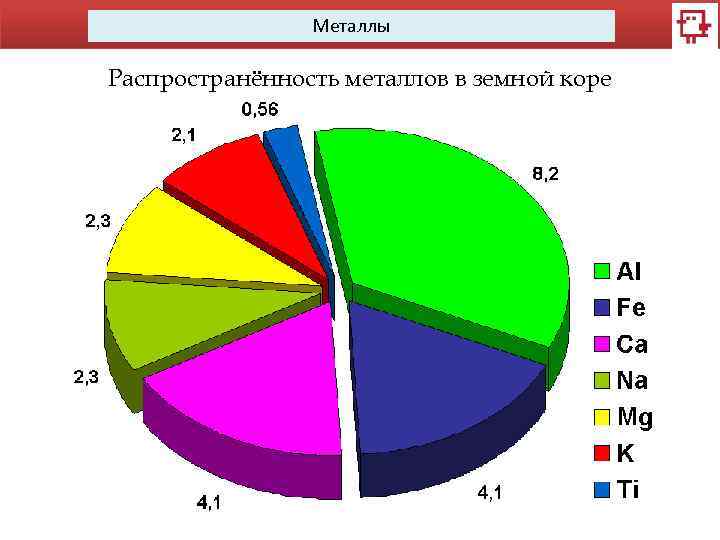 Металлы Распространённость металлов в земной коре
Металлы Распространённость металлов в земной коре
 Металлы Нахождение металлов в природе Активные: - Хлориды Na. Cl, KCl, Mg. Cl; - Сульфаты Na 2 SO 4, Ca. SO 4, Mg. SO 4; - Нитраты Na. NO 3, KNO 3; - Ортофосфаты Ca 3(PO 4)2 Средней активности: - Оксиды Fe 2 O 3, Fe 3 O 4, Cr 2 O 3; - Сульфиды Pb. S, Hg. S, Zn. S Благородные: - в самородном виде Ag, Au, Pt
Металлы Нахождение металлов в природе Активные: - Хлориды Na. Cl, KCl, Mg. Cl; - Сульфаты Na 2 SO 4, Ca. SO 4, Mg. SO 4; - Нитраты Na. NO 3, KNO 3; - Ортофосфаты Ca 3(PO 4)2 Средней активности: - Оксиды Fe 2 O 3, Fe 3 O 4, Cr 2 O 3; - Сульфиды Pb. S, Hg. S, Zn. S Благородные: - в самородном виде Ag, Au, Pt
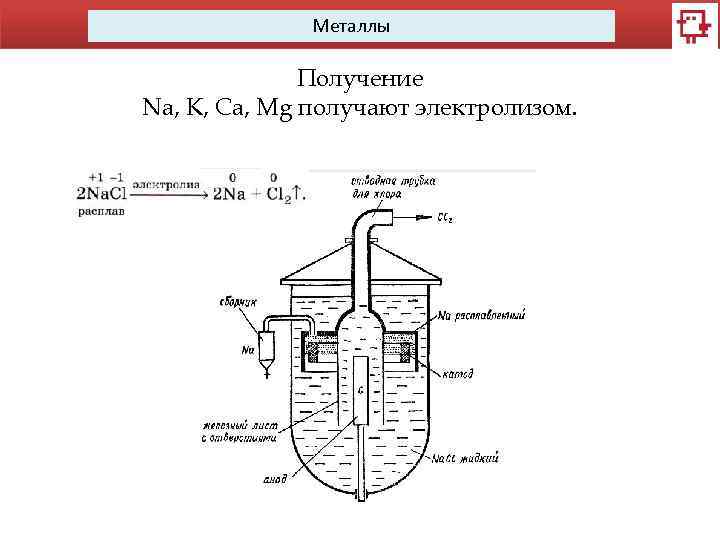 Металлы Получение Na, K, Ca, Mg получают электролизом.
Металлы Получение Na, K, Ca, Mg получают электролизом.
 Металлы Получение Менее активные металлы получают восстановлением с С, CO или Al. Sn. O 2 + C = Fe 2 O 3 + CO = Mn. O 2 + Al =
Металлы Получение Менее активные металлы получают восстановлением с С, CO или Al. Sn. O 2 + C = Fe 2 O 3 + CO = Mn. O 2 + Al =
 Металлы Получение Менее активные металлы получают восстановлением с С, CO или Al. Сульфиды сначала обжигают. Zn. S + O 2 = Zn. O + C =
Металлы Получение Менее активные металлы получают восстановлением с С, CO или Al. Сульфиды сначала обжигают. Zn. S + O 2 = Zn. O + C =
 Металлы Предположить электронное строение для пероксидов металлов 1 й группы.
Металлы Предположить электронное строение для пероксидов металлов 1 й группы.