 Урок 9 класса Щелочные металлы
Урок 9 класса Щелочные металлы
 Металлы IA группы (щелочные) Генетическая связь для Na и его соединений: Na + …. - Na. Cl + …. . Na 2 CO 3 + …. - Na. HCO 3 + …. . Na + …. - Na 2 O 2 + …. - Na 2 O + …. . Na + …. - Na. H + …. . Na. OH + …. - Cu(OH)2 + …. .
Металлы IA группы (щелочные) Генетическая связь для Na и его соединений: Na + …. - Na. Cl + …. . Na 2 CO 3 + …. - Na. HCO 3 + …. . Na + …. - Na 2 O 2 + …. - Na 2 O + …. . Na + …. - Na. H + …. . Na. OH + …. - Cu(OH)2 + …. .
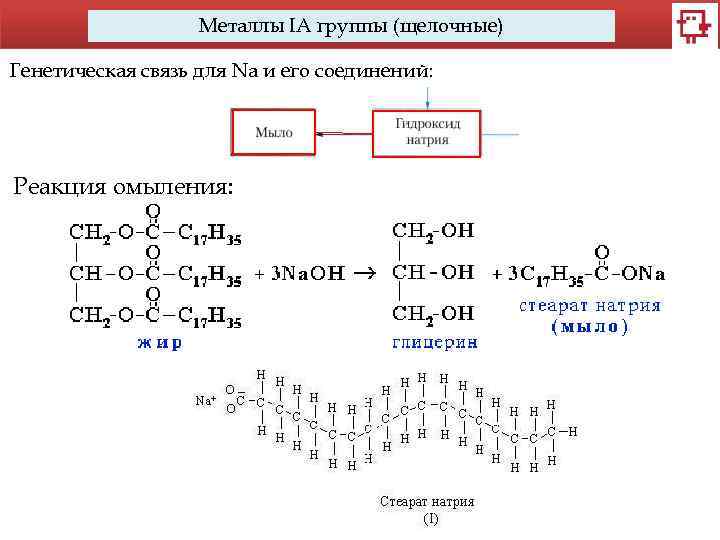 Металлы IA группы (щелочные) Генетическая связь для Na и его соединений: Реакция омыления:
Металлы IA группы (щелочные) Генетическая связь для Na и его соединений: Реакция омыления:
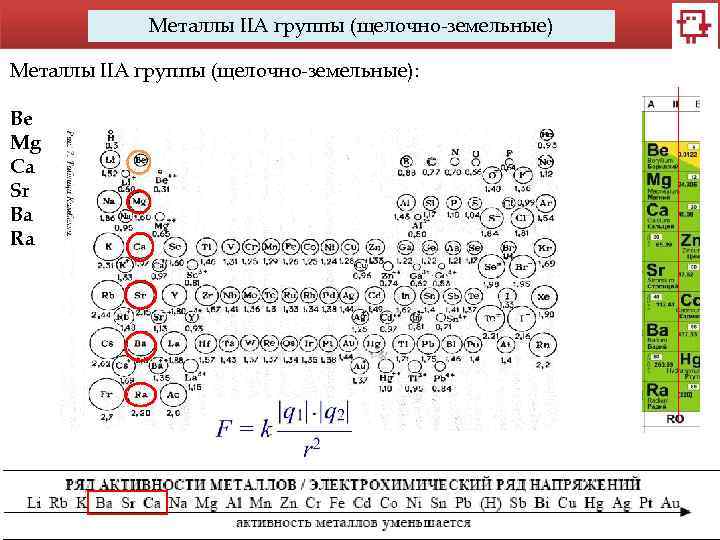 Металлы IIA группы (щелочно-земельные): Be Mg Ca Sr Ba Ra
Металлы IIA группы (щелочно-земельные): Be Mg Ca Sr Ba Ra
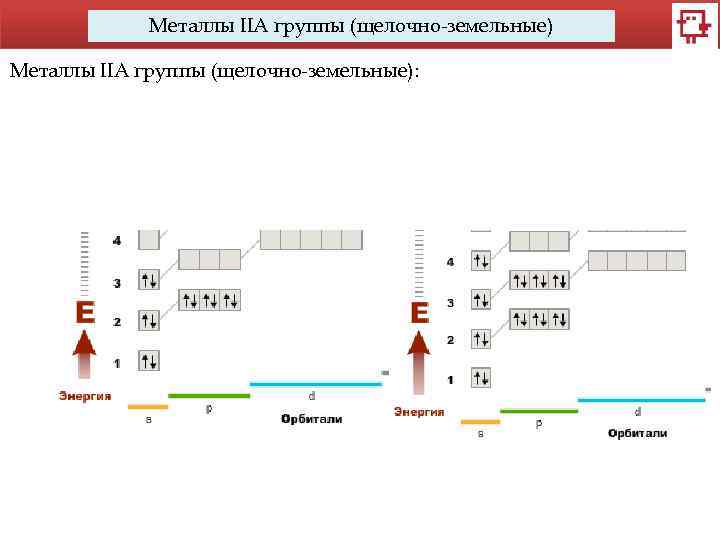 Металлы IIA группы (щелочно-земельные):
Металлы IIA группы (щелочно-земельные):
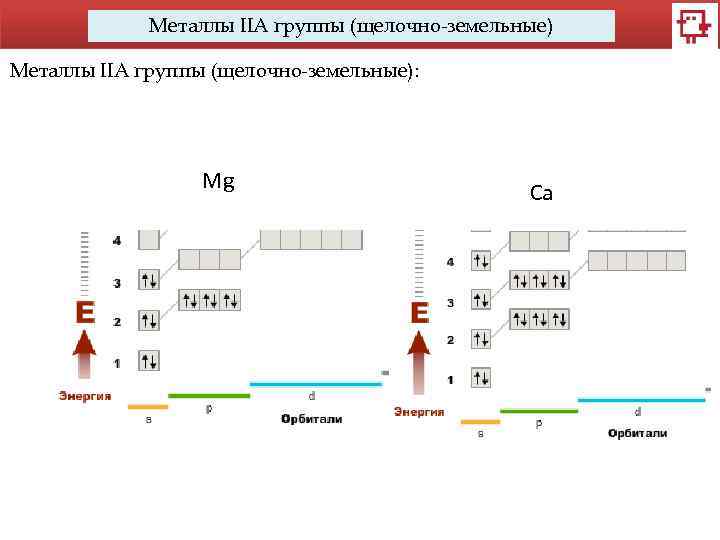 Металлы IIA группы (щелочно-земельные): Mg Ca
Металлы IIA группы (щелочно-земельные): Mg Ca
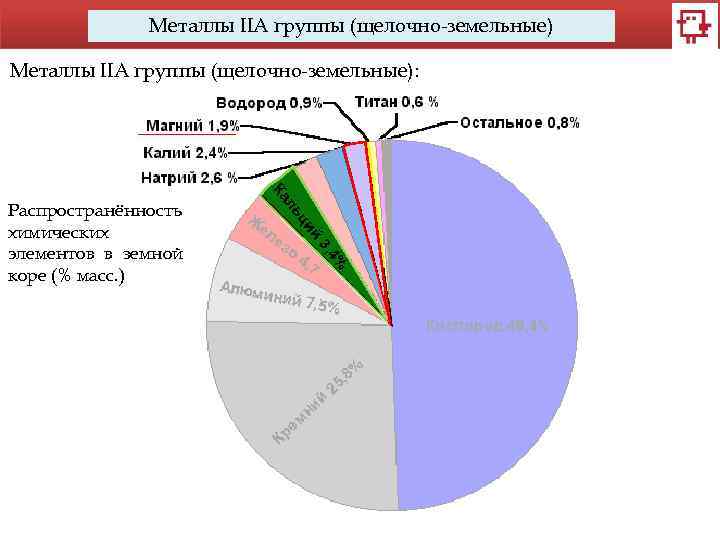 Металлы IIA группы (щелочно-земельные): Распространённость химических элементов в земной коре (% масс. )
Металлы IIA группы (щелочно-земельные): Распространённость химических элементов в земной коре (% масс. )
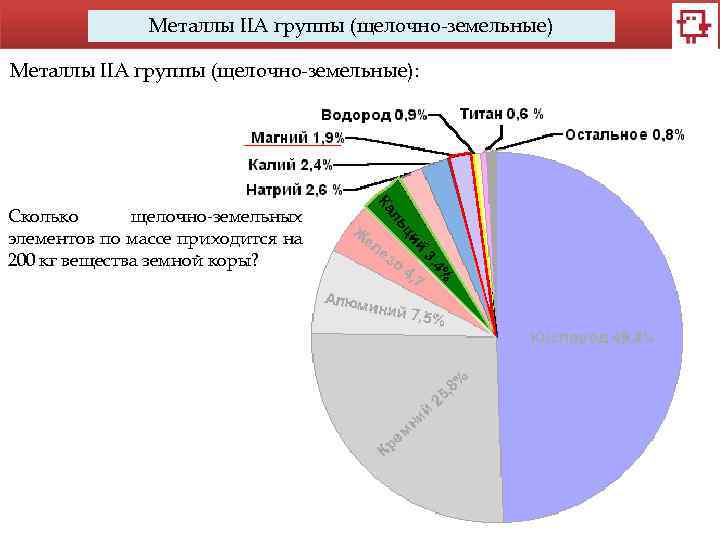 Металлы IIA группы (щелочно-земельные): Сколько щелочно-земельных элементов по массе приходится на 200 кг вещества земной коры?
Металлы IIA группы (щелочно-земельные): Сколько щелочно-земельных элементов по массе приходится на 200 кг вещества земной коры?
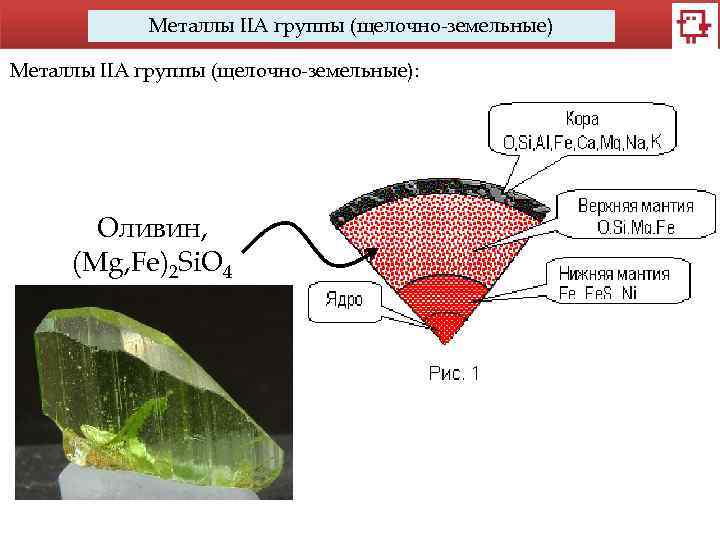 Металлы IIA группы (щелочно-земельные): Оливин, (Mg, Fe)2 Si. O 4
Металлы IIA группы (щелочно-земельные): Оливин, (Mg, Fe)2 Si. O 4
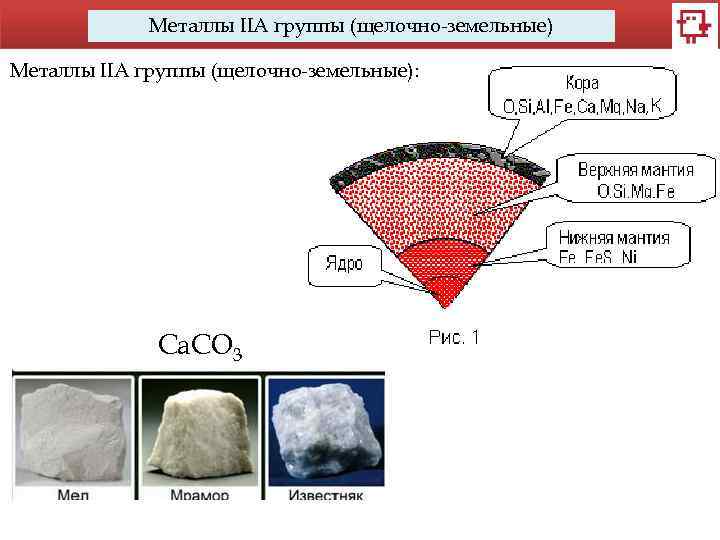 Металлы IIA группы (щелочно-земельные): Ca. CO 3
Металлы IIA группы (щелочно-земельные): Ca. CO 3
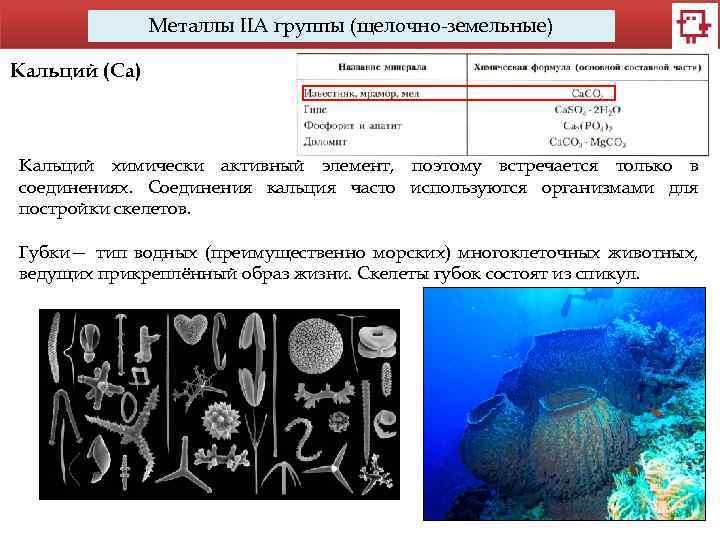 Металлы IIA группы (щелочно-земельные) Кальций (Са) Кальций химически активный элемент, поэтому встречается только в соединениях. Соединения кальция часто используются организмами для постройки скелетов. Губки— тип водных (преимущественно морских) многоклеточных животных, ведущих прикреплённый образ жизни. Скелеты губок состоят из спикул.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Кальций химически активный элемент, поэтому встречается только в соединениях. Соединения кальция часто используются организмами для постройки скелетов. Губки— тип водных (преимущественно морских) многоклеточных животных, ведущих прикреплённый образ жизни. Скелеты губок состоят из спикул.
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Гипс типичный осадочный минерал. Используется как удобрение; в целлюлозно-бумажной промышленности; для получения красок, эмали, глазури. В медицине и строительстве как вяжущий материал.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Гипс типичный осадочный минерал. Используется как удобрение; в целлюлозно-бумажной промышленности; для получения красок, эмали, глазури. В медицине и строительстве как вяжущий материал.
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Ca 10(PO 4)6(OH, F, Cl)2 Апатит – минерал концентратор фтора и кальция, имеющий большую твёрдость. Апатит — главная неорганическая составляющая костей и зубов позвоночных животных, и человека.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Ca 10(PO 4)6(OH, F, Cl)2 Апатит – минерал концентратор фтора и кальция, имеющий большую твёрдость. Апатит — главная неорганическая составляющая костей и зубов позвоночных животных, и человека.
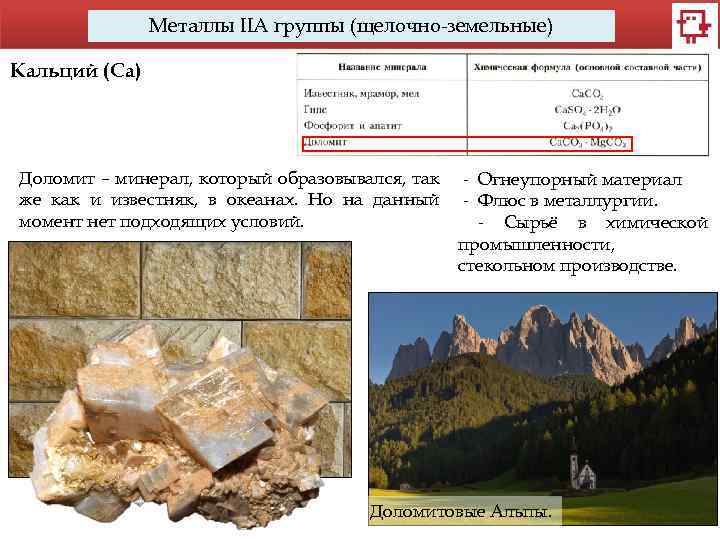 Металлы IIA группы (щелочно-земельные) Кальций (Са) Доломит – минерал, который образовывался, так же как и известняк, в океанах. Но на данный момент нет подходящих условий. - Огнеупорный материал - Флюс в металлургии. - Сырьё в химической промышленности, стекольном производстве. Доломитовые Альпы.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Доломит – минерал, который образовывался, так же как и известняк, в океанах. Но на данный момент нет подходящих условий. - Огнеупорный материал - Флюс в металлургии. - Сырьё в химической промышленности, стекольном производстве. Доломитовые Альпы.
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Получают кальций, в основном, электролизом Ca. Cl 2, реже из Ca. F 2. Или с помощью алюминотермии: 4 Ca. O + 2 Al Ca. Al 2 O 4 + 3 Ca
Металлы IIA группы (щелочно-земельные) Кальций (Са) Получают кальций, в основном, электролизом Ca. Cl 2, реже из Ca. F 2. Или с помощью алюминотермии: 4 Ca. O + 2 Al Ca. Al 2 O 4 + 3 Ca
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Физические свойства. Имеет серебристо-белый цвет, легок (р = 1. 55 гсм 3). Твёрже щелочных металлов и имеет высокую температуру плавления 838, 85. Металл кальций существует в двух аллотропных модификациях, с границей по температуре 443 С. Соединения Са окрашивают пламя в кирпично-красный цвет.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Физические свойства. Имеет серебристо-белый цвет, легок (р = 1. 55 гсм 3). Твёрже щелочных металлов и имеет высокую температуру плавления 838, 85. Металл кальций существует в двух аллотропных модификациях, с границей по температуре 443 С. Соединения Са окрашивают пламя в кирпично-красный цвет.
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Химические свойства.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Химические свойства.
 Металлы IIA группы (щелочно-земельные) Кальций (Са) Напишите уравнение электролиза расплава хлорида кальция. Какой продукт выделяется на катоде? Какой продукт выделяется на аноде? Какие свойства (окислительные или восстановительные) может проявлять кальций? Приведите 3 примера в доказательство.
Металлы IIA группы (щелочно-земельные) Кальций (Са) Напишите уравнение электролиза расплава хлорида кальция. Какой продукт выделяется на катоде? Какой продукт выделяется на аноде? Какие свойства (окислительные или восстановительные) может проявлять кальций? Приведите 3 примера в доказательство.


