9Ч_14-15_9.pptx
- Количество слайдов: 20
 Урок 9 класса. Электролитическая диссоциация. 14. 09. 2016 1
Урок 9 класса. Электролитическая диссоциация. 14. 09. 2016 1
 Электролиты Когда электролит попадает в воду он «разваливается» на составляющие его катионы и анионы. Na. Cl = Na+ + Cl. CH 3 COOH =H+ + CH 3 COO- 14. 09. 2016 2
Электролиты Когда электролит попадает в воду он «разваливается» на составляющие его катионы и анионы. Na. Cl = Na+ + Cl. CH 3 COOH =H+ + CH 3 COO- 14. 09. 2016 2
 Растворение Na. Cl = Na+ + Cl. Долгое время считалось, что процесс растворения имеет только физическую природу. Например, при разбавлении серной кислоты сосуд со смесью нагревается. Поэтому существует правило: серную кислоту наливают тонкой струйкой в воду при постоянном перемешивании! 14. 09. 2016 3
Растворение Na. Cl = Na+ + Cl. Долгое время считалось, что процесс растворения имеет только физическую природу. Например, при разбавлении серной кислоты сосуд со смесью нагревается. Поэтому существует правило: серную кислоту наливают тонкой струйкой в воду при постоянном перемешивании! 14. 09. 2016 3
 Вода как растворитель Почему вода растворитель? 14. 09. 2016 4
Вода как растворитель Почему вода растворитель? 14. 09. 2016 4
 Вода как растворитель 14. 09. 2016 5
Вода как растворитель 14. 09. 2016 5
 Урок 9 класса. Электролитическая диссоциация. Продолжение… 15. 09. 2016 1
Урок 9 класса. Электролитическая диссоциация. Продолжение… 15. 09. 2016 1
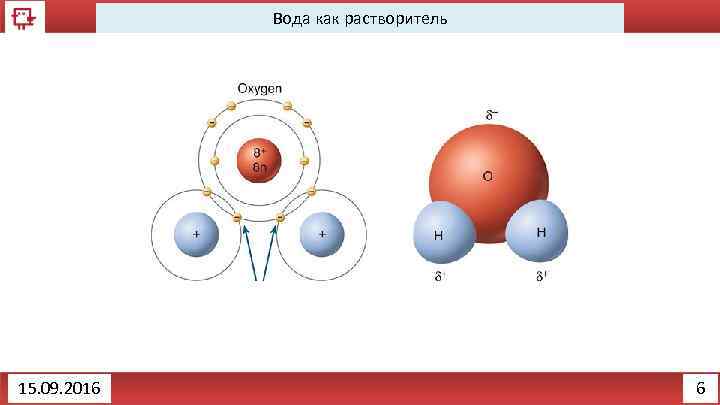 Вода как растворитель 15. 09. 2016 6
Вода как растворитель 15. 09. 2016 6
 Вода как растворитель Вещества с какой связь лучше будут растворяться в воде? • С ковалентной неполярной • С ковалентной полярной • С ионной • С металлической 16. 09. 2016 7
Вода как растворитель Вещества с какой связь лучше будут растворяться в воде? • С ковалентной неполярной • С ковалентной полярной • С ионной • С металлической 16. 09. 2016 7
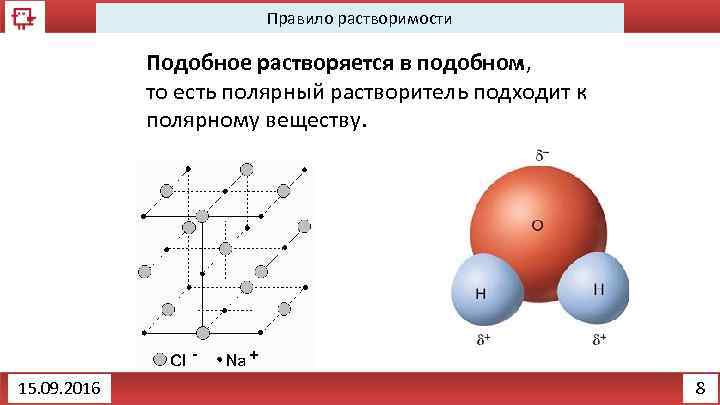 Правило растворимости Подобное растворяется в подобном, то есть полярный растворитель подходит к полярному веществу. 15. 09. 2016 8
Правило растворимости Подобное растворяется в подобном, то есть полярный растворитель подходит к полярному веществу. 15. 09. 2016 8
 Гидратация – присоединение воды к ионам, атомам или молекулам. Продукты такого процесса называют гидратами. Обратная реакция называется дегидратацией. 15. 09. 2016 9
Гидратация – присоединение воды к ионам, атомам или молекулам. Продукты такого процесса называют гидратами. Обратная реакция называется дегидратацией. 15. 09. 2016 9
 Гидратация Кристаллогидраты – кристаллические вещества, в состав которых входит химически связанная вода. Такую воду называют кристаллизационной водой. 15. 09. 2016 10
Гидратация Кристаллогидраты – кристаллические вещества, в состав которых входит химически связанная вода. Такую воду называют кристаллизационной водой. 15. 09. 2016 10
 Основные положения электролитической диссоциации Основные положения теории электролитической диссоциации: 1. Электролиты при растворении или плавлении распадаются на ионы (диссоциируют) – положительные и отрицательные. 2. Под действием электрического тока ионы приобретают направленное движение: положительные ионы стремятся к катоду, отрицательные - к аноду. 3. Направленное движение происходит в результате притяжения их противоположно заряженными электродами. 4. Диссоциация – обратимый процесс: одновременно вещество распадается на ионы и ионы собираются в вещество. 15. 09. 2016 11
Основные положения электролитической диссоциации Основные положения теории электролитической диссоциации: 1. Электролиты при растворении или плавлении распадаются на ионы (диссоциируют) – положительные и отрицательные. 2. Под действием электрического тока ионы приобретают направленное движение: положительные ионы стремятся к катоду, отрицательные - к аноду. 3. Направленное движение происходит в результате притяжения их противоположно заряженными электродами. 4. Диссоциация – обратимый процесс: одновременно вещество распадается на ионы и ионы собираются в вещество. 15. 09. 2016 11
 Диссоциация разных веществ Диссоциировать могут соли, кислоты, щелочки. Наиболее хорошо диссоцируют вещества с ионной связью (большой разностью электроотрицательностей). 2 H 2 O H 3 O+ К и с л о т ы 15. 09. 2016 Ион гидроксония HCl H+ + Cl. HCl + H 2 O H 3 O+ + Cl. HNO 3 + n. H 2 O H 3 O+ + NO 3 - + m. H 2 O HNO 3 NO 3 - + H+ 12
Диссоциация разных веществ Диссоциировать могут соли, кислоты, щелочки. Наиболее хорошо диссоцируют вещества с ионной связью (большой разностью электроотрицательностей). 2 H 2 O H 3 O+ К и с л о т ы 15. 09. 2016 Ион гидроксония HCl H+ + Cl. HCl + H 2 O H 3 O+ + Cl. HNO 3 + n. H 2 O H 3 O+ + NO 3 - + m. H 2 O HNO 3 NO 3 - + H+ 12
 Диссоциация кислот Кислоты – такие вещества, при диссоциации в водных растворах которых в качестве катиона отщепляется только водород (или гидроксония ион). 2 H 2 O H+ + OHК и с л о т ы 15. 09. 2016 HCl H+ + Cl. HCl + H 2 O H 3 O+ + Cl. HNO 3 + n. H 2 O H 3 O+ + NO 3 - + m. H 2 O HNO 3 NO 3 - + H+ 13
Диссоциация кислот Кислоты – такие вещества, при диссоциации в водных растворах которых в качестве катиона отщепляется только водород (или гидроксония ион). 2 H 2 O H+ + OHК и с л о т ы 15. 09. 2016 HCl H+ + Cl. HCl + H 2 O H 3 O+ + Cl. HNO 3 + n. H 2 O H 3 O+ + NO 3 - + m. H 2 O HNO 3 NO 3 - + H+ 13
 Диссоциация кислот H 2 SO 4 HSO 4 - + H+ HSO 4 - SO 42 - + H+ H 3 PO 4 H+ +H 2 PO 4 - дигидроортофосфат ион H 2 PO 4 - H+ +HPO 42 - гидроортофосфат ион HPO 42 - H+ + PO 43 - ортофосфат ион 15. 09. 2016 14
Диссоциация кислот H 2 SO 4 HSO 4 - + H+ HSO 4 - SO 42 - + H+ H 3 PO 4 H+ +H 2 PO 4 - дигидроортофосфат ион H 2 PO 4 - H+ +HPO 42 - гидроортофосфат ион HPO 42 - H+ + PO 43 - ортофосфат ион 15. 09. 2016 14
 Диссоциация щелочей Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы (OH -). 2 H 2 O H+ + OHЩ е л о ч и 15. 09. 2016 Гидроксид-ион Na. OH Na+ + OHBa(ОН)2 Bа(ОН)+ + OH- Ba(OH)+ Ba 2++OH 15
Диссоциация щелочей Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы (OH -). 2 H 2 O H+ + OHЩ е л о ч и 15. 09. 2016 Гидроксид-ион Na. OH Na+ + OHBa(ОН)2 Bа(ОН)+ + OH- Ba(OH)+ Ba 2++OH 15
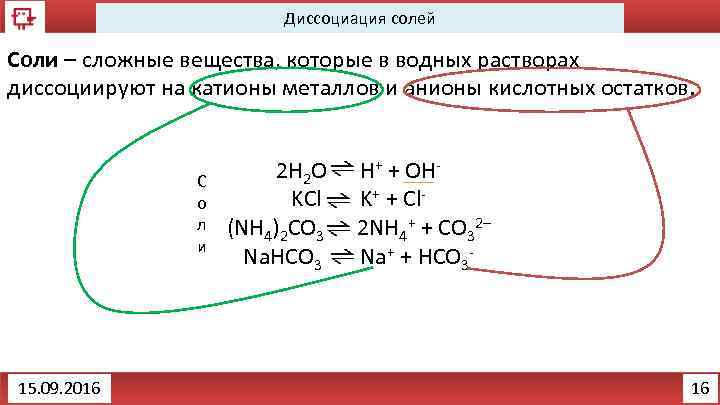 Диссоциация солей Соли – сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. С о л и 15. 09. 2016 2 H 2 O H+ + OHKCl K+ + Cl(NH 4)2 CO 3 2 NH 4+ + CO 32– Na. HCO 3 Na+ + HCO 3 - 16
Диссоциация солей Соли – сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. С о л и 15. 09. 2016 2 H 2 O H+ + OHKCl K+ + Cl(NH 4)2 CO 3 2 NH 4+ + CO 32– Na. HCO 3 Na+ + HCO 3 - 16
 Сильные и слабые электролиты Бывают электролиты распадающиеся полностью, например: Na. OH Na+ + OHБывают электролиты распадающиеся не полностью: H 2 CO 3 H+ + HCO 3 Сильные электролиты – химические соединения, которые при растворении в воде полностью распадаются на ионы. Слабые электролиты – соединения, которые незначительно диссоциируют на ионы. 15. 09. 2016 17
Сильные и слабые электролиты Бывают электролиты распадающиеся полностью, например: Na. OH Na+ + OHБывают электролиты распадающиеся не полностью: H 2 CO 3 H+ + HCO 3 Сильные электролиты – химические соединения, которые при растворении в воде полностью распадаются на ионы. Слабые электролиты – соединения, которые незначительно диссоциируют на ионы. 15. 09. 2016 17
 Степень диссоциации Различить слабые электролиты и сильные электролиты помогает показатель степень диссоциации (α). 15. 09. 2016 18
Степень диссоциации Различить слабые электролиты и сильные электролиты помогает показатель степень диссоциации (α). 15. 09. 2016 18
 Подготовить ответ на вопрос На следующем уроке, на оценку один из вас ответит на вопрос: Почему водный раствор сульфата натрия проводит ток? Приведите уравнение процесса. 15. 09. 2016 19
Подготовить ответ на вопрос На следующем уроке, на оценку один из вас ответит на вопрос: Почему водный раствор сульфата натрия проводит ток? Приведите уравнение процесса. 15. 09. 2016 19


