 Урок 8 класса. Кислоты Соли
Урок 8 класса. Кислоты Соли
 Соли – это сложные вещества, образованные атомами металлов и кислотными остатками. Fe + 2 HCl = Fe. Cl 2 + H 2 Mg + H 2 SO 4 = Mg. SO 4 + H 2 Fe 2 O 3 + 6 HCl = 2 Fe. Cl 3 + 3 H 2 O
Соли – это сложные вещества, образованные атомами металлов и кислотными остатками. Fe + 2 HCl = Fe. Cl 2 + H 2 Mg + H 2 SO 4 = Mg. SO 4 + H 2 Fe 2 O 3 + 6 HCl = 2 Fe. Cl 3 + 3 H 2 O
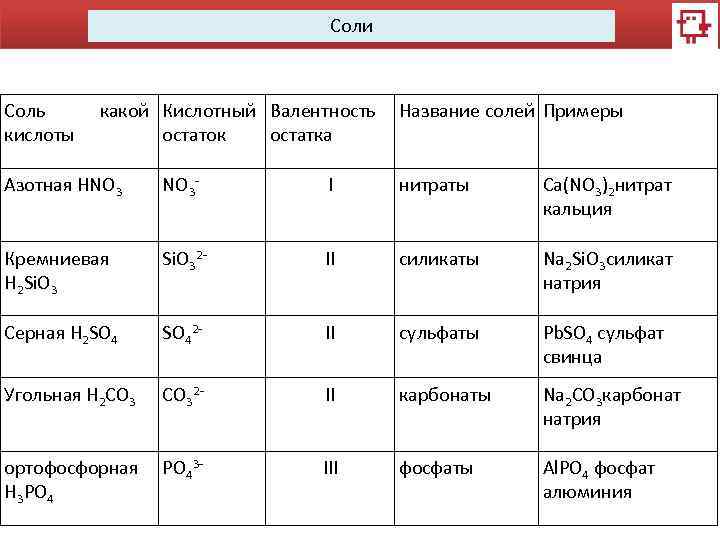 Соли Соль кислоты какой Кислотный Валентность Название солей Примеры остаток остатка Азотная HNO 3 - I нитраты Ca(NO 3)2 нитрат кальция Кремниевая H 2 Si. O 32 - II силикаты Na 2 Si. O 3 силикат натрия Серная H 2 SO 42 - II сульфаты Pb. SO 4 сульфат свинца Угольная H 2 CO 32 - II карбонаты Na 2 CO 3 карбонат натрия ортофосфорная PO 43 H 3 PO 4 III фосфаты Al. PO 4 фосфат алюминия
Соли Соль кислоты какой Кислотный Валентность Название солей Примеры остаток остатка Азотная HNO 3 - I нитраты Ca(NO 3)2 нитрат кальция Кремниевая H 2 Si. O 32 - II силикаты Na 2 Si. O 3 силикат натрия Серная H 2 SO 42 - II сульфаты Pb. SO 4 сульфат свинца Угольная H 2 CO 32 - II карбонаты Na 2 CO 3 карбонат натрия ортофосфорная PO 43 H 3 PO 4 III фосфаты Al. PO 4 фосфат алюминия
 Соли Исключение соли аммония, в которых с кислотными остатками связаны не атомы металла, а частицы NH 4+ Соли аммония - это сложные вещества, в состав которых входят ионы аммония NH 4+, соединённые с кислотными остатками. Например, NH 4 Cl – хлорид аммония (NH 4)2 SO 4 - сульфат аммония NH 4 NO 3 – нитрат аммония (NH 4)3 PO 4 – ортофосфат аммония (NH 4)2 HPO 4 – гидроортофосфат аммония NH 4 H 2 PO 4 – дигидроортофосфат аммония
Соли Исключение соли аммония, в которых с кислотными остатками связаны не атомы металла, а частицы NH 4+ Соли аммония - это сложные вещества, в состав которых входят ионы аммония NH 4+, соединённые с кислотными остатками. Например, NH 4 Cl – хлорид аммония (NH 4)2 SO 4 - сульфат аммония NH 4 NO 3 – нитрат аммония (NH 4)3 PO 4 – ортофосфат аммония (NH 4)2 HPO 4 – гидроортофосфат аммония NH 4 H 2 PO 4 – дигидроортофосфат аммония
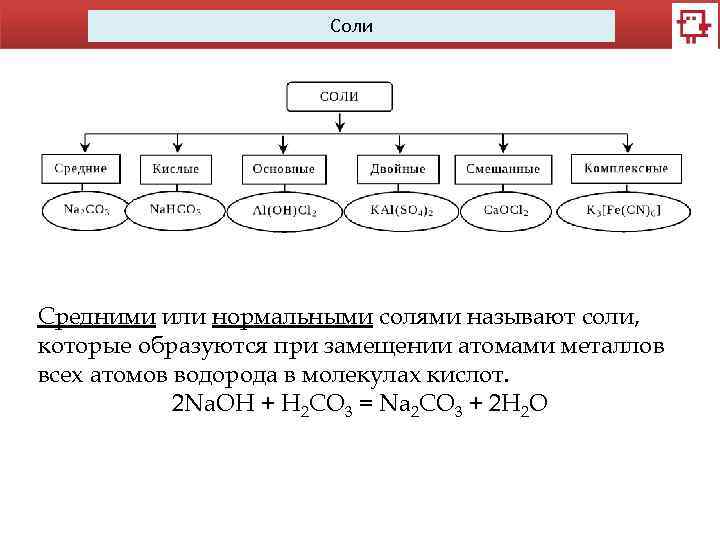 Соли Средними или нормальными солями называют соли, которые образуются при замещении атомами металлов всех атомов водорода в молекулах кислот. 2 Na. OH + H 2 CO 3 = Na 2 CO 3 + 2 H 2 O
Соли Средними или нормальными солями называют соли, которые образуются при замещении атомами металлов всех атомов водорода в молекулах кислот. 2 Na. OH + H 2 CO 3 = Na 2 CO 3 + 2 H 2 O
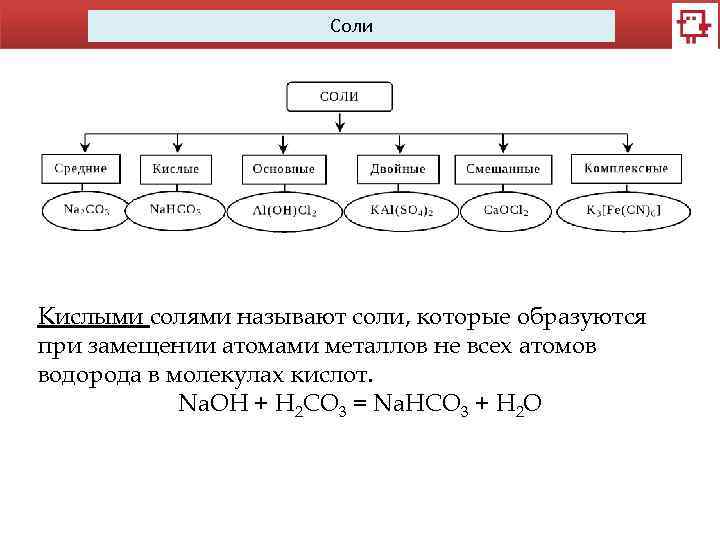 Соли Кислыми солями называют соли, которые образуются при замещении атомами металлов не всех атомов водорода в молекулах кислот. Na. OH + H 2 CO 3 = Na. НCO 3 + H 2 O
Соли Кислыми солями называют соли, которые образуются при замещении атомами металлов не всех атомов водорода в молекулах кислот. Na. OH + H 2 CO 3 = Na. НCO 3 + H 2 O
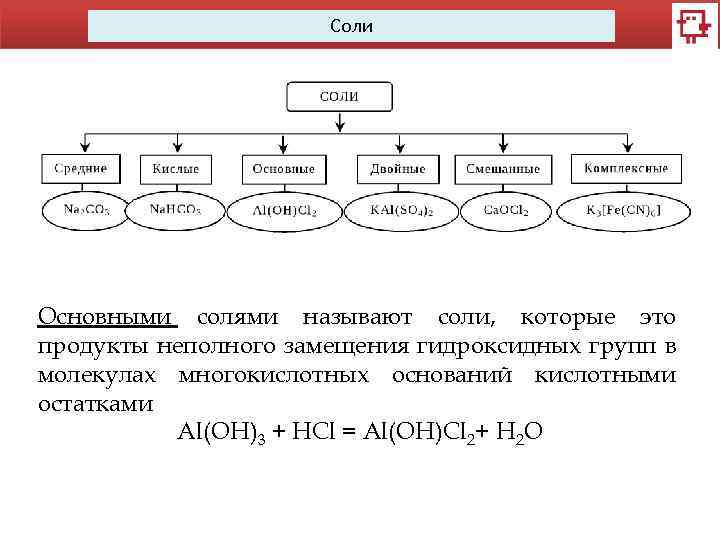
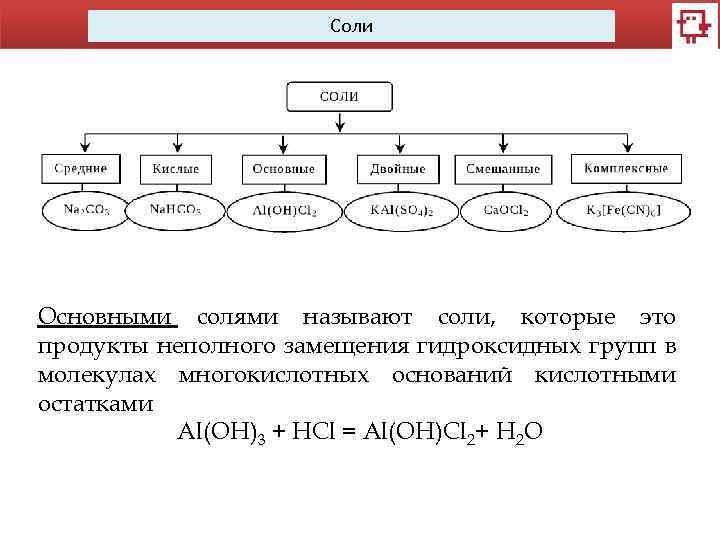 Соли Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками Al(OH)3 + HCl = Al(OH)Cl 2+ H 2 O
Соли Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками Al(OH)3 + HCl = Al(OH)Cl 2+ H 2 O
 Соли Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками Al(OH)3 + HCl = Al(OH)Cl 2+ H 2 O
Соли Основными солями называют соли, которые это продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками Al(OH)3 + HCl = Al(OH)Cl 2+ H 2 O
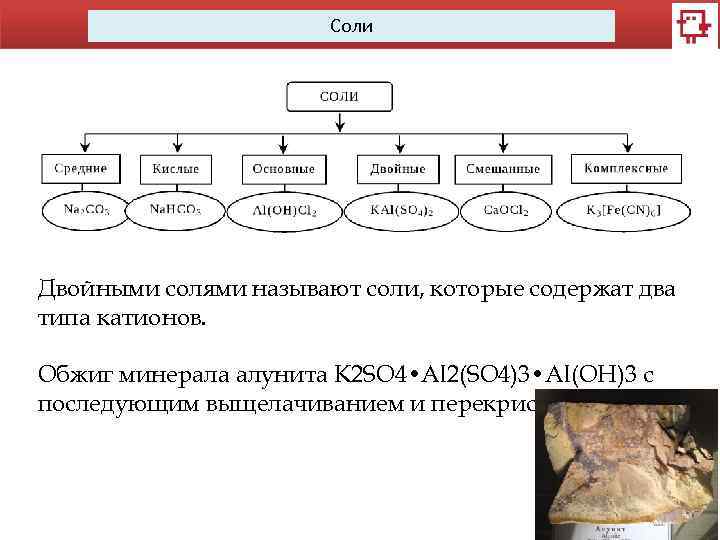 Соли Двойными солями называют соли, которые содержат два типа катионов. Обжиг минерала алунита K 2 SO 4 • Al 2(SO 4)3 • Al(OH)3 с последующим выщелачиванием и перекристаллизацией.
Соли Двойными солями называют соли, которые содержат два типа катионов. Обжиг минерала алунита K 2 SO 4 • Al 2(SO 4)3 • Al(OH)3 с последующим выщелачиванием и перекристаллизацией.
 Соли Обжиг минерала алунита K 2 SO 4 • Al 2(SO 4)3 • Al(OH)3 с последующим выщелачиванием и перекристаллизацией. Совместная кристаллизация сульфатов алюминия и калия.
Соли Обжиг минерала алунита K 2 SO 4 • Al 2(SO 4)3 • Al(OH)3 с последующим выщелачиванием и перекристаллизацией. Совместная кристаллизация сульфатов алюминия и калия.
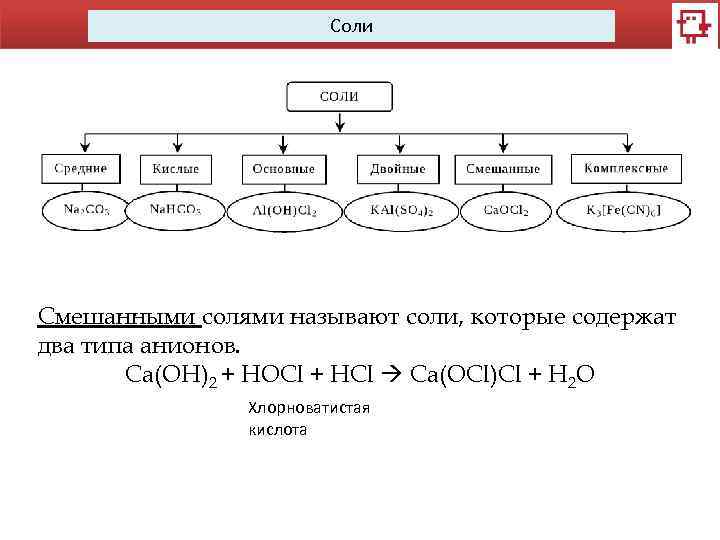 Соли Смешанными солями называют соли, которые содержат два типа анионов. Ca(OH)2 + HOCl + HCl Ca(OCl)Cl + H 2 O Хлорноватистая кислота
Соли Смешанными солями называют соли, которые содержат два типа анионов. Ca(OH)2 + HOCl + HCl Ca(OCl)Cl + H 2 O Хлорноватистая кислота
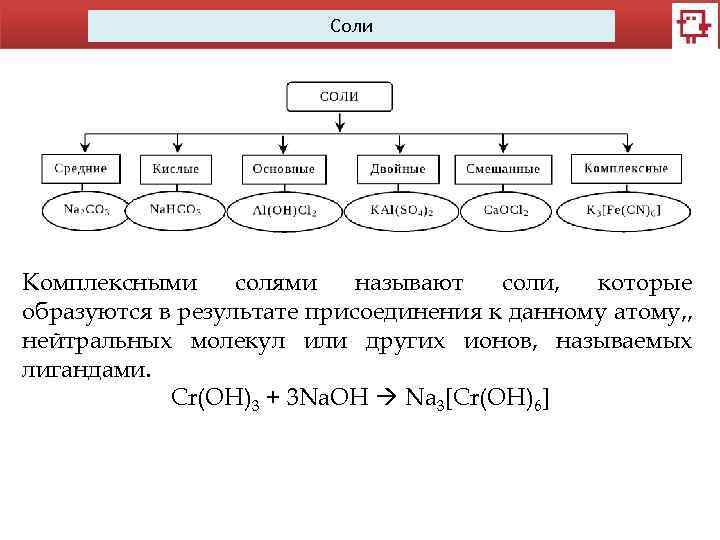 Соли Комплексными солями называют соли, которые образуются в результате присоединения к данному атому, , нейтральных молекул или других ионов, называемых лигандами. Cr(OH)3 + 3 Na. OH Na 3[Cr(OH)6]
Соли Комплексными солями называют соли, которые образуются в результате присоединения к данному атому, , нейтральных молекул или других ионов, называемых лигандами. Cr(OH)3 + 3 Na. OH Na 3[Cr(OH)6]
 Соли 1. Действие кислот на металлы, основные оксиды и основания: Fe + H 2 SO 4(разб. ) = Fe. SO 4 + H 2 SO 4 + Cu. O = Cu. SO 4 + H 2 O + 2 KOH = K 2 SO 4 + 2 H 2 O 2. Реакция кислотных оксидов со щелочами или основными оксидами: Ca(OH)2 Ca. O + CO 2 = Ca. CO 3↓ + H 2 O + SO 3 = Ca. SO 4
Соли 1. Действие кислот на металлы, основные оксиды и основания: Fe + H 2 SO 4(разб. ) = Fe. SO 4 + H 2 SO 4 + Cu. O = Cu. SO 4 + H 2 O + 2 KOH = K 2 SO 4 + 2 H 2 O 2. Реакция кислотных оксидов со щелочами или основными оксидами: Ca(OH)2 Ca. O + CO 2 = Ca. CO 3↓ + H 2 O + SO 3 = Ca. SO 4
 Соли 3. Взаимодействие солей с кислотами, щелочами, металлами, нелетучими кислотными оксидами и другими солями: Ca 3(PO 4)2 +3 H 2 SO 4 = 3 Ca. SO 4 +2 H 3 PO 4 Fe 2(SO 4)3 + 6 Na. OH = 2 Fe(OH)3 + 3 Na 2 SO 4 Cu. SO 4 + Fe = Fe. SO 4 + Cu Ca. CO 3 + Si. O 2 = Ca. Si. O 3 + CO 2 Al 2(SO 4)3 + 3 Ba. Cl 2 = 3 Ba. SO 4 +2 Al. Cl 3 4. Взаимодействие металлов с неметаллами: 2 K + Cl 2 = 2 KCl
Соли 3. Взаимодействие солей с кислотами, щелочами, металлами, нелетучими кислотными оксидами и другими солями: Ca 3(PO 4)2 +3 H 2 SO 4 = 3 Ca. SO 4 +2 H 3 PO 4 Fe 2(SO 4)3 + 6 Na. OH = 2 Fe(OH)3 + 3 Na 2 SO 4 Cu. SO 4 + Fe = Fe. SO 4 + Cu Ca. CO 3 + Si. O 2 = Ca. Si. O 3 + CO 2 Al 2(SO 4)3 + 3 Ba. Cl 2 = 3 Ba. SO 4 +2 Al. Cl 3 4. Взаимодействие металлов с неметаллами: 2 K + Cl 2 = 2 KCl
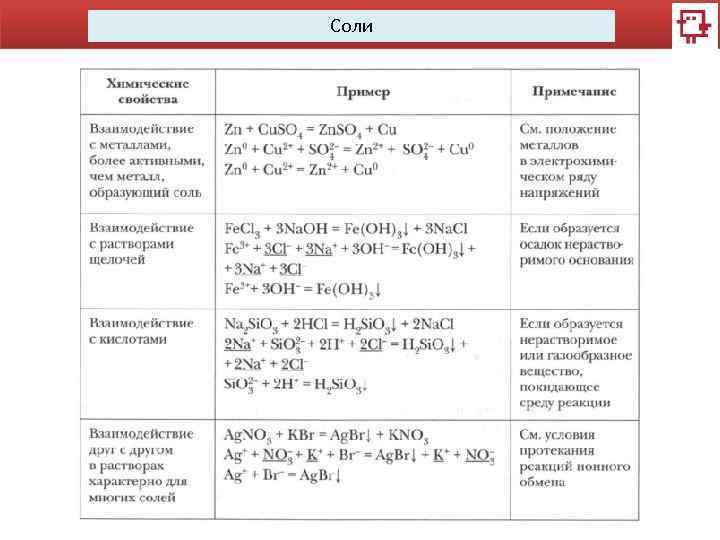 Соли
Соли
 Соли 1. 2. 3. 4. C какими из перечисленных ниже металлов будет взаимодействовать соляная кислота: 1) алюминий; 2) серебро; 3) ртуть; 4) олово? Составьте уравнения реакций между серной кислотой и следующими веществами: а) магнием; б) оксидом магния; в) оксидом алюминия; г) оксидом калий; д) цинком. Дайте названия следующим соединениям (солям): а) KCl; б) Ca. CO 3; в) K 3 PO 4; г) H 2 CO 3; д) Fe. SO 4; е) Fe 2(SO 4)3; ж) Cu(NO 3)2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Соли 1. 2. 3. 4. C какими из перечисленных ниже металлов будет взаимодействовать соляная кислота: 1) алюминий; 2) серебро; 3) ртуть; 4) олово? Составьте уравнения реакций между серной кислотой и следующими веществами: а) магнием; б) оксидом магния; в) оксидом алюминия; г) оксидом калий; д) цинком. Дайте названия следующим соединениям (солям): а) KCl; б) Ca. CO 3; в) K 3 PO 4; г) H 2 CO 3; д) Fe. SO 4; е) Fe 2(SO 4)3; ж) Cu(NO 3)2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:


