урок 30 газовые законы.ppt
- Количество слайдов: 18
 УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА. ГАЗОВЫЕ ЗАКОНЫ
УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА. ГАЗОВЫЕ ЗАКОНЫ
 СОДЕРЖАНИЕ • Уравнение состояния идеального газа …. . . • Понятие изопроцесса …………. . . . • Изотермический процесс…………. . • Изобарный процесс ……………… • Изохорный процесс ……………. . • Тестовые задания ………………. . .
СОДЕРЖАНИЕ • Уравнение состояния идеального газа …. . . • Понятие изопроцесса …………. . . . • Изотермический процесс…………. . • Изобарный процесс ……………… • Изохорный процесс ……………. . • Тестовые задания ………………. . .
 Зависимость давления идеального (достаточно разреженного) газа от температуры и концентрации его молекул имеет вид: p = nk. T Попытаемся получить на основе этой зависимости уравнение, связывающее все три макроскопических параметра, характеризующие состояние идеального газа: p, V , T p = nk. T n=N V p = N k. T V m N= N M А 1 m N k. T p= V M А m NА k. T обе части уравнения умножим на V, получим : p. V = M NAk = R = 6, 02 х 10 231/моль х 1, 38 х10 -23 Дж/К = 8, 31 Дж/(моль. К) R = 8, 31 Дж/(моль К) – универсальная газовая постоянная m p. V = RT M уравнение состояния идеального газа
Зависимость давления идеального (достаточно разреженного) газа от температуры и концентрации его молекул имеет вид: p = nk. T Попытаемся получить на основе этой зависимости уравнение, связывающее все три макроскопических параметра, характеризующие состояние идеального газа: p, V , T p = nk. T n=N V p = N k. T V m N= N M А 1 m N k. T p= V M А m NА k. T обе части уравнения умножим на V, получим : p. V = M NAk = R = 6, 02 х 10 231/моль х 1, 38 х10 -23 Дж/К = 8, 31 Дж/(моль. К) R = 8, 31 Дж/(моль К) – универсальная газовая постоянная m p. V = RT M уравнение состояния идеального газа
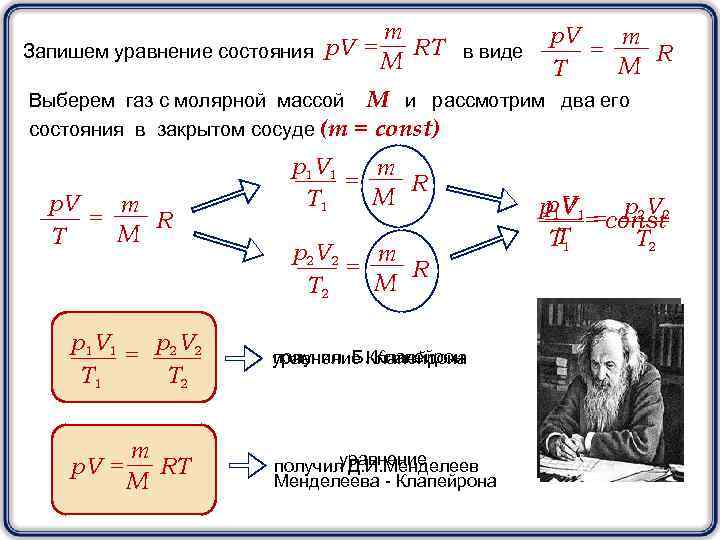 m RT в виде Запишем уравнение состояния p. V = M Выберем газ с молярной массой состояния в закрытом сосуде (m p. V m = R M T М и рассмотрим два его = const) p 1 V 1 m = R M T 1 p 2 V 2 m = R M T 2 p 1 V 1 p. V = 2 2 T 1 T 2 получил Б. Клапейрон уравнение Клапейрона m p. V = RT M уравнение получил Д. И. Менделеева - Клапейрона p. V p 1 V 1 p. V = 2 = const 2 T T 1 T 2
m RT в виде Запишем уравнение состояния p. V = M Выберем газ с молярной массой состояния в закрытом сосуде (m p. V m = R M T М и рассмотрим два его = const) p 1 V 1 m = R M T 1 p 2 V 2 m = R M T 2 p 1 V 1 p. V = 2 2 T 1 T 2 получил Б. Клапейрон уравнение Клапейрона m p. V = RT M уравнение получил Д. И. Менделеева - Клапейрона p. V p 1 V 1 p. V = 2 = const 2 T T 1 T 2
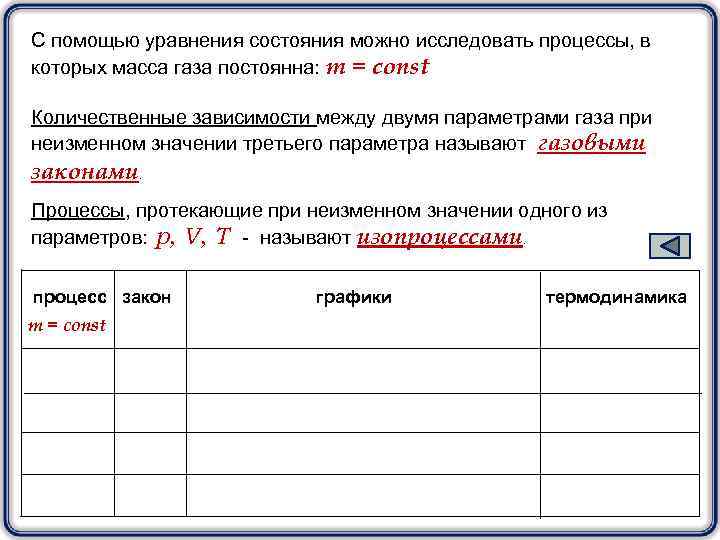 С помощью уравнения состояния можно исследовать процессы, в которых масса газа постоянна: m = const Количественные зависимости между двумя параметрами газа при неизменном значении третьего параметра называют газовыми законами. Процессы, протекающие при неизменном значении одного из параметров: p, V, T - называют изопроцессами. процесс закон m = const графики термодинамика
С помощью уравнения состояния можно исследовать процессы, в которых масса газа постоянна: m = const Количественные зависимости между двумя параметрами газа при неизменном значении третьего параметра называют газовыми законами. Процессы, протекающие при неизменном значении одного из параметров: p, V, T - называют изопроцессами. процесс закон m = const графики термодинамика
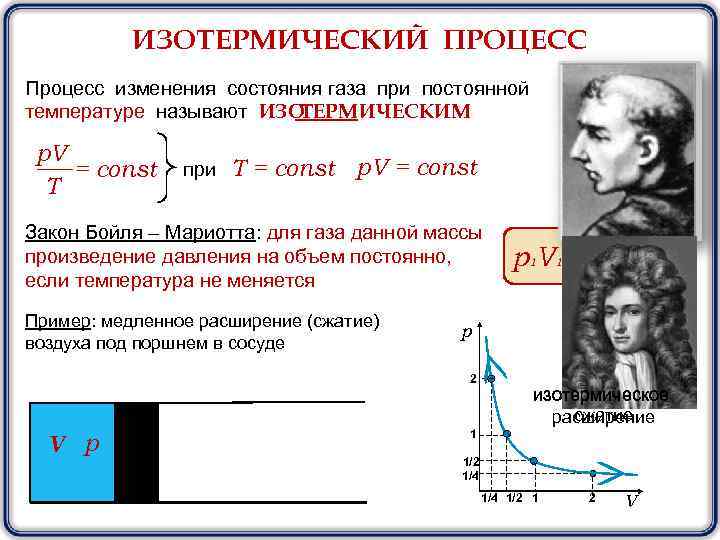 ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС Процесс изменения состояния газа при постоянной ТЕРМ ИЧЕСКИМ температуре называют ИЗО p. V = const T при Т = const p. V = const Закон Бойля – Мариотта: для газа данной массы произведение давления на объем постоянно, если температура не меняется Пример: медленное расширение (сжатие) воздуха под поршнем в сосуде p 2 V р р1 V 1 = р2 V 2 изотермическое сжатие расширение 1 1/2 1/4 1/2 1 2 V
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС Процесс изменения состояния газа при постоянной ТЕРМ ИЧЕСКИМ температуре называют ИЗО p. V = const T при Т = const p. V = const Закон Бойля – Мариотта: для газа данной массы произведение давления на объем постоянно, если температура не меняется Пример: медленное расширение (сжатие) воздуха под поршнем в сосуде p 2 V р р1 V 1 = р2 V 2 изотермическое сжатие расширение 1 1/2 1/4 1/2 1 2 V
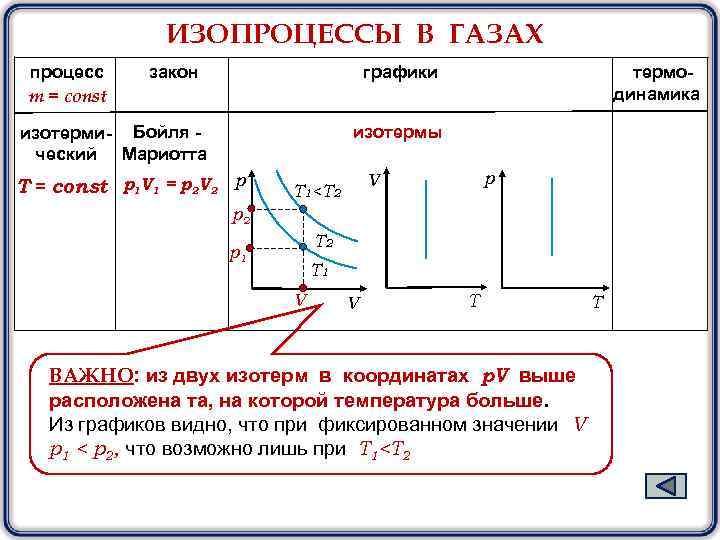 ИЗОПРОЦЕССЫ В ГАЗАХ процесс m = const закон графики изотерми- Бойля ческий Мариотта термодинамика изотермы Т = const р1 V 1 = р2 V 2 р р V T 1
ИЗОПРОЦЕССЫ В ГАЗАХ процесс m = const закон графики изотерми- Бойля ческий Мариотта термодинамика изотермы Т = const р1 V 1 = р2 V 2 р р V T 1
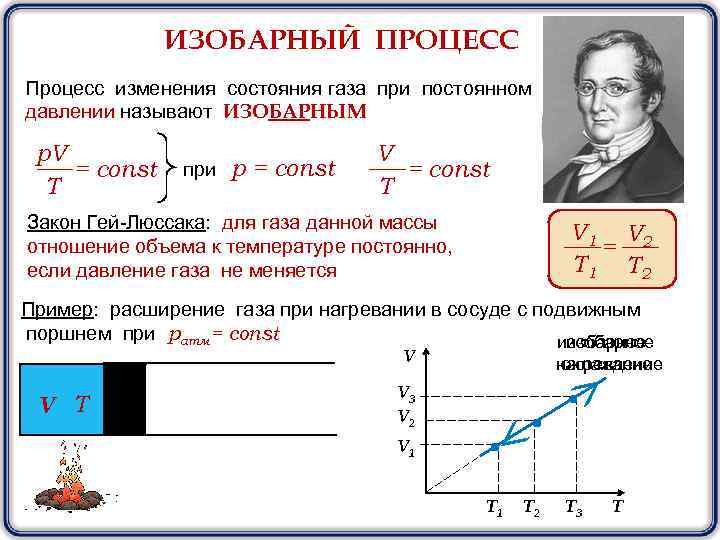 ИЗОБАРНЫЙ ПРОЦЕСС Процесс изменения состояния газа при постоянном давлении называют ИЗОБАРНЫМ p. V = const T при р = const V = const T Закон Гей-Люссака: для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется V 1 V 2 = T 1 T 2 Пример: расширение газа при нагревании в сосуде с подвижным поршнем при ратм= const изобарное V V Т нагревание охлаждение V 3 V 2 V 1 T 2 T 3 T
ИЗОБАРНЫЙ ПРОЦЕСС Процесс изменения состояния газа при постоянном давлении называют ИЗОБАРНЫМ p. V = const T при р = const V = const T Закон Гей-Люссака: для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется V 1 V 2 = T 1 T 2 Пример: расширение газа при нагревании в сосуде с подвижным поршнем при ратм= const изобарное V V Т нагревание охлаждение V 3 V 2 V 1 T 2 T 3 T
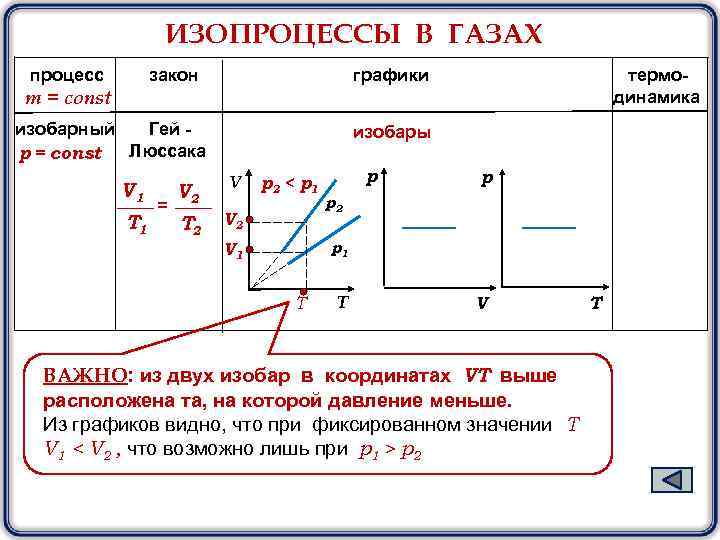 ИЗОПРОЦЕССЫ В ГАЗАХ процесс закон графики термодинамика m = const изобарный Гей Люссака р = const V 1 T 1 = изобары V 2 V T 2 V 2 p 2 < p 1 р р р2 р1 V 1 T T V ВАЖНО: из двух изобар в координатах VТ выше расположена та, на которой давление меньше. Из графиков видно, что при фиксированном значении Т V 1 < V 2 , что возможно лишь при p 1 > p 2 T
ИЗОПРОЦЕССЫ В ГАЗАХ процесс закон графики термодинамика m = const изобарный Гей Люссака р = const V 1 T 1 = изобары V 2 V T 2 V 2 p 2 < p 1 р р р2 р1 V 1 T T V ВАЖНО: из двух изобар в координатах VТ выше расположена та, на которой давление меньше. Из графиков видно, что при фиксированном значении Т V 1 < V 2 , что возможно лишь при p 1 > p 2 T
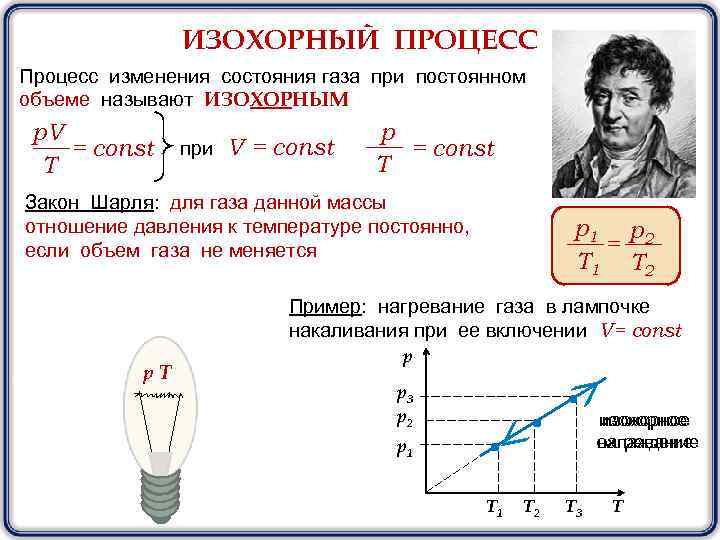 ИЗОХОРНЫЙ ПРОЦЕСС Процесс изменения состояния газа при постоянном объеме называют ИЗОХОРНЫМ p. V = const T при V = const p = const T Закон Шарля: для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется р1 р2 = T 1 T 2 Пример: нагревание газа в лампочке накаливания при ее включении V= const р. Т р р3 р2 изохорное охлаждение нагревание р1 T 2 T 3 T
ИЗОХОРНЫЙ ПРОЦЕСС Процесс изменения состояния газа при постоянном объеме называют ИЗОХОРНЫМ p. V = const T при V = const p = const T Закон Шарля: для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется р1 р2 = T 1 T 2 Пример: нагревание газа в лампочке накаливания при ее включении V= const р. Т р р3 р2 изохорное охлаждение нагревание р1 T 2 T 3 T
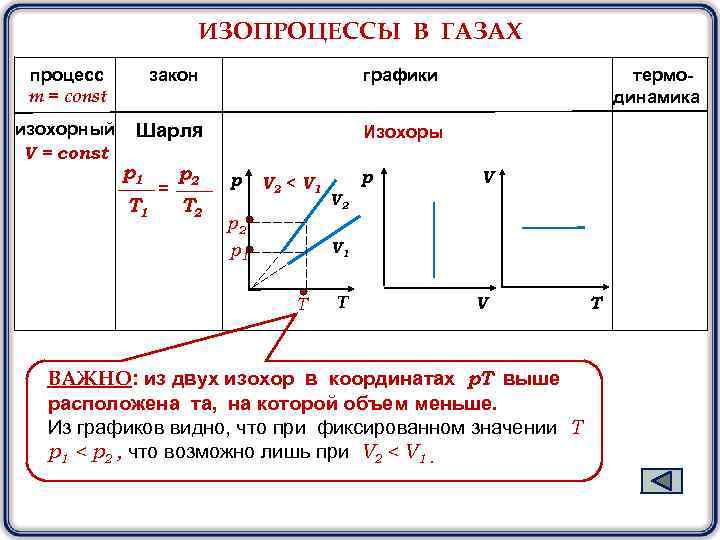 ИЗОПРОЦЕССЫ В ГАЗАХ процесс m = const закон графики изохорный V = const Шарля Изохоры p 1 T 1 = p 2 T 2 р V 2 < V 1 p 2 p 1 р термодинамика V V 2 V 1 T T V ВАЖНО: из двух изохор в координатах p. Т выше расположена та, на которой объем меньше. Из графиков видно, что при фиксированном значении Т р1 < р2 , что возможно лишь при V 2 < V 1. T
ИЗОПРОЦЕССЫ В ГАЗАХ процесс m = const закон графики изохорный V = const Шарля Изохоры p 1 T 1 = p 2 T 2 р V 2 < V 1 p 2 p 1 р термодинамика V V 2 V 1 T T V ВАЖНО: из двух изохор в координатах p. Т выше расположена та, на которой объем меньше. Из графиков видно, что при фиксированном значении Т р1 < р2 , что возможно лишь при V 2 < V 1. T
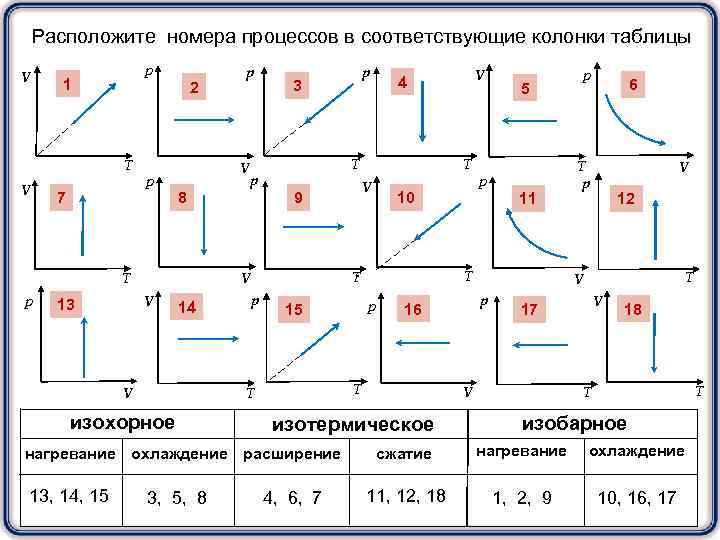 Расположите номера процессов в соответствующие колонки таблицы V р 1 2 T V 7 р V 14 изохорное нагревание охлаждение расширение 13, 14, 15 3, 5, 8 4, 6, 7 6 T р V 12 T V 17 18 T T V изотермическое р V р 16 T T V 11 T р 15 р 10 : T р 5 T V 9 V 4 T V V 13 р 8 T р р изобарное сжатие нагревание охлаждение 11, 12, 18 1, 2, 9 10, 16, 17
Расположите номера процессов в соответствующие колонки таблицы V р 1 2 T V 7 р V 14 изохорное нагревание охлаждение расширение 13, 14, 15 3, 5, 8 4, 6, 7 6 T р V 12 T V 17 18 T T V изотермическое р V р 16 T T V 11 T р 15 р 10 : T р 5 T V 9 V 4 T V V 13 р 8 T р р изобарное сжатие нагревание охлаждение 11, 12, 18 1, 2, 9 10, 16, 17
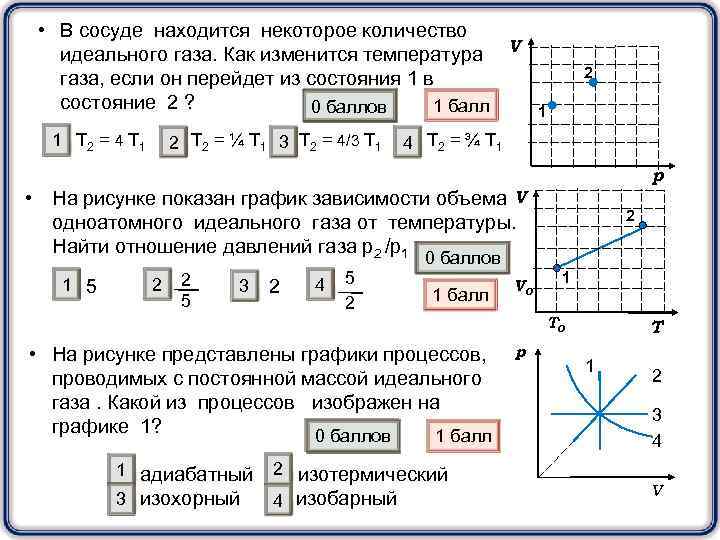 • В сосуде находится некоторое количество идеального газа. Как изменится температура V газа, если он перейдет из состояния 1 в состояние 2 ? 1 балл 0 баллов 1 Т 2 = 4 Т 1 2 Т 2 = ¼ Т 1 3 Т 2 = 4/3 Т 1 2 1 4 Т 2 = ¾ Т 1 р • На рисунке показан график зависимости объема V одноатомного идеального газа от температуры. Найти отношение давлений газа р2 /р1 1 5 2 2 5 3 2 4 5 2 0 баллов 1 балл • На рисунке представлены графики процессов, проводимых с постоянной массой идеального газа. Какой из процессов изображен на графике 1? 0 баллов 1 балл 0 баллов 1 адиабатный 3 изохорный 2 2 изотермический 4 изобарный V 0 1 Т 0 р Т 1 2 3 4 V
• В сосуде находится некоторое количество идеального газа. Как изменится температура V газа, если он перейдет из состояния 1 в состояние 2 ? 1 балл 0 баллов 1 Т 2 = 4 Т 1 2 Т 2 = ¼ Т 1 3 Т 2 = 4/3 Т 1 2 1 4 Т 2 = ¾ Т 1 р • На рисунке показан график зависимости объема V одноатомного идеального газа от температуры. Найти отношение давлений газа р2 /р1 1 5 2 2 5 3 2 4 5 2 0 баллов 1 балл • На рисунке представлены графики процессов, проводимых с постоянной массой идеального газа. Какой из процессов изображен на графике 1? 0 баллов 1 балл 0 баллов 1 адиабатный 3 изохорный 2 2 изотермический 4 изобарный V 0 1 Т 0 р Т 1 2 3 4 V
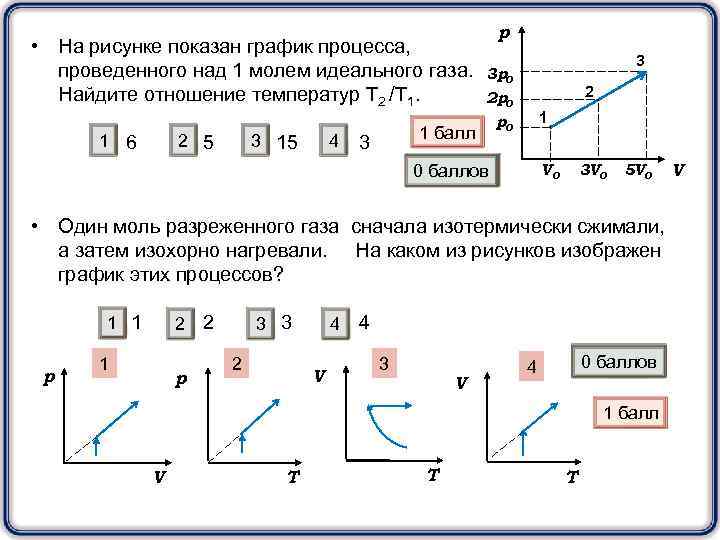 • На рисунке показан график процесса, проведенного над 1 молем идеального газа. Найдите отношение температур Т 2 /Т 1. 1 6 2 5 3 15 4 1 балл 3 р 3 3 р0 2 р0 р0 2 1 V 0 0 баллов 3 V 0 5 V 0 • Один моль разреженного газа сначала изотермически сжимали, а затем изохорно нагревали. На каком из рисунков изображен график этих процессов? 1 1 р 2 3 3 2 4 V 4 3 V 0 баллов 4 1 балл V Т Т Т V
• На рисунке показан график процесса, проведенного над 1 молем идеального газа. Найдите отношение температур Т 2 /Т 1. 1 6 2 5 3 15 4 1 балл 3 р 3 3 р0 2 р0 р0 2 1 V 0 0 баллов 3 V 0 5 V 0 • Один моль разреженного газа сначала изотермически сжимали, а затем изохорно нагревали. На каком из рисунков изображен график этих процессов? 1 1 р 2 3 3 2 4 V 4 3 V 0 баллов 4 1 балл V Т Т Т V
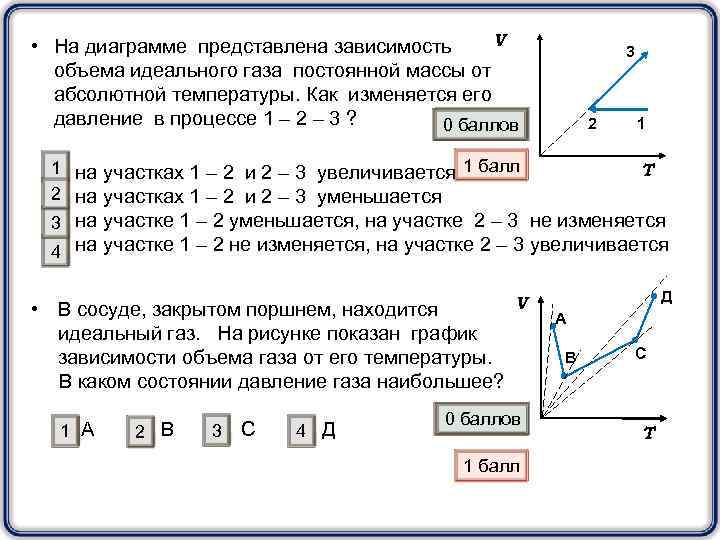 V • На диаграмме представлена зависимость объема идеального газа постоянной массы от абсолютной температуры. Как изменяется его давление в процессе 1 – 2 – 3 ? 0 баллов 3 2 1 1 на участках 1 – 2 и 2 – 3 увеличивается 1 балл Т 2 на участках 1 – 2 и 2 – 3 уменьшается 3 на участке 1 – 2 уменьшается, на участке 2 – 3 не изменяется 4 на участке 1 – 2 не изменяется, на участке 2 – 3 увеличивается • В сосуде, закрытом поршнем, находится идеальный газ. На рисунке показан график зависимости объема газа от его температуры. В каком состоянии давление газа наибольшее? 1 А 2 В 3 С 4 Д V 0 баллов 1 балл Д А В С Т
V • На диаграмме представлена зависимость объема идеального газа постоянной массы от абсолютной температуры. Как изменяется его давление в процессе 1 – 2 – 3 ? 0 баллов 3 2 1 1 на участках 1 – 2 и 2 – 3 увеличивается 1 балл Т 2 на участках 1 – 2 и 2 – 3 уменьшается 3 на участке 1 – 2 уменьшается, на участке 2 – 3 не изменяется 4 на участке 1 – 2 не изменяется, на участке 2 – 3 увеличивается • В сосуде, закрытом поршнем, находится идеальный газ. На рисунке показан график зависимости объема газа от его температуры. В каком состоянии давление газа наибольшее? 1 А 2 В 3 С 4 Д V 0 баллов 1 балл Д А В С Т
 • Разреженный углекислый газ изобарно сжимается. Масса газа постоянна. Как надо изменить абсолютную температуру газа, чтобы уменьшить его объем в 4 раза? 0 баллов 1 2 повысить в 16 раз 3 понизить в 16 раз 4 повысить в 4 раза понизить в 4 раза 1 балл • В цилиндрическом сосуде под поршнем находится идеальный газ, давление которого 4 х 105 Па и температура 300 К. Как надо изменить объем газа, не меняя его температуры, чтобы давление увеличилось до 0, 8 х 106 Па? 0 баллов 1 увеличить в 2 раза 3 уменьшить в 2 раза 2 увеличить в 4 раза 4 уменьшить в 4 раза 0 баллов 1 балл • Давление 3 моль водорода в сосуде при температуре 300 К равно р1. Каково давление 1 моль водорода в этом сосуде при вдвое большей температуре? 0 баллов 1 3/2 р1 2 2/3 р1 3 1/6 р1 4 6 р1 1 балл
• Разреженный углекислый газ изобарно сжимается. Масса газа постоянна. Как надо изменить абсолютную температуру газа, чтобы уменьшить его объем в 4 раза? 0 баллов 1 2 повысить в 16 раз 3 понизить в 16 раз 4 повысить в 4 раза понизить в 4 раза 1 балл • В цилиндрическом сосуде под поршнем находится идеальный газ, давление которого 4 х 105 Па и температура 300 К. Как надо изменить объем газа, не меняя его температуры, чтобы давление увеличилось до 0, 8 х 106 Па? 0 баллов 1 увеличить в 2 раза 3 уменьшить в 2 раза 2 увеличить в 4 раза 4 уменьшить в 4 раза 0 баллов 1 балл • Давление 3 моль водорода в сосуде при температуре 300 К равно р1. Каково давление 1 моль водорода в этом сосуде при вдвое большей температуре? 0 баллов 1 3/2 р1 2 2/3 р1 3 1/6 р1 4 6 р1 1 балл
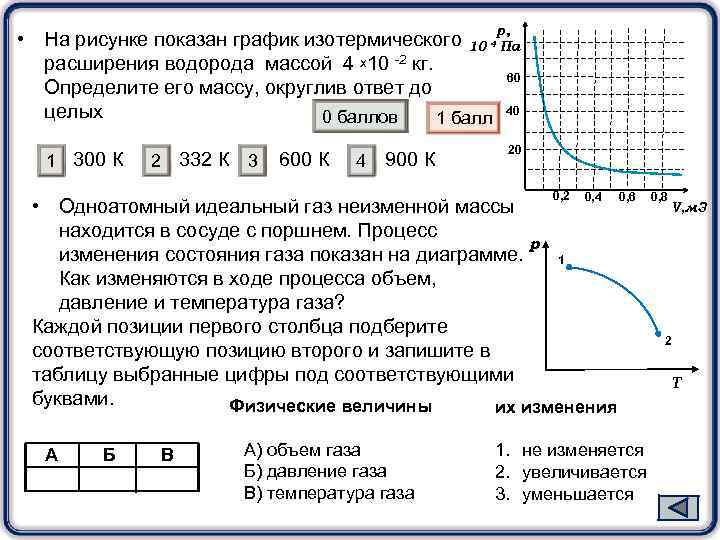 р, • На рисунке показан график изотермического 10 4 Па расширения водорода массой 4 х10 -2 кг. 60 Определите его массу, округлив ответ до 40 целых 0 баллов 1 балл 1 300 К 2 332 К 3 600 К 4 900 К 20 0, 2 0, 4 • Одноатомный идеальный газ неизменной массы находится в сосуде с поршнем. Процесс р изменения состояния газа показан на диаграмме. 1 Как изменяются в ходе процесса объем, давление и температура газа? Каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами. Физические величины их изменения А Б В А) объем газа Б) давление газа В) температура газа 0, 6 1. не изменяется 2. увеличивается 3. уменьшается 0, 8 V, м 3 2 Т
р, • На рисунке показан график изотермического 10 4 Па расширения водорода массой 4 х10 -2 кг. 60 Определите его массу, округлив ответ до 40 целых 0 баллов 1 балл 1 300 К 2 332 К 3 600 К 4 900 К 20 0, 2 0, 4 • Одноатомный идеальный газ неизменной массы находится в сосуде с поршнем. Процесс р изменения состояния газа показан на диаграмме. 1 Как изменяются в ходе процесса объем, давление и температура газа? Каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами. Физические величины их изменения А Б В А) объем газа Б) давление газа В) температура газа 0, 6 1. не изменяется 2. увеличивается 3. уменьшается 0, 8 V, м 3 2 Т
 Использованная литература • Физика : Учеб. для 10 кл. общеобразоват. учреждений / Г. Я. Мякишев, Б. Б. Буховцев, Н. Н. Сотский. – 12 -е изд. – М. : Просвещение, 2004. • ЕГЭ 2011. Физика. Универсальные материалы для подготовки учащихся / ФИПИ – М. : Интеллект – Центр. 2011. • Самое полное издание типовых вариантов ЕГЭ: 2011, 2012 : Физика / авт. – сост. А. В. Берков, В. А. Грибов. – М. : АСТ: Астрель, 2011, 2012. • Портреты ученых – страницы свободного доступа сети интернет • Рекомендации по использованию триггеров в тестовых заданиях даны Г. Ф. Кузнецовым.
Использованная литература • Физика : Учеб. для 10 кл. общеобразоват. учреждений / Г. Я. Мякишев, Б. Б. Буховцев, Н. Н. Сотский. – 12 -е изд. – М. : Просвещение, 2004. • ЕГЭ 2011. Физика. Универсальные материалы для подготовки учащихся / ФИПИ – М. : Интеллект – Центр. 2011. • Самое полное издание типовых вариантов ЕГЭ: 2011, 2012 : Физика / авт. – сост. А. В. Берков, В. А. Грибов. – М. : АСТ: Астрель, 2011, 2012. • Портреты ученых – страницы свободного доступа сети интернет • Рекомендации по использованию триггеров в тестовых заданиях даны Г. Ф. Кузнецовым.


