 Уран И. Г. Тананаев
Уран И. Г. Тананаев
 Открытие урана Уран - черное с металлическим блеском вещество - был открыт Клапротом в 1789 г. из золотистой смоляной руды ( «земли» ). Элемент назван «Ураном» в честь открытой в 13 марта 1781 г. Гершелем планеты Уран. Солнце
Открытие урана Уран - черное с металлическим блеском вещество - был открыт Клапротом в 1789 г. из золотистой смоляной руды ( «земли» ). Элемент назван «Ураном» в честь открытой в 13 марта 1781 г. Гершелем планеты Уран. Солнце
 В греческой мифологии, Уран – бог неба, супруг богини Земли Геи и отец титанов – обладал невидимой мощи. Титаны - боги первого поколения. Они породили новое поколение титанов, том числе Прометея.
В греческой мифологии, Уран – бог неба, супруг богини Земли Геи и отец титанов – обладал невидимой мощи. Титаны - боги первого поколения. Они породили новое поколение титанов, том числе Прометея.
 «Уран Клапрота» числился металлом всего 50 лет. В 1841 г Пелиго доказал, что «уран Клапрота» является его диоксидом - UO 2: UO 2+ С + 2 С 12 = UC 14+СO 2 UC 14 + 4 K = 4 KC 1 + U. Произошло второе открытие элемента, атомный вес Которого определили 120. В 1874 г Д. И. Менделеев высказал предположение, что «вес атома урана следует увеличивать в два раза и положить U = 240» . Он поместил U в самой дальней клетке свой таблицы.
«Уран Клапрота» числился металлом всего 50 лет. В 1841 г Пелиго доказал, что «уран Клапрота» является его диоксидом - UO 2: UO 2+ С + 2 С 12 = UC 14+СO 2 UC 14 + 4 K = 4 KC 1 + U. Произошло второе открытие элемента, атомный вес Которого определили 120. В 1874 г Д. И. Менделеев высказал предположение, что «вес атома урана следует увеличивать в два раза и положить U = 240» . Он поместил U в самой дальней клетке свой таблицы.
 В начале XX в. не проводились ни добыча урана, ни разработка урановых руд, любое его производство было побочным. Уран получали для окрашивания керамики и стекол фонарей семафоров и светофоров в красный и зеленый цвет. Содержание урана 0. 3 … 6 % UO 3. Уран вводится в шихту в виде одного из следующих соединений: - жёлтого ураната натрия Na 2 UO 4; - темно-зелёного U 3 O 3 = UO 2 + 2 UO 3; - оранжевого окисла UO 3; - коричневого окисла UO 2.
В начале XX в. не проводились ни добыча урана, ни разработка урановых руд, любое его производство было побочным. Уран получали для окрашивания керамики и стекол фонарей семафоров и светофоров в красный и зеленый цвет. Содержание урана 0. 3 … 6 % UO 3. Уран вводится в шихту в виде одного из следующих соединений: - жёлтого ураната натрия Na 2 UO 4; - темно-зелёного U 3 O 3 = UO 2 + 2 UO 3; - оранжевого окисла UO 3; - коричневого окисла UO 2.
 Архип Куинджи. Лунная ночь на Днепре. 1880 г.
Архип Куинджи. Лунная ночь на Днепре. 1880 г.
 Соли урана служили катализаторами окисления ароматических углеводородов и использовались в фотографии для окрашивания позитивов в коричневый цвет. Уран шел также на производство стали и сплавов, которые приобретали содержащий примерно 66% U и 33% Ni, устойчив даже в царской водке. Однако все эти применения имели весьма ограниченный масштаб. «Убежденный в том, что исследование урана поведет еще ко многим новым открытиям…» . Д. И. Менделеев, 1903 г.
Соли урана служили катализаторами окисления ароматических углеводородов и использовались в фотографии для окрашивания позитивов в коричневый цвет. Уран шел также на производство стали и сплавов, которые приобретали содержащий примерно 66% U и 33% Ni, устойчив даже в царской водке. Однако все эти применения имели весьма ограниченный масштаб. «Убежденный в том, что исследование урана поведет еще ко многим новым открытиям…» . Д. И. Менделеев, 1903 г.
 Анри Беккерель Открытие явления радиоактивности, 1896 г. 92 U 5 f 36 d 1 238. 0289 Клапрот 1789
Анри Беккерель Открытие явления радиоактивности, 1896 г. 92 U 5 f 36 d 1 238. 0289 Клапрот 1789
 Беккерель выдерживал на свету K 2 UO 2(SO 4) поверх фото пластинки, завернутой в черную бумагу. Между урановым препаратом и защитной бумагой он помещал металлические кольца, считая, что возбуждаемые солнечным светом Х-лучи легко пройдут сквозь бумагу, но будут задержаны металлом. В этом случае на пластинке должна появиться кольцевая тень. Опыты оказались успешными: после проявления на пластинке четко просматривались очертания кольца. В конце февраля настали ненастные дни, и приготовленные для опытов препараты и пластинки остались в ящике профессорского стола. Первого марта вновь засияло солнце, но пунктуальнейший Беккерель поставил опыт сравнения – «старые» пластинки были проявлены. Силуэты урановых препаратов и металлических колец оказались даже более четкими, чем в прежних «солнечных» экспериментах. Стало ясно, что проникающее излучение никак не связано с фосфоресценцией, и связано с наличием урана.
Беккерель выдерживал на свету K 2 UO 2(SO 4) поверх фото пластинки, завернутой в черную бумагу. Между урановым препаратом и защитной бумагой он помещал металлические кольца, считая, что возбуждаемые солнечным светом Х-лучи легко пройдут сквозь бумагу, но будут задержаны металлом. В этом случае на пластинке должна появиться кольцевая тень. Опыты оказались успешными: после проявления на пластинке четко просматривались очертания кольца. В конце февраля настали ненастные дни, и приготовленные для опытов препараты и пластинки остались в ящике профессорского стола. Первого марта вновь засияло солнце, но пунктуальнейший Беккерель поставил опыт сравнения – «старые» пластинки были проявлены. Силуэты урановых препаратов и металлических колец оказались даже более четкими, чем в прежних «солнечных» экспериментах. Стало ясно, что проникающее излучение никак не связано с фосфоресценцией, и связано с наличием урана.
 Три загадки планеты Уран • Кольца – невидимки. • Необычное направление оси его вращения, которая наклонена на 98 градусов, то есть ось вращения Урана лежит почти в плоскости его орбиты. Поэтому движение Урана вокруг Солнца совершенно особенное - он катится вдоль своей орбиты, переворачиваясь с боку на бок, подобно колобку. Такие особенности движения и вращения Урана не согласуются с общей картиной возникновения планет из допланетного облака, все части которого вращались в одном и том же направлении вокруг Солнца. • Уран излучает тепла не больше, чем получает от Солнца, следовательно и скорее всего, он холоден внутри. Напротив, тепловой поток от планет-гигантов в 2 -2, 5 раза больше получаемого от Солнца.
Три загадки планеты Уран • Кольца – невидимки. • Необычное направление оси его вращения, которая наклонена на 98 градусов, то есть ось вращения Урана лежит почти в плоскости его орбиты. Поэтому движение Урана вокруг Солнца совершенно особенное - он катится вдоль своей орбиты, переворачиваясь с боку на бок, подобно колобку. Такие особенности движения и вращения Урана не согласуются с общей картиной возникновения планет из допланетного облака, все части которого вращались в одном и том же направлении вокруг Солнца. • Уран излучает тепла не больше, чем получает от Солнца, следовательно и скорее всего, он холоден внутри. Напротив, тепловой поток от планет-гигантов в 2 -2, 5 раза больше получаемого от Солнца.
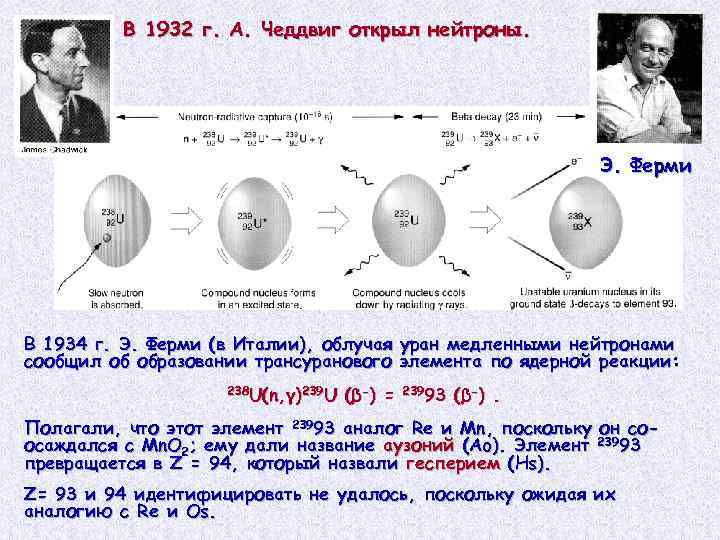 В 1932 г. А. Чеддвиг открыл нейтроны. Э. Ферми В 1934 г. Э. Ферми (в Италии), облучая уран медленными нейтронами сообщил об образовании трансуранового элемента по ядерной реакции: 238 U(n, γ)239 U ( β -) = 23993 ( β -). Полагали, что этот элемент 23993 аналог Re и Mn, поскольку он соосаждался с Mn. O 2; ему дали название аузоний (Ao). Элемент 23993 превращается в Z = 94, который назвали гесперием (Hs). Z= 93 и 94 идентифицировать не удалось, поскольку ожидая их аналогию с Re и Os.
В 1932 г. А. Чеддвиг открыл нейтроны. Э. Ферми В 1934 г. Э. Ферми (в Италии), облучая уран медленными нейтронами сообщил об образовании трансуранового элемента по ядерной реакции: 238 U(n, γ)239 U ( β -) = 23993 ( β -). Полагали, что этот элемент 23993 аналог Re и Mn, поскольку он соосаждался с Mn. O 2; ему дали название аузоний (Ao). Элемент 23993 превращается в Z = 94, который назвали гесперием (Hs). Z= 93 и 94 идентифицировать не удалось, поскольку ожидая их аналогию с Re и Os.
 В 1938 г. , О. Ган и Ф. Штрассман установили, что в результате нейтронной бомбардировки урана образуются продукты с химическими свойствами бария и лантана. В 1939 г. появилось письмо Л. Майтнер и О. Фриша, объяснявших эти результаты. Майтнер и Фриш впервые выдвинули термин «деление ядра» , оценили энергию его распада. Статьи Гана и Штрассмана, Майтнер и Фриша знаменовали новый этап в изучении свойств урана.
В 1938 г. , О. Ган и Ф. Штрассман установили, что в результате нейтронной бомбардировки урана образуются продукты с химическими свойствами бария и лантана. В 1939 г. появилось письмо Л. Майтнер и О. Фриша, объяснявших эти результаты. Майтнер и Фриш впервые выдвинули термин «деление ядра» , оценили энергию его распада. Статьи Гана и Штрассмана, Майтнер и Фриша знаменовали новый этап в изучении свойств урана.
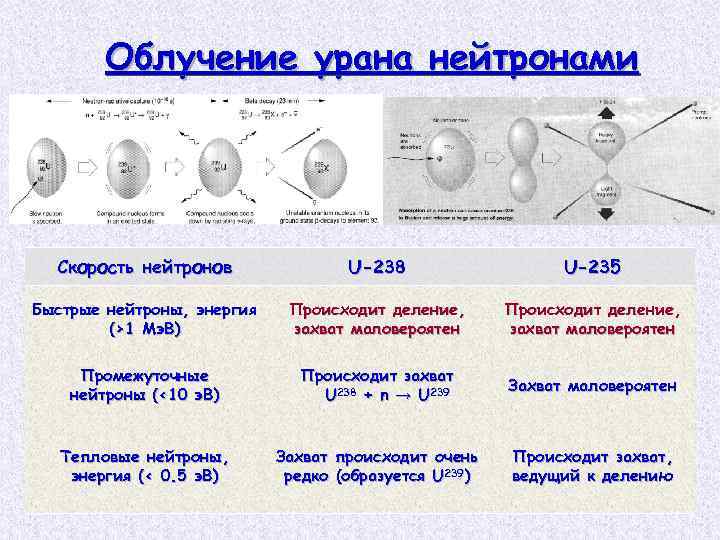 Облучение урана нейтронами Скорость нейтронов U-238 U-235 Быстрые нейтроны, энергия (>1 Мэ. В) Происходит деление, захват маловероятен Промежуточные нейтроны (<10 э. В) Происходит захват U 238 + n → U 239 Захват маловероятен Тепловые нейтроны, энергия (< 0. 5 э. В) Захват происходит очень редко (образуется U 239) Происходит захват, ведущий к делению
Облучение урана нейтронами Скорость нейтронов U-238 U-235 Быстрые нейтроны, энергия (>1 Мэ. В) Происходит деление, захват маловероятен Промежуточные нейтроны (<10 э. В) Происходит захват U 238 + n → U 239 Захват маловероятен Тепловые нейтроны, энергия (< 0. 5 э. В) Захват происходит очень редко (образуется U 239) Происходит захват, ведущий к делению
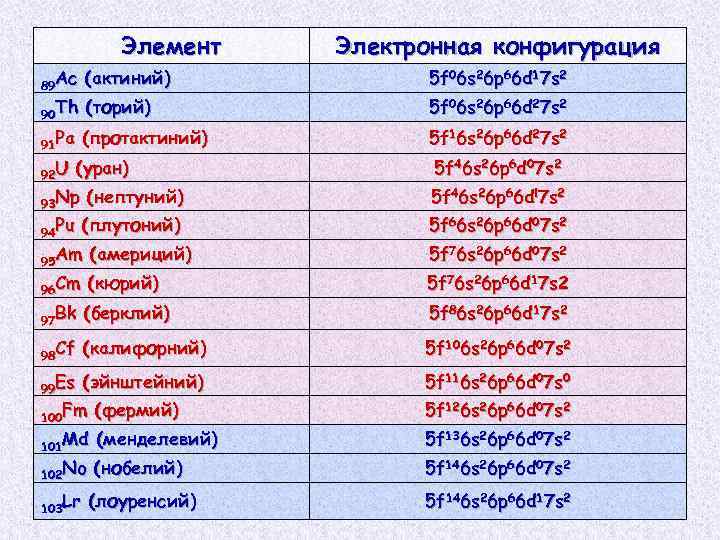 Элемент Электронная конфигурация 89 Ас (актиний) 5 f 06 s 26 p 66 d 17 s 2 90 Тh (торий) 5 f 06 s 26 p 66 d 27 s 2 91 Ра (протактиний) 5 f 16 s 26 p 66 d 27 s 2 92 U (уран) 93 Np 94 Рu 5 f 46 s 26 p 6 d 07 s 2 (нептуний) 5 f 46 s 26 p 66 dl 7 s 2 (плутоний) 5 f 66 s 26 p 66 d 07 s 2 95 Аm (америций) 5 f 76 s 26 p 66 d 07 s 2 96 Cm (кюрий) 5 f 76 s 26 p 66 d 17 s 2 97 Вk (берклий) 5 f 86 s 26 p 66 d 17 s 2 98 Cf (калифорний) 5 f 106 s 26 p 66 d 07 s 2 99 Es (эйнштейний) 5 f 116 s 26 p 66 d 07 s 0 100 Fm (фермий) 5 f 126 s 26 p 66 d 07 s 2 (менделевий) 5 f 136 s 26 p 66 d 07 s 2 102 No (нобелий) 5 f 146 s 26 p 66 d 07 s 2 (лоуренсий) 5 f 146 s 26 p 66 d 17 s 2 101 Md 103 Lr
Элемент Электронная конфигурация 89 Ас (актиний) 5 f 06 s 26 p 66 d 17 s 2 90 Тh (торий) 5 f 06 s 26 p 66 d 27 s 2 91 Ра (протактиний) 5 f 16 s 26 p 66 d 27 s 2 92 U (уран) 93 Np 94 Рu 5 f 46 s 26 p 6 d 07 s 2 (нептуний) 5 f 46 s 26 p 66 dl 7 s 2 (плутоний) 5 f 66 s 26 p 66 d 07 s 2 95 Аm (америций) 5 f 76 s 26 p 66 d 07 s 2 96 Cm (кюрий) 5 f 76 s 26 p 66 d 17 s 2 97 Вk (берклий) 5 f 86 s 26 p 66 d 17 s 2 98 Cf (калифорний) 5 f 106 s 26 p 66 d 07 s 2 99 Es (эйнштейний) 5 f 116 s 26 p 66 d 07 s 0 100 Fm (фермий) 5 f 126 s 26 p 66 d 07 s 2 (менделевий) 5 f 136 s 26 p 66 d 07 s 2 102 No (нобелий) 5 f 146 s 26 p 66 d 07 s 2 (лоуренсий) 5 f 146 s 26 p 66 d 17 s 2 101 Md 103 Lr
 Для начала цепной реакции делящийся материал должен образовывать критическую массу – достаточное количество расщепляющегося вещества, при котором число выделяющихся нейтронов больше числа поглощенных. Критическая масса, в кг Шар с Ø, см Бомбы США линзой U-235 50 кг 15 -23 кг 13 см Хиросима 60 кг Pu-239 5, 6 кг 0, 8 кг 4 см Нагасаки 6, 1 кг; 8 см
Для начала цепной реакции делящийся материал должен образовывать критическую массу – достаточное количество расщепляющегося вещества, при котором число выделяющихся нейтронов больше числа поглощенных. Критическая масса, в кг Шар с Ø, см Бомбы США линзой U-235 50 кг 15 -23 кг 13 см Хиросима 60 кг Pu-239 5, 6 кг 0, 8 кг 4 см Нагасаки 6, 1 кг; 8 см
 Содержание урана в природе Содержание U в земной коре 2. 10 -4 %, что в ~103 раз больше, чем Au; в 30 чем Ag; и столько же, сколько Zn и Pb. Уран распространенный элемент. В Черном море 2, 9. 10 -6 г/л, в Баренцевом море 1, 6. 10 -6 г/л. Известно >150 минералов, включающих U как важный компонент (>1%). Урановые минералы можно разделить на две основные группы: первичные и вторичные. Первичные находятся в магматических гидротермальных жилах и пегматитах. К первичным относят уранинит (UO 2) и урановая смолка (U 3 O 8) - наиболее рентабельные минералы, в которых содержится бòльшая часть мировых запасов U. В первичных минералах U имеет с. о. IV; они окрашены в черный или темные цвета. Вторичные же минералы обычно содержат уран (VI) и окрашены в яркие цвета от желтого и зеленого до красного.
Содержание урана в природе Содержание U в земной коре 2. 10 -4 %, что в ~103 раз больше, чем Au; в 30 чем Ag; и столько же, сколько Zn и Pb. Уран распространенный элемент. В Черном море 2, 9. 10 -6 г/л, в Баренцевом море 1, 6. 10 -6 г/л. Известно >150 минералов, включающих U как важный компонент (>1%). Урановые минералы можно разделить на две основные группы: первичные и вторичные. Первичные находятся в магматических гидротермальных жилах и пегматитах. К первичным относят уранинит (UO 2) и урановая смолка (U 3 O 8) - наиболее рентабельные минералы, в которых содержится бòльшая часть мировых запасов U. В первичных минералах U имеет с. о. IV; они окрашены в черный или темные цвета. Вторичные же минералы обычно содержат уран (VI) и окрашены в яркие цвета от желтого и зеленого до красного.
 Добыча урана в мире Суммарный объем добычи U в мире в 2007 г. составил 41 тыс. т. 10 стран обеспечивают >94% мирового производства: Канада, Австралия, Казахстан, Россия, Нигер, Намибия, Узбекистан, США, Украина и Китай. Лидером по добыче U в мире является Канада (9, 475 тыс. т). Второе - Австралия (8, 6 тыс. т). Казахстан с 2003 г - 3 место (6, 6 тыс. т, прирост в 2007 г 26%).
Добыча урана в мире Суммарный объем добычи U в мире в 2007 г. составил 41 тыс. т. 10 стран обеспечивают >94% мирового производства: Канада, Австралия, Казахстан, Россия, Нигер, Намибия, Узбекистан, США, Украина и Китай. Лидером по добыче U в мире является Канада (9, 475 тыс. т). Второе - Австралия (8, 6 тыс. т). Казахстан с 2003 г - 3 место (6, 6 тыс. т, прирост в 2007 г 26%).
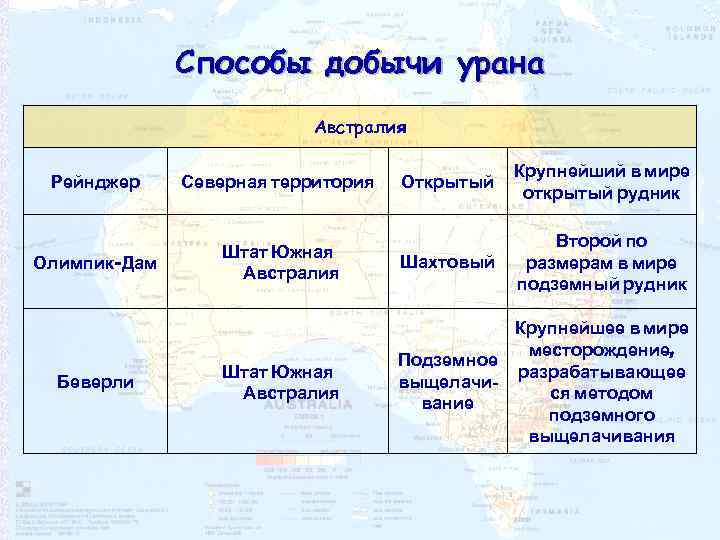 Способы добычи урана Австралия Открытый Крупнейший в мире открытый рудник Штат Южная Австралия Шахтовый Второй по размерам в мире подземный рудник Штат Южная Австралия Крупнейшее в мире месторождение, Подземное разрабатывающее выщелачися методом вание подземного выщелачивания Рейнджер Северная территория Олимпик-Дам Беверли
Способы добычи урана Австралия Открытый Крупнейший в мире открытый рудник Штат Южная Австралия Шахтовый Второй по размерам в мире подземный рудник Штат Южная Австралия Крупнейшее в мире месторождение, Подземное разрабатывающее выщелачися методом вание подземного выщелачивания Рейнджер Северная территория Олимпик-Дам Беверли
 Добыча урана в России 93 % - месторождение в Читинской обл. (г. Краснокаменск, «Приаргунское производственное горно-химическое объединение» , ТВЭЛ) шахтовым способом. 7 % - ЗАО «Далур» (Курганская обл. ) и ОАО «Хиагда» (Бурятия) методом подземного выщелачивания. Полученные руды и урановый концентрат перерабатываются на Чепецком механическом заводе. Природная окись урана U 3 O 8 стоит порядка 200$ за кг.
Добыча урана в России 93 % - месторождение в Читинской обл. (г. Краснокаменск, «Приаргунское производственное горно-химическое объединение» , ТВЭЛ) шахтовым способом. 7 % - ЗАО «Далур» (Курганская обл. ) и ОАО «Хиагда» (Бурятия) методом подземного выщелачивания. Полученные руды и урановый концентрат перерабатываются на Чепецком механическом заводе. Природная окись урана U 3 O 8 стоит порядка 200$ за кг.
 1. г. Силламяэ, Эстония. Разработка и переработка урано-фосфатных руд. 2. г. Желтые Воды, Днепропетровская обл. Разработка урано-железных руд. 3. г. Лермонтов, Ставропольский край. Разработка урано-молибденовых руд. 4. пос. Чупа, Карелия. Месторождение ураносодержащих материалов. 5. Северозападное побережье Онежского оз. Месторождение урана. 6. Ловозерская тундра, Кольский п-ов. Месторождение ураносодержащих минералов. 7. п. Вишневогорск, Челябинская обл. Месторождение ураносодержащих минералов. 8. п. Новогорный, Челябинская обл. Месторождение ураносодержащих минералов. 9. п. Аксуек, ст. Кияхты, Джамбульская обл. , Казахстан. Разработка урановых руд. 10. ст. Коктас, Джамбульская обл. Разработка ураносодержащих медных руд. 11. г. Степногорск, Целиноградская обл. , Казахстан. 12. пос. Ак-Тюз, п. Бордунский, Киргизия. Разработка уран- и торийсодержащих руд. 13. пос. Чигирик, Ташкентская обл. Переработка урановых руд. 14. пос. Гранитогорск, Джамбульская обл. Разработка урано-свинцовых руд. 15. пос. Мин-Куш, Нарынская обл. , Киргизия. Разработка ураносодержащих руд 16. пос. Тюя-Муюн, Ошская обл. , Киргизия. Месторождение урано-ванадиевых руд. 17. пос. Кызыл-Джар, Ошская обл. Разработка ураносодержаших руд. 18. пос. Каджи-Сай, Иссык-Кульская обл. , Киргизия. Разработка ураносодержащих руд. 19. пос. Табошар, Ленинабадская обл. , Таджикистан. Разработка урано-ванадиевых руд. 20. г. Чкаловск, Ленинабадская обл. Переработка табошарских руд. 21. пос. Сумсар, Таласская обл. , Киргизия. Разработка урановых руд. 22. г. Учкудук, Навоийская обл. , Узбекистан. Разработка ураносодержащих руд. 23. пос. Наугарзан, Леннабадская обл. Разработка урановых руд. 24. пос. Чаркесар, Наманганская обл. , Узбекистан. Разработка урановых руд. 25. пос. Чавлисак - г. Янгиабад, Ташкентская обл. Разработка урановых руд. 26. г. Кара-Балта, Киргизия. Переработка урановых руд. 27. г. Вихоревка, Иркутская обл. Разработка урано-ториевых руд. 28. г. Краснокаменск, Читинская обл. Месторождение урановых руд. 29. г. Слюдянка, Иркутская обл. Разработка урановых руд. 30. г. Алдан, Якутия. Разработка уран- и торийсодержащих руд.
1. г. Силламяэ, Эстония. Разработка и переработка урано-фосфатных руд. 2. г. Желтые Воды, Днепропетровская обл. Разработка урано-железных руд. 3. г. Лермонтов, Ставропольский край. Разработка урано-молибденовых руд. 4. пос. Чупа, Карелия. Месторождение ураносодержащих материалов. 5. Северозападное побережье Онежского оз. Месторождение урана. 6. Ловозерская тундра, Кольский п-ов. Месторождение ураносодержащих минералов. 7. п. Вишневогорск, Челябинская обл. Месторождение ураносодержащих минералов. 8. п. Новогорный, Челябинская обл. Месторождение ураносодержащих минералов. 9. п. Аксуек, ст. Кияхты, Джамбульская обл. , Казахстан. Разработка урановых руд. 10. ст. Коктас, Джамбульская обл. Разработка ураносодержащих медных руд. 11. г. Степногорск, Целиноградская обл. , Казахстан. 12. пос. Ак-Тюз, п. Бордунский, Киргизия. Разработка уран- и торийсодержащих руд. 13. пос. Чигирик, Ташкентская обл. Переработка урановых руд. 14. пос. Гранитогорск, Джамбульская обл. Разработка урано-свинцовых руд. 15. пос. Мин-Куш, Нарынская обл. , Киргизия. Разработка ураносодержащих руд 16. пос. Тюя-Муюн, Ошская обл. , Киргизия. Месторождение урано-ванадиевых руд. 17. пос. Кызыл-Джар, Ошская обл. Разработка ураносодержаших руд. 18. пос. Каджи-Сай, Иссык-Кульская обл. , Киргизия. Разработка ураносодержащих руд. 19. пос. Табошар, Ленинабадская обл. , Таджикистан. Разработка урано-ванадиевых руд. 20. г. Чкаловск, Ленинабадская обл. Переработка табошарских руд. 21. пос. Сумсар, Таласская обл. , Киргизия. Разработка урановых руд. 22. г. Учкудук, Навоийская обл. , Узбекистан. Разработка ураносодержащих руд. 23. пос. Наугарзан, Леннабадская обл. Разработка урановых руд. 24. пос. Чаркесар, Наманганская обл. , Узбекистан. Разработка урановых руд. 25. пос. Чавлисак - г. Янгиабад, Ташкентская обл. Разработка урановых руд. 26. г. Кара-Балта, Киргизия. Переработка урановых руд. 27. г. Вихоревка, Иркутская обл. Разработка урано-ториевых руд. 28. г. Краснокаменск, Читинская обл. Месторождение урановых руд. 29. г. Слюдянка, Иркутская обл. Разработка урановых руд. 30. г. Алдан, Якутия. Разработка уран- и торийсодержащих руд.
 лейкбогаит уранинит фергусонит карнотит эвксенит
лейкбогаит уранинит фергусонит карнотит эвксенит
 Искусственные изотопы урана М. ч. Свойства 232 α-излучатель; τ 233 делящийся нуклид; по своим ядерным свойствам близок к 235 U и 239 Ри. 237 β-излучатель; τ 1/2 = 68, 9 лет = 6, 75 дня
Искусственные изотопы урана М. ч. Свойства 232 α-излучатель; τ 233 делящийся нуклид; по своим ядерным свойствам близок к 235 U и 239 Ри. 237 β-излучатель; τ 1/2 = 68, 9 лет = 6, 75 дня
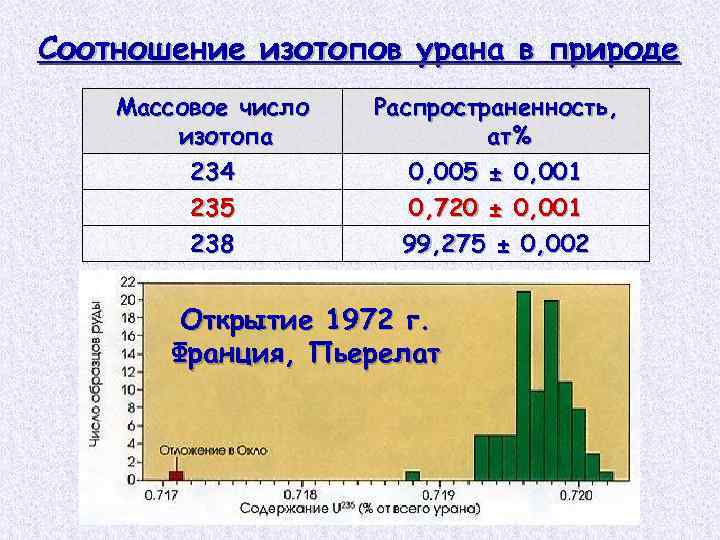 Соотношение изотопов урана в природе Массовое число изотопа 234 235 238 Распространенность, ат% 0, 005 ± 0, 001 0, 720 ± 0, 001 99, 275 ± 0, 002 Открытие 1972 г. Франция, Пьерелат
Соотношение изотопов урана в природе Массовое число изотопа 234 235 238 Распространенность, ат% 0, 005 ± 0, 001 0, 720 ± 0, 001 99, 275 ± 0, 002 Открытие 1972 г. Франция, Пьерелат
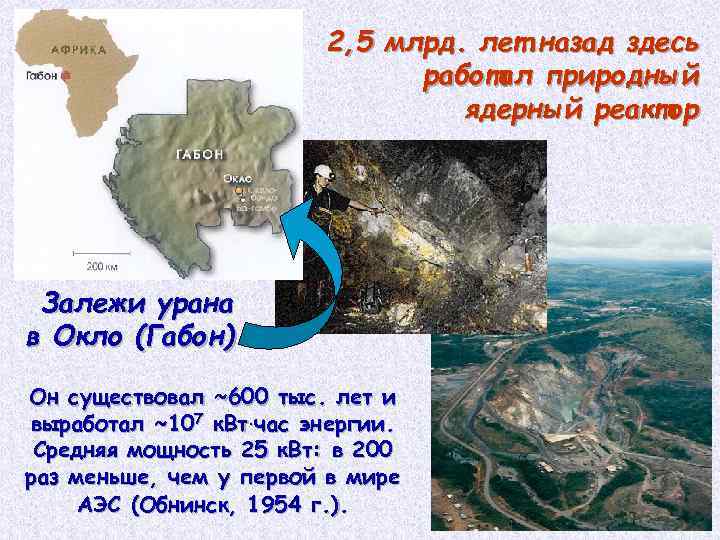 2, 5 млрд. лет назад здесь работал природный ядерный реактор Залежи урана в Окло (Габон) Он существовал ~600 тыс. лет и выработал ~107 к. Вт. час энергии. Средняя мощность 25 к. Вт: в 200 раз меньше, чем у первой в мире АЭС (Обнинск, 1954 г. ).
2, 5 млрд. лет назад здесь работал природный ядерный реактор Залежи урана в Окло (Габон) Он существовал ~600 тыс. лет и выработал ~107 к. Вт. час энергии. Средняя мощность 25 к. Вт: в 200 раз меньше, чем у первой в мире АЭС (Обнинск, 1954 г. ).
 „Феномен Окло заставляет вспомнить высказывание Э. Ферми, построившего первый ядерный реактор, и П. Л. Капицы, которые независимо друг от друга утверждали, что только человек способен создать нечто подобное. Однако древний природный реактор опровергает эту точку зрения, подтверждая мысль А. Эйнштейна о том, что Бог более изощрён…“ С. П. Капица
„Феномен Окло заставляет вспомнить высказывание Э. Ферми, построившего первый ядерный реактор, и П. Л. Капицы, которые независимо друг от друга утверждали, что только человек способен создать нечто подобное. Однако древний природный реактор опровергает эту точку зрения, подтверждая мысль А. Эйнштейна о том, что Бог более изощрён…“ С. П. Капица
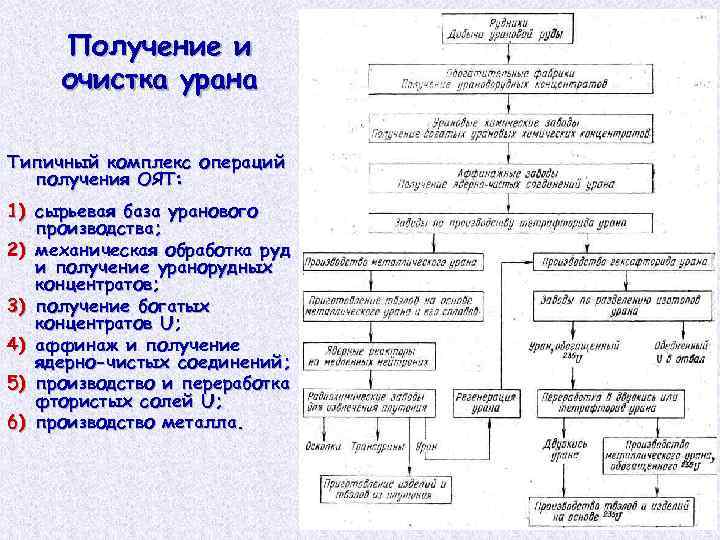 Получение и очистка урана Типичный комплекс операций получения ОЯТ: 1) сырьевая база уранового производства; 2) механическая обработка руд и получение уранорудных концентратов; 3) получение богатых концентратов U; 4) аффинаж и получение ядерно-чистых соединений; 5) производство и переработка фтористых солей U; 6) производство металла.
Получение и очистка урана Типичный комплекс операций получения ОЯТ: 1) сырьевая база уранового производства; 2) механическая обработка руд и получение уранорудных концентратов; 3) получение богатых концентратов U; 4) аффинаж и получение ядерно-чистых соединений; 5) производство и переработка фтористых солей U; 6) производство металла.
 Метод кучного выщелачивание урана § Перед выщелачиванием руду подвергают высокотемпературному кальцинированию. При окислительном отжиге уран переводят в растворимую форму, удаляя серу и другие мешающие примеси. При восстановительном обжиге уран переводят в нерастворимую форму для извлечения побочных растворимых продуктов. § Выщелачивание руды действием на нее кислых или щелочных реагентов – первая химическая стадия. Выбор реагента определяется химической природой минерала урана и рудными породами. Кислым реагентом обычно бывает серная кислота. Для уранинита и урановой смолки при выщелачивании вводят окислители (Mn. O 2, Fe. III, Cl 2, O 2). Наиболее часто используются Mn. O 2 (5 кг на тонну руды) и хлорат-ион (1, 5 кг на тонну руды) в присутствии железа в качестве катализатора.
Метод кучного выщелачивание урана § Перед выщелачиванием руду подвергают высокотемпературному кальцинированию. При окислительном отжиге уран переводят в растворимую форму, удаляя серу и другие мешающие примеси. При восстановительном обжиге уран переводят в нерастворимую форму для извлечения побочных растворимых продуктов. § Выщелачивание руды действием на нее кислых или щелочных реагентов – первая химическая стадия. Выбор реагента определяется химической природой минерала урана и рудными породами. Кислым реагентом обычно бывает серная кислота. Для уранинита и урановой смолки при выщелачивании вводят окислители (Mn. O 2, Fe. III, Cl 2, O 2). Наиболее часто используются Mn. O 2 (5 кг на тонну руды) и хлорат-ион (1, 5 кг на тонну руды) в присутствии железа в качестве катализатора.
 На урановых заводах, использующих традиционную технологию, до 99, 8% сырья на заводе сбрасывается в хвостохранилища. Это ~0, 9 т твердых и >3 м 3 жидких отходов на 1 т руды, то есть 1 т отходов на 1 кг извлеченного урана! Кара-балтийский гидрометаллургический завод
На урановых заводах, использующих традиционную технологию, до 99, 8% сырья на заводе сбрасывается в хвостохранилища. Это ~0, 9 т твердых и >3 м 3 жидких отходов на 1 т руды, то есть 1 т отходов на 1 кг извлеченного урана! Кара-балтийский гидрометаллургический завод
 Подземное выщелачивание Для рудных массивов, имеющих малую проницаемость подстилающей породы и подходящую пористость, выщелачивание состоит в закачивании кислого раствора в скважины руды, а обогащенный раствор откачивают из других скважин. Такая технология существенно снижает затраты на получения конечного продукта. Так, известно, что стоимость подземной добычи и транспортировки руды на завод составляет около 40% общей стоимости извлекаемого урана, в то время как расходы по подземному выщелачиванию и откачке продукционного раствора на урановый завод не превышают 5%.
Подземное выщелачивание Для рудных массивов, имеющих малую проницаемость подстилающей породы и подходящую пористость, выщелачивание состоит в закачивании кислого раствора в скважины руды, а обогащенный раствор откачивают из других скважин. Такая технология существенно снижает затраты на получения конечного продукта. Так, известно, что стоимость подземной добычи и транспортировки руды на завод составляет около 40% общей стоимости извлекаемого урана, в то время как расходы по подземному выщелачиванию и откачке продукционного раствора на урановый завод не превышают 5%.
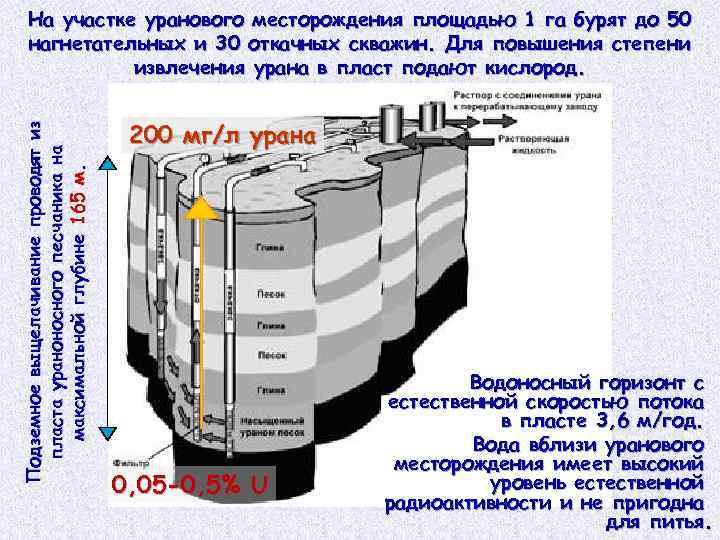 Подземное выщелачивание проводят из пласта ураноносного песчаника на максимальной глубине 165 м. На участке уранового месторождения площадью 1 га бурят до 50 нагнетательных и 30 откачных скважин. Для повышения степени извлечения урана в пласт подают кислород. 200 мг/л урана 0, 05 -0, 5% U Водоносный горизонт с естественной скоростью потока в пласте 3, 6 м/год. Вода вблизи уранового месторождения имеет высокий уровень естественной радиоактивности и не пригодна для питья.
Подземное выщелачивание проводят из пласта ураноносного песчаника на максимальной глубине 165 м. На участке уранового месторождения площадью 1 га бурят до 50 нагнетательных и 30 откачных скважин. Для повышения степени извлечения урана в пласт подают кислород. 200 мг/л урана 0, 05 -0, 5% U Водоносный горизонт с естественной скоростью потока в пласте 3, 6 м/год. Вода вблизи уранового месторождения имеет высокий уровень естественной радиоактивности и не пригодна для питья.
 Бактериальное подземное выщелачивание урана Бактериальное извлечение осуществляется в аэробных условиях при температурах окружающей среды под действием бактерии Thiobacillus ferrooxidans - одноклеточных организмов Ø 0, 25 мкм и длиной 1 мкм). При этом происходит окислительное растворение урана. Растворы для бактериального выщелачивания готовят в специальном бассейне, куда подают воздух и где с помощью бактерий Fe(II) окисляют до Fe(III). Затем растворы с р. Н 2, 5 2, 9 с содержанием Fe 3+ ~ 2, 0 г/л закачивают в скважины, через которые они поступают в рудоносный пласт при подземном выщелачивании или в систему орошения при кучном выщелачивании. После извлечения урана продукционные растворы возвращают в бактериальный бассейн для регенерации. Бактериальное выщелачивание пока не получило широкого распространения, однако как весьма перспективное направление изучается в опытно-промышленном масштабе.
Бактериальное подземное выщелачивание урана Бактериальное извлечение осуществляется в аэробных условиях при температурах окружающей среды под действием бактерии Thiobacillus ferrooxidans - одноклеточных организмов Ø 0, 25 мкм и длиной 1 мкм). При этом происходит окислительное растворение урана. Растворы для бактериального выщелачивания готовят в специальном бассейне, куда подают воздух и где с помощью бактерий Fe(II) окисляют до Fe(III). Затем растворы с р. Н 2, 5 2, 9 с содержанием Fe 3+ ~ 2, 0 г/л закачивают в скважины, через которые они поступают в рудоносный пласт при подземном выщелачивании или в систему орошения при кучном выщелачивании. После извлечения урана продукционные растворы возвращают в бактериальный бассейн для регенерации. Бактериальное выщелачивание пока не получило широкого распространения, однако как весьма перспективное направление изучается в опытно-промышленном масштабе.
 Извлечение урана их растворов Извлечение урана из растворов после кислотного или щелочного выщелачивания проводят различными методами: осаждение, ионный обмен и экстракция. Процессы избирательного осаждения урана применялись только на заре уранового производства в конце 1940 -1950 гг. и в настоящее от нее отказались. В схемах ионного обмена U(VI) извлекают из сульфатных или карбонатных растворов на анионообменных смолах. Десорбцию урана с анионообменных смол в сульфатном или карбонатном процессах обычно осуществляют с помощью 1 М Na. Cl или Na. NO 3. Несмотря на избирательность процесса, в кислых средах в качестве примесей ионитами удерживаются ванадаты, сульфатные комплексы молибдена, политионаты, цианидные комплексы кобальта и золота. В карбонатном процессе из "вредных" компонентов, ухудшающих сорбцию урана являются ванадат-, арсенат-, фосфат-, силикат-ионы, а также комплексы титана, тория, гафния, ниобия и сурьмы. Процесс экстракции имеет преимущество перед ионообменной, поскольку она осуществляется в непрерывном противоточном режиме. Экстракционную очистку урана от примесей впервые использовал еще в 40 -х годах IXX века Э. Пелиго. Он первый установил большую растворимость уранил-нитрата в диэтиловом эфире, что было использовано в ранних схемах аффинажа урана. Позднее диэтиловый эфир стал применяться в качестве экстрагента и при переработке облученного ядерного топлива.
Извлечение урана их растворов Извлечение урана из растворов после кислотного или щелочного выщелачивания проводят различными методами: осаждение, ионный обмен и экстракция. Процессы избирательного осаждения урана применялись только на заре уранового производства в конце 1940 -1950 гг. и в настоящее от нее отказались. В схемах ионного обмена U(VI) извлекают из сульфатных или карбонатных растворов на анионообменных смолах. Десорбцию урана с анионообменных смол в сульфатном или карбонатном процессах обычно осуществляют с помощью 1 М Na. Cl или Na. NO 3. Несмотря на избирательность процесса, в кислых средах в качестве примесей ионитами удерживаются ванадаты, сульфатные комплексы молибдена, политионаты, цианидные комплексы кобальта и золота. В карбонатном процессе из "вредных" компонентов, ухудшающих сорбцию урана являются ванадат-, арсенат-, фосфат-, силикат-ионы, а также комплексы титана, тория, гафния, ниобия и сурьмы. Процесс экстракции имеет преимущество перед ионообменной, поскольку она осуществляется в непрерывном противоточном режиме. Экстракционную очистку урана от примесей впервые использовал еще в 40 -х годах IXX века Э. Пелиго. Он первый установил большую растворимость уранил-нитрата в диэтиловом эфире, что было использовано в ранних схемах аффинажа урана. Позднее диэтиловый эфир стал применяться в качестве экстрагента и при переработке облученного ядерного топлива.
 При этом к ним предъявляли следующее требования: § высокий коэффициент распределения урана при экстракции, что является важнейшей характеристикой экстрагента; § его селективность и избирательность в отношении урана; § малая взаимная растворимость органического реагента в воде, и воды в нем, а также быстрое и полное расслоение фаз; § химическая, окислительная и радиационная стойкость экстрагента; § его минимальная летучесть, вязкость, токсичность; максимально высокая температура вспышки, а еще лучше полная негорючесть; § относительно невысокая стоимость, доступность и простота синтеза.
При этом к ним предъявляли следующее требования: § высокий коэффициент распределения урана при экстракции, что является важнейшей характеристикой экстрагента; § его селективность и избирательность в отношении урана; § малая взаимная растворимость органического реагента в воде, и воды в нем, а также быстрое и полное расслоение фаз; § химическая, окислительная и радиационная стойкость экстрагента; § его минимальная летучесть, вязкость, токсичность; максимально высокая температура вспышки, а еще лучше полная негорючесть; § относительно невысокая стоимость, доступность и простота синтеза.
 Классификация принятой в экстракционной технологии урана В первую группу включают нейтральные экстрагенты спирты, простые и сложные эфиры, альдегиды, кетоны и нейтральные фосфорорганические соединения. Экстракция металлов сопровождается образованием сольватов и проходит за счет их комплексообразования с вытеснением воды из внутренней координационной сферы комплекса: [UO 2(Н 2 O)6](NO 3)2 + 2(С 2 Н 5)2 O = [UO 2(Н 2 O)4(С 2 Н 5)2 O]2(N 03)2+2 Н 2 O Эти экстрагенты экстрагируют преимущественно из азотнокислых растворов и для них характерна очень высокая растворимость (емкость) образующихся сольватов в избытке растворителя. Она достигает в некоторых случаях растворимости уранил-нитрата в воде (56%): для диэтилового эфира до 51%, ТБФ до 25%, изоамилового спирта до 44%.
Классификация принятой в экстракционной технологии урана В первую группу включают нейтральные экстрагенты спирты, простые и сложные эфиры, альдегиды, кетоны и нейтральные фосфорорганические соединения. Экстракция металлов сопровождается образованием сольватов и проходит за счет их комплексообразования с вытеснением воды из внутренней координационной сферы комплекса: [UO 2(Н 2 O)6](NO 3)2 + 2(С 2 Н 5)2 O = [UO 2(Н 2 O)4(С 2 Н 5)2 O]2(N 03)2+2 Н 2 O Эти экстрагенты экстрагируют преимущественно из азотнокислых растворов и для них характерна очень высокая растворимость (емкость) образующихся сольватов в избытке растворителя. Она достигает в некоторых случаях растворимости уранил-нитрата в воде (56%): для диэтилового эфира до 51%, ТБФ до 25%, изоамилового спирта до 44%.
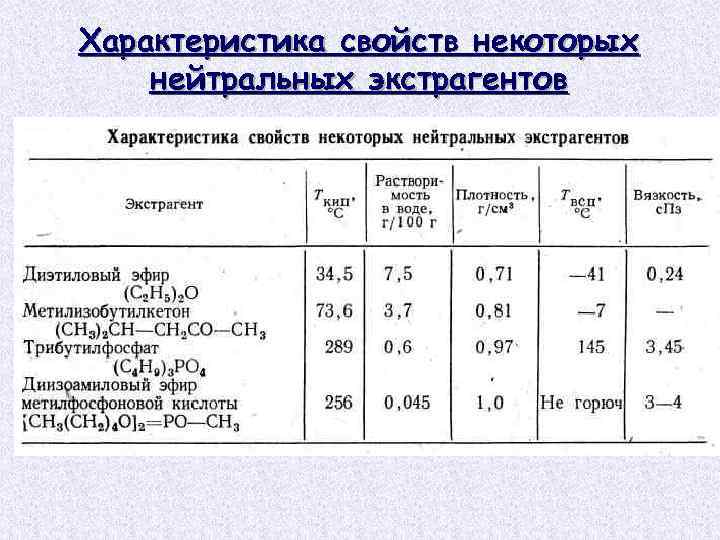 Характеристика свойств некоторых нейтральных экстрагентов
Характеристика свойств некоторых нейтральных экстрагентов
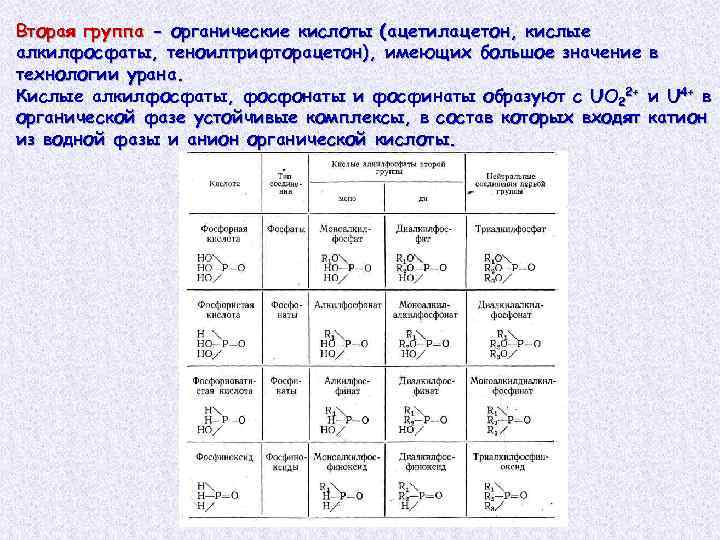 Вторая группа - органические кислоты (ацетилацетон, кислые алкилфосфаты, теноилтрифторацетон), имеющих большое значение в технологии урана. Кислые алкилфосфаты, фосфонаты и фосфинаты образуют с UO 22+ и U 4+ в органической фазе устойчивые комплексы, в состав которых входят катион из водной фазы и анион органической кислоты.
Вторая группа - органические кислоты (ацетилацетон, кислые алкилфосфаты, теноилтрифторацетон), имеющих большое значение в технологии урана. Кислые алкилфосфаты, фосфонаты и фосфинаты образуют с UO 22+ и U 4+ в органической фазе устойчивые комплексы, в состав которых входят катион из водной фазы и анион органической кислоты.
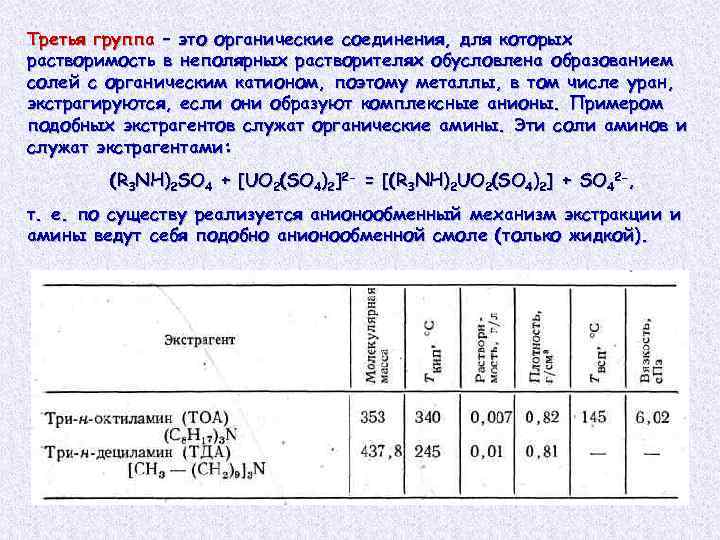 Третья группа – это органические соединения, для которых растворимость в неполярных растворителях обусловлена образованием солей с органическим катионом, поэтому металлы, в том числе уран, экстрагируются, если они образуют комплексные анионы. Примером подобных экстрагентов служат органические амины. Эти соли аминов и служат экстрагентами: (R 3 NH)2 SО 4 + [UО 2(SО 4)2]2 - = [(R 3 NH)2 UО 2(SО 4)2] + SO 42 -, т. е. по существу реализуется анионообменный механизм экстракции и амины ведут себя подобно анионообменной смоле (только жидкой).
Третья группа – это органические соединения, для которых растворимость в неполярных растворителях обусловлена образованием солей с органическим катионом, поэтому металлы, в том числе уран, экстрагируются, если они образуют комплексные анионы. Примером подобных экстрагентов служат органические амины. Эти соли аминов и служат экстрагентами: (R 3 NH)2 SО 4 + [UО 2(SО 4)2]2 - = [(R 3 NH)2 UО 2(SО 4)2] + SO 42 -, т. е. по существу реализуется анионообменный механизм экстракции и амины ведут себя подобно анионообменной смоле (только жидкой).
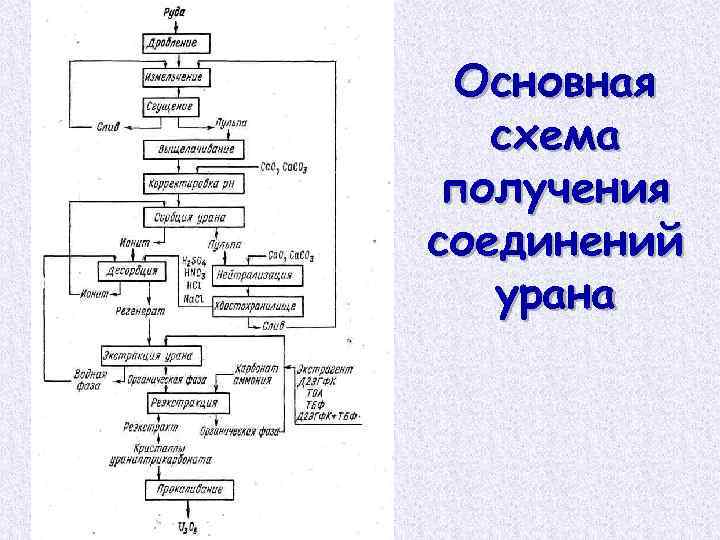 Основная схема получения соединений урана
Основная схема получения соединений урана
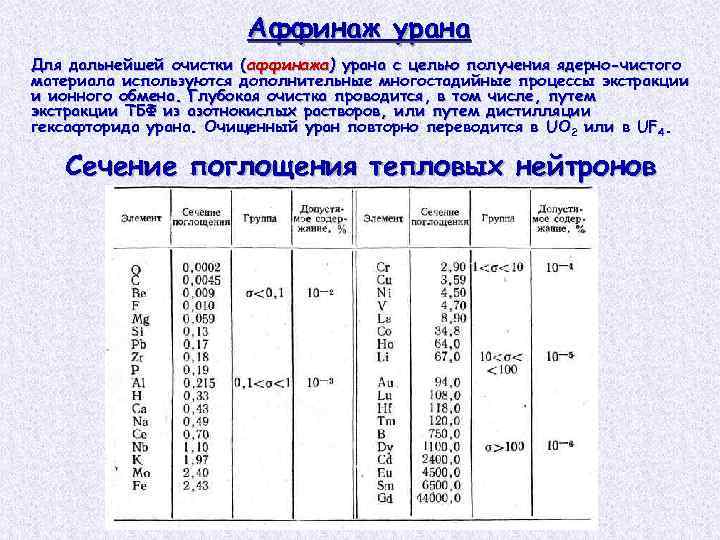 Аффинаж урана Для дальнейшей очистки (аффинажа) урана с целью получения ядерно-чистого материала используются дополнительные многостадийные процессы экстракции и ионного обмена. Глубокая очистка проводится, в том числе, путем экстракции ТБФ из азотнокислых растворов, или путем дистилляции гексафторида урана. Очищенный уран повторно переводится в UO 2 или в UF 4. Сечение поглощения тепловых нейтронов
Аффинаж урана Для дальнейшей очистки (аффинажа) урана с целью получения ядерно-чистого материала используются дополнительные многостадийные процессы экстракции и ионного обмена. Глубокая очистка проводится, в том числе, путем экстракции ТБФ из азотнокислых растворов, или путем дистилляции гексафторида урана. Очищенный уран повторно переводится в UO 2 или в UF 4. Сечение поглощения тепловых нейтронов
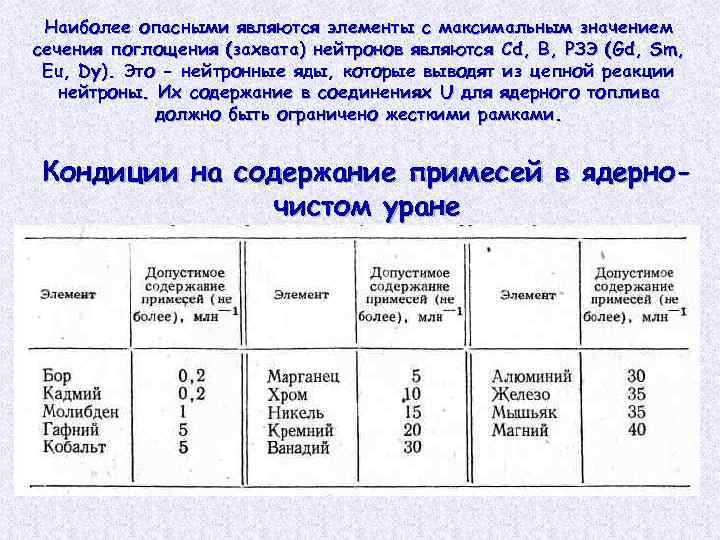 Наиболее опасными являются элементы с максимальным значением сечения поглощения (захвата) нейтронов являются Cd, В, РЗЭ (Gd, Sm, Eu, Dy). Это - нейтронные яды, которые выводят из цепной реакции нейтроны. Их содержание в соединениях U для ядерного топлива должно быть ограничено жесткими рамками. Кондиции на содержание примесей в ядерночистом уране
Наиболее опасными являются элементы с максимальным значением сечения поглощения (захвата) нейтронов являются Cd, В, РЗЭ (Gd, Sm, Eu, Dy). Это - нейтронные яды, которые выводят из цепной реакции нейтроны. Их содержание в соединениях U для ядерного топлива должно быть ограничено жесткими рамками. Кондиции на содержание примесей в ядерночистом уране
 Методы аффинажа урана Пероксидная очистка Метод пероксидной очистки основан на выделении из раствора пероксида урана UО 4. 2 H 2 О. Схема пероксидной очистки проста, но имеет особые правила: 1) реакция осаждения UО 4. 2 H 2 О протекает по уравнению: UО 2(NО 3)2 + Н 2 О 2 + 2 Н 2 О = UO 4. 2 Н 2 О + 2 HNО 3 в котором необходим избыток Н 2 О 2 и дальнейшая нейтрализация продукта; 2) необходимо избегать разогрева, т. к. Н 2 О 2 разрушается; 3) надо стремиться получить относительно хорошо фильтрующийся осадок, чего обычно достигают медленным введением осадителя.
Методы аффинажа урана Пероксидная очистка Метод пероксидной очистки основан на выделении из раствора пероксида урана UО 4. 2 H 2 О. Схема пероксидной очистки проста, но имеет особые правила: 1) реакция осаждения UО 4. 2 H 2 О протекает по уравнению: UО 2(NО 3)2 + Н 2 О 2 + 2 Н 2 О = UO 4. 2 Н 2 О + 2 HNО 3 в котором необходим избыток Н 2 О 2 и дальнейшая нейтрализация продукта; 2) необходимо избегать разогрева, т. к. Н 2 О 2 разрушается; 3) надо стремиться получить относительно хорошо фильтрующийся осадок, чего обычно достигают медленным введением осадителя.
 Методы аффинажа урана Карбонатная очистка Один из совершенных и эффективных методов аффинажа урана: трикарбонатная очистка, основанная на образовании устойчивого комплексного соединения (NН 4)4[UO 2(СOз)з] на существование которого впервые указал Берцелиус еще в 1824 г. Это тяжелые зеленовато-желтые кристаллы моноклинной сингонии. Они хорошо растворяются в воде, но высаливаются под действием одноименного иона. Следовательно, добавкой карбоната аммония уран в виде (NH 4)4[UО 2(CО 3)3] можно полностью в осадок. Кроме того, уран можно выделить в осадок в виде монокарбоната при кипячении раствора.
Методы аффинажа урана Карбонатная очистка Один из совершенных и эффективных методов аффинажа урана: трикарбонатная очистка, основанная на образовании устойчивого комплексного соединения (NН 4)4[UO 2(СOз)з] на существование которого впервые указал Берцелиус еще в 1824 г. Это тяжелые зеленовато-желтые кристаллы моноклинной сингонии. Они хорошо растворяются в воде, но высаливаются под действием одноименного иона. Следовательно, добавкой карбоната аммония уран в виде (NH 4)4[UО 2(CО 3)3] можно полностью в осадок. Кроме того, уран можно выделить в осадок в виде монокарбоната при кипячении раствора.
 Методы аффинажа урана Экстракционный аффинаж урана Впервые экстракционный процесс для очистки урана применил Пелиго в 1842 г используя диэтиловый эфир. Этот же эфир использовали американцы через 100 лет, в 1942 г. , для тонкой очистки технической U 3 O 8 при изготовлении первой атомной бомбы. Таким путём получали ядерноочистную UO 2 с содержанием примесей 10 -4 - 10 -5%. В 1947 г. Уорф предложил трибутилфосфат (ТБФ) в качестве экстрагента для урана. В 1950 - 1954 гг. были разработаны и проверены схемы экстракционного аффинажа урана с применением ТБФ. Ввысокая плотность ТБФ (0, 973 г/см 3) обусловливает необходимость применения инертных органических разбавителей: керосина, бензола, ССl 4, дибутилового эфира, гексана. Керосин - высококипящая фракция предельных углеводородов, практически не нитруется, не корродирует аппаратуру. Поэтому на практике для аффинажа применяют 30 -40%-ный раствор ТБФ в керосине. ТБФ растворяется в воде до 0, 2 - 0, 4 г/л. Н 2 О растворяется в ТБФ от 1, 4 г/л (10% ТБФ) до 64 г/л (100% ТБФ).
Методы аффинажа урана Экстракционный аффинаж урана Впервые экстракционный процесс для очистки урана применил Пелиго в 1842 г используя диэтиловый эфир. Этот же эфир использовали американцы через 100 лет, в 1942 г. , для тонкой очистки технической U 3 O 8 при изготовлении первой атомной бомбы. Таким путём получали ядерноочистную UO 2 с содержанием примесей 10 -4 - 10 -5%. В 1947 г. Уорф предложил трибутилфосфат (ТБФ) в качестве экстрагента для урана. В 1950 - 1954 гг. были разработаны и проверены схемы экстракционного аффинажа урана с применением ТБФ. Ввысокая плотность ТБФ (0, 973 г/см 3) обусловливает необходимость применения инертных органических разбавителей: керосина, бензола, ССl 4, дибутилового эфира, гексана. Керосин - высококипящая фракция предельных углеводородов, практически не нитруется, не корродирует аппаратуру. Поэтому на практике для аффинажа применяют 30 -40%-ный раствор ТБФ в керосине. ТБФ растворяется в воде до 0, 2 - 0, 4 г/л. Н 2 О растворяется в ТБФ от 1, 4 г/л (10% ТБФ) до 64 г/л (100% ТБФ).
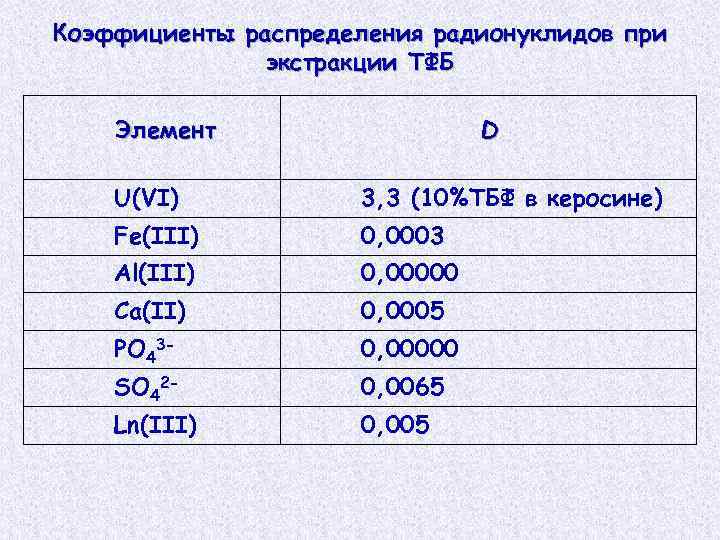 Коэффициенты распределения радионуклидов при экстракции ТФБ Элемент D U(VI) 3, 3 (10%ТБФ в керосине) Fe(III) 0, 0003 Al(III) 0, 00000 Ca(II) 0, 0005 PO 43 - 0, 00000 SO 42 - 0, 0065 Ln(III) 0, 005
Коэффициенты распределения радионуклидов при экстракции ТФБ Элемент D U(VI) 3, 3 (10%ТБФ в керосине) Fe(III) 0, 0003 Al(III) 0, 00000 Ca(II) 0, 0005 PO 43 - 0, 00000 SO 42 - 0, 0065 Ln(III) 0, 005
 Физические свойства урана Уран очень тяжёлый, серебристо-белый глянцеватый металл. В чистом виде он немного мягче стали, ковкий, гибкий, обладает небольшими парамагнитными свойствами. Уран имеет три аллотропные формы: альфа (призматическая, стабильна до 667, 7 °C), бета (четырёхугольная, стабильна от 667, 7 °C до 774, 8 °C), гамма (с объёмно центрированной кубической структурой, существующей от 774, 8 °C до точки плавления). Основные физические свойства урана: температура плавления температура кипения плотность (в альфа-фазе) 1132 °C; 3818 °C; 18. 95 г/см 3; удельная теплоемкость 6. 65 кал/моль/°C; прочность на разрыв 450 МПа.
Физические свойства урана Уран очень тяжёлый, серебристо-белый глянцеватый металл. В чистом виде он немного мягче стали, ковкий, гибкий, обладает небольшими парамагнитными свойствами. Уран имеет три аллотропные формы: альфа (призматическая, стабильна до 667, 7 °C), бета (четырёхугольная, стабильна от 667, 7 °C до 774, 8 °C), гамма (с объёмно центрированной кубической структурой, существующей от 774, 8 °C до точки плавления). Основные физические свойства урана: температура плавления температура кипения плотность (в альфа-фазе) 1132 °C; 3818 °C; 18. 95 г/см 3; удельная теплоемкость 6. 65 кал/моль/°C; прочность на разрыв 450 МПа.
 Влияние облучения на уран Блоки из металлического урана при облучении в ядерном реакторе приводят к структурным и размерным изменениям. Блок удлиняется, круглое сечение становится эллиптическим, наблюдается шероховатость и коробление поверхности. Для стабилизации размеров уран легируют ( «доводка» ) путем введения легирующих добавок. Типичное урановое топливо с "доводкой" содержит 0, 025% Fe; 0, 08% Аl; 0, 035% Si и 0, 06% С. Рекомендованы блоки (твелы), представляющие собой полый сердечник из U с добавкой 0, 04% Fe; 0, 1% Аl; окруженный оболочкой из Zr – Mo – Nb.
Влияние облучения на уран Блоки из металлического урана при облучении в ядерном реакторе приводят к структурным и размерным изменениям. Блок удлиняется, круглое сечение становится эллиптическим, наблюдается шероховатость и коробление поверхности. Для стабилизации размеров уран легируют ( «доводка» ) путем введения легирующих добавок. Типичное урановое топливо с "доводкой" содержит 0, 025% Fe; 0, 08% Аl; 0, 035% Si и 0, 06% С. Рекомендованы блоки (твелы), представляющие собой полый сердечник из U с добавкой 0, 04% Fe; 0, 1% Аl; окруженный оболочкой из Zr – Mo – Nb.
 Химические свойства урана Химически уран очень активный металл. Быстро окисляясь на воздухе, он покрывается радужной пленкой оксида. Мелкий порошок урана самовоспламеняется на воздухе, он зажигается при температуре 150 -175 °C, образуя U 3 O 8. При 1000 °C уран соединяется с азотом, образуя желтый нитрид урана. Вода способна разъедать металл, медленно при низкой температуре, и быстро при высокой. Уран растворяется в соляной, азотной и других кислотах, образуя четырехвалентные соли, зато не взаимодействует с щелочами. Уран вытесняет водород из неорганических кислот и солевых растворов таких металлов как ртуть, серебро, медь, олово, платина и золото. При сильном встряхивании металлические частицы урана начинают светиться. III Степени окисления урана IV V VI
Химические свойства урана Химически уран очень активный металл. Быстро окисляясь на воздухе, он покрывается радужной пленкой оксида. Мелкий порошок урана самовоспламеняется на воздухе, он зажигается при температуре 150 -175 °C, образуя U 3 O 8. При 1000 °C уран соединяется с азотом, образуя желтый нитрид урана. Вода способна разъедать металл, медленно при низкой температуре, и быстро при высокой. Уран растворяется в соляной, азотной и других кислотах, образуя четырехвалентные соли, зато не взаимодействует с щелочами. Уран вытесняет водород из неорганических кислот и солевых растворов таких металлов как ртуть, серебро, медь, олово, платина и золото. При сильном встряхивании металлические частицы урана начинают светиться. III Степени окисления урана IV V VI
 Оксиды урана В литературе известно о следующих оксидах урана (приводятся в порядке увеличения отношения O/U): UO, UO 2, U 4 O 9, U 16 O 37, U 3 O 7, U 8 O 19, U 2 O 5, U 5 O 13, U 13 O 34, U 8 О 21, U 11 О 29, U 3 О 8, U 12 O 35 и UO 3. На практике особо важны следующие оксиды урана: UO 2 + O 2 = U 3 O 8 (700 o. C) UO 2 C 2 O 4 = UO 3 + CO 2 + CO (350 o. C) U 308 + 2 СО = 3 U 02 + 2 С 02 (750 o. C) UO 2 - применяется в качестве ядерного топлива, в том числе МОКС топлива с Pu. O 2; U 3 О 8 – исходное вещество для получения соединений урана; UO 3 - удобен для хранения, продукт получения всех соединений U(VI).
Оксиды урана В литературе известно о следующих оксидах урана (приводятся в порядке увеличения отношения O/U): UO, UO 2, U 4 O 9, U 16 O 37, U 3 O 7, U 8 O 19, U 2 O 5, U 5 O 13, U 13 O 34, U 8 О 21, U 11 О 29, U 3 О 8, U 12 O 35 и UO 3. На практике особо важны следующие оксиды урана: UO 2 + O 2 = U 3 O 8 (700 o. C) UO 2 C 2 O 4 = UO 3 + CO 2 + CO (350 o. C) U 308 + 2 СО = 3 U 02 + 2 С 02 (750 o. C) UO 2 - применяется в качестве ядерного топлива, в том числе МОКС топлива с Pu. O 2; U 3 О 8 – исходное вещество для получения соединений урана; UO 3 - удобен для хранения, продукт получения всех соединений U(VI).
 На ПО Маяк впервые созданы новые топливные композиции на основе нанофракций диоксида урана Определены условия приготовления нанодисперсных порошков UO 2, исследованы их физико-химические свойства и реакционная способность в зависимости от способов получения и хранения. Показано, что введение наноструктурированной фракции диоксида урана к товарному UO 2 приводит к существенному повышению керамического качества таблетки МОКС-топлива (пористость, гомогенность распределения металлов, однородность образовавшихся твердых растворов). SБЭТ = 10 м 2/г; Ø 100 -120 нм Стандартная микроструктура ядерного топлива, полученного с использованием нанодобавок
На ПО Маяк впервые созданы новые топливные композиции на основе нанофракций диоксида урана Определены условия приготовления нанодисперсных порошков UO 2, исследованы их физико-химические свойства и реакционная способность в зависимости от способов получения и хранения. Показано, что введение наноструктурированной фракции диоксида урана к товарному UO 2 приводит к существенному повышению керамического качества таблетки МОКС-топлива (пористость, гомогенность распределения металлов, однородность образовавшихся твердых растворов). SБЭТ = 10 м 2/г; Ø 100 -120 нм Стандартная микроструктура ядерного топлива, полученного с использованием нанодобавок
 Фториды урана Тетрафторид урана - твердое нелетучее негигроскопичное вещество изумрудно-зеленого цвета, не растворимое в воде, получают методами высокотемпературного синтеза: UО 2 + 4 HF = UF 4 + 2 Н 2 О. Гексафторид урана - бесцветное кристаллическое вещество, возгоняется при 56, 5 °С при атмосферном давлении минуя жидкую фазу. Получают прямым фторированием твердого тетрафторида урана: UF 4 + F 2 = UF 6 Благодаря высокой летучести нашел широкое промышленное применение для разделения изотопов урана. Первые технологии получения тоннажных количеств UF 6 были разработаны в рамках Атомного проекта в СССР и в США. UF 6 поставляется на газодиффузионные заводы в твердом виде в контейнерах вместимостью до 14 т. Контейнер с UF 6 нагревают паром до температуры возгонки. Газообразный UF 6 перетекает в диффузионный каскад, где и происходит последующее изотопное разделение.
Фториды урана Тетрафторид урана - твердое нелетучее негигроскопичное вещество изумрудно-зеленого цвета, не растворимое в воде, получают методами высокотемпературного синтеза: UО 2 + 4 HF = UF 4 + 2 Н 2 О. Гексафторид урана - бесцветное кристаллическое вещество, возгоняется при 56, 5 °С при атмосферном давлении минуя жидкую фазу. Получают прямым фторированием твердого тетрафторида урана: UF 4 + F 2 = UF 6 Благодаря высокой летучести нашел широкое промышленное применение для разделения изотопов урана. Первые технологии получения тоннажных количеств UF 6 были разработаны в рамках Атомного проекта в СССР и в США. UF 6 поставляется на газодиффузионные заводы в твердом виде в контейнерах вместимостью до 14 т. Контейнер с UF 6 нагревают паром до температуры возгонки. Газообразный UF 6 перетекает в диффузионный каскад, где и происходит последующее изотопное разделение.
 Газофторидный метод переработки ОЯТ Газофторидный метод переработки основан на фторировании ОЯТ молекулярным фтором в аппаратах различного типа. Основные параметры процесса фторирования в аппарате движущегося слоя: § производительность до 30 кг/час при рабочей температуре 4500 С без дробление ОЯТ; § U, Pu выделяются в виде летучих UF 6 и Pu. F 6; § фториды ПД образуют нерастворимые фториды. Эксперименты, проведенные на установке «Фрегат» (НИИАР), показали возможность осуществления газофторидной переработки облучённого МОКС-топлива БОР-60 (68% U, 13%Pu, 19% ПД+ О 2) с использованием миниатюрного пламенного реактора фторирования. Было показало, что U на ~99% а Pu на 90% переходит в гексафториды и требуется дополнительное фторирование шлаков ( «огарков» ) для полного перевода плутония в Pu. F 6.
Газофторидный метод переработки ОЯТ Газофторидный метод переработки основан на фторировании ОЯТ молекулярным фтором в аппаратах различного типа. Основные параметры процесса фторирования в аппарате движущегося слоя: § производительность до 30 кг/час при рабочей температуре 4500 С без дробление ОЯТ; § U, Pu выделяются в виде летучих UF 6 и Pu. F 6; § фториды ПД образуют нерастворимые фториды. Эксперименты, проведенные на установке «Фрегат» (НИИАР), показали возможность осуществления газофторидной переработки облучённого МОКС-топлива БОР-60 (68% U, 13%Pu, 19% ПД+ О 2) с использованием миниатюрного пламенного реактора фторирования. Было показало, что U на ~99% а Pu на 90% переходит в гексафториды и требуется дополнительное фторирование шлаков ( «огарков» ) для полного перевода плутония в Pu. F 6.
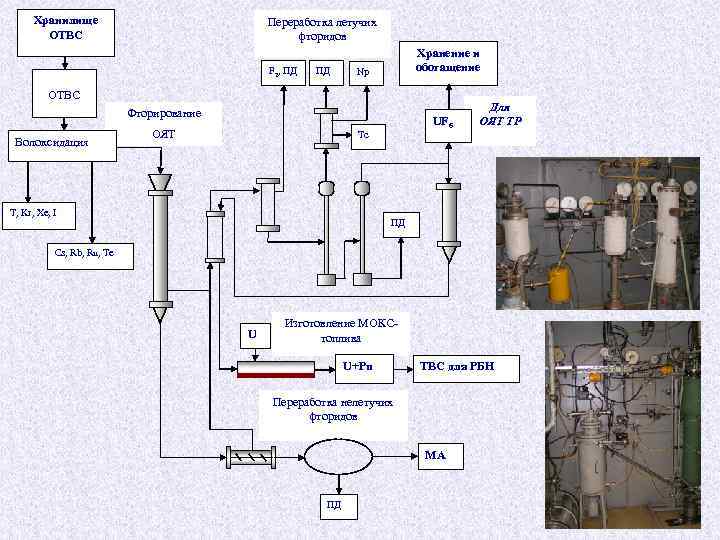 Хранилище ОТВС Переработка летучих фторидов F 2, ПД Резка ОТВС ПД Хранение и обогащение Np Фторирование Волоксидация ОЯТ UF 6 Tc T, Kr, Xe, I Для ОЯТ ТР ПД Cs, Rb, Ru, Te U Изготовление МОКСтоплива U+Pu ТВС для РБН Переработка нелетучих фторидов МА ПД
Хранилище ОТВС Переработка летучих фторидов F 2, ПД Резка ОТВС ПД Хранение и обогащение Np Фторирование Волоксидация ОЯТ UF 6 Tc T, Kr, Xe, I Для ОЯТ ТР ПД Cs, Rb, Ru, Te U Изготовление МОКСтоплива U+Pu ТВС для РБН Переработка нелетучих фторидов МА ПД
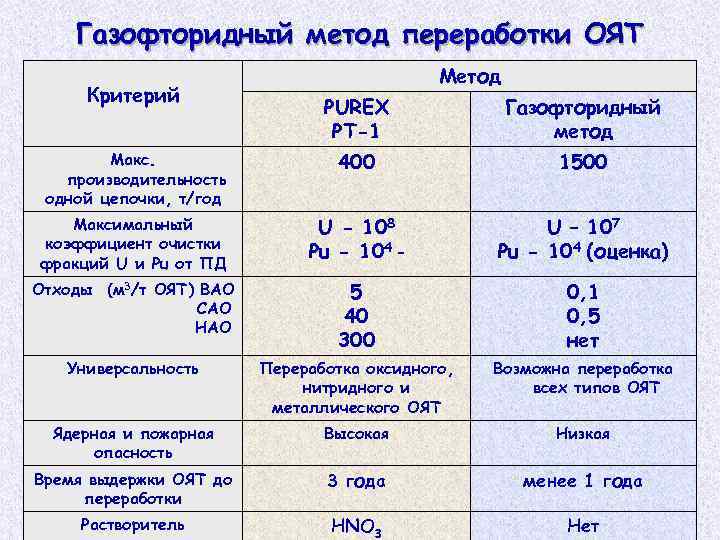 Газофторидный метод переработки ОЯТ Критерий Метод PUREX РТ-1 Газофторидный метод Макс. производительность одной цепочки, т/год 400 1500 Максимальный коэффициент очистки фракций U и Pu от ПД U - 108 Pu - 104 ‑ U – 107 Pu - 104 (оценка) Отходы (м 3/т ОЯТ) ВАО САО НАО 5 40 300 0, 1 0, 5 нет Универсальность Переработка оксидного, нитридного и металлического ОЯТ Возможна переработка всех типов ОЯТ Ядерная и пожарная опасность Высокая Низкая Время выдержки ОЯТ до переработки 3 года менее 1 года Растворитель HNO 3 Нет
Газофторидный метод переработки ОЯТ Критерий Метод PUREX РТ-1 Газофторидный метод Макс. производительность одной цепочки, т/год 400 1500 Максимальный коэффициент очистки фракций U и Pu от ПД U - 108 Pu - 104 ‑ U – 107 Pu - 104 (оценка) Отходы (м 3/т ОЯТ) ВАО САО НАО 5 40 300 0, 1 0, 5 нет Универсальность Переработка оксидного, нитридного и металлического ОЯТ Возможна переработка всех типов ОЯТ Ядерная и пожарная опасность Высокая Низкая Время выдержки ОЯТ до переработки 3 года менее 1 года Растворитель HNO 3 Нет
 Соединения урана, получаемые из водных растворов В водных растворах уран наиболее устойчив в с. о. (VI) в виде UО 22+, в меньшей степени для него характерно состояние U 4+, но он может находится даже в виде U 3+. Пятивалентный уран существует в растворе в виде ураноил-иона UO 2+. Для Pa(V) существует уникальная ионная форма Pa. O 3+. Уменьшение Ø ядра U приводит к увеличению его ионного потенциала φ = Z/r 2 и присоединению второго атома кислорода с образованием катиона МO 2+, который характерен и для других актинидов. U(V) существует только в сильно комплексообразующей среде при р. Н 2 -2, 5 вследствие склонности к диспропорционированию и гидролизу. Как правило, U(V) - лишь промежуточное состояние в окислительновосстановительных реакциях с участием U(IV) и U(VI). Из растворов U 3+, U 4+ и UО 22+ было получено большое число твердых соединений.
Соединения урана, получаемые из водных растворов В водных растворах уран наиболее устойчив в с. о. (VI) в виде UО 22+, в меньшей степени для него характерно состояние U 4+, но он может находится даже в виде U 3+. Пятивалентный уран существует в растворе в виде ураноил-иона UO 2+. Для Pa(V) существует уникальная ионная форма Pa. O 3+. Уменьшение Ø ядра U приводит к увеличению его ионного потенциала φ = Z/r 2 и присоединению второго атома кислорода с образованием катиона МO 2+, который характерен и для других актинидов. U(V) существует только в сильно комплексообразующей среде при р. Н 2 -2, 5 вследствие склонности к диспропорционированию и гидролизу. Как правило, U(V) - лишь промежуточное состояние в окислительновосстановительных реакциях с участием U(IV) и U(VI). Из растворов U 3+, U 4+ и UО 22+ было получено большое число твердых соединений.
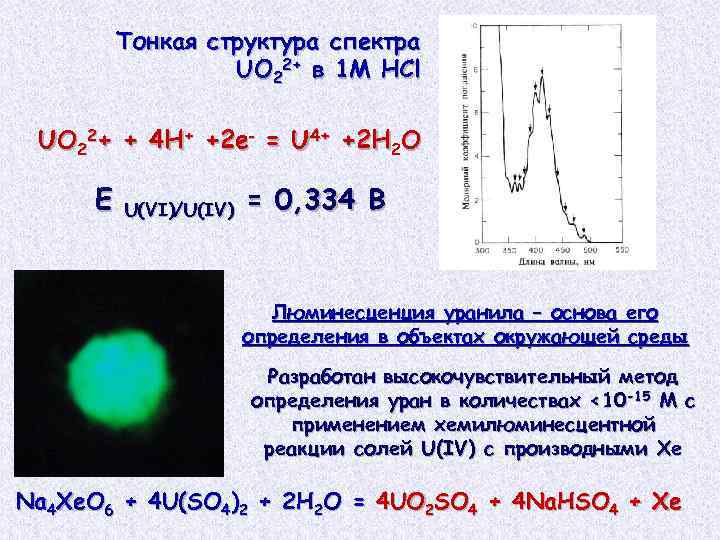 Тонкая структура спектра UO 22+ в 1 М HCl UO 22+ + 4 Н+ +2 е‑ = U 4+ +2 Н 2 O E U(VI)/U(IV) = 0, 334 В Люминесценция уранила – основа его определения в объектах окружающей среды Разработан высокочувствительный метод определения уран в количествах <10 -15 М с применением хемилюминесцентной реакции солей U(IV) с производными Xe Na 4 Xe. O 6 + 4 U(SO 4)2 + 2 Н 2 О = 4 UO 2 SO 4 + 4 Na. HSO 4 + Xe
Тонкая структура спектра UO 22+ в 1 М HCl UO 22+ + 4 Н+ +2 е‑ = U 4+ +2 Н 2 O E U(VI)/U(IV) = 0, 334 В Люминесценция уранила – основа его определения в объектах окружающей среды Разработан высокочувствительный метод определения уран в количествах <10 -15 М с применением хемилюминесцентной реакции солей U(IV) с производными Xe Na 4 Xe. O 6 + 4 U(SO 4)2 + 2 Н 2 О = 4 UO 2 SO 4 + 4 Na. HSO 4 + Xe
 Трехвалентный уран Водные растворы U 3+ получают растворением UCl 3 трихлорида урана в воде или восстановлением U(IV) электролитически на ртутном катоде, например U 2(SО 4)3. 8 H 2 О или М 2 SO 4. U 2(SO 4)3. Водные растворы U 3+ неустойчивы, поскольку трехвалентный уран легко окисляется молекулами воды с образованием водорода и U 4+. Быстрое окисление U 3+ затрудняет исследование его свойств в растворах и достоверные данные в этой области отсутствуют. Поэтому ни одно соединение трехвалентного урана в технологии или для разработки методов аналитического определения или выделения элемента не было применено.
Трехвалентный уран Водные растворы U 3+ получают растворением UCl 3 трихлорида урана в воде или восстановлением U(IV) электролитически на ртутном катоде, например U 2(SО 4)3. 8 H 2 О или М 2 SO 4. U 2(SO 4)3. Водные растворы U 3+ неустойчивы, поскольку трехвалентный уран легко окисляется молекулами воды с образованием водорода и U 4+. Быстрое окисление U 3+ затрудняет исследование его свойств в растворах и достоверные данные в этой области отсутствуют. Поэтому ни одно соединение трехвалентного урана в технологии или для разработки методов аналитического определения или выделения элемента не было применено.
 Четырехвалентный уран Растворы U(IV) широко применяются в радиохимической технологии в качестве восстановителя. Несмотря на это, в литературе немного сведений о химии соединений урана (IV). Известен ряд сульфатов, сульфит урана (IV), серия его фосфатов, формиат, ацетат и силикат. Эти соединения выделены в твердом виде, большинство солей окрашены в цвета от светло- до темно-зеленого, за исключением безводного сине-фиолетового U(C 2 O 4)2.
Четырехвалентный уран Растворы U(IV) широко применяются в радиохимической технологии в качестве восстановителя. Несмотря на это, в литературе немного сведений о химии соединений урана (IV). Известен ряд сульфатов, сульфит урана (IV), серия его фосфатов, формиат, ацетат и силикат. Эти соединения выделены в твердом виде, большинство солей окрашены в цвета от светло- до темно-зеленого, за исключением безводного сине-фиолетового U(C 2 O 4)2.
 Пятивалентный уран Упаковка комплексных анионов кеггиновского тип в виде отдельных октаэдров MO 6 (Кеггин). Разработан метод получения комплексов неоксигенированного иона U 5+ с гетерополианионами P 2 W 17 O 6110 -, Si. W 11 O 398 -, PW 11 O 397 -. Показана обратимость перехода U 5+ ↔ U 4+ и измерены потенциалы пар U 5+/U 4+ в указанных комплексах. Устойчивость состояния U 5+ растет в ряду Si. W 11 O 398 - > P 2 W 17 O 6110 - > PW 11 O 397 -. [Ce 20 Ge 10 W 100 O 376(OH)4(H 2 O)30]56
Пятивалентный уран Упаковка комплексных анионов кеггиновского тип в виде отдельных октаэдров MO 6 (Кеггин). Разработан метод получения комплексов неоксигенированного иона U 5+ с гетерополианионами P 2 W 17 O 6110 -, Si. W 11 O 398 -, PW 11 O 397 -. Показана обратимость перехода U 5+ ↔ U 4+ и измерены потенциалы пар U 5+/U 4+ в указанных комплексах. Устойчивость состояния U 5+ растет в ряду Si. W 11 O 398 - > P 2 W 17 O 6110 - > PW 11 O 397 -. [Ce 20 Ge 10 W 100 O 376(OH)4(H 2 O)30]56
 Шестивалентный уран С. о. U(VI) наиболее устойчиво в водных растворах. Обычные соли уранила и их растворы окрашены в желтый цвет. Некоторые соединения шестивалентного урана белые или почти белые (гексафторид и уранил-фторид). Соли уранила, как правило, отличаются высокой растворимостью в водных и органических средах. Так, растворимость UО 2 SО 4. 3 H 2 О в воде составляет 20, 5 г/100 г (15°С); UO 2(NO 3)2. 6 Н 20 – 170 г/100 г (0°С); при нагревании указанное соединение просто растворяется в собственной кристаллизационной воде. Важнейшие труднорастворимые соли урана - диуранат аммония, уранаты щелочных и щелочноземельных элементов, фосфаты уранила типа Me. UО 2 PО 4, тетрафторид UF 4, фосфат урана (IV), уранованадаты и другие. Они часто применяются в технологии для выделения урана и очистки его соединений.
Шестивалентный уран С. о. U(VI) наиболее устойчиво в водных растворах. Обычные соли уранила и их растворы окрашены в желтый цвет. Некоторые соединения шестивалентного урана белые или почти белые (гексафторид и уранил-фторид). Соли уранила, как правило, отличаются высокой растворимостью в водных и органических средах. Так, растворимость UО 2 SО 4. 3 H 2 О в воде составляет 20, 5 г/100 г (15°С); UO 2(NO 3)2. 6 Н 20 – 170 г/100 г (0°С); при нагревании указанное соединение просто растворяется в собственной кристаллизационной воде. Важнейшие труднорастворимые соли урана - диуранат аммония, уранаты щелочных и щелочноземельных элементов, фосфаты уранила типа Me. UО 2 PО 4, тетрафторид UF 4, фосфат урана (IV), уранованадаты и другие. Они часто применяются в технологии для выделения урана и очистки его соединений.
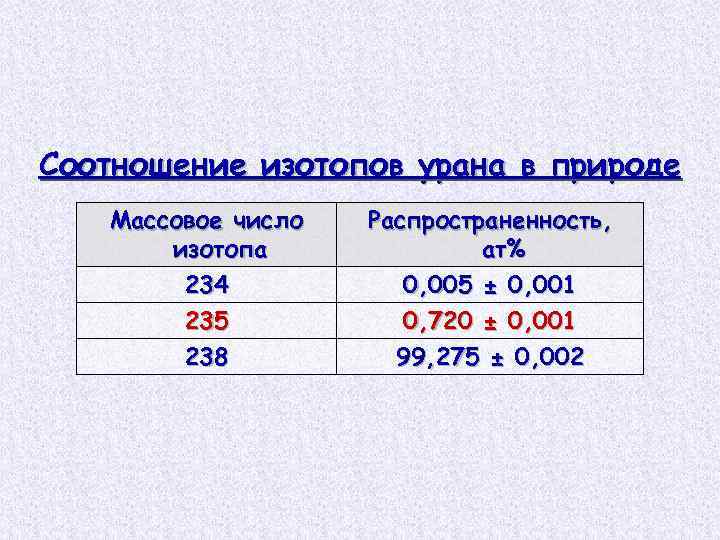 Соотношение изотопов урана в природе Массовое число изотопа 234 235 238 Распространенность, ат% 0, 005 ± 0, 001 0, 720 ± 0, 001 99, 275 ± 0, 002
Соотношение изотопов урана в природе Массовое число изотопа 234 235 238 Распространенность, ат% 0, 005 ± 0, 001 0, 720 ± 0, 001 99, 275 ± 0, 002
 Разделение изотопов урана Разделение природных изотопов урана представляет собой чрезвычайно трудную задачу. Оно может быть выполнено с помощью методов, в которых используются небольшие различия в физических свойствах соединений 235 U и 238 U. В настоящее время нашли применение следующие методы разделения изотопов урана: §лазерный метод; §газодиффузионный метод; §метод электромагнитного разделения; §метод жидкостной термодиффузии; §газоцентрифужный метод; §метод разделительного сопла. Делались также попытки использовать метод разделения изотопов урана, основанный на применении химических равновесных реакций. Ниже кратко обсуждаются наиболее перспективные методы.
Разделение изотопов урана Разделение природных изотопов урана представляет собой чрезвычайно трудную задачу. Оно может быть выполнено с помощью методов, в которых используются небольшие различия в физических свойствах соединений 235 U и 238 U. В настоящее время нашли применение следующие методы разделения изотопов урана: §лазерный метод; §газодиффузионный метод; §метод электромагнитного разделения; §метод жидкостной термодиффузии; §газоцентрифужный метод; §метод разделительного сопла. Делались также попытки использовать метод разделения изотопов урана, основанный на применении химических равновесных реакций. Ниже кратко обсуждаются наиболее перспективные методы.
 Метод электромагнитного разделения. Метод электромагнитного разделения основан на различном действии магнитного поля на одинаково электрически заряженные частицы различной массы. По сути дела такие установки, называемые калютронами, являются огромными массспектрометрами. Ионы разделяемых веществ, двигаясь в сильном магнитном поле, закручиваются с радиусами, пропорциональными их массам и попадают в приемники, где и накапливаются.
Метод электромагнитного разделения. Метод электромагнитного разделения основан на различном действии магнитного поля на одинаково электрически заряженные частицы различной массы. По сути дела такие установки, называемые калютронами, являются огромными массспектрометрами. Ионы разделяемых веществ, двигаясь в сильном магнитном поле, закручиваются с радиусами, пропорциональными их массам и попадают в приемники, где и накапливаются.
 Метод электромагнитного разделения Это была исторически первая техника, способная к производству оружейного урана. Она использовалась в электромагнитном сепараторе с применением кольцевого магнита-ускорителя заряженных частиц Y 12 в Ок-Ридже (США) во время второй мировой войны. Двух этапов разделения достаточно для обогащения урана до 80 -90%. Два остальных метода, доступных в то время - газовая диффузия, жидкостная термодиффузия - применялись для начального обогащения урана и увеличения выхода электромагнитного сепаратора по отношению к сырью из природного урана. Весь использованный в хиросимской бомбе уран произведен по этой технологии В связи с высокими накладными расходами Y-12 был закрыт в 1946 году. В более позднее время только Ирак пытался промышленно использовать этот метод в своей атомной программе. Завод для электромагнитного разделения в Ок-Ридже (США)
Метод электромагнитного разделения Это была исторически первая техника, способная к производству оружейного урана. Она использовалась в электромагнитном сепараторе с применением кольцевого магнита-ускорителя заряженных частиц Y 12 в Ок-Ридже (США) во время второй мировой войны. Двух этапов разделения достаточно для обогащения урана до 80 -90%. Два остальных метода, доступных в то время - газовая диффузия, жидкостная термодиффузия - применялись для начального обогащения урана и увеличения выхода электромагнитного сепаратора по отношению к сырью из природного урана. Весь использованный в хиросимской бомбе уран произведен по этой технологии В связи с высокими накладными расходами Y-12 был закрыт в 1946 году. В более позднее время только Ирак пытался промышленно использовать этот метод в своей атомной программе. Завод для электромагнитного разделения в Ок-Ридже (США)
 Газодиффузионный метод был первым в рамках реализации Атомного проекта в СССР и во всем мире. В основу процесса положен закон Грэма (1829 г. ), заключающийся в том, что при постоянной температуре средние скорости молекул газа зависят от их масс. В итоге легкие молекулы будут чаще взаимодействовать со внутренней стенкой фильтра из проницаемого материала. Для диффузии 235 UF 6 и 238 UF 6 максимальный коэффициент разделения всего 1, 00429, однако для 3000 ступеней разделения можно получить 235 U с 90% обогащением из природного (0, 711 мас %). Проектирование такого производства связано с решением сложных проблем. Во-первых, необходим надежный диффузионный поток газа через фильтры с однородными порами <5. 10 -8 м; для значительных количеств продукта газодиффузионные фильтры имеют площади в гектар. Во-вторых: процесс должен проводиться при 70 -80°С и давлениях. В-третьих, UF 6 чрезвычайно активно взаимодействует с Н 2 О, металлами, и не совместим с органическими материалами. Поэтому в технологии применяют фторированные материалы, высокочистые никель и алюминий для оборудования. Кроме того, сама каскадная установка должна быть герметичной.
Газодиффузионный метод был первым в рамках реализации Атомного проекта в СССР и во всем мире. В основу процесса положен закон Грэма (1829 г. ), заключающийся в том, что при постоянной температуре средние скорости молекул газа зависят от их масс. В итоге легкие молекулы будут чаще взаимодействовать со внутренней стенкой фильтра из проницаемого материала. Для диффузии 235 UF 6 и 238 UF 6 максимальный коэффициент разделения всего 1, 00429, однако для 3000 ступеней разделения можно получить 235 U с 90% обогащением из природного (0, 711 мас %). Проектирование такого производства связано с решением сложных проблем. Во-первых, необходим надежный диффузионный поток газа через фильтры с однородными порами <5. 10 -8 м; для значительных количеств продукта газодиффузионные фильтры имеют площади в гектар. Во-вторых: процесс должен проводиться при 70 -80°С и давлениях. В-третьих, UF 6 чрезвычайно активно взаимодействует с Н 2 О, металлами, и не совместим с органическими материалами. Поэтому в технологии применяют фторированные материалы, высокочистые никель и алюминий для оборудования. Кроме того, сама каскадная установка должна быть герметичной.
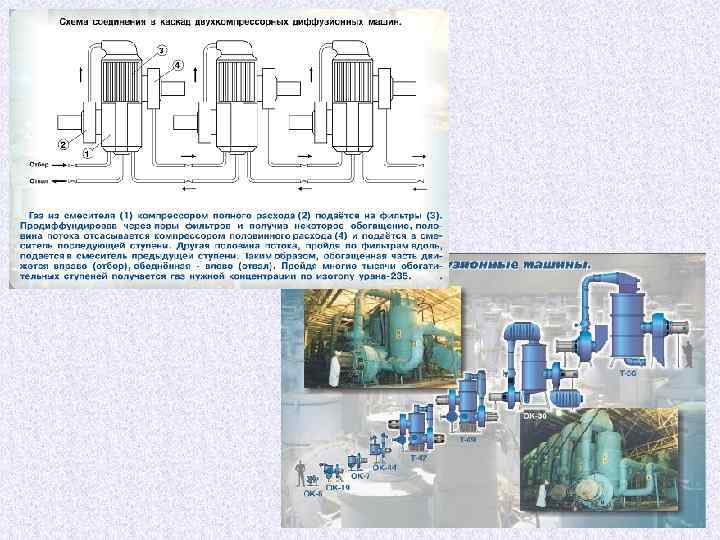
 Газодиффузионный метод Построенное во время второй мировой войны производство K-25 в Ок-Ридже состояло из 3024 ступеней обогащения и продолжало функционировать до конца 1970 -х. K-25 изначально содержал 162 000 м 2 мембранной поверхности. Огромные размеры обогатительной системы ведут к длительному времени заполнения ее материалом (обогащаемым веществом), до начала выхода продукта. Обычно это время установления равновесия составляет 3 месяца. В СССР на СХК (г. Северск) были построен завод по производству гексафторида урана (1954 г. ), завод по обогащению урана методом газовой диффузии (1953 г. ).
Газодиффузионный метод Построенное во время второй мировой войны производство K-25 в Ок-Ридже состояло из 3024 ступеней обогащения и продолжало функционировать до конца 1970 -х. K-25 изначально содержал 162 000 м 2 мембранной поверхности. Огромные размеры обогатительной системы ведут к длительному времени заполнения ее материалом (обогащаемым веществом), до начала выхода продукта. Обычно это время установления равновесия составляет 3 месяца. В СССР на СХК (г. Северск) были построен завод по производству гексафторида урана (1954 г. ), завод по обогащению урана методом газовой диффузии (1953 г. ).
 Город Новоуральск
Город Новоуральск
 Завод № 813 Кикоин И. К. Морохов И. Д. В 1936 – 1943 гг работал в Уральском физико-техническом ин-те и возглавлял кафедру физики Политехнического ин-та (Свердловск). С 1943 г был одним из первых физиков, с которыми И. В. Курчатов начал разработку комплекса атомной проблемы. Был научным руководителем проблемы разделения изотопов урана диффузионным методом. При его участии был построен Уральский электрохимический комбинат, научным руководителем которого он был много лет. В начале 1960 -х гг. был внедрен предложенный Кикоином и его сотрудниками центробежный метод разделения изотопов урана.
Завод № 813 Кикоин И. К. Морохов И. Д. В 1936 – 1943 гг работал в Уральском физико-техническом ин-те и возглавлял кафедру физики Политехнического ин-та (Свердловск). С 1943 г был одним из первых физиков, с которыми И. В. Курчатов начал разработку комплекса атомной проблемы. Был научным руководителем проблемы разделения изотопов урана диффузионным методом. При его участии был построен Уральский электрохимический комбинат, научным руководителем которого он был много лет. В начале 1960 -х гг. был внедрен предложенный Кикоином и его сотрудниками центробежный метод разделения изотопов урана.
 Газоцентрифужный метод Впервые эта технология была разработана в Германии, во время второй мировой, но промышленно нигде не применялась до начала 50 -х. Если газообразную смесь изотопов пропускать через высокоскоростные центрифуги, то центробежная сила разделит более легкие или тяжелые частицы на слои, где их и можно будет собрать. Большое преимущество центрифугирования состоит в зависимости коэффициента разделения от абсолютной разницы в массе, а не от отношения масс. Степень разделения пропорциональна квадрату отношения скорости вращения к скорости молекул в газе. Отсюда типичные линейные скорости вращающихся роторов до 600 м/с.
Газоцентрифужный метод Впервые эта технология была разработана в Германии, во время второй мировой, но промышленно нигде не применялась до начала 50 -х. Если газообразную смесь изотопов пропускать через высокоскоростные центрифуги, то центробежная сила разделит более легкие или тяжелые частицы на слои, где их и можно будет собрать. Большое преимущество центрифугирования состоит в зависимости коэффициента разделения от абсолютной разницы в массе, а не от отношения масс. Степень разделения пропорциональна квадрату отношения скорости вращения к скорости молекул в газе. Отсюда типичные линейные скорости вращающихся роторов до 600 м/с.
 Проблемы утилизации обедненного урана • В СССР производство фторидов урана (IV) и (VI) осуществлялось с 1947 г. , и его суммарные запасы оценивается от 10 до 100 тыс. тонн. • В США имеется 560 тыс. тонн обедненного урана (DUO 2) в форме токсичного гексафторида, хранящегося в контейнерах на трех площадках Портсмута (Огайо), Ок Риджа (Теннеси) и Падука (Кентукки). • В настоящее время проводится международное сотрудничество по утилизации DUO 2 с целью: (1) создания радиационно-защитных контейнеров ОЯТ; (2) разработки матриц на основе DUO 2 для иммобилизации трансурановых актинидов. (3) стекло и керамика обладает повышенной коррозионной стойкостью, способностью противостоять внутренней радиоактивности и снижать радиационный фон.
Проблемы утилизации обедненного урана • В СССР производство фторидов урана (IV) и (VI) осуществлялось с 1947 г. , и его суммарные запасы оценивается от 10 до 100 тыс. тонн. • В США имеется 560 тыс. тонн обедненного урана (DUO 2) в форме токсичного гексафторида, хранящегося в контейнерах на трех площадках Портсмута (Огайо), Ок Риджа (Теннеси) и Падука (Кентукки). • В настоящее время проводится международное сотрудничество по утилизации DUO 2 с целью: (1) создания радиационно-защитных контейнеров ОЯТ; (2) разработки матриц на основе DUO 2 для иммобилизации трансурановых актинидов. (3) стекло и керамика обладает повышенной коррозионной стойкостью, способностью противостоять внутренней радиоактивности и снижать радиационный фон.
 БОЕПРИПАСЫ С ОБЕДНЕННЫМ УРАНОМ Тяжёлый урановый наконечник бронебойного снаряда твёрже и прочнее стали (1600 МПа), изменяет распределение масс и улучшает его аэродинамическую устойчивость. Процесс разрушения брони сопровождается измельчением в пыль урановой болванки и воспламенением её. 300 тонн обеднённого U остались на поле боя во время операции «Буря в пустыне» (снарядов 30 -мм пушки GAU-8 штурмовых самолётов A-10, содержит 272 г U сплава). 15 тонн было применено в войне на Балканах.
БОЕПРИПАСЫ С ОБЕДНЕННЫМ УРАНОМ Тяжёлый урановый наконечник бронебойного снаряда твёрже и прочнее стали (1600 МПа), изменяет распределение масс и улучшает его аэродинамическую устойчивость. Процесс разрушения брони сопровождается измельчением в пыль урановой болванки и воспламенением её. 300 тонн обеднённого U остались на поле боя во время операции «Буря в пустыне» (снарядов 30 -мм пушки GAU-8 штурмовых самолётов A-10, содержит 272 г U сплава). 15 тонн было применено в войне на Балканах.
 Потенциальные матрицы на основе DUO 2 для иммобилизации трансурановых и редкоземельных элементов: Твердый раствор: U(An, REE, Zr)O 2 -x с решеткой флюоритового типа An 3+/4+ = Np, Pu, Am, Cm; REE = La, Ce, Nd, Pr, Gd (поглотитель нейтронов). Емкость по DUO 2: 70 -80 масс. %. Устойчива в восстановительных условиях, Eh <-100 m. V. Титано-цирконаты вида: (Ca, U, An, REE)2(Ti, Zr)2 O 7 -x - с решеткой пирохлора, (U, An 4+)Ti 2 O 6 - типа браннерита. Емкость: 40 - 50 масс. % DUO 2. Устойчива для окислительных условий.
Потенциальные матрицы на основе DUO 2 для иммобилизации трансурановых и редкоземельных элементов: Твердый раствор: U(An, REE, Zr)O 2 -x с решеткой флюоритового типа An 3+/4+ = Np, Pu, Am, Cm; REE = La, Ce, Nd, Pr, Gd (поглотитель нейтронов). Емкость по DUO 2: 70 -80 масс. %. Устойчива в восстановительных условиях, Eh <-100 m. V. Титано-цирконаты вида: (Ca, U, An, REE)2(Ti, Zr)2 O 7 -x - с решеткой пирохлора, (U, An 4+)Ti 2 O 6 - типа браннерита. Емкость: 40 - 50 масс. % DUO 2. Устойчива для окислительных условий.
 Методы синтеза матриц на основе DUO 2 для иммобилизации трансурановых и редкоземельных элементов Самораспространяющийся высокотемпературный синтез Температура: 2500 о. С, Время минералообразования: 1 -2 мин. Матрицы: титанатный и цирконатный пирохлор Емкость: 30 масс. % An и REE. Холодное прессование - спекание Температура: до 1400 о. C, Время минералообразования: 3 - 4 час. Матрица: пирохлор(Ca, U, An, REE)2(Ti, Hf)2 O 7 -x Емкость: 10 % Pu и 20 % U.
Методы синтеза матриц на основе DUO 2 для иммобилизации трансурановых и редкоземельных элементов Самораспространяющийся высокотемпературный синтез Температура: 2500 о. С, Время минералообразования: 1 -2 мин. Матрицы: титанатный и цирконатный пирохлор Емкость: 30 масс. % An и REE. Холодное прессование - спекание Температура: до 1400 о. C, Время минералообразования: 3 - 4 час. Матрица: пирохлор(Ca, U, An, REE)2(Ti, Hf)2 O 7 -x Емкость: 10 % Pu и 20 % U.
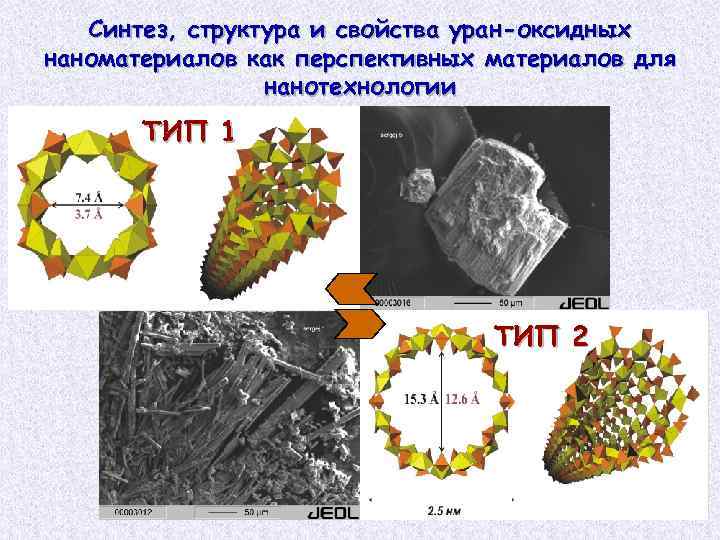 Синтез, структура и свойства уран-оксидных наноматериалов как перспективных материалов для нанотехнологии 1. 7 nm ТИП 1 ТИП 2
Синтез, структура и свойства уран-оксидных наноматериалов как перспективных материалов для нанотехнологии 1. 7 nm ТИП 1 ТИП 2
 План исследования: Синтез уран-оксидных нанотрубок на основе DUO 2, изучение механизма образования и химического состава методами микрозондового анализа, ICP-MS, синхротронного излучения; Исследование структур нанотрубок, в том числе их поверхности, с применением методов электронной микроскопии, рентгеноструктурного анализа и синхротронного излучения; Определение ионнообменных, каталитических, механических, термохимических, люминесцентных, электропроводных свойств урановых оксидных трубок для создания сверхактивных адсорбентов для токсичных металлов, новых катализаторов, сенсоров, молекулярных мембран, и других.
План исследования: Синтез уран-оксидных нанотрубок на основе DUO 2, изучение механизма образования и химического состава методами микрозондового анализа, ICP-MS, синхротронного излучения; Исследование структур нанотрубок, в том числе их поверхности, с применением методов электронной микроскопии, рентгеноструктурного анализа и синхротронного излучения; Определение ионнообменных, каталитических, механических, термохимических, люминесцентных, электропроводных свойств урановых оксидных трубок для создания сверхактивных адсорбентов для токсичных металлов, новых катализаторов, сенсоров, молекулярных мембран, и других.
 «… я смело рекомендую тем, кто ищет новых предметов для исследования, особо тщательно заниматься урановыми соединениями» . Д. И. Менделеев, 1903 г.
«… я смело рекомендую тем, кто ищет новых предметов для исследования, особо тщательно заниматься урановыми соединениями» . Д. И. Менделеев, 1903 г.



