галогены.ppt
- Количество слайдов: 44


Улыбнись новому знанию At F Давайте изучим мы сегодня отменно элементы галогены. А по-русски - солероды, Все – от фтора и до йода. Даже неустойчивый астат Быть в семействе этом рад. Cl Br I
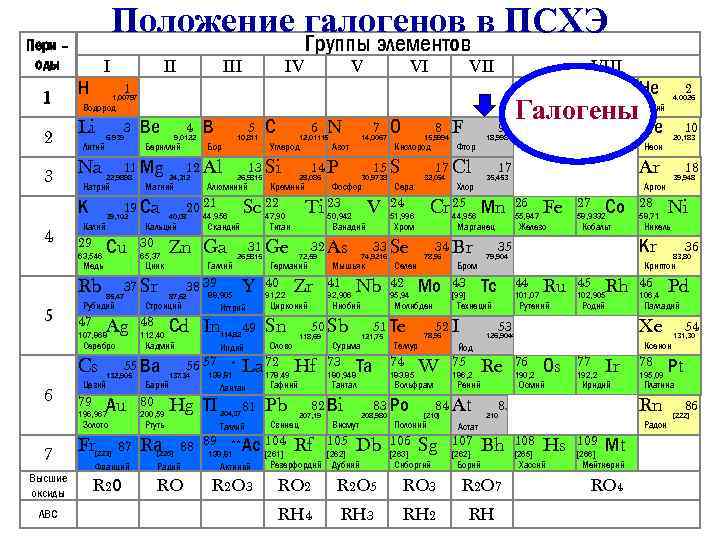
Положение галогенов в ПСХЭ Пери – оды 1 I Н Na Литий 3 6. 939 Калий 29 39, 102 Сu Медь Rb Ag Серебро Cs Цезий 55 Ва 132, 905 196, 967 Золото Fr 112, 40 [223] Алюминий VI Иттрий Сd In 114, 82 80 200, 59 Rа Hg ТI [226] * 138, 81 204, 37 Таллий Zr Цирконий Sn VII Мышьяк 41 92, 906 Nb Сурьма 73 Та VIII Свинец Rf [262] Селен 42 95, 94 Теллур Db Дубний Фтор Марганец 34 Br 78, 96 Мо [263] 26 55, 847 Fe 27 Со 58, 9332 Кобальт 52 I 44 101, 07 Ru Рутений 45 Rh 102, 905 Родий 75 186, 2 Re Рений 84 At Sg Сиборгий 76 190, 2 Оs 77 192, 2 Ir Иридий [262] Bh Франций Радий Актиний Резерфордий Борий R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH Никель 46 106, 4 36 83, 80 Pd Палладий 78 195, 09 54 Радон 108 [265] Hs Хассий 109 [266] Мt Мейтнерий RO 4 131, 30 Рt Платина Rn 85 210 Астат 107 Ni Ксенон Осмий [210] 58, 71 Xe 126, 9044 Йод W 28 Криптон 53 78, 96 18 39, 948 Кr 35 Технеций Полоний 106 [99] 10 20, 183 Аргон Железо Тс 43 Гелий Ar 79, 904 Бром 2 4. 0026 Неон 17 Хлор Не Nе 35, 453 44, 956 Вольфрам 83 Ро Висмут 105 51, 996 183. 85 208, 980 9 Галогены 18, 9984 Cr 25 Мn 24 74 180, 948 Тантал 207, 19 Сера 32, 064 Молибден 121, 75 F 17 Cl 51 Тe 82 Вi Pb Кислород 33 Se 74, 9216 50 Sb Гафний 8 15, 9994 Хром Ниобий 118, 69 Олово 88 89 ** Ас 104 138, 81 [261] V 32 As 178. 49 81 Фосфор Ванадий 72, 59 О 15 S 30, 9738 50, 942 Германий 91, 22 Азот Ti 23 La 72 Hf Лантан Ртуть 87 49 Индий Барий Кремний 40 7 14, 0067 14 P 28, 086 31 Ge Y N 12, 01115 Титан 26, 9815 88, 905 56 57 Углерод 47, 90 Скандий 38 39 137. 34 6 Sc 22 44, 956 Галлий 87, 62 С 13 Si 26, 9815 Zn Ga Стронций 48 Бор Кадмий Аu 79 65, 37 5 10, 811 20 21 40, 08 Кальций 37 Sr 85, 47 107, 868 ЛВС Магний 30 В 12 Al 24, 312 Цинк Рубидий 47 4 9, 0122 Бериллий 19 Сa 63, 546 Высшие оксиды Ве 11 Мg 22, 9898 Натрий К 7 V Водород 3 6 IV 1 Li 5 III 1, 00797 2 4 II Группы элементов 86 [222]
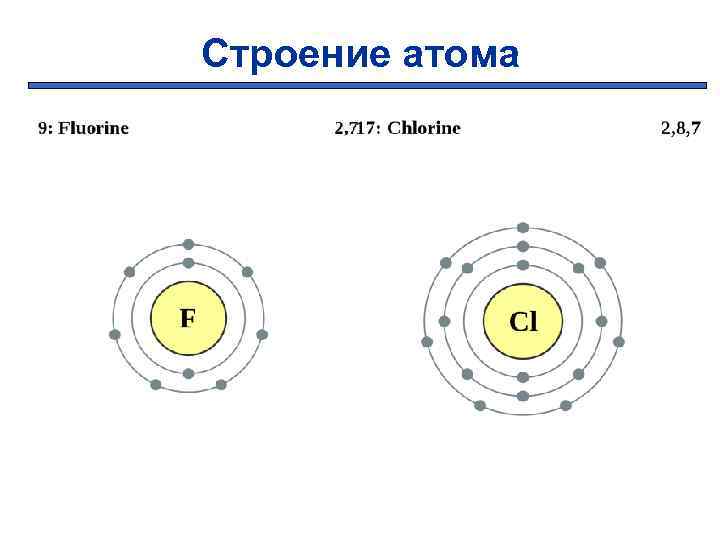
Строение атома
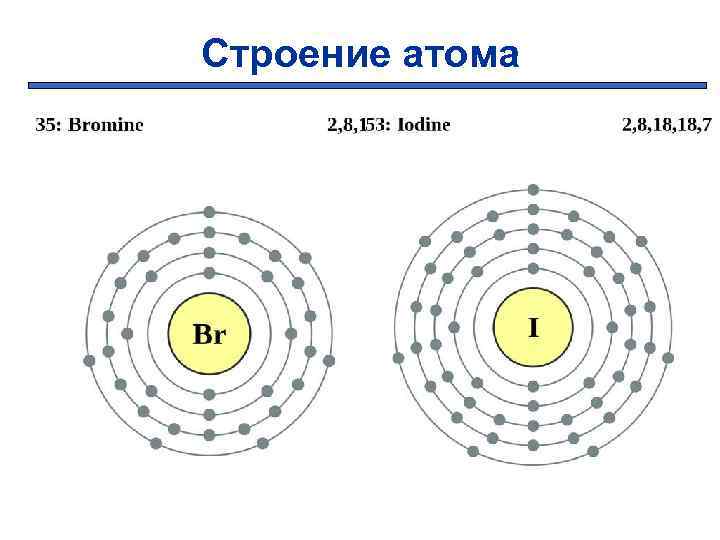
Строение атома
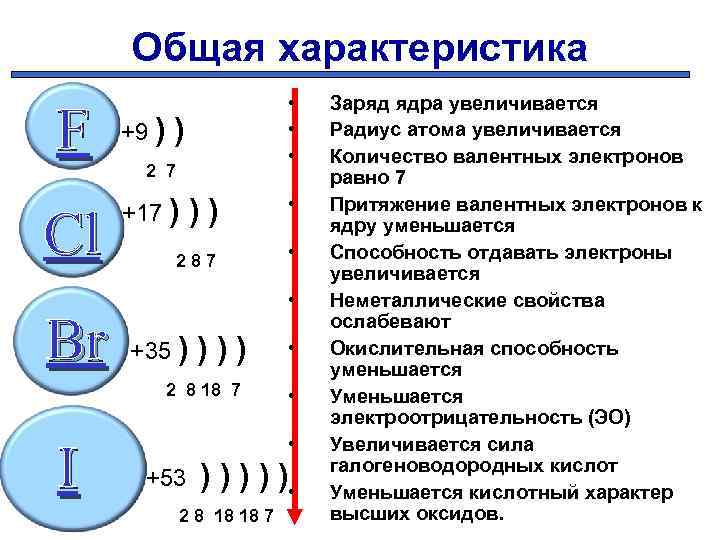
Общая характеристика • • • Заряд ядра увеличивается Радиус атома увеличивается +9 Количество валентных электронов 2 7 равно 7 • Притяжение валентных электронов к +17 ядру уменьшается • Способность отдавать электроны 287 увеличивается • Неметаллические свойства ослабевают • Окислительная способность +35 уменьшается 2 8 18 7 • Уменьшается электроотрицательность (ЭО) • Увеличивается сила галогеноводородных кислот +53 • Уменьшается кислотный характер высших оксидов. 2 8 18 18 7 F Cl Br )) )))) I )))))
История открытия галогенов At F 2 Cl 2 I 2 Br 2

История открытия фтора В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры – 23°C (в жидкости должно содержаться немного фторида калия, который обеспечивает ее электропроводимость), смог на аноде получить первую порцию нового, газа. В первых опытах для получения фтора А. Муассан использовал очень дорогой электролизер, изготовленный из платины и иридия. При этом каждый грамм полученного фтора «съедал» до 6 г платины. 2 HF→H 2↑ + F 2↑ Анри Муассан (1852 – 1907 г. )

История открытия хлора Карл Вильгельм Шееле (1742 – 1786 г. ) В 1774 году шведский аптекарь К. Шееле открыл хлор. «Я поместил смесь черной магнезии с муриевой кислотой в реторту, к горлышку которой присоединил пузырь, лишенный воздуха, и поставил ее на песчаную баню. Пузырь наполнился газом, который имел желто-зеленый цвет и пронзительный запах» . В 1807 году английский химик Гемфри Дэви получил тот же газ. Он пришел к выводу, что получил новый элемент и назвал его "хлорин" (от "хлорос" - желто-зеленый). В 1812 году Гей-Люсеок дал газу название хлор. Mn. O 2+ 4 HCl Cl 2+ Mn. Cl 2 + 2 H 2 O

История открытия брома В 1825 году французский химик А. Ж. Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал - "мурид" (от латинского слова muria, означающего "рассол"). Комиссия Академии, проверив это сообщение, подтвердила открытие Балара и предложила назвать элемент бромом (от "бромос", с греческого "зловонный"). Балар писал: «Точь-в-точь как ртуть есть единственный металл, который имеет жидкую фазу при комнатной температуре, бром есть единственный жидкий неметалл» . 2 Na. Br + Cl 2 → 2 Na. Cl + Br 2 Антуан Жером Балар (1802 – 1876 г. )

История открытия йода В 1811 году французский химик Бернар Куртуа открыл йод путём перегонки маточных растворов от азотнокислого кальция с серной кислотой Чтобы другие химики могли изучать новое вещество, Б. Куртуа подарил его (фармацевтической фирме в Дижоне. В 1813 году Ж. -Л. Гей-Люссак подробно изучил этот элемент и дал ему современное название. Название "иод" происходит от греческого слова "иодэс" - "фиолетовый" (по цвету паров). Бернар Куртуа (1777 – 1838 г. ) 2 Na. I + 2 H 2 SO 4 = I 2 + SO 2 + Na 2 SO 4 + 2 H 2 O

История открытия астата В 1869 г Д. И. Мендеелеев предсказал его существование и возможность открытия в будущем (как «эка-иод» ). Впервые астат был получен искусственно в 1940 г. открыт Д. Корсоном, К. Маккензи и Э. Сегре (Калифорнийский университет в Беркли). Для синтеза изотопа 211 At они облучали висмут альфачастицами. Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1, 6 км содержится всего 70 мг астата. 209 Bi + 4 He → 211 At + 2 1 n 83 2 85 0 Эрст Сегре (1914 – 1985 г. )
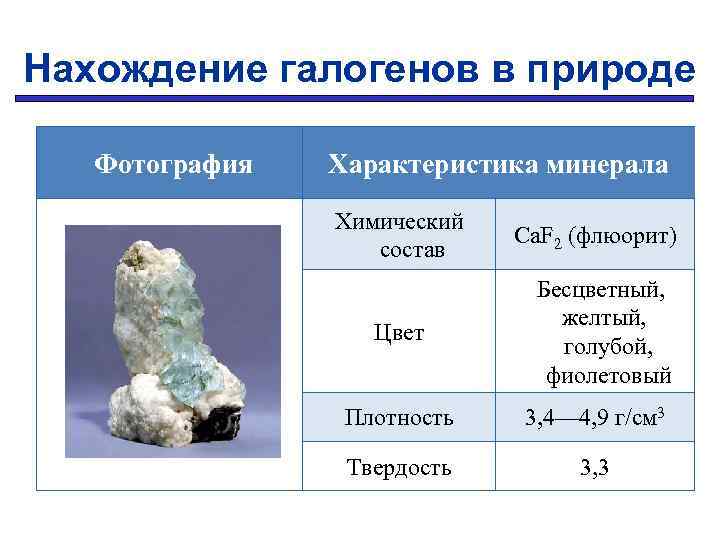
Нахождение галогенов в природе Фотография Характеристика минерала Химический состав Ca. F 2 (флюорит) Цвет Бесцветный, желтый, голубой, фиолетовый Плотность 3, 4— 4, 9 г/см 3 Твердость 3, 3
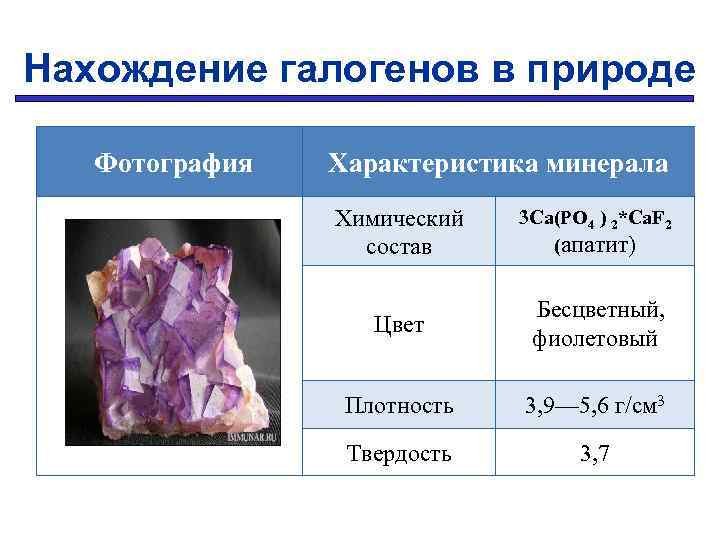
Нахождение галогенов в природе Фотография Характеристика минерала Химический состав 3 Ca(PO 4 ) 2*Ca. F 2 (апатит) Цвет Бесцветный, фиолетовый Плотность 3, 9— 5, 6 г/см 3 Твердость 3, 7
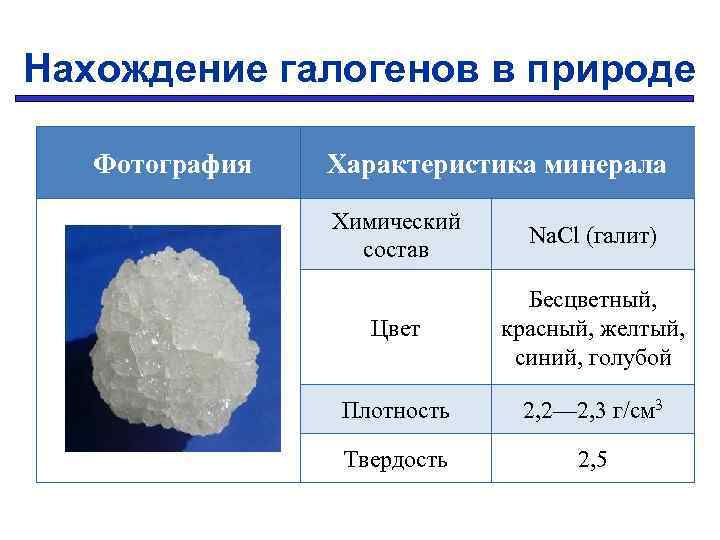
Нахождение галогенов в природе Фотография Характеристика минерала Химический состав Na. Сl (галит) Цвет Бесцветный, красный, желтый, синий, голубой Плотность 2, 2— 2, 3 г/см 3 Твердость 2, 5
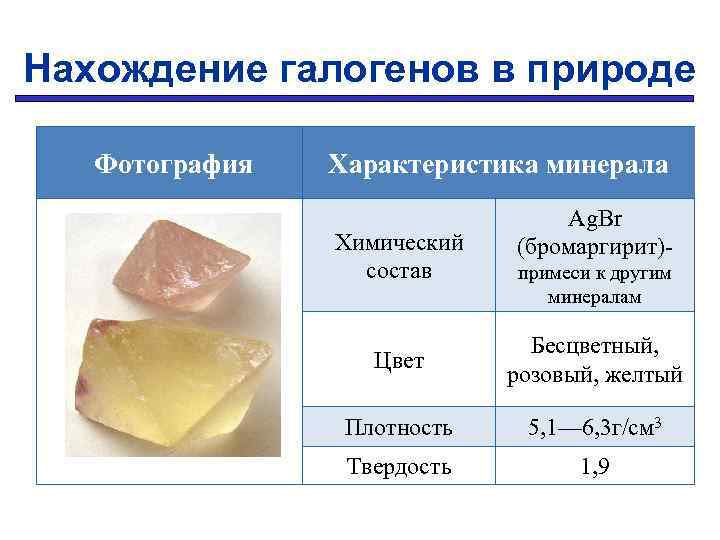
Нахождение галогенов в природе Фотография Характеристика минерала Химический состав Ag. Br (бромаргирит)примеси к другим минералам Цвет Бесцветный, розовый, желтый Плотность 5, 1— 6, 3 г/см 3 Твердость 1, 9

Нахождение галогенов в природе Фотография Характеристика минерала Химический состав Ag. I (йодаргирит)примесь к другим минералам Цвет Бесцветный, красный, желтый Плотность 5, 8— 7, 1 г/см 3 Твердость 1, 7
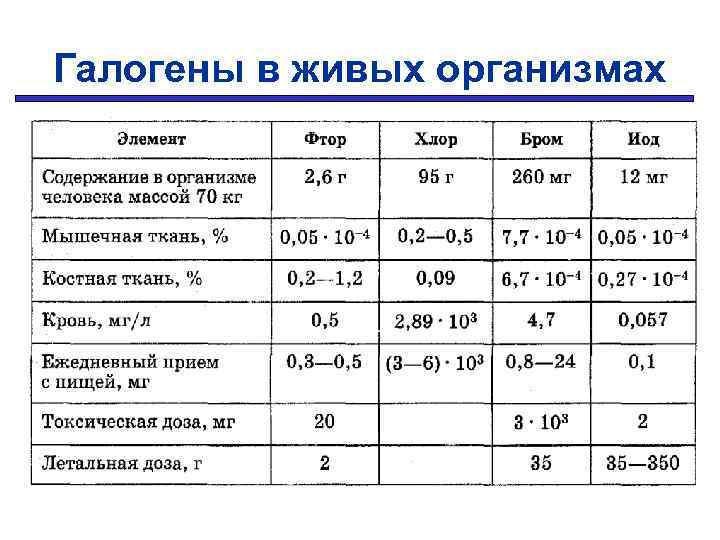
Галогены в живых организмах

ды ды ФТОР Группы элементов ио ер П Ря I 1 Фтор/Fluorum (F) II 2 Внешний вид Бледно-жёлтый газ. простого вещества Очень ядовит. III 3 IV V VI VII I II 5 6 7 9 10 IV V VI VIII Электронная коефигуранция ЭО (по Полингу) Степень окисления Плотность 4 8 III F 2 [He] 2 s 2 2 p 5 Температура плавления Температура кипения 53, 53 К 4 (САМЫЙ ЭО ЭЛЕМЕНТ) − 1 (ВСЕГДА) (при − 189 °C)1, 108 г/см ³ 85, 01 К

ды ды ио ер П Ря I ХЛОР Группы элементов 1 II II III V VI VII 4 5 6 7 8 9 10 V VI Внешний вид простого вещества Электронная коефигуранция ЭО (по Полингу) Степень окисления Плотность 3 IV IV VIII Хлор / Chlorum (Cl) 2 III I Cl 2 Температура плавления Температура кипения Газ жёлто-зеленого цвета с резким запахом. Ядовит. [Ne] 3 s 2 3 p 5 3, 16 7, 6, 5, 4, 3, 1, − 1 (при − 33. 6 °C)1, 56 г/см ³ 172. 2 К 238. 6 К

ды ды ио ер П Ря I БРОМ Группы элементов 1 II II III 3 IV V VI VII 4 5 6 7 8 9 10 IV V VI VIII Бром / Bromum (Br) 2 III I Br 2 Внешний вид простого вещества Электронная конфигуранция ЭО (по Полингу) Степень окисления Плотность Температура плавления Температура кипения Красно-бурая жидкость с резким запахом [Ar] 3 d 10 4 s 2 4 p 5 2, 96 7, 5, 3, 1, -1 3, 12 г/см³ 265, 9 К 331, 9 К

ды ды ио ер П Ря I ЙОД Группы элементов 1 II IV V VI VII IV V VI Черно-фиолетовые Внешний вид простого вещества кристаллы с металлическим блеском 3 Электронная [Kr] 4 d 10 5 s 2 5 p 5 конфигуранция ЭО 2, 66 (по Полингу) Степень окисления 7, 5, 3, 1, -1 4 5 6 7 Плотность 8 10 VIII Ио д / Iodum (I) 2 9 VII I 2 4, 93 г/см³ Температура плавления Температура кипения 386, 7 К 457, 5 К
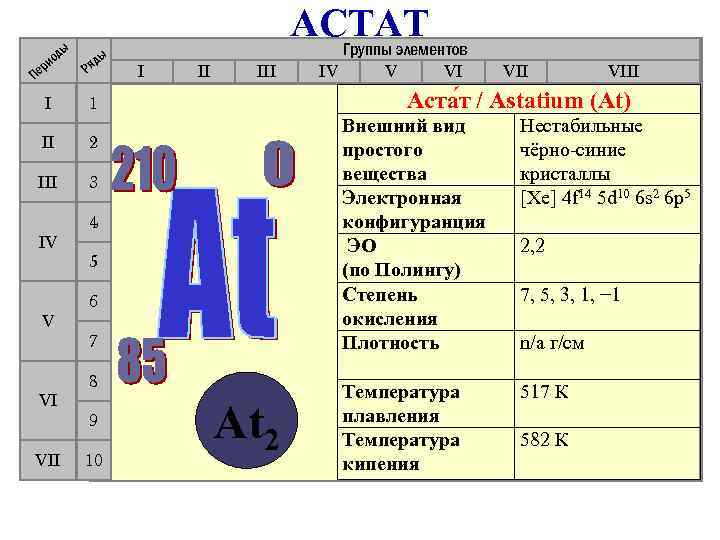
ды ды ио ер П Ря I АСТАТ Группы элементов 1 II II III V VI VII 4 5 6 7 8 9 10 V VI VIII Внешний вид простого вещества Электронная конфигуранция ЭО (по Полингу) Степень окисления Плотность 3 IV IV Аста т / Astatium (At) 2 III I At 2 Нестабильные чёрно-синие кристаллы [Xe] 4 f 14 5 d 10 6 s 2 6 p 5 Температура плавления Температура кипения 517 К 2, 2 7, 5, 3, 1, − 1 n/a г/см 582 К

Галогены

Сравнение физических свойств F 2 Cl 2 Br 2 I 2 At 2 светло-желтый газ • Интенсивность цвета желто-зеленый газ усиливается • Плотность красно-бурая увеличивается жидкость (возгоняется) • Температуры плавления и кипения фиолетовые кристаллы с металлическим блеском увеличиваются черно-синие кристаллы

Возгонка йода Кристаллический йод обладает способностью при нагревании переходить из твердого состояния в газообразное, минуя жидкое (возгонка), превращаясь в фиолетовые пары.

Химические свойства галогенов Хлор хвалился: «Нет мне равных! Галоген я - самый главный. Зря болтать я не люблю: Всё на свете отбелю!» Йод красой своей гордился, Твердым был, но испарился. Фиолетовый как ночь, Далеко умчался прочь. Бром разлился океаном, Хоть зловонным. Но румяным. Бил себя он грозно в грудь: «Я ведь бром! Не кто-нибудь!. . » Фтор молчал и думал: «Эх!. . Ведь приду – окислю всех…»
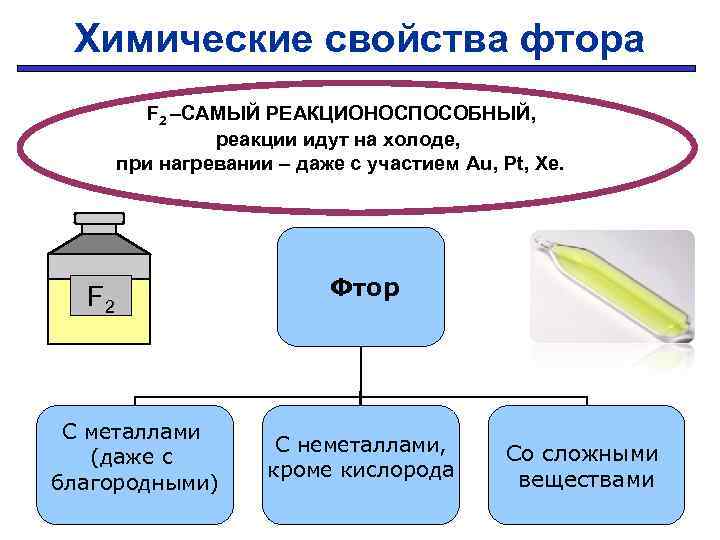
Химические свойства фтора F 2 –САМЫЙ РЕАКЦИОНОСПОСОБНЫЙ, реакции идут на холоде, при нагревании – даже с участием Au, Pt, Xe. F 2 С металлами (даже с благородными) Фтор С неметаллами, кроме кислорода Проверить Со сложными веществами

Химические свойства фтора С С МЕталлами простыми веществами: С Неметаллами F 2 → 2 Na. F H + F → 2 HF 2 Na + F 2 2 2 Mo + 3 F 2 → Mo. F 6 Xe + 2 F 2 → Xe. F 4 Со сложными веществами: Вода горит во 2 H 2 O + F 2 → 4 HF + O 2 фторе фиолетовым 2 KCl + F 2 → Cl 2 + 2 Na. F пламенем 2 KBr + F 2 → Br 2 + 2 КF 2 KI + F 2 → I 2 + 2 КF Фтор вытесняет любой галоген из соли
Химические свойства хлора Cl 2 - сильно реакционоспособен (искл. C, O 2, N 2 и некот. др. ). Отбеливает ткани и бумагу. Cl 2 С металлами (кроме благородных) Хлор С неметаллами, кроме кислорода и азота, углерода Со сложными веществами

Химические свойства хлора С простыми веществами: С МЕталлами С НЕметаллами 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 H 2 + Cl 2 → 2 HCl (tº, hυ) Cu + Cl 2 → Cu Cl 2 2 P + 5 Cl 2 → 2 PCl 5 ( tº, в изб. Сl 2) Cl 2 Со сложными веществами: H 2 O + Cl 2 → HCl+HCl. O 2 Na. OH + Cl 2 → Na. OCl + Na. Cl + H 2 O жавелевая вода 2 KBr + Cl 2 → Br 2 + 2 КCl 2 KI + Cl 2 → I 2 + 2 КCl Хлор отбеливает ткани Горение железа в хлоре за счет атомарного кислорода, выделяемого из НCl. O
Химические свойства брома Br 2 - умеренно реакционоспособен. Вытесняется из солей фтором и хлором. Br 2 С металлами (кроме благородных) при Т Бром С неметаллами, кроме кислорода и азота, серы, бора, углерода Со сложными веществами

Химические свойства брома С простыми веществами: С МЕталлами С НЕметаллами Br 2 Fe + 3 Br 2 → 2 Fe. Br 3 H 2 + Br 2 → 2 HBr 2 Cu + Br 2 → Cu Br 2 2 P + 5 Br 2 → 2 PBr 5 Со сложными веществами: Br 2 + H 2 O → HBr + HBr. O 2 KI + Br 2 → I 2 + 2 КCl Чаще чем фтор и хлор используется в органическом синтезе Обладает высокой селективностью (избирательностью)
Химические свойства йода I 2 - мало реакционоспособен. Вытесняется из солей фтором, хлором и бромом. I 2 С металлами (кроме благородных) при Т Йод С активными неметаллами при Т Со сложными веществами при Т

Химические свойства йода С простыми веществами: С металлами С неметаллами I 2 Hg + I 2 → Hg. I 2 H 2 + I 2 → 2 HI (tº) 2 Al + 3 I 2 → 2 Al. I 3 2 P + 3 Br 2 → 2 PI 3 Со сложными веществами: I 2 + H 2 O → HI + HIO (практически не идет) I 2 + р-р крахмала → темно-синее окрашивание Окисляется конц. серной и азотной кислотами

Определение галогенид-ионов Определить в какой пробирке находится раствор хлорида, бромида, иодида, фторида I II IV ?
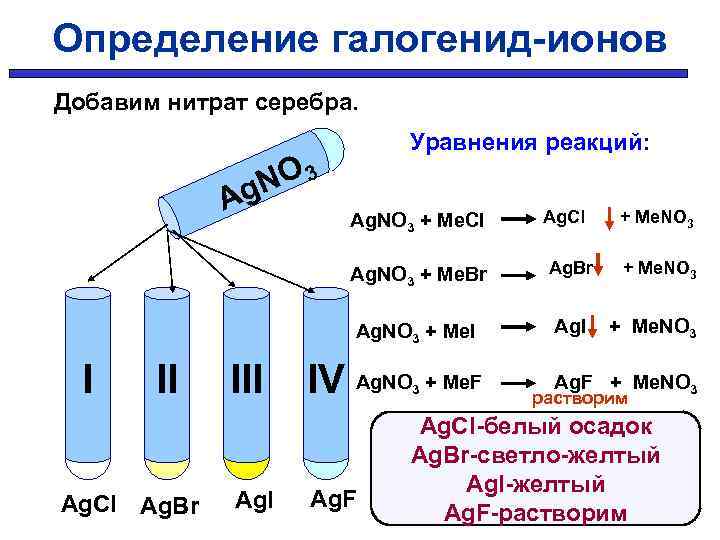
Определение галогенид-ионов Добавим нитрат серебра. Уравнения реакций: NO 3 g A Ag. NO 3 + Me. Cl Ag. NO 3 + Me. Br Ag. NO 3 + Me. I I II Ag. Cl Ag. Br III Ag. Br Ag. I IV Ag. NO Ag. F 3 + Me. F + Me. NO 3 Ag. F + Me. NO 3 растворим Ag. Cl-белый осадок Ag. Br-светло-желтый Ag. I-желтый Ag. F-растворим
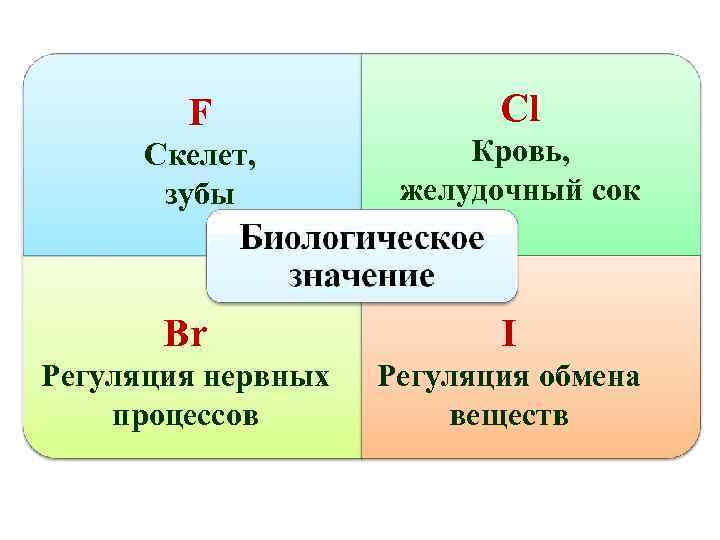
F Скелет, зубы Сl Кровь, желудочный сок Br I Регуляция нервных процессов Регуляция обмена веществ
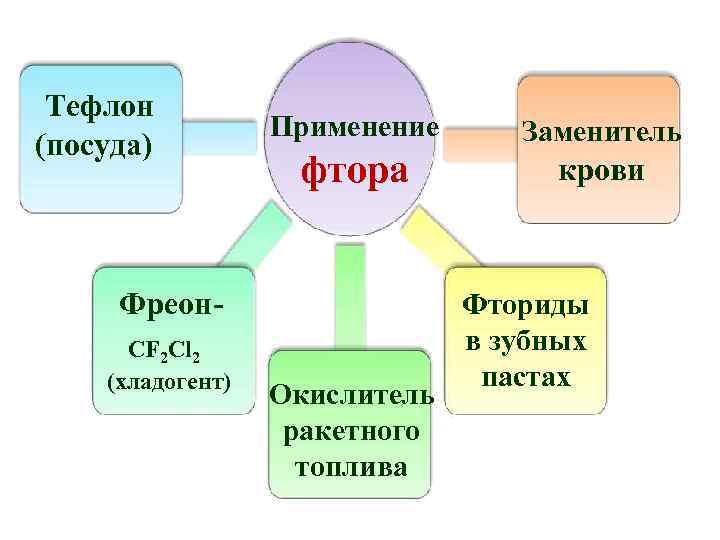
Тефлон (посуда) Применение фтора Фреон- CF 2 Cl 2 (хладогент) Окислитель ракетного топлива Заменитель крови Фториды в зубных пастах
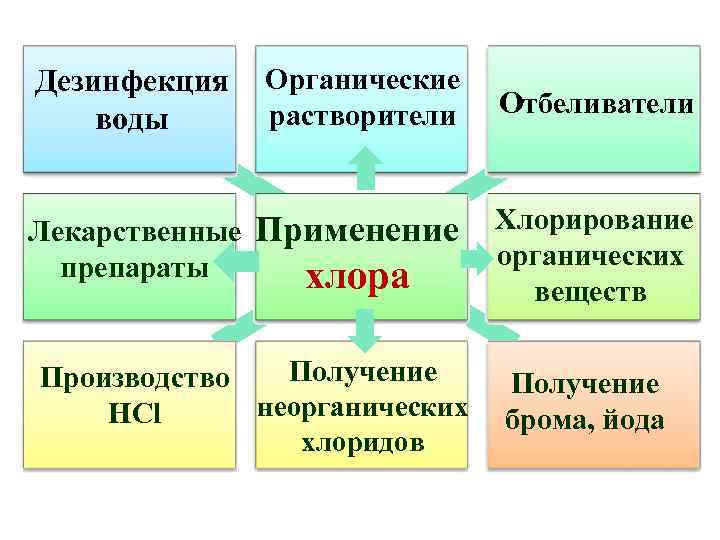
Дезинфекция Органические растворители Отбеливатели воды Лекарственные Применение Хлорирование органических препараты хлора веществ Получение Производство Получение неорганических брома, йода HCl хлоридов
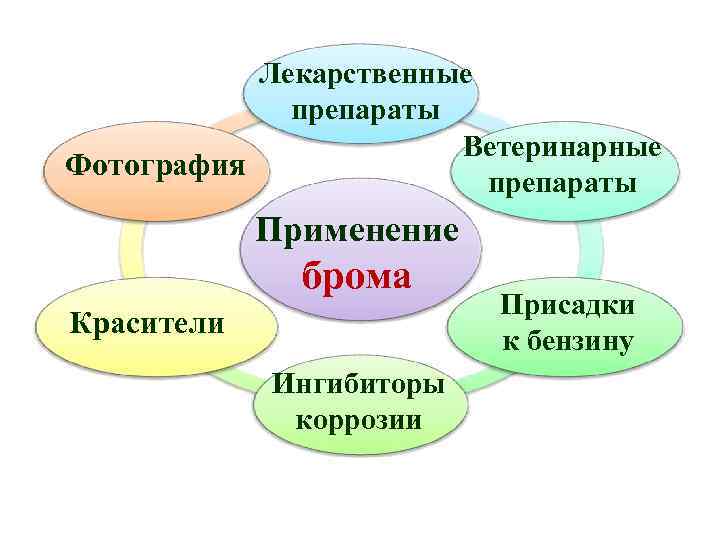
Лекарственные препараты Ветеринарные Фотография препараты Применение брома Красители Ингибиторы коррозии Присадки к бензину
Лекарственные препараты Ag. I для создания искусственных осадков Применение Фотография йода Галогеновые электролампы Красители

Проверь себя 2 H 2 O + 2 F 2 = 2 Na. OH + H 2 +Cl 2 Xe + 2 F 2 = 2 Na. Cl + I 2 H 2 + F 2 = 2 Au. Cl 3 2 Au + 3 Cl 2 = Xe. F 4 2 Na. Cl + 2 H 2 O = 4 HF + O 2 2 Na. I + Cl 2 = 2 HF

Домашнее задание • Составьте кроссворд по теме «Галогены» Ключевым словом является слово «АСТАТ» . • Решите задачу: Определите объем хлора (н. у), который образуется при действии на 5, 8 г перманганата калия раствора соляной кислоты массой 100 г, с массовой долей кислоты 36%.
галогены.ppt