L5-MONOSAKhARA.ppt
- Количество слайдов: 38
 УГЛЕВОДЫ - природные органические соединения, имеющие, как правило, общую формулу
УГЛЕВОДЫ - природные органические соединения, имеющие, как правило, общую формулу
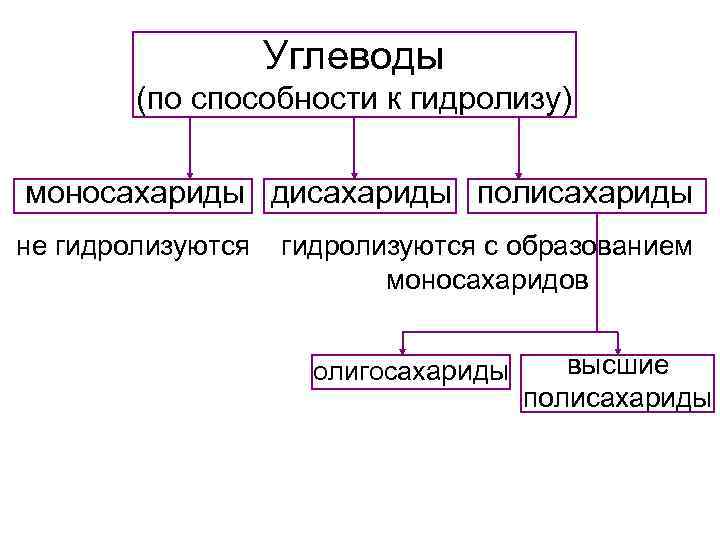 Углеводы (по способности к гидролизу) моносахариды дисахариды полисахариды не гидролизуются с образованием моносахаридов олигосахариды высшие полисахариды
Углеводы (по способности к гидролизу) моносахариды дисахариды полисахариды не гидролизуются с образованием моносахаридов олигосахариды высшие полисахариды
 ПОЛИСАХАРИДЫ гомополисахариды гетерополисахариды состоят из одинаковых моносахаридов состоят из разных моносахаридов
ПОЛИСАХАРИДЫ гомополисахариды гетерополисахариды состоят из одинаковых моносахаридов состоят из разных моносахаридов
 МОНОСАХАРИДЫ - гетерофункциональные соединения, содержащие карбонильную и гидроксильные группы Общая формула:
МОНОСАХАРИДЫ - гетерофункциональные соединения, содержащие карбонильную и гидроксильные группы Общая формула:
 Классификация а) по числу углеродных атомов С 3 Н 6 О 3 – триозы С 4 Н 8 О 4 – тетрозы С 5 Н 10 О 5 – пентозы С 6 Н 12 О 6 – гексозы … С 10 Н 20 О 10 – декозы
Классификация а) по числу углеродных атомов С 3 Н 6 О 3 – триозы С 4 Н 8 О 4 – тетрозы С 5 Н 10 О 5 – пентозы С 6 Н 12 О 6 – гексозы … С 10 Н 20 О 10 – декозы
 б) по природе карбонильной группы Оба признака объединяют в одном названии: глюкоза – это альдогексоза; фруктоза – это кетогексоза
б) по природе карбонильной группы Оба признака объединяют в одном названии: глюкоза – это альдогексоза; фруктоза – это кетогексоза
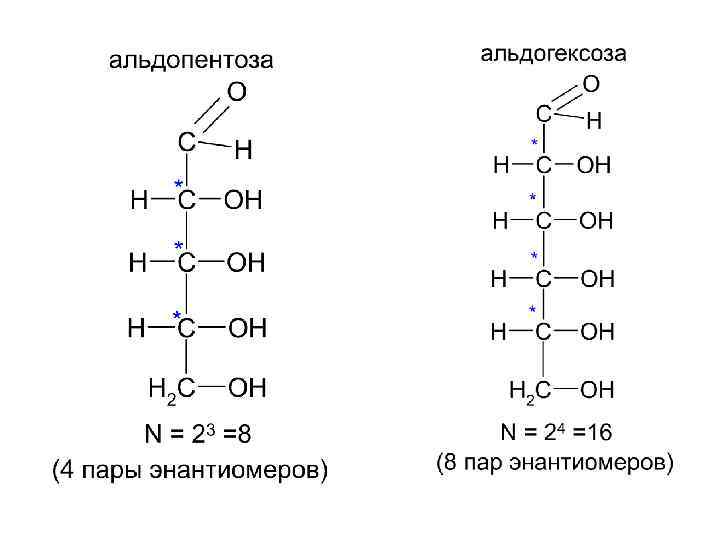
 Изомерия Пространственная: Оптическая (зеркальная) изомерия связана с наличием у моносахаридов асимметричных атомов углерода (С*). Оптические изомеры D и L (энантиомеры) относятся друг к другу как предмет и несовместимое с ним зеркальное изображение Число пространственных изомеров (стереоизомеров) определяется по формуле: N = 2 n , где n– число С*
Изомерия Пространственная: Оптическая (зеркальная) изомерия связана с наличием у моносахаридов асимметричных атомов углерода (С*). Оптические изомеры D и L (энантиомеры) относятся друг к другу как предмет и несовместимое с ним зеркальное изображение Число пространственных изомеров (стереоизомеров) определяется по формуле: N = 2 n , где n– число С*
 Пара энантиомеров имеет индивидуальное название, с обозначением конфигурации (D или L) для каждого вещества. Конфигурация моносахаридов определяется по конфигурационному стандарту (Розанова) - глицериновому альдегиду. При этом для сравнения берется последний асимметричный атом углерода. Большинство природных моносахаридов относится к D-ряду (исключения: L-рамноза, L-арабиноза).
Пара энантиомеров имеет индивидуальное название, с обозначением конфигурации (D или L) для каждого вещества. Конфигурация моносахаридов определяется по конфигурационному стандарту (Розанова) - глицериновому альдегиду. При этом для сравнения берется последний асимметричный атом углерода. Большинство природных моносахаридов относится к D-ряду (исключения: L-рамноза, L-арабиноза).

 Стереоизомеры, относящиеся к одному ряду (D или L), но отличающиеся конфигурацией одного или нескольких асимметричных атомов углерода, называются диастереомерами. Перечисление конфигураций асимметричных атомов углерода производят снизу вверх.
Стереоизомеры, относящиеся к одному ряду (D или L), но отличающиеся конфигурацией одного или нескольких асимметричных атомов углерода, называются диастереомерами. Перечисление конфигураций асимметричных атомов углерода производят снизу вверх.

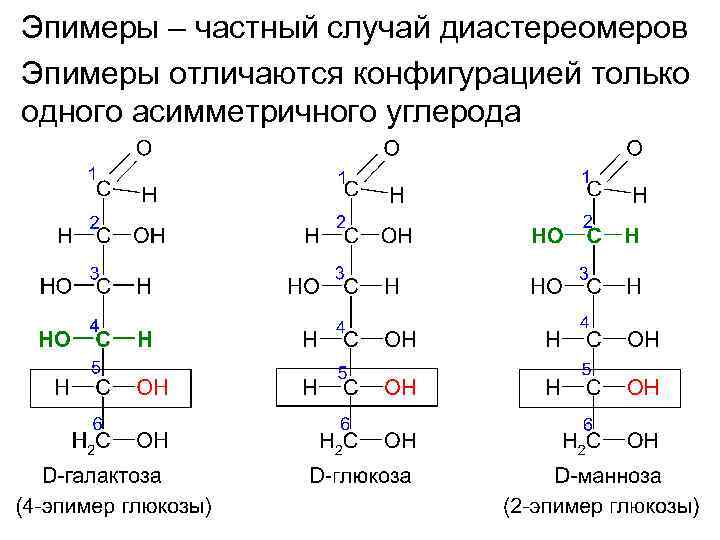 Эпимеры – частный случай диастереомеров Эпимеры отличаются конфигурацией только одного асимметричного углерода
Эпимеры – частный случай диастереомеров Эпимеры отличаются конфигурацией только одного асимметричного углерода
 Структурная изомерия: цикло-оксо (кольчато-цепная) таутомерия В твердом состоянии моносахариды существуют в циклической форме. В растворе моносахариды находятся в виде равновесной смеси таутомеров - открытой и циклических форм. Циклическая форма моносахаридов – внутренний полуацеталь.
Структурная изомерия: цикло-оксо (кольчато-цепная) таутомерия В твердом состоянии моносахариды существуют в циклической форме. В растворе моносахариды находятся в виде равновесной смеси таутомеров - открытой и циклических форм. Циклическая форма моносахаридов – внутренний полуацеталь.
 Взаимодействие альдегидов и спиртов с образованием полуацеталей: Альдегидная (кето-) группа моносахаридов взаимодействует с гидроксо-группой при 5 или 4 атомах углерода, при этом образуется новая гидроксо-группа, которая называется полуацетальный, или гликозидный гидроксил.
Взаимодействие альдегидов и спиртов с образованием полуацеталей: Альдегидная (кето-) группа моносахаридов взаимодействует с гидроксо-группой при 5 или 4 атомах углерода, при этом образуется новая гидроксо-группа, которая называется полуацетальный, или гликозидный гидроксил.
 Полуацетальный механизм образования циклической формы
Полуацетальный механизм образования циклической формы
 В результате внутримолекулярного взаимодействия карбонильной и гидроксогрупп образуются пятичленые циклы – фуранозные и шестичленные – пиранозные. В циклических формах моносаридов возникает дополнительный асимметричный атом углерода, с которым связан гликозидный гидроксил. Это обуславливает существование еще двух стереоизомеров – α- и β-аномеров.
В результате внутримолекулярного взаимодействия карбонильной и гидроксогрупп образуются пятичленые циклы – фуранозные и шестичленные – пиранозные. В циклических формах моносаридов возникает дополнительный асимметричный атом углерода, с которым связан гликозидный гидроксил. Это обуславливает существование еще двух стереоизомеров – α- и β-аномеров.
 В циклических формах D-ряда α-аномер содержит гликозидный гидроксил под плоскостью цикла, β-аномер – над плоскостью цикла. Для циклических форм L-ряда – все наоборот.
В циклических формах D-ряда α-аномер содержит гликозидный гидроксил под плоскостью цикла, β-аномер – над плоскостью цикла. Для циклических форм L-ряда – все наоборот.
 Структурные формулы углеводов принято изображать в виде проекционных формул Фишера, Хеуорса, Колли-Толленса структурная формула цепная форма формулы Фишера циклическая форма формулы Хеуорса, формулы Колли-Толленса
Структурные формулы углеводов принято изображать в виде проекционных формул Фишера, Хеуорса, Колли-Толленса структурная формула цепная форма формулы Фишера циклическая форма формулы Хеуорса, формулы Колли-Толленса
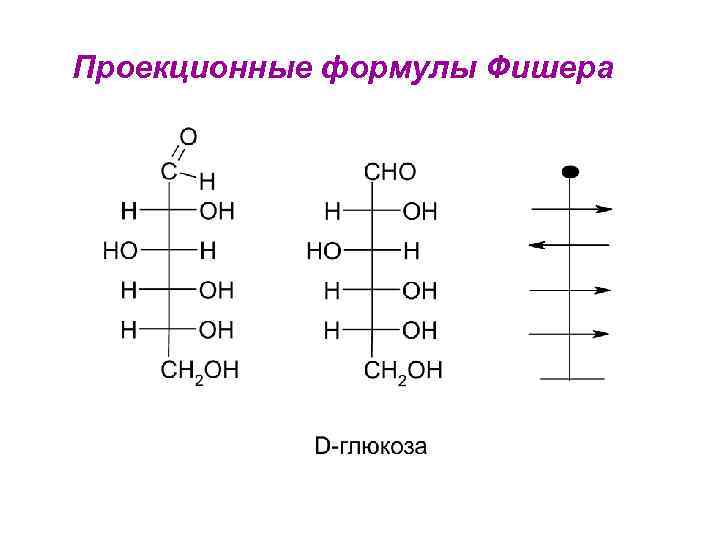 Проекционные формулы Фишера
Проекционные формулы Фишера
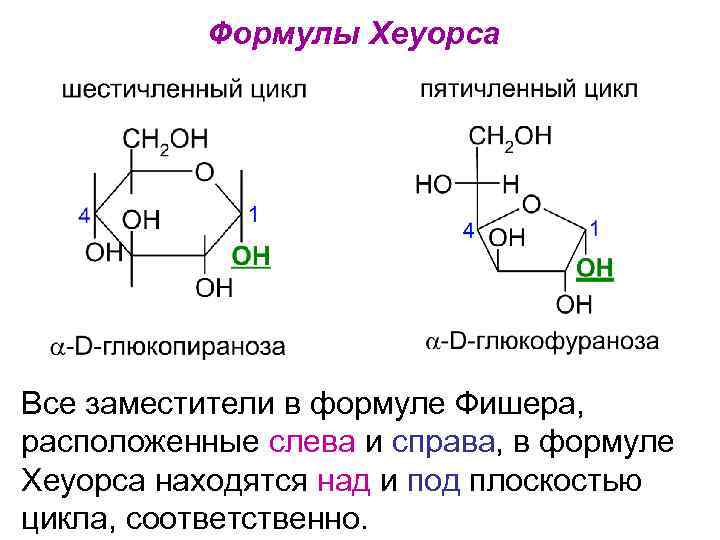 Формулы Хеуорса Все заместители в формуле Фишера, расположенные слева и справа, в формуле Хеуорса находятся над и под плоскостью цикла, соответственно.
Формулы Хеуорса Все заместители в формуле Фишера, расположенные слева и справа, в формуле Хеуорса находятся над и под плоскостью цикла, соответственно.
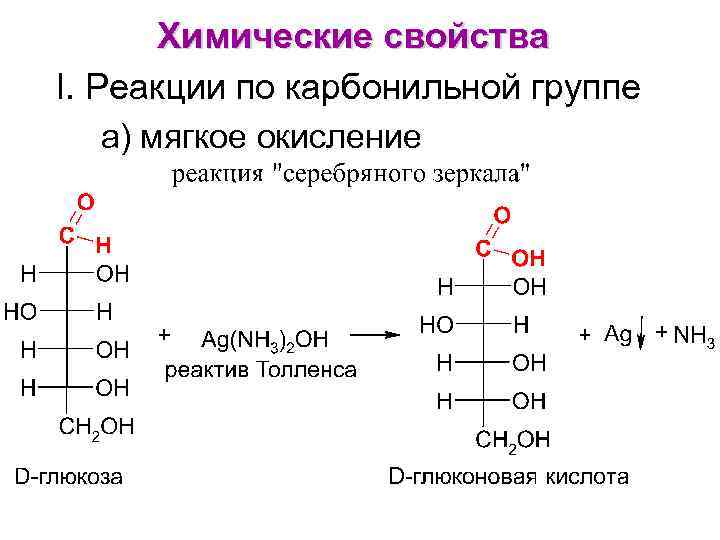 Химические свойства I. Реакции по карбонильной группе а) мягкое окисление
Химические свойства I. Реакции по карбонильной группе а) мягкое окисление
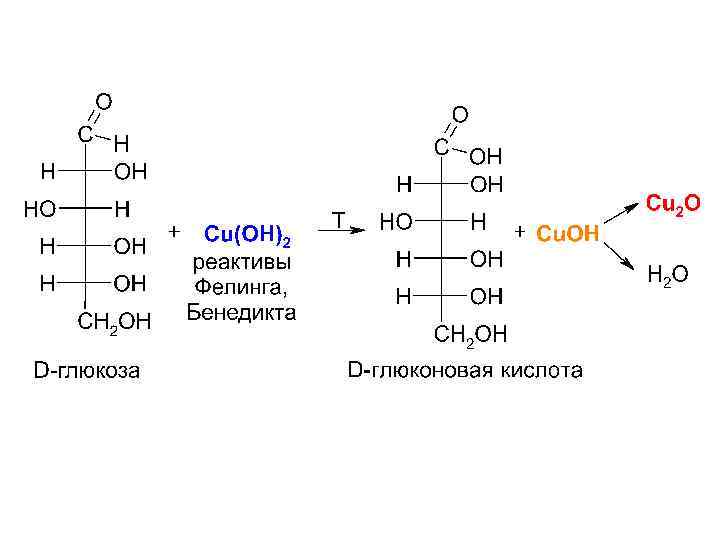

 б) жесткое окисление
б) жесткое окисление
 в) восстановление
в) восстановление

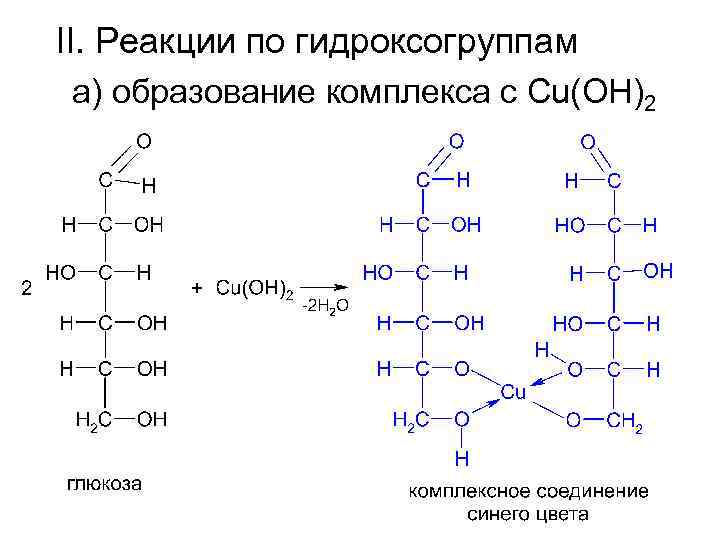 II. Реакции по гидроксогруппам а) образование комплекса с Cu(OH)2
II. Реакции по гидроксогруппам а) образование комплекса с Cu(OH)2
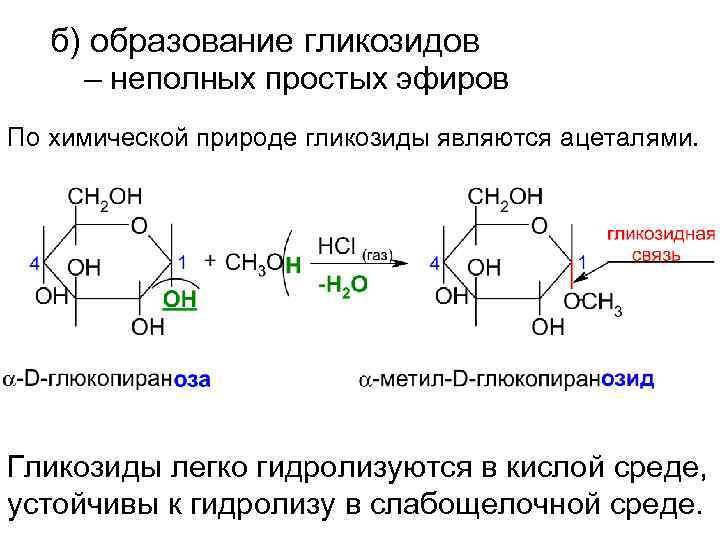 б) образование гликозидов – неполных простых эфиров По химической природе гликозиды являются ацеталями. Гликозиды легко гидролизуются в кислой среде, устойчивы к гидролизу в слабощелочной среде.
б) образование гликозидов – неполных простых эфиров По химической природе гликозиды являются ацеталями. Гликозиды легко гидролизуются в кислой среде, устойчивы к гидролизу в слабощелочной среде.
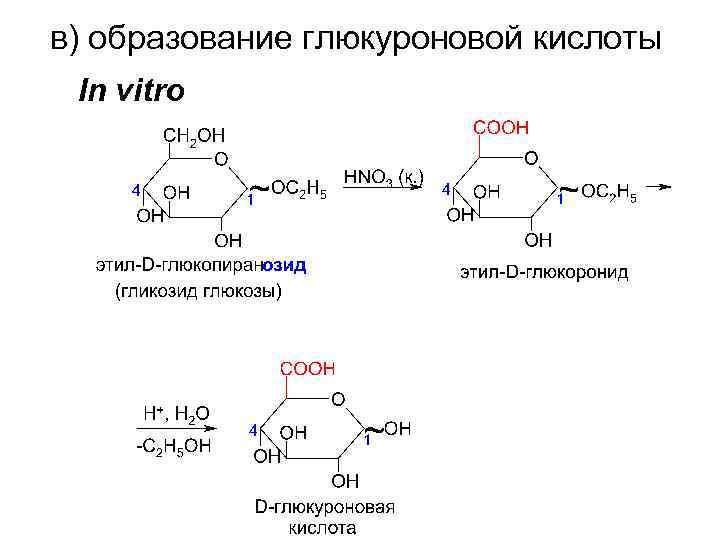 в) образование глюкуроновой кислоты In vitro
в) образование глюкуроновой кислоты In vitro
 г) образование полных простых эфиров
г) образование полных простых эфиров
 Гидролизу легко подвергается только гликозидная связь:
Гидролизу легко подвергается только гликозидная связь:
 г) образование сложных эфиров
г) образование сложных эфиров
 д) образование фосфорных эфиров In vivo
д) образование фосфорных эфиров In vivo
 Биологическое значение моносахаридов • Моносахариды (глюкоза, фруктоза, галактоза) – важнейший источник энергии для организма (около 500 г/сут). Широко распространены в природе в форме разнообразных полисахаридов. • Используются почти во всех биосинтетических процессах организма (гликоген, структурные полисахариды, жиры, ХС и стероиды и др. ). • Рибоза и 2 -дезоксирибоза необходимы для биосинтеза нуклеотидов и нуклеиновых кислот. • Глюкуроновая кислота необходима для обезвреживания и выведения ксенобиотиков из организма. • Сиаловые кислоты входят в состав поверхностных антигенов клетки, необходимых для правильной работы иммунной системы. • Применяются в лечебных целях (глюкоза, глюконат кальция, витамин С) и входят в состав лекарств.
Биологическое значение моносахаридов • Моносахариды (глюкоза, фруктоза, галактоза) – важнейший источник энергии для организма (около 500 г/сут). Широко распространены в природе в форме разнообразных полисахаридов. • Используются почти во всех биосинтетических процессах организма (гликоген, структурные полисахариды, жиры, ХС и стероиды и др. ). • Рибоза и 2 -дезоксирибоза необходимы для биосинтеза нуклеотидов и нуклеиновых кислот. • Глюкуроновая кислота необходима для обезвреживания и выведения ксенобиотиков из организма. • Сиаловые кислоты входят в состав поверхностных антигенов клетки, необходимых для правильной работы иммунной системы. • Применяются в лечебных целях (глюкоза, глюконат кальция, витамин С) и входят в состав лекарств.
 Особая роль D-глюкозы • Универсальное питательное вещество для любых клеток. • Используется клетками как в энергетических, так и в пластических целях. • Единственный источник энергии для клеток человека в анаэробных условиях, абсолютно необходима для эритроцитов, чрезвычайно важна для нейронов. • Используется клетками для биосинтеза практически всех метаболитов и запасающих веществ, содержится в крови (3, 3 -5, 5 ммоль/л), при недостатке биосинтезируется из лактата, глицерина, аминокислот (белков организма). • Широко распространена в природе, в основном в виде биополимеров – полисахаридов.
Особая роль D-глюкозы • Универсальное питательное вещество для любых клеток. • Используется клетками как в энергетических, так и в пластических целях. • Единственный источник энергии для клеток человека в анаэробных условиях, абсолютно необходима для эритроцитов, чрезвычайно важна для нейронов. • Используется клетками для биосинтеза практически всех метаболитов и запасающих веществ, содержится в крови (3, 3 -5, 5 ммоль/л), при недостатке биосинтезируется из лактата, глицерина, аминокислот (белков организма). • Широко распространена в природе, в основном в виде биополимеров – полисахаридов.
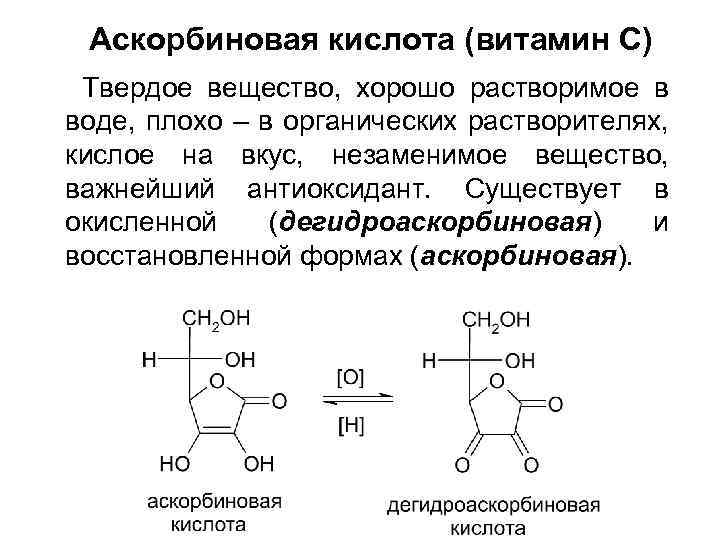 Аскорбиновая кислота (витамин С) Твердое вещество, хорошо растворимое в воде, плохо – в органических растворителях, кислое на вкус, незаменимое вещество, важнейший антиоксидант. Существует в окисленной (дегидроаскорбиновая) и восстановленной формах (аскорбиновая).
Аскорбиновая кислота (витамин С) Твердое вещество, хорошо растворимое в воде, плохо – в органических растворителях, кислое на вкус, незаменимое вещество, важнейший антиоксидант. Существует в окисленной (дегидроаскорбиновая) и восстановленной формах (аскорбиновая).
 Необходима для биосинтеза коллагена, норадреналина, стероидных гормонов, регенерации витамина Е в клеточных мембранах. Потребность 50 -125 мг/сут, при недостатке развивается цинга.
Необходима для биосинтеза коллагена, норадреналина, стероидных гормонов, регенерации витамина Е в клеточных мембранах. Потребность 50 -125 мг/сут, при недостатке развивается цинга.


