Моносахариды органика.pptx
- Количество слайдов: 105
 Углеводы моносахариды Сn. H 2 n. On n=3 -10 o олигосахариды (С 6 H 10 O 5)n n<10 o полисахариды (С 6 H 10 O 5)n n>10 o 2
Углеводы моносахариды Сn. H 2 n. On n=3 -10 o олигосахариды (С 6 H 10 O 5)n n<10 o полисахариды (С 6 H 10 O 5)n n>10 o 2
 Значение углеводов: o Источник энергии Структурная функция o Участвуют в иммунных реакциях организма o Используются в фармации и медицине o 3
Значение углеводов: o Источник энергии Структурная функция o Участвуют в иммунных реакциях организма o Используются в фармации и медицине o 3
 МОНОСАХАРИДЫ циклические полуацетали альдегидоили кетономногоатомных спиртов, существующие в растворе в равновесии со своими таутомерными ациклическими формами 4
МОНОСАХАРИДЫ циклические полуацетали альдегидоили кетономногоатомных спиртов, существующие в растворе в равновесии со своими таутомерными ациклическими формами 4
 Моносахариды образуются в процессе фотосинтеза х. CO 2 + у. H 2 O + Е → Cx(H 2 O)y + x. O 2 5
Моносахариды образуются в процессе фотосинтеза х. CO 2 + у. H 2 O + Е → Cx(H 2 O)y + x. O 2 5
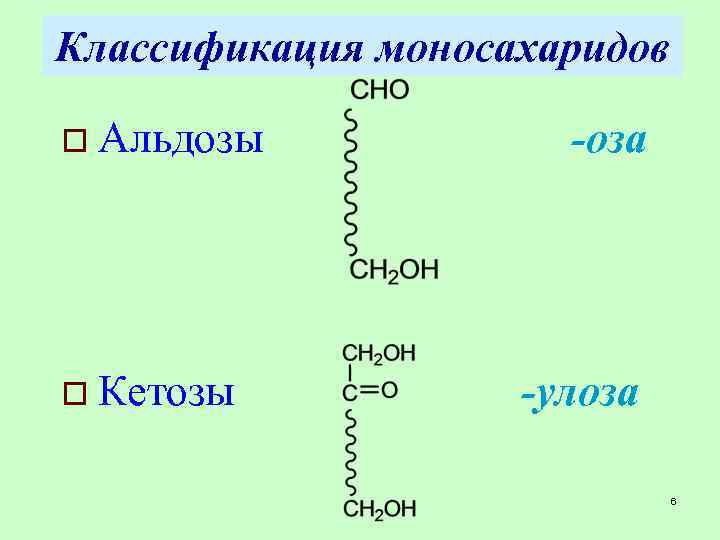 Классификация моносахаридов o Альдозы o Кетозы -оза -улоза 6
Классификация моносахаридов o Альдозы o Кетозы -оза -улоза 6
 Классификация моносахаридов по числу атомов углерода Триозы o Тетрозы o Пентозы o Гексозы o по отношению к стереохимическому ряду Do Lo 7
Классификация моносахаридов по числу атомов углерода Триозы o Тетрозы o Пентозы o Гексозы o по отношению к стереохимическому ряду Do Lo 7
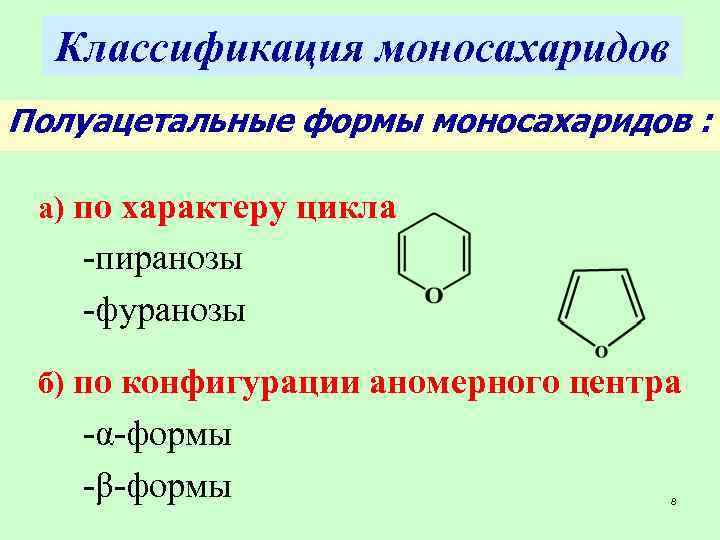 Классификация моносахаридов Полуацетальные формы моносахаридов : а) по характеру цикла -пиранозы -фуранозы б) по конфигурации аномерного центра -α-формы -β-формы 8
Классификация моносахаридов Полуацетальные формы моносахаридов : а) по характеру цикла -пиранозы -фуранозы б) по конфигурации аномерного центра -α-формы -β-формы 8
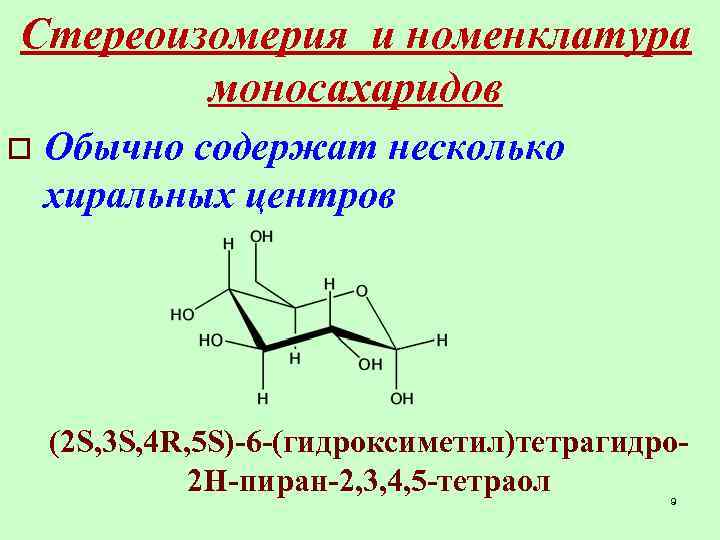 Стереоизомерия и номенклатура моносахаридов o Обычно содержат несколько хиральных центров (2 S, 3 S, 4 R, 5 S)-6 -(гидроксиметил)тетрагидро 2 H-пиран-2, 3, 4, 5 -тетраол 9
Стереоизомерия и номенклатура моносахаридов o Обычно содержат несколько хиральных центров (2 S, 3 S, 4 R, 5 S)-6 -(гидроксиметил)тетрагидро 2 H-пиран-2, 3, 4, 5 -тетраол 9
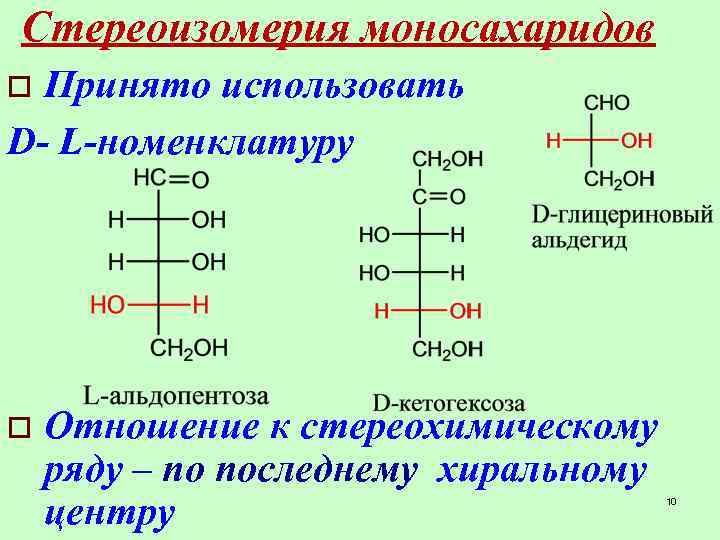 Стереоизомерия моносахаридов Принято использовать D- L-номенклатуру o o Отношение к стереохимическому ряду – по последнему хиральному центру 10
Стереоизомерия моносахаридов Принято использовать D- L-номенклатуру o o Отношение к стереохимическому ряду – по последнему хиральному центру 10
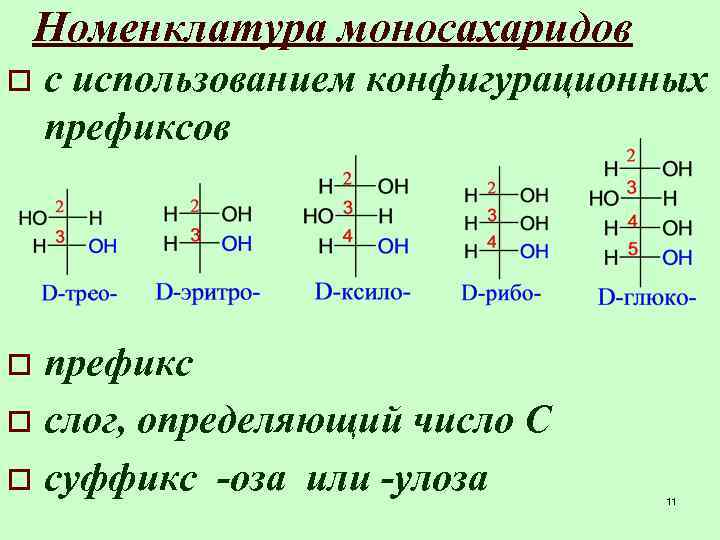 Номенклатура моносахаридов o с использованием конфигурационных префиксов префикс o слог, определяющий число С o суффикс -оза или -улоза o 11
Номенклатура моносахаридов o с использованием конфигурационных префиксов префикс o слог, определяющий число С o суффикс -оза или -улоза o 11
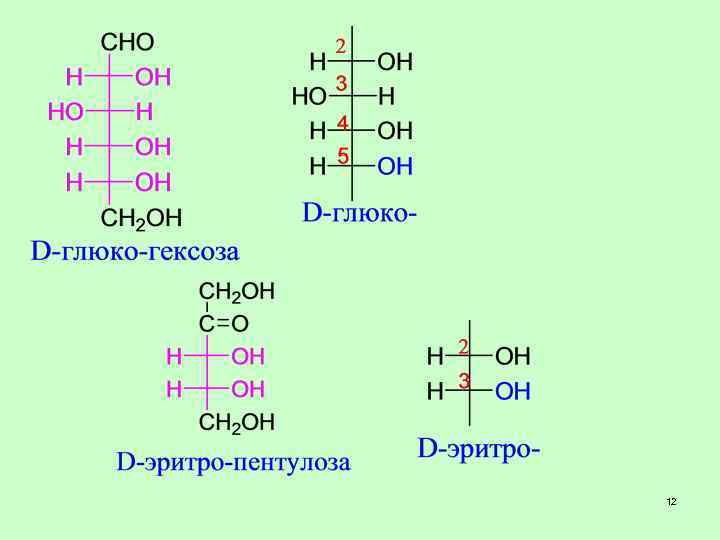 12
12
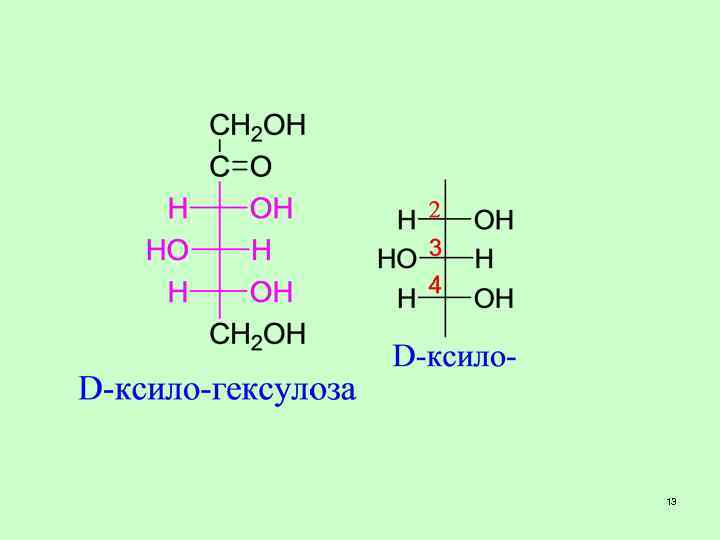 13
13
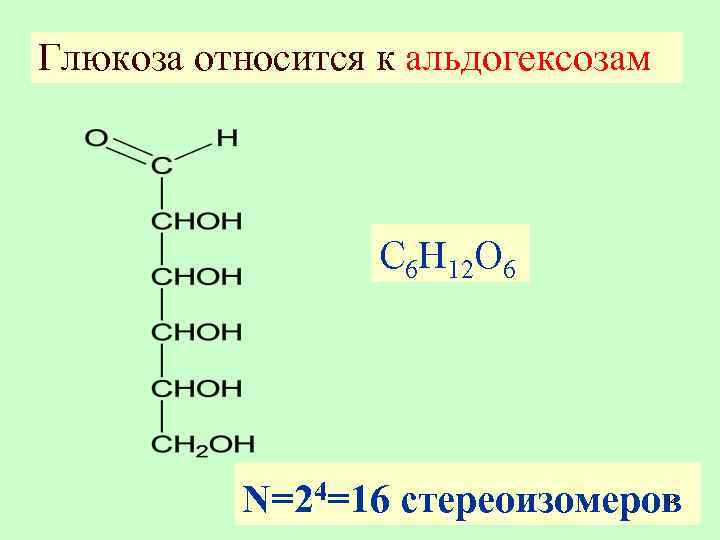 Глюкоза относится к альдогексозам С 6 H 12 O 6 N=24=16 стереоизомеров 14
Глюкоза относится к альдогексозам С 6 H 12 O 6 N=24=16 стереоизомеров 14
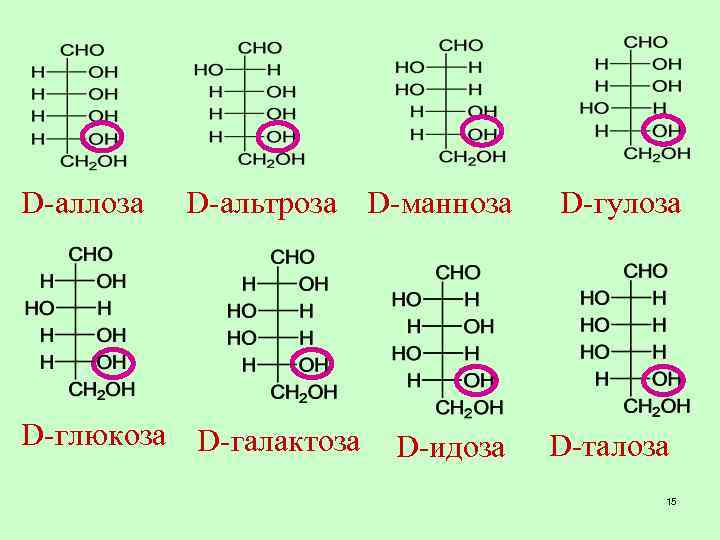 D-аллоза D-альтроза D-манноза D-глюкоза D-галактоза D-идоза D-гулоза D-талоза 15
D-аллоза D-альтроза D-манноза D-глюкоза D-галактоза D-идоза D-гулоза D-талоза 15
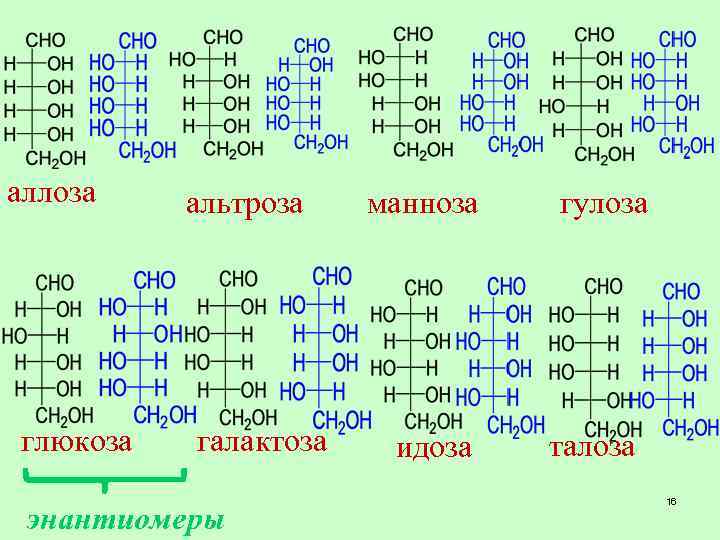 аллоза глюкоза альтроза галактоза энантиомеры манноза идоза гулоза талоза 16
аллоза глюкоза альтроза галактоза энантиомеры манноза идоза гулоза талоза 16
 Эпимеры o Это стереоизомеры, отличающиеся конфигурацией только 1 хирального центра 17
Эпимеры o Это стереоизомеры, отличающиеся конфигурацией только 1 хирального центра 17
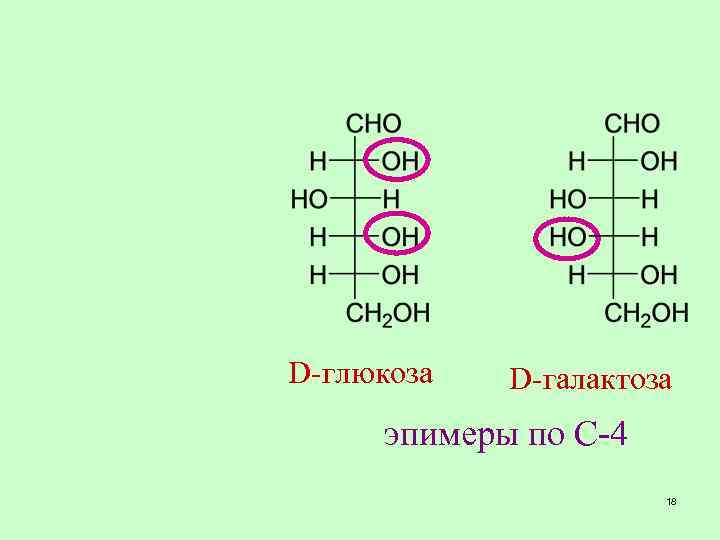 D-манноза эпимеры по С-2 D-глюкоза D-галактоза эпимеры по С-4 18
D-манноза эпимеры по С-2 D-глюкоза D-галактоза эпимеры по С-4 18
 Неклассические моносахариды. Производные моносахаридов o Моносахариды, в которых отсутствует спиртовая группа, называют дезоксисахарами o Моносахариды, в которых гидроксильная группа замещена на амино группу, называют аминосахарами 19
Неклассические моносахариды. Производные моносахаридов o Моносахариды, в которых отсутствует спиртовая группа, называют дезоксисахарами o Моносахариды, в которых гидроксильная группа замещена на амино группу, называют аминосахарами 19
 Неклассические моносахариды. Производные моносахаридов o Многоатомные спирты, образованные восстановлением карбонильной группы моносахарида, называют альдитолами o Монокарбоновые кислоты, образованные окислением альдегидной группы моносахарида, называют альдоновыми кислотами 20
Неклассические моносахариды. Производные моносахаридов o Многоатомные спирты, образованные восстановлением карбонильной группы моносахарида, называют альдитолами o Монокарбоновые кислоты, образованные окислением альдегидной группы моносахарида, называют альдоновыми кислотами 20
 Неклассические моносахариды. Производные моносахаридов o Монокарбоновые кислоты, образованные окислением первичноспиртовой группы, называют уроновыми кислотами o Дикарбоновые кислоты, образованные окислением альдегидной и первичноспиртовой групп, называют альдаровыми кислотами 21
Неклассические моносахариды. Производные моносахаридов o Монокарбоновые кислоты, образованные окислением первичноспиртовой группы, называют уроновыми кислотами o Дикарбоновые кислоты, образованные окислением альдегидной и первичноспиртовой групп, называют альдаровыми кислотами 21
 Неклассические моносахариды. Производные моносахаридов o Смешанные ацетали моносахаридов называют гликозидами 22
Неклассические моносахариды. Производные моносахаридов o Смешанные ацетали моносахаридов называют гликозидами 22
 D-глюкоза декстроза +52, 5° 23
D-глюкоза декстроза +52, 5° 23
 Открытые формулы не объясняют следующие факты: o o в спектрах поглощения отсутствует полоса, соответствующая карбонильной группе в реакции ацетализации присоединяется только 1 моль спирта растворы моносахаридов не дают реакцию с фунсинсернистой кислотой для растворов моносахаридов характерна мутаротация 24
Открытые формулы не объясняют следующие факты: o o в спектрах поглощения отсутствует полоса, соответствующая карбонильной группе в реакции ацетализации присоединяется только 1 моль спирта растворы моносахаридов не дают реакцию с фунсинсернистой кислотой для растворов моносахаридов характерна мутаротация 24
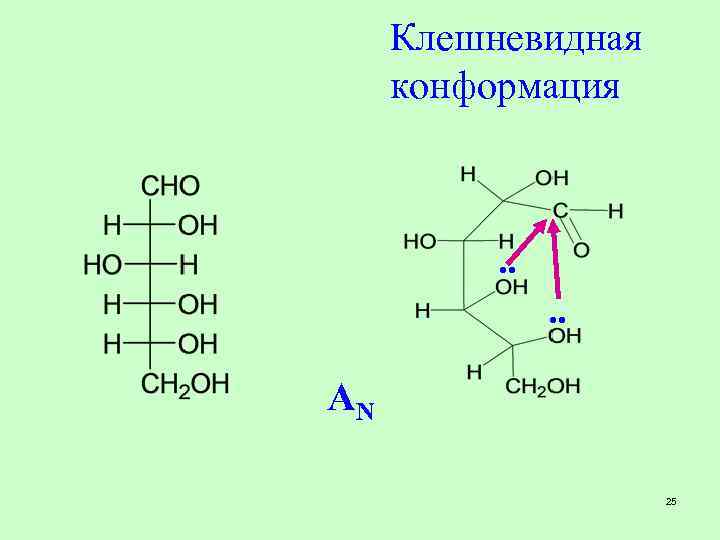 Клешневидная конформация . . AN 25
Клешневидная конформация . . AN 25
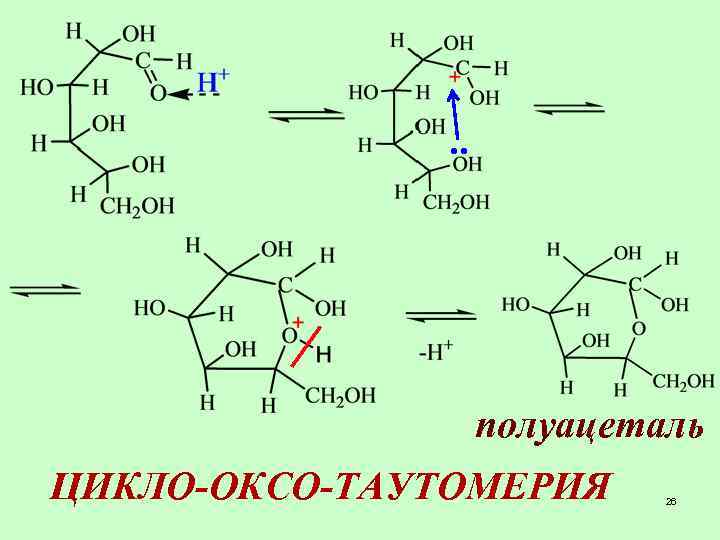 . . полуацеталь ЦИКЛО-ОКСО-ТАУТОМЕРИЯ 26
. . полуацеталь ЦИКЛО-ОКСО-ТАУТОМЕРИЯ 26
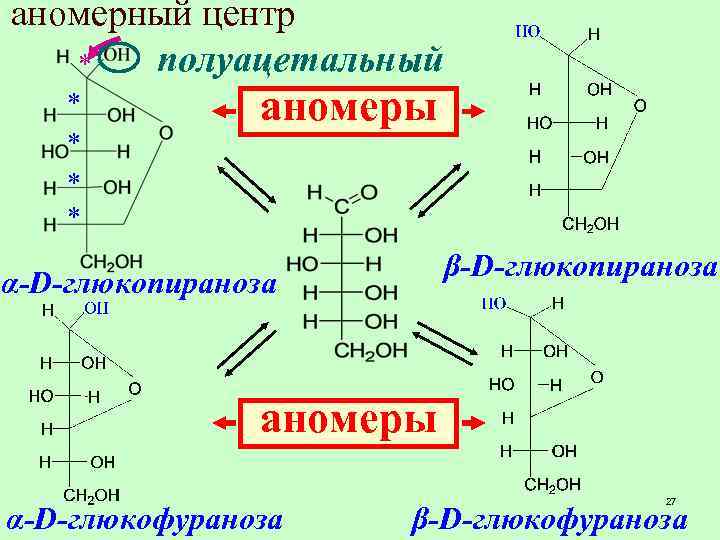 аномерный центр полуацетальный * * * аномеры β-D-глюкопираноза α-D-глюкопираноза аномеры α-D-глюкофураноза 27 β-D-глюкофураноза
аномерный центр полуацетальный * * * аномеры β-D-глюкопираноза α-D-глюкопираноза аномеры α-D-глюкофураноза 27 β-D-глюкофураноза
 Аномеры-пара стереоизомеров, отличающихся конфигурацией аномерного центра o Аномеры-это диастереомеры o В кристаллическом состоянии только в циклической форме o В растворе моносахариды преимущественно в циклической форме o 28
Аномеры-пара стереоизомеров, отличающихся конфигурацией аномерного центра o Аномеры-это диастереомеры o В кристаллическом состоянии только в циклической форме o В растворе моносахариды преимущественно в циклической форме o 28
 В растворе моносахарида – 0. 01% ациклической формы 99. 99% - циклические формы o o в спектрах поглощения отсутствует полоса, соответствующая карбонильной группе растворы моносахаридов не дают реакцию с фунсинсернистой кислотой 29
В растворе моносахарида – 0. 01% ациклической формы 99. 99% - циклические формы o o в спектрах поглощения отсутствует полоса, соответствующая карбонильной группе растворы моносахаридов не дают реакцию с фунсинсернистой кислотой 29
 Мутаротация o – изменение угла вращения плоскости поляризованного света у свежеприготовленных растворов моносахаридов в течение некоторого времени (1, 5 -2 ч. ) 30
Мутаротация o – изменение угла вращения плоскости поляризованного света у свежеприготовленных растворов моносахаридов в течение некоторого времени (1, 5 -2 ч. ) 30
![[α]20=+19° [α]20=+112° 1, 5 -2 ч. [α]20=+52, 5° 31 [α]20=+19° [α]20=+112° 1, 5 -2 ч. [α]20=+52, 5° 31](https://present5.com/presentation/1/9058081_160357042.pdf-img/9058081_160357042.pdf-30.jpg) [α]20=+19° [α]20=+112° 1, 5 -2 ч. [α]20=+52, 5° 31
[α]20=+19° [α]20=+112° 1, 5 -2 ч. [α]20=+52, 5° 31
 Мутаротация В растворе моносахаридов преобладают пиранозные формы α-D-глюкопираноза +112, 5 β-D-глюкопираноза +19, 5 Равновесие устанавливается через 1, 5 -2 ч. +52, 5 2/3β-D-глюкопираноза ⇄1/3α-D-глюкопираноза Переход осуществляется только через открытую форму 32
Мутаротация В растворе моносахаридов преобладают пиранозные формы α-D-глюкопираноза +112, 5 β-D-глюкопираноза +19, 5 Равновесие устанавливается через 1, 5 -2 ч. +52, 5 2/3β-D-глюкопираноза ⇄1/3α-D-глюкопираноза Переход осуществляется только через открытую форму 32
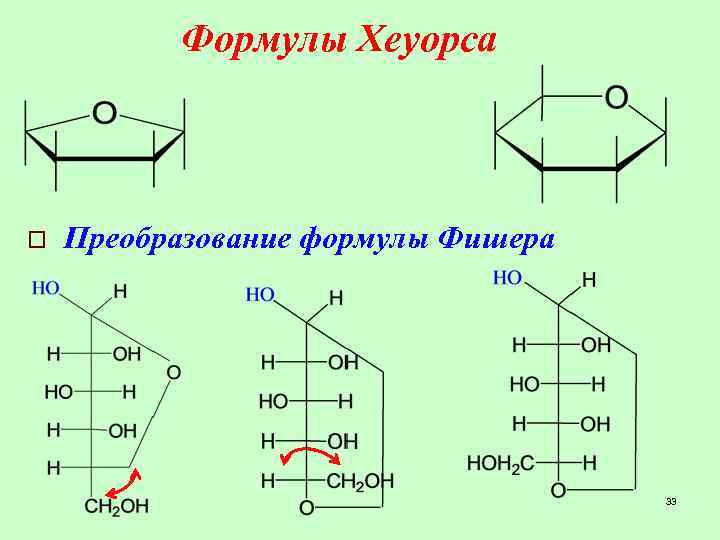 Формулы Хеуорса o Преобразование формулы Фишера 33
Формулы Хеуорса o Преобразование формулы Фишера 33
 Формулы Хеуорса СН 2 ОН ОН ОН 34
Формулы Хеуорса СН 2 ОН ОН ОН 34
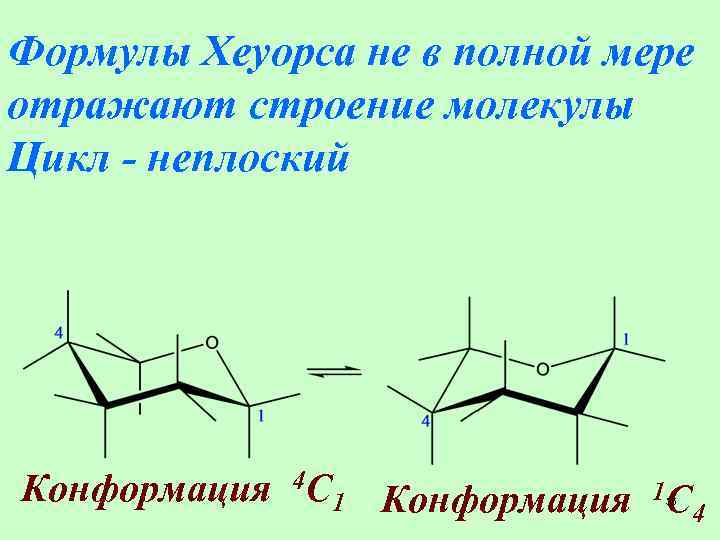 Формулы Хеуорса не в полной мере отражают строение молекулы Цикл - неплоский Конформация 4 С 1 Конформация 1 С 4 35
Формулы Хеуорса не в полной мере отражают строение молекулы Цикл - неплоский Конформация 4 С 1 Конформация 1 С 4 35
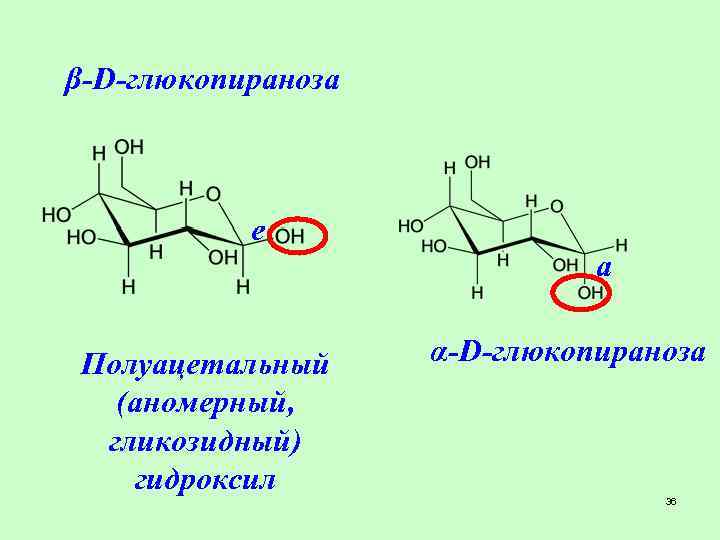 β-D-глюкопираноза е а Полуацетальный (аномерный, гликозидный) гидроксил α-D-глюкопираноза 36
β-D-глюкопираноза е а Полуацетальный (аномерный, гликозидный) гидроксил α-D-глюкопираноза 36
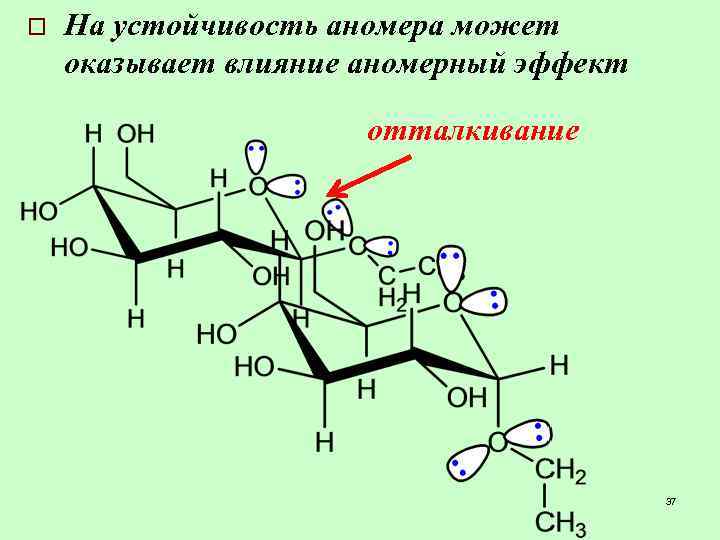 o На устойчивость аномера может оказывает влияние аномерный эффект отталкивание 37
o На устойчивость аномера может оказывает влияние аномерный эффект отталкивание 37
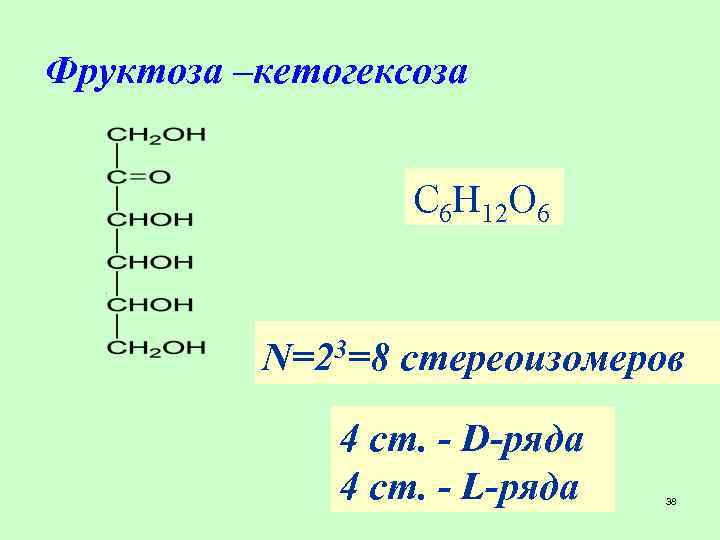 Фруктоза –кетогексоза С 6 H 12 O 6 N=23=8 стереоизомеров 4 ст. - D-ряда 4 ст. - L-ряда 38
Фруктоза –кетогексоза С 6 H 12 O 6 N=23=8 стереоизомеров 4 ст. - D-ряда 4 ст. - L-ряда 38
 Фруктоза D-фруктоза левулоза -82° 39
Фруктоза D-фруктоза левулоза -82° 39
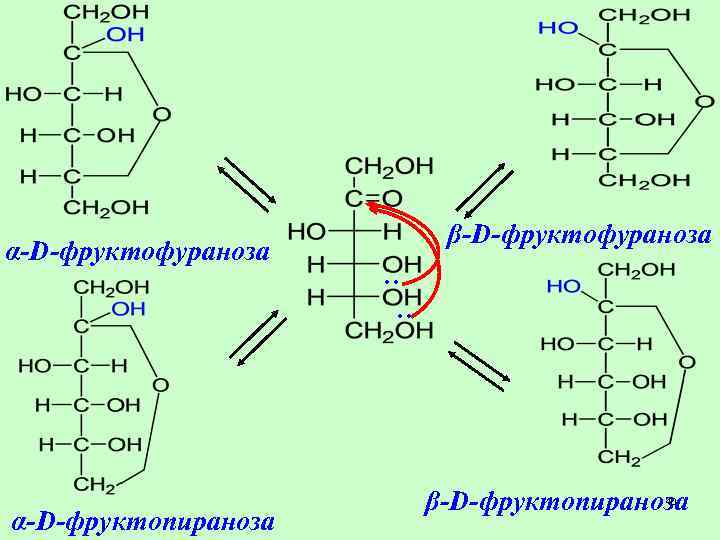 α-D-фруктофураноза α-D-фруктопираноза β-D-фруктофураноза . . β-D-фруктопираноза 40
α-D-фруктофураноза α-D-фруктопираноза β-D-фруктофураноза . . β-D-фруктопираноза 40
 Формулы Хеуорса 41
Формулы Хеуорса 41
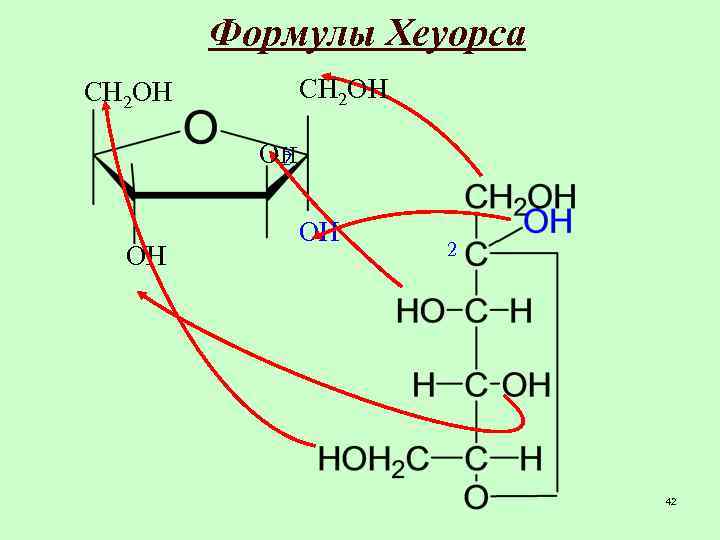 Формулы Хеуорса СН 2 ОН ОН 2 42
Формулы Хеуорса СН 2 ОН ОН 2 42
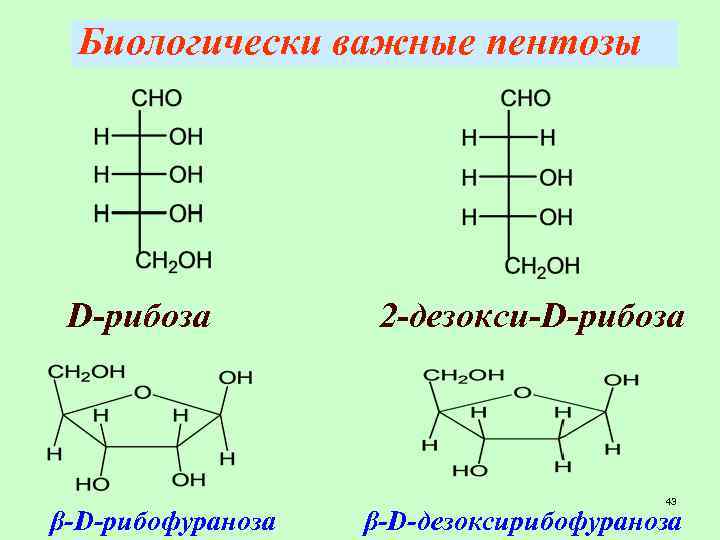 Биологически важные пентозы D-рибоза β-D-рибофураноза 2 -дезокси-D-рибоза 43 β-D-дезоксирибофураноза
Биологически важные пентозы D-рибоза β-D-рибофураноза 2 -дезокси-D-рибоза 43 β-D-дезоксирибофураноза
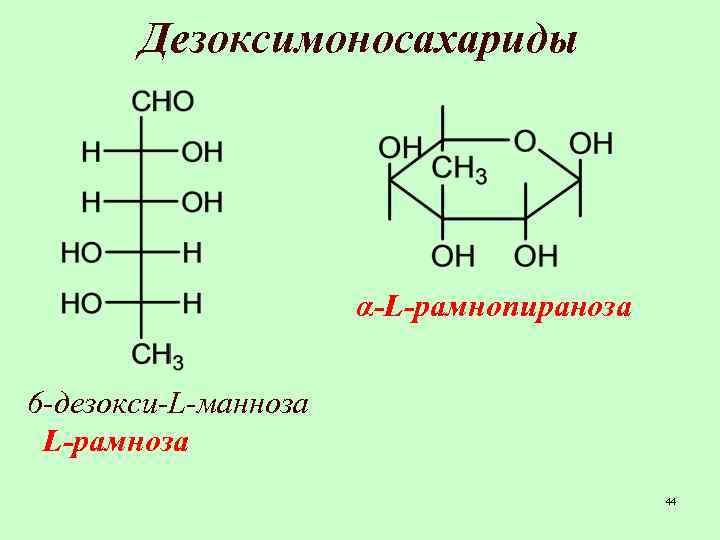 Дезоксимоносахариды α-L-рамнопираноза 6 -дезокси-L-манноза L-рамноза 44
Дезоксимоносахариды α-L-рамнопираноза 6 -дезокси-L-манноза L-рамноза 44
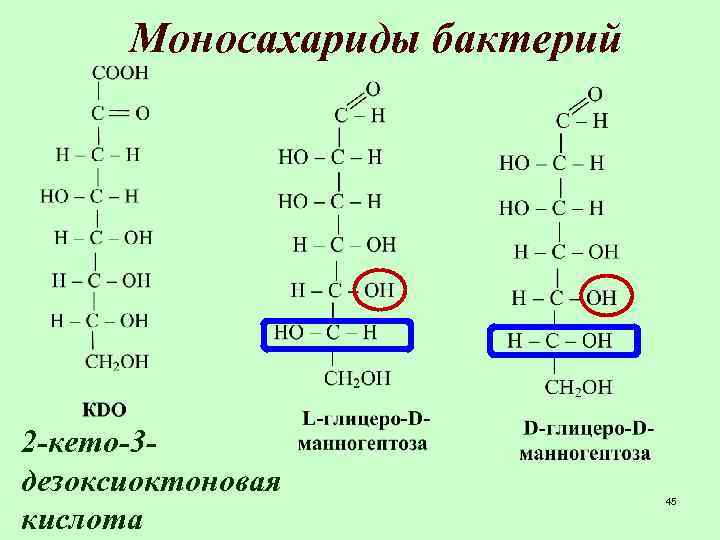 Моносахариды бактерий 2 -кето-3 дезоксиоктоновая кислота 45
Моносахариды бактерий 2 -кето-3 дезоксиоктоновая кислота 45
 Физические свойства моносахаридов o o o кристаллические вещества o гидроксильные группы образуют водородные связи хорошо растворимы в воде, плохо – в малополярных растворителях в водных растворах - сильно гидратированы и образуют вязкие растворы, трудно кристаллизуются 46
Физические свойства моносахаридов o o o кристаллические вещества o гидроксильные группы образуют водородные связи хорошо растворимы в воде, плохо – в малополярных растворителях в водных растворах - сильно гидратированы и образуют вязкие растворы, трудно кристаллизуются 46
![o o имеют сладкий вкус растворы обладают оптической активностью [α]D+112→+52, 5 o использование раствора o o имеют сладкий вкус растворы обладают оптической активностью [α]D+112→+52, 5 o использование раствора](https://present5.com/presentation/1/9058081_160357042.pdf-img/9058081_160357042.pdf-46.jpg) o o имеют сладкий вкус растворы обладают оптической активностью [α]D+112→+52, 5 o использование раствора глюкозы для проведения дезинтоксикации 47
o o имеют сладкий вкус растворы обладают оптической активностью [α]D+112→+52, 5 o использование раствора глюкозы для проведения дезинтоксикации 47
 Химические свойства o Моносахариды – гетерофункциональные соединения o Возможно превращение моносахаридов друга 48
Химические свойства o Моносахариды – гетерофункциональные соединения o Возможно превращение моносахаридов друга 48
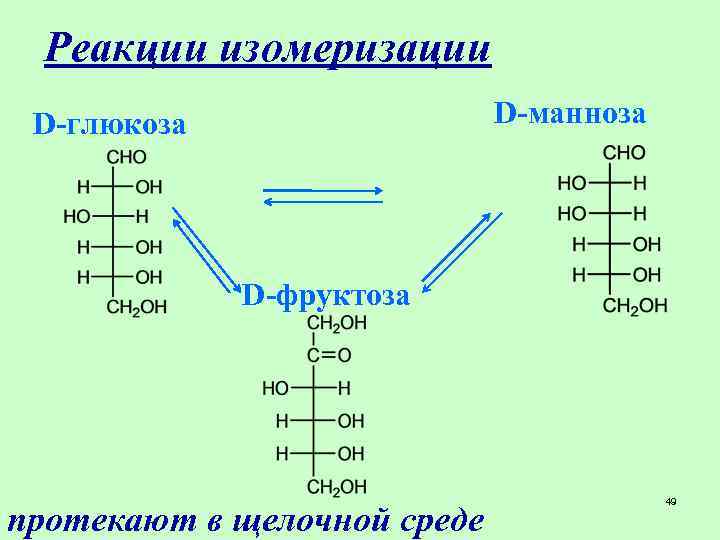 Реакции изомеризации D-манноза D-глюкоза D-фруктоза протекают в щелочной среде 49
Реакции изомеризации D-манноза D-глюкоза D-фруктоза протекают в щелочной среде 49
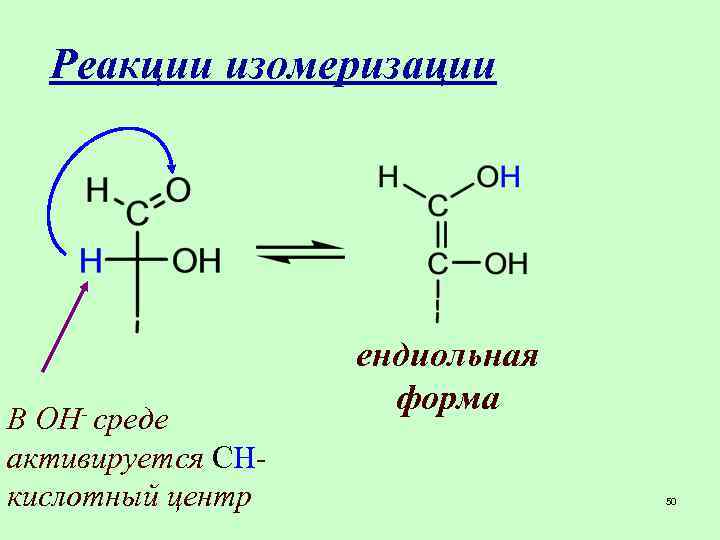 Реакции изомеризации В ОН- среде активируется СНкислотный центр ендиольная форма 50
Реакции изомеризации В ОН- среде активируется СНкислотный центр ендиольная форма 50
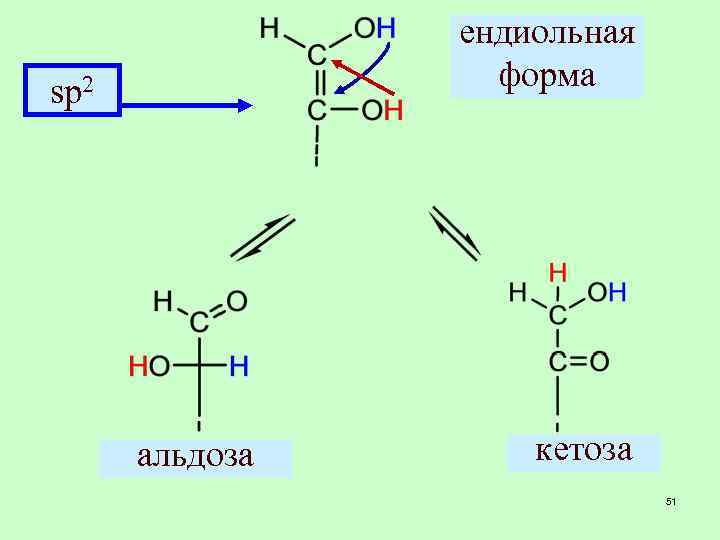 ендиольная форма sp 2 альдоза кетоза 51
ендиольная форма sp 2 альдоза кетоза 51
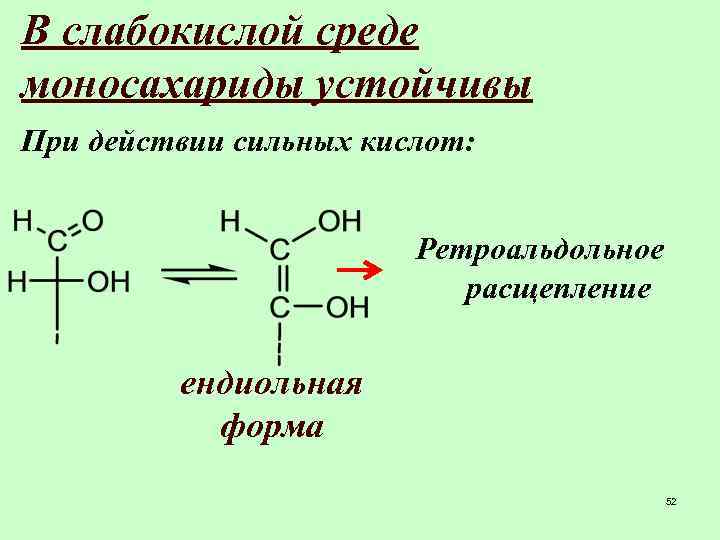 В слабокислой среде моносахариды устойчивы При действии сильных кислот: Ретроальдольное расщепление ендиольная форма 52
В слабокислой среде моносахариды устойчивы При действии сильных кислот: Ретроальдольное расщепление ендиольная форма 52
 o Реакции полуацетального гидроксила Гликозиды – смешанные ацетали циклических форм альдоз или кетоз 53
o Реакции полуацетального гидроксила Гликозиды – смешанные ацетали циклических форм альдоз или кетоз 53
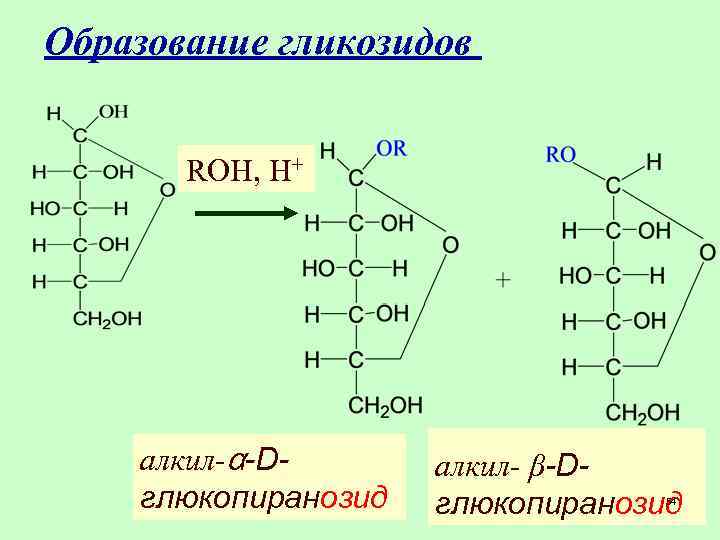 Образование гликозидов ROH, Н+ алкил-α-Dглюкопиранозид алкил- β-Dглюкопиранозид 54
Образование гликозидов ROH, Н+ алкил-α-Dглюкопиранозид алкил- β-Dглюкопиранозид 54
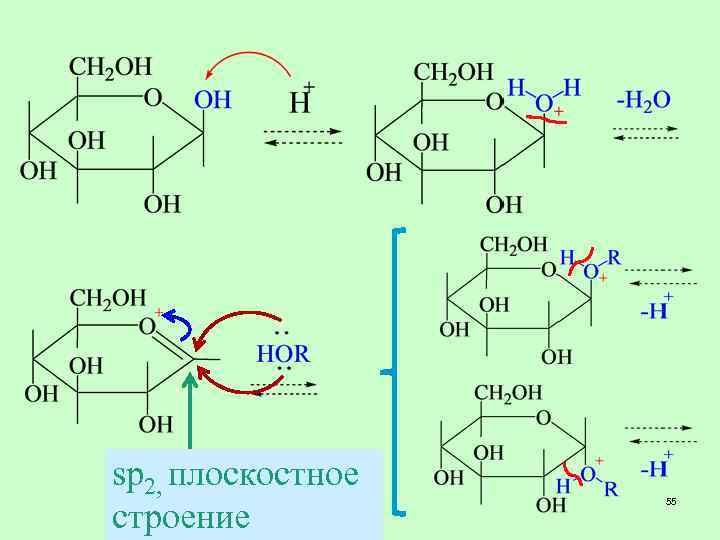 sp 2, плоскостное строение 55
sp 2, плоскостное строение 55
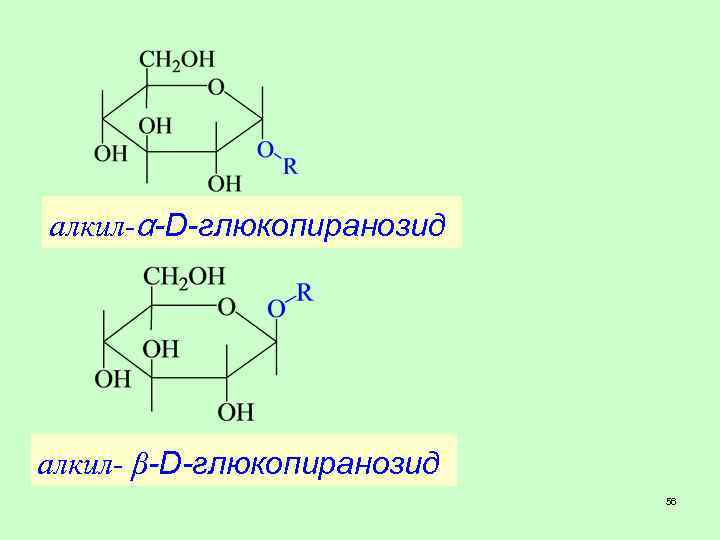 алкил-α-D-глюкопиранозид алкил- β-D-глюкопиранозид 56
алкил-α-D-глюкопиранозид алкил- β-D-глюкопиранозид 56
 гликозиды гидролизуются только в кислой среде гликозиды не мутаротируют Состоят из углеводной части и агликона 57
гликозиды гидролизуются только в кислой среде гликозиды не мутаротируют Состоят из углеводной части и агликона 57
 Различают пиранозиды фуранозиды О-гликозиды N-гликозиды S-гликозиды С-гликозиды 58
Различают пиранозиды фуранозиды О-гликозиды N-гликозиды S-гликозиды С-гликозиды 58
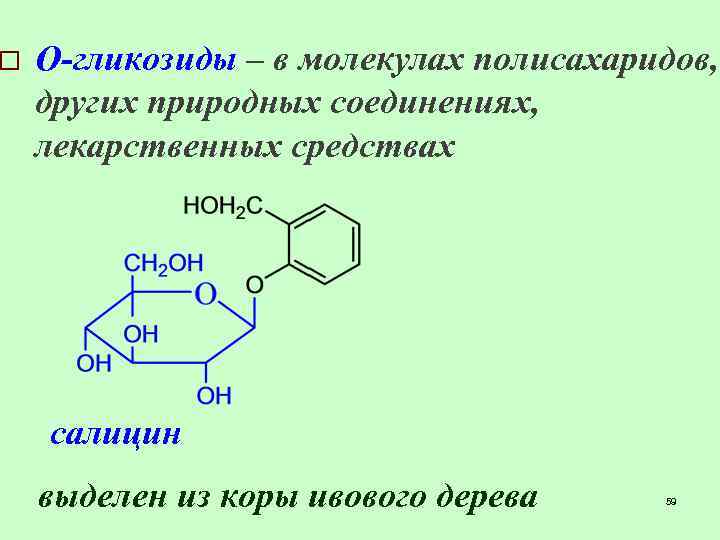 o О-гликозиды – в молекулах полисахаридов, других природных соединениях, лекарственных средствах салицин выделен из коры ивового дерева 59
o О-гликозиды – в молекулах полисахаридов, других природных соединениях, лекарственных средствах салицин выделен из коры ивового дерева 59
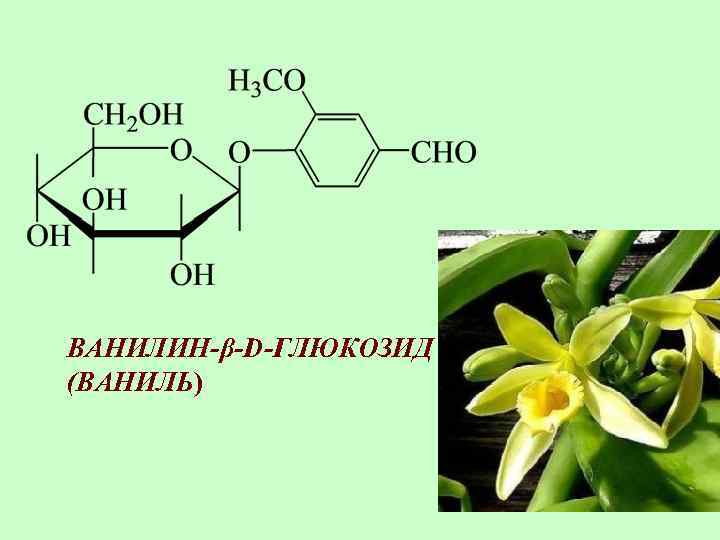 ВАНИЛИН-β-D-ГЛЮКОЗИД (ВАНИЛЬ) 60
ВАНИЛИН-β-D-ГЛЮКОЗИД (ВАНИЛЬ) 60
 o N-гликозиды гликозиламины o гликозиламиды o нуклеозиды o 61
o N-гликозиды гликозиламины o гликозиламиды o нуклеозиды o 61
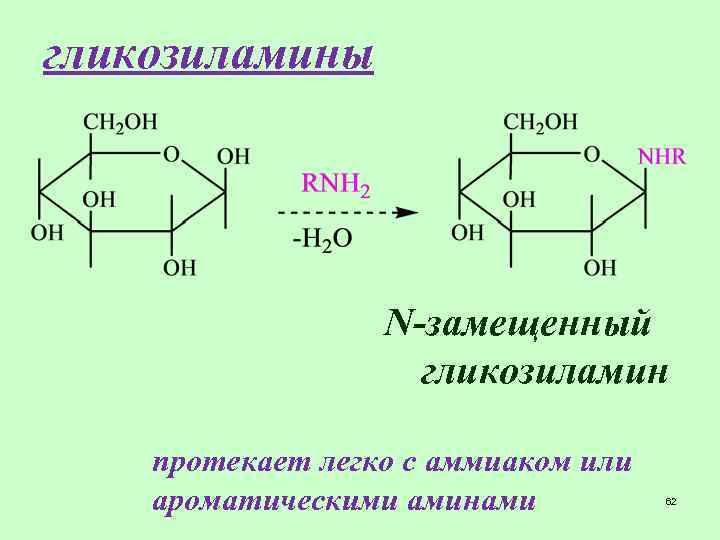 гликозиламины N-замещенный гликозиламин протекает легко с аммиаком или ароматическими аминами 62
гликозиламины N-замещенный гликозиламин протекает легко с аммиаком или ароматическими аминами 62
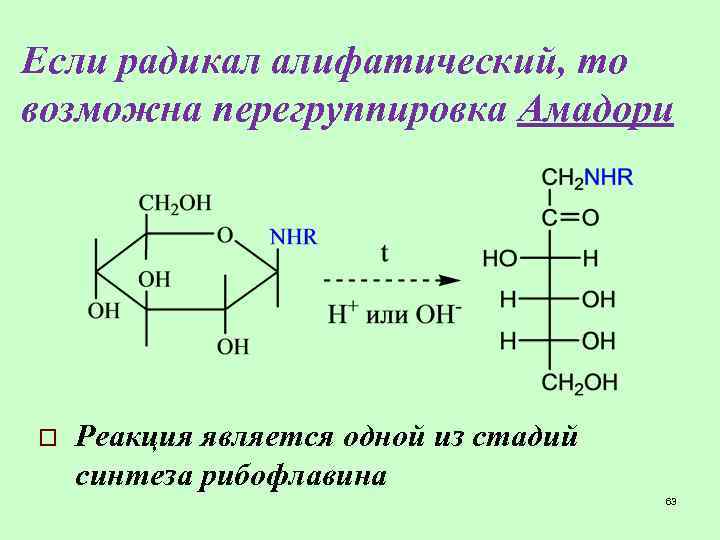 Если радикал алифатический, то возможна перегруппировка Амадори o Реакция является одной из стадий синтеза рибофлавина 63
Если радикал алифатический, то возможна перегруппировка Амадори o Реакция является одной из стадий синтеза рибофлавина 63
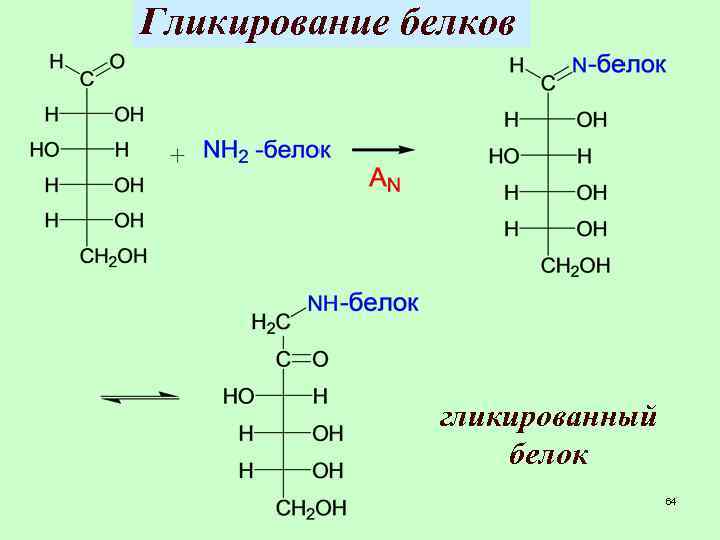 Гликирование белков гликированный белок 64
Гликирование белков гликированный белок 64
 o гликозиламины легко гидролизуются o способны к мутаротации 65
o гликозиламины легко гидролизуются o способны к мутаротации 65
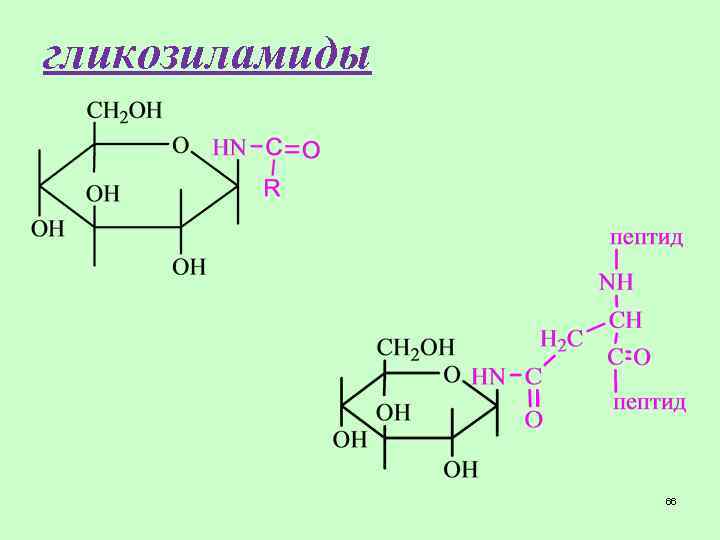 гликозиламиды 66
гликозиламиды 66
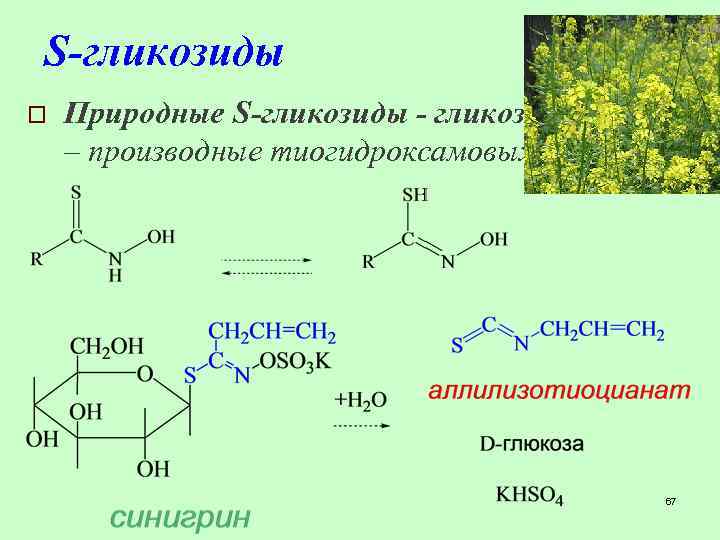 S-гликозиды o Природные S-гликозиды - гликозинолаты – производные тиогидроксамовых кислот 67
S-гликозиды o Природные S-гликозиды - гликозинолаты – производные тиогидроксамовых кислот 67
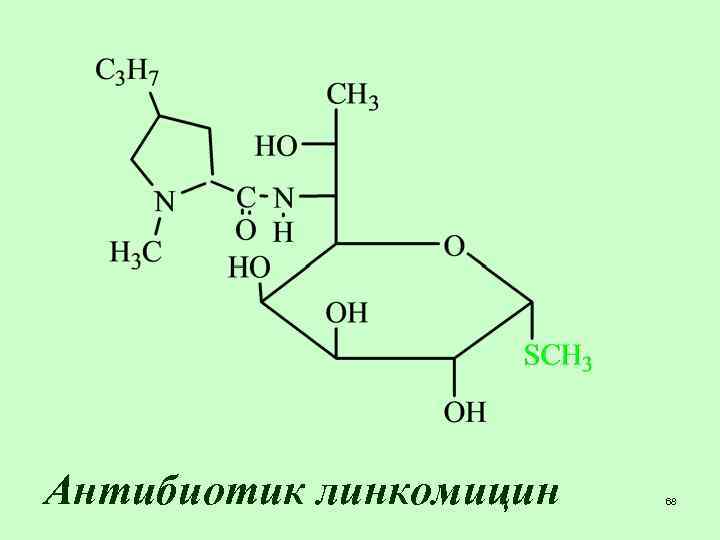 Антибиотик линкомицин 68
Антибиотик линкомицин 68
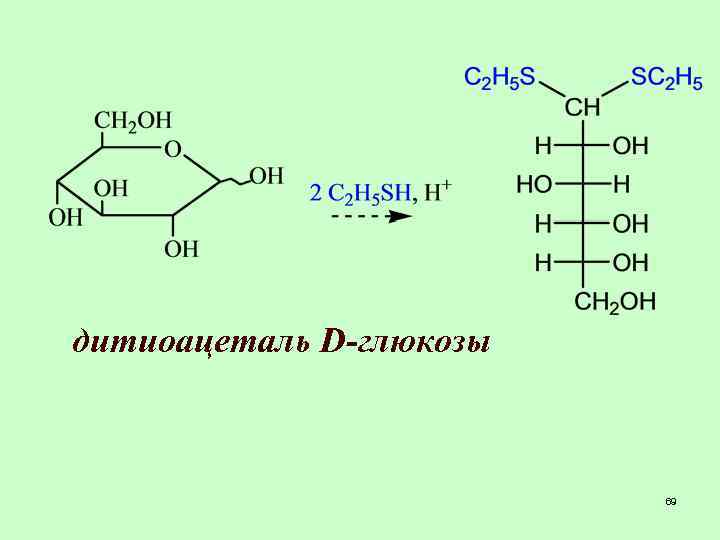 дитиоацеталь D-глюкозы 69
дитиоацеталь D-глюкозы 69
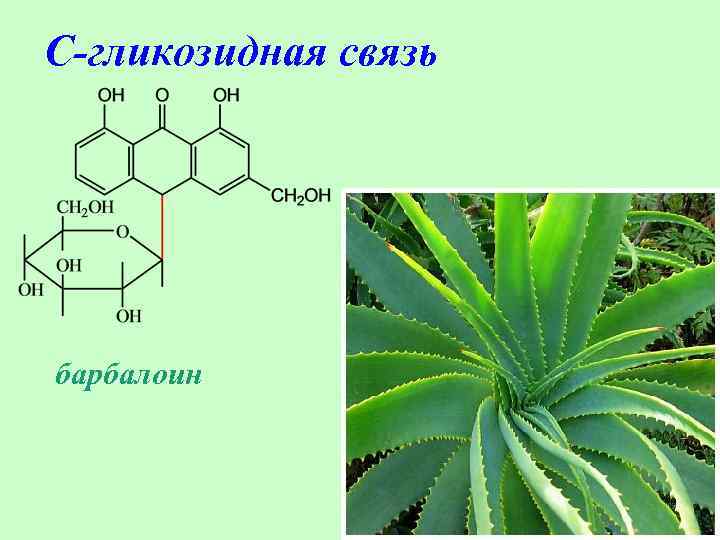 С-гликозидная связь барбалоин 70
С-гликозидная связь барбалоин 70
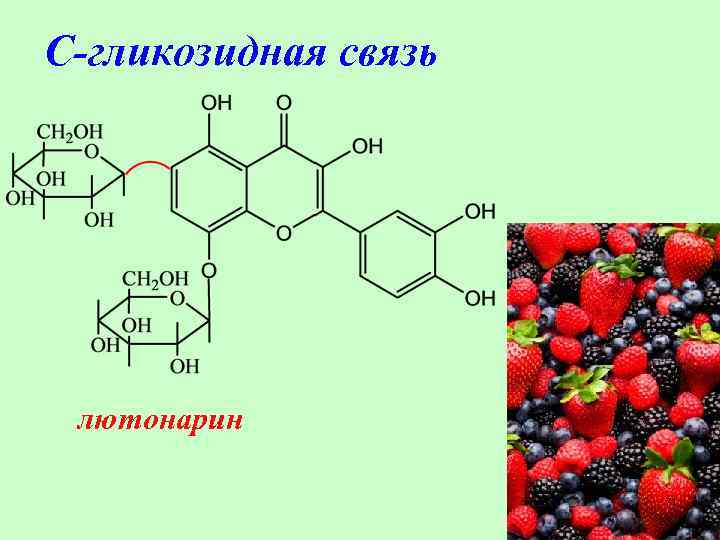 С-гликозидная связь лютонарин 71
С-гликозидная связь лютонарин 71
![Реакции окисления в ОН- среде: Реактив Толленса [Ag(NH 3)2]OH Реактив Фелинга o Сu 2+ Реакции окисления в ОН- среде: Реактив Толленса [Ag(NH 3)2]OH Реактив Фелинга o Сu 2+](https://present5.com/presentation/1/9058081_160357042.pdf-img/9058081_160357042.pdf-71.jpg) Реакции окисления в ОН- среде: Реактив Толленса [Ag(NH 3)2]OH Реактив Фелинга o Сu 2+ Реактив Бенедикта • характерно для альдоз и кетоз 72
Реакции окисления в ОН- среде: Реактив Толленса [Ag(NH 3)2]OH Реактив Фелинга o Сu 2+ Реактив Бенедикта • характерно для альдоз и кетоз 72
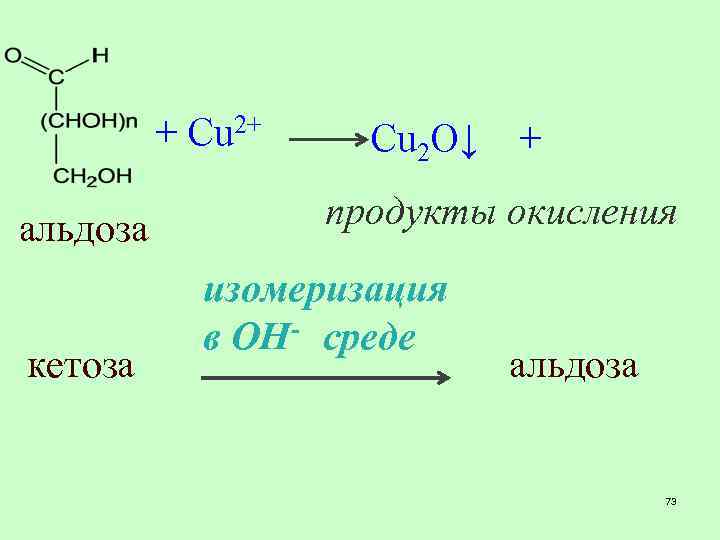 + Cu 2+ альдоза кетоза Cu 2 O↓ + продукты окисления изомеризация в ОН- среде альдоза 73
+ Cu 2+ альдоза кетоза Cu 2 O↓ + продукты окисления изомеризация в ОН- среде альдоза 73
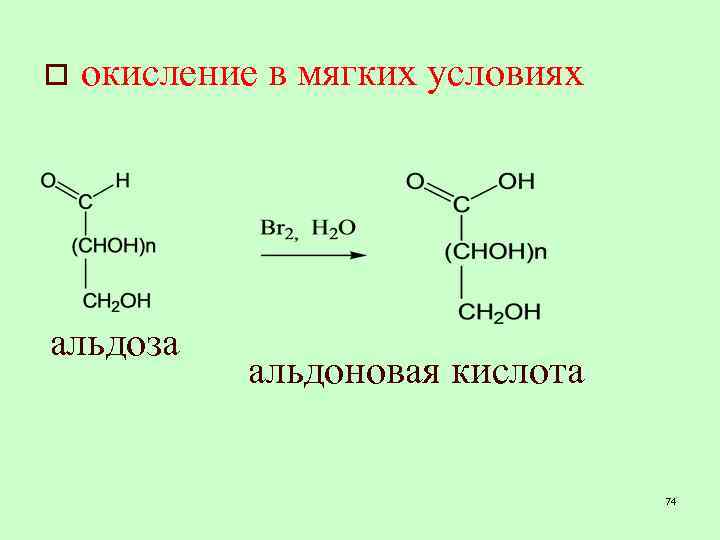 o окисление в мягких условиях альдоза альдоновая кислота 74
o окисление в мягких условиях альдоза альдоновая кислота 74
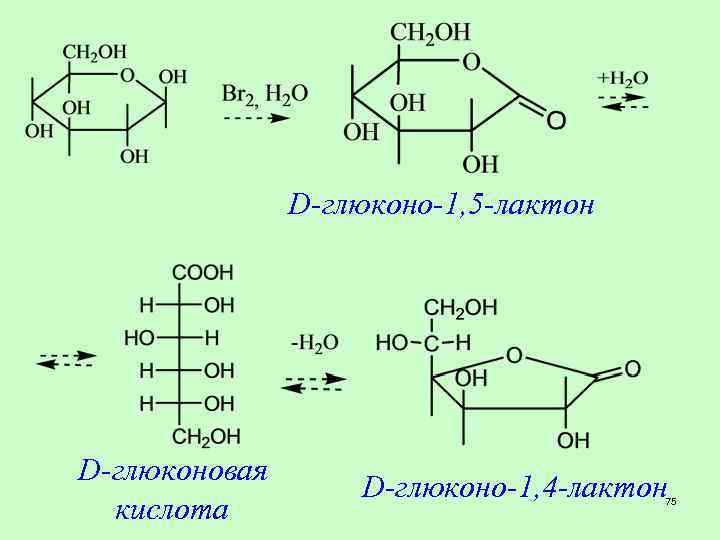 D-глюконо-1, 5 -лактон D-глюконовая кислота D-глюконо-1, 4 -лактон 75
D-глюконо-1, 5 -лактон D-глюконовая кислота D-глюконо-1, 4 -лактон 75
 Глюконат кальция 76
Глюконат кальция 76
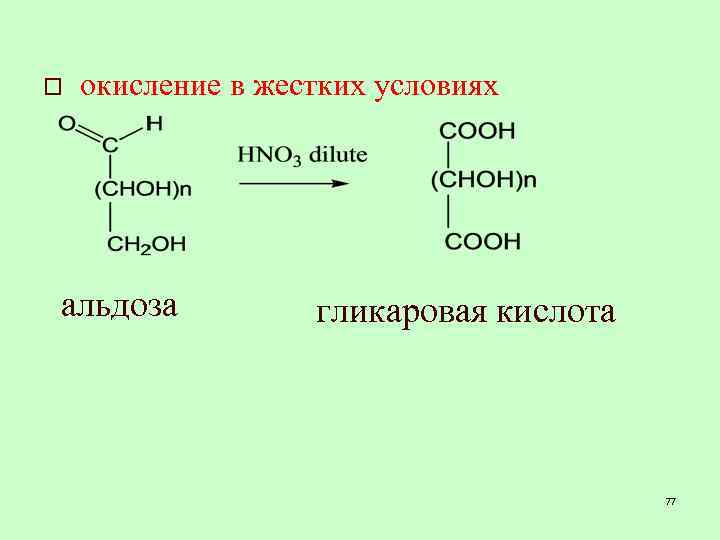 o окисление в жестких условиях альдоза гликаровая кислота 77
o окисление в жестких условиях альдоза гликаровая кислота 77
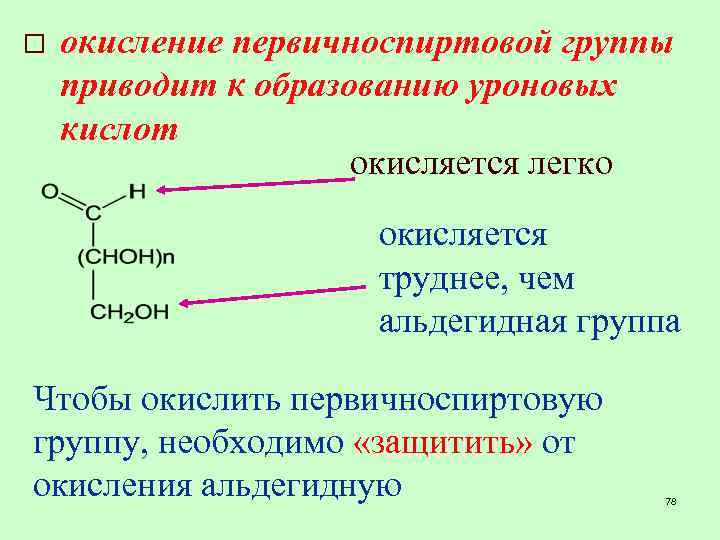 o окисление первичноспиртовой группы приводит к образованию уроновых кислот окисляется легко окисляется труднее, чем альдегидная группа Чтобы окислить первичноспиртовую группу, необходимо «защитить» от окисления альдегидную 78
o окисление первичноспиртовой группы приводит к образованию уроновых кислот окисляется легко окисляется труднее, чем альдегидная группа Чтобы окислить первичноспиртовую группу, необходимо «защитить» от окисления альдегидную 78
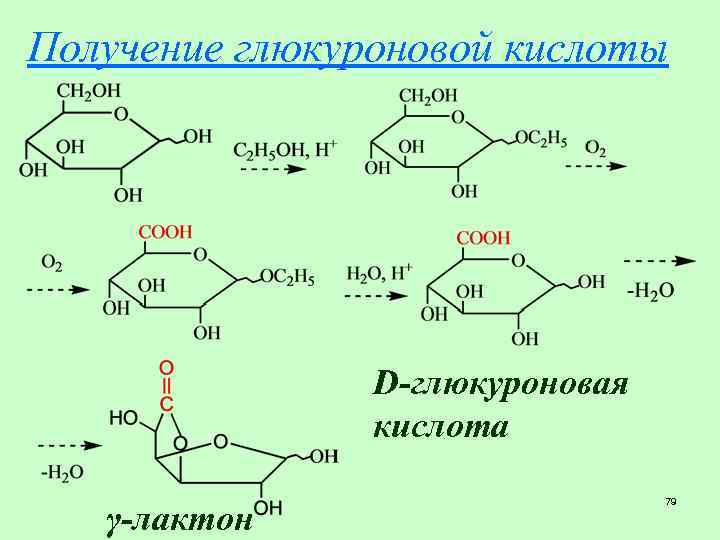 Получение глюкуроновой кислоты D-глюкуроновая кислота γ-лактон 79
Получение глюкуроновой кислоты D-глюкуроновая кислота γ-лактон 79
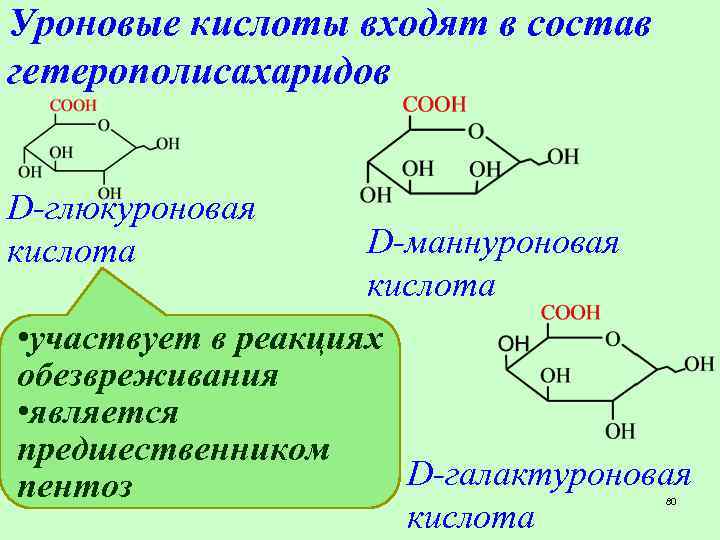 Уроновые кислоты входят в состав гетерополисахаридов D-глюкуроновая кислота D-маннуроновая кислота • участвует в реакциях обезвреживания • является предшественником D-галактуроновая пентоз кислота 80
Уроновые кислоты входят в состав гетерополисахаридов D-глюкуроновая кислота D-маннуроновая кислота • участвует в реакциях обезвреживания • является предшественником D-галактуроновая пентоз кислота 80
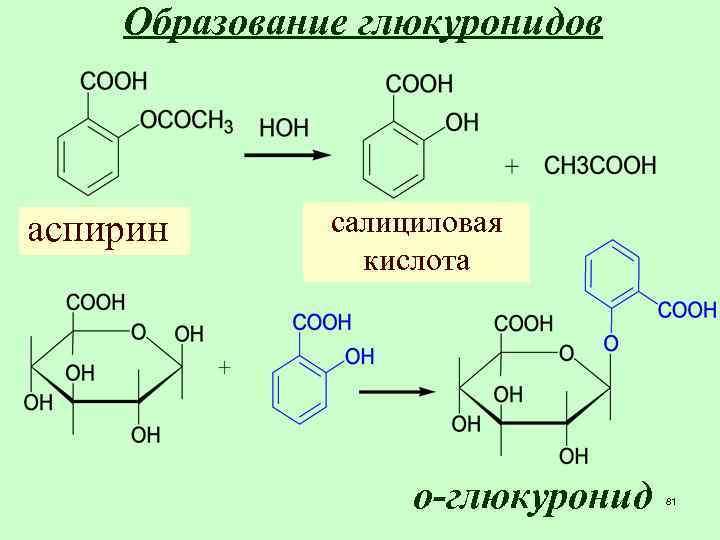 Образование глюкуронидов аспирин салициловая кислота о-глюкуронид 81
Образование глюкуронидов аспирин салициловая кислота о-глюкуронид 81
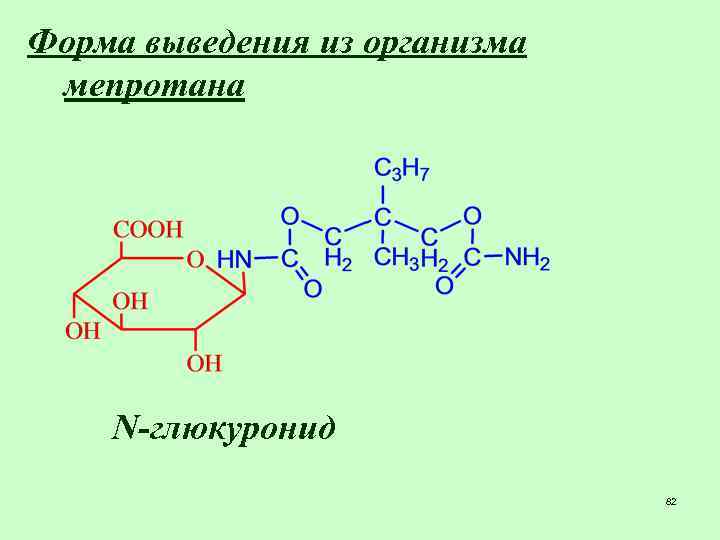 Форма выведения из организма мепротана N-глюкуронид 82
Форма выведения из организма мепротана N-глюкуронид 82
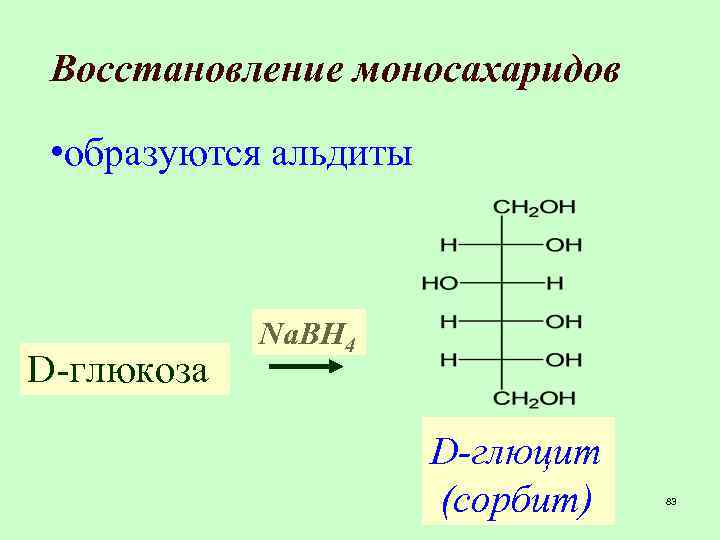 Восстановление моносахаридов • образуются альдиты D-глюкоза Na. BH 4 D-глюцит (сорбит) 83
Восстановление моносахаридов • образуются альдиты D-глюкоза Na. BH 4 D-глюцит (сорбит) 83
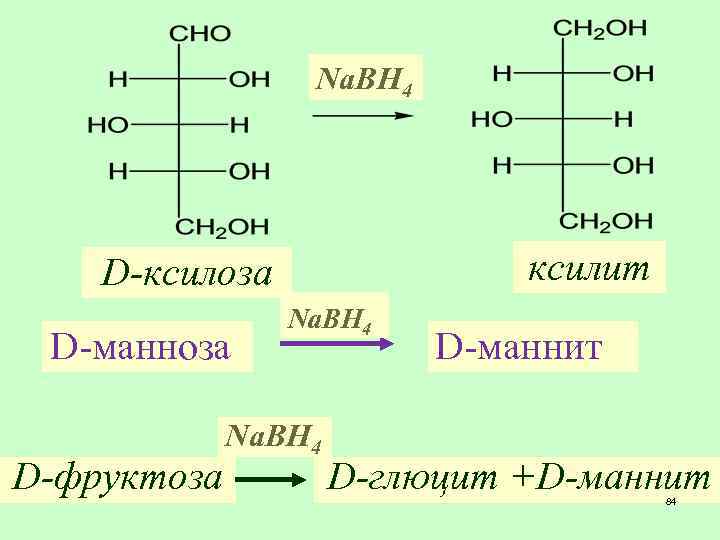 Na. BH 4 ксилит D-ксилоза D-манноза D-фруктоза Na. BH 4 D-маннит D-глюцит +D-маннит 84
Na. BH 4 ксилит D-ксилоза D-манноза D-фруктоза Na. BH 4 D-маннит D-глюцит +D-маннит 84
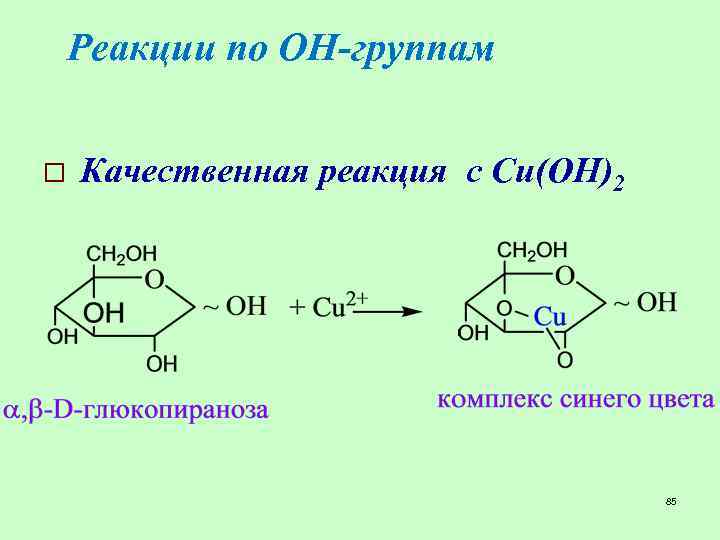 Реакции по ОН-группам o Качественная реакция с Cu(OH)2 85
Реакции по ОН-группам o Качественная реакция с Cu(OH)2 85
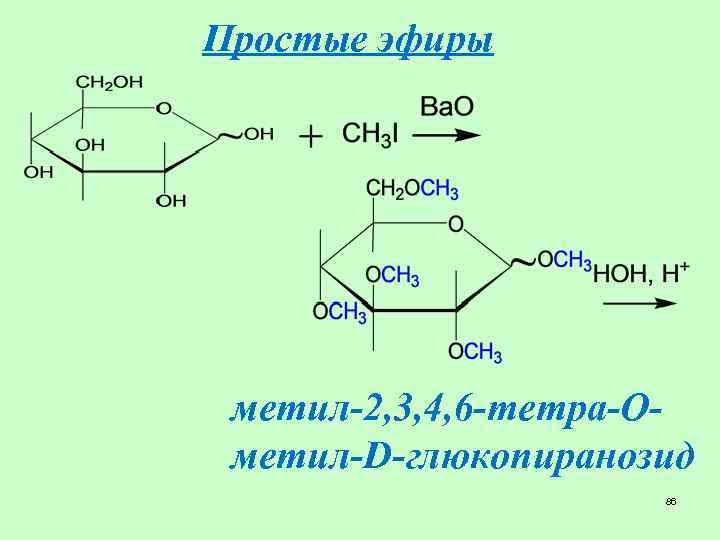 Простые эфиры метил-2, 3, 4, 6 -тетра-Ометил-D-глюкопиранозид 86
Простые эфиры метил-2, 3, 4, 6 -тетра-Ометил-D-глюкопиранозид 86
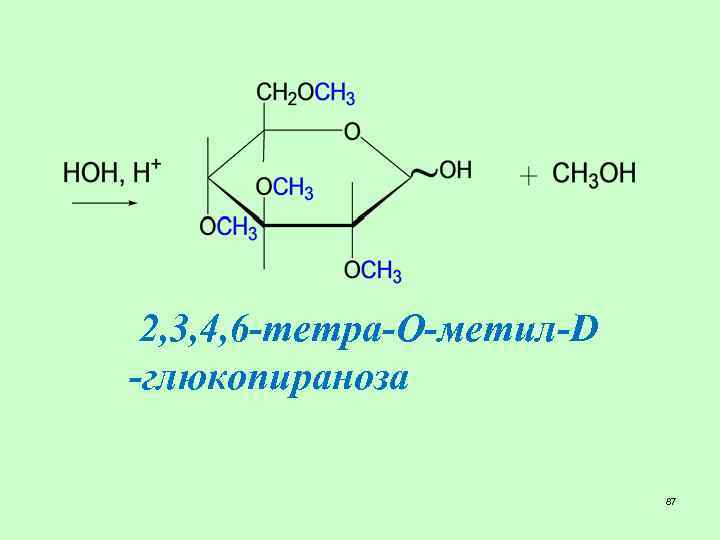 2, 3, 4, 6 -тетра-О-метил-D -глюкопираноза 87
2, 3, 4, 6 -тетра-О-метил-D -глюкопираноза 87
 o Бензиловые эфиры получают при помощи бензилбромида Используют для защиты функциональных групп o Тритиловые эфиры могут быть получены избирательно по первичному гидроксилу Тритиловая группа – Tr- 88
o Бензиловые эфиры получают при помощи бензилбромида Используют для защиты функциональных групп o Тритиловые эфиры могут быть получены избирательно по первичному гидроксилу Тритиловая группа – Tr- 88
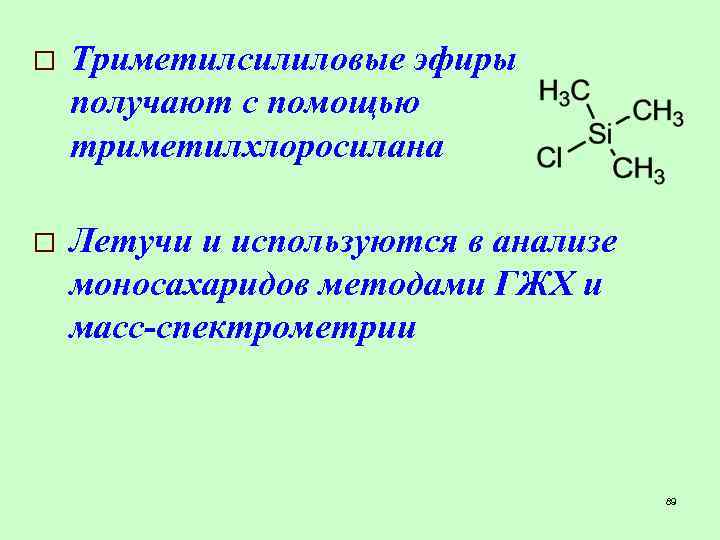 o Триметилсилиловые эфиры получают с помощью триметилхлоросилана o Летучи и используются в анализе моносахаридов методами ГЖХ и масс-спектрометрии 89
o Триметилсилиловые эфиры получают с помощью триметилхлоросилана o Летучи и используются в анализе моносахаридов методами ГЖХ и масс-спектрометрии 89
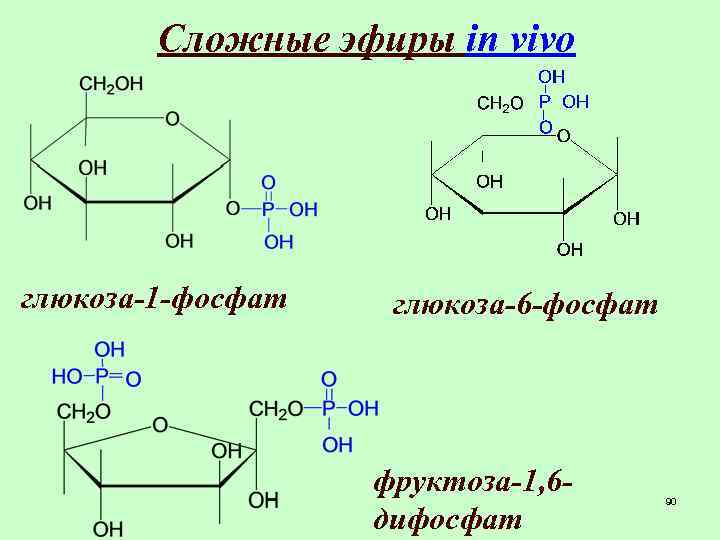 Сложные эфиры in vivo глюкоза-1 -фосфат глюкоза-6 -фосфат фруктоза-1, 6 дифосфат 90
Сложные эфиры in vivo глюкоза-1 -фосфат глюкоза-6 -фосфат фруктоза-1, 6 дифосфат 90
 Таннины – сложные эфиры глюкозы и галловой или дигалловой кислот галловая кислота дигалловая кислота 91
Таннины – сложные эфиры глюкозы и галловой или дигалловой кислот галловая кислота дигалловая кислота 91
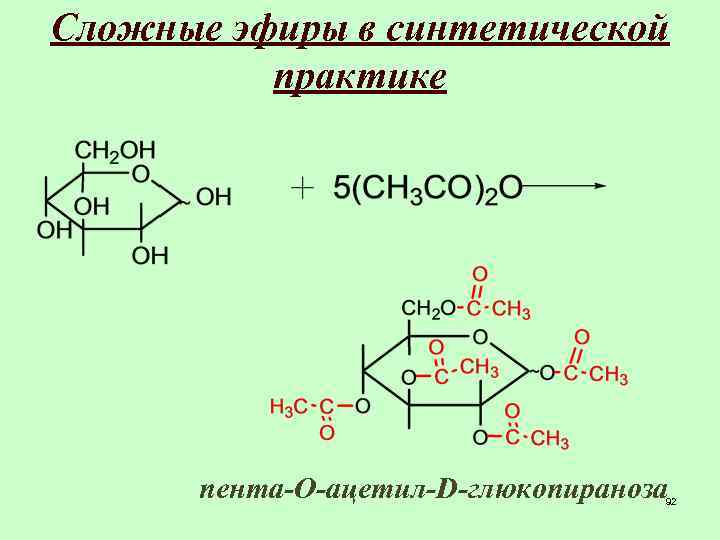 Сложные эфиры в синтетической практике пента-О-ацетил-D-глюкопираноза 92
Сложные эфиры в синтетической практике пента-О-ацетил-D-глюкопираноза 92
 Гидролиз сложных эфиров: o o o в кислой среде в щелочной среде переэтерификация – обычно используется для удаления ацильных групп 93
Гидролиз сложных эфиров: o o o в кислой среде в щелочной среде переэтерификация – обычно используется для удаления ацильных групп 93
 Переэтерификация CH 3 OH (изб. ), CH 3 ONa + CH 3 COOCH 3 94
Переэтерификация CH 3 OH (изб. ), CH 3 ONa + CH 3 COOCH 3 94
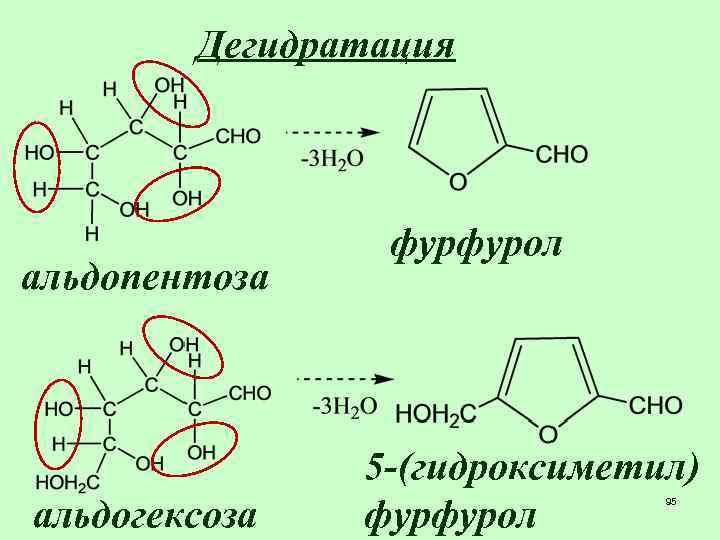 Дегидратация альдопентоза альдогексоза фурфурол 5 -(гидроксиметил) фурфурол 95
Дегидратация альдопентоза альдогексоза фурфурол 5 -(гидроксиметил) фурфурол 95
 Реакции брожения o Брожение – процесс анаэробного расщепления органических веществ, происходящий под влиянием ферментов микроорганизмов Спиртовое брожение (дрожжи) глюкоза → ПВК → С 2 Н 5 ОН + СО 2 o 96
Реакции брожения o Брожение – процесс анаэробного расщепления органических веществ, происходящий под влиянием ферментов микроорганизмов Спиртовое брожение (дрожжи) глюкоза → ПВК → С 2 Н 5 ОН + СО 2 o 96
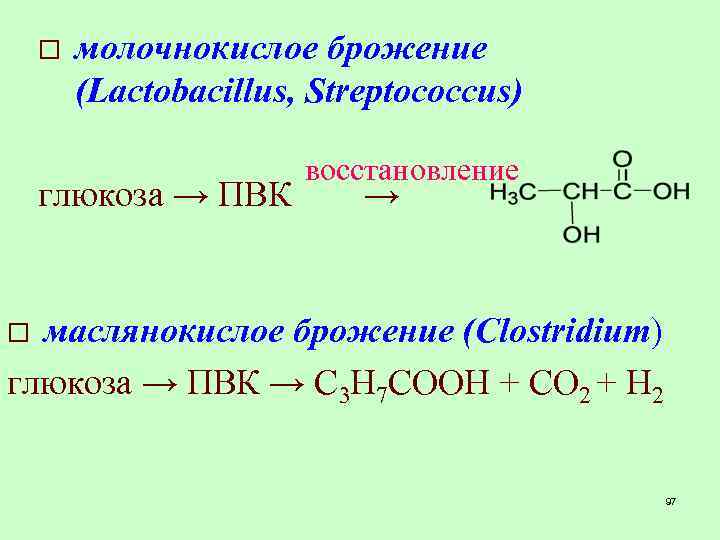 o молочнокислое брожение (Lactobacillus, Streptococcus) глюкоза → ПВК восстановление → маслянокислое брожение (Clostridium) глюкоза → ПВК → С 3 Н 7 COОН + СО 2 + H 2 o 97
o молочнокислое брожение (Lactobacillus, Streptococcus) глюкоза → ПВК восстановление → маслянокислое брожение (Clostridium) глюкоза → ПВК → С 3 Н 7 COОН + СО 2 + H 2 o 97
![o лимоннокислое брожение (Aspergillus) глюкоза + [O]→ + HOH 98 o лимоннокислое брожение (Aspergillus) глюкоза + [O]→ + HOH 98](https://present5.com/presentation/1/9058081_160357042.pdf-img/9058081_160357042.pdf-97.jpg) o лимоннокислое брожение (Aspergillus) глюкоза + [O]→ + HOH 98
o лимоннокислое брожение (Aspergillus) глюкоза + [O]→ + HOH 98
 Производные моносахаридов 99
Производные моносахаридов 99
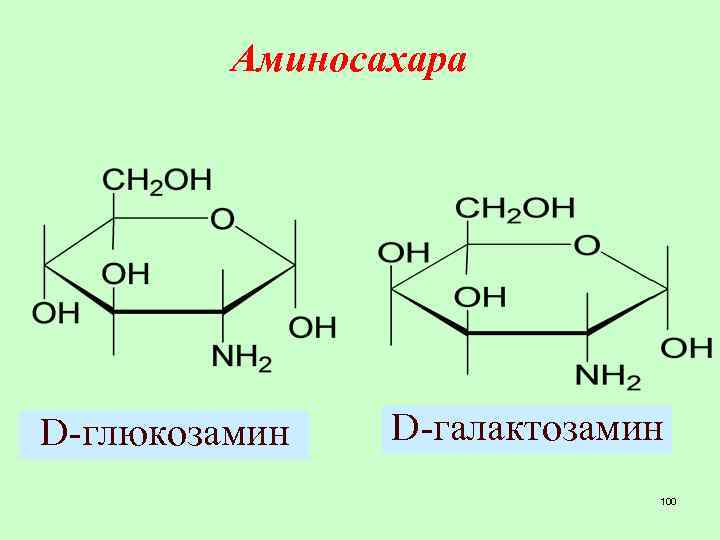 Аминосахара D-глюкозамин D-галактозамин 100
Аминосахара D-глюкозамин D-галактозамин 100
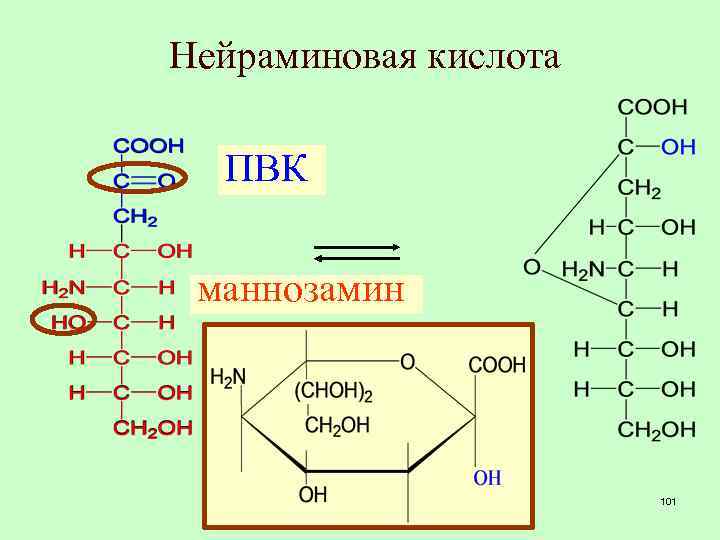 Нейраминовая кислота ПВК маннозамин 101
Нейраминовая кислота ПВК маннозамин 101
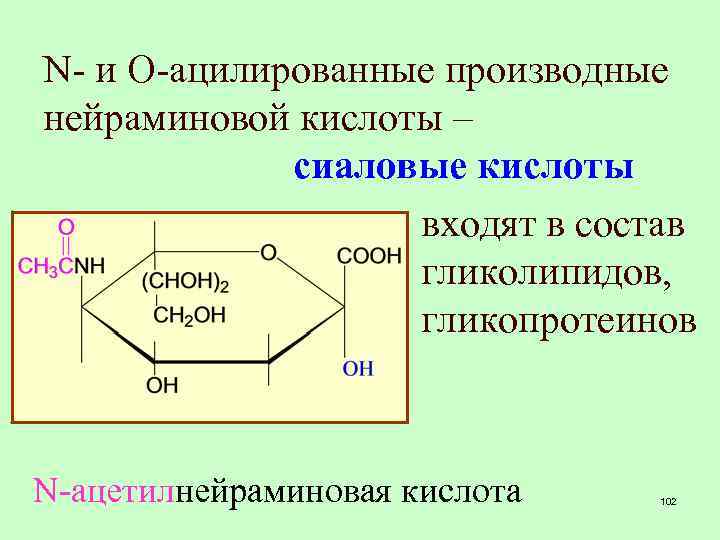 N- и O-ацилированные производные нейраминовой кислоты – сиаловые кислоты входят в состав гликолипидов, гликопротеинов N-ацетилнейраминовая кислота 102
N- и O-ацилированные производные нейраминовой кислоты – сиаловые кислоты входят в состав гликолипидов, гликопротеинов N-ацетилнейраминовая кислота 102
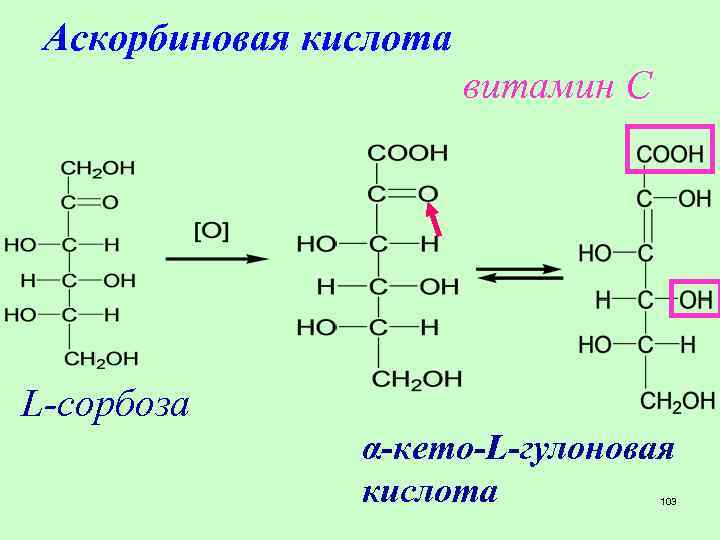 Аскорбиновая кислота витамин С L-сорбоза α-кето-L-гулоновая кислота 103
Аскорбиновая кислота витамин С L-сорбоза α-кето-L-гулоновая кислота 103
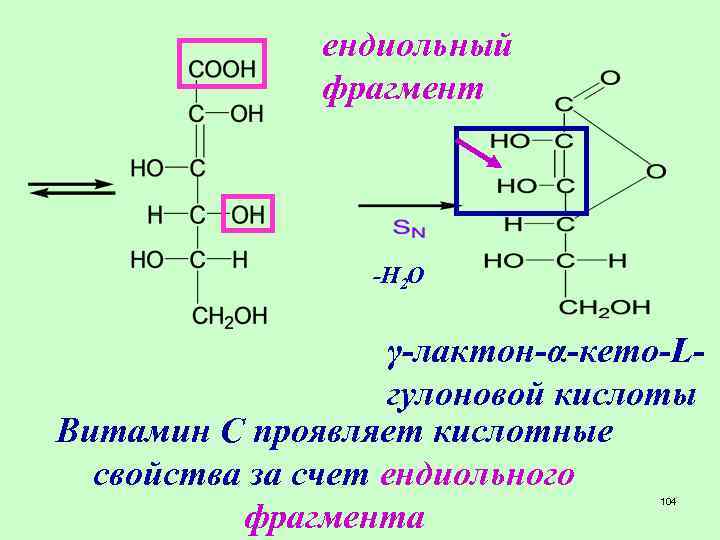 ендиольный фрагмент -H 2 O γ-лактон-α-кето-Lгулоновой кислоты Витамин С проявляет кислотные свойства за счет ендиольного фрагмента 104
ендиольный фрагмент -H 2 O γ-лактон-α-кето-Lгулоновой кислоты Витамин С проявляет кислотные свойства за счет ендиольного фрагмента 104
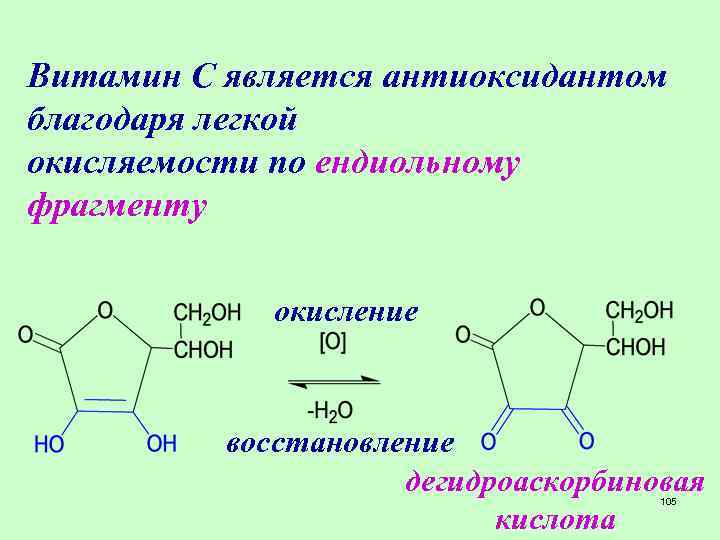 Витамин С является антиоксидантом благодаря легкой окисляемости по ендиольному фрагменту окисление восстановление дегидроаскорбиновая кислота 105
Витамин С является антиоксидантом благодаря легкой окисляемости по ендиольному фрагменту окисление восстановление дегидроаскорбиновая кислота 105
 Аскорбиновая кислота: o является антиоксидантом o участвует в реакциях гидроксилирования в клетке 106
Аскорбиновая кислота: o является антиоксидантом o участвует в реакциях гидроксилирования в клетке 106


